口服固体制剂压缩空气系统验证报告
压缩空气系统验证报告

1 概述本压缩空气系统由预处理系统连接管路至车间各用气点构成。
预处理系统位于制剂大楼二楼空调机房内,主要有LS16—75H固定式螺杆空压机、储气罐、主管路过滤器、冷冻式压缩空气干燥机、压缩空气精密过滤器等设施,这些设施于2011年5月采购,2011年10月进行安装;连接管路及阀门全部采用304L不锈钢材质,并且双面抛光。
系统为工艺生产气动设备及仪表的使用而提供无油无水的干燥空气,空压机排出的压缩空气,首先经过主管路过滤器,过滤粒径为1µm,然后经过冷冻式压缩空气干燥机除去水份,最后分别再经过二台0.01µm的压缩空气精密过滤器,保证了压缩空气质量满足GMP生产要求。
验证小组根据验证方案中法规要求和风险分析结论,对压缩空气系统进行了设计确认(DQ)、安装确认(IQ)运行确认(OQ)、性能确认(PQ)。
现对验证过程中所取得的数据进行收集和整理报告如下:2 验证范围检查并确认验证范围包括(1)压缩空气系统的设计确认(DQ)(2)压缩空气系统的安装确认(IQ)(3)压缩空气系统的运行确认(OQ)(4)压缩空气系统的性能确认(PQ)3 验证目的3。
1 检查并确认该系统所有设备所用材质、设计、制造及制造厂家符合GMP和本公司生产工艺的要求.3.2 检查该系统的文件资料齐全且符合GMP要求;检查并确认设备的安装符合生产要求,公用工程系统配套齐全且符合设计要求;确认该设备的各种仪器、仪表经过校正且合格。
3.3 调查设备的运行性能,确认该设备在空载运行时,能稳定运行;检查标准操作规程是否符合设备的实际操作.3。
4 检查并确认验证系统生产出的压缩空气质量符合D级洁净度要求。
4 验证进度验证小组完全按照已制订和批准的验证方案中所规定的标准对压缩空气系统进行了设计确认(DQ)、安装确认(IQ)、运行确认(OQ)、性能确认(PQ),具体时间如下:5 验证组织及职责5.1 验证小组职责5.1。
1 审核验证方案;印发验证文件;5.1.2审核和批准压缩空气系统工艺流程图和设计参数;5。
口服液体制剂车间空气净化系统确认报告
上海***药业股份有限公司确认报告报告名称口服液体制剂车间空气净化系统确认报告文件编码WP-E-7·12-003版本号00 项目签名所在部门日期起草人部门审核QA审核批准人目录一、确认依据 (1)二、内容 (1)1.设计确认 (1)2、验证用仪器仪表的校验 (1)3、安装确认 (1)4、运行确认 (3)5、性能确认 (6)三、相关建议及(再确认)周期 (7)四、确认小组签名 (7)五、偏差和措施 (8)六、确认结果分析与评价 (8)七、最终批准 (8)八、附件 (9)编码:WP-E-7·12-003版本号:00共9页第1页为了确认本公司新购口服液体制剂车间空气净化系统是否符合洁净区工艺要求,确认小组及相关人员(附件1)于月日对《口服液体制剂车间空气净化系统确认方案》(WP-E-7.12-003)的具体内容进行了培训,根据《口服液体制剂车间空气净化系统确认方案》(WP-E-7.12-003)于年月日至年月日对该设备进行了设计确认、安装确认、运行确认以及性能确认,现将确认情况报告如下:一、确认依据《口服液体制剂车间空气净化系统确认方案》(WP-E-7.12-003)二、内容1、设计确认确认项目确认结果HVAC系统设计原理图系统的特性指标和功能的说明(洁净度、温湿度、压差、气流组织、换气次数、自净时间、风量及风量平衡等。
)HVAC系统所采用设备以及其它部件详细规格说明空调净化调节系统关键部位的关键参数设定供应商有关资质材料设计确认结论:结论人:日期:年月日2、验证用仪器仪表的校验HVAC系统的测试、调整及监控过程中,监控参数的测定需要通过准确可靠的仪表及仪器来完成。
为保证测量数据的准确可靠,必须对仪器、仪表进行校验。
主要校验的仪器有温湿度计、风速仪、风压表、压差计、悬浮粒子计数器等,将仪器、仪表校验情况记录于附件2。
3、安装确认3.1、安装确认所需文件资料资料名称存放处保管人编码:WP-E-7·12-003版本号:00共9页第2页环境控制区平面布局图及空气流向图(包括各房间的洁净度、气流流向、压差、温湿度要求、人流物流流向)控制区HVAC系统划分的描述及设计说明HVAC系统设备档案仪器仪表检定记录及鉴定证书系统操作手册备用件及消耗品清单HVAC系统操作、维护保养程序设备及管道泄漏检测报告空调设备及风管的清洗规程及清洗记录高效过滤器完整性测试报告高效过滤器检漏程序3.2、HVAC系统性能、质量、适用性评价根据系统改造设计方案及技术参数、设计图纸、采购定单、供应商提供的技术资料等对HVAC 系统进行评价,评价内容应包括系统性能、质量、适用性等。
【示例8 -1】压缩空气系统验证

【示例8 -1】压缩空气系统验证x x药业有限公司验证文件一、螺杆式压缩空气机压缩空气系统验证方案题目:螺杆式压缩空气机压缩空气系统验证方案验证方案编号:VDP-SS-008 -01 -1起草人:日期:审核人:日期:批准人:日期:颁发部门:质量部生效日期:分发部门:工程设备部、生产部、固体制剂车间、QA目录(略)正文1验证目的:安装在口服固体制剂车间的SCR 40M - 8/SKT、SCRI0T - 8/SKT二台螺杆式压缩空气机,该设各为x x 斯可洛公司制造。
本验证的目的是:确认本设备的设计、选型、安装符合要求,确定有关文件和资料符GMP要求;并确认:①该设备提供的直接接触药物的压缩空气洁净度能满足净化的洁净空气(D级)的要求;(2)空气压缩机的标准操作规程(SOP)。
2职责及工作内容2. 1验证领导小组:公司验证领导小组成员名单(略)2.2职责和工作内容:(略)2.3项目验证小组:成员名单(略)2.4职责和工作内容2.4.1工程设备部:①负责验证方案的起草,设备的安装、调试并做好记录。
②建立设备档案,收集各种记录资料,总结验证结果报验证领导小组审批。
③编制设备标准操作、使用维护保养规程。
2.4.2质量部:①QA负责核查生产部提供的工艺技术参数。
②QC负责验证过程中的取样、测试工作,并出具检验报告。
2.4.3生产部:提供与设备有关的工艺技术参数和与生产工艺有关的安装要求。
2.4.4固体液体制剂车问:设备运行和性能确认;指派操作人员依据标准操作规程并进行操作;各种试验材料的准备工作。
3设备基本情况3. 1系统概况:该设备由x x x公司生产。
该设备是一种容积式的,单级压缩的,喷油双螺杆压缩机,电机通过皮带或是弹性联轴器与压缩机机头的阳转子相连进而驱动压缩机旋转,本机机头为原装进口,加工精良,因而机组具有良好的动力性,经济型可靠性。
本系统有以下设备。
①无油空压机:具有中间冷却器设置于空气压缩机一级气缸之后,其主要目的是冷却一级气缸排出的高温(约160℃)空气,供二级气缸使用,可节省能量、提高效率。
制剂车间空调净化系统验证报告

制剂车间空调净化系统验证报告一、引言制剂车间是药品生产的重要环节,空气质量的好坏直接关系到药品的质量和安全。
为了保证制剂车间空气质量的稳定和符合相关标准,我公司对空调净化系统进行了验证和评估,并编写了本报告,以便于监管部门和客户了解我们的空调净化系统的运行情况。
二、验证目的本次验证的目的是评估制剂车间空调净化系统的运行情况,包括空气净化效果、系统稳定性、设备运行情况等,以确保空气质量符合相关标准要求。
三、验证范围本次验证范围包括制剂车间空调净化系统的所有设备和组件,包括空调设备、过滤器、送风口、回风口等。
四、验证方法1. 空气质量监测:通过在不同位置设置空气质量监测仪器,对空气中的微粒物质和细菌进行监测,以评估空气净化效果。
2. 设备运行情况检查:对空调设备、过滤器等进行检查,评估设备的运行情况和稳定性。
3. 温湿度监测:监测制剂车间的温湿度情况,评估空调系统的温湿度控制能力。
五、验证结果1. 空气质量监测结果显示,制剂车间空气中的微粒物质和细菌浓度均符合相关标准要求,空气质量良好。
2. 设备运行情况良好,空调系统稳定运行,过滤器过滤效果良好,没有发现漏气或漏水现象。
3. 温湿度监测结果显示,空调系统对制剂车间的温湿度控制良好,符合相关要求。
六、验证结论根据以上验证结果,制剂车间空调净化系统的运行情况良好,空气质量符合相关标准要求,设备稳定性良好,温湿度控制能力良好。
七、改进措施根据本次验证结果,我们将继续加强对空调净化系统的维护和管理,定期对设备进行检查和维护,确保空调系统的稳定运行和空气质量的稳定。
八、结语本次制剂车间空调净化系统验证报告对我们的空调净化系统进行了全面的评估和验证,验证结果良好,我们将继续加强对空调系统的管理和维护,确保制剂车间空气质量的稳定和符合相关标准要求。
同时,我们也欢迎监管部门和客户对我们的空调净化系统进行监督和检查,以确保我们的空调系统的运行情况和空气质量的稳定。
压缩空气系统验证报告

空气压缩系统验证报告编号:起草人:起草日期:审核人:审核日期:批准人:批准日期:目录1.引言1.1.验证小组人员及责任1.2.概述1.3.压缩空气系统的组成1.4.主要技术参数1.5.验证目的1.6.验证文件准备1.7.测试用仪器仪表2.预确认3.安装确认4.运行确认5.性能确认5.1.微生物(沉降菌)测试5.2.无水测试5.3.无油测试5.4.悬浮粒子测试6.结果分析与评价7.根据本次验证结果确定的再验证周期及日常监控项目和周期。
8.验证证书1.引言1.1.验证小组人员及责任1.2.概述压缩空气经冷冻、干燥、三级过滤后可直接供口服液产品生产中的瓶子清洗、气动设备及仪表使用。
1.2.1.为提取系统、瓶子清洗系统等提供洁净气源保证。
1.2.2.压缩空气与内包装直接接触的设备有瓶子清洗机。
1.3.压缩空气系统的组成LGFD-3/7-X型空气压缩机、电脑控制器、油气分离器、水气分离器、储气罐、预过滤器、冷干机、二级过滤器、压缩空气管道及设备自带过滤器组成。
1.4.主要技术参数1.4.1.设备数量:一台1.4.2.生产厂家: 1.4.3.购置日期:1996年9月1.4.4.安装、调试日期:年1 月20日1.4.5.定置:口服液车间动力岗位1.5.验证目的经过验证,证明压缩空气系统符合设计要求,压缩空气经净化达到30万级洁净空气的要求,可用于直接接触药品的生产;资料和文件符合GMP的管理要求。
1.6.验证文件准备(应当有下列资料档案)结论:洁净压缩空气系统验证所需的文件经检查符合方案和管理的要求。
检查人:日期:年1月20日1.7.测试用仪器仪表准备结论:尘埃粒子计数仪经检定合格,可以投入使用。
检查人:日期:年1月20日2.预确认结论:从设备的性能、材质、结构、参数等角度,并参照设备说明书对空气压缩系统加以考查,结果表明适合生产工艺、校正、维修保养、洁净度等方面的要求。
检查人:日期:年1月20日3.安装确认安装确认是对系统安装(包括计量)的确认,对安装进行检查的目的在于保证系统设备在规定限度内和承受能力下能正常持续运行。
某制药公司压缩空气设备验证文件

某制药公司压缩空气设备验证文件
某制药公司是一家专门从事制药品开发和生产的公司,其生产的药品质量和安全性备受欢迎。
而其中一项重要的生产环节就是制药过程中所使用的压缩空气设备。
为保证该设备的质量和标准化,某制药公司针对压缩空气设备开展了验证和验收工作,以确保设备能够安全高效地运行。
某制药公司压缩空气设备验证文件主要包括以下方面的内容:
一、压缩空气设备的描述
在文件中要详细描述设备的型号、制造商、额定工作压力以及容量等方面的信息。
此外,压缩空气设备还包括多个组件,例如滤芯、分离器、除湿器等,这些组件的安装位置和使用规范也需要在文件中描述。
二、验证的目的和方法
验证的目的是为了评估压缩空气设备的性能和质量,确保其能够安全有效地运行。
验证的方法主要包括:开展压力测试、温度测试、流量测试和紧急关停测试等,通过这些测试能够确保设备符合制药标准和规范要求。
三、验证的结果和结论
在进行整个验证过程中,必须记录每次测试的结果并进行比对,以便最终得出验证结论。
与此同时,还需确定验证期限和如何进行维护保养。
四、贯彻执行验证的要求
最后,要明确验证文件的执行标准和相关流程,阐述其重要性和必要性,并规定设备人员和操作人员应如何操作设备,以确保生产过程的顺利进行。
总之,某制药公司制定的压缩空气设备验证文件,对于其品牌质量保障控制具有重要的保障作用。
只有不断优化验证方法,提升验证的严谨性和可靠性,才能更好地保障制药品的质量和安全性,提高市场竞争力。
压缩空气系统再验证报告

压缩空气系统再验证报告起草人审核人批准人起草日期审核日期批准日期颁发部门:质量管理部分发部门与数量:设备工程部.1,质量管理部.1,生产技术部.1,通化金恺威药业有限公司验证证书验证项目名称: 压缩空气系统再验证验证文件(方案) 编号: STP-SB-X-ZYB-03再验证周期: 1.设备大修或更换时2.一年定期再验证验证评价: 该系统经验证,确认系统的安装运行、性能符合要求;系统可靠,批准使用,文件可交付使用。
批准人:批准日期: 年月日再验证报告审批表起草人所在部门签字日期审核人所在部门签字日期质量管理部生产技术部设备工程部批准人所在部门签字日期验证委员会备注目录1.验证组织系统2.概述3.验证目的4.相关文件5.验证范围6.人员培训7.验证内容7.1压缩空气系统安装情况的稳定性检查7.2运行确认7.3性能确认8 特殊情况处理9再验证结果评定与结论10文件执行11文件归档12附表附表1:再验证方案变更申请表附表2:压缩空气系统机组上仪器仪表校验记录附表3:压缩空气系统空调机组安装检查记录附件4:压缩空气系统运行确认检测记录附表5:压缩空气系统油污检测记录附表6:压缩空气系统尘埃粒子数检测报告附表7:压缩空气系统微生物数检测记录附表8:漏项、偏差处理表附表9:压缩空气系统空气干燥检测记录1验证组织系统1.1验证委员会机构验证委员会工艺验证小组设备验证小组系统验证小组清洁验证小组1.1.1验证委员会成员及其职责职务姓名所在部门职务主任赵登峰——总经理委员丁年质量管理部部长委员高光波生产技术部部长委员范晓光设备工程部部长1.1.2验证委员会职责主任:负责验证方案、验证报告的批准;负责签发验证证书。
委员:审核验证方案、验证报告,制定验证计划。
1.2验证小组成员及其职责1.2.1系统验证小组成员小组成员姓名所在部门组长质量管理部王永欣组员生产技术部孟范静组员设备工程部郝世功组员化验室张静组员综合制剂车间张惠群1.2.2各成员职责组长——负责验证实施全过程的组织协调工作;组员——负责验证过程中的具体工作,并做好记录工作。
口服液体制剂车间空气净化系统验证报告

车间空气净化系统再验证报告编号:1.目的为了通过口服液体制剂车间空气净化系统的安装确认、运行确认、性能确认,证明本系统的安装、运行、性能符合GMP要求,特制定本验证报告。
报告中,根据验证方案的实施过程中收集到的各种数据和记录,制定了本空气净化系统的再验证周期、洁净厂房的消毒周期和日常监测程序等。
2.验证小组成员2.检查验证所需相关文件的准备《洁净区卫生管理规程》《悬浮粒子测定操作规程》《沉降菌检测操作规程》《洁净区人员进入更衣管理规程》《空气净化系统运行操作规程》《空调机组维修保养规程》《洁净区环境控制标准》《洁净区卫生管理规程》检查结论:___________________________________________________检查人:___________________ ;时间:___________________________复核人:___________________ ;时间:___________________________3.培训参加验证人员需进行本文件及下述内容的培训并考核合格。
《药品生产质量管理规范》《洁净区卫生管理规程》第 1 页共8 页车间空气净化系统再验证报告编号:《悬浮粒子测定操作规程》《沉降菌检测操作规程》《洁净区人员进入更衣管理规程》《空气净化系统运行操作规程》《空调机组维修保养规程》《洁净区环境控制标准》《洁净区卫生管理规程》检查结论:___________________________________________________检查人:________________________ 时间:______________________复核人:________________________ 时间:______________________4.安装确认4.1.检查验证所需仪器、仪表是否已进行校验,校验是否合格并是否有合格证。
检查结果:________________________________________________检查人:________________,检查时间:______________________复核人:________________,复核时间:______________________4.2.检查确认洁净区建材及施工质量洁净区的内表面应平整光滑,无裂缝,接口严密,无颗粒物脱落,并能耐受清洗和消毒,墙壁与地面的交界处成弧形,减少灰尘积聚和便于清洁。
06VR02001-01压缩空气系统再验证报告

G M P文件云南滇池制药有限公司压缩空气系统再验证报告目录1.验证项目概述1.1项目简介1.2验证内容2.验证目的3.验证实施条件3.1验证小组成员与分工3.2验证实施时间3.3验证实施条件确认3.3.1验证方案培训确认3.3.2人员确定3.3.3检验仪器与方法4.验证内容与结果4.1安装确认4.2运行确认4.3性能确认5.验证评价与建议6.验证结论7.验证小组成员签名8.报告附件清单1.验证项目概述1.1项目简介1.1.1我公司的压缩空气系统由压缩空气制备系统与管路分配系统组成,压缩空气制备系统由天津市晟途净化技术设备有限公司提供,包括STL-22A螺杆式空气压缩机、G M P文件云南滇池制药有限公司编号06VR02003-01页码3/10题目压缩空气系统再验证报告JHD0040F冷冻式压缩空气干燥机、储气罐与多级别过滤器[V级(预过滤器:5μm)、A 级(精过滤器: 1μm)、AB级(微过滤器: 0.01μm)、AC级(活性炭除味过滤器)]组成;分配系统装主要由压力调节器与不锈钢管道组成,可以根据仪表或设备的用气需要来调节气压大小。
由压缩空气制备系统生产出的洁净压缩空气通过管路分配系统,输送至车间各用气点,为口服固体制剂车间提供动力气源和洁净压缩空气。
1.1.2工艺流程空气经空气压缩机压缩后进入储气罐,经过V级预过滤器(5μm)、A级精过滤器(1μm)除去压缩空气中的液态水和油污后进入冷冻式压缩空气干燥机;进入冷冻式压缩空气干燥机的压缩空气通过降温至结露点把大部分尘粒、油滴、水滴形成废液除去;较洁净的压缩空气再经过AB级微过滤器(0.01μm)、AC级活性炭除味过滤器,更进一步除去油污、微粒和水滴,通过不锈钢管道,送至车间各使用点。
1.2验证内容:本系统自2005年09月的验证后,其构造、安装等主要因素未发生重大变更,故此次再验证只对其进行部分安装确认、关键性能的运行确认和性能确认,以确认该系统能始终如一提供药品生产所需要的洁净压缩空气。
012 空气压缩机(D级)确认报告(口服固体制剂车间)

起草人:日期:2013年9月18日审核人:日期:2013年9月20日批准人:日期:2013年9月25日1.概况:HTA-100H微型往复活塞空气压缩机及配套的空气过滤器、储气罐、输气管道、减压阀等组成。
空气压缩机使用压力:1.2MPa,容积流量:0.84m³/min。
空气过滤器由初效过滤器、中效过滤器、高效过滤器构成。
压缩空气经过过滤器的三级过滤才能达到洁净的目的。
2.确认目的:对系统的设计、安装、运行、性能确认,确认符合GMP的要求。
对经系统处理后的压缩空气的洁净度进行确认,确认符合GMP的要求。
3.确认时间2013年8月22日——2013年9月15日4.确认组织确认小组组成:质量保证部、生产供应部、后勤保障部确认小组组长:确认小组成员:5.范围本确认报告适用于口服固体制剂车间空气压缩机系统的确认。
6.确认程序:6.1设计确认根据生产的需求,设备设计确认符合技术要求。
检查人:复核人:检查日期:年月日6.2安装确认6.2.1安装确认所需资料及存放处检查人:复核人:检查日期:年月日6.2.2设备安装确认标准与测试方法设备安装确认标准与测试方法根据安装的情况确认,设备安装符合技术要求。
检查人:复核人:检查日期:年月日6.3运行确认6.3.1运行确认所需文件资料检查人:复核人:检查日期:年月日6.3.2运行认证标准与测试方法设备运行认证标准与测试方法根据试运行的情况确认,设备运行符合设计要求。
检查人:复核人:检查日期:年月日6.4性能确认6.4.1压缩空气净化后应达到标准6.4.2测试方法与记录6.4.2.1物理外观的测试:取洁白涤纶布套在取样口,缓慢放出压缩空气,1分钟后取出,检验过滤面上有无污迹。
每个点检查3次,作记录。
物理外观测试记录结论:合格。
检查人:复核人:检查日期:年月日6.4.3.2悬浮粒子测试:将已洁净的塑料袋(容积约20L)连接压缩空气,先让压缩空气充满塑料袋后,向袋挤压,排除袋中空气,反复3次,然后再充满压缩空气,用手握住袋口。
压缩空气系统的验证报告

文件编号:压缩空气系统验证报告验证报告起草: 年月日验证报告审核: 年月日验证报告批准: 年月日验证实施小组:目录1.概述2.验证的目的3.职责4.安装确认5.运行确认6.性能确认7.验证结果分析与评价8.验证周期与再验证9.偏差10.验证合格证1.概述1.1压缩空气主要用于气动元件及泡罩包装机等设备,我公司现有HAS-11微油螺杆空压机两台,正常生产时用一台螺杆空压机完全满足生产,另一台作为备用,我公司所用螺杆空压机经分离过滤后再经干燥机干燥,最后通过三级精滤器过滤后所出之气为洁净区压缩空气送至各用气点。
根据GMP和《冀衡药业验证管理标准》的要求,对该设备进行完整系统的检查再确认,完善该设备的验证文档,完善设备操作规程。
延续、系统化设备验证的管理工作。
所有压缩空气必须经过验证合格后方可使用。
1.2.设备概况设备名称: HAS-11微油螺杆空压机设备型号: HAS-11型制造厂家:无锡五洋赛德压缩机有限公司设备编号:安装日期: 年月日安装部位:空气压缩机组主要由HAS-11微油螺杆空压机、贮气罐、冷却干燥器(除油过滤器)、精密过滤器、空气输送管路管线等设施组成,具有可靠性能高,使用寿命长、噪音低、体积小、使用操作及维护方便等特点。
采用集中式供气系统,其产生的压缩空气可供应不同区域,多个元件同时使用。
2.验证的目的通过对该设备安装确认、运行确认、性能确认,确认压缩空气系统是否达到设计要求。
能够稳定、连续提供合格的气源,设备的相关文件资料规范、并符和工艺和GMP的管理要求。
3、职责:3. 1验证小组3. 1.1起草验证方案:3. 1.2组织协调设备部、质量管理部、生产管理部、生产车间对验证方案进行实施。
3. 1.3起草验证方案及验证报告、确定验证周期,报质量管理部审核。
3.2质量管理部3. 2.1根据验证对象成立验证小组:3. 2.2质量管理部负责验证方案的审核批准:3. 2.3质量管理部负责验证报告的审核批准:3. 2.4负责设备再验证周期的确认:3. 2.5负责发放验证合格证书:3. 2.6负责组织验证小组对验证相关人员进行培训。
制剂压缩空气系统再验证方案

制剂压缩空气系统再验证方案引言:制剂压缩空气系统是工业生产中常用的设备之一、该系统通过将大气中的空气经过处理后进行压缩,以满足工业生产中对高压气体的需求。
然而,由于该系统的安全性和稳定性要求较高,因此需要进行再验证。
本文将就制剂压缩空气系统的再验证方案进行探讨。
一、确定再验证的目标和范围在进行再验证之前,需要明确再验证的目标和范围。
由于制剂压缩空气系统是一个较为复杂的系统,因此可以将再验证的目标和范围分为以下几个方面:1.系统的传输效率:验证系统在正常工作状态下,传输效率是否达到设计要求,包括压缩比、系统效能等。
2.系统的安全性:验证系统在各种工作条件下,运行安全可靠,没有泄漏、故障等问题。
3.系统的稳定性:验证系统在长时间工作状态下,能够保持压力的稳定性,不会出现过压或欠压等问题。
4.系统的节能性:验证系统在运行过程中的能耗状况,是否达到节能要求。
二、再验证的方法和步骤1.实验验证:通过搭建实际的压缩空气系统实验平台,对系统进行各项性能测试和参数测量,以评估系统的传输效率、安全性、稳定性和节能性。
2.模拟验证:利用计算机模拟软件,对制剂压缩空气系统进行建模,并进行各项参数分析和性能评估,以获取系统的性能数据和优化建议。
3.记录验证:通过对制剂压缩空气系统的运行记录进行分析和比对,评估系统的性能和运行状态是否符合要求。
在再验证的方法确定后,可以按照以下步骤进行具体操作:1.收集和整理系统的设计文档和技术资料,包括设备参数、管线布置图等。
2.搭建实验平台或建立模拟模型,根据系统的设计要求和参数进行设置。
3.进行系统实验或模拟分析,获取系统的性能数据和运行状态。
4.对实验数据或模拟结果进行分析,评估系统的传输效率、安全性、稳定性和节能性。
5.根据分析结果,提出优化建议和改进措施。
6.根据优化建议和改进措施,对制剂压缩空气系统进行改装或调整。
7.进行再验证,重复以上步骤,直至系统的性能满足要求。
三、再验证结果的分析和应用在完成再验证后,需要对再验证结果进行分析和应用。
压缩空气验证报告
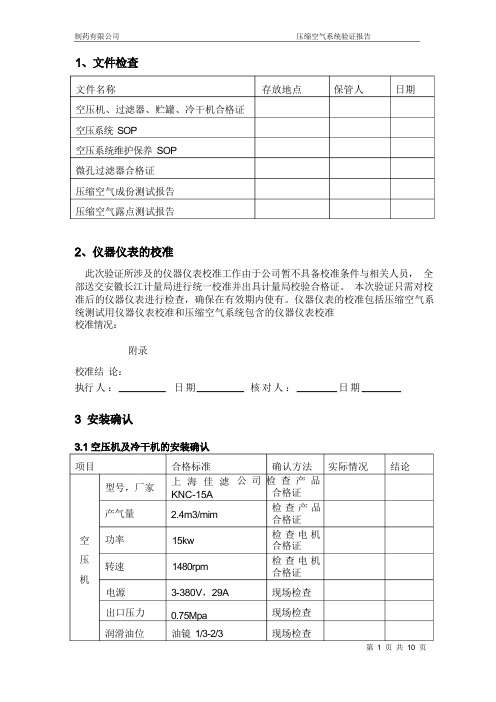
此次验证所涉及的仪器仪表校准工作由于公司暂不具备校准条件与相关人员, 全 部送交安徽长江计量局进行统一校准并出具计量局校验合格证。
本次验证只需对校 准后的仪器仪表进行检查,确保在有效期内使有。
仪器仪表的校准包括压缩空气系 统测试用仪器仪表校准和压缩空气系统包含的仪器仪表校准 校准情况:附录校准结 论: 执行 人 :日 期 核 对 人 : 日 期确认方法 实际情况 公 司 检 查 产 品合格证 检 查 产 品合格证 检 查 电 机合格证 检 查 电 机合格证 现场检查 现场检查 现场检查合格标准 上 海 佳 滤 KNC-15A2.4m3/mim15kw1480rpm3-380V ,29A0.75Mpa 油镜 1/3-2/3型号,厂家产气量功率转速电源 出口压力 润滑油位空 压 机项目结论文件名称 存放地点 保管人 日期 空压机、过滤器、贮罐、冷干机合格证 空压系统 SOP空压系统维护保养 SOP 微孔过滤器合格证 压缩空气成份测试报告 压缩空气露点测试报告项目 前置过滤器主管过滤器精密过滤器 合格标准C 级,安装于贮罐与冷干机 之间,可以滤除大量液体以 及 3um 以上固体颗粒, 含油 率可达 5ppmT 级,安装于冷干机排气口 与精密过滤器之间,可以滤 除 1um 以上固体颗粒, 含油 率可达 0.1ppm安装在主管过滤器之后,可 以滤除 0.01um 以上固体颗 粒,含油率可达 0.01ppm确认方法 实际情况 结论 检查产品合格 证检查产品合格证检查产品合格证合格标准0.6M 38kg已清洁,无灰尘 二类压力容器 罐底设有排水阀 在检验有效期内项目 体积 额定压力 内壁 压力容器 排水阀 安全阀实际情况 确认方法 结论上 海 佳 滤 公 司 , KN-30H 3.8 m3/mim2kw-40℃设有时间定时装置 排水器清洁,通畅无 阻塞。
检 查 产 品 合格证检 查 产 品 合格证 检 查 电 机合格证 检 查 产 品合格证 现场检查现场检查 型号,厂家处理量功率露点温度时间累计 自动排水器冷 干 机否良好。
食品饮料厂压缩空气系统验证报告

1.目的:确认经验证后的压缩空气系统在一定的生产周期后没有发生显著的验证状态的漂移。
2.范围:本方案适用于ATLAS COPCO-GA37P螺杆空压机+冷干机+后级精过滤器系统的验证。
3.职责:设备部:负责验证方案的起草,并负责预确认、安装确认、运行确认的组织实施。
生产部:负责性能确认的组织实施,并协助性能确认方案的起草。
品控部:协助验证方案的起草,组织协调验证工作;按计划完成验证中的相关检验任务,确保检验结论正确可靠。
并总结验证结果,起草验证报告。
品控部部长:负责验证方案及报告的审核。
GMP小组组长:负责验证方案及报告的批准。
4.验证内容4.1 概述符合本公司的空压系统要求为:①生产用压缩空气最大量(6m3/min)的机型。
②压缩空气压力≥0.6MPa,并可根据实际需要设定空压系统的压差上下限(△P为 0.15~0.2MPa)。
③为保证空压系统的可靠性,空压机应有一备一用,空压机的启停可由生产的实际用气量及压力自动控制。
④为减少空压机的频繁启停,稳定系统压力,应配置合适的贮气罐(须有压力容器使用许可证)。
⑤系统应有压缩空气除水、除油、除尘、除臭、除菌装置,通往使用点的压缩空气应符合食品生产要求。
⑥压缩空气管道材质应符合要求。
⑦系统噪声≤75db。
⑧生产操作安全可靠。
⑨能提供及时、优质的售后服务。
4.2 验证小组根据验证方案要求,本公司成立由设备部、生产部及品控部组成的5人验证小组,其中组长:组员:4.3 验证计划本次验证计划安排如下:验证时间:2021.4.26-2021.4.28验证项目:1)预验证;2)安装验证;3)运行验证;4)性能验证。
4.4 验证记录4.4.1 预验证记录预验证记录如下表所示:表1 预验证记录4.4.2 安装确认记录安装确认记录如下表所示:表2 安装确认记录4.4.3 运行确认记录运行确认记录如下表所示:表3 运行确认记录4.4.4 性能确认记录性能确认记录如下表所示:表4 性能确认记录5.验证分析、评价与结果验证分析、评价与结果见下表:表5 利乐自动包装机验证分析、评价及结论6.相关文件《压缩空气系统标准操作规程》。
RYZ008-01压缩空气系统验证报告
起草人:
审核人:
批准人:
起草日期:
审核日期:
批准日期:
验证小组会签
部门
岗位
签名签名日期颁源自部门:[质量部]Copy№:[ ]
行政部[ ]物供部[ ]质量部QA[ ]质量部QC[ ]研发部[ ]生技部[ ]
疫苗车间[ ]分包装车间[ ]工程部[ ]保安部[ ]营销部[ ]财务部[ ]
变更记载:
修订号批准日期执行日期
变更原因及目的:
验证报告
1验证项目名称:压缩空气系统
2验证实施日期:年月日~年月日
3验证结果与结论:
验证阶段
验证项目
标准要求
结果
结论
文件及仪表校验确认
文件资料的确认
所有资料应能满足压缩空气系统生产工艺要求和GMP的要求。
仪器仪表的校正确认
所有的仪器、仪表必须经过校正,并校正合格
运行确认
系统运行检查确认
系统运行正常,各项功能均达到设计要求。
性能确认
终端过滤器起泡点试验确认
各终端过滤器起泡点试验合格
微生物限度确认
过滤后的膜培养菌落数应为0。
尘埃粒子数的测定
要求符合百级洁净气体质量标准:≥0.5µm尘埃粒子数≤3,500个/ m3,≥5µm尘埃粒子数为0。
4评价和建议:
5验证结论:
6再验证周期:
评价人:
日期:
固体制剂车间压缩空气过滤系统验证11.4

≥5μm≤60,000
4、该验证方案由固体制剂车间制订,质监科、生产科会签并协助执行。
5、进度计划
5.1方案制订在2000年8月完成。
申请部门:固体制剂车间
2000年7月3日
批准:厂验证领导小组负责人:
2000年月日
固体制剂车间压缩空气过滤系统验证小组人员组成申请
厂验证领导小组:
根据固体制剂车间压缩空气过滤系统验证申请及验证项目,决定成立压缩空气过滤系统验证小组,由下列人员组成:
部门
技术副主任
负责验证具体工作
生产科
生产科科长
负责协调验证相关部门
压缩机管理人员
负责验证所需气源
质监科
质监科科长
负责气体质量检验,效果评价
QA
负责协助取样
1.1压缩空气:厂用氮气由供应商提供。
1.2压缩空气采用LU610-11A型螺杆式空气压缩机所产。
空气压缩机参数。
排气量
1.5m3/min
轴功率
11KW
公称排气压力
0.8Mpa
转速
1460r/min
1.3管道钝化处理记录见附表一。
1.4压缩空气的终端使用点共三个:高效包衣机、沸腾干燥机、湿法制粒机各一个
1.4.1压缩空气过滤器确认:
项目
设计要求及规格
安装情况
检查
初级过滤
泡沫
泡沫卷PE棒
中级过滤
PE棒0.45μm
PE棒0.45μm
结论:压缩空气过滤器的规格符合要求。
检查人:日期:年月日
复核人:日期:年月日
分发部门
底稿留存
2、验证目的:
2.1检查过滤压缩空气是否符合工艺生产及产品质量的要求。
GT34压缩空气验证报告(1)分解
1目的 (2)2概述 (2)3验证过程 (2)4收集资料 (2)5数据分析 (2)6评价和建议 (3)7再验证与验证周期 (3)8验证结论 (3)9验证结论的评审 (3)1目的本验证报告的目的是对压缩空气系统的验证工作的实施进行总结,统计相关记录数据。
2概述本次验证是在 ______________ 至____________ 之间实施的,具体工作依照压缩空气系统验证方案实施。
2.1开始日期:年月日2.2完成日期:年月日2.3报告日期:年月日3验证过程3.1实施部门:设备部。
3.2协助部门:质量管理部、生产技术部。
3.3实施地点:压缩机机房及各车间使用点。
3.4实施时间:年月日至年月日4收集资料4.1压缩空气系统设计确认由设备部、生产部:等人员于年月日进行检查,检查情况见记录14.2压缩空气系统文件确认由设备部、生产部:等人员于年月日进行检查,检查情况见记录2。
4.3压缩空气系统安装确认由设备部、生产部、质量管理部:等人员于年月日进行检查,检查情况见记录3。
4.4压缩空气系统运行确认由设备部、生产部:等人员进行调试,于年月日进行,运行确认情况见记录4、记录5。
4.5压缩空气系统性能确认由设备部、生产部、质量管理部:等人员负责,于年月日至月日进行,检测情况见附件记录6及检验记录5数据分析5.1通过对压缩空气系统安装及运行确认,可以确定压缩空气系统的选型、安装及运行符合要求。
5.2通过对压缩空气系统性能确认,可以确定压缩空气系统性能达到生产设计要求。
6评价和建议6.1通过对压缩空气系统安装和运行的确认,可以确定设备在投入生产使用前的一系列工作已经达到要求。
6.2通过对压缩空气系统的性能确认,可确认压缩空气系统的综合性能已经达到生产使用要求。
6.3通过对设备部操作人员进行操作标准规程、维护保养标准操作规程的培训,操作者完全能能够胜利此工作。
7再验证与验证周期出现以下情况时,需要进行再验证:7.1该设备在使用过程中,若进行重要技术改造或变更时,必须进行再验证7.2如生产无其他特殊情况,压缩空气系统的再验证周期定为一年。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.验证目的检查确认本设备设计、材质、制造符合GMP要求。
通过对该设备安装、运行、性能测试结果的确认,验证本系统能否达到工艺要求。
验证本系统控制功能,操作与设计相符。
2.验证小组成员组长:组员:3.设备资料本系统设备由天津市晟途净化技术设备有限公司生产,安装于口服固体制剂车间,由空气压缩机、贮气缸、冷冻干燥机、高效过滤器及分配管路组成。
空气经压缩机压缩后,经冷冻干燥机去除水份,通过高效过滤器去除尘粒,油分,由分配管路输出。
主要技术参数空气压缩机排气端压力:0.7MPa 空气压缩机温控开关设定值:95℃空气压缩机容积:3.55m3/min 主电机功率:22KW冷冻干燥机处理流量:4Nm3/min 制冷剂:R22压缩机电源:220/1/50(V/P/H2)贮气缸容积:1.0m3主机型号:Y90L-4 1.5KW4.预确认文件5.培训对参加验证人员进行验证,开箱验收,安装调试操作等内容的培训。
培训合格后方可参加测试。
检查结果_______________________________________(培训记录附后)检查人_____________________________________时间_________________________________6.安装确认6.1.设备鉴定,检查设备与合同的一致性。
检查结果____________________________________________检查人_____________________________________时间________________________________6.2.开箱验收6.2.1.设备到达后,按照《设备调研、选购、验收管理规程》对设备进行开箱检查,记录检查情况,填写《设备开箱验收入库单》。
6.2.2.技术文件检查图纸,设备使用维修说明书,出厂合格证等技术文件,并做好文件归档。
6.2.3.检查设备外观无损坏,材质及包装符合要求。
(见附件8)检查结果_________________________________________检查人___________________________________检查时间__________________________________ 6.3.设备清洁润滑设备安装前应将设备进行全面清洁,各润滑点加注新润滑油。
检查结果_________________________________________(设备清洁润滑记录附后)检查人___________________________________检查时间________________________________ 6.4.材质检查全面检查系统各组成设备,检查其材质,数量是否符合合同及安装使用说明书的要求。
主要零部件检查结果_________________________________________检查人___________________________________检查时间_______________________________6.5.检查设备所附计量仪表是否已进行校验,校验是否合格检查结果_________________________________________ 见附件1检查人___________________________________检查时间_______________________________6.6.主机安装主机安装位置符合《车间设备安装平面图》要求,安装操作按照产品说明书要求,连接正确,接口严密。
阀门、开关、仪表安装正确。
电源与设备连接正确,电压380V,有接地保护。
检查结果_________________________________________(设备安装记录附后)检查人___________________________________检查时间_______________________________6.7.高效过滤器检查检查高效过滤器安装正确,材质证明,合格证性能指标测试报告完整。
检查结果_________________________________________检查人___________________________________检查时间_______________________________6.8安装确认结论(附件2)结论:签字___________________________________ 签字时间_______________________________批准人________________________________ 批准时间_______________________________7.运行及性能确认7.1.验证目的确认生产的压缩空气能够满足生产工艺要求。
7.2.开启设备,稳定运行20分钟后,检查系统各部分是否正常,管路是否有泄漏。
检查结果_________________________________________检查人___________________________________检查时间_______________________________7.3.压缩空气的外观取洁净的白色棉布,折叠3层,套在取样口,调节压力,缓慢放出压缩空气,5分钟后取下观察,目测棉布过滤面,应无异物,油斑。
每个用气点均取样检测,每天一次,连续三天。
可接受标准:所有点均应符合企业压缩空气质量标准的要求。
检查结果_________________________________________检查人___________________________________检查时间_______________________________7.4.压缩空气的水分用软管将压缩空气通入变色硅胶,注意调节压力,使压缩空气缓慢通过变色硅胶,10分钟后观察硅胶应不变色。
检查结果_________________________________________检查人___________________________________检查时间_______________________________7.5压缩空气的油分取洁净的滤纸,折叠3层,套在取样口,调节压力,缓慢放出压缩空气,5分钟取下观察,应无油斑。
检查结果_________________________________________检查人___________________________________检查时间_______________________________7.6压缩空气微生物测定7.6.1.材料灭菌生理盐水耐压导管7.6.2.取样准备配制生理盐水,盛于锥形瓶中,100ml/瓶,121℃灭菌30钟备用。
将耐压导管浸泡在75%的酒精中至少1小时消毒备用。
7.6.3.操作步骤在压缩空气的使用点处安装已灭菌的耐压胶管,将胶管的终端放入灭菌的生理盐水瓶中,打开阀门,调好压力,使气体缓慢进入100ml灭菌生理盐水中,保持15分钟(相当收集量为1m3),随后关闭阀门,盖好胶塞,封严口。
按相同的方法连续三天监测。
取上述生理盐水1ml,注入一个平皿,倒入营养琼脂培养基,于30~35℃培养48小时计菌落数。
每个样做2个平皿,以平均值报告。
取一瓶空白生理盐水做阴性对照。
7.6.4.合格标准见附件<50个/瓶检查结果_________________________________________(检验原始记录,检验报告附后)检查人___________________________________检查时间______________________________7.7尘埃粒子测定7.7.1.采用尘埃粒子计数器测量压缩空气尘埃粒子数量。
7.7.2.操作步骤取洁净的塑料袋(容积约30L),取样口用软管连接压缩空气,调节压力,,先放入压缩空气使其充满塑料袋,取下塑料袋并挤压,排掉袋中的空气后。
再重复上述步骤,再次使压缩空气充满袋子,用手握住袋口,将尘埃粒子计数器的采样器用软管连接伸入袋中取样监测。
每次2.83L。
每个监测两次,取平均值。
评价标准:尘埃粒子最大允许数:≥0.5μm,应≤3500000粒/m³≥5μm ,应≤20000粒/m³, 7.7.3.合格标准尘埃粒子最大允许数≥0.5μm3500000粒/m3≥5μm 20000粒/m3检查结果_________________________________________(检验原始记录,检验报告附后)检查人___________________________________检查时间______________________________7.8.运行及性能确认结论结论:签字___________________________________ 签字时间_______________________________批准人________________________________ 批准时间_______________________________8.验证评价签字___________________________________ 签字时间_______________________________批准人________________________________ 批准时间_______________________________9.建议建议人__________________________________建议时间_______________________________批准人________________________________ 批准时间_______________________________。
