高中生物课程中常见染色剂染色原理及使用注意事项
高中生物实验中酒精、盐酸,氢氧化钠、染色剂、细胞状态、使用显微镜的实验总结

高中生物实验中酒精、盐酸,氢氧化钠、染色剂、细胞状态、使用显微镜的实验总结高中生物实验中酒精的作用1、体积分数为50%的酒精 (必修1 P18)作用洗去浮色。
原理苏丹?是弱酸性染料,易溶于体积分数为50%酒精。
应用脂肪的鉴定实验。
2、体积分数为95%的酒精 (必修1 P115,必修2 P88)作用: 解离原理:用质量分数为15%的盐酸和体积分数为95%的酒精1?1混合,能使组织中的细胞相互分离开来。
应用:观察植物细胞的有丝分裂;低温诱导植物染色体数目的变化(冲洗卡诺氏液)。
3、体积分数为70%的酒精(75%酒精也可以)作用:消毒杀菌。
原理:体积分数为75%的酒精,能够顺利地渗入到细菌体内,吸收细菌蛋白的水分,使其脱水变性凝固而失去功能,以达到消毒杀菌的目的。
应用:果酒和果醋的制作(选修1 P4)微生物的培养;植物组织培养(选修1P34)。
70%的酒精擦拭双手,擦拭接种台。
土壤中小动物类群丰富度的研究(作为防腐剂,保存土壤小动物必修3 P76) 4、无水乙醇 (必修1 P97)作用:提取色素。
原理:叶绿体中的各种色素均是有机物,能溶解在有机溶剂中,各色素在无水酒精中的溶解度较大,且酒精无毒,方便操作。
应用:绿叶中色素的提取与分离。
5、工业酒精(一般是体积分数为95%的酒精)作用燃烧加热。
原理酒精是富含能量的有机物,燃烧能产生大量的热量。
应用必须加热的实验,如生物组织中还原糖的鉴定(必修1 P18),比较过氧化氢在不同条件下的分解(必修1P),微生物培养(选修1P15、21),胡萝卜素的提取、分离鉴定(选修1P78)等实验。
高中生物实验中盐酸的作用1、实验:观察DNA和RNA在细胞中的分布必修1 P26(1) 质量分数8%盐酸(水解)能改变细胞膜的通透性,加速染色剂进入细胞; (2) 质量分数8%盐酸(水解)使染色体中DNA与蛋白质分离,便于DNA与染色剂结合。
2、实验:影响酶活性的条件必修1 P84质量分数5%盐酸用于调节PH值。
染色的基本原理、方法及注意事项!

染⾊的基本原理、⽅法及注意事项!染⾊的基本原理、⽅法及注意事项!!染⾊的基本原理、⽅法及注意事项百欧博伟⽣物涂⽚及染⾊是微⽣物学的基本技术,也是观察细菌最简单且⾏之有效的⽅法。
通常情况下,由于细菌个体较⼩,较透明或半透明,如未经染⾊往往不易观察识别。
因此借助于染⾊法可使细菌着⾊,与视野背景形成鲜明对⽐,从⽽易于在显微镜下进⾏观察。
简单染⾊法即只⽤⼀种染料对涂⽚进⾏染⾊,该法简便易⾏,适⽤于菌体的⼀般形态观察。
通常情况下由于细菌菌体多带负电荷,易和带正电荷的碱性染料结合⽽被染⾊,因此常⽤碱性染料进⾏简单染⾊,如美蓝、碱性复红、结晶紫、孔雀绿、番红等。
所有的苯胺染料,均可⽤来做简单染⾊法的染⾊剂。
在进⾏染⾊之前的制⽚过程是影响染⾊结果好坏的关键性步骤。
制备细菌染⾊⽚⼀般要经过涂⽚、固定、染⾊、⽔洗、⼲燥等步骤(见下图),然后⽤显微镜,甚⾄油镜观察。
(⼀)涂⽚取⼀⼲净的载玻⽚,滴加⼀⼩滴蒸馏⽔于载玻⽚中央。
按⽆菌操作要求,接种环经灼烧灭菌,待冷却后⽤接种环从菌种试管斜⾯上(培养⽫表⾯)挑取少量培养物(不要挑破培养基),置于载玻⽚上的⽔滴中,与⽔混合并轻轻涂布成直径约1cm左右的均匀薄层。
操作完成后,接种环要再经灼烧灭菌,放归原处。
(⼆)⼲燥将涂⽚于室温中⾃然⼲燥或者置于酒精灯⽕焰⾼处,微热烘⼲。
切记不能直接在⽕焰上烘烤,以免菌体烤焦变形,影响对菌体的观察。
(三) 固定涂⽚标本⾯向上,快速通过酒精灯⽕焰外焰2次~3次,进⾏标本固定。
固定的⽬的在于杀死细菌以固定其细胞结构;保证菌体牢固地粘附在载玻⽚上,染⾊或⽔洗时不⾄于脱落;同时改变菌体对染料的通透性,有利于着⾊,增强染⾊效果。
固定时,以载玻⽚背⾯加热处触及⽪肤⽽不觉过烫为宜(⼀般不超过60 )。
(四)染⾊标本玻⽚⽔平放置,滴加1滴~2滴染⾊液,使染⾊液完全覆盖涂⽚区域,染⾊时间视不同标本和染料的性质⽽定。
(五)⽔洗染⾊到⼀定时间后,倾去染液,斜置玻⽚,⾃玻⽚上端⽤⾃来⽔冲洗⾄流下的⽔⽆⾊为⽌;或将玻⽚置于玻⽚架上,⽤洗瓶倾注⽔流进⾏⽔洗。
高中生物常用的染色剂染色机理

普知--关于遗传物质被碱性染料染色~碱性液染色后能保持几年。
洋红溶液出现浑浊时要过滤后再用1.2龙胆紫C笛HIN具有金属光泽的暗绿色粉末。
能溶于水、三氯甲烷和醇;难溶于醚。
加热至275℃分解。
其1%一2%溶液俗称紫药水,是人们所熟悉的外用药。
2染色剂的配制2.1配方1醋酸一洋红染液取100mL45%冰醋酸,煮沸后徐徐加入洋红1g,搅拌均匀后加入1颗锈铁钉,煮沸10min,冷却后过滤,贮存在棕色瓶内。
2.2配方2龙胆紫染液,取龙胆紫1~2g,溶解在100mL2%乙酸溶液中,直到溶液成深紫色为止(实验过程中视具体情况溶液可适当稀释)。
保存在棕色瓶内。
3染料的作用机理3.1碱性染料染色试剂的酸碱性与溶液的酸碱性不是一回事。
染色试剂的酸碱性,其划分依据在于染料分子电离后的有色成分是阳离子还是阴离子,如果着色的基团是阳离子的为碱性染料,着色的基团是阴离子的为酸性染料3_2染色机理龙胆紫能不能染DNA?还是只是把染色质上的蛋白质染色?或是DNA和蛋白质都被染色?上文提到,碱性染料的着色基团是阳离子,着色基团可以与细胞中的带负电荷部分牢固地结合。
DNA是酸性物质,可电离出H,其余的部分就带上了负电荷。
因此,带负电荷部分就能和碱性染料电离出的着色阳离子通过电荷问的引力作用牢固结合,而被染上颜色。
有的染色作用随溶液中的pH值而变动。
细胞的主要成分是蛋白质,它含有氨基和羧基,在酸性溶液中,当溶液的pH值小于该蛋白质的等电点时,则蛋白质带正电荷,易被酸性染料染色;在碱性溶液中,当溶液的DH值大于该蛋白质的等电点时,则蛋白质带负电荷。
容易被碱性染料染色。
所以,可以得出结论:碱性染料使染色体着色,使DNA和蛋白质都被染色。
只不过这2种物质被染色的机理是不同的。
4碱性染料用酸配制的原因龙胆紫和洋红都溶于水和酒精。
而做实验用的龙胆紫和洋红溶液。
却都是用醋酸溶液配制的。
这又是为什么呢?原因有2个:1)是为了染色物能方便地进入细胞内,又不会发生细胞膨胀。
高考生物知识点总结染色剂

高考生物知识点总结染色剂染色剂是一种特定的化合物或物质,常用于染色实验、工业生产以及日常生活中。
在生物学中,染色剂在显微镜下用于染色细胞和组织,以便观察和研究其结构和功能。
下面将对高考生物中与染色剂相关的知识点进行总结。
一、染色剂的分类染色剂可以根据其化学性质和应用领域进行分类。
常见的分类包括:1.生物染色剂:如增强细胞和组织的对比度,使其更易于观察。
常见的生物染色剂有伊红、姬蓝、甲苯红等。
2.生理染色剂:用于检测生物体内各种化学成分的存在和变化,如碘液检测淀粉、苏丹红检测脂肪等。
3.荧光染料:具有荧光性质的染色剂,可用于显微镜下观察光学反应和细胞成分。
亚甲基蓝和荧光素是常见的荧光染料。
4.工业染料:应用于纺织、皮革和造纸等工业领域的染料,如亚甲基橙、甲基紫等。
二、染色剂的作用原理染色剂通过与物质的化学反应或物理吸附,使其显色。
主要的作用原理有:1.酸碱性染色:染料与细胞或组织中的某种成分发生酸碱反应,达到染色的目的。
例如靛蓝染色DNA时,DNA的磷酸基团与靛蓝形成盐类。
2.亲和性染色:染料与细胞或组织中的某种成分具有生物亲和性,通过物理吸附来染色。
例如血红蛋白与伊红发生亲和性染色。
3.氧化还原反应染色:某些染剂需要经过氧化还原反应才能显色。
例如苏丹红通过氧化还原反应将脂肪染色为红色。
三、染色剂在生物学中的应用染色剂在生物学中具有广泛的应用,如:1.组织染色:通过染色剂将组织特定的结构或成分显色,便于观察和研究。
常用的组织染色剂有伊红、姬蓝、碘液等。
2.细胞染色:染色剂可以用于染色细胞的不同部位或细胞器,如细胞核、线粒体等。
常用的细胞染色剂有苏丹红、亚甲基蓝等。
3.生物化学实验:染色剂在生物化学实验中用于检测和分析特定的化学成分。
例如用碘液检测淀粉或重铬酸钾检测脂肪。
4.药物研发:染色剂在药物研发过程中用于观察和评估新药的吸收、分布和代谢情况。
四、染色剂的安全性和环保性染色剂在使用过程中需要注意其安全性和环保性。
高中生物必修一实验知识点总结

绿叶中的色素不止一种,他们都能溶解在层析液中。然而,它们在层析液中的溶 解度不同;溶解度高的随层析液在滤纸上扩散的快;反之则慢。这样,几分钟之 后绿叶中的色素就会随着层析液在滤纸上的扩散而分离开。且溶解度最高的是胡 萝卜素,它随层析液在滤纸上扩散的最快;叶黄素和叶绿素a的溶解度次之,叶 绿素b的溶解度最低,扩散的最慢。
比较项目
斐林试剂
双缩脲试剂
使用方 法
呈色反 应条件 不 同 反应原 点 理 颜色 浓度 相同点
甲液和乙液混合均匀后 使用时先加A液再加B 方可使用,且现配现用 液
需水浴加热 不需加热即可反应
还原糖中的醛基被 Cu(OH)2氧化, Cu(OH)2被还原为 Cu2O
砖红色
具有两个以上肽键的化 合物在碱性条件下与 Cu2+反应生成络合物
问题探讨: 1、在做还原糖、蛋白质鉴定的实验时,为什么要留出 一部分样液? 作对照 2、使用双缩脲试剂时为什么B液只能加3~4滴而不能 过量?
过量的双缩脲试剂B会与试剂A反应,使溶液呈蓝色,
而掩盖生成的紫色。
3、为什么斐林试剂要现配现用,不能放置太久? 时间太长,Cu(OH)2悬浊液就沉淀在试管底部而 无法参与反应。
取少量脂肪样液,加入苏 丹Ⅲ,震荡,可看到溶液 呈了橘黄色,本实验我们 用苏丹Ⅲ做染液。
蛋白质+双缩脲试剂→紫色络合物
豆浆、蛋清、牛奶都是很 好的实验材料。
本实验我们用蛋清做实验材料, 在用蛋清做实验材料时,要注意 将蛋清稀释,如果稀释不够,反 应后的产物会粘固在试管内壁上, 使反应不容易彻底。
深化
实验课题:观察DNA和RNA在细胞中的分布 一、实验原理 1.碱性染料能使核酸着色,甲基绿和吡罗红均为碱性染料; DNA﹢甲基绿→绿色,RNA ﹢吡罗红→红色。 甲基绿与吡罗红作为混合染料使用可显示细胞中DNA和RNA在细胞中的分布。 2.盐酸能够改变细胞膜的通透性,加速染色剂进入细胞,同时使染色体中的DNA与 蛋白质分离,有利于DNA与染色剂结合。
高中生物实验颜色反应与各种试剂作用总结

高中生物颜色反应1.还原糖+斐林试剂→砖红色沉淀2.苏丹Ⅲ+脂肪→橘黄色;苏丹Ⅳ+脂肪→红色3.蛋白质+双缩脲试剂→紫色4.淀粉+碘液→蓝色5.DNA的染色与鉴定染色原理:DNA+甲基绿→绿色应用:可以显示DNA在细胞中的分布。
鉴定原理:DNA+二苯胺→蓝色应用:用于DNA粗提取实验的鉴定试剂。
6.RNA的染色与鉴定染色原理:RNA+吡罗红→红色应用:可以显示RNA在细胞中的分布。
注意:在观察DNA和RNA在细胞中的分布时用的是甲基绿和吡罗红混合染色剂,而不是单独染色,而且要现配现用。
7.健那绿专一性染线粒体的活细胞染料原理:健那绿(Janus green B)染液,是专一性染线粒体的活细胞染料,可以使活细胞中的线粒体呈现蓝绿色,而细胞质接近无色。
线粒体能在健那绿染液中维持活性数小时,通过染色,可以在高倍显微镜下观察到生活状态的线粒体的形态和分布。
(另:观察细胞中叶绿体不用染色)8.酒精的检测原理:橙色的重铬酸钾溶液在酸性条件下与酒精发生化学反应,变成灰绿色。
9.CO2的检测原理:CO2可以使澄清的石灰水变混浊,也可使溴麝香草酚蓝水溶液由蓝变绿再变黄。
10.染色体(或染色质)的染色原理:染色体容易被碱性染料(如龙胆紫溶液或醋酸洋红溶液或改良的苯酚品红)染成深色。
应用:用高倍镜观察细胞的有丝分裂。
11.亚硝酸盐的检测出现玫瑰红原理:在盐酸酸化条件下,亚硝酸盐与对氨基苯磺酸发生重氮化反应后,与N-1-萘基乙二胺盐酸盐结合形成玫瑰红色染料。
应用:将显色反应后的样品与已知浓度的标准液进行目测比较,可以大致估算出泡菜中亚硝酸盐的含量。
12.脲酶的检测原理:细菌合成的脲酶可以将尿素分解成氨,氨会使培养基的碱性增强,使PH升高,从而使酚红指示剂变红。
应用:在以尿素为唯一氮源的培养基加入酚红指示剂,培养某种细菌后,看指示剂变红与否可以鉴定这种细菌能否分解尿素。
13.伊红美蓝检测大肠杆菌原理:在伊红美蓝培养基上,大肠杆菌的代谢产物(有机酸)与伊红美蓝结合使菌落呈现黑色。
高考生物试题中有关染色剂使用的考查

高考生物试题中有关染色剂使用的考查一染色剂的应用1 DNA和RNA的染色鉴定甲基绿和吡罗红是混合染色剂。
甲基绿是具有金属光泽的绿色微结晶或亮绿色粉末。
溶于水,显蓝绿色。
稍溶于乙醇,不溶于戊醇。
吡咯在盐酸作用下聚合成为吡咯红,可与 RNA 结合呈现红色。
这两种染色剂对DNA和RNA的亲和力不同,甲基绿使DNA呈现绿色,吡罗红使RNA呈现红色。
利用甲基绿、吡罗红混合染色剂将细胞染色,可以观察到DNA和RNA在细胞中的分布情况。
注意:①盐酸能改变细胞膜的通透性,加速染色剂进人细胞,同时使染色体中的DNA与蛋白质分离,有利于DNA与染色剂结合。
② 2种染色剂要混合使用,而且要现配现用。
2 健那绿染液与线粒体的观察健那绿染液是专一性的线粒体的活细胞染料,线粒体中细胞色素氧化酶使染料保持氧化状态( 即有色状态)呈蓝绿色,而在周围的细胞质中染料被还原成为无色状态。
因此可以使活细胞中的线粒体呈现蓝绿色,而细胞质接近无色。
线粒体能在健那绿染液中维持活性数小时,通过染色,可以在高倍显微镜下观察到生活状态的线粒体的形态和分布。
3. 碱性染料与染色体的观察生物实验中所用的染料,按其来源可分为天然染料和人工染料两大类。
人工染料根据其主要化学成分的性质,又分成碱性染料、酸性染料和中性染料三大类,其碱性、酸性和中性是由染料中有色部分的性质所决定的。
若染料的有色部分为阴离子,即为“酸性”染料;若染料的有色部分为阳离子,则称为“碱性”染料;若染料的阴、阳离子均有颜色,则称为“中性”染料。
染色体(质)是细胞核内容易被碱性染料染成深色的物质。
在观察植物细胞有丝分裂实验中,常用龙胆紫溶液使染色体染成紫色,也使用醋酸洋红溶液使染色体着红色。
二者染色时间都不可过长。
l %~ 2 %龙胆紫溶液俗称紫药水,是人们所熟悉的外用药。
龙胆紫溶液的配制是将龙胆紫溶解在质量分数为2%的醋酸溶液中配制而成。
染色中使用的龙胆紫溶液略呈酸性,l%醋酸洋红本身也是酸性,同样具有碱性的助色基团。
高一生物染色知识点

高一生物染色知识点生物染色是生物学研究中重要的技术手段之一,通过染色可以使细胞、组织和器官的结构更加清晰可见,方便观察和研究。
本文将介绍一些高一生物学中常见的染色知识点,包括原核生物染色、真核生物染色以及染色体的结构和功能。
一、原核生物染色原核生物是指没有真核细胞核的生物,如细菌。
在对原核生物进行染色时,常用的染色方法有革兰氏染色和抗酸抗碱染色。
革兰氏染色是一种常用的细菌染色方法,分为革兰氏阳性染色和革兰氏阴性染色。
革兰氏阳性细菌染色后呈紫色,而革兰氏阴性细菌染色后呈粉红色。
抗酸抗碱染色可用于鉴定结核杆菌等具有酸酶分泌能力的细菌。
抗酸染色方法中最常用的是抗酸快速染色法和抗酸琼脂红法,染色后结核杆菌呈红色。
二、真核生物染色真核生物是指具有真核细胞核的生物,如动植物细胞。
在对真核生物进行染色时,常用的染色方法有核染色和细胞器染色。
核染色常用的染料有伊红、格里姆萨染料、苏木精和五甲基绿等。
对细胞核进行染色后,能够使核的形态结构清晰可见,便于研究细胞核的内部组织。
细胞器染色是对特定的细胞器进行染色,常用的染料有苏木素、亮蓝色素和伊红等。
细胞器染色可以使细胞器的形态和分布情况更加明显,帮助研究细胞器的功能和作用机制。
三、染色体的结构和功能染色体是生物体细胞核中的一种细长的结构,它携带了生物体遗传信息的基本单位。
染色体由DNA和蛋白质组成。
染色体的主要功能是储存和传递遗传信息。
在染色体的结构中,中心区域为着丝粒,两侧为染色体臂。
着丝粒的主要作用是参与有丝分裂过程中染色体的运动和分离。
染色体臂则包含了基因信息,其中的DNA序列决定了生物体的遗传特征。
染色体能够通过染色体构象变化来调控基因的表达。
在正常的细胞周期中,染色体会发生收缩、扩展、屈曲等不同的构象变化,从而使得特定的基因在特定的时期被启动或关闭。
这样,生物体可以根据不同的环境和发育需求来调控基因的表达,实现细胞的分化和功能的多样化。
总结生物染色是生物学研究中的重要技术,通过染色可以使细胞和组织的结构更加清晰可见,便于观察和研究。
考马斯亮蓝染色总结

考马斯亮蓝染色总结考马斯亮蓝染色是一种常用的染色技术,在细胞学、组织学、生物学和医学等领域中被广泛使用。
它能够使细胞和组织的结构和成分在显微镜下清晰可见,便于观察和分析。
本文将对考马斯亮蓝染色的原理、步骤、应用以及优缺点进行详细的总结。
首先,我们来介绍考马斯亮蓝染色的原理。
考马斯亮蓝是一种碱性染料,它能与细胞和组织中的酸性成分结合,形成可见的颜色。
它主要与核酸、一些蛋白质和类脂质等结合。
考马斯亮蓝染色的原理是通过酸碱反应,使细胞和组织的酸性成分能与考马斯亮蓝发生结合,形成明亮的蓝色,从而使细胞和组织的细节清晰可见。
接下来,我们将介绍考马斯亮蓝染色的步骤。
考马斯亮蓝染色的步骤主要包括固定、脱水、脱脂、染色和封片。
首先,固定是将待染色的细胞或组织固定在载玻片上,一般使用甲醛等常见的固定剂。
然后,脱水是将样本经过一系列酒精梯度溶液进行脱水处理,以除去细胞和组织中的水分。
接着,脱脂是用苯、醇和苯酚等溶剂将固定的样本中的脂质等脂溶性物质清洗掉。
随后,样本进行染色,一般使用考马斯亮蓝溶液进行染色,时间一般为数分钟至数十分钟不等。
最后,样本进行封片,将其与封片剂混合后覆盖载玻片,以保护和固定样本。
然后,我们来介绍考马斯亮蓝染色的应用。
考马斯亮蓝染色在生物学和医学研究中有广泛的应用。
在细胞学和组织学中,考马斯亮蓝染色可用于观察细胞和组织的形态、结构和成分,如细胞核形态、染色体结构、细胞器分布等。
在病理学中,考马斯亮蓝染色可用于检测肿瘤细胞的增殖和分化情况,辅助诊断和分析。
此外,考马斯亮蓝染色还可应用于植物学中观察植物的细胞和组织结构,饮食学中观察食物中的纤维成分等。
最后,我们来探讨考马斯亮蓝染色的优缺点。
考马斯亮蓝染色具有染色效果明显、染色时间短、成本低等优点,能够提供有关细胞和组织结构的重要信息。
然而,考马斯亮蓝染色也存在一些缺点,如对细胞和组织的杀伤性较大,染色的特异性不高等。
综上所述,考马斯亮蓝染色作为一种常用的染色技术,在生物学和医学领域中具有广泛的应用。
伊红染色原理

伊红染色原理伊红染色是一种广泛应用于生物学、医学、病理学等领域的染色技术。
它的原理是利用伊红染剂对细胞或组织中的核酸、蛋白质等物质进行染色,从而使其在显微镜下更加清晰可见。
本文将介绍伊红染色的原理、方法、应用及注意事项。
一、伊红染色的原理伊红染色的原理是利用伊红染剂对细胞或组织中的核酸、蛋白质等物质进行染色。
伊红是一种碱性染料,它能够与细胞中的酸性物质如核酸、核蛋白等结合,从而呈现出红色或蓝色的颜色。
伊红染色的原理是基于酸碱理论的,即伊红染剂是一种碱性染料,它能够与酸性物质结合,形成盐类,从而呈现出颜色。
二、伊红染色的方法伊红染色的方法主要分为以下几个步骤:1、取适量的细胞或组织样本,将其固定在载玻片上。
2、用乙醇或甲醇等溶剂使细胞或组织透明化。
3、用伊红染剂浸泡样本,让其充分染色。
4、用去离子水洗去多余的染料。
5、用苏木精或其他染料染色,以增强对比度。
6、用去离子水洗去多余的染料。
7、最后用透明剂覆盖载玻片,使其光滑。
三、伊红染色的应用伊红染色技术在生物学、医学、病理学等领域有着广泛的应用。
以下是伊红染色的应用举例:1、细胞和组织形态学研究:伊红染色可以使细胞和组织的形态结构更加清晰可见,从而有助于细胞和组织的形态学研究。
2、病理学诊断:伊红染色可以用于病理学诊断,如肿瘤的诊断、炎症的诊断等。
3、生物医学研究:伊红染色可以用于生物医学研究,如对DNA、RNA、蛋白质等生物分子的研究。
4、食品检测:伊红染色可以用于食品检测,如检测鱼肉中的寄生虫等。
四、伊红染色的注意事项1、样本处理要注意:样本处理对伊红染色结果有着很大的影响,因此要注意样本的固定、透明化、染色等操作。
2、染色时间要掌握好:染色时间过长会导致染色过度,染色时间过短会导致染色不充分,因此要掌握好染色时间。
3、注意控制染料浓度:染料浓度过高会导致染色不均匀,浓度过低会导致染色不充分,因此要注意控制染料浓度。
总之,伊红染色是一种重要的生物学、医学、病理学等领域的染色技术,它的应用广泛,但在操作时要注意样本处理、染色时间、染料浓度等方面的控制,以保证染色结果的准确性和可靠性。
高中生物实验染色剂染色原理

高中生物实验染色剂染色原理作为染色剂必须具备两个条件:一是具有颜色;二是要与被染组织间有亲和力。
染料的颜色和它与组织间的亲和力是由染料本身的分子结构决定的,产生颜色的发色基团和与组织间产生亲和力的助色基团共同决定了染色剂的染色性质。
作为染料物质,除了有发色基团外,还需要有一种使化合物发生电离作用的助色基团。
染色剂的酸、碱性界定并非由染料溶液的pH值决定,而是根据染料物质中助色基团电离后所带的电荷来决定。
一般来说,助色基团带正电荷的染色剂为碱性染色剂,反之则为酸性染色剂。
1 甲基绿和吡罗红:甲基绿和吡罗红两种染色剂对DNA和RNA的亲和力不同,甲基绿使DNA呈现绿色,吡罗红使RNA呈现红色.利用甲基绿,吡罗红混合染色剂将细胞染色,可以显示DNA和RNA在细胞中的分布.2 龙胆紫和醋酸洋红:染色质(体)容易被碱性染料染成深色。
醋酸洋红常被用作核、染色体的固定和染色剂。
在煮沸的45%醋酸中加洋红使之饱和,再加入微量的铁离子,便使醋酸洋红材料在为醋酸固定的同时,洋红将核或染色体染成红色。
用龙胆紫可将染色体染成蓝紫色。
3 伊红美蓝:伊红和美蓝是两种苯胺类染料,可以抑制革兰氏阳性菌的生长。
同时,这些染料可以区分那些发酵乳糖的微生物。
大肠菌群因其强烈发酵乳糖而产生大量的混合酸,使菌体表面带上正电荷,可染上伊红染料,伊红与美蓝结合,菌体被着上深紫色,在含有两种染料呈紫色的培养基上,形成带核心、具金属光泽的菌落。
因此可以用伊红和美蓝鉴别革兰氏阴性菌(大肠杆菌)的存在。
4 二苯胺二苯胺是一种非极性芳香族有机分子,有毒,熔点比水低,微溶解于水,易溶解于酒精、冰乙酸等有机溶剂。
化学性质活泼,遇光易变色。
因此要放置于暗处保存。
二苯胺试剂鉴定DNA的原理:DNA分子中的脱氧核糖在酸性环境下生成ω-羟基-γ-酮基戊醛,再与二苯胺试剂结合显蓝色,颜色的深浅与溶液中的DNA含量成正比。
5 双缩脲:鉴定生物组织中是否含有蛋白质时,常用双缩脲法,使用的是双缩脲试剂,发生的是双缩脲反应。
高中生物染色剂大全
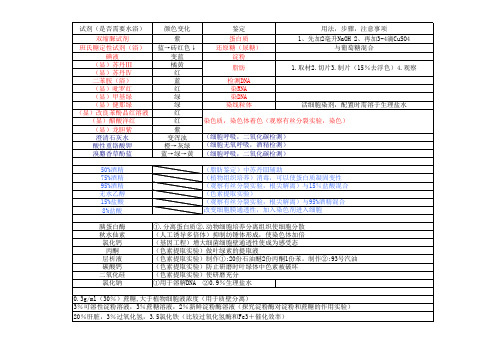
鉴定
蛋白质 还原糖(尿糖)
淀粉
脂肪
检测DNA 染RNA 染DNA 染线粒体
用法,步骤,注意事项 1、先加2毫升NaOH 2、再加3-4滴CuSO4
与葡萄糖混合 1.取材2.切片3.制片(15%去浮色)4.观察
活细胞染剂,配置时需溶于生理盐水
染色质,染色体着色(观察有丝分裂实验,染色)
(细胞呼吸,二氧化碳检测) (细胞无氧呼吸,酒精检测) (细胞呼吸,二氧化碳检测)
0.3g/ml(30%)蔗糖,大于植物细胞液浓度(用于质壁分离) 3%可溶性淀粉溶液,3%蔗糖溶液,2%新鲜淀粉酶溶液(探究淀粉酶对淀粉和蔗糖的作用实验)
20%肝脏,3%过氧化氢,3.5氯化铁(比较过氧化氢酶和Fe3+催化效率)
氯化钙 丙酮 层析液 碳酸钙 二氧化硅 氯化钠
①.分离蛋白质②.动物细胞培养分离组织使细胞分散 (人工诱导多倍体)抑制纺锤体形成,使染色体加倍 (基因工程)增大细菌细胞壁通透性使成为感受态 (色素提取实验)做叶绿素的提取液 (色素提取实验)制作①:20份石油醚2份丙酮1份苯。制作②:93号汽油 (色素提取实验)防止研磨时叶绿体中色素被破坏 (色素提取实验)使研磨充分 ①用于溶解DNA ②0.9%生理盐水
50%酒精 75%酒精 95%酒精 无水乙醇 15%盐酸 8%盐酸
(脂肪鉴定)中苏丹Ⅲ辅助 (植物组织培养)消毒,可以使蛋白质凝固变性 (观察有丝分裂实验,根尖解离)与15%盐酸混合 (通透性,加入染色剂进入细胞
胰蛋白酶 秋水仙素
试剂(是否需要水浴)
双缩脲试剂 班氏糖定性试剂(浴)
碘液 (显)苏丹Ⅲ (显)苏丹Ⅳ 二苯胺(浴) (显)吡罗红 (显)甲基绿 (显)健那绿 (显)改良苯酚品红溶液 (显)醋酸洋红 (显)龙胆紫
高中生物实验染色剂染色原理

高中生物实验染色剂染色原理一、染色剂选择原则:1.选择合适的染色剂:根据实验目的选择合适的染色剂。
例如,要染色细胞核,可以选择染色剂伊红或甲基绿染色;若要染色细胞器,如线粒体、内质网等,可以选择适合的染色剂。
2.染色剂的稳定性:染色剂应具有稳定的化学性质,不易分解,否则会影响实验结果的准确性。
3.染色剂的渗透性:染色剂要能够渗透到细胞内,使其与目标结构发生作用。
4.染色剂的特异性:染色剂应具有选择性作用,即只与目标结构发生特异性作用,而不与其他结构发生作用。
二、染色原理:染色剂的染色原理主要有两种类型:酸性染料和碱性染料。
1.酸性染料:酸性染料是一类带有酸性基团的染料,其分子带有正电荷。
这些染料能够与细胞内的带有负电荷的成分结合,如DNA、RNA、细胞核蛋白等。
常用的酸性染料有伊红、伊红B、甲基绿等。
以伊红染色为例,其染色原理为:伊红分子中带有阳离子基团,能够与细胞内的DNA带负电的磷酸基团结合。
伊红染料进入细胞后,与细胞核中的DNA结合,使细胞核染成红色,从而使细胞核更加清晰可见。
2.碱性染料:碱性染料属于带有碱性基团的染料,其分子带有负电荷。
这类染料能够与细胞内带有正电荷的成分结合,如细胞质中的酸性蛋白、线粒体等。
常用的碱性染料有甲苯黑、苏木素、溴酚蓝等。
以甲苯黑染色为例,其染色原理为:甲苯黑分子中带有阴离子基团,能够与细胞质中带正电的成分结合,如蛋白质等。
甲苯黑染料进入细胞后,与蛋白质结合,使细胞质染成黑色,从而使细胞质更加清晰可见。
三、染色剂染色过程:染色剂的染色过程通常包括几个步骤:固定、染色、洗涤和封片。
1.固定:细胞固定是为了使细胞结构保持原貌,并防止细胞溶解或变形。
常用的固定剂有甲醛、福尔马林等。
2.染色:将染色剂溶液滴在细胞上,使其充分与细胞结构发生作用。
一般情况下,染色时间不宜过长,以免染色剂过多或过深,影响观察结果。
3.洗涤:染色剂作用完毕后,需要用适量的缓冲液或蒸馏水洗去多余的染色剂,以免对观察造成干扰。
高中生物颜色反应知识点总结

高中生物颜色反应知识点总结一、细胞中的颜色反应概述在高中生物实验中,颜色反应是一种常用的观察和区分细胞内不同化学物质的方法。
通过特定的染色剂与细胞内的物质发生反应,可以产生不同颜色的变化,从而帮助我们识别和了解细胞的结构和功能。
二、核酸的颜色反应1. 甲基绿-吡罗红染色法- 原理:甲基绿与DNA结合呈现蓝绿色,吡罗红与RNA结合呈现红色。
- 应用:用于区分细胞核和细胞质中的DNA和RNA。
2. 瑞氏染色法- 原理:利用瑞氏染料与核酸的亲和力不同,使得DNA和RNA呈现不同的颜色。
- 应用:常用于观察细菌和病毒的核酸分布。
三、蛋白质的颜色反应1. 比氏试剂法- 原理:比氏试剂(含铜离子的碱性溶液)与蛋白质反应生成紫色复合物。
- 应用:用于检测和定量蛋白质。
2. 布拉德福德法- 原理:布拉德福德染料与蛋白质中的芳香族氨基酸反应,产生颜色变化。
- 应用:用于蛋白质浓度的测定。
四、糖类的颜色反应1. 安托诺夫试剂法- 原理:安托诺夫试剂与多糖反应,生成黄色至红色不等的沉淀。
- 应用:用于检测多糖。
2. 费林(Fehling)试剂法- 原理:费林试剂与还原糖在加热条件下反应,生成砖红色沉淀。
- 应用:用于检测还原糖。
五、脂类的颜色反应1. 苏丹III或苏丹IV染色法- 原理:苏丹染料与脂肪反应,生成橘黄色或红色的脂肪颗粒。
- 应用:用于检测细胞内的脂肪。
2. 脂溶性色素法- 原理:某些脂溶性色素可以与类固醇等脂类物质结合,产生特定颜色。
- 应用:用于观察和鉴定类固醇激素等脂类物质。
六、酶的颜色反应1. 酶底物法- 原理:特定酶作用于含有显色团的底物,产生颜色变化。
- 应用:用于酶活性的定性和定量分析。
2. 酶联免疫吸附法(ELISA)- 原理:利用抗体与抗原特异性结合,通过显色底物产生颜色变化来检测抗原。
- 应用:广泛应用于免疫学检测。
七、结语颜色反应在高中生物实验中占有重要地位,通过上述各种颜色反应的学习和掌握,学生可以更好地理解生物体内各种化学物质的存在和作用,为进一步的生物学学习和研究打下坚实的基础。
高中生物实验所有染色剂及其性质详解

高中生物实验所有染色剂及其性质详解1斐林试剂检测可溶性还原糖原理:还原糖+斐林试剂→砖红色沉淀注意:斐林试剂的甲液和乙液要等量混合均匀后方可使用,而且是现用现配,条件需要水浴加热.应用:检验和检测某糖是否为还原糖;不同生物组织中含糖量高低的测定;在医学上进行疾病的诊断,如糖尿病、肾炎.2苏丹Ⅲ、苏丹Ⅲ检测脂肪原理:苏丹Ⅲ+脂肪→橘黄色;苏丹Ⅲ+脂肪→红色注意:脂肪的鉴定需要用显微镜观察.应用:检测食品中营养成分是否含有脂肪.3双缩脲试剂检测蛋白质原理:蛋白质+双缩脲试剂→紫色注意:双缩脲试剂在使用时,先加A液再加B液,反应条件为常温(不需要加热).应用:鉴定某些消化液中含有蛋白质;用于劣质奶粉的鉴定.4碘液检测淀粉原理:淀粉+碘液→蓝色注意:这里的碘是单质碘,而不是离子碘.应用:检测食物中营养成分是不是含有淀粉5 DNA的染色与鉴定染色道理:DNA+甲基绿→绿色应用:能够显示DNA在细胞中的分布.鉴定道理:DNA+二苯胺→蓝色应用:用于DNA粗提取实验的鉴定试剂.6吡罗红使RNA呈现红色原理:RNA+吡罗红→红色应用:能够显示RNA在细胞中的分布.注意:在观察DNA和RNA在细胞中的分布时用的是甲基绿和吡罗红混合染色剂,而不是单独染色.7台盼蓝使死细胞染成蓝色原理:正常的活细胞,细胞膜结构完整具有选择透过性能够排斥台盼蓝,使之不能够进入胞内;死细胞或细胞膜不完整的细胞,胞膜的通透性增加,可被台盼蓝染成蓝色.应用:区分活细胞和死细胞;检测细胞膜的完整性.8线粒体的染色道理:健那绿染液是埋头性染线粒体的活细胞染料,能够使活细胞中的线粒体呈现蓝绿色,而细胞质接近无色.应用:能够用高倍镜观察细胞中线粒体的存在.9酒精的检测原理:橙色的重铬酸钾溶液在酸性条件下与酒精发生化学反应,变成灰绿色.应用:探究酵母菌细胞呼吸的方式;制作果酒时检验是否产生了酒精;检查司机是否酒后驾驶.10 CO2的检测原理:CO2可以使澄清的石灰水变混浊,也可使溴麝香草酚蓝水溶液由蓝变绿在变黄.应用:根据石灰水混浊程度或溴麝香草酚蓝水溶液变黄的时间长短,能够检测酵母菌造就液中CO2的产生情况.11染色体(或染色质)的染色道理:染色体容易被碱性染料(如龙胆紫溶液或醋酸洋红溶液)染成深色.应用:用高倍镜观察细胞的有丝盘据.12吲哚酚试剂与维生素C溶液呈褪色反应道理:吲哚酚即2,6-二氯酚靛酚钠,其水溶液为蓝紫色,维生素C具有还原性,能将其褪色.应用:可用于检测食品营养成分中是否含有维生素C.13亚硝酸盐的检测出现玫瑰红原理:在盐酸酸化条件下,亚硝酸盐与对氨基苯磺酸发生重氮化反应后,与N-1-萘基乙胺盐酸盐结合形成玫瑰红色染料.应用:将显色反应后的样品与已知浓度的标准液进行目测比较,可以大致估算出泡菜中亚硝酸盐的含量.14脲酶的检测道理:细菌合成的脲酶能够将尿素分解成氨,氨会使造就基的碱性增强,使PH降低,从而使酚红唆使剂变红.应用:在以尿素为唯一氮源的培养基加入酚红指示剂,培养某种细菌后,看指示剂变红与否可以鉴定这种细菌能否分解尿素.15伊红美蓝检测大肠杆菌原理:在伊红美蓝培养基上,大肠杆菌的代谢产物(有机酸)与XXX结合使菌落呈现黑色.应用:用滤膜法测定水中大肠杆菌的含量.16刚果红检测纤维素分解菌道理:刚果红是一种染料,它能够与像纤维素这样的多糖物资形成白色复合物,但其实不和水解后的纤维二糖和葡萄糖发生这种反应.当在含有纤维素的造就基中插手刚果红时,刚果红能与造就基中的纤维素形成白色复合物.当纤维素被纤维素分解菌分解后,刚果红-纤维素的复合物就没法形成,造就基中会出现以纤维素分解菌为中心的透明圈.应用:筛选纤维素分解菌.弥补(有局部重复):1、斐林试剂配制:1)甲液质量浓度为0.1g/ml,取10gNaOH溶于蒸馏水,稀释至100ml2)乙液质量浓度为0.05g/ml,取5gCuSO4溶于蒸馏水,稀释至100ml临用时将甲、乙液等量混合作用:鉴定还原性糖:C6H12O6、果糖、麦芽糖、乳糖等.还原性糖与斐林试剂发生作用,生成砖红色沉淀.如用于鉴定组织液中有否还原性糖、糖尿病人尿成分分析、酶专一性探索等.2、班氏尿糖定性试剂配制:称取17.4克无水硫酸铜(CuSO4)溶解于100毫升热蒸馏水中,冷却后,稀释到150毫升.称取柠檬酸钠173克及无水碳酸钠(Na2CO3)100克,加蒸馏水600毫升,加热使之溶解,冷却后,稀释到850毫升.把硫酸铜溶液倾入柠檬酸钠及碳酸钠溶液中,搅匀后即为班氏尿糖定性试剂.用细口瓶贮存备用(为了防止氢氧化铜沉淀的生成,故加入柠檬酸钠.柠檬酸钠是一种亲水性掩蔽性络合物形成剂,它能与铜离子形成可溶性络盐).利用方法同斐林试剂,所不同的是班氏试剂可长期利用.3、双缩脲试剂配制:A液:质量浓度为0.1g/ml,取10gNaOH溶于蒸馏水,稀释至100mlB液:质量浓度为0.01g/ml,取1gCuSO4溶于蒸馏水,稀释至100ml利用时,先加A液,后加B液作用:鉴定蛋白质,蛋白质与双缩脲试剂发生作用,可产生紫色反应.也可用于鉴定多肽.4、苏丹Ⅲ配制:取0.1g苏丹Ⅲ,溶解在20ml95%酒精中作用:鉴定脂肪,脂肪可以被苏丹Ⅲ染成橘黄色(或被苏丹Ⅲ染成红色).5、质量分数为15%的盐酸和体积分数为95%的酒精溶液的混合液(1:1).作用:用于洋葱根尖的解离,即使组织中的细胞相互分离开来.能杀死细胞固定.。
生物学--生物染色剂

生物染色剂斐林试剂:检测可溶性还原糖(葡萄糖、果糖、麦芽糖),沸水浴加热,出现砖红色沉淀。
苏丹Ⅲ和苏丹Ⅳ:检测脂肪,苏丹Ⅲ遇到脂肪出现橘黄色,苏丹Ⅳ遇到脂肪出现红色。
双缩脲试剂:检测蛋白质,出现紫色甲基绿:检测DNA在细胞中分布,遇到DNA出现绿色。
吡罗红:检测RNA在细胞中分布,遇到RNA出现红色。
二苯胺:检测DNA的存在,DNA遇到二苯胺,水浴加热出现蓝色。
健那绿:检测细胞中的线粒体,线粒体遇到健那绿呈现蓝绿色。
碘液:检测淀粉,淀粉遇到碘液出现蓝色。
澄清石灰水:检测CO2,二氧化碳可以使澄清的石灰水变浑浊。
溴麝香草酚蓝水溶液:检测二氧化碳,二氧化碳可以使溴麝香草酚蓝水溶液由蓝色变成绿色再变成黄色。
重铬酸钾溶液:检测酒精,可以在酸性条件下与酒精发生反应出现灰绿色。
龙胆紫或者醋酸洋红:检测细胞核中的染色质,可以将染色质染成深色。
高中生物学重要的酶(部分)限制性核酸内切酶:将DNA分子的双链骨架切割,一种限制性核酸内切酶识别一种序列,而且从特定的位点切割。
限制性核酸内切酶破坏DNA分子的骨架上的磷酸二酯键。
DNA连接酶:将被限制酶切割的双链DNA片断连接起来。
DNA连接酶连接DNA分子的骨架上的磷酸二酯键。
DNA聚合酶:在DNA复制的时候需要,将单个脱氧核苷酸一个一个的连接起来,DNA聚合酶连接DNA骨架上的磷酸二酯键。
解旋酶:将DNA的双螺旋解开,解旋酶破坏的是氢键。
(也可以用高温解旋)RNA聚合酶:催化DNA转录为mRNA分子。
胰蛋白酶:将动物细胞间隙的蛋白质水解,使组织分散成游离细胞。
逆转录酶:催化RNA逆转录形成DNA分子。
生物染色剂高中几种染色剂的使用原理、使用方法归纳1。
甲基绿和吡罗红:实验原理:甲基绿和吡罗红两种染色剂对DNA和RNA的亲和力不同,甲基绿使DNA呈现绿色,吡罗红使RNA呈现红色.利用甲基绿,吡罗红混合染色剂将细胞染色,可以显示DNA和RNA在细胞中的分布.试剂及配制方法(1)试剂质量分数为0.9%的NaCl溶液,质量分数为8%的盐酸,乙酸钠,乙酸,蒸馏水,吡罗红甲基绿混装粉。
染色法的原理和应用

染色法的原理和应用1. 引言染色法是一种常见的科学技术,在生物学、医学、化学等许多领域都有广泛的应用。
染色法可以用于观察细胞结构、研究生物分子、分析化学物质等。
本文将介绍染色法的原理和一些常见的应用。
2. 染色法的原理染色法的原理是利用染料分子与待染物质之间的特定相互作用,将染料分子添加到待染物质中,以使其颜色发生改变。
具体来说,染色法的原理可以分为以下几种:2.1 吸附式染色法吸附式染色法是指染料分子通过与待染物质表面的物质相互作用,以吸附在其上并改变其颜色。
例如,常用的吸附式染色法包括酸性染料在碱性环境中与细胞核酸结合形成染色体的观察,以及金胺染料在银盐摄影中的应用。
2.2 化学反应染色法化学反应染色法是指染料分子通过与待染物质之间发生化学反应,以改变其颜色。
例如,常见的化学反应染色法包括血红蛋白与化学试剂的反应形成颜色的变化,以及酮类与胍类化合物反应生成有色产物的化学反应。
2.3 结合染色法结合染色法是指染料分子与待染物质之间通过特定的化学键结合,以改变其颜色。
例如,常见的结合染色法包括免疫组织化学染色中的抗体与抗原结合、荧光染料与标记物质的结合等。
3. 染色法的应用染色法在许多领域都有广泛的应用,以下是一些常见的应用示例:3.1 细胞生物学染色法在细胞生物学中具有非常重要的应用。
通过使用染色法,可以观察细胞核酸、蛋白质、细胞器等的分布和结构,并研究细胞的功能和变化。
3.2 组织学在医学领域的组织学中,染色法被广泛应用于组织切片的染色和观察。
染色技术可以帮助医生或研究人员观察组织器官的结构、病变情况,从而提供诊断和研究的重要依据。
3.3 分子生物学染色法在分子生物学研究中也有重要应用。
例如,荧光染料可以标记DNA、RNA、蛋白质等分子,利用荧光显微镜观察其分布和相互作用,从而研究基因组的结构和功能。
3.4 化学分析在化学分析领域,染色法被广泛应用于定性和定量分析。
例如,比目鱼试剂可以通过染色反应检测氮含量,甲基橙试剂可以用于检测氧化还原反应等。
高一生物染色试剂知识点

高一生物染色试剂知识点生物是一门研究生命现象和规律的学科,而染色试剂在生物实验中起着至关重要的作用。
染色试剂是将细胞和组织中复杂的生化物质染成可见的颜色,从而能够观察、研究其结构和功能。
本文将介绍高一生物中常用的染色试剂,帮助同学们更好地理解生物实验中的染色技术。
1. 伊红染色试剂伊红染色试剂是一种酸性染料,常用于观察细胞的形态和结构。
它能染亮细胞核和胞浆,使细胞形状清晰可见。
在生物实验中,我们可以将伊红染色试剂应用于根尖细胞染色实验,以观察细胞的有丝分裂现象,进而了解细胞生长和分裂的过程。
2. 嗜乙酸伊红染色试剂嗜乙酸伊红染色试剂是一种碱性染料,常用于染色体的观察。
它能够特异染色染色体,使其清晰可见。
通过染色体的观察,我们可以研究染色体的数量、结构和性状等遗传信息,从而了解基因的传递和变异规律。
3. 维氏染色试剂维氏染色试剂是一种复杂的复合染料,主要用于染色细菌。
它能够染亮细菌的形态和结构,使其在显微镜下更加清晰可见。
通过观察染色后的细菌形态,我们可以判断细菌的类型、数量和分布情况,从而进行相关的研究。
4. 甲苯胺蓝染色试剂甲苯胺蓝染色试剂是一种碱性染料,常用于染色生物薄片。
它能够染亮细胞核和细胞质,使细胞结构清晰可见。
通过甲苯胺蓝染色,我们可以观察细胞的数量、形状和结构特征,从而研究细胞的功能和变异情况。
5. 阿鲁金蓝染色试剂阿鲁金蓝染色试剂是一种酸性染料,常用于观察细胞色素和细胞器。
它能够染亮线粒体和叶绿体等细胞器,使其在显微镜下更加显著。
通过阿鲁金蓝染色,我们可以了解细胞的代谢活动和能量转化过程,从而研究细胞的功能和机制。
染色试剂在生物实验中具有不可替代的作用。
它们不仅能够帮助我们观察细胞和组织的形态结构,还能够探索生命的奥秘。
因此,对于高一生物学习来说,掌握染色试剂的相关知识是非常重要的。
除了常用的染色试剂外,还有许多其他的染色试剂可以在生物实验中应用。
比如,格里姆纳染色试剂、那瓦染色试剂、偏碱性洛伊斯染色试剂等等。
生物染料变色知识点总结

生物染料变色知识点总结一、生物染料的基本概念生物染料是一种从生物体内提取或合成出来的能够给纺织品、食品等物质着色的物质。
它们通常是天然的有机分子,可以均匀地附着到纤维或其他材料上,使得它们具有颜色。
生物染料的使用已经有几千年的历史,早在古埃及和古希腊时期,人们就开始使用植物、昆虫和动物组织中的色素来染色。
二、生物染料的作用原理生物染料的作用原理可以概括为“吸附、渗透、结合”,即生物染料首先要与纤维等物质表面产生物理吸附、静电吸附等物理吸附作用,然后通过渗透作用,将染料颜料颗粒渗透入纤维、薄膜等表面内部,最后与目标物质发生化学反应,形成牢固的结合并产生色彩。
三、生物染料的变色知识点1. 变色的基本原理:生物染料的颜色变化是由于染料分子的分子结构、功能团、化学键以及材料体系的相互作用发生改变而产生的。
这种变化涉及到物质的光谱特性、化学反应、光物理性质等多方面的知识。
2. 影响染料颜色的因素:染料颜色的变化受到多种因素的影响,例如溶剂、温度、pH值、电解质浓度、氧化还原体系等。
当这些因素发生变化时,染料的颜色也会产生相应的变化。
3. 变色的机制:生物染料发生变色的机理包括化学反应、光物理作用等多种形式。
染料颜色变化的机制不仅和染料自身的化学结构相关,还与含有染料的材料的物理性质相关。
4. 变色技术:由于生物染料的应用范围非常广泛,因此需要针对不同的应用领域使用不同的变色技术。
例如,在纺织品染色中,需要考虑到染料对纤维的渗透性和色牢度等问题,在食品着色中需要考虑染料的安全性等。
5. 变色的应用:生物染料的变色技术在纺织工业、食品加工、医药领域等多个行业都有应用。
通过研究染料的变色机理和技术,可以开发出更加适合各个行业需求的新型生物染料。
6. 染料的毒性问题:染料的毒性一直是人们关注的焦点。
染料对人类和环境的影响一直备受关注,因此在生物染料的研发和应用过程中,需要考虑到染料的毒性问题,以保障人们的健康和环境的安全。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中生物课程中常见染色剂染色原理及使用注意事项朱秋霖,马天兵兰州二中,兰州 730000 摘要:目的:探究高中生物试验中常见染色剂的使用方法及常见问题与注意事项方法:通过一些简单的实验验证与参考文献得出结论。
结果:验证与总结出生物试验中常见染色剂的染色原理及所遇到的染色问题的原因。
关键词:高中生物学实验染色剂显色原理注意事项The common dye staining principle and precautions in the highschool biology curriculumZhu Qiulin,Ma TianbingLanzhou NO.2 middle secondary school class8 grade2,lanzhou 730000Abstract:Objective: To explore the use of high school biology test stains and FAQs Notemethod: through some simple experiments verify references concluded.Results:Validation andsummed up a common biological test stain dyeing principle and coloring problem encountered byreason.Keywords:high school biology experiment stain color rendering principle Precautions1.常见染色剂常见的高中生物染色显色反应,其实质是化学反应或者物理反应,按照其反应本质,可分为下列几类[5]:1.1 氧化还原反应类染色剂通过氧化还原反应生成某些具有特殊颜色的物质,利用其与生物组织中某些具有还原性的物质或代谢产物进行化学反应,宏观上产生颜色变化,通过颜色变化,鉴别某些生物组织中的目标物质。
1.1.1 斐林试剂由于生物组织中的葡萄糖,果糖和麦芽糖等含有具有还原性的醛基,因此称其为还原性糖[1]。
利用斐林试剂,与还原糖发生还原反应,生成砖红色沉淀。
利用这一性质,可鉴定生物组织液中的还原性糖的存在与否,亦可以用来分析糖尿病人尿液成分。
配方为2.5mol/L的氢氧化钠溶液(甲液);约0.31mol/L的硫酸铜溶液(乙液)。
其化学反应原理如下所示:2CH3(CH2OH)4CHO + 2Cu(OH)2→ 2CH3(CH2OH)4COOH + Cu2O↓ + 2H2O当甲乙两液混合后,立即生成蓝色的氢氧化铜沉淀(Cu(OH)2)。
Cu(OH)2与随后加入的还原性糖类在加热的条件下,会被还原性糖中的醛基还原成为砖红色的氧化亚铜(Cu2O)沉淀,从而鉴定还原糖。
1.1.2 班氏试剂班氏试剂亦是用以鉴定鉴别糖类物质的染色显色剂,但常用于尿糖的定性检测[3]。
常见配方如下:17.4克无水硫酸铜(CuSO4)溶解于100毫升热蒸馏水中,冷却后,稀释到150毫升。
称取柠檬酸钠173克与无水碳酸钠(Na2CO3)100克,加入蒸馏水600毫升,加热溶解。
冷却后,稀释到850毫升。
把硫酸铜溶液倾入柠檬酸钠及碳酸钠溶液中,搅匀后即为班氏尿糖定性试剂。
1.1.3 重铬酸钾酵母菌无氧呼吸产生乙醇,可用重铬酸钾(俗称红矾钾,分子式K2Cr2O7)溶液进行鉴定鉴别。
其染色显色过程中的化学反应方程式如下所示:3CH3CH2OH + 2K2Cr2O7 + 8H2SO4 → 3CH3COOH + 2Cr2(SO4)3 + 2K2SO4 + 11H2O橙色的重铬酸钾在酸性的条件下,与醇类反应,被还原成为灰绿色的硫酸铬。
从而用以鉴别醇类物质。
1.2 络合物(配合物)类染色显色剂络合物(又称配合物),是由可以给出孤对电子或多个不定域电子的一定数目的离子或分子(配体),和具有接受孤对电子或多个不定域电子的空位的原子或离子(统称为中心原子),按照一定的组成和空间构型所形成的化合物。
这类物质吸收光后,自身产生变化,光照消失后恢复原样,从而产生颜色变化。
1.2.1 碘,碘的乙醇溶液1864年德国科学家萨克斯在分析光合作用产物时,就利用了碘可以用于检测淀粉的性质(反应)。
直链淀粉由α-葡萄糖分子缩合而成螺旋状的长长的螺旋体,每个葡萄糖单元都仍有羟基暴露在螺旋外,碘分子跟这些羟基作用,使碘分子嵌入淀粉螺旋体的轴心部位,两者形成一种蓝黑色络合物。
实验证明,单独的碘分子不能使淀粉-)。
这并非是淀粉与碘发生了化学反变蓝,实际上使淀粉变蓝的是碘分子离子(I3应,而是淀粉螺旋中央空穴恰能容下碘分子。
支链淀粉遇碘呈紫红色,淀粉跟碘显色结果,与淀粉的聚合度或相对分子质量有关。
1.2.2 双缩脲试剂双缩脲试剂用于鉴定蛋白质,为碱性含铜试液,呈蓝色。
由1%氢氧化钾、1%硫酸铜和酒石酸钾钠配制。
当底物中含有肽键时,试剂中的铜与多肽物质配位反应,配合物呈紫色。
双缩脲试剂中主要作用物为硫酸铜,而氢氧化钾仅仅是为了提供碱性环境,因此它可被其他碱如氢氧化钠所代替。
向试剂中加入碘化钾,可延长试剂的使用寿命。
双缩脲鉴定多肽物质(包括蛋白质)的反应原理:双缩脲(H2NOC-NH-CONH2)是有2个分子尿素在加热后放出一分子氨后得到的产物[1]。
在强碱性环境中,双缩脲与硫酸铜(CuSO4)作用,形成紫红色络合物,该反应即双缩脲反应。
双缩脲反应是肽和蛋白质所特有的,而为氨基酸所没有的一种颜色反应。
一般分子中含有两个肽键的化合物与碱性铜溶液作用,就会形成紫色或蓝紫色络合物。
但是需要注意的是,除了-CO-NH-有此反应外,(-CONH2-)、(-CH2-)、(-NH2-)、(-CS-CS-NH2)等基团亦有此反应。
1.3 有机染色剂染色[6]利用有机染色剂染色的必备条件是具有颜色并且与被染物质之间有强的亲和力。
1.3.1 苏丹染色剂目前常见的染色剂为苏丹Ⅲ与苏丹Ⅳ染色剂。
苏丹Ⅲ与苏丹Ⅳ是人工合成的苏丹系列染色剂,常作为工业染色剂。
苏丹染色剂为亲脂性偶氮化合物,在脂肪类物质中的溶解度大于在其他溶质(酒精、丙酮)中的溶解度时,染色剂颗粒便在脂肪颗粒中大量积累,并呈现橘黄色或红色。
1.3.2 甲基绿、吡咯红、二苯胺在观察细胞中DNA和RNA的分布时,需要用甲基绿和吡罗红染色。
甲基绿是具有金属光泽的绿色结晶,溶于水,呈现蓝绿色。
在盐酸中显示红黄色,在碱性溶液中显示为无色。
在进行DNA的鉴别鉴定中,使用其对DNA进行染色显色。
吡咯红是含有氮原子的杂环化合物,与RNA结合呈现红色。
DNA在酸性条件下加热,生成嘌呤碱基,脱氧核糖与脱氧嘧啶核苷酸,其中,脱氧核糖在酸性条件下加热,发生脱水反应,并生成ω-羟基-γ-酮基戊糖,与二苯胺(分子式C12H11N)反应,生成蓝色物质。
1.3.3 龙胆紫、醋酸洋红、刚果红龙胆紫与醋酸洋红用于细胞染色体的染色显色反应,在观察植物细胞有丝分裂时经常用来使染色质或染色体着色。
龙胆紫的稀溶液俗称紫药水,虽然在使用龙胆紫溶液染色时,溶液略显酸性,但因为其具有碱性基团,故其为一种碱性阳离子染色剂。
醋酸洋红(胭脂红、卡红)中的醋酸,是该染色剂的溶质。
醋酸增加了染色时细胞的通透性,利于洋红进入细胞核对染色体进行染色。
刚果红(棉红、直接大红、直接朱红)可以使纤维素直接着色的一种偶氮化合物染色剂。
1.4 酸碱指示剂类酸碱指示剂是一类结构复杂,但使用简单的弱有机酸或碱。
它们在溶液中能够部分电离,并且由于结构发生变化,导致其粒子的颜色发生变化,因而在不同的pH环境下呈现不同的颜色。
生物学实验中常用的酸碱指示剂有溴麝香草酚蓝的水溶液和酚红。
高中生物课程实验中“探究酵母菌的呼吸方式”,可以用溴麝香草酚蓝的水溶液来鉴定是否有二氧化碳的生成。
由于酵母菌无氧呼吸生成的二氧化碳并与水反应生成碳酸呈弱酸性,所以由蓝变黄,其中间过渡色为绿色。
酚红为有机弱酸,变色范围为6.8至8.0由黄变红。
可用来检测尿素分解细菌的产物——氨(在溶液中为铵)2. 常见问题及注意事项2.1为什么经常碘遇淀粉不变蓝?课本中经常提及淀粉遇碘变蓝,可是在中学生物或化学实验中,经常见到淀粉遇碘不呈现蓝色,而是呈现紫色或其他颜色。
中学生甚至教师经常被这个问题所困扰,究其原因,主要是因为淀粉的结构及实验条件如温度、PH值等所导致的。
淀粉为白色粉末,由10%~30%的直链淀粉和70%~90%的支链淀粉组成。
溶于水的直链淀粉借助分子内的氢键卷曲成螺旋状。
如果加入碘液,碘液中的碘分子便嵌入到螺旋结构的空隙处,并借助范德华力与直链淀粉分子联系在一起,形成了一种络合物。
在此络合物中,淀粉链以直径0.13 pm绕成螺旋状,碘分子处在螺旋的轴心部位,淀粉与碘生成的包合物的颜色,跟淀粉的聚合度或相对分子质量有关。
在一定的聚合度或相对分子质量范围内,随聚合度或相对分子质量的增加,络合物的颜色的变化由无色、橙色、淡红、紫色到蓝色。
例如,直链淀粉的聚合度是200~980或相对分子质量范围是32,000~160,000时,络合物的颜色是蓝色。
分支很多的支链淀粉,在支链上的直链平均聚合度20~28,这样形成的包合物是紫色的。
支链淀粉部分水解可产生称为糊精的混合物。
糊精的聚合度更低,显棕红色、红色、淡红色等。
除结构外,还有以下因素也会影响:①温度:随着温度的升高, 淀粉溶液与碘显色的灵敏度降低, 且当温度高于45℃时此显色反应现象几乎看不到。
这是因为直链淀粉与碘显色的实质是直链淀粉的螺旋状圆柱刚好能容纳碘分子的钻入, 并受范德华引力吸引而形成络合物, 加热时络合物离解,碘分子从络合物中脱下,所以蓝色褪去;而冷却后, 脱下来的碘分子又逐渐与淀粉结合而再显蓝色。
② pH值:在不同的pH 值溶液中显色情况是不同的。
淀粉与碘的蓝色蓝色反应在pH= 3-5 的弱酸性溶液中进行最灵敏, 在pH小于8的弱碱性溶液中次之;在强酸性溶液中, 反应呈现蓝紫色;在pH大于9的碱性溶液中不显色。
发生上述不同显色反应的原因是:淀粉在强酸中会水解, 产生糊精等, 糊精和碘分子作用呈现红色, 在与深色的碘单质混合后,则呈现蓝紫色; 在强碱性溶液中, 碱将歧化成次碘酸盐和碘化物, 基本无单质碘的存在, 因而不显色; 在弱酸性溶液中, 碘基本不参与歧化反应, 所以单质碘数量多, 有利于与淀粉结合, 故显色反应比较明显。
③淀粉的新鲜程度:淀粉溶液越新鲜, 显色反应越明显。
配好的淀粉溶液放置的时间不同, 与碘分子作用时显示的颜色也有所不同。
淀粉溶液存放时间越长, 呈现的紫色越明显。
这是因为淀粉水溶液会缓慢地水解,为糊精等物质, 糊精与碘作用显红色, 因而久置的淀粉溶液会降低反应的灵敏度, 而且反应呈蓝紫色, 甚至紫红色。
