药品不良反应文献检索程序文件
药品不良反应数据规整处理标准操作程序

药品不良反应数据规整处理标准操作程序1目的规范对药品不良反应数据进行科学的、规范化和标准化的整合,为不良反应监测信息提供高质量的数据和高效率的应用。
2范围对收集到的药品不良反应进行数据规整处理的过程。
3职责3.1本文件由药物警戒部制定。
4定义药品不良反应数据规整:是指专业人员对收集的药品不良反应病例报告进行的标准化和规范化处理。
具体包括不良反应数据(药品分类及通用名称、生产企业名称、剂型、给药途径、原患疾病、用药原因、不良反应及累及系统等)研究、建立、标准化处理、日常维护,以及对于药品不良反应病例报告的规范化处理。
5参考文件/依据5.1GVP6正文6.1药品不良反应数据规整的必要性6.1.1药品上市许可持有人药品不良反应直接报告系统是公司药品不良反应信息的主要来源,而填报内容取决于报告人,在上报时,无法保证所有填报人都能准确、规范的填报,不能保证填报人对数据的理解与报表的要求完全一致。
6.1.2通过数据规整,探索药品不良反应数据规整机制、工作流程,建立相应的标准数据库、规则库,从而实现规整工作的日常性和持续性。
6.1.3标准和规范的药品不良反应数据库有利于不良反应信息后续的利用,例如开展药品安全风险信号监测、药品安全定期分析、药物警戒年度报告撰写、定期安全性更新报告撰写等。
6.2数据规整原则:规整数据与原始数据表达意义一致,关联性评价尊重原结论,保持数据的真实性。
数据信息尽可能核实完善,如有信息无法确定或无法获取,可填不详。
6.3药品不良反应数据规整的具体工作内容6.3.1药品不良反应数据收集规整。
药物警戒部收集公司产品的所有药品不良反应数据,包括药品上市许可持有人药品不良反应直接报告系统反馈的药品不良反应报告、文献检索、互联网及相关途径、上市后研究和项目等收集的药品不良反应信息。
药物警戒部依据现有标准、参考有关资料、结合专业知识对药品不良反应数据进行分类、名称术语规整。
6.3.1.1基本信息规整药物警戒部对收集的不良反应数据(如报告信息、患者基本信息、患者其他重要信息、药品基本信息、合并用药相关信息、相关器械信息、其他信息等基本信息)进行核实规整,具体信息如下:➢报告信息:报告编号、企业内部编号、首次获知时间、首次/跟踪报告、报告类型、报告来源、境内/境外。
药品不良反应信息检索

监管机构公告与警示
国家药品监督管理局(NMPA)公告
发布药品安全监管政策、药品不良反应信息通报等重要信息。
欧洲药品管理局(EMA)警示
针对欧洲市场上出现的药品安全问题,发布相关警示信息。
美国食品药品监督管理局(FDA)警告信 对违反药品安全法规的行为发出警告信,涉及药品不良反应的重要内容。
03
信息检索方法与技巧
与学术界的合作,共同开展药品不良反应的研究和分析。
03
加强国际合作与交流
学习借鉴国际先进经验和做法,加强与国际组织和其他国家的合作与交
流,共同推动药品不良反应信息检索工作的发展。
06
未来展望与建议
完善药品不良反应信息数据库建设
扩大数据库覆盖范围
积极收集全球范围内的药品不良反应信息,提高数据库的全面性 和时效性。
案例三:某中药注射剂不良反应事件追踪报道
事件追踪
关注某中药注射剂不良反应事件 的报道,持续收集相关信息。
信息来源
从药品监管部门、医疗机构、新 闻媒体等多个渠道获取该中药注
射剂的不良反应信息。
数据分析
对收集到的不良反应信息进行统 计分析,包括发生时间、地点、 患者年龄性别分布、临床表现、 处理措施等,以评估该中药注射
加强信息筛选和整合能力
培训相关人员对检索结果进行筛选、分类和整合, 提取有价值的信息,为药品不良反应研究提供全 面、准确的数据支持。
推动跨学科合作
鼓励医学、药学、统计学等多学科背景的专家合 作,共同开展药品不良反应的深入研究。
推动监管机构、企业和学术界之间的信息交流与合作
加强监管机构与企业的沟通
建立定期的信息交流机制,使企业能够及时了解药品不良反应的 最新信息和监管要求,加强自我管理和风险控制。
药物警戒-不良反应文献检索和利用操作规程

不良反应文献检索和利用操作规程一、目的:建立药品不良反应文献检索和利用的工作标准,规范药品不良反应文献检索、检索信息的利用等过程。
二、范围:适用本公司上市后药品不良反应文献检索与利用的操作。
三、责任:药品不良反应监测与报告专职人员。
四、内容:1、文献检索是指文献查找、分析判定、判定评价、有效利用的过程。
2、药品不良反应文献检索的目的(1)满足监管部门的相关要求:《药品不良反应报告和监测指南(试行)》、《药品定期安全性更新报告撰写规范》等法规要求。
(2)安全性信息收集的有效途径之一。
(3)为药品上市后风险管理提供支持,为药品安全性问题提供预警。
(4)进一步评估药品获益与风险提供支持。
(5)识别潜在的风险信号,及时对已存在的风险信号采取措施。
3、药品不良反应文献检索相关人员及工作内容药品不良反应监测与报告专职人员每月定时检索各文献数据库(必检索:万方、维普、中国知网等),收集可疑药品安全性信息。
工作内容如下:(1)定期(每月一次)检索文献;(2)审阅并记录检索结果;(3)评价和判断是否为有效的不良事件;(4)处理和形成检索报告。
4、药品不良反应文献检索范围国内文献要求至少要同时检索万方、维普、中国知网此三个数据库,还需检索国家食品药品监督管理总局网站药品安全警示专栏,国家药品不良反应监测中心网站相关专栏;如有资源,外文可检索MEDLINE(Pubmed)、Embase、MICROMEDEX等数据库。
5、药品不良反应文献检索过程文献检索的过程即为:选择合适的数据库,优选合适的文献,构建合理的检索策略,保证查全率,查准率。
5.1前期准备准备药品名称(商品名称、通用名称、别名、曾用名),制剂处方、工艺,有效成分,相关不良反应,相同成分的不同剂型等信息资料。
5.2制定检索策略A检索词确定药品不良反应的文献检索通常以“主题词/关键词”途径进行。
主题词/关键词:药品名称、不良反应/副作用/毒性,直接检索。
主题词/关键词:药品名称/活性物质、致、导致、作用、临床、使用、出现、引起、不良事件。
药品不良反应文献检索标准操作规程完整

一、目的:为了规范药品不良反应文献检索工作,特制定本规程。
二、适用范围:适用于本公司生产药品有关的不良反应文献检索工作。
三、责任人:药品不良反应管理专员负责药品不良反应文献检索工作、QA主管、质量管理负责人及质量受权人依据其职责执行本规程。
四、程序:1 质量管理部负责本公司药品不良反应文献检索工作。
具体检索申报工作由不良反应专员负责。
2 在下列情况下,应进行不良反应文献检索工作2.1药品注册申请时,申报资料项目中需要提交相应药品不良反应文献检索报告时;2.2申报非处方药;2.3申报中药保护或延长保护期;2.4申报药品进口注册;2.5申请单独定价或优质优价;2.6申请药品再注册;2.7申请药品不良反应文献跟踪检索;2.8其他安全性评价时。
3 不良反应文献检索申请3.1药品不良反应专员根据检索目的,填写《药品不良反应文献检索申请表》。
其内容包含如下内容。
3.1.1药品名称:根据拟查询药品的说明书填写该药品的相应名称,如中文名称、商品名称、英文名称;3.1.2药品类别:根据药品的类别性质,选择对应的药品类别。
类别包含非处方药、国家基本药品、化学药品、生物制品、中药、进口药品、医保药品、中药保护品种。
3.1.3药品的基本信息:剂型、规格、处方/配方、不良反应/禁忌、批准文号、上市时间、药品标准。
3.1.4申报单位:据实填写申报单位信息,包含:单位名称、通讯地址、邮编、联系人、电话、传真。
3.1.5检索目的:根据检索需求,选择填写相应的目的。
目的包含:申报非处方药、申报中药保护或延长保护期、申报药品进口注册、申请单独定价或优质优价、申请药品再注册、申请药品不良反应文献跟踪检索、其他。
3.1.6其他:选择性填写内容,包含取报告方式、是否加急、交送材料的电子版本(药品说明书、药品质量标准、国内外ADR情况、中药材地方标准)。
3.1.7在填写完整的《药品不良反应文献检索申请表》申报单位相应位置加盖鲜公章。
3.2其他证明文件3.2.1资料项目包含3.2.1.1药品不良反应文献检索申请表、质量标准和说明书及其相关证明性文件;3.2.1.2处方/配方中的中药材地方标准;3.2.1.3自我真实性保证声明;3.2.1.4《授权委托书》3.2.2证明性文件:药品批准证明文件及药品监督管理部门批准变更的文件:药品批准证明文件、历次补充申请批件和备案情况公示结果:包括药品注册批件、统一换发批准文号的文件、药品注册证、与取得批准文号有关的其他文件;经批准按《药品说明书和标签管理规定》(局令第24号)修订说明书的补充申请批件(备案情况公示)及说明书样稿;其他补充申请批件、备案情况。
药品不良反应文献检索程序

目的:建立药品不良反应文献检索程序。
适用X围:适用药品不良反应相关文献检索。
负责人:药品不良反应监测办公室主任、质量保证部部长、科研中心监测人员。
内容:一、国内文献检索(一)、中国知网(KI)1、简介中国知网(),是国家知识基础设施(National Knowledge Infrastructure,NKI)的概念,由清华大学、清华同方发起,始建于1999年6月。
中国知网已经发展成为集期刊杂志、博士论文、硕士论文、会议论文、报纸、工具书、年鉴、专利、标准、国学、海外文献资源为一体的、具体国际领先水平的网络出版平台。
分为基础科学、工程科技、农业科技、医药卫生科技等10个专业文献总库,168个专题数据库,中心的日更新文献量达5万篇以上。
其中医药卫生科技文献库涵盖预防医学与卫生学,中医学,中药学,中西医结合,基础医学,临床医学,感染性疾病及传染病,心血管系统疾病,呼吸系统疾病,消化系统疾病,内分泌腺及全身性疾病,外科学,泌尿科学,妇产科学,儿科学,神经病学,精神病学,肿瘤学,眼科与耳鼻咽喉科,口腔科学,皮肤病与性病,特种医学,急救医学,军事医学与卫生,药学等医药学领域。
截至2011年6月,收录国内学术期刊7778种,全文文献总量3200多万篇,其中药学方面的文献量达61万多篇;收录来自397家培养单位的博士学位论文15万多篇,其中药学方面的文献量达5600多篇。
收录来自598家培养单位的优秀硕士学位论文115万多篇,其中药学方面的文献量达2万多篇。
2、检索方法KI有文献检索、知识元检索、引文检索等多条途径。
本书仅介绍文献检索、高级检索两种方式,更多检索方式可从KI获取。
1)简单简单检索即在全文中进行检索。
在检索框中输入检索关键词后,点击“”按钮进行检索,见图1图12)高级检索点击“高级检索”进入高级检索页面。
页面上提供高级检索及其相应的检索控制项(主题、篇名、作者、作者单位、发表时间、文献来源、支持基金)。
药品不良反应文献检索标准操作规程
2.5申请单独定价或优质优价;2.6申请药品再注册;2.7申请药品不良反应文献跟踪检索;2.8其他安全性评价时。
3 不良反应文献检索申请3.1药品不良反应专员根据检索目的,填写《药品不良反应文献检索申请表》。
其内容包含如下内容。
3.2其他证明文件药品不良反应文献检索申请表、质量标准和说明书及其相关证明性文件;处方/3.33.3.13.3.23.3.33.3.4药品代理机构申请检索时需要提供生产企业提供加盖公章的《授权委托书》及自我保证真实性说明。
3.4资料的提交3.4.1以上资料可直接送交国家药品不良反应中心,也可以通过邮递、传真方式递交。
3.4.2在递交上述纸质申请资料的同时,发送药品不良反应文献检索申请表、质量标准、说明书4 费用缴纳4.1按照规定缴纳必要的检索费用。
4.2一般情况下,每份申请表检索费1000元,加急检索费1500元。
在递交申请资料时缴纳现金或支票,也可通过银行电汇。
传真电话号码及收件人详见最新国家不良反应中心网站公告。
检测中心在收到检索费用和全部申请材料后开始检索。
102 相关表格六、变更记载:附件药品不良反应文献检索申请表(请仔细阅读检索申请须知)文件编号:REC-QA-XXX-01位电话:传真:检索目的:申报非处方药□申请中药保护或延长保护期□申请药品进口注册□申请单独定价或优质优价□单位签章申请药品再注册□申请药品不良反应文献跟踪检索□其他 _____________________________取报告方式:自取□邮递□是否加急:是□否□。
10药品不良反应信息检索

药品不良反应信息检索程序1. 药品不良反应监测员应对不良反应信息每月检索1次,并形成具体的检索记录。
不良反应检索记录见附表一。
2、药品不良反应信息种类有:公开发表的病例报告;ADR报告系统的病例报告;专题研究论文;综述性资料;ADR方法学研究;新闻类资料;政策法规性资料3、药品不良反应信息的来源主要有:参考书、工具书;报纸、杂志;会议资料, 临床资料及各种宣传材料;药品不良反应报告系统4.药品不良反应信息检索方式4.1图书检索4.1.1图书检索方法手检:中图分类号、作者名、图书名等。
软件检索:作者、编辑、出版团体机构、书名、分类号、索书号、主题词以及期刊名、ISBN、ISSN号等为检索入口进行检索4.1.2 常用的参考书和工具书4.1.2.1 M.N.G.Dukes: Meyler‘s Side Effects of Drugs (文本, CD-ROM)公认ADR的权威著作, 1957-1997已出12版.,每章有参考文献。
索引系统:别名索引(Index of synonyms)、药物索引(Index of drugs)、主要副作用索引(Index of major side effects)、主要相互作用索引(Index of major interactions)。
4.1.2.2 M.N.G.Dukes: Side Effects of Drugs Annual (1977创刊,每年1月出版)世界范围的年度新资料和动态调查, Meyler's的姊妹篇。
索引系统:药物索引(Index of drugs)、副作用索引(Index of side effects)。
4.1.2. 3 Martindale- The Complete Drug Reference (1999, 32ed, UK) (文本和CD- ROM)每种药品有“不良反应,处理,注意"一节,有较全面的概述,病例报告及参考文献,通常可先查阅此书。
各种药品不良反应收集途径说明及制药行业常用数据库和相关网站

药品不良反应收集途径说明一、通过医疗机构/药品经营企业收集①医疗机构②营销部门/销售部③药物警戒部1、路径:①②③1)②向①说明不良反应收集的要求,发放纸质记录。
2)②定期拜访、电话或传真向①了解不良反应收集情况,及时向③反馈不良反应收集途中存在的问题。
同时可让医务人员等扫二维码链接上传不良反应。
3)③定期了解②不良反应收集情况,协调解决收集中存在的问题。
4)③定期开展药物警戒培训,普及基础知识、记录填报要求。
2、路径:①③药品包装上印有投诉/咨询电话、二维码链接上报不良反应、微信公众号。
存在问题:1)该怎么设计适宜医务人员或销售部人员便捷填写的纸质记录?2)定期开展哪些人员培训(关系到不良反应收集的人员)?3)怎样设计收集不良反应的二维码、APP、公司微信公众号、公司网站?4)公司内部不良反应收集的联系人员、联系方式、网络结构是怎样的?二、电话和投诉患者、公众、医务人员等通过公司说明书、药品标签、公司网站、公司微信公众号等公布的联系电话报告不良反应或咨询用药问题。
1、制定文件,设制咨询或不良反应投诉记录。
2、药物警戒部安排专人接听咨询或不良反应投诉电话,填写相关记录。
3、根据药品说明书等资料制定基础咨询问题的回答标准、基础投诉的处理流程。
4、电话有录音功能,在非工作时间设置语音留言,重要投诉或咨询进行录音,留有证据。
三、文献1、检索频率:首次上市或首次进口五年内的新药至少每两周进行一次检索,其他药品原则上每月进行一次,也可根据公司药品的安全性特征制定检索频率。
2、检索数据库:检索国内外各两个数据库。
数据库如果公司经济条件允许可正规途径购买数据库使用权限,费用是一个数据库2-3万/年;可购买中国知网会员卡,计费是阅读全文/下载:0.2-1元/页,如果检索阅读/下载的数量多,费用也多;通过淘宝网够买知网等账号,费用很便宜,缺点:通过第三方途径进入知网等,界面不稳定。
1)国内数据库:中国知网(CNKI)、维普网(VIP)、万方数据库等2)国外数据库:PubMed、Embase、Ovid等2、文献类型:个案报道、病例系列、不良反应综述等。
国家药品不良反应监测系统使用操作规范流程

国家药品不良反应监测系统使⽤操作规范流程⽬的:为确保本公司⽣产的所有药品发⽣药品不良反应/事件,经调查处理后的数据及时准确的上报,特制定本操作规程⽂件。
围:适⽤于国家药品不良反应监测系统数据填报操作。
职责:药品不良反应监督专员执⾏本操作规程,质量部经理负责监督管理。
容:1.法规要求:中华⼈民国《药品不良反应报告和监测管理办法》(卫⽣部令第81号)第⼗三条:药品⽣产、经营企业和医疗机构应当建⽴药品不良反应报告和监测管理制度。
药品⽣产企业应当设⽴专门机构并配备专职⼈员,药品经营企业和医疗机构应当设⽴或者指定机构并配备专(兼)职⼈员,承担本单位的药品不良反应报告和监测⼯作。
第⼗五条:药品⽣产、经营企业和医疗机构获知或者发现可能与⽤药有关的不良反应,应当通过国家药品不良反应监测信息⽹络报告;不具备在线报告条件的,应当通过纸质报表报所在地药品不良反应监测机构,由所在地药品不良反应监测机构代为在线报告。
报告容应当真实、完整、准确。
2. 药品不良反应/事件发⽣后的上报时间:2.1⼀般药品不良反应:应在发⽣后30⽇报告;2.2新的、严重的药品不良反应在15⽇报告;2.3死亡病例须⽴即报告,其中死亡群体事件调查表先或即时通讯等⽅式联系市中⼼,经组织核查为真实后,按照要求再进⾏在线填报;2.4有随访信息的,应当及时报告。
3.国家药品不良反应监测系统登⼊地址:电信⽤户:211.103.186.220联通⽤户:114.255.93.220也可百度搜索‘国家药品不良反应监测系统’点击进⼊;如下图:填写⽤户名、密码及验证码,点击“登⼊”系统;4.报告表的上报与填写:4.1登录系统后查看⾸页,页⾯左侧显⽰的是所有功能树,中间显⽰的是公告通知和预警信息,下⾯显⽰的是提醒信息等;⾸次报告:个例不良反应上报,使⽤此功能模块。
严重跟踪报告:对本企业已上报的严重报告表进⾏跟踪操作时,使⽤此功能模块;报告表检索:查看本企业已上报的报告表时,使⽤此功能模块;已报告列表:查找本企业上报的所有报告表时,使⽤此功能模块;报告查重:在此功能模块;可以查找重复报告;暂存报告:想查找在填报时由系统⾃动暂存或者⼈⼯⼿动暂存的报告时,使⽤此功能模块;补充材料管理:可以查看到本级要求下级补充资料的报告表与上级单位要求本级补充资料的报告表;修改申请管理:对已经上报的报告表进⾏修改,需要向上级单位进⾏申请,上级单位过后会在“修改申请管理”模块⾥进⾏修改;4.2上报个例药品不良反应:单机“⾸次报告”打开“药品不良反应/事件报告表”,填写基本情况、患者基本情况、使⽤药品情况、不良反应过程描述、关联性评价、报告⼈和报告单位信息6部分容;4.2.1药品不良反应/事件报告表编码由系统⾃动⽣成;4.2.2选择报告类型:新的药品不良反应:是指药品说明书中未载明的不良反应;说明书已载,但不良反应发⽣的性质、程度、后果或者频率与说明书描述不⼀致或者更严重的,按照新的药品不良反应处理。
药品不良反应信息的检索

万方数字化期刊
维普中文电子期刊
13
期刊检索
三种检索方式 : (发展的三个阶段)
● 手工检索--印刷版
● 光盘检索--光盘版 ● Internet检索--网络版
14
期刊检索
检索工具
对原始文献进行内容上的提炼、压缩、按一定规 定和方法编制而成,用以积累和查找文献的工具
• 书本式
– 期刊式
(中文科技资料目录)
8
ADR信息的作用
•为临床药理研究、合理用药提供依据 •为临床出现ADR鉴别提供背景材料 •为开展流行病学研究和毒理学研究提供线索 •新药研制、审批、注册、上市后评价提供依据 •中药ADR研究对WHO指导草药安全合理使用的贡献 •为公众提供信息服务 •为政府部门决定提供技术支持
9
ADR信息的获取
期刊检索
CBMDisk与手工检索工具比较:
• CBMDisk检索功能完备,为手工检索不能比较 的。 • CBMDisk包括了《中国药学文摘》95%以上的 内容,但中草药与生物学方面收录的文献不够 全,《中目-中草药》《中国生物学文摘》分别 有近16%和46%的期刊未被CBMDisk收录。
结论: CBMDisk不能完全取代手工检索工具
36
期刊检索
网上药学期刊检索
我国三大网上药学期刊数据库:
•中国期刊全文数据库 •万芳数字化期刊 •维普中文期刊数据库
37
期刊检索
中国期刊全文数据库 CJFD
• 中国学术期刊(光盘版)电子杂志社,全文 • “中国知识基础设施工程”( CNKI)的一部 分 • 6100种核心期刊与专业特色期刊 • 免费检索到篇名、刊号、作者、机构 • 全文收费,检索卡 • CAJ-CD版,专题光盘版 • 日更新 ,光盘月更,专题年更
药品不良反应文献检索和利用标准操作规程

目的建立药品不良反应文献检索和利用的工作标准,规范药品不良反应文献检索、检索信息的利用等过程。
适用范围适用于公司上市后药品不良反应文献检索。
职责药品不良反应监测与报告专职人员、其他药品安全委员会成员。
内容1.药品不良反应监测与报告专职人员每个月定时检索各文献数据库(如:万方、维普、中国知网等),收集可疑药品安全性信息。
工作内容如下:1.1 每个月定期检索文献;1.2 审阅并记录检索结果;1.3 评价和判断是否有有效的不良事件;1.4 处理和形成检索报告。
2.药品不良反应文献检索范围国内文献检索万方、维普、中国知网,还需检索国家食品药品监督管理总局网站药品安全警示专栏,国家药品不良反应监测中心网站相关专栏;如有资源,外文可检索MEDLINE (Pubmed)、Embase、MICROMEDEX等数据库。
3.药品不良反应文献检索过程文献检索的过程为:选择合适的数据库,优选适合的文献,构建合理的检索策略,保证查全率、查准率。
3.1 制定检索策略A检索词确定药品不良反应的文献检索通常以“主题词/关键词”途径进行。
主题词/关键词:药品名称,直接检索。
主题词/关键词:药品名称/活性物质、致、导致、作用、临床、使用、出现、引起、不良事件。
(或含)B检索日期设置通过设置检索记录的开始日期和结束日期锁定,进行检索;3.2 文献筛选通过阅读题目、摘要、全文,排除与药品安全性无关的文献(包括重复文献、细胞、动物实验;成品含量测定实验没有提及不良事件的试验等),得到最终纳入药品安全性研究的文献数量,记录数字。
文献筛选流程图如下:3.3 有效文献中信息处理文献中病例信息的收集,采用可疑即收集的原则,即不能排除是否为本公司产品时,需收集报告。
A对于个案病例报告收集信息,填写《药品安全信息登记表》,并处理、分析、报告。
B对于临床研究报告先查重;个例报告:如果文献中发生的不良反应比较明确,就按照出现不良反应的人数分别拆成相应的不良反应信息报告,收集填写《药品安全信息登记表》,并处理、分析、报告。
药品不良反应信息的检索

学术搜索引擎
学术搜索引擎是指用于检索学可以了解到 最新的药品不良反应研究成果和进展, 有助于深入了解药品安全问题。
这些搜索引擎不仅可以检索到学术论 文、研究报告等文献资料,还可以检 索到药品不良反应的相关信息。
专业的药品信息数据库
药品监管与决策
01
药品监管机构通过检索药品不良 反应信息,全面了解药品的安全 性情况,为制定科学合理的药品 监管政策提供依据。
02
药品监管机构根据检索结果,对 存在安全隐患的药品采取相应的 风险控制措施,如暂停销售、召 回等,以保障公众用药安全。
药品研发与改进
药品研发企业通过检索药品不良反应 信息,了解已上市药品的安全性特征 和潜在风险,为新药研发提供参考和 借鉴。
患者报告信息的局限性
患者报告的不良反应信息可能存在主观性和误报的情况,且缺乏专 业医生的诊断和评估,影响信息的可靠性。
信息更新与维护的挑战
法规和政策变化
药品监管政策和法规的变化可能 影响药品不良反应信息的收集、 报告和发布,需要不断更新和维
护数据库以适应变化。
数据量庞大
随着药品市场的扩大和患者数量 的增加,药品不良反应数据的数 量呈现爆炸性增长,对信息更新
05
药品不良反应信息检索 的挑战与展望
信息质量与准确性的挑战
数据来源多样
药品不良反应信息可能来源于临床试验、上市后监测、患者报告 等多种途径,数据来源的多样性导致信息质量参差不齐。
诊断标准不统一
不同国家和地区对药品不良反应的诊断标准可能存在差异,导致信 息分类和编码不统一,影响检索结果的准确性。
B型不良反应
与药物固有的药理作用无关的不良 反应,发生率较低,但通常难以预 测,与剂量无明确关系,如过敏反 应、致癌、致畸等。
文献检索和利用标准操作规程

文献检索和利用标准操作程序1目的学术文献是高质量的药品不良反应信息来源之一,根据法规要求制定文献检索和利用标准操作程序,规范文献检索和利用程序。
2范围适用于公司药品不良反应文献检索和利用。
3职责3.1本文件由药物警戒部制定。
3.2药物警戒部按本文件规定履行文献检索和利用的相关职责。
4定义4.1文献检索,是指将信息按一定的方式组织和存储起来,并根据信息用户的需要找出有关的信息过程,包括文献查找、分析判定、判定评价、有效利用的综合过程。
4.2检索式,是检索提问的逻辑表达式,由检索词以及系统支持的检索算符和检索字段构成。
5参考文件/依据5.1关于发布个例药品不良反应收集和报告指导原则的通告(2018年第131号)5.2《药品不良反应报告和监测检查指南(试行)》5.3关于发布上市药品临床安全性文献评价指导原则(试行)的通告(2019年第27号)6正文6.1文献检索的频率和时间范围要求6.1.1文献检索的频率首次上市或首次进口五年内的新药,文献检索至少每两周进行一次,其他药品原则上每月进行一次,也可根据药品风险情况确定。
6.1.2文献检索的时间范围检索的时间范围要有连续性,不能间断。
6.2文献检索的数据库来源药物警戒专员应对广泛使用的文献数据库进行检索,国内外文献均要求至少要同时检索两个数据库。
➢国内文献数据库:中国知网(CNKI)、维普网(VIP)、万方数据库等➢国外文献数据库:PubMed、Embase、Ovid等➢其他相关网站:国家药品监督管理总局网站药品安全警示专栏、国家药品不良反应监测中心网站相关专栏。
6.3文献检索的类型有关不良反应的文献类型主要包括:个案报道、病例系列、不良反应综述等,此外临床有效性和安全性研究、荟萃分析等也可能涉及到药品的不良反应。
6.4文献检索流程药物警戒专员根据要求定期进行公司药品不良反应文献的检索,收集可疑药品安全性信息。
6.4.1明确查找目的与要求,明确需检索的药品名称(商品名称、通用名称、别名、曾用名)、活性成分、相关不良反应、相同成分的不同剂型等信息资料。
药品不良反应文献检索程序文件

药品不良反应文献检索程序文件一、目的药品不良反应(Adverse Drug Reaction,ADR)的监测和研究对于保障公众用药安全至关重要。
本程序文件旨在规范药品不良反应文献检索的流程和方法,确保能够全面、准确、及时地获取相关文献信息,为药品不良反应的评估、管理和预防提供科学依据。
二、适用范围本程序适用于药品研发、生产、经营企业、医疗机构、药品监管部门以及从事药品不良反应监测和研究的相关机构和人员。
三、职责分工1、文献检索人员负责按照本程序的要求进行文献检索,制定检索策略,筛选和获取相关文献,并对检索结果进行整理和分析。
2、质量控制人员对文献检索的过程和结果进行质量控制,确保检索的准确性和完整性。
3、项目负责人负责审核文献检索方案和检索结果,协调解决检索过程中出现的问题。
四、检索资源1、国内外专业数据库如 PubMed、Embase、Web of Science、中国知网(CNKI)、万方数据知识服务平台等。
2、药品监管部门网站如国家药品监督管理局网站、美国食品药品监督管理局(FDA)网站等。
3、专业学会和协会网站如国际药物监测合作中心(UMC)网站、中国药学会网站等。
4、其他相关网站如医学论坛、学术博客等。
五、检索策略的制定1、确定检索主题明确需要检索的药品名称、不良反应症状、治疗疾病等关键信息。
2、选择检索词根据检索主题,选择合适的关键词和主题词。
关键词可以包括药品通用名、商品名、活性成分、不良反应名称、症状描述等。
主题词应参考相关数据库的主题词表。
3、构建检索式运用逻辑运算符(如“AND”“OR”“NOT”)将检索词组合成合理的检索式。
例如,检索“阿司匹林引起的胃肠道出血”,检索式可以为“阿司匹林 AND 胃肠道出血”。
4、调整检索策略在检索过程中,根据初步检索结果的数量和相关性,适时调整检索策略,如增加或减少检索词、改变逻辑运算符、限定检索范围等。
六、检索流程1、数据库选择根据检索需求和数据库的特点,选择合适的数据库进行检索。
药物不良反应-中国方剂数据库
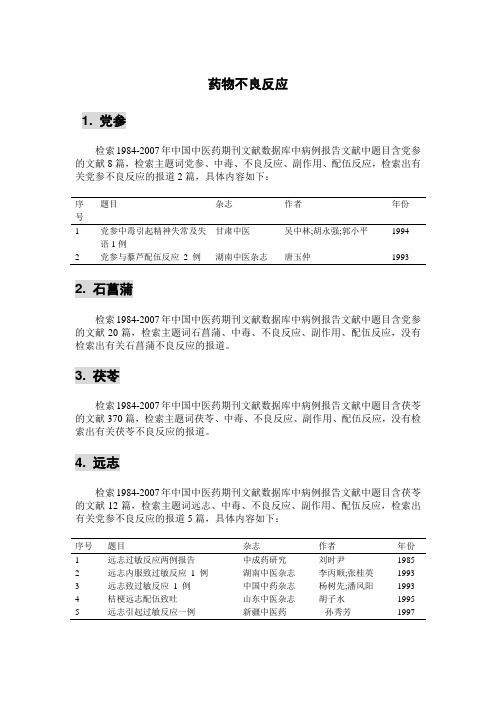
药物不良反应1. 党参检索1984-2007年中国中医药期刊文献数据库中病例报告文献中题目含党参的文献8篇,检索主题词党参、中毒、不良反应、副作用、配伍反应,检索出有关党参不良反应的报道2篇,具体内容如下:题目杂志作者年份序号1 党参中毒引起精神失常及失甘肃中医吴中林;胡永强;郭小平1994 语1例2 党参与藜芦配伍反应2 例湖南中医杂志唐玉仲1993 2. 石菖蒲检索1984-2007年中国中医药期刊文献数据库中病例报告文献中题目含党参的文献20篇,检索主题词石菖蒲、中毒、不良反应、副作用、配伍反应,没有检索出有关石菖蒲不良反应的报道。
3. 茯苓检索1984-2007年中国中医药期刊文献数据库中病例报告文献中题目含茯苓的文献370篇,检索主题词茯苓、中毒、不良反应、副作用、配伍反应,没有检索出有关茯苓不良反应的报道。
4. 远志检索1984-2007年中国中医药期刊文献数据库中病例报告文献中题目含茯苓的文献12篇,检索主题词远志、中毒、不良反应、副作用、配伍反应,检索出有关党参不良反应的报道5篇,具体内容如下:序号题目杂志作者年份1 远志过敏反应两例报告中成药研究刘时尹19852 远志内服致过敏反应1 例湖南中医杂志李丙顺;张桂英19933 远志致过敏反应1 例中国中药杂志杨树先;潘风阳19934 桔梗远志配伍致吐山东中医杂志胡子水19955 远志引起过敏反应一例新疆中医药孙秀芳19975. 桂枝检索1984-2007年中国中医药期刊文献数据库中病例报告文献中题目含茯苓的文献1338篇,检索主题词桂枝、中毒、不良反应、副作用、配伍反应,没有检索出有关桂枝不良反应的报道。
6. 龙骨检索1984-2007年中国中医药期刊文献数据库中病例报告文献中题目含龙骨的文献232篇,检索主题词龙骨、中毒、不良反应、副作用、配伍反应,检索出有关龙骨不良反应的报道3篇,具体内容如下:序号 题目杂志 作者 年份 1 接触龙骨粉致过敏反应二例中药通报 张礼洪 1987 2 柴胡加龙骨牡蛎汤致贫血2例报告四川中医 鄢建君 1987 3龙骨牡蛎用于戒毒患者致便血1例报道山西中医学院学报李成年20027. 熟地检索1984-2007年中国中医药期刊文献数据库中病例报告文献中题目含熟地的文献22篇,检索主题词熟地、中毒、不良反应、副作用、配伍,检索出有关龙骨不良反应的报道3篇,具体内容如下:8. 首乌检索1984-2007年中国中医药期刊文献数据库中病例报告文献中题目含首乌的文献81篇,检索主题词首乌、中毒、不良反应、副作用、配伍,检索出有关首乌不良反应的报道10篇,具体内容如下:序号 题目杂志作者 年份 1 何首乌引起过敏反应一例报告中医研究 靳华 1988 2何首乌引起药物热 1 湖南中医杂志刘fan1990序号 题目杂志作者 年份 1莱菔子与何首乌、熟地配伍致不良反应1例中国中西医结合杂志蔡新荣1996例3 何首乌致眼部色素沉着1例中国中医眼科杂志叶存喜19944 家族性何首乌过敏案陕西中医李寿彭19935 服制首乌出现副作用1例报告江西中医药李小衡1992 6 何首乌致皮肤瘙痒一例湖北中医杂志朱彤;江培春19927 服用何首乌致急性中毒性肝病1例中国中西医结合杂志叶亲华19968 口服首乌片出现严重肝损害一例新药与临床牛建海19969 何首乌致上消化道出血一例新疆中医药蔡红永199510 服首乌片致肝损害 1例新中医李方香19979. 山萸肉检索1984-2007年中国中医药期刊文献数据库中病例报告文献中题目含茯苓的文献7篇,检索主题词山萸肉、中毒、不良反应、副作用、配伍反应,没有检索出有关山萸肉不良反应的报道。
(2023版)药品不良反应的数据处理标准操作规程(新版)

文件名称:文件编码:编制人及日期:审核人及日期:批准人及日期:发放部门:质量保证部生效日期: 2022 年 12 月 01 日发放范围:质量保证部、销售部、办公室建立药品不良反应数据采集与处理操作规程,加强药品不良反应信息的采集和处理能力。
合用于公司药品不良反应相关数据的采集和处理。
药品不良反应监测与报告专职人员、其他药品安全委员会成员。
1. 药品不良反应数据的采集1.1 医疗机构1.1.1 医药代表采集途径指定医药代表,通过日常拜访医生、药师或者通过电子邮件、电话、传真等方式沟通,采集临床发生的药品不良反应信息。
1.1.2 利用经销商与医疗机构合同采集经销商在与医疗机构签订药品购销合同时,让医疗机构充分知晓不良反应报告的责任,鼓励医生向公司报告不良反应。
1.2 药品经营企业1.2.1 直接从药品零售企业采集公司销售人员直接从药品零售企业采集不良反应信息,通过日常拜访、电话等方式沟通并采集1.2.2 通过药品经销商采集不良反应在与经销商签订药品购销合同或者销售协议时,明确经销商的相关责任,敦促其采集不良反应。
1.3 电话和投诉1.3.1 药品说明书、标签中发布的电话的监管通过销售部、办公室及质量部电话的接听,记录并采集相关的不良反应信息。
1.3.2 通过法律诉讼渠道获悉的不良反应的需报告1.4 学术文献学术文献是高质量的药品不良反应信息来源之一,应定期对文献进行检索,并报告文献中涉及的不良反应。
1.4.1 频率:文献检索频率原则上每一个月进行一次1.4.2 检索库:中国知网(CNKI)、维普网(VIP)、万方数据库等国内文献数据库和PubMed、Embase、Ovid等国外文献数据库。
要求至少要同时检索两个数据库。
1.4.3 文献类型个案报导、病例系列、不良反应综述等,此外临床有效性和安全性研究、荟萃分析等文献来源也可能涉及到不良反应。
个案报导(对单个患者的不良反应进行描述和讨论)病例系列(对多个患者同一性质的不良反应进行描述及讨论)1.5 互联网及相关途径利用公司门户网站采集,在公司网站发布完整的产品说明书并及时更新,提供药品不良反应相关知识和合理用药指导。
药品不良反应文献检索程序

目的:建立药品不良反应文献检索程序。
适用范围:适用药品不良反应相关文献检索。
负责人:药品不良反应监测办公室主任、质量保证部部长、科研中心监测人员。
内容:一、国内文献检索(一)、中国知网(CNKI)1、简介中国知网(),是国家知识基础设施(National Knowledge Infrastructure,NKI)的概念,由清华大学、清华同方发起,始建于1999年6月。
中国知网已经发展成为集期刊杂志、博士论文、硕士论文、会议论文、报纸、工具书、年鉴、专利、标准、国学、海外文献资源为一体的、具体国际领先水平的网络出版平台。
分为基础科学、工程科技、农业科技、医药卫生科技等10个专业文献总库,168个专题数据库,中心网站的日更新文献量达5万篇以上。
其中医药卫生科技文献库涵盖预防医学与卫生学,中医学,中药学,中西医结合,基础医学,临床医学,感染性疾病及传染病,心血管系统疾病,呼吸系统疾病,消化系统疾病,内分泌腺及全身性疾病,外科学,泌尿科学,妇产科学,儿科学,神经病学,精神病学,肿瘤学,眼科与耳鼻咽喉科,口腔科学,皮肤病与性病,特种医学,急救医学,军事医学与卫生,药学等医药学领域。
截至2011年6月,收录国内学术期刊7778种,全文文献总量3200多万篇,其中药学方面的文献量达61万多篇;收录来自397家培养单位的博士学位论文15万多篇,其中药学方面的文献量达5600多篇。
收录来自598家培养单位的优秀硕士学位论文115万多篇,其中药学方面的文献量达2万多篇。
2、检索方法CNKI有文献检索、知识元检索、引文检索等多条途径。
本书仅介绍文献检索、高级检索两种方式,更多检索方式可从CNKI网站获取。
1)简单简单检索即在全文中进行检索。
在检索框中输入检索关键词后,点击“”按钮进行检索,见图1图12)高级检索点击“高级检索”进入高级检索页面。
页面上提供高级检索及其相应的检索控制项(主题、篇名、作者、作者单位、发表时间、文献来源、支持基金)。
疑似药品不良反应收集标准操作程序、收集记录、访问记录、信息收集计划、评估记录、记录填报要求

疑似药品不良反应信息收集标准操作程序1参考文件/依据1.1《药品不良反应报告和监测管理办法》(2011.07.01生效版);1.2关于发布个例不良反应收集和报告指导原则的通告(2018年第131号);1.3关于发布《上市许可持有人药品不良反应报告表(试行)》及填表说明的通知(2020.01.08) 。
1.4《药物警戒质量管理规范》(2021.05.13)2正文2.1医疗机构2.1.1销售部或经销商在与医疗机构签订药品采购合同时,将药品不良反应信息收集的职责加入其中。
确保医疗机构知晓药品不良反应收集的要求和方式,鼓励医务人员向持有人报告不良反应。
2.1.2公司销售人员每月拜访相应的医疗机构,了解医疗机构报告不良反应情况,发放“疑似药品不良反应信息收集记录”或相应二维码链接收集疑似药品不良反应信息,并及时向药物警戒部反馈不良反应收集过程中存在的问题。
2.1.3药物警戒部每月采取电子邮件、电话、传真等方式向医务人员收集临床发生的药品不良反应信息。
2.2药品生产企业、药品经营企业2.2.1在与药品生产企业或药品经营企业签订委托协议时,将药品不良反应信息收集的职责加入其中,明确信息收集和传递的要求。
2.2.2药物警戒部及相关部门每年定期评估生产企业或经销商履行信息收集责任的能力,采取必要措施确保所收集信息的数量和质量,填写“疑似药品不良反应信息收集情况评估记录”。
2.2.3持有人督促药品生产企业、经销商在与药品零售企业签订药品购销合同时,将药品不良反应信息收集的职责加入其中,确保药品零售企业知晓药品不良反应收集的职责。
2.2.4药物警戒部每年制定向药品生产企业或经销商收集不良反应信息的计划,并适时更新。
2.2.5督促经销商每年制定向药品零售企业收集不良反应信息的计划。
2.2.6销售部每年至少组织一次药品生产企业或经销商关于不良反应信息收集的培训,使其了解信息收集的目标、方式、方法、内容、保存和记录要求等,以提高不良反应信息的准确性、完整性和可追溯性。
我国药品不良反应相关文献分析

“病 例 报 告 ”栏 目 中 的 第 1, 4, 7, 10… 篇 进 行 研 读 分 析 , 统 计
严重 ADR
严重 ADR 的报道。
构成比( %)
例数( n) 总计( n)
2000 年 2001 年 2002 年 2003 年 2004 年 2005 年
74
76
100
84
88
100
522
34
结果21文献的数量对每一时间段发表在所选的5种药学期刊上篇名含不良反应的文献数量进行统计图22文献的类别及其构成比对每一时间段发表在所选的5种药学期刊上的相关文122所述方法进行分类统计计算每类文献在该时间段内占所检索文献总数的构成比图23严重不良反应报道的数量及其构成比对每一时间段发表在药物不良反应杂志病例报告栏目中严重adr报告的数量及其构成比进行统计1可见20002005年篇名含有不良反应的文献仅在所选的5种药学期刊上就有543篇其中以药物不良反应杂志报道数量最多达204篇占总数的3757
ports, as the basis of ADR research, still have the largest number of literature in recent years, accounted for 48.62%
on average. The number of research literature accounts for 9.33% during 2000 to 2002 and rise to 20.92% during
够导致人体永久的或显著的伤残; 对器官功能产 时 间 延 长[3]。 对 2000~2005 年 共 32 期
表 各时间段严重药品不良反应报道的数量统计
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
目的:建立药品不良反应文献检索程序。
适用范围:适用药品不良反应相关文献检索。
负责人:药品不良反应监测办公室主任、质量保证部部长、科研中心监测人员。
内容:
一、国内文献检索
(一)、中国知网(CNKI)
1、简介
中国知网(),是国家知识基础设施(National Knowledge Infrastructure,NKI)的概念,由清华大学、清华同方发起,始建于1999年6月。
中国知网已经发展成为集期刊杂志、博士论文、硕士论文、会议论文、报纸、工具书、年鉴、专利、标准、国学、海外文献资源为一体的、具体国际领先水平的网络出版平台。
分为基础科学、工程科技、农业科技、医药卫生科技等10个专业文献总库,168个专题数据库,中心网站的日更新文献量达5万篇以上。
其中医药卫生科技文献库涵盖预防医学与卫生学,中医学,中药学,中西医结合,基础医学,临床医学,感染性疾病及传染病,心血管系统疾病,呼吸系统疾病,消化系统疾病,内分泌腺及全身性疾病,外科学,泌尿科学,妇产科学,儿科学,神经病学,精神病学,肿瘤学,眼科与耳鼻咽喉科,口腔科学,皮肤病与性病,特种医学,急救医学,军事医学与卫生,药学等医药学领域。
截至2011年6月,收录国内学术期刊7778种,全文文献总量3200多万篇,其中药学方面的文献量达61万多篇;收录来自397家培养单位的博士学位论文15万多篇,其中药学方面的文献量达5600多篇。
收录来自598家培养单位的优秀硕士学位论文115万多篇,其中药学方面的文献量达2万多篇。
2、检索方法
CNKI有文献检索、知识元检索、引文检索等多条途径。
本书仅介绍文献检索、高级检索两种方式,更多检索方式可从CNKI网站获取。
1)简单
简单检索即在全文中进行检索。
在检索框中输入检索关键词后,点击“”按钮进行检索,见图1
图1
2)高级检索
点击“高级检索”进入高级检索页面。
页面上提供高级检索及其相应的检索控制项(主题、篇名、作者、作者单位、发表时间、文献来源、支持基金)。
见图2 高级检索步骤:
第一步:选择主题:在主题框中的下拉列表中选择篇名、关键词、摘要、全文、参考文献、中图分类号,可以通过主题框前方来增加或减少检索条件;
第二步:输入检索词:在检索框中输入;
第三步:设置其他检索项和检索词以及逻辑运算符(并含、或含、不含);
第四步:选择检索控制:根据需要选择下列检索控制条件:扩展、关系、起止年份、匹配。
第五步:点击检索键进行检索。
图2
3、文献下载
以“双黄连注射液不良反应”为检索词为例,利用简单检索方式,在检索词输入框中输入“双黄连注射液不良反应”,进行检索。
图3
可检索到相关文献84篇,在检索结果列表中可查看相关文献的题名、作者、来源、发表时间、数据库等信息,见图4。
鼠标点击文献题名可进入下载界面,如点击第一篇文献“清开灵及双黄连注射液不良反应90例分析”进行文献下载界面,如图5所示。
右键点击“PDF下载”或“CAJ下载”按钮,点击“目标另存为”,下载PDF格式或CAJ格式的文献全文。
图4
图5
4、付费方式
CNKI中所有文献的题录和文摘是免费检索和使用的,但下载文献全文需要付费。
个人下载全文需要以下几个步骤:(1)在中国知网注册用户;(2)给注册账户充值;(3)下载PDF 阅读器,或是CAJViewer阅读器;(4)检索、下载或阅读文献。
全文下载或在线阅读按0.5元/页计费。
对于机构用户单位,可以包库使用。
二、重庆维普资讯网
1、简介
重庆维普资讯网(《中文科技期刊数据库》)是重庆维普资讯公司产品,是经国家新闻出版总署批准的大型连续电子出版物,收录中文期刊12000余种,全文3000余万篇,学科范围包含社会科学、自然科学、工程技术、农业科学、医药卫生、经济管理、教育科学和图书情报。
2、检索方法
维普网上供广大读者检索使用的是《中文科技期刊数据库》。
网站提供的检索方式有快速检索、传统检索、分类检索、高级检索和期刊导航。
1)简单检索
登录维普网首页,在数据库检索区,输入需要查找的检索词,点击“搜索”按钮即实现快速搜索。
见图6。
图6
文献搜索框下拉菜单中还有期刊搜索、学者搜索、机构搜索等搜索对象。
可对不同检索对象选定不同的特征属性进行检索。
2)高级检索
登录维普网首页,在数据库检索区“开始搜索”下方,点击“高级检索”,即可进入高级检索页面,见图7。
高级检索中检索对象顺序可以通过题名或关键词框下拉菜单进行选择,分别有题名、关键词、文摘、作者、第一作者机构、刊名、分类号、作者简介等。
第一步:设置检索字段,在检索字段下拉框中选择,检索字段包括任意字段、机构、题名或关键词等;
第二步:输入所设置字段的检索关键词;
第三步:依照前两步设置其他检索字段和关键词,并设置逻辑关系(与、或、非);
第四步:点击“检索”按钮,检索文献。
图7
3、文献下载
以“清开灵注射液过敏性休克”为检索关键词为例,利用快速检索方式检索文献,见图8。
可检索到相关文献113篇,在检索结果列表中可查看相关文献的题名、作者、出处、部分摘要等信息。
点击文献题名可以查看文献关键词、全文快照、摘要等更多信息。
点击“在线阅读”或“下载全文”了解文献全文信息。
图8
二、国外文献检索
1、PubMed简介
PubMed (Public Medline),是一个免费的生物医学文摘数据库,提供部分论文的摘要及指向全文的链接。
它的数据库来源主要为MEDLINE。
其核心主题为医学,但亦包括其他与医学相关的领域,如护理学或者其他健康学科。
该数据库是由美国国立医学图书馆下属的生物医学信息中心开发。
PubMed的资源并不提供期刊论文的全文,但提供指向全文提供者(付费或免费)的链接。
数据类型有期刊论文、综述、以及与其它数据库链接。
2、检索方法
以检索药品不良反应信号检测理论(signal detetion theory)为例,简单介绍PubMed 的检索方法。
第一步:登录网站输入检索关键词“signal detetion theory”,点击“Search”按钮,如图,如图9。
图9
检索出有关“signal detetion theory”5202篇,检索结果页面每页显示20条,如图10.在检索结果页面的文献列表中,可以查看文献的题目、作者、是否有免费全文(Free PMC
Article)等信息。
PubMed的资源并不提供期刊论文的全文,但可能提供指向全文提供者(付费或免费)的链接。
检索结果页面右上角可以查看免费全文(Free full text)的文献数为8篇,并可以点击进入查看所有免费全文文献详细信息。
检索结果页面的文献列表中,点击“Free PMC Article”标示,可以查看附有该标示的文献全文。
三、变更记载和原因:。
