中国一类新药汇总
中药6类新药注册分类

中药6类新药注册分类【知识文章】中药6类新药注册分类导语:中药作为我国悠久的传统文化之一,拥有着广泛的疗效和应用价值。
然而,随着科技的不断进步和医药行业的发展,中药的注册分类正面临着新的挑战和机遇。
本文将为大家介绍中药6类新药注册分类,并探讨其对中药产业的影响和意义。
第一类:中药化学药品中药化学药品是指以中药为原料,通过化学合成或半合成方法制得的药品。
这类药品具有药理活性明确、结构清晰、质量稳定的特点。
典型的代表是阿司匹林和普萘洛尔等,它们在西医临床中有广泛的应用。
中药化学药品的注册分类,有助于提升中药在临床应用中的地位和可信度,促进中西医药的融合与发展。
第二类:植物药植物药是指以中草药为原料,通过提取、浸膏、粉碎等工艺制得的药品。
这类药品具有较为广泛的适应症和疗效,如金银花颗粒、三七胶囊等。
通过注册分类,可以明晰植物药的品质标准和药效,进一步规范生产流程和质量控制,保证植物药安全有效的使用。
第三类:动物药动物药是指以动物组织、器官或其分离物为原料制成的药品。
这类药品广泛应用于骨伤科、妇产科等领域,如龟板胶囊、牛黄解毒片等。
通过注册分类,有助于确保动物药品的来源和工艺符合规范,促进动物药产业的良性发展。
第四类:矿物药矿物药是指以矿物质为主要成分制成的药品,如石斛、雪莲等。
这类药品的疗效主要依赖于其中的微量元素和矿物质,具有较为独特的药理作用。
注册分类可以帮助规范矿物药的生产和应用,促进其在医疗领域的推广和应用。
第五类:虫草药虫草药是指以虫草菌为主要原料制成的药品,如冬虫夏草等。
虫草药具有免疫调节、抗肿瘤等独特的药理作用。
注册分类有助于确保虫草药的质量和产地的可追溯性,提高其在临床实践中的规范性和可信度。
第六类:其他中药除以上五类外,还有一些中药不属于特定类别,但具有一定疗效和应用价值。
这些中药或者具有独特的活性成分,或者依据临床实践逐渐形成一定用法用量等,如人参、黄芪等。
通过注册分类,可以更好地规范这些中药的生产和应用,保证其质量和疗效。
国家一类新药汇总

国家一类新药汇总★双环醇片(Bicyclol)商品名“百赛诺”,由中国医学科学院、中国协和医科大学药物所开发的产品,是我国第一个具有自主知识产权一类抗肝炎合成创新药物。
1996年12月经卫生部批准进入临床试验,2001年9月获得原SDA颁发的新药证书及生产批准文,由北京协和药厂生产上市。
目前已在世界16个国家地区获得20年发明专利保护,国内享有12年的行政保护期。
本品是在降酶药物联苯双酯和五味子基础上,经过化学合成筛选的药物,其良好的双重机制,能清除自由基作用以保护细胞膜,并且能保护肝细胞核DNA免疫受损,减少细胞凋亡的发生。
临床显示对乙肝病毒有较好的抑制作用,安全性好,毒性小,无致突变性不良反应,适用于轻、中度慢性肝炎。
临床显示远期疗效优于联苯双酯,已成为抗慢性病毒性肝炎的首选药物之一。
★爱普列特爱普列特是一种新型的5α-还原酶选择性抑制剂,1993年7月由中国药科大学、中科院上海有机化学研究所、扬州制药厂共同协作开发,1996年,爱普列特已批准进入临床研究阶段,1999年8月获得原SDA颁发的原料药及片剂新药证书与生产批件,2001年获得转正,现已成为联环药业的主导产品,享受12年的独家生产保护期。
爱普列特能选择性抑制5α-还原酶,其抑制作用的选择性优于非那雄胺,不良反应小,是安全有效的药物,也是竞争性较强的治疗药品。
该药可抑制睾酮的转化过程,使前列腺体内双氢睾酮含量下降,导致增生的前列腺体萎缩,从而达到改善良性前列腺增生病人排尿困难等症状,具有安全可靠性。
该药已列入《国家基本医疗保险药品目录》。
★恩必普(简称NBP)由中国医学科学院药物研究所和石家庄制药集团有限公司共同开发的,主要成分为丁苯酞,是我国心脑血管领域首个拥有自主知识产权的一类新药,获得两项国家专利。
“恩必普”适用于缺血性脑卒中(俗称脑中风)的治疗,主要成分丁苯酞与从芹菜籽中提取的芹菜甲素结构相同。
“恩必普”按现行的注册管理办法可划分为1.1类,其原料药化学名丁苯酞,油状,最初从南方生的水芹菜及其籽中提取分离而得,现已实现化学合成。
抗肿瘤药汇总表
47
阿糖胞苷
注射液
医疗保险(甲)
适用于急性白血病的诱导缓解期及维持巩固期。对急性非淋巴细胞性白血病效果较好,对慢性粒细胞白血病的急变期,恶性淋巴瘤。
70
酚磺乙胺氯化钠
注射液
71
阿替洛尔
注射液
72
果糖二磷酸钠
注射液
新药转正27
73
降钙素(重组,鲑鱼)
注射液
1.禁用或不能使用常规雌激素与钙制剂联合治疗的早期和晚期绝经后骨质疏松症以及老年性骨质疏松症。2.继发于乳腺癌、肺癌或肾癌、骨髓瘤和其他恶性肿瘤骨转移所致的高钙血症。3.变形性骨炎
74
丙酸睾酮
注射液
31
多西他赛
注射液
乳腺癌和非小细胞癌。肺癌、卵巢癌有效,对胰腺癌、胃癌、头颈癌等也有效。
32
盐酸阿扎司琼
注射液
用于放化疗、手术引起的恶心、呕吐;预防椎管内吗啡止痛引起的恶心、呕吐
33
高三尖杉酯碱
氯化钠注射液
医疗保险(甲)
适用于各型急性非淋巴细胞白血病,艰骨髓增生异常综合征、慢性粒细胞性白血病及真性红细胞增多症等有一定疗效。
胶囊、注射液
用于预防和治疗放疗、化疗引起的恶心、呕吐。
26
顺铂
注射液
地升国2
医疗保险(乙)
抗肿瘤药,为治疗多钟实体瘤的一线用药。
27
苯甲酸雌二醇
注射液
1、补充雌激素不足,如萎缩性阴道炎、女性性腺的功能不良、外阴干枯症、绝经期血管舒缩症状、卵巢切除、原发卵巢衰竭等;2、晚期前列腺癌(乳腺癌、卵巢癌患者禁用);3、与孕激素类药物合用,能抑制排卵;4、闭经、月经异常、功能性子宫出血、子宫发育不良。
国内主要医药公司新药汇总

翰森 制药
阿美替尼(3 代 EGFR), 氟马 替尼(Bcr-Abl ), 聚乙二醇洛塞 那肽(GLP-1)
依那利珠 单抗
(CD19), HS-10234 (逆转录酶
抑制剂)
聚乙二醇胸腺素 α1(胸腺肽 α1), 培 化西海马肽(长效
E-PO 类似物)
HS-10182(EGFR/H ER2),
HS-10220(H+/K+A TPase), 阿齐沙坦 醇铵片(AngII 受体
BPI-16350(CDK4/6), MRX2843(MerTK/FLT3), BPI-17509(FGFR1/2/3),
BPI-23314(BET), BPI-27336(ERK1/2), BPI-28592(NTRK), BPI-43487(FGFR 14), BPI-3016
G12C), BPI-38000(MEK), BPI-42000(RAS), BPI-18000(RAF), BPI-24000, BPI-25000, BPI-22000(IDH), BPI-33000(CD47), BPI-31000(OX40),
阿片受体),
SHR-A1403(c-Met), SHR2554(EZH2), SHR2042(GLP-1), SHR7280(GnRH), 呋格列泛 (GPR40), HRS5091(HBV 病毒核 衣壳), 环咪德吉(Hedgehog),
SHR9146(IDO),
SHR-1501(IL-15), SHR-1703(IL-5), SHR-1802(LAG-3),
国内主要上市公司新药一览公司已上市nda三期二期一期临床前恒瑞医药艾瑞昔布cox2瑞马唑仑gabaa受体吡咯替尼her2卡瑞利珠单抗pd1阿帕替尼vegfr氟唑帕利parpsp2086dpp4恒格列净sglt2海曲泊帕乙醇胺tposhr6390cdk46法米替尼多靶点tkishr4640uratishr3680雄激素受体shr1316pdl1shr1701pdl1tgf诺利糖肽glp1shr1314il17ashr0302jak1shr1209psck9shr0410阿片受体shr8554阿片受体shr5126a2arhao472aml1etoshr1459btkshr1704cd40shr1603cd47hs12041cmetshra1403cmetshr2554ezh2shr2042glp1shr7280gnrh呋格列泛gpr40hrs5091hbv病毒核衣壳环咪德吉hedgehogshr9146idoshr1501il15shr1703il5shr1802lag3shr7390mekshr0814盐酸r氯胺酮鼻喷剂nmda受体等shr0532romkshr9549serdshr1222sostshr1702tim3公司已上市nda三期二期一期临床前shr2150tlr7hrs9950tlr8盐酸右美托咪定鼻喷剂2肾上腺素受体m6g阿片受体ddo3055phdshr2285ins068胰岛素受体shr8008真菌cyp51酶中国生物制药安罗替尼多靶点tki异甘草酸镁注射液派安普利单抗pd1tqb2450pdl1tqb3139alktqb2440her2tqb3525pi3ktqb3101ros1al2846cmettqa3334tlr7tqf3083dpp4fhnd94013代egfrtqb3455idh2tq05510tqa3526fxrtqb3395egfrtqb3234mek12tqb3203喜树碱衍生物tqb3473braftqa3326ns5atqb3474hsp90tq05105jak2tqb3616cdk46tqa3563tqb38044代egfrtqc3564tqb3303cdk46tqb3602tqb3454idh1tqb3728iaptqb34563代egfrrd101pcsod翰森制药阿美替尼3代egfr氟马替尼bcrabl聚乙二醇洛塞那肽glp1依那利珠单抗cd19hs10234逆转录
1类新药分类

1类新药分类
一类新药分类有很多,以下是一些常见的例子:
1. 化学合成药物:这是最常见的新药分类,通过合成或化学方法制造的药物,如抗生素、抗癌药物等。
2. 生物制剂:这是使用生物技术制造的药物,如重组蛋白药物、基因治疗药物等。
3. 植物药物:这是使用植物提取物或植物化合物制造的药物,如中草药、植物精油等。
4. 功能性药物:这是一类具有特定功能的药物,如抗凝血药物、镇痛药物等。
5. 靶向药物:这是一类能够针对特定疾病分子靶点的药物,如靶向肿瘤治疗药物。
6. 基因编辑药物:这是一类使用基因编辑技术改变细胞或基因结构的药物,如CRISPR-Cas9技术开发的药物。
7. 免疫疗法药物:这是一类利用免疫系统来治疗疾病的药物,如免疫检查点抑制剂、CAR-T细胞疗法等。
以上仅是一些常见的新药分类,实际上还有许多其他的新药分类,随着科学技术的不断发展和创新,新的药物分类也在不断出现。
中药新药分类

中药新药分类 Prepared on 22 November 20201. 1.其主要成分为表没食子儿茶素没食子酸酯(EGCg),还有7种儿茶素类化合物成分。
局部使用治疗外生殖器和肛周疣。
2.中药新药研发分类一类未在国内外上市销售的药品:(1)通过合成或者半合成的方法制得的原料药及其制剂;(2)天然物质中提取或者通过发酵提取的新的有效单体及其制剂;(3)用拆分或者合成等方法制得的已知药物中的光学异构体及其制剂;(4)由已上市销售的多组份药物制备为较少组份的药物;(5)新的复方制剂;(6)已在国内上市销售的制剂增加国内外均未批准的新适应症。
二类改变给药途径且尚未在国内外上市销售的制剂。
三类已在国外上市销售但尚未在国内上市销售的药品:(1)已在国外上市销售的制剂及其原料药,和/或改变该制剂的剂型,但不改变给药途径的制剂;(2)已在国外上市销售的复方制剂,和/或改变该制剂的剂型,但不改变给药途径的制剂;(3)改变给药途径并已在国外上市销售的制剂;(4)国内上市销售的制剂增加已在国外批准的新适应症。
四类改变已上市销售盐类药物的酸根、碱基(或者金属元素),但不改变其药理作用的原料药及其制剂。
五类改变国内已上市销售药品的剂型,但不改变给药途径的制剂。
六类已有国家药品标准的原料药或者制剂。
3.药学研究资料:1. 药学研究资料综述2. 原料药生产工艺的研究资料及文献资料;制剂处方及工艺的研究资料及文献资料3.确证化学结构或者组分的试验资料及文献资料4.质量研究工作的试验资料及文献资料5.药品标准及起草说明,并提供标准品或者对照品6样品的检验报告书7.原料药、辅料的来源及质量标准、检验报告书8.药物稳定性研究的试验资料及文献资料9.直接接触药品的包装材料和容器的选择依据及质量标准4.改用沸点较低的乙醚提取药研发过程中,还是应以药理活性和药物疗效为核心。
不能将所有的萃取产物均视为有效成分。
如有研究发现,超临界CO2容易萃取出的地肤子油抗菌效果不明显,而有效成分是在萃取出油之后加入乙醇作提携剂提出的部分。
2023年ASCO会议国产新药进展更新报告

12023年ASCO会议国产新药进展更新报告ASCO 年会中国创新持续增加⏹美国临床肿瘤学会(American Society of Clinical Oncology ,ASCO )是全球领先的肿瘤专业学术组织,宗旨是预防癌症及改善癌症服务,拥有来自100多个国家超过40000名会员。
ASCO 年会固定在每年6月初于芝加哥举行,是肿瘤领域最重要的学术会议。
⏹从2011年开始,中国肿瘤学术研究逐渐登上ASCO 舞台。
自2021年以来,ASCO 年会上每年都有18-19项口头报告来自于国内学者。
ASCO2023年会上有19项国产口头报告,以“China”为关键字搜索每年ASCO 的摘要,也可以看出中国创新药产业的迅速发展趋势。
ASCO2023年会上,大部分中国创新药企将进行口头报告和壁报讨论,部分重磅靶点新药的进展有望给相应公司带来价值跃迁,建议重点关注。
┃ASCO 年会中国学者口头报告数量(个)┃ASCO 摘要China 关键字数量(个)51015202011201220132014201520162017201820192020202120222023501001502002503003504002015201620172018201920202021202220232公司产品靶点适应症阶段方案人数ORR(%)mPFS(月)mOS(月)Oral百利天恒BL-B01D1EGFR×HER3 ADC NSCLC(EGFRm);NSCLC (EGFRwt);SCLC;NPC;HNSCCI34;42;7;24;1361.8;40.5;14.3;45.8;7.7科伦药业KL590586RET RET突变实体瘤I6964百济神州Zanidatamab HER2双抗经治HER2扩增BTC IIb8041恒瑞医药SHR-1701PD-L1/TGF-βRII淋巴瘤和实体瘤I联合SHR25542657.7迪哲医药Golidocitinib JAK1R/R 外周T细胞瘤关键3543.8迪哲医药Sunvozertinib EGFR ex20EGFR ex20insNSCLC关键9760.8亘喜生物GC012F BCMA/CD19 CAR-T R/R MM I2993.138Poster & Publication only百利天恒SI-B001EGFR×HER3无驱动基因突变NSCLCII联合PBC;联合多西他赛;48;2231.3;45.5百利天恒SI-B001EGFR×HER3头颈鳞癌II PD-1+PBC进展;多西他赛经治或未经治9;14;822.2;64.3;12.5百利天恒SI-B003PD-1/CTLA-4实体瘤I5616.1 3.7科伦药业SKB-264TROP2 ADC NSCLC II EGFR野生型;突变型19;2026;60 5.3;11.1贝达药业BPI-16350CDK4/6HR+/HER2-mBC I单药;联合氟维司群24;43 4.2;60.5康宁杰瑞KN026+KN046HER2双抗+PD-L1/CTLA-4HER2+实体瘤II2653.8 5.6科济药业CT0180GPC3 scFv-CD3ε T晚期肝细胞癌I728.611.6首药控股SY-5007RET RET实体瘤I5062首药控股SY-3505ALK ALK+ NSCLC I/II8234.2公司产品靶点适应症阶段方案人数ORR(%)mPFS(月)mOS(月)Poster & Publication only百济神州BGB-11417BCL-2成熟B细胞瘤I3935.9百济神州LBL-007LAG3晚期黑色素瘤I联合特瑞普利单抗±阿昔替尼55;1123.6;45.4 5.7;5.5百济神州Zanidatamab HER2双抗1L HER2+BC Ib/II 联合多西他赛3390.9百济神州BGB-A445OX40实体瘤I±替雷丽珠单抗50;304;23百济神州ociperlimab TIGIT GC/GEJC Ib联合替雷丽珠单抗+化疗5950.8和黄医药HMPL-453FGFR胆管癌II12;1331.8;50 5.7;NR恒瑞医药SHR-1701PD-L1/TGF-βRII宫颈癌Ib/III 联合铂类化疗+贝伐珠3177.4信达生物IBI351KRAS G12C结直肠癌I4047.5信达生物IBI110LAG31L HER2-胃癌Ib1788.212.9NR信达生物IBI110LAG31L肝细胞癌联合信迪利单抗+仑伐替尼2729.6信达生物IBI939TIGIT NSCLC联合信迪利单抗vs 信迪利单抗28 vs 1413.2信达生物/驯鹿生物CT103A BCMA CAR-T R/R MM Ib/II8198.8亚盛医药alrizomadlin MDM2/p53黑色素瘤II联合K药2623.1亚盛医药alrizomadlin MDM2/p53恶性周边神经腱鞘瘤II1753亚盛医药APG-2449FAK/ALK NSCLC I3170.6泽璟制药ZG19018KRAS G12C实体瘤1216.7再鼎医药ZL-1211CLDN18.2实体瘤I/II966.70%康方生物AK112PD-1/VEGF1L无驱动基因突变NSCLC II联合化疗SCC 63;75;55non-SCC 72艾力斯furmonertinib EGFR EGFR ex20ins NSCLC2070公司产品靶点适应症阶段方案人数ORR(%)mPFS(月)mOS(月)Poster & Publication only嘉和生物GB263T EGFR/c-MET三抗EGFRm NSCLC I/II50嘉和生物lerociclib CDK4/6HR+/HER2-mBC III联合氟维司群vs 氟维司群137 vs 13811.07 vs 5.49迪哲医药Sunvozertinib EGFR ex20初治EGFR ex20ins NSCLC2673.1迪哲医药Sunvozertinib EGFR ex20EGFR TKI治疗失败NSCLC3221.9君实生物tifcemalimab BTLA ES-SCLC I/II联合特瑞普利单抗3826.3翰森制药HS-10241c-MET EGFRm NSCLC Ib联合阿美替尼2254.5翰森制药HS-20093B7H3 ADC实体瘤I4035和铂医药HBM4003CTLA-4肝细胞癌Ib联合特瑞普利单抗16;1246.7;9.1荣昌生物RC48HER2 ADC HER2+实体瘤II联合PD-1/PD-L1荣昌生物RC48HER2 ADC HER2+尿路上皮癌Ib/II联合特瑞普利单抗4173.2石药集团ALMB-0168GJA1骨肉瘤I1315.4石药集团SYSA1801CLDN18.2 ADC GC I1747.1亘喜生物GC012F BCMA/CD19 CAR-T R/R B-NHL I9100益方生物D-1553KRAS G12C结直肠癌I/II2420.87.62创胜集团TST001CLDN18.21L G/GEJC I/IIa联合CAPOX4067.5康辰药业KC1036Flt3;Axl;VEGFR2实体瘤I3613.9康辰药业KC1036Flt3;Axl;VEGFR2食管鳞癌II2429映恩生物DB-1303HER2 ADC实体瘤I/IIa5244.2诗健生物ESG401TROP2 ADC实体瘤I1136同宜医药CBP-1018PSMA/FRα ADC实体瘤I1007.2同宜医药CBP-1008TRPV6/FRα ADC实体瘤I8225.6赞荣医药ZN-1041HER2BC I单药;联合卡培他滨+曲妥珠21;1950;78.9赞荣医药ZN-1041HER2BC I单药714.3百利天恒:BL-B01D1临床I期数据更新⏹BL-B01D1是百利天恒研发的全球首创的EGFR×HER3双抗ADC药物,单药已开展了5个Ia/Ib期临床研究,覆盖16种肿瘤,已有涉及12种不同肿瘤类型的200余例受试者入组,已完成3个单药双臂III期注册临床及2个单药单臂关键注册临床研究的沟通交流申请的递交。
一类新药、二类新药、三类新药

二、化学药品
第一类:首创的原料药及其制剂。 1. 通过合成或半合成的方法制成的原料药及其制剂。 2. 天然物质中提取的或通过发酵提取的有效单体及其制剂。 3. 国外已有药用研究报道,尚未获一国药品管
第一类: 1. 中药材的人工制成品。 2. 新发现的中药材及其制剂。 3. 中药材中提取的有效成分及其制剂。 4. 复方中提取的有效成分。
第二类: 1. 中药注射剂。 2. 中药材新的药用部位及其制剂。 3. 中药材、天然药物中提取的有效部位及其制剂。 4. 中药材以人工方法在动物体内的制取物及其制剂。 5. 复方中提取的有效部位群。
第二类: 1. 已在国外获准生产上市,但未载入药典,我国也未进口的药品。 2. 用拆分、合成的方法首次制得的某一已知药物中的光学异构体及其制剂。 3. 国外尚未上市的由口服、外用或其他途径改变为注射途径给药者,或由局部用药改为全身给药者(如 口服、吸入等制剂)。
第三类: 1. 由化学药品新组成的复方制剂。 2. 由化学药品与中药新组成的复方制剂并以化学药品发挥主要作用者。 3. 由已上市的多组份药物制备为较少组分的原料药及其制剂。 4. 由动物或其组织、器官提取的新的多组分生化药品。
中药新药分类、研制程序及有关要求

中药新药分类、研制程序及有关要求扬州大学张传力中药学1. 中药新药研发分类一类未在国内外上市销售的药品:(1)通过合成或者半合成的方法制得的原料药及其制剂;(2)天然物质中提取或者通过发酵提取的新的有效单体及其制剂;(3)用拆分或者合成等方法制得的已知药物中的光学异构体及其制剂;(4)由已上市销售的多组份药物制备为较少组份的药物;(5)新的复方制剂;(6)已在国内上市销售的制剂增加国内外均未批准的新适应症。
二类改变给药途径且尚未在国内外上市销售的制剂。
三类已在国外上市销售但尚未在国内上市销售的药品:(1)已在国外上市销售的制剂及其原料药,和/或改变该制剂的剂型,但不改变给药途径的制剂;(2)已在国外上市销售的复方制剂,和/或改变该制剂的剂型,但不改变给药途径的制剂;(3)改变给药途径并已在国外上市销售的制剂;(4)国内上市销售的制剂增加已在国外批准的新适应症。
四类改变已上市销售盐类药物的酸根、碱基(或者金属元素),但不改变其药理作用的原料药及其制剂。
五类改变国内已上市销售药品的剂型,但不改变给药途径的制剂。
六类已有国家药品标准的原料药或者制剂。
2. 研制步异和审批程序2.1. 新药选题选题为关键环节,如选题不当,不但风险大,成功率低,即使研制成功,市场“寿命”也很短。
选题应根据中医药学术特点、优势和国内外医药市场需求信息,针对常见病、多发病、疑难病及功能紊乱性、免疫性疾病,从传统古方、名医验方、民间验方和科研方等方面选方,要求具有科学性、先进性、实用性,强调创新和应用。
凡无特色、属低水平重复或毒副作用严重者不宜开发研制。
可请有关专家咨询论证和进行预实验,然后定方立题。
2.2. 临床前研究新药研究题目确定后,根据新药类别规定进行临床前研究,包括工艺、质量标准、稳定性试验、药理、毒理研究等。
临床前研究结束后,打印各项申报资料,准备上报申请临床研究。
2.3. 临庆研究的审批研制单位将完整的申报资料连同样品报省卫生厅药政处,填写新药临床研究申请表。
中国一类新药汇总(SummaryofnewdrugsinChina)

中国一类新药汇总(Summary of new drugs in China)Summary of a new drug in ChinaAssumesXiaohezi7844 (gold coin +0, VIP+0): ThanksXiaohezi7844 (gold coin +3, VIP+0): ThanksLwf991229 (gold coin +1, VIP+0): 3Q~ thank you for sharing ~!This paper introduces some new drugs developed in China, and more than 20 new drugs which are being tested in clinical trials (NCE or traditional Chinese Medicine), hoping to add information about other new drugs* gendince (P53 injection)The world's first gene therapy product (P53 injection) has been known to have been treated in more than 5000 patients, but it has not yet published clinical trials in international journals (except for review):Phase I: phase I clinical stage. In March 9, 1998, Shenzhen SiBiono Gene Technology Co. Ltd. was established; in December 28, 1998, the State Drug Administration approved Recombinant Human Ad-p53 Injection entered phase I clinical trials.The second stage: phase II clinical stage. In October 7, 2000, the State Drug Administration approved Recombinant HumanAd-p53 Injection entered phase II clinical trial; December 2000,gene therapy products production plant built in Shenzhen; in July 3, 2002, the production process to obtain the State Intellectual Property Office issued a patent; November 22, 2002, access to the drug production license issued by the drug regulatory department of Guangdong province.The third stage: the new drug certificate and the formal listing stage. In October 16, 2003, Recombinant Human Ad-p53 Injection was approved by the State Food and drug administration to obtain a new drug certificate. In January 20, 2004, approved the production of quasi name brand production.* bicyclol (bicycol Bicyclol)Commodity name "bicycol", was developed by Chinese Academy of Medical Sciences and Peking Union Medical College pharmaceutical products, Chinese is first with independent intellectual property rights of a class of synthetic anti hepatitis drug innovation. In 1996, the Ministry of Health approved the clinical trial in, and got the new drug certificate and production approval document issued by the original SDA in September 2001. It was listed on the market by Beijing Xiehe pharmaceutical company. It has been granted patent protection for invention for 20 years in 16 countries and regions, and enjoys administrative protection for 12 years in china. This product is in reducing enzyme drug biphenylbiester and Schisandra basis, through chemical synthesis drug screening, the dual mechanism, can free radical scavenging action to protect the cell membrane, and can protect the liver nuclear DNA immune damage. Clinical shows that it has good inhibitory effect on hepatitis B virus, safe, small toxicity, nomutagenicity, adverse reactions, suitable for mild, moderate chronic hepatitis. Clinical results show that the long-term efficacy is better than that of biphenyl diester, and it is expected to become one of the first choice drugs in the treatment of chronic viral hepatitis.Epristeride.Epp Leo Te is a new type of 5 alpha reductase inhibitors, July 1993 by China Medicine University, Shanghai Institute of organic chemistry, Yangzhou pharmaceutical factory cooperation development, in 1996, Epp Leo Te has been approved in clinical trials, August 1999 SDA issued the original raw material and tablets drug certificate and production approval, 2001 was positive, has become a joint pharamceutical leading products, enjoy the exclusive production of 12 years. The drug can inhibit the conversion of testosterone to dihydrotestosterone in vivo, content of prostate gland hyperplasia decreased, resulting the forefront of atrophy, so as to improve the benign prostatic hyperplasia patients with dysuria symptoms, with certain safety and reliability. According to the requirements of a class of drugs, the drug in clinical study of the opening stage, and achieved satisfactory results, the drug has been included in the "directory" of the national basic medical insurance drug products listed at the beginning, Epristeride rising stage, the market share is not high, can become a drug therapy are still competitive the test of the market to be strong.Dl-3-butylphthalide.The main component of "Pu Pu" is butylphthalide, which is jointly developed by the Institute of drug research, Chinese Academy of Medical Sciences and Shijiazhuang Pharmaceutical Group Ltd,It is the first class of new drugs with independent intellectual property rights in the field of cardiovascular and cerebrovascular in China. It has won two national patents. The treatment of ischemic stroke (commonly known as stroke) is the main component of butylphthalide, which is similar to the apigenin extracted from celery seeds. The market for many years of the product, the market share is not high, Lenovo Hony Pharmaceutical Group entered after can have a new look, not only to look at the management, but also depends on the clinical data and reflect the doctor.Injection hematoporphyrin.Hematoporphyrin is a kind of photosensitizer first invented in China. It belongs to a new kind of drug and is a new drug for the treatment of malignant tumor. It is known as "photochemical missile"". Chongqing modern biological pharmacy in 2003 won the approval of the original SDA production, exclusive production of the listing, commodity name "happy" points".The drug is administered by intravenous drip and reaches the malignant tumor tissue along with blood circulation, and accumulates and accumulates in it. Laser irradiation therapy is needed in a specific wavelength of these tumors, the incidence of drug photochemical reaction, produce a price of oxygen, directly kill the tumor tissue, the whole process ofnormal human tissue is not much damage. Whether for primary cancer or recurrent cancer, can achieve the purpose of treatment or improvement.* CMNaA new class of anticancer sensitizing agent of sodium glycididazole (CMNa) is our own design and development of innovative drugs, with independent intellectual property rights, the 2002 Guangzhou Laitai pharmaceutical get a new drug certificate issued by the original SDA and the production of documents, the exclusive production market, commodity name "sodium glyci didazole".As one of the very few toxic and highly effective chemotherapeutic sensitizing agents in the world, it is an innovative chemical synthetic drug. The drug was developed by radiology Laboratory of Second Military Medical University in 1983 and has been developed for more than 10 years. In September 1993, the State Patent Office granted the invention patent right; in early 2000, the patent was awarded the gold medal of invention issued by the State Intellectual Property Office and the world intellectual property organization. Clinical studies have shown that the treatment of cancer has a good therapeutic effect, and has a certain market prospect.RmhTNF (rmhTNF).Injection of recombinant mutant human tumor necrosis factor (rmhTNF) was injected to Shanghai celstar Biological Pharmaceutical Co. Ltd. to develop the use of recombinantmutant human tumor necrosis factor, commodity name "rmhTNF", to get a new drug certificate in April 24, 2003, is the world's first approved on the systemic application of the tumor necrosis factor mutant. The product of a variety of malignant tumors in particular has a better curative effect on the respiratory system of malignant tumor, its mechanism is mainly: kill the tumor cells directly destroy tumor tissues; blood supply; regulation mediated immune; enhance the chemosensitivity of /. This product is put on the market, the current sales are limited, whether the future can get better economic benefits remains to be observed.Naftopidil TabletsNaftopidil Tablets is a new class of anti hypertension chemical synthesis has independent intellectual property rights of China's first by the Guizhou eakan Pharmaceutical Group 8 years of independent research and development success, (trade name: Bo Di), listed in May 2001. It is said to be the first class of new synthetic chemicals in China, thus ending the history of none of the new anti hypertensive synthetic chemicals made in china. Naftopidil Tablets has its own unique advantages in the treatment of hypertension: the drug is super selective alpha 1 - adrenergic receptor blockers, with 5 - HT1A receptor agonist and Ca2 + channel antagonists; with multiple antihypertensive mechanism, effective control of blood pressure in the same time, can avoid the "first effect" position hypotension and reflex tachycardia adverse reaction rate, has good effect on the metabolism of blood glucose, blood lipid, can improve prostate hypertrophy caused by dysuria, perhaps is a safe and effective drug for long-term treatment of newhypertension. But due to various reasons and similar products competition, the sale of this drug has been unsatisfactory. There are some difficulties in changing the situation.* artemisininResearch is a successful example of the development of new drugs in exploring the treasure basis of TCM in our country, it is the five Military Medical Science Academy of the PLA pharmacy researchers experience cooperation achievements over the development of the national major scientific research projects. In addition to the effective treatment of antimalarial drugs, the application prospect of artemisinin in the treatment of anti blood worms and anticancer drugs is also promising at home and abroad. But the new breakthrough is still in the compound preparation.Boanmycin (Boanmycin).A class of drugs, antitumor antibiotic boanmycin is China's first development of antitumor antibiotics, a class of drugs. Boanmycin originally called Bleomycine A6, is Streptoverticillium Pingyang (Streptomyces verticilus Var. Pingyangensis new variant of n.sp.) produced by bleomycin (B1eomycin), which belongs to the family of boanmycin (Boanmycin) and bleomycin (B1eomycin) has the same anti-tumor spectrum, of liver cancer, gastric cancer, lung cancer and colon cancer have a high inhibition ability, and pulmonary toxicity was significantly lower than that of other similar products.* retinoic acid for the treatment of leukemia (APL)By the treatment of arsenic trioxide (APL, MDS, MM, leukemia)Nobex (NOBEX).Composition of mouse nerve growth factor (mNGF), has been listed as the State Planning Commission high tech industrialization demonstration project, was also the 2002 National Torch project, it is the national Xiamen beidazhilu Biological Engineering Co. Ltd. and the Ministry of health of Lanzhou Biological Products Research Institute jointly developed a new drug (pharmaceutical). The indications for development are cyclohexane induced neurological damage. For the treatment of various types of nerve injury. The current market situation, the media rarely reported. The industry is not very optimistic.Endostar (Endostar).The world's first anti tumor drug Endostar recombinant human endostatin (Endostar) in 2006 listed on the first Chinese! The drug belongs to the first class of biological products "by Yantai medgenn bioengineering Limited by Share Ltd (to be renamed the Shandong Herald medgenn bio Pharmaceutical Co., Ltd.) presided over the development of a novel antitumor drug, have all intellectual property rights, the successful development of the drug research and development also marks the China in anti-tumor angiogenesis the drug is walking in the forefront of the world.Endostar is the basis of detecting vascular endothelial growth factor of the scientists in the United States, through the appropriate modification and special protein refolding process is developed, it has no obvious effect when used alone, but in combination with other anticancer drugs in use, can increase the effect of chemotherapy. (Endostar) the successful listing is to the United States scholar Dr. Luo Yongzhang (a professor at the Tsinghua University, Changjiang Scholars, medgenn biotechnology company chief scientist) led product research and development team, led by academician Sun Yan, a clinical multicenter study of collaborative group and Simcere professional marketing team of three party closely, common wisdom conceived.Comments: it is understood that Endostar sales in good condition, the drug's clinical stage four is underway, the median survival of patients with critical data needs to be disclosed. Look forward to the international academic journals and clinical papers published the objective weight, this is a short board China company, not good at the international stage and academic forum to promote their own achievements, light media hype, it will make people dissatisfied or suspicion. I wish to be the first to break the China company harbinger of publicity, the products do go abroad.ZT-1.Shanghai new drug research and development in the development of natural anti dementia drugs based on the present in Europe has completed 6 trials, the results gratifying, the foreign partner Debiao group has developed a new long-actingformulations, more suitable for the patients with convenient use. The progress of clinical trials China slowly, associated with the Chinese current regulatory system。
1-6类新药

1、未在国内外上市销售的药品:(1)通过合成或者半合成的方法制得的原料药及其制剂;(2)天然物质中提取或者通过发酵提取的新的有效单体及其制剂;(3)用拆分或者合成等方法制得的已知药物中的光学异构体及其制剂;(4)由已上市销售的多组份药物制备为较少组份的药物。
(5)新的复方制剂;2、改变给药途径且尚未在国内外上市销售的制剂。
3、已在国外上市销售但尚未在国内上市销售的药品:(1)已在国外上市销售的原料药及其制剂;(2)已在国外上市销售的复方制剂;(3)改变给药途径并已在国外上市销售的制剂。
4、改变已上市销售盐类药物的酸根、碱基(或者金属元素),但不改变其药理作用的原料药及其制剂。
5、改变国内已上市销售药品的剂型,但不改变给药途径的制剂。
6、已有国家药品标准的原料药或者制剂。
这是1-6类药的概念,略微有一点点不全,但大概是这样。
我慢慢说。
所谓1类新药,是彻彻底底的新药,新结构,新疗效,新创造,底下的五大类分类指的是一类新药的研发途径和方式。
化学合成,还真别觉得恶心,绝大多数的药物,都是化学方法合成的。
生物发酵或者生物提取,这种基本都需要做皮试,因为每批的药杂差别会很大。
对现有有效成分进行拆分,比如某治疗高血压的药物,左旋异构体80%,右旋异构体20%,日本研发,当时做了右旋异构体毒理,对人体无害,但也没疗效,有疗效的是左旋,于是就复合成分申报了,也过了,现在在卖,但是美爹把这个药物做了拆分,现在以完全左旋异构体作为单一成分重新申报,噱头是更纯疗效更好,这个也算一类药。
在药企内部,潜规则里,这个属于很无耻的行为。
第四种,属于存在于传说中的一类药,国内20年没见以此为理由申报的。
第五种,是中国现阶段比较多的一类药,最著名的就是少儿氨酚黄那敏颗粒,简单说,就是把A药和B药变成A+B,这就算你的一类新药了。
看起来很坑爹是不?但这不是简单的搀和在一块就完了,所有的药理(主要指疗效),临床,毒理(主要指副作用)【括号里面的,下面我就不重复了】都是要重新做的。
新药注册分类精简汇总(附表格)

新药注册分类精简汇总(附表格)
1类:境内外均未上市的创新药。
指含有新的结构明确的、具有药理作用的化合物,且具有临床价值的药品。
2类:境内外均未上市的改良型新药。
指在已知活性成份的基础上对其结构、剂型、处方工艺、给药途径、适应症等进行优化,且具有明显临床优势的药品。
2.1含有用拆分或者合成等方法制得的已知活性成份的光学异构体,或者对已知活性成份成酷,或者对已知活性成份成盐(包括含有氢键位公形键的盐),或者改变已知盐类活性成份的酸根、碱基或金属元素成其他非共价键衍生物(如络合物、整合物或包合物),且具有明显临床优势的药品。
2.2含有已知活性成份的新剂型(包括新的给药系统)、新处方工艺新给药途径,且具有明显临床优势的药品。
2.3含有已知活性成份的新复方制剂,且具有明显临床优势。
2.4含有已知活性成份的新适应症的药品。
3类: 境内申请人仿制境外上市但境内未上市原研药品的药品。
该类药品应与参比制剂的质量和疗效一致。
4类: 境内申请人仿制已在境内上市原研药品的药品。
该类药品应与参比制的质量和疗效一致。
5类:境外上市的药品申请在境内上市。
5.1境外上市的原研药品和改良型药品申请在境内上市。
改良型药品应具有明显临床优势。
5.2境外上市的仿制药申请在境内上市。
成都新特药(汇总)

10ml 25mg*20s 25mg*100s 1ml:250μ g*1s 10s 200mg*12s 5mg*20 0.5g*60s 4000ml 5g*10袋 0.4g*20 0.2g*6s 100mg:2ml*5支 5g:50mg 20s 1mg*30s 0.1g*30s 25片 1mg*30s 18ug*10s 18ug*10s 10mg*50s 50ug*100s 5mg*10s 14g 0.4ml 10ml*1g*5支 0.2g:0.02g:30s 1ml:30mg*10支 4g*6 200mg*10s 2ml:4400IU 0.25g*6袋 3ml:300单位 50mg*10s 6g*12袋 15ml:7.04Gg 5g*15袋 0.5g*48 0.5g*24s 4g*12袋 25mg*10s 10mg*10 50mg美国 支 荧光素钠注射液 5ml:0.5g(10%)*12支 美国 瓶 再普乐(奥氮平片) 5mg*28s 美国 盒 (进口)思然/聚乙二醇滴眼液 5ml 美国AlconL 支 胰岛素注射笔针头(BD超细超短型) 1*20mm 美国爱尔兰制造 支 疏血通注射液 2ml*10支 牡丹江友博药业有限责任公司 盒 酒石酸托特罗定片舍尼亭 2mg*14s 南京美瑞制药有限公司盒 舍尼通/普适泰片 70/4mg*14s 南京美瑞制药有限公司瓶 利维爱/替勃龙片(蛋白同化制剂) 2.5mg*7s 南京欧加农制药 盒 巴氯芬片 10mg*10s 宁波市天衡制药有限公司 盒 (冷)诺和灵30R笔芯/精蛋白生物合成人胰岛素注射液(预混30R)诺和诺德 300IU*3ml 支 精蛋白生物合成人胰岛素注射液(预混50R) 3ml:300iu 诺和诺德 支 生物合成人胰岛素注射液(诺和灵R) 3ml:300iu 诺和诺德 支 (诺和锐30特充)门冬胰岛素30注射液 3ml:300iu 诺和诺德(中国)制药支 门冬胰岛素注射液(诺和锐) 3ml:300iu 诺和诺德(中国)制药支 诺和灵30R笔芯精蛋白生物合成人胰岛素注射液 3ml:300 诺和诺德(中国)制药支 胰岛素笔式注射器(诺和笔4) 诺和诺德(中国)制药盒 诺和锐30笔芯/门冬胰岛素30注射液 300IUml*3ml 诺和诺德(中国)制药有限公司分包装 盒 (进口)欧维婷/雌三醇乳膏 15g:15mg 欧加农(爱尔兰)公司 盒 普罗布考片 0.125g*32s 齐鲁制药有限公司 盒 普南扑灵/普拉洛芬滴眼液 5ml:5mg 日本千寿制药株式会社支 麦滋林/L-谷氨酰胺呱仑酸钠颗粒 0.67g*15袋*10g 日本寿制药株式会社 包 密固达/唑来膦酸注射液 100ml:5mg 瑞士诺华制药 支 安博维/厄贝沙坦片 0.15g*7 赛诺菲(杭州)制药有限公司 盒 甘精胰岛素注射液 3ml:300iu 赛诺菲安万特 支 亚莫利/格列美脲片 2mg*15 赛诺菲安万特(北京)制药有限公司 盒 (可达龙)盐酸胺碘酮片 0.2g*10s 赛诺菲安万特(杭州)制药 盒 注射用重组人白介素-11 1.5mg 山东阿华生物药业有限公司 支 肝素钠乳膏 20g 山东博士伦福瑞达制药有限公司 支 步长/稳心颗粒(无糖型) 5g*9袋 山东步长制药有限公司盒 步长稳心颗粒 9g*9袋 山东步长制药有限公司盒 羟乙基淀粉130/0.4氯化钠注射液 500ml 山东长富洁晶药业 瓶 复方红衣补血口服液 10ml*10支 山东翔宇健康制药 盒 升血小板胶囊 0.45g*24 陕西郝其军制药股份有限公司 盒 复方皂矾丸 0.2g*72 陕西郝其军制药有限责任公司 盒 替米沙坦氢氯噻嗪片 7s 上海勃林格 盒 爱全乐/异丙托溴铵气雾剂 10ml:200揿 20ug/揿 上海勃林格殷格翰药业有限公司 支 美卡素/替米沙坦片 80mg*7s 上海勃林格殷格翰药业有限公司 盒 溴吡斯的明片 60mg*60s 上海三维制药有限公司瓶 恩替卡韦片(博路定) 0.5mg*7s 上海施贵宝药业 盒 艾洛松糠酸莫米松乳膏 5g 上海先灵葆雅制药 支 祥鹤/脑安胶囊 0.4g*30s 上海翔鹤药业有限公司瓶 产复康颗粒 5g*15 深圳三顺制药有限公司盒 乳增宁片 0.6g*24s 深圳三顺制药有限公司盒
最新医保目录中抗肿瘤药物及适应症总结2024

最新医保目录中抗肿瘤药物及适应症总结20242023年12月13日,2023版国家医保目录调整结果公布,新增126种药品!新版医保目录将于2024年1月1日正式实施。
在谈判/竞价环节,143个目录外药品参加,其中121个谈判/竞价成功,成功率为84.6%,平均降价61.7%,成功率和价格降幅均与2023年基本相当。
其中,新增抗肿瘤药物21种,涉及多个癌种。
以下是2023年国家医保药品目录提到的抗肿瘤药物,已按不同癌症类型分类整理,可按需查询。
非小细胞肺癌1甲磺酸奥希替尼片限:1IB-HIA期存在表皮生长因子受体(EGFR)外显子19缺失或外显子21(1858R)置换突变的非小细胞肺癌(NSe1C)患者的治疗,患者须既往接受过手术切除治疗,并由医生决定接受或不接受辅助化疗;2.具有表皮生长因子受体(EGFR)外显子19缺失或外显子21(1858R)置换突变的局部晚期或转移性非小细胞肺癌(NSC1e)成人患者的一线治疗;3.既往经EGFR酪氨酸激酶抑制剂(TKI)治疗时或治疗后出现疾病进展,并且经检测确认存在EGFRT790M突变阳性的局部晚期或转移性NSC1C成人患者的治疗。
有效期:2024年1月1日至2024年12月31日2甲磺酸阿美替尼片限:1.表皮生长因子受体(EGFR)外显子19缺失或外显子21(1858R)置换突变的局部晚期或转移性非小细胞肺癌(NSC1C)成人患者的一线治疗;2.既往经EGFR酪氨酸激酶抑制剂(TK1)治疗时或治疗后出现疾病进展,并且经检测确认存在EGFRT790M突变阳性的局部晚期或转移性非小细胞肺癌成人患者的治疗。
有效期:2023年3月1日至2024年12月31日3克理替尼胶囊限间变性淋巴瘤激酶(A1K)阳性的局部晚期或转移性非小细胞肺癌患者或ROS1阳性的晚期非小细胞肺癌患者。
有效期:2023年3月1日至2024年12月31日4塞瑞替尼胶囊限间变性淋巴瘤激酶(A1K)阳性的局部晚期或转移性非小细胞肺癌(NSC1C)患者的治疗。
国家一类、二类、三类、四类药物的意思

国家一类、二类、三类药物
并不是说一类二类的质量就好点,三类的就差点.这个与质量无关的.这个主要与研发的难度有关.一类新药,我国现在很少能研发的.现在大部分是三四五类新药.
一类未在国内外上市销售的药品:
(1)通过合成或者半合成的方法制得的原料药及其制剂;
(2)天然物质中提取或者通过发酵提取的新的有效单体及其制剂;
(3)用拆分或者合成等方法制得的已知药物中的光学异构体及其制剂;
(4)由已上市销售的多组份药物制备为较少组份的药物;
(5)新的复方制剂;
(6)已在国内上市销售的制剂增加国内外均未批准的新适应症。
二类改变给药途径且尚未在国内外上市销售的制剂。
三类已在国外上市销售但尚未在国内上市销售的药品:
(1)已在国外上市销售的制剂及其原料药,和/或改变该制剂的剂型,但不改变给药途径的制剂;
(2)已在国外上市销售的复方制剂,和/或改变该制剂的剂型,但不改变给药途径的制剂;
(3)改变给药途径并已在国外上市销售的制剂;
(4)国内上市销售的制剂增加已在国外批准的新适应症。
四类改变已上市销售盐类药物的酸根、碱基(或者金属元素),但不改变其药理作用的原料药及其制剂。
五类改变国内已上市销售药品的剂型,但不改变给药途径的制剂。
六类已有国家药品标准的原料药或者制剂。
国内医药领域核心品种大全

国内医药领域的部分核心品种首仿药系列1、恒瑞医药:奥沙利柏、多西他赛、伊利替康;2、恩华医药:齐拉西酮,原研厂家辉瑞;3、白云山:福泰(仿达菲);4、海南海药:紫杉醇注射液、头孢西丁钠;5、信立泰:泰嘉(硫酸氢氯吡格雷);6、上海医药:仿达菲;7、海正药业:达菲中间体;8、同仁堂:3个仿制品种已进入审批生产程序;9、双鹤药业:2009年3月27日正式推出了公司最新仿制药研发成果—“冠爽通用名:匹伐钙”;10、长春高新:艾塞那肽产品在国内首家通过国家食品药品监督管理局的审批,该药被国际糖尿病专家列为四大潜力药物之首;11、康芝药业:瑞芝清(尼美苏利颗粒)。
独家中药系列1、云南白药:白药系列,国家绝密配方,国家一类中药保护品种;2、片子癀:片子癀系列,国家绝密配方,国家一类中药保护品种;3、沃华医药:心可舒片,国家中药保护品种;4、东阿阿胶:阿胶系列,国家首批非物质文化遗产扩展项目名录;5、精华制药:王氏保赤丸、季德胜蛇药片,国家中药保密品种;6、中恒集团:血栓通注射液;7、千金药业:妇科千金片;8、中新药业:速效救心丸,国家级机密中药品种;9、广州药业:消渴丸;10、马应龙:麝香痔疮膏;11、独一味:独一味系列;12、金陵药业;脉络宁注射液;13、天士力:复方丹参滴丸;14、华润三九:999感冒灵、皮炎平、正天丸、胃泰,华蟾注射液,国家保密配;15、九芝堂:驴胶补血冲剂、乙肝宁冲剂,国家二级中药保护品种。
赤丹退黄颗粒,国家保密配方;16、同仁堂:六味地黄丸;17、太极集团:急支糖浆;18、桐君阁:桂枝合剂、四君子合剂、驱虫消食片,国家中药保护品种;19、海南海药:枫蓼肠胃康颗粒剂,国家中药保护品种;20、嘉应制药:双料喉风散;21、桂林三金:三金片,西瓜霜系列;22、奇正藏药:奇正消痛贴膏,国家中药保护品种,国家保密品种;23、西藏药业:诺迪康系列;24、羚锐制药:通络去痛膏、壮骨麝香止痛膏;25、美罗药业:伤科接骨片、鱼鳞病片、珠珀安神丹,国家中药保护品种;26、亚宝药业:丁桂脐贴;27、康缘药业:热毒宁注射液、痛安注射液;28、康恩贝:可达灵,国家中药保护独家品种。
第一期药学简报新药介绍目录

2005年新药介绍目录及第一期新药介绍一、抗感染药物类:1、青霉素类:盐酸仑氨苄西林、阿洛西林、呋布西林钠、2、头孢菌素类:头孢噻吩钠、头孢替安、头孢替唑钠、头孢丙烯、头孢地嗪、头孢硫脒、头孢尼西钠、头孢泊肟酯、头孢匹胺钠、头孢他美酯、头孢唑肟、头孢克肟。
3、氧头孢烯类:拉氧头孢、头孢米诺。
4、其他β-内酰胺类抗生素:美洛培南。
5、氨基糖苷类:依替米星。
6、四环素类:多西环素。
7、大环内酯类:克拉霉素、地红霉素。
8、氯霉素类:甲砜霉素。
9、万古霉素类:去甲万古霉素。
10、磺胺类:磺胺二甲嘧啶钠、磺胺嘧啶银。
11、喹诺酮类:司帕沙星、加替沙星、盐酸芦氟沙星。
12、硝基咪唑类:奥硝唑。
13、林可霉素类、多粘菌素类及硝基呋喃类无新药购进。
14、抗病毒药:喷昔洛韦、咪喹莫特乳膏剂。
二、抗肿瘤类:1、烷化剂类:尼莫司汀、卡莫司汀、氮烯咪胺(达卡巴嗪)。
2、抗代谢类抗肿瘤药:替加氟-尿嘧啶、去氧氟尿苷、卡莫氟、卡培他滨、吉西他滨。
3、激素类抗肿瘤药:来曲唑、他莫西芬。
4、抗生素类抗肿瘤药:无新药购进。
5、抗肿瘤抗体类:无新药购进。
6、天然来源抗肿瘤药:多西他赛(多西紫杉醇)、拓朴替康、去甲斑蝥酸钠。
7、其他抗肿瘤药及抗肿瘤辅助药:奥沙利铂、奈达铂(捷佰舒)、门冬酰胺酶、托烷司琼、艾迪注射液。
三、心血管系统药物:1、强心药:米力农。
2、抗心律失常药:艾司洛尔、索他洛尔。
3、降血压药:①、α肾上腺素受体阻滞药:特拉唑嗪、甲磺酸多沙唑嗪。
②、β肾上腺素受体阻滞药:美托洛尔、富马酸比索洛尔、盐酸塞利洛尔。
③、αβ受体阻滞药:拉贝洛尔、卡维地洛。
④、血管紧张素转换酶抑制剂:马来酸依那普利、苯那普利、赖诺普利、盐酸喹那普利、福辛普利钠、盐酸贝那普利。
⑤、血管紧张素受体拮抗药:缬沙坦、厄贝沙坦、坎地沙坦酯⑥、血管扩张药:尼可地尔。
⑦、利尿药:吲达帕胺、布美他尼、阿米洛利、托拉塞米。
⑧、中枢性降压药:盐酸莫索尼定。
4、钙通道阻滞剂:拉西地平、苯磺酸氨氯地平、左旋氨氯地平、尼索地平、贝尼地平。
我国自主研发一类新药分析报告

我国自主研发一类新药分析报告从“十一五”起,国家启动了“重大新药创制专项”鼓励新药自主研发。
在“十一五”累计投入超过66亿元的基础下,“十二五”新药创制专项投入进一步加大。
巨大的研发投入和全社会对新药创制的关注,使得中国新药创制进展迅速。
中药缺席一类新药盛宴这种情况与“中西并举”的思路相悖,不过,有3个中药一类新药完成了临床试验,目前正在申报生产批件阶段。
20个获批原创一类新药中无中药品种,这似乎不符合国家新药创制提出的“中西并举”的思路。
根据“重大新药创制”专项计划,有超过1/3的项目为中药项目,然而中药开发整体缓慢,尽管研发的一类中药新药数量不少,但2006年以来尚无一类中药品种获批,大多数品种依然长期停留在临床研究阶段。
这一方面说明中药一类新药的开发难度巨大,另一方面也说明中药的开发思路存在一定问题。
而值得关注的是,银杏内酯B注射液、人参皂苷Rd 注射液和注射用银杏叶3个中药一类新药均完成了临床试验,目前正在申报生产批件阶段,有望获批。
在中药注射剂安全性受质疑的大背景下,开发高纯度单一组分的中药注射剂有望重塑中药注射剂的形象,也具备很好的市场前景。
抗肿瘤药最受关注根据22大城市样本医院数据,抗肿瘤用药金额已超过抗感染用药,成为最大类别用药市场。
不过,该类药物临床满意度依然偏低,疗效有限,不良反应依然较多,且新上市品种定价普遍过高,因此市场对于自主研发的抗肿瘤新药非常期待。
2006年以来,国内获批的我国自主研发一类抗肿瘤新药共有5个,其中靶向用药共有4个,非靶向用药仅有索普兴大的双环铂注射液。
此外,主要针对化疗后粒细胞减少症的药物——石药的聚乙二醇化重组人粒细胞刺激因子注射液,于2011年获准上市,商品名为津优力。
2006年上市的重组人5型腺病毒注射液商品名为安柯瑞,由上海三维生物自主开发,具有全球知识产权。
安柯瑞利用肿瘤细胞内P53基因及其通路的异常,能特异性在肿瘤细胞内复制并将其杀死。
临床研究显示其安全性和靶向性都很好,但适应症较窄(头颈部肿瘤)和瘤内注射的给药方式阻碍了产品推广。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
★双环醇片(百赛诺 Bicyclol)
商品名“百赛诺”,是由中国医学科学院、中国协和医科大学药物所开发的产品,是中国第一个具有自主知识产权一类抗肝炎合成创新药物。1996年12月经卫生部批准进入临床试验,2001年9月获得原SDA颁发的新药证书及生产批准文,由北京协和药厂生产上市。目前已在世界16个国家地区获得20年发明专利保护,国内享有12年的行政保护期。本品是在降酶药物联苯双酯和五味子基础上,经过化学合成筛选的药物,其良好的双重机制,能清除自由基作用以保护细胞膜,并且能保护肝细胞核DNA免疫受损。临床显示对乙肝病毒有较好的抑制作用,安全性好,毒性小,无致突变性不良反应,适用于轻、中度慢性肝炎。临床显示远期疗效优于联苯双酯,有望成为抗慢性病毒性肝炎的首选药物之一。
★甘氨双唑钠
一类新药抗癌增敏剂甘氨双唑钠(CMNa)是我国自行设计、研制,具有自主知识产权的创新药物,2002年广州莱泰制药获得原SDA颁发的一类新药证书和生产批文,独家生产上市,商品名“希美纳”。
甘氨双唑钠是创新化学合成药物,是目前世界极少数上市的低毒高效化疗增敏剂之一。该药1983年由第二军医大学放射研究室研制开发,历经10多年开发过程。 1993年9月获国家专利局授予发明专利权;2000年初该专利又获得了国家知识产权局和世界知识产权组织颁发的发明金奖。临床研究表明,甘氨双唑钠在抗癌治疗中发挥出较好的治疗作用,具有一定的市场前景。
★纳科思(rmhTNF)
注射用重组改构人肿瘤坏死因子(rmhTNF)是上海赛达生物药业有限公司研制生产的注射用重组改构人肿瘤坏死因子,商品名“纳科思”,于2003年4月24日获得一类新药证书,为世界上首家获准上市的全身应用的肿瘤坏死因子变构体。该品对多种恶性肿瘤特别是呼吸系统恶性肿瘤有较好的疗效,其作用机理主要是:直接杀伤肿瘤细胞;破坏肿瘤组织血液供应;介导机体免疫调节作用;增强放/化疗敏感性。该品投放市场,目前销量有限,未来是否能获得较好的经济效益有待观察。
★ZT-1
上海药物所研究人员在开发天然抗老年痴呆药的基础上开发的新药,目前在欧洲已完成6项临床试验,结果喜人,目前国外合作方德标集团已开发出新的长效制剂,更适合患者方便使用。中国的临床试验进度缓慢,与中国现行药政管理体系有关
★青蒿素
研究成果是在发掘我国中医药宝库基础上研制新药的成功典范,它是军事医学科学院五所药学室等研究人员经历多年开发的国家重大科研攻关项目的合作成果。目前该药物除了有效治疗抗疟疾外,青蒿素类治疗抗血虫, 抗癌药物的应用前景也在国内外看好。但新的突破近期还是在复方制剂方面。
★博安霉素(Boanmycin)
★恩度(Endostar)
世界第一个重组人血管内皮抑制素抗肿瘤新药恩度(Endostar)2006年在中国首发上市!该药属于“生物制品第一类”,是由烟台麦得津生物工程股份有限公司(即将更名为山东先声麦得津生物制药有限公司)主持研发的国家一类抗肿瘤新药,拥有全部的知识产权,该药的成功研发也标志着中国在血管抑制类抗肿瘤药物的研发方面正走在世界前沿。
恩度是在美国科学家发现血管生长因子的基础上,通过适当修饰和特殊蛋白复性工艺研制而成的,它在单独使用时并无明显疗效,但与其他抗肿瘤药联合使用时,能增加化疗的效果。(Endostar)的成功上市是以留美学者罗永章博士(现任清华大学教授、长江学者,麦得津生物公司首席科学家)为首的产品研发团队、以孙燕院士牵头的临床多中心研究协作小组以及先声药业的专业营销团队三方紧密合作,共同孕育的智慧结晶。
★维甲酸治疗白血病 (APL)
★三氧化二砷治疗白血病 (APL, MDS, MM)
★恩经复(NOBEX)
成分是鼠神经生长因子(mNGF)、曾被列为国家计委高技术产业化示范工程项目、还曾是国家2002年火炬计划项目,它是是厦门北大之路生物工程有限公司和卫生部兰州生物制品研究所联合开发的国家一类新药(生物药品)。开发的适应症是环己烷中毒性神经损伤。用于治疗各类神经损伤。该项目目前行情如何,媒体少有报道。业内并不十分看好。
交流]中国一类新药汇总
★ ★ ★ ★
xiaohezi7844(金币+0,VIP+0):thanks
xiaohezi7844(金币+3,VIP+0):thanks
lwf991229(金币+1,VIP+0):3Q~感谢分享~
介绍国内部分研究开发的一类新药, 还有20多种正在临床试验的新药,( NCE 或中药), 希望各位添加补充其他新药信息.
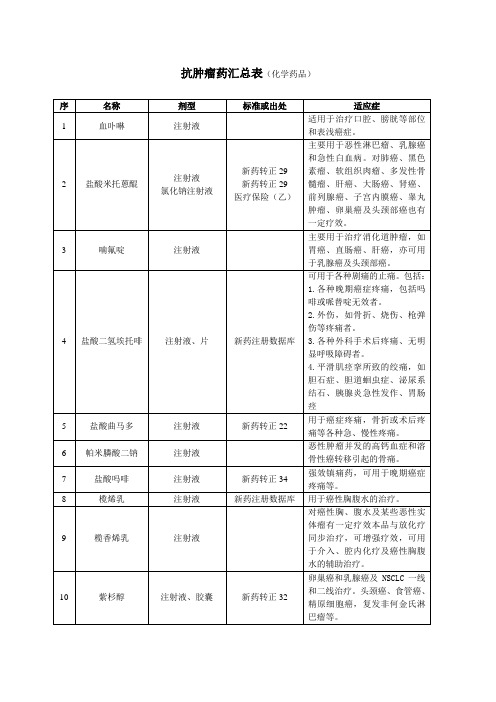
★血卟啉注射液
血卟啉是我国首创的一种光敏剂,属于一类新药,是治疗恶性肿瘤的新药,被誉为“光化导弹”。重庆华鼎现代生物制药于2003年获得原SDA颁发的生产批文,独家生产上市,商品名“喜泊分”。
该药物通过静脉滴注给药,随着血液循环到达恶性肿瘤组织,并聚集和潴留在里面。治疗时需要用特定波长的激光照射这些肿瘤部位,使药物发生光化反应,产生一种单价氧,直接杀死恶性肿瘤组织,全过程对正常人体组织并无多大损伤。无论对原发癌症或复发癌症,可达普”的主要成分为丁苯酞,是由中国医学科学院药物研究所和石家庄制药集团有限公司共同开发的,是我国心脑血管领域首个拥有自主知识产权的一类新药,获得两项国家专利。“恩必普”适用于缺血性脑卒中(俗称脑中风)的治疗,其主要成分丁苯酞,与从芹菜籽中提取的芹菜甲素结构相同。该产品的上市多年,目前市场占有率仍不高,在联想弘毅入主石药集团后能否有新的气色,既要看管理,更要看临床数据和医生反映。
第二阶段:Ⅱ期临床阶段。2000年10月7日,国家药品监督管理局批准重组人p53腺病毒注射液进入Ⅱ期临床试验;2000年12月,基因治疗制品生产厂房在深圳建成;2002年7月3日,获得国家知识产权局颁发的生产工艺发明专利;2002年11月22日,获得广东省药品监督管理部门颁发的药品生产许可证。
第三阶段:获得新药证书和正式上市阶段。2003年10月16日,重组人p53腺病毒注射液经国家食品药品监督管理局批准,获得新药证书。2004年1月20日,经批准获得准字号生产批文。
抗肿瘤抗生素一类新药——博安霉素为我国首创性开发的抗肿瘤抗生素一类新药。博安霉素原称争光霉素A6,是轮枝链霉菌平阳新变种(Streptomyces verticilus Var. Pingyangensis n.sp.)所产生,属于博莱霉素(B1eomycin)族,博安霉素(Boanmycin)除了具有与博莱霉素(B1eomycin)相同的抗瘤谱外,还对肝癌、胃癌、肺癌、结肠癌有很高的抑制能力,而且肺毒性显著低于其它同类产品。
★今又生(P53注射液)
全球第一个基因治疗产品(P53注射液),据了解,已有5000多人接受过治疗,但尚未在国际知名杂志发表临床试验论文(综述除外)它的研制过程:
第一阶段:Ⅰ期临床阶段。1998年3月9日,深圳市赛百诺基因技术有限公司成立;1998年12月28日,国家药品监督管理局批准重组人p53腺病毒注射液进入Ⅰ期临床试验。
★爱普列特
爱普列特是一种新型的5α-还原酶选择性抑制剂,1993年7月由中国药科大学、中科院上海有机化学研究所、扬州制药厂共同协作开发,1996年,爱普列特已批准进入临床研究阶段,1999年8月获得原SDA颁发的原料药及片剂新药证书与生产批件,2001年获得转正,现已成为联环药业主导产品,享受12年的独家生产保护期。该药可抑制睾酮的转化过程,使前列腺体内双氢睾酮含量下降,导致增生的前列腺体萎缩,从而达到改善良性前列腺增生病人排尿困难等症状,具有一定的安全可靠性。根据国家一类新药的要求,该药在开放性Ⅳ期临床研究中,取得较为满意的结果,该药已被列入了《国家基本医疗保险药品目录》,爱普列特产品上市后处于起步上升阶段,市场占有率还不高,是否能成为竞争性较强的治疗药品尚有待于市场考验。
★萘哌地尔片
萘哌地尔片是最先由贵州益康医药集团历时8年时间独立研制开发成功的、拥有我国自主知识产权的抗高血压化学合成一类新药(商品名:博帝),2001年5月上市。据称是我国第一个化学合成类的一类新药,从而结束了国产抗高血压化学合成药无一类新药的历史。萘哌地尔片在治疗高血压病方面有着自身独特的优势:该药是超高选择性α1-肾上腺素受体阻滞剂,兼有5-HT1A受体激动剂和Ca2+通道拮抗剂的作用;具有多重降压机理,在有效地控制血压的同时,能避免“首剂效应”体位性低血压及反射性心动过速等不良反应,对血脂、血糖代谢有良性作用,能改善前列腺肥大引起的排尿困难,或许是长期治疗高血压安全有效的新型药物。但因各种原因和同类产品的竞争,该药销售一直不理想。改变局面恐怕有难处。
点评: 据了解,恩度销售状况不错,该药的四期临床正在进行之中,患者的中位生存时间等关键数据尚待披露。国际学术刊物期待有份量和客观的临床论文发表,这是中国公司的短板,不善于利用国际舞台和学术论坛去宣传自己的成果,光用报刊媒体吵作,难免让人不服或有猜疑。但愿先声能率先打破中国公司的宣传方式,把产品做到国外去。
