米诺磷酸一水说明书日文
米诺膦酸

目录
1 2 3
项目基本情况 国内外研发状况
市场情况
临床研究
4
项目基本情况
1.通用名:米诺膦酸片
英文名:minodronic acid Tables 2.主要成份:米诺膦酸,其化学名为[1-羟基-2-(异吡唑[1,2-a] 嘧啶-3-基)亚乙基] 二膦酸一水合物。
欢迎贵司各位领导莅临我司参观指导!
药理作用及作用机制
药理作用
药理作用 (1)骨吸收抑制作用 在家兔破骨细胞培养体系中,本品可抑制I型胶原N末端肽从骨中的游离(体外)。 (2)在骨质疏松模型动物中的作用 1)在大鼠离体卵巢模型中,本品可抑制尿中脱氧吡啶诺林浓度的升高,抑制骨密度及骨强度 的下降。 2)在食蟹猴离体卵巢模型中,本品可抑制尿中I型胶原N末端肽和脱氧吡啶诺林浓度的升高。 另外,抑制骨密度和骨强度的下降,确认骨密度和骨强度呈正相关。 3)在大鼠类固醇诱导模型中,本品可抑制尿中脱氧吡啶诺林浓度的升高,抑制骨密度及骨强 度的下降。 4)在大鼠固定模型中,本品可抑制骨密度的降低。 (3)对骨钙化的影响 在正常大鼠中,在相当于可使骨量增加的剂量的100倍量下仍未发现本品可抑制骨钙化。 另外,在大鼠及食蟹猴离体卵巢模型中未见类骨质范围增大。 (4)对骨折治愈的影响 在大鼠腓骨骨折模型中,在相当于临床用量约1.5倍以上的剂量下本品可使的吸收延迟,但在 相当于临床用量约15倍的剂量下仍未发现骨强度降低。
3.药理类型:二碳磷酸盐化合物 。 4.作用机制:米诺膦酸通过抑制破骨细胞内的焦磷酸法 5.适应症:用于治疗骨质疏松症。 6.用法用量:口服,每日一次,每次1mg,服药后至少30分钟 内不可横卧,至少30分钟以内避免摄取水以外的食品饮料。 7.规格:1mg/片 8.原研厂家:由日本Astellas公司和小野公司共同开发,2009 年1月在日本上市。
米诺膦酸片说明书
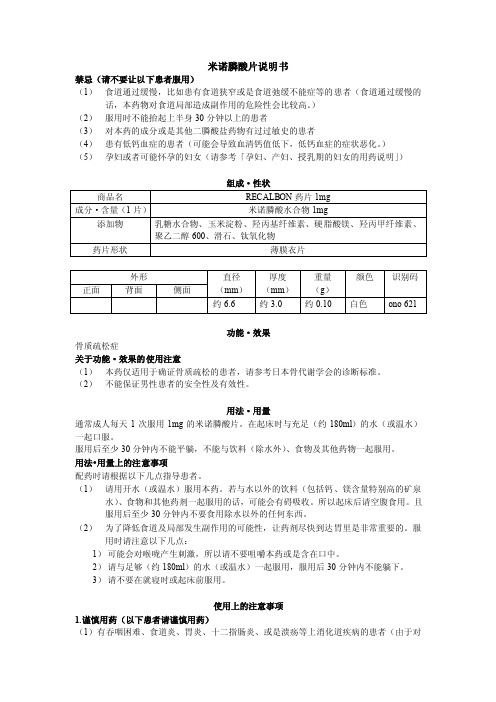
米诺膦酸片说明书禁忌(请不要让以下患者服用)(1)食道通过缓慢,比如患有食道狭窄或是食道弛缓不能症等的患者(食道通过缓慢的话,本药物对食道局部造成副作用的危险性会比较高。
)(2)服用时不能抬起上半身30分钟以上的患者(3)对本药的成分或是其他二膦酸盐药物有过过敏史的患者(4)患有低钙血症的患者(可能会导致血清钙值低下,低钙血症的症状恶化。
)(5)孕妇或者可能怀孕的妇女(请参考「孕妇、产妇、授乳期的妇女的用药说明」)组成·性状功能·效果骨质疏松症关于功能·效果的使用注意(1)本药仅适用于确证骨质疏松的患者,请参考日本骨代谢学会的诊断标准。
(2)不能保证男性患者的安全性及有效性。
用法·用量通常成人每天1次服用1mg的米诺膦酸片。
在起床时与充足(约180ml)的水(或温水)一起口服。
服用后至少30分钟内不能平躺,不能与饮料(除水外)、食物及其他药物一起服用。
用法•用量上的注意事项配药时请根据以下几点指导患者。
(1)请用开水(或温水)服用本药。
若与水以外的饮料(包括钙、镁含量特别高的矿泉水)、食物和其他药剂一起服用的话,可能会有碍吸收。
所以起床后请空腹食用。
且服用后至少30分钟内不要食用除水以外的任何东西。
(2)为了降低食道及局部发生副作用的可能性,让药剂尽快到达胃里是非常重要的。
服用时请注意以下几点:1)可能会对喉咙产生刺激,所以请不要咀嚼本药或是含在口中。
2)请与足够(约180ml)的水(或温水)一起服用,服用后30分钟内不能躺下。
3)请不要在就寝时或起床前服用。
使用上的注意事项1.谨慎用药(以下患者请谨慎用药)(1)有吞咽困难、食道炎、胃炎、十二指肠炎、或是溃疡等上消化道疾病的患者(由于对上消化道黏膜有成绩作用,可能会导致相关疾病恶化。
)(2)肾功能损害严重的患者(可能会延缓排泄。
)2.重要的基本注意事项(1)由于对上消化道有副作用,所以在出现这些症状的时候请停止服用本药并接受诊察。
米诺磷酸原研英文版说明书

- Osteoporosis treatment -
Note) Prescription drug: Caution – Use only pursuant to the prescription of a physician, etc
CONTRAINDICATIONS (RECALBON® is contraindicated in the following patients.) (1) Patients with disorder which delays esophageal transit such as esophageal stricture or achalasia (esophageal achalasia). [Delayed esophageal transit of RECALBON may increase the risk of adverse reactions developing in the esophagus region.] (2) Patients who cannot stand or sit upright at least 30 minutes when taking RECALBON. (3) Patients with a history of hypersensitivity to any of the components of RECALBON or other bisphosphonate drugs. (4) Patients with hypocalcemia. [Symptoms of hypocalcemia may be aggravated due to the decrease in serum calcium level.] (5) Pregnant women or women who may possibly be pregnant. (See “Use during Pregnancy, Delivery or Lactation”.)
米诺膦酸片

一.品种基本情况1。
品种基本情况(1)药品名称:通用名:米诺膦酸英文名: minodronic acid汉语拼音: Minuolinsuan结构式为:分子式: C 9 H 12 N 2 O 7 P 2分子量: 322。
16理化性质:本品为白色—微红白色的结晶或结晶性粉末。
本品极难溶于水,基本不溶于乙醇( 99。
5 ).本品可溶于氢氧化钠试验溶液。
( 2 ) 药品的药理作用及作用机制:药理作用:米诺膦酸是一种含氮的二碳磷酸盐化合物,可用于治疗骨质疏松症.作用机制:米诺膦酸通过抑制破骨细胞内的焦磷酸法尼酯合成酶,抑制破骨细胞的骨吸收功能,进而使骨代谢循环减退。
(3)临床适应症及用法用量:适应症:骨质疏松症。
用法用量:口服,每日一次,每次 1mg ,服药后至少 30 分钟内不可横卧,至少 30 分钟以内避免摄取水以外的食品饮料。
(4)注册分类及其依据:米诺膦酸由日本 Astellas 公司开发, 2009 年 1 月在日本上市. 该品种在我国没有授权专利和行政保护,也未在国内生产销售。
根据《药品注册管理办法》的有关规定,已在国外上市销售但尚未在国内上市销售的原料,属于化学药品注册3类.所以我公司申报的米诺膦酸片属化学药品注册第3。
1类。
2。
规格: 1mg2010年6月修订(第4版)2009年9月修订(指定医院用品规划区分的废除伴随的修订)骨质疏松症治疗药剂烈性药,处方药(注)米诺膦酸片 1mg保存方法:温室保存 recalbon使用有效期:3年米诺膦酸水合物第一页【禁忌(有如下症状的患者请勿使用本品)】(1)食道狭窄又称(食道迟缓不能症)等一些食道有延迟障碍的患者【本药剂的副作用对比食道通过的延迟障碍来说,在食道局部发现其危险性也比较高.】(2)服用的时候上身不能坐起,时间长达3 0分钟以上的患者(3)有对包含本药剂成分在内的其他双聚羧酸乙基次膦类药剂过敏的患者(4)有低钙血症的患者【血清钙的数值低下且有低钙血症的症状恶化的情况】(5)孕妇和可能有妊娠的妇女(【孕妇、产妇、哺乳期妇女等给药】的项目参阅)【组成·性状】通用名米诺膦酸片 1mg成分·含量米诺膦酸水合物·1mg添加物乳糖水合物、玉米淀粉、羟丙基纤维素、羟丙甲纤维素聚乙二醇6000 、二氧化钛、酸化钛外形直径、厚度、质量色调识别码表面、里面、侧面效能·效果骨质疏松症《与效能·效果有关的使用上的注意事项》(1)本药剂的适用对象是:以日本骨代学会的诊断基准等为参考、确诊为骨质疏松症的患者。
米诺膦酸片中文版说明书

**2006年6月修订(第4版)*2009年9月修订(因废止指定药物的区别规定而修订)骨质疏松治疗药剂烈性药、处方药米诺膦酸片《RECALBON○R 》米诺膦酸水合物片———————————————————————————————————————储藏:常温保存保质期:如外包装所示(3年)(2)对骨质疏松症动物模型的效果1)在摘除卵巢的老鼠模型实验中,有效抑制了尿中脱氧吡啶酚浓度的上升,和抑制骨密度和骨强度的降低。
13)2)在摘除卵巢的猿猴模型实验中,有效抑制了尿中骨胶质的上升。
同时,也抑制了骨密度和骨强度的降低,确定骨密度和骨强度有正面的相关关联。
14)3)在诱发老鼠类固醇模型实验中,有效抑制了尿中脱氧吡啶酚浓度的上升,和抑制骨密度和骨强度的降低。
15)4)在老鼠不动化模型实验中,有效抑制了骨密度降低。
16)(3)骨质石灰化以及影响对正常老鼠实验中,将用量增加到是骨量增加正常用量的100倍,未发现骨质石灰化障碍。
(4)治愈骨折以及影响在腓骨骨折的老鼠模型试验中,将用量增加到临床用量的约1.5倍以上出现假骨吸收延迟的现象,但用量达到临床用量的15倍时,未发现骨强度降低的现象。
〔有效成分的理化学知识〕通用名:米诺磷酸(M inodronic acid Hydrate)化学名:[1-Hydroxy-2-(imidaz[o 1,2-]pyridin-3-yl)ethylidene]bisphosphonic acid monohydrate结构式:分子式::C 9H 12N 2O 7P 2・H 2O 分子量:340.16性状:本品呈白色~微带红白色晶体或结晶性粉末。
本品极难溶与水、乙醇(99.5)。
可溶于氢氧化钠。
熔点:约250℃(分解)〔包装〕米诺磷酸片1mg:100片(PTP,散包装)140片(PTP )700片(PTP )〔主要文献〕1)上里一雄及其他:药理和临床,18(Suppl.1):S285,20082)前田彰及其他:药理和临床,18(Suppl.1):S239,20083)上里一雄及其他:药理和临床,18(Suppl.1):S275,20084)前田彰及其他:药理和临床,18(Suppl.1):S253,20085)碓井孝志及其他:药理和临床,18(Suppl.1):S215,20086)碓井孝志及其他:药理和临床,18(Suppl.1):S151,20087)小野药品工业:第Ⅲ期双盲骨密度测试(内部资料)8)小野药品工业:第Ⅲ期双盲骨折测试(内部资料)9)小野药品工业:第Ⅲ期双盲骨折持续用药测试(内部资料)10)野崎一敏及其他:药理和临床,18(Suppl.1):S7,200811)森裕史及其他:破骨细胞数减少的作用(内部资料)12)森裕史及其他:药理和临床,18(Suppl.1):S19,200813)Tanaka M.et al.:Bone,43:894,200814)Mori H.et al.:Bone,43:840,200815)森裕史及其他:药理和临床,18(Suppl.1):S75,200816)野崎一敏及其他:药理和临床,18(Suppl.1):S65,2008〔文献申请地址〕申请主要文献中记录的公司内部资料,请到以下地址申请.小野药品工业株式会社医药资料部〒541-8564大阪市中央区久太郎町1丁目8番2号电话:0120-626-190〔制造销售〕小野药品工业株式会社大阪市中央区久太郎町1丁目8番2号。
米诺膦酸片中文版说明书

⽶诺膦酸⽚中⽂版说明书**2006年6⽉修订(第4版)*2009年9⽉修订(因废⽌指定药物的区别规定⽽修订)⾻质疏松治疗药剂烈性药、处⽅药⽶诺膦酸⽚《RECALBON○R 》⽶诺膦酸⽔合物⽚———————————————————————————————————————储藏:常温保存保质期:如外包装所⽰(3年)(2)对⾻质疏松症动物模型的效果1)在摘除卵巢的⽼⿏模型实验中,有效抑制了尿中脱氧吡啶酚浓度的上升,和抑制⾻密度和⾻强度的降低。
13)2)在摘除卵巢的猿猴模型实验中,有效抑制了尿中⾻胶质的上升。
同时,也抑制了⾻密度和⾻强度的降低,确定⾻密度和⾻强度有正⾯的相关关联。
14)3)在诱发⽼⿏类固醇模型实验中,有效抑制了尿中脱氧吡啶酚浓度的上升,和抑制⾻密度和⾻强度的降低。
15)4)在⽼⿏不动化模型实验中,有效抑制了⾻密度降低。
16)(3)⾻质⽯灰化以及影响对正常⽼⿏实验中,将⽤量增加到是⾻量增加正常⽤量的100倍,未发现⾻质⽯灰化障碍。
(4)治愈⾻折以及影响在腓⾻⾻折的⽼⿏模型试验中,将⽤量增加到临床⽤量的约1.5倍以上出现假⾻吸收延迟的现象,但⽤量达到临床⽤量的15倍时,未发现⾻强度降低的现象。
〔有效成分的理化学知识〕通⽤名:⽶诺磷酸(M inodronic acid Hydrate)化学名:[1-Hydroxy-2-(imidaz[o 1,2-]pyridin-3-yl)ethylidene]bisphosphonic acid monohydrate结构式:分⼦式::C 9H 12N 2O 7P 2?H 2O 分⼦量:340.16性状:本品呈⽩⾊~微带红⽩⾊晶体或结晶性粉末。
本品极难溶与⽔、⼄醇(99.5)。
可溶于氢氧化钠。
熔点:约250℃(分解)〔包装〕⽶诺磷酸⽚1mg:100⽚(PTP,散包装)140⽚(PTP )700⽚(PTP )〔主要⽂献〕1)上⾥⼀雄及其他:药理和临床,18(Suppl.1):S285,20082)前⽥彰及其他:药理和临床,18(Suppl.1):S239,20083)上⾥⼀雄及其他:药理和临床,18(Suppl.1):S275,20084)前⽥彰及其他:药理和临床,18(Suppl.1):S253,20085)碓井孝志及其他:药理和临床,18(Suppl.1):S215,20086)碓井孝志及其他:药理和临床,18(Suppl.1):S151,20087)⼩野药品⼯业:第Ⅲ期双盲⾻密度测试(内部资料)8)⼩野药品⼯业:第Ⅲ期双盲⾻折测试(内部资料)9)⼩野药品⼯业:第Ⅲ期双盲⾻折持续⽤药测试(内部资料)10)野崎⼀敏及其他:药理和临床,18(Suppl.1):S7,200811)森裕史及其他:破⾻细胞数减少的作⽤(内部资料)12)森裕史及其他:药理和临床,18(Suppl.1):S19,200813)Tanaka M.et al.:Bone,43:894,200814)Mori H.et al.:Bone,43:840,200815)森裕史及其他:药理和临床,18(Suppl.1):S75,200816)野崎⼀敏及其他:药理和临床,18(Suppl.1):S65,2008〔⽂献申请地址〕申请主要⽂献中记录的公司内部资料,请到以下地址申请.⼩野药品⼯业株式会社医药资料部〒541-8564⼤阪市中央区久太郎町1丁⽬8番2号电话:0120-626-190〔制造销售〕⼩野药品⼯业株式会社⼤阪市中央区久太郎町1丁⽬8番2号。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1. 妊婦等: (1)
妊婦又は妊娠している可能性のある婦人には投与しないこと。[他のビ スホスホネート系薬剤と同様、生殖試験(ラット)において、低カルシ ウム血症による分娩障害の結果と考えられる母動物の死亡並びに出生 率の低下等がみられている。] (2) ビスホスホネート系薬剤は骨基質に取り込まれた後に全身循環へ徐々 に放出されるので、妊娠する可能性のある婦人へは、治療上の有益性が 危険性を上回ると判断される場合にのみ投与すること。[全身循環への 放出量はビスホスホネート系薬剤の投与量・期間に相関する。ビスホス ホネート系薬剤の中止から妊娠までの期間と危険性との関連は明らか ではない。] 2. 授乳婦: 授乳中の婦人には、本剤投与中は授乳を中止させること。[母動物(ラ ット)へ投与した場合、乳汁中に移行することが示されている。]
重大な副作用
上部消化管障害 十二指腸潰瘍(0.3%)、胃潰瘍(0.1%)等の上部消化管障害があらわ れることがあるので、観察を十分に行い、異常が認められた場合には投 与を中止するなど、適切な処置を行うこと。
重大な副作用(類薬)
1. 低カルシウム血症 他のビスホスホネート系薬剤において痙攣、テタニー、しびれ、失見当 識、QT 延長等を伴う低カルシウム血症があらわれるとの報告があるの で、観察を十分に行い、異常が認められた場合には投与を中止し、適切 な処置を行うこと。
4. **ビスホスホネート系薬剤による治療を受けている患者において、投与 経路によらず顎骨壊死・顎骨骨髄炎があらわれることがある。報告され た症例の多くが抜歯等の歯科処置や局所感染に関連して発現している。 リスク因子としては、悪性腫瘍、化学療法、コルチコステロイド治療、 放射線療法、口腔の不衛生、歯科処置の既往等が知られている。 本剤の投与にあたっては、患者に対し適切な歯科検査を受け、必要に応 じて抜歯等の顎骨に対する侵襲的な歯科処置を投与前に済ませるよう 指示するとともに、本剤投与中は、歯科において口腔内管理を定期的に 受けるとともに、抜歯等の顎骨に対する侵襲的な歯科処置はできる限り 避けるよう指示すること。また、口腔内を清潔に保つことや歯科受診時 に本剤の使用を歯科医師に告知するなど、患者に十分な説明を行い、異 常が認められた場合には、直ちに歯科・口腔外科に受診するよう注意す ること。
3999026F1026 承認・許可番号 承認番号
22100AMX00391 商標名
Bonoteo Tablets 1mg 薬価基準収載年月
2009 年 3 月
販売開始年月
2009 年 4 月
貯法・使用期限等
貯法 室温保存
使用期限 ケース等に表示(製造後 3 年)
規制区分
劇薬 処方せん医薬品
注意-医師等の処方せんにより使用すること
5. **ビスホスホネート系薬剤を長期使用している患者において、非外傷性 の大腿骨転子下及び近位大腿骨骨幹部のストレス骨折が発現したとの 報告があるので、X 線検査等を実施し、十分に観察しながら慎重に投与 すること。この骨折では、X 線検査時に骨皮質の肥厚等、特徴的な画像 所見がみられ、完全骨折が起こる数週間から数ヶ月前に、罹患部位の前 駆痛があるため、そのような場合には適切な処置を行うこと。また、両 側性の骨折が生じる可能性があることから、片側で骨折が起きた場合 は、他方の大腿骨の画像検査も行うこと。
用法及び用量に関連する使用上の注意
投与にあたっては次の点を患者に指導すること。 1. 本剤は水(又はぬるま湯)で服用すること。水以外の飲料(Ca、Mg 等 の含量の特に高いミネラルウォーターを含む)、食物及び他の薬剤と一 緒に服用すると、吸収を妨げることがあるので、起床後、最初の飲食前 に服用し、かつ服用後少なくとも 30 分は水以外の飲食を避ける。 2. 食道及び局所への副作用の可能性を低下させるため、速やかに胃内へと 到達させることが重要である。服用に際しては、以下の事項に注意する こと。 (1) 口腔咽頭刺激の可能性があるので、本剤を噛んだり又は口中で溶かした りしないこと。 (2) 十分量(約 180mL)の水(又はぬるま湯)とともに服用し、服用後 30 分は横たわらないこと。 (3) 就寝時又は起床前に服用しないこと。
小児等への投与
低出生体重児、新生児、乳児、幼児又は小児に対する安全性は確立して いない。(使用経験がない。)
過量投与
症状: 低カルシウム血症、上部消化管障害(胃不調、胸やけ、食道炎、胃炎、 又は胃潰瘍等)が発現する可能性がある。
処置: 吸収を抑えるために、多価陽イオンを含有する制酸剤あるいは牛乳を投 与する。また、未吸収薬剤を除去するために胃洗浄を考慮する。なお、 低カルシウム血症には必要に応じて、カルシウムの静脈内投与等の処置 を行う。
その他の副作用
次の副作用があらわれることがあるので、異常が認められた場合には投 与を中止するなどの適切な処置を行うこと。 過敏症 1%未満 発疹、そう痒、アレルギー性皮膚炎 消化器 1~5%未満 胃・腹部不快感、腹痛、胃炎 消化器 1%未満 逆流性食道炎、悪心、嘔吐、下痢、便秘、腹部膨満、消化不良、食欲不 振、口内炎、口唇炎 血液 1%未満 白血球減少、赤血球減少、血小板減少、単球増加 肝臓 1%未満 AST(GOT)上昇、ALT(GPT)上昇、γ-GTP 上昇、ビリルビン上昇、ア ルカリホスファターゼ上昇、LDH 上昇 腎臓 1%未満 BUN 上昇、尿酸上昇、クレアチニン上昇 筋・骨格系 1~5%未満 血中カルシウム減少 筋・骨格系 1%未満 アルカリホスファターゼ減少、CK(CPK)上昇 精神神経系 1%未満 しびれ、坐骨神経痛、めまい その他 1%未満 胸痛、コレステロール増加、脱毛、膀胱炎、副鼻腔炎、倦怠感、血圧上 昇、血中リン上昇、血中リン減少 **その他 頻度不明 顔面浮腫
1. 上部消化管に関する副作用が報告されているので、これらの症状があら われた場合は、本剤の服用を中止して診察を受けるよう指導すること。
2. 骨粗鬆症の発症にエストロゲン欠乏、加齢以外の要因が関与しているこ ともあるので、治療に際してはこのような要因を考慮する必要がある。
3. 患者の食事によるカルシウム、ビタミン D の摂取が不十分な場合は、カ ルシウム又はビタミン D を補給すること。ただし、カルシウム補給剤及 びカルシウム、アルミニウム、マグネシウム含有製剤は、本剤の吸収を 妨げることがあるので、服用時刻を変えて服用させること。(「相互作 用」の項参照)
2. 肝機能障害、黄疸 他のビスホスホネート系薬剤において重篤な肝機能障害、黄疸があらわ れるとの報告があるので、観察を十分に行い、異常が認められた場合に は投与を中止し、適切な処置を行うこと。
3. 顎骨壊死・顎骨骨髄炎 他のビスホスホネート系薬剤において顎骨壊死・顎骨骨髄炎があらわ れることが報告されているので、観察を十分に行い、異常が認められた 場合には投与を中止するなど、適切な処置を行うこと。
適用上の注意
薬剤交付時: PTP 包装の薬剤は PTP シートから取り出して服用するよう指導するこ と。[PTP シートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更に は穿孔を起こして縦隔洞炎等の重篤な合併症を併発することが報告さ れている。]
薬物動態
1. 血中濃度 (1) 単回投与
健康高齢男女各 10 例(65~79 歳)及び非高齢男女各 10 例(20~31 歳) にミノドロン酸水和物 1mg を空腹時に単回経口投与したとき、高齢・非 高齢者とも性差は認められなかった。また、高齢者の Cmax、AUC 及び投 与後 24 時間までの尿中未変化体排泄率は非高齢者に比べて 2.1 倍、2.4 倍及び 2.0 倍高く、加齢により本剤の吸収率は上昇することが示唆され た 1)。(「薬物動態の表」表 1 参照) (2) 反復投与 健康成人男子 6 例にミノドロン酸水和物 2mg を 1 日 1 回 7 日間反復投与 したときの血漿中未変化体濃度は遅くとも投与 7 日目に定常状態に到 達していると推察された。反復投与 7 日目の Cmax 及び AUC は投与初日 と比較してそれぞれ 1.1 倍及び 1.3 倍であった 2)。 (注)本剤の承認された用量は「1mg を 1 日 1 回、経口投与する。」で ある。 (3) 食事の影響 健康成人男子 29 例にミノドロン酸水和物 1mg を空腹時に単回経口投与 したとき、血漿中濃度は投与後 1.2 時間で最高に達し、その濃度は 0.39ng/mL で、消失半減期は 9.7 時間であった。また、食前 30 分投与 では空腹時投与に比し Cmax は約 0.5 倍、AUC は約 0.3 倍に低下した 3)。 (「薬物動態の表」表 2 参照)
使用上の注意
慎重投与
(次の患者には慎重に投与すること) 1.
嚥下困難、食道炎、胃炎、十二指腸炎、又は潰瘍等の上部消化管障害が ある患者[上Байду номын сангаас消化管粘膜に対し、刺激作用を示すことがあるので基礎 疾患を悪化させるおそれがある。] 2.
重篤な腎障害のある患者[排泄が遅延するおそれがある。]
重要な基本的注意
副作用
副作用等発現状況の概要
承認時までの調査における 1,108 例中 206 例(18.6%)に副作用(臨床 検査値の異常を含む)が認められた。主なものは胃・腹部不快感 35 例 (3.2%)、腹痛 27 例(2.4%)、血中カルシウム減少 22 例(2.0%) 及び胃炎 15 例(1.4%)等であった。(承認時:2009 年 1 月)
相互作用
併用注意
(併用に注意すること)
薬剤名等水以外の飲料、食物 特に牛乳や乳製品のような高カルシウム含有飲食物 多価陽イオン(カルシウム、鉄、マグネシウム、アルミニウム等)含有製剤 ミネラル入りビタミン剤、制酸剤等 臨床症状・措置方法
