16-重氮化合物
有机化学课后习题答案16十六章重氮化合物和偶氮化合物

NH2 N N
4.
NO2
Br2/H2O Br
NO2
Fe/HCl Br
NH2
N2+ClNaNO2/HCl Br NH2
CH3 CH3 HNO3/H2SO4 Fe/HCl
CH3 CH3COCl NH2 CH3
CH3
NO2 CH3
NHCOCH3 CH3
5.
HNO3/H2SO4 NO2 NHCOCH3 CH3 CuBr Br NHCOCH3
Fe/HCl NH2 NHCOCH3 CH3 H3O+ Br NH2
NaNO2/HCl
N2+ClNHCOCH3 CH3
NaNO2/HCl
H3PO2 Br
196
CH3 CH3 HNO 3/H2SO4 Fe/HCl
CH3 CH3COCl NH2 CH3
CH3 HNO3/H2 SO4 NHCOCH3 COOH KMnO4 / H+ NO2 OH OH NO2
N2
+Cl-
10.
二.完成下列反应式。 1.
OH
2.
Br
3.
I
4.
CH3 O
5.
C 2H5
6.
ON
CH3
N
CH3
CH3
CH3
)
CH3
7.
( NH2
) (
)
(
( NH2
) ( NO2
) NO2 N2+Cl、
CH3
、
N2+Cl-
NHCOCH3、
NO2 NHCOCH3、
、
NO2
8.
192
CH3
9.
NH2
第16章 重氮化合物和偶氮(2012)(1)

历程:
O AgO RC CHN2 - N2
O R C .. CH H2O RCH2COOH RCH2COOR' RCH2CONH2
R CH C O + R'OH NH3 (烯酮)
(3)与醛酮的反应
O R R
O + -CH2 N+ N
O R' + CH2N2 R R
-
C
C O C
CH2R' CH3
3) 被-CN和-NO2取代
N2+ClCuCN/KCN CN + N2
Gattermann reaction 由于-CN可以水解成羧基, 故此也为把羧基引入苯环的方法。
HBF4/NaNO2 NaNO2 Cu
O2N
NH2
O2N
N2+Cl-
O2N
NO2
4) 被-H原子取代 (重氮盐的还原):
CH3CH2OH
+N
N Cl-
芳香族重氮盐稳定性大于脂肪族重氮盐
苯环中的p-轨道与 两个氮原子上的p轨道平行,有π-π 共轭。
脂肪族重氮盐非常不稳定一旦生成,立刻分解! 芳香族重氮盐也很活泼,但在0~5℃可稳定存在。所以,芳 香族重氮盐在有机合成上可用来制备一系列芳香族化合物和 有颜色的化合物。
重氮盐的性质与铵盐类似,溶于水、能电离等;与碱作用可 生成重氮碱:
-O S 3
N N H
N+(CH3)2
黄
甲基橙
红
研究表明,偶氮化合物的颜色与分子中所含的偶氮基-N=N-以 及分子的结构有关。
1)颜色与化合物结构的关系
自然可见光:400-800 nm;波长越短,能量越高,颜色越浅。 反之亦然。 互补光:若两种不同波长的光混在一起能变成白光,则称其 为互补光。如红与青绿色光等。 物质的颜色:就是吸收了某一互补光的结果。如吸收红色则 显青绿色;反之则显红色。
第16章 重氮化合物和偶氮化合物

重氮部分 -H+
偶联部分
N=N + -Y H -Y
N=N
Y 表示强供电子基:-OH 、-NH2、-NHR、-NR2等 亲电取代反应,发生在羟基或氨基的邻、对位(空间效 应影响,一般发生在对位;对位被占时发生在邻位)。
a)与苯酚偶联 + N2Cl OH
NaOH(pH~ 8)
+ 条件:
0~5 ℃
N=N
第十六章 重氮化合物和偶氮化合物
16.1 16.2 16.3 16.4 重氮化反应 重氮盐的性质及其在合成上的应用 偶氮化合物和偶氮染料 重氮甲烷和碳烯
本章作业
习题 4. 习题 6. (2), (3), (4), (5) 习题 8.
重氮和偶氮化合物都含有-N=N-结构 -N=N(-N2-) 偶氮化合物 —— 两端都与碳相连
C:重氮甲烷受光或热作用,生成碳烯(卡宾)
二、 碳烯——卡宾
一个二价碳的反应中间体,活性高、寿命短。 (一)碳烯的生成
(二)碳烯的结构——未成键电子的状态
(三)碳烯的化学性质 (1)加成反应—碳烯(缺电子)与烯烃发生亲电加成:
• 单线态碳烯 (重氮甲烷在液态用光分解产生)和碳碳双键的加成 是一步反应,形成过渡态后,即得三元产物:
OH
NH2
CH3 -OH CH3 -OH 不反应
16.3 偶氮化合物和偶氮染料
芳香族重氮盐的偶联反应,可以合成偶氮染料。 古代所用染料主要从植物中提取(靛蓝、茜素等)。由 于有机化学的发展,合成了品种多,成本低的合成染料,偶 氮染料就是其中的一种。 芳香族偶氮化合物都有颜色,显色原因与分子的-N=N-基有关。 .. -N=N- 偶氮基 -OH .. 亚硝基 -N=O -NH2 .. = = 醌 -OCH3 助色团 发色团 .. O O -X .. -C—C- 1,2-二酮基 -SO3H -CH=N 亚胺基 = =
第十六章 重氮化合物和偶氮化合物
CH3COONa 0-5 C
。
NaO3S
N=N
N(CH3)2
甲基橙 (酸红碱黄,变色范围pH3.1-4.4)
能产生颜色的有机物一般都含有生色基和助色基。 能产生颜色的有机物一般都含有生色基和助色基。
27
生色基一般含有共轭体系, 生色基一般含有共轭体系,如:
11
例如:
从 OH
Br 溴会在碱熔时水解
NO2
NO2
Br2/Fe Fe+HCl
NH2 Br OH Br
解:
混酸
50 C
。
N2+ HSO4HNO2+过量H2SO4 0-5 C
。
H2O
Br
Br
12
例如: 由苯制取间硝基苯酚。 例如 由苯制取间硝基苯酚。
部分还原
13
、-Cl、- 、-I) ⑶重氮基被卤素取代 (X=-F、- 、- 、- - 、- 、-Br、-
近来报导用重氮氟磷酸盐代替重氮氟硼酸盐,产率高 近来报导用重氮氟磷酸盐代替重氮氟硼酸盐,产率高: 重氮氟磷酸盐代替重氮氟硼酸盐
16
例: 解: CH3
CH3 由
CH3 F
CH3
混酸
CH3 + NO2
CH3
Fe+HCl (CH3CO)2O
CH3 NHCOCH3
HNO2+过量H 2SO4 0-5 C
NO2
偶氮染料———苏丹红 苏丹红 偶氮染料
30
苏丹红,学名苏丹,分为Ⅰ 苏丹红,学名苏丹,分为Ⅰ、Ⅱ、Ⅲ、Ⅳ号,是一类合 成型偶氮染料, 主要用于溶剂、 成型偶氮染料 主要用于溶剂、油、蜡、汽油增色以及鞋和 地板等的增光。 地板等的增光。 在苏丹红事件中,包括30家企业的 家企业的88个食品样品先后被 在苏丹红事件中,包括 家企业的 个食品样品先后被 检出含有苏丹红Ⅰ 检出含有苏丹红Ⅰ号。中国检验检疫科学院食品安全研究所 副所长储晓刚表示,送检的几份(鸭蛋)样品里苏丹红Ⅳ 副所长储晓刚表示,送检的几份(鸭蛋)样品里苏丹红Ⅳ号 含量最高达到0.137mg/kg。国际癌症研究机构将苏丹 mg/kg。国际癌症研究机构将苏丹 含量最高达到 mg/kg。 号列为三类致癌物。 红Ⅳ号列为三类致癌物。
重氮化和偶合反应

重氮化重氮化和偶合反应是重要的有机合成反应,在精细化工中有很重要的地位,该类反应在染料合成中应用很广,是两个主要的工序。
可合成酸性、冰染、直接、分散、活性、阳离子等类型的染料,还可合成各类黄色、红色偶氮型有机颜料。
一.重氮化和重氮化合物1.重氮化反应及影响因素芳香族伯胺和亚硝酸作用生成重氮盐的反应称为重氮化。
重氮化反应要在强酸中进行,实际上是亚硝酸作用于铵离子。
由于亚硝酸不稳定,通常使用亚硝酸钠和盐酸或硫酸,使反应生成的亚硝酸立刻与芳伯胺反应,避免亚硝酸的分解。
为了使反应能顺利进行,必须首先把芳伯胺转化为铵正离子。
芳胺的碱性较弱,因此重氮化要在较强的酸中进行。
有些芳胺碱性非常弱,要用特殊的方法才能进行重氮化。
重氮化是放热反应,重氮盐对热不稳定,因此要在冷却的情况下进行,一般都用冰盐浴冷却,并调节亚硝酸钠的加入速度,维持反应温度在0℃附近,由于重氮盐不稳定,一般就用它们的溶液,随做随用。
固体重氮盐遇热或震动、摩擦,都将发生爆炸,必需应用某些稳定性好的固体重氮盐时,也需谨慎小心。
自重氮化反应发现以来,人们为了弄清楚其反应的影响因素,对重氮化反应的机理进行了反复研究,已普遍接受了重氮化反应的亚硝化学说即重氮化反应是由亚硝酸产生的亲电质点对游离芳伯胺基进行亲电取代反应的机理,其反应的主要影响因素如下。
(1).酸的影响酸的影响主要考虑酸的种类、用量及浓度的影响。
重氮化所用的酸,从反应速度来说,以盐酸或氢溴酸等最快,硫酸与硝酸较次。
由反应式可以看出酸的理论用量为2摩尔,在反应中无机酸的作用是:首先是使芳胺溶解,其次可和亚硝酸钠生成亚硝酸,最后是生成稳定的重氮盐。
重氮盐一般来讲是容易分解的,只有在过量的酸液中才稳定,所以重氮化时实际上酸用量过量很多,常达3~4摩尔。
反应完毕时介质应呈强酸性,PH值为3,对刚果红试剂呈蓝色,重氮化过程经常检查介质的PH值是十分重要的。
反应时若酸量不足,生成的重氮盐容易和未反应的芳胺偶合,生成重氮胺基化合物。
新的命名原则中含氮化合物的命名解读

大 学 化 学Univ. Chem. 2022, 37 (3), 2106027 (1 of 7)收稿:2021-06-10;录用:2021-08-05;网络发表:2021-09-15*通讯作者,基金资助:河北省高等教育教学改革研究与实践项目(2020GJJG557)•师生笔谈• doi: 10.3866/PKU.DXHX202106027 新的命名原则中含氮化合物的命名解读田霞,韩建荣*,甄小丽,苏伟河北科技大学理学院,石家庄 050018摘要:有机化合物的命名是有机化学教学中的重要环节,而含氮化合物在其中占有很重的比例。
本文对新的命名原则《有机化合物命名原则2017》中的含氮化合物的命名方法进行解读,以便于师生在有机化学的教授和学习中掌握新版的有机化合物命名规则,尽快实现旧命名原则向新命名原则的过渡和转化。
关键词:含氮化合物;有机化合物命名原则;特性基团中图分类号:G64;O6Interpretation of Nitrogenous Compounds Nomenclature under the New Nomenclature RulesXia Tian, Jianrong Han *, Xiaoli Zhen, Wei SuCollege of Science, Hebei University of Science & Technology, Shijiazhuang 050018, China.Abstract: The nomenclature of organic compounds is an important component in the teaching of organic chemistry, in which nitrogenous compounds occupy a considerable proportion. In this paper, the nomenclature of nitrogenous compounds based on “Nomenclature of Organic Compounds-2017” is explained to assist teachers and students master the new version of organic compounds nomenclature in the teaching and learning of organic chemistry, and realize the rapid transition of the nomenclature rules.Key Words: Nitrogenous compounds; Nomenclature of organic compounds; Characteristic group有机化合物种类繁多,数目庞大,且随着人类对自然的探索还在不断地涌现出大量新的有机化合物。
第十一章,第十二章,第十三章,第十四章有机化学名词解释

名词解释第十一章1.振动光谱——分子振动能级间的能量差比同一振动能级中转动能级之间能量差大100倍左右,他们大多在近红外区域内,因此称为红外光谱。
2.转动光谱——分子转动能级之间的能量差很小,转动光谱位于电磁波谱中的远红外及微波区域内。
3.红外吸收峰的位置——分子振动的频率决定分子所吸收的红外光频率。
4.红外吸收光谱——分子吸收红外光引起的振动和转动能级跃迁产生的信号。
5.红外光谱产生的条件——当一定频率的红外光照射物质时,如果分子中某一基团的振动频率正好与其相同,物质就能吸收这一频率的红外光从低能级跃迁到较高的能级,产生红外吸收光谱。
6.叁键和累积双键区——2500~2000 cm-1各种叁键基团和累积双键的伸缩振动区域7.氢键区——4000~2500cm-1含氢基团的伸缩振动区。
8.双键区——2000~1500 cm-1各种双键基团包括共轭双键以及苯基伸缩振动区域。
9.特征吸收峰——用于鉴定官能团存在的吸收峰。
10.特征谱带区——氢键,双键,叁键区的特征性强,所以4000~1500 cm-1的区域称为官能团特征频率区。
11.核磁共振谱——记录原子核对射频区电磁波的吸收,简称NMR。
12.质子磁共振谱——氢原子核共振谱,简称PMR。
13.化学位移——由于化学环境所引起的核磁共振信号位置的变化。
14.自旋偶合——相邻碳上氢核的相互影响。
15.硝基化合物的还原——硝基苯在强酸介质中,用金属还原时,总是得到苯胺,用催化加氢也可得到同样的结果。
16.胺的碱性——胺与氨相似,氮原子上的未共用电子对能与质子结合,形成带正电的铵离子。
17.胺——可看作氨的衍生物,即氨分子中的氢原子被烃基取代的产物。
18.胺的烃基化——与卤代烃(通常为伯卤代烃和具有活泼卤原子的芳卤化物),醇等烃基化试剂作用,胺基上的氢原子被烃基取代。
19.胺的酰基化——伯胺和仲胺作为亲核试剂可与酰卤,酸酐等酰基化试剂反应,生成N-取代酰胺和N,N-二取代酰胺。
柴油十六烷值改进剂的最新研究进展

柴油十六烷值改进剂的最新研究进展宗丽娜【摘要】The achievements of cetane number improvers of diesel fuel was introduced.The working mechanism of improvers in improving the cetane number of diesel fuel was stated, the traditional and the new type of cetane number improvers were contrasted, the future trends of cetane number improvers were pointed out.The classification and the development of cetane number improver for diesel fuel were nitric acid esters, the effects of such substances were good, but extremely increased the risk because of the instability of the synthesis, storage and transport.A good effect could be achieved if the other substances were added into nitric acid esters at a proper proportion.Environmental-friendly cetane number improvers have broader application prospects.%综合论述了柴油十六烷值改进剂的研究进展,阐述了十六烷值改进剂的作用机理,并对传统十六烷值改进剂和新型十六烷值改进剂两个方面进行分析比较,从而合理预测十六烷值改进剂发展方向。
含氮有机化合物和杂环汇总

CH3NHCH2CH3 甲乙胺 (仲胺) 甲基-乙基-环丙基 H 3C N CH2CH3 胺(叔胺)
6
NHCH 3
N-甲基苯胺
邻-甲基苯胺 N-甲基-N-乙基 苯胺
7
NH 2 CH3
N CH3 CH2CH3
CH2NH 2
+ NH 3 Cl
苯甲胺(苄胺) 氯化苯铵 溴化四甲铵
-
(CH3)4N Br
31
第二节 重氮化合物 和偶氮化合物
重氮化合物 R-N=N(Ar)
偶氮化合物
R-N=N-R’ (Ar)
32
重氮化合物的化学性质 1.重氮基取代反应(放氮反应)
33
OH
+
N2
H
+
3 PO 2+ H 2O
O H2
/ △
N2
N2
N) 2 C ( u 2 C N KC
+
Cu
2X 2
+H
X
CN N2
X
+
27
(3) 叔胺和亚硝酸反应
N(CH3)2
N(CH3)2
+ HNO2
N O
28
鉴别:
伯胺 脂 肪 族 仲胺
HNO2
N2 黄色油 状物
叔胺
溶解
29
五.与医学有关的胺类
苯胺
NH 2 + 3Br2(水)
Br Br NH 2 Br + HBr
白
30
ห้องสมุดไป่ตู้
拓展
“新洁尔灭”
溴化二甲基十二烷基苄基铵,又称苯扎溴 铵(C6H5CH2N+(CH3)2C12H25Br-),商品名为 “新洁尔灭”。它为季铵盐型阳离子表面活性 广谱杀菌剂,杀菌力和去垢效力强,对皮肤和 组织无刺激性,对金属、橡胶制品无腐蚀作用, 不污染衣服,性质稳定,易于保存,属消毒防 腐类药物。1:1000~2000的新洁尔灭溶液广泛 用于手、皮肤、粘膜、器械等的消毒。
有机化学II-16重氮化合物和偶氮化合物
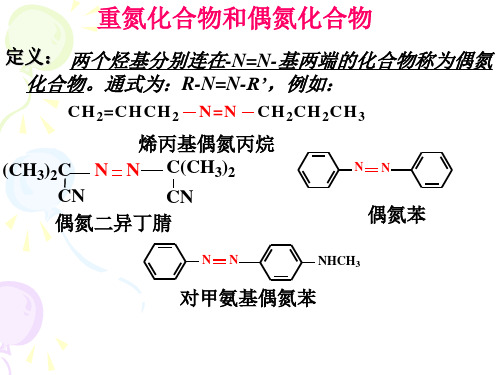
N
(I)
-OH、-NH2(NHR、NR2)都是很强的第一类定位基,
N
N
(II)
N+
在偶合反应中,极限结构(Ⅱ)作为亲电试剂,进攻芳环而 发生亲电取代反应:
N N
+
+
G -H+
N N H N N
G
G = OH, NH2,NHR,NR2
G
由于重氮正离子中氮原子上的正电荷可以离域到苯环 上,因此它是一个很弱的亲电试剂,只能与高度活化的苯 环才能发生偶合反应。 可以预料:
N N N
+
N
按共振论的观点,重氮正离子是下列极限共振结构的 共振杂化体:
N N N N
当苯环上连有强吸电子时,重氮正离子的稳定性将↑。
重氮化反应机理如下:
-H2O
HO
N O
H2O N O
N O
[N
O
O
N O]
亚硝酰正离子
Ar NH2
+
Ar
NH2 N
-H+
Ar
NH N O
互变异构
-H2O
H+
Ar
Ar N
OH
H+
OH2
+
NR2
H+
NR2 H
+
而在强碱介质中,重氮盐正离子与碱作用,可生成重 氮酸或其盐。
:
Ar N
+
N:
Ar N
N:
+
NaOH
Ar N
N OH
NaOH
Ar N
N O Na
+
重氮盐
重氮酸
有机化学各大名校考研真题十六、十七、十八章

名校考研真题(16--1)推测下列反应的机理。
CH 3OHCH 2NH 2解:此反应通过伯胺与硝酸钠/盐酸得到重氮化化合物,其水解后得到羟基,氧原子上的共用电子对与碳正离子结合,脱去质子后成双键,反应机理为:OHCH 2NH 2CH 3CHCHCH 3O(16--2)合成 (1)NH2解:(1)由反应产物来看,要利用氨基的定位效应通过硝化,溴代反应在苯环上连上硝基和溴原子,然后通过重氮盐将氨基脱除,合成过程为:NH2CH COCL NHCOCH32Br 22N 2CLBrNO 22(2)NHCOCH 3OHBr(2)由乙酰苯胺合成对溴硝基苯,可以先通过与溴水进行取代反应,然后再水解得到对溴苯胺,再经过重氮化水解得到产物。
NHCOCH3NHCOCH3BrNH 2BrN 2HSO 4BrNaNO 24(16-3) 请按照要求设计下列目标分子的合成路线CH 2CLOHCN解:通过取代反应将甲基上的氯原子取代为氰基,然后通过硝化反应在苯环上连上硝基,将硝基还原为氨基,然后重氮化、水解得到酚羟基。
合成过程为:Me2SO4 TBAB,NaOHCNHNO3H2SO4CN NO2Fe4CNNH2(1)NaNO+浓HCl,0C~5C°°(2)H2SO4/H20refluxCNOH(16—4)按要求从指定原料出发合成目标化合物,其他有机与无机试剂任选。
(1),OOHNH2解:(1)通过酰基化在苯环上连上羟基,然后用锌汞齐将羟基还原为烷基,可以用硝化反应在苯环上取代硝基,然后还原为胺,得到产物。
合成过程为:OH SOClCl+AlCl3OZn(Hg)HClNO2 NH2(2)ONH,CH2CH2CHCN(16--5)用重氮化反应,由甲苯制备邻苯甲腈。
解:根据重氮化反应在苯环上连上重氮基,然后再用CuCN取代苯环上的重氮基得到反应产物,合成过程为:CH3CH 3NO 2+CH 3ON 2CH 3NO2CH3NNCl -CH 3CN(16--6)完成转化(除指定原料外,可选用任何有机、无机原料和试剂)CH3解:要利用氨基的定位效应通过溴代反应在苯环上连上溴原子,然后通过重氮盐将氨基脱除,合成过程为:CH 33H SOCH3NH2CH 3BrBr(16--7)由苯、丙二酸二已醋和不超过4个碳的原料和必要的试剂合成下列化合物。
chem-16.重氮化合物
SO3H
13
(5) 强碱性溶液中
+ N NCl
KOH
N N OH
N N OK
不能进行亲电反应
14
P406 4(1) 8(2)
6(2.5)
对伯芳胺和仲芳胺则: 对伯芳胺和仲芳胺则
+ N2X + NH2 N N NH H+ N N
11
NH2
(2) 重氮组分的重氮盐邻对位有吸电子基团时反应活 性增强。 性增强。
O2N H3C NO2 + N2X + NO2 H3C NO2 CH3 O2N N NO2 H3C N H3C CH3
(3) 重氮组分的重氮盐邻对位有推电子基团时 , 对 重氮组分的重氮盐邻对位有推电子基团时, 反应不利。 反应不利。
⑴ 被羟基取代
NH2 NaNO2/H2SO4 0~ 5 ℃
NH2 NaNO2-H2SO4 Br Br
N2HSO4 H2O
N+HSO2 3 H2O
OH
OH
+ N2↑
Br
制备酚的方法
5
例1:间硝基苯酚的制备 间硝基苯酚的制备
NO2
混酸 (NH4)2S
NH2
NaNO2/H2SO4
N2HSO4
H2O
NO2 OH + N2↑
12
(4) 酚类偶合在弱碱性溶液中,芳胺偶合在中性或 酚类偶合在弱碱性溶液中, 弱酸性溶液中进行。 弱酸性溶液中进行。
OH + OH O- (活活 活)
OH +
+H
+ OH2
(钝 活 活)
+ ArNH2 + H
pH = 5~7
第16章重氮

碱
Ph
OH
Ph
Ph
ArN NN ON
稳定性:E>Z
2、放氮反应(重氮基被取代)——制备芳烃衍生物
N2+
+
Y
慢 -N2
Y-
快
3、留氮反应 ——制备偶氮化合物
–N+ 2
X
–Y
–Y + N2↑
去氨基 反应
重氮基可以被–H、–OH、–X、–CN……取代
学习要点: 反应条件、 实用价值、注意问题。
§16-2 重氮盐的性质
三、重氮和偶氮化合物 ——脂肪族不稳定,
(一) 分类、结构和命名
以芳香族为主。
(二) 重氮盐的制备
偶氮基 –N=N–
两端连烃基称“偶氮”
一端连烃基称“重氮”
(三) 重氮盐的性质和应用(重点) –N=N–OH
–N=N–
偶氮苯
氢氧化重氮苯
–N=N–SO3Na 重氮苯磺酸钠
重点–N+介≡N绍X-
重氮盐
+–N2Cl
+ArN2Cl
KCN+CuCN
ArCN
*该反应被认为是 自由基反应,亚铜盐起传递电子 的作用
§16-2 重氮盐的性质
(4)被硝基取代——Gatterman(伽特曼)反应
+N2 BF4 NaNO2,Cu
NO2
(5)被氟取代——Schiemann(希曼)反应
+ N2Cl
HBF4
或 NaBF4
+N2 BF4
2、重氮基被取代的反应 OH
H2O △
+ N2
N2+Cl
Cu2Cl2,HCl 1 6~ 60℃
含氮有机化合物和杂环

NO2
Fe / HCl 或Sn / HCl
NH2
12
2. 腈和酰胺的还原
RCN
H2 / Pt LiAlH4
RCH2NH2
O H3C C NH 2
H2/Ni
CH3CH2NH2
13
3. Hofmann降解反应
O R C NH2
Br2 / NaOH or Cl2 / NaOH
RNH2 + NaBr + Na2CO3
O
CH3CCl
NO 2
NHCOCH 3
HNO3 / H2SO4
NHCOCH 3
H2O / OH-
NH 2
NO 2
NO 2
21
4. 与亚硝酸反应
拓展
亚硝酸钠
亚硝酸钠是一种有毒的氧化剂,大量进入血液
后,将血红蛋白中的二价铁氧化为三价铁,形成高 铁血红蛋白血症,失去携氧能力,造成机体组织细 胞缺氧症状,严重影响中枢神经系统,可引起呼吸 困难、循环衰竭。在腌咸肉或加工熟食卤味时,有 时为了使肉色鲜红而加入亚硝酸盐,如加入过量, 同样会引起中毒。另外,食用富含亚硝酸盐的食物 还与一些肿瘤发生有关。据调查发现,食管癌高发 区居民食腌菜者较普遍,食管癌的发病率与食腌菜 量相关,在这些腌制的咸菜中含有大量的亚硝酸盐。
第十章 含氮有机化合物
1
胺
含
氮 重氮化合物、偶氮化合物
有
机 酰胺
化
合 物
含氮杂环
生物碱
2
第一节 胺 一. 胺的分类和命名
1.分类
3
名称 伯胺 仲胺 叔胺 季铵盐 季铵碱
分子式
RNH2 R2NH R3N R4N+XR4N+OH-
有机化学---第16章 重氮和偶氮化合物
②
H3 C
——Schiemann(希曼)反应
2、保留氮的反应
(1) 还原反应
+ Cl N2
SnCl2 + HCl
NHNH2 HCl
.
OH-
NHNH2
苯肼盐酸盐
+ Cl N2
苯 肼
HCl , H2O
100℃
Na2SO3
N N SO3Na H H
NHNH2 HCl
.
OH-
NHNH2
+ Cl N2
Zn + HCl
+ -H
.. ..
N N
G
由于重氮正离子中氮原子上的正电荷可以离域到 苯环上*,因此它是一个很弱的亲电试剂,只能与高度
活化的苯环才能发生偶合反应。
规 律:
对重氮盐而言,当芳环上连有-I、-C基团(如— NO2)时,将使其亲电能力↑,加速反应的进行;反之,
将不利于反应的进行。
+ N N:
δ+
+ N N:
N
N
OH
对位 偶合
+
OH
OH
NaOH (pH=8~10) 0℃
N
N
CH3
邻位 偶合
CH3
5-甲基-2-羟基偶氮苯
(ⅱ) 与芳胺的偶合 a: 叔芳胺 与酚相似,优先在对位偶合; 若对位已占,则在邻位偶合。
+ N N: N(CH3)2
+
CH3 COONa (pH=5~7) 0~5℃
N
N
N(CH3)2
对-(N,N-二甲氨基)偶氮苯 4-(N,N-二甲氨基)偶氮苯
b: 伯芳胺和仲芳胺
由于N上还保留着活泼H原子,因此偶合反应首先
16重氮化合物和偶氮化合物

★★三 ★★三、重氮盐的性质及其应用 放出氮的反应 (N2) 重氮盐的化学性质非常活泼 保留氮的反应 (一)放氮反应 重氮盐中的重氮基可被-H、 取代, 重氮盐中的重氮基可被 、-OH、-X、-CN取代, 、 、 取代 同时放出氮气。 同时放出氮气。 1、 被氢原子取代 、 ArN2HSO4+H3PO2+H2O →Ar-H+N2↑+H3PO3+H2SO4 ArN2HSO4+HCHO+NaOH → Ar-H+N2↑+HCOONa 重氮盐与乙醇作用, 重氮盐与乙醇作用,重氮基亦可被氢原子取代 ArN2HSO4用途:从苯环上除去 2↑+CH3—NO +C2H5OH → Ar-H+N NH 用途:从苯环上除去—NH2或 CHO NO2 注意:往往有副产物醚生成。 注意:往往有副产物醚生成。 起在特定位置上“占位、定位”的作用。 起在特定位置上“占位、定位”的作用。
HBF4
-N2BF4
-N2HSO4
重 氮
反 应
-N2Br
化
操作方法:将芳伯胺溶解于过量的酸中,将溶液冷却 操作方法:将芳伯胺溶解于过量的酸中, 后慢慢加入亚硝酸钠溶液,同时进行冷却和搅拌。 后慢慢加入亚硝酸钠溶液,同时进行冷却和搅拌。 对于重氮化反应, 应注意以下几点: 对于重氮化反应 应注意以下几点: (1)反应要在低温下进行不超过 ℃,否则分解; )反应要在低温下进行不超过5℃ 否则分解; (2)反应要在强酸性介质中进行,防止偶联; )反应要在强酸性介质中进行,防止偶联; (3)亚硝酸不能过量;否则,将促使重氮盐分解。 )亚硝酸不能过量;否则,将促使重氮盐分解。 可用淀粉-碘化钾试纸来确定重氮化反应终点 可用淀粉 碘化钾试纸来确定重氮化反应终点 2HCl + 2HNO2 + 2KI === I2 + NO↑+2KCl + 2H2O 变蓝色! 变蓝色!
重氮盐定稿
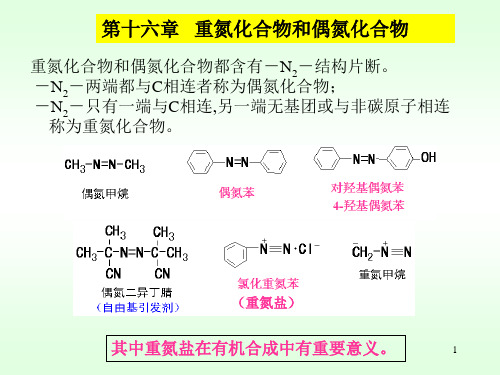
克莱森酯缩合的缩合产物为-酮酸酯.
反应过程:两个乙酸乙酯分子发生羰基的亲核取代 (加成-消除), 酯
乙酸乙酯的α-H有一 定的酸性,类似于醛酮,可以由此进行两分子 酯的缩合。
乙酸乙酯
在醇 钠中 进行
(4)
酸化(5)
三乙
C2H5ONa
H+
三乙钠盐 三乙
反应特点:
1)反应前三步是主要的,在醇钠中反应,在醇钠中得到三乙。 由于三乙酸性大于醇,因此三乙和醇钠反应得到三乙的钠 盐(第4步),然后进行酸化(第5),最终得到三乙。 因此反应条件:1)C2H5ONa 2)H+酸化
OH + HCl
对羟基偶氮苯(桔红色)
OH
N=N
+ HCl
重氮组分
CH3
偶联组分(注意为有-OH的一侧,
优与酚的偶合,在弱碱(pH=8-10)进行,是因为ArO-的 给电子能力比ArOH更强,苯环活性更高;但若pH>10, 则重氮盐转变为氢氧化重氮苯Ph-N=N-OH,副产物多。
16.2.1 放出氮的反应(类似亲核取代机理)
4
(1)重氮基被羟基取代(反应条件:酸性水溶液加热,该 反应一般用硫酸盐)
N2+HSO4- + H2O H+
OH + N2 + H2SO4
例如制备间溴苯酚,1)Br与OH均为邻 对位定位基,无法得到间溴苯酚;2)苯 酚的制备常用碱熔法(p252),但苯上 的溴也能够被碱熔分解掉,因此常规方 法无法制备,只能用重氮盐方法:
在pH=5-7时,最有利于偶合反应进行。
17
② 偶合位置一般在氨基对位,对位有取代基,在氨
基邻位偶合,注意判断重氮组分和偶联组分:
16重氮和偶氮化合物

C
..
C H H C H H H
H
C-H:0.103nm 1360
制备:
CH2N2 CH2=C=O
hr hr
: 2 + N2 CH
: 2 + CO CH
(1)碳烯的应用:碳烯具有很大的反应活性,一般生成后立即进行
下一步反应。 (A) 加成反应:例如在2-丁烯存在下,重氮甲烷分解为碳烯(单线态)后反
N
(2) 制备:
H3C SO 2-N-CH3 + C2H5OH
KOH
CH2N2 + CH3
SO 2-OC2H5 + H2O
NO
CH 3NH 2
HNO 2
H3 C
SO2-NHCH3
H3 C
SO2 Cl
R-CO-NH-CH3
HNO2
R-CO-N-CH3 NO
KOH
CH2N2 + RCOOK + H2O
(3)性质和应用
R'OH
NH3
CH2N2
hr
: 2 CH
+ N2
16.4.2 碳烯 (1)结构和制备 碳烯又叫卡宾,它是一个二价碳的反应中间体,活性高、寿 命短。在碳烯中的碳原子只有6个价电子,其中2个电子未成键, 所以存在两种结构。如下图所示:
..
H C H
C-H:0.112nm 1030 单线态结构 三线态结构
在氟硼酸催化下 能反应
NO !
CH3-COOCH3 + N2 O-CH3 H3C CH3 + N2
NO2 R-CO-Cl + CH2N2
H2 O
NO2 R-CO-CHN2 + CH3Cl + N2 R-CH2COOH + N2 R-CH2COOR' + N2 R-CH2-CO-NH2 + N2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ArCN
ArCN
CN→COOH,故这是在苯环上引入-COOH的很好办法。
CH3 Br NaNO2
HCl
CH3 Br CuCN
KCN
CH3 Br H+
H2O
CH3 Br COOH
NH2
N2+Cl-
CN
16.2.2 保留氮的反应
1、还原:用锌粉盐酸还原为苯胺。
用氯化亚锡和盐酸(或亚硫酸氢钠)还原可得苯肼盐 酸盐,再加碱即得苯肼。
第十六章 重氮化合物和偶氮化合物
基本要求:
1.重氮化反应。
2.掌握重氮盐的性质及其在有机合成上的应用。 3. 偶氮化合物和偶氮染料。
结构与命名: 这两类化合物都含有-N2-官能团。其中-N2-与两个
碳原子相连的为偶氮化合物( N=N)。如果-N2-与一 个碳原子相连,另一个自由价与非碳原子相连,则为重氮 化合物( N N )。
CH3 N=N CH3
N=N
偶氮苯
CH3
N=N
OH
偶氮甲烷
4-甲基-4’-羟基偶氮苯
(CH3)2C N=N C(CH3)2 CN CN
偶氮二异丁腈
C6H5N N Cl氯化重氮苯
16.1 重氮化反应
定义:伯芳胺与亚硝酸作用,生成重氮盐的反应。
(低温和酸性条件,P391)
NaNO2 + HCl 0-5oC
邻位发生反应。
16.3 偶氮化合物和偶氮染料(自学) 16.4 重氮甲烷
分子式: 结构式: CH2N2
轨道示意图:
制备: (1)N-甲基-N-亚硝基对甲苯磺酰胺在碱作用下分解。
(2) N-甲基-N-亚硝基酰胺在碱作用下分解。
KOH HONO CH3NCOR - H O CH3NCOR 2
H
NO
CH2N2 + RCOOK + H2O
[H]
Br2/H2O
Br
Br
N2ClBr H3PO2
Br Br Br
HNO2 HCl
Br
Br
Br
苯甲酸制2,4,6-三溴苯甲酸
COOH COOH COOH COOH
[H] NO2
Br2/H2O NH2
Br
Br
NH2 Br
COOH
COOH Br
HNO2 HCl
Br
H3PO2
Br
Br
N2ClBr Br
+O
HNO2
H3PO2
CH3
重氮盐变为苯没有任何意义,但是可以用于导向合 成,把氨基作为导向基,引导进入基团到要求位置,然 后把氨基变为重氮基脱除。 例如: 由苯制1,3,5-三溴苯; 苯甲酸制2,4,6-三溴苯甲酸; 甲苯制间溴甲苯或间硝基甲苯。
由苯制备1,3,5-三溴苯
NO2 NH2 NH2
重氮甲烷是一个有毒的气体,具有爆炸性。它能溶于乙醚, 并且比较稳定,一般均使用它的乙醚溶液。重氮甲烷非常 活泼,它的碳原子既有亲核性又有亲电性,能够发生多种 类型的反应,在有机合成上是一个重要的试剂。
重氮甲烷的反应
重氮甲烷是个重要的甲基化试剂!
②
OH CH3 + CH2CN2 NO2
OCH3 CH3 + N2 NO2
Ar-N=N CH 3
相同点:反应一般对位发生;若对位占据,则邻位发生。
不同点:与酚偶联pH = 8-10,与芳胺偶联pH = 5-7
(3) 与伯(芳)胺、仲(芳)胺偶联 苯胺与重氮盐发生偶联反应先生成苯重氮氨基苯,如在
盐酸或苯胺盐酸盐溶液中加热30~400C则发生重排,生 成4-氨基偶氮苯:
N2x
+
NH 2
N=N NH
N=N NH2
萘胺和萘酚与重氮盐的偶联反应:
(1)α-萘胺和 α- 萘酚发生在同环另一个α- 位; 另一个α- 位被占据,则在相邻β-位。
(2)β-萘胺和β-萘酚发生在相邻的 α- 位,如果这 个α- 位被占据,则不发生偶联反应。
OH(NH 2) N=N OH(NH 2)
OH(NH 2) N2X
+
OH(NH 2) N=N
CH3 OH(NH 2)
CH3
OH(NH 2) N=N
CH3 OH(NH 2)
不反应
同时具有氨基和羟基的萘的衍生物与重氮盐进行偶联反 应时,pH值对反应位置选择很重要,例如:
2
pH=5~7 弱酸性,在氨基的邻位发生;pH=8~9,为弱 碱性,酚以酚氧负离子存在,这个环活泼,在羟基的
+
C6H5-NH2
[ C6H5-N N ] Cl
-
*1 碱性弱的芳香胺不易发生重氮化反应。 *2 重氮化反应必须在酸性溶液中进行。 *3 重氮盐通常不从溶液中分离出来。
1°重氮化反应必须在低温下进行(温度高重氮盐易分解)。 2°亚硝酸不能过量(亚硝酸有氧化性,不利于重氮盐的稳
定)。
3°重氮化反应必须保持强酸性条件(弱酸条件下易发生副 反应——生成的重氮盐易和未反应的苯胺偶合)。 重氮盐的结构:
热分解产生氟苯。(1927年发现)
NH2
NaNO2 / H2O HCl 0 oC
[ C6H5-N N ] Cl
+
-
HBF4 NaBH4
[ C6H5-N N ] BF4
+
-
不稳定
溶解度较小, 稳定性较高
F + N2 + BF3
各类卤代反应总结
HBr + CuBr or HCl + CuCl 桑德迈耳反应 Cu + HBr or Cu + HCl
2
,
重要的羰基试剂,也是合成 药物和染料的原料。
2、偶合反应
定义:重氮盐正离子可以作为亲电试剂(弱)与酚,芳胺等
活泼的芳香化合物进行芳环上的亲电取代,生成偶 氮化合物,这类反应称为偶联反应。
(1) 与酚偶联
Ar-N N
+
Ar-N=N
+
OH pH=8-10
Ar-N=N
OH
重氮组分
偶联组分
偶氮化合物
Ar-N=N-O
N N N N
(1)
(2)
16.2 重氮盐在合成上的应用
(1)重氮盐的水解
(2)桑德迈耳反应和加特曼反应
(3)希曼反应 (4)重氮盐的还原 (5)偶合反应
N2 Cl
去氮反应 (取代反应) 保留氮的反应 还原反应 偶联反应
16.2.1 放出氮的反应
1、被羟基取代生成酚(水解)
ArN2HSO4 + H2O H+ ArOH + N2 + H2SO4
N2Cl + H3PO 2 + H2O
+ H3PO 3+ N2+ HCl
或氢氧化钠-甲醛溶液。
N2Cl + HCHO + 2NaOH + N2 + HCOONa + NaCl + H 2O
应用:在合成中,借用氨基定位,继而脱除氨基。
CH3
乙酰化
HNO3 Cl2
还原
Cl CH3
O NHCCH3
Cl
H3
甲苯制间溴甲苯或间硝基甲苯
CH3 CH3 [H] CH3 CH3COCl CH3 Br2 Br NO2 NH2 NHOCCH 3 NHOCCH 3 Br CH3 CH3
CH3
CH 3 [H]
CH3 CH3COCl
CH3 HNO 3/H2SO4
NO2 CH3 H3O+ NO2 NHOCCH 3
NH2 CH3
用重氮苯硫酸盐,不用盐酸盐,防止生成氯苯。酸度小有偶 联副反应(P393)。 用来制特殊酚,例如制间硝基苯酚:
NO2 HNO 3/H2SO4 Na2S NO2 OH
40~50%H2SO 4NH2 NaNO 2/H2S Nhomakorabea4 NO2
N2HSO 4
+N2
NO2 NO2
→
2、被氢取代(实际上是氧化还原反应,重氮盐被还原, 次磷酸等被氧化)。
NHOCCH 3 CH3
NO2 NH2
NO2
3、被卤原子取代制卤苯:碘苯、氟苯必须用此方法, 特殊氯苯、溴苯必须用此方法。
若催化剂改为铜粉,反应也可以进行, 但产率低,称伽特曼反应。
桑德迈尔 反应
希曼反应(Schiemann)
定义:芳香重氮盐和冷的氟硼酸反应,生成溶解度较小,
稳定性较高的氟硼酸盐,经过滤、干燥,然后加
Ar-N N Cl +
ArBr or ArCl
ArBr or ArCl
加特曼反应 ① HBF4 ② △ 希曼反应
ArF ArI 引入I的很好方法
KI
由苯制备间二溴苯和间氯溴苯。
4、被CN取代制苯腈,水解生成羧基。
KCN + CuCN (中性条件)
Ar-N N Cl +
推广的桑德迈耳反应 Cu + KCN 推广的加特曼反应
pH>10,则易形成ArN2OH。
(2) 与叔芳胺偶联
Ar-N NCl
+
-
+
N(CH3)2
HOAc H2O pH= 5-7 0OC
Ar-N=N
Ar-N NCl - + H3C
+
N(CH3)2
N(CH3)2
HOAc H2O pH= 5-7 0OC
N(CH 3)2
pH<5,则易形成-N+R2。是成 为强的制钝基团,间位定位。
