季铵碱的霍夫曼_Hoffmann_消除
华中科技大学有机化学第十二章 胺

重氮盐在铜作用下,还可与NaNO2,Na2SO3置换,得到硝基芳烃和芳烃 磺酸盐。
重氮盐与氢的置换实际上是去胺化反应,它在合成上极为重要。例如, 由苯合成1,3,5-三溴苯,直接溴化是得不到的。但由苯胺进行溴化得2,4,6三溴苯胺,再进行去胺化,则很容易得到:
(2) 重氮偶合反应 芳香族重氮盐是弱的亲核试剂,它们可以和高度活化的芳香族化合物发生 偶合得到偶氮化合物。这种反应称为重氮偶合反应,最常用于合成偶氮染料。 高度活化的芳香族化合物一般为酚与3o芳胺。
醇 、酚、酸与CH2N2反应历程基本一样。即:
而与酰氯反应则稍有不同。
重氮甲烷可由N-甲基-N-亚硝基酰胺或磺酰胺与浓的KOH水溶液在 乙醚与水溶液的两相体系中反应得到,产物溶于乙醚中。
3.叠氮化合物 叠氮化合物RN3是具有4电子的1,3-偶极化合物,其共振结构为:
N3-是很好的亲核试剂,与卤代烷反应经还原可得1o胺, 放出N2。 NaN3与酰氯反应可以得到酰基叠氮化物。加热分解放出氮气并形 成异氰酸酯,加水形成胺;或直接在水中加热分解得到胺。此反应称 为Curtius反应。
胺的酸性强弱次序与胺的碱性次序正相反,为芳香胺>氨>脂肪胺。
2.胺的烷基化 氨,1o胺,2o胺与3o胺可与1o及2o卤代烷发生SN2反应,得到相应的 1o,2o,3o胺与4o铵盐。
若用大大过量的氨与卤代烷反应,可以减少多烷基化产物,
实质上胺的烷基化反应是胺作为亲核试剂进行的取代反应,所以亲核性(碱 性)弱或空间位阻大都很难使反应正常进行。 在烷基化反应中,卤代烷只能用1o与2o卤代烷,3o卤代烷几乎全部进行消除 反应;一般芳基卤化物不能反应,但邻、对位有强吸电子基的芳基卤化物仍可 反应,如对硝基溴苯可以与胺反应。烷基化试剂除卤代烷外,还可用硫酸酯, 如硫酸二甲酯及对甲苯磺酸酯等。
中药化学习题及答案

第六章黄酮类化合物一、概念1、黄酮类化合物:泛指两个苯环通过三碳链相互连接而成的一系列化合物。
2、盐酸—镁粉反应:将黄酮类化合物试样溶于甲醇或乙醇中,加入少许镁粉振摇,再加几滴浓盐酸呈色。
3、锆盐—枸椽酸反应:鉴定3 –或5- OH黄酮,黄色。
4、SbCl5反应:鉴定查耳酮5、氨性氯化锶反应:鉴定3‘4’ 邻二OH黄酮二、填空1.目前黄酮类化合物是泛指两个(苯)环,通过( C3 )链相连,具有(2 –苯基色原酮)基本结构的一系列化合物。
2.黄酮类化合物在植物体内主要以(苷)的形式存在,少数以(苷元)的形式存在。
3.黄酮类化合物的颜色与分子结构中是否存在(交叉共轭体系)有关。
4.色原酮本身(无)色,但在2—位上引入(苯)基后就有颜色。
如果(双健)氢化,则(交叉共轭体系)中断,故二氢黄酮醇(无)色。
黄酮类化合物在4/7—位引入( -OH )基团,使颜色加深。
异黄酮的共轭体系被(破坏),故呈(微黄)色。
查耳酮分子中存在(交叉共轭体系)结构,故呈(黄)色。
5.花色素的颜色随( pH )改变。
一般(小与7)时显红色,(大与8.5 )时显蓝色,(等于8.5 )时显紫色。
6.游离黄酮类化合物一般难溶或不溶于(水)中,可溶于(乙醇)、(正丁醇)及(氯仿)中,游离黄酮类化合物一般分子呈平面型,它在水中溶解的程度(<)与非平面型分子。
例如(二氢黄酮)在水中溶解大与(黄酮)。
7.花色素因以(离子型)形式存在,具有(离子)的通性,故水溶性(强)。
8.黄酮苷元分子中引入羟基后,水溶性增(大),引入羟基越多,其水溶性越(强)。
而羟基甲基化后,其水溶性(减弱)。
9.黄酮苷一般溶于(水)、(丙酮)及(正丁醇)等中,而难溶或不溶于(氯仿)、(乙醚)等有机溶剂中。
10.黄酮类化合物因分子中具有(酚羟基)而显酸性。
其酸性强弱顺序为:7,4’-二OH(5%NAHCO3)>7-或4‘-OH(5%NA2CO3)>一般酚羟基(0.2%NAOH)>5-OH(4%NAOH) 11.黄酮类、二氢黄酮类、黄酮醇类、异黄酮类与HCl—Mg粉反应呈(红)色。
有机化学考研知识点总结

H
B 消去
2)水合反应
CC
H 2O, H 2SO 4 H2SO 4
CC H OH
X
含有吸电子基团,
为反马氏产物
【特点】反式共平面加成、
马氏加成物、重排
3) 加X2反应
X2
CC
CC XX
【特点】反式加成、马 氏加成产物
16
第二节 有机化学的基本反应
4)加XOH反应
CC
X OH
5)硼氢化-氧化反应
CC
3. 考虑反应的区域选择性问题:消除反应:扎依切夫规则还是霍夫 曼规则; 加成反应:马氏规则还是反马氏规则; 重排反应:哪个基团迁移、 不对称酮的反应:热力学控制还是动力学控制等。
4. 考虑立体选择性问题:消除反应:顺消还是反消、加成反应:顺 加还是反加、重排反应:构型保持还是构型翻转、SN1:重排、SN2:构型 翻转等。
歧化反应
按电荷行协为同:反亲应电—反—应周环亲反核应反应
D-A反应
9
第二节 有机化学的基本反应
一、取代反应 ——自由基取代、亲电取代和亲核取代 1.自由基取代 【特点】有自由基参与、光照、加热或过氧化物存在 【注意】 ①烷烃的卤代一卤代较差,溴卤代的选择性较好
hv
CH3CH 2CH 3 + Cl2
13
RONO 2 + AgX
第二节 有机化学的基本反应
2) 羰基化合物亲核加成-消除反应
O
O
C + Nu H R R' 亲核试剂
R C Nu + HR'
F
3) 重氮盐取代反应 【特点】低温环境,强酸介质
【应用】制备芳香族亲电取代 反应难制备的化合物
有机合成知到章节答案智慧树2023年兰州文理学院

有机合成知到章节测试答案智慧树2023年最新兰州文理学院绪论单元测试1.1805年,科学家从鸦片中获得了第一个生物碱,称为:()。
参考答案:吗啡2.根据当代的观点,有机物应该是()。
参考答案:含碳的化合物3.1828年维勒(F.Wohler)合成尿素时,他用的是()。
参考答案:氰酸铵4.有机物的结构特点之一就是多数有机物都以 ( ) 。
参考答案:共价键结合5.通常有机物分子中发生化学反应的主要结构部位是()。
参考答案:官能团(功能基)6.黄鸣龙是我国著名的有机化学家,他的贡献不是()。
参考答案:完成了青霉素的合成;在有机半导体方面做了大量工作;在元素有机方面做了大量工作7.“化学成键作用是由于两个原子间共享电子对的结果。
”此化学键理论中一个最根本的思想由谁首先提出?()。
参考答案:Lewis8.下列四种溶剂的比重小于1的是()。
参考答案:乙醚;正庚烷;环己烷9.1989年,Kishi合成了海葵毒素,被称为是世纪工程。
()参考答案:对10.在1828年,Fischer,E首次由氰酸铵制的尿素。
()参考答案:错第一章测试1.完成反应所用的氧化剂()参考答案:丙酮/异丙醇铝2.某烯烃经臭氧化和水解后生成等物质的量的丙酮和乙醛,则该化合物是()。
参考答案:(CH3)2C=CHCH33.分子式为C7H14的化合物G与高锰酸钾溶液反应生成4-甲基戊酸,并有一种气体逸出,G的结构式是:()。
参考答案:(CH3)2CHCH2CH2CH=CH24.由的主要试剂有()。
参考答案:O3/Me2S5.下列化合物不能使酸性高锰酸钾褪色的是()。
参考答案:丙烷6.为了检查司机是否酒后驾车采用呼吸分析仪,其中装有KCrO + HSO,如果司机血液中含有乙醇量超过标准,则该分析仪显示绿色,其原理()参考答案:乙醇被氧化7.环己烯经酸性高锰酸钾氧化后,再加热,生成的主要产物是酸酐。
()参考答案:对8.可用溴的四氯化碳溶液鉴别环丙烷和丙烯。
顺式阿曲库铵霍夫曼降解反应

顺式阿曲库铵(Cisatracurium)是一种非去极化型肌肉松弛药,在体内主要通过霍夫曼消除(Hofmann Elimination)途径进行降解。
霍夫曼消除是一个立体选择性的生物转化过程,其特点是在肌松药的季铵结构中发生N-甲基转移和随后的脱烷基反应。
具体到顺式阿曲库铵,由于其分子结构中含有一个叔胺氮原子和一个相邻的酯基,它在体内可以被酯酶水解酯键,生成活性代谢产物,然后这个代谢产物继续通过霍夫曼消除过程失去一个甲基,形成一个叔胺和一个酮酸,后者进一步代谢为无活性物质并最终经肾脏排出体外。
这个降解过程使得顺式阿曲库铵具有较短的时效和良好的恢复特性,尤其适用于需要短期肌肉松弛且对长时间残留作用有严格限制的临床情况。
顺式阿曲库铵(Cisatracurium)是一种非去极化型神经肌肉阻滞剂,其在体内的主要代谢途径之一是霍夫曼消除反应(Hofmann Elimination)。
这是一种化学反应类型,通常发生在含有季铵结构的化合物中。
顺式阿曲库铵分子结构中包含一个叔胺基团和一个邻近的酯基团。
在体内,该药物首先通过酯酶催化水解酯键,形成活性代谢产物。
然后这个代谢产物经历霍夫曼消除过程,即N-甲基从叔胺基团转移至相邻碳原子上,并伴随着一个烷基的脱除,生成相应的酮酸和季胺衍生物。
由于霍夫曼消除具有立体选择性和时间依赖性,使得顺式阿曲库
铵相较于其他肌松药,具有相对较短的时效和良好的恢复特性,尤其适用于需要短期肌肉松弛并且对恢复速度有较高要求的临床麻醉过程中。
胺的定义氨的烃基取代物
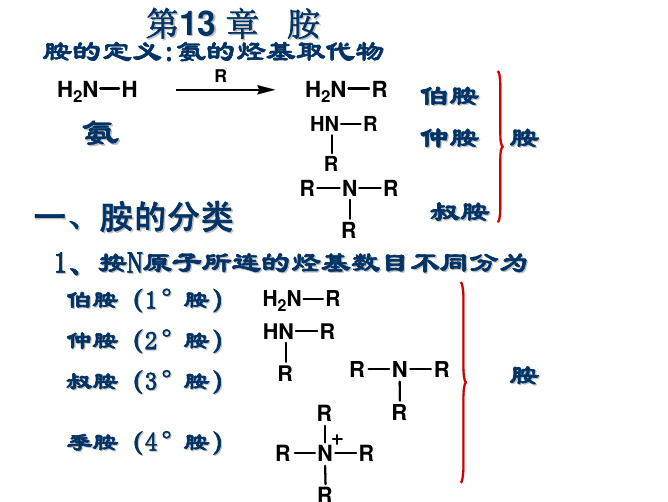
CH3CH CHCH2CH3
量少
作业:1、4、5、6、7、8、14、17、18
C-亚硝基化合物的颜色变化
ON 翠绿色
H NR2
OH
HO N
NR2
橘黄色
z 随酸碱度不同而发生结构互变,从而呈现 出不同的颜色变化,此类物质可用于酸碱 指示剂。类似物质如偶氮染料甲基橙等
6、重氮盐的反应
H2
NN
线型分子, N原子为SP杂化
(1)干燥品易爆炸,低温酸 性可存在于溶液中
+
热或振荡
NN
CH2=CH2 + N(CH3)3
Hofmann规则:几种不同的β-H时,在加热时可 生成几种烯烃,其主要产物是双键上有较少取 代基的烯烃.
② β-H
① β-H
CH3CH2CHCH3
180℃ CH3CH2CH CH2
95%
+N(CH3)3OH
+ CH3CH CHCH3 + (CH3)N 5%
Hofmann规则解释:E2机理 β-H的酸性对消除的取向起决定性的作用。 当β-碳上连有供电子基时,可使酸性减弱; 连有吸电子基时,则使酸性增强。 反应时,OH-主要进攻酸性较强的β-氢而得到 Hofmann消除反应产物。
CH3CH2-NH-CH2CH3 二乙胺
NH2-CH2-CH2-NH2 乙二胺
NH2 苯胺
NH2
环己胺
注意:z
若脂肪烃基连在芳胺氮原子上,则在脂 肪烃基名称前加字母“N” ,以便与苯
环取代物相区别。
CH3 N
N,CNH-3二甲基苯胺
CH3 N
CH2CH3
N-甲基-N-乙基苯胺
• 比较复杂的胺命名
胺的定义氨的烃基取代物

z 季铵碱与酸作用生成季铵盐,遇到强 碱不会游离出季铵碱,这是因为季铵 盐的N原子上没有H原子,不能发生质 子转移生成水,说明季铵碱是强碱。
-
R4N+OH + HCl
-
R4N+Cl + NaOH
-
R4N+Cl + H2O
-
R4N+OH + NaCl
碱性的应用
91
4.20
乙胺 ethylamine
C2H5NH2
-81
16.6
易溶
3.29
二乙胺 diethylamine
(C2H5)2NH
-48
56.3
易溶
3.0
三乙胺 triethylamine (C2H5)3N
-114.7 89.3
14
3.25
脂肪胺的碱性: 仲胺>伯胺,叔胺
各类胺碱性强弱的大致排列顺序
CH2=CH2 + N(CH3)3
Hofmann规则:几种不同的β-H时,在加热时可 生成几种烯烃,其主要产物是双键上有较少取 代基的烯烃.
② β-H
① β-H
CH3CH2CHCH3
180℃ CH3CH2CH CH2
95%
+N(CH3)3OH
+ CH3CH CHCH3 + (CH3)N 5%
Hofmann规则解释:E2机理 β-H的酸性对消除的取向起决定性的作用。 当β-碳上连有供电子基时,可使酸性减弱; 连有吸电子基时,则使酸性增强。 反应时,OH-主要进攻酸性较强的β-氢而得到 Hofmann消除反应产物。
CH3CH CHCH2CH3
含氮化合物练习题
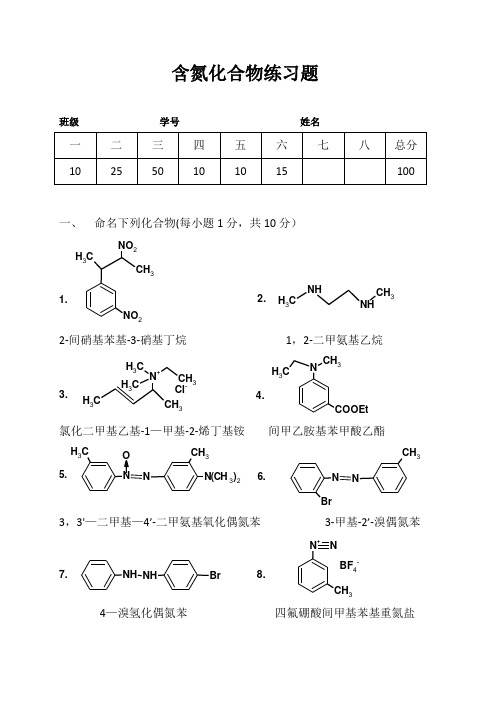
含氮化合物练习题班级 学号 姓名一、 命名下列化合物(每小题1分,共10分)NO 2CH 3CH 3NO 21.2.CH 3NH CH 32-间硝基苯基-3-硝基丁烷 1,2-二甲氨基乙烷3.4.CH 3CH 3N +CH 3CH 3CH3Cl -N CH 3C H 3COOEt 氯化二甲基乙基-1—甲基-2-烯丁基铵 间甲乙胺基苯甲酸乙酯NCH 3C H 3N(CH 3)25.6.N NCH 3Br3,3'—二甲基—4’-二甲氨基氧化偶氮苯 3-甲基-2’-溴偶氮苯7.8.NH NHBrN +NCH 3BF 4-4—溴氢化偶氮苯 四氟硼酸间甲基苯基重氮盐9.10.CH 3CH 3CH 3N CH 3NO氧化甲乙胺 N -亚硝基甲乙胺二、 完成下列反应方程式,注明产物的立体构型和主要产物(每小题1分,共25分)1.CH 3NO 2NaOH2.HNO2CH 3NO 23.Fe + HClCH 3NO 24.H /PdCH 3NO 25.23NO26.NO 27.4NO 28.LiAlH 4NO 29.NaOHNO 2NO 2Br10.HNO NH 2Br11.NH BrCH 3HNO 212.N CH 3C H 3HNO 213.NC H 3CH 3CH 3HNO214.CH3CH2N(CH3)2H2O215.NHCOCH3Br216.NHCOCH3ClO2CH3NH217.Heat CH3CH3N+CH3CH3CH3FOH-18.NHCOCH3ClO2SCH3NH219.N 1.CH3I2.Ag2O/H2O 3.Heat20.NH2NaNO2/HCl0-5C21.N+NCH3H3PO2HSO4-22.CuCl/HCl N+NClHSO4-23.CuCN/KCN N+NBrHSO4-24.NaNO2/Cu N+N BF4-25.NH4Cl N+NBrHSO4-NH CH3+三、选择题(每小题1分,共30分)1.酸性最强的是AA.硝基甲烷B.硝基乙烷C.硝基异丙烷D.硝基苯2.与亚硝酸反应产物的碱溶液呈红色的是B A.氨基甲烷B.硝基乙烷C.硝基异丙烷D.硝基苯3.可用于鉴别硝基化合物的是DA.Fe+HClB.Sn+HClC.As2O3+NaOHD.NaNO2/HCl+NaOH4.可使硝基苯还原成苯胺的是AA.Fe+HClB.葡萄糖/ NaOHC.Zn/NaOHD.Zn/NH4Cl5.可使硝基苯还原成氧化偶氮苯的是B A.Fe+HClB.葡萄糖/ NaOHC.Zn/NaOHD.Zn/NH4Cl6.可使硝基苯还原成氢化偶氮苯的是C A.Fe+HClB.葡萄糖/ NaOHC.Zn/NaOHD.Zn/NH4Cl7.可使硝基苯还原成偶氮苯的是CA.Fe+HClB.葡萄糖/ NaOHC.Zn/NaOHD.Zn/NH4Cl8.水溶液中碱性最强的是B A.甲胺B.二甲胺C.三甲胺D.苯胺9.碱性最强的是ANH23NH2ClNH2ClNH2CH3A. B. C. D.10.与TsCl反应的产物加碱澄清,加酸又浑浊的的是A A.甲胺B.二甲胺C.三甲胺D.氢氧化四甲铵11.与亚硝酸反应生成黃色油状物的是BA.甲胺B.二甲胺C.三甲胺D.氢氧化四甲铵12.与亚硝酸反应生成绿色沉淀的是CA.苯胺B.N-甲基苯胺C.N,N—二甲基苯胺D.三甲铵13.苯胺类物质常用于保护氨基的反应是B A.磺酰化B.乙酰化C.重氮化D.酸化14.常用于鉴别苯胺的试剂是BA.氯水B.溴水C.碘/四氯化碳D.硝酸15.磺胺类药物的基本结构是AA.对氨基苯碘酰胺B.对羟基苯碘酰胺C.间氨基苯碘酰胺D.间羟基苯碘酰胺16.季铵碱的Hoffmann热消除反应的机理是DA.E1B.E2C.E1CBD.介于E1CB与E2之间17.季铵碱的热消除反应常用于AA.测定胺的结构B.测定胺分子中的氮原子数C.测定胺分子中的环数D.制备烯烃18.不能将芳香族重氮盐的重氮基用氢取代的是D A.次磷酸B.乙醇C.HCHO/NaOHD.甲醇19.能将重氮基还原成肼的是AA.Sn+HClB.葡萄糖/ NaOHC.Zn/NaOHD.Zn/NH4Cl20.重氮盐与酚的偶联介质是DA.强酸性B.强碱性C.弱酸性D.弱碱性21.重氮盐与苯胺的偶联介质是C A.强酸性B.强碱性C.弱酸性D.弱碱性22.重氮基被碘取代的催化剂是D A.CuB.CuIC.CuClD.不用催化剂23.重氮基被溴取代的催化剂是B A.CuB.CuBrC.CuClD.不用催化剂24.重氮基被硝基取代的催化剂是A A.CuB.CuBrC.CuClD.不用催化剂25.重氮基被氟取代的催化剂是DA.CuB.CuBrC.CuClD.不用催化剂四、试用化学方法鉴别下列化合物(10分)1.1—己醇、2-戊酮、3-戊酮、己烷、环已醇2.乙醇,3-戊醇,乙醛、己烷、3-戊酮五、合成(每小题5分,共10分)1.由苯合成间溴氯苯2.由苯合成对苯二胺3.由苯合成均三溴苯4.由苯合成3,5—二溴甲苯5.由苯合成间硝基甲苯同46.由苯合成4—甲基—2,6—二溴苯酚同4六、推断题(每小题2、5、3分,共10分)1.A(C6H15N)+HCl→溶解,+HNO2→N2+B,B+I2/OH—→黄↓,B+浓硫酸共热→C(C6H12),C+KMnO4/H+→乙酸+2—甲基丙酸。
13.4季铵碱的霍夫曼_Hoffmann_消除

②若季铵碱的烃基上有-H,加热时生成叔胺和烯烃
13-04 季铵碱的 Hoffmann 消除
含-H季铵碱加热分解反应历程(双分子消除反应E2)
13-04 季铵碱的 Hoffmann 消除
季铵碱存在多个烃基反应时,-氢被消除的难易次序如下
霍夫曼(Hoffmann)消除:消除反应中含多种-H的季铵碱 主要产物为双键上烷基最少的烯烃
13-04 季铵碱的 Hoffmann 消除mann 消除
(1)季铵碱的制备
季铵盐与强碱作用时,得到含有季铵碱的平衡混合物
常用湿的氧化银与季铵盐作用促进反应
13-04 季铵碱的 Hoffmann 消除
(2)季铵碱的性质------热分解
季铵碱加热到100-150℃会分解 ①若季铵碱的烃基上没有-H,加热时生成叔胺和醇
13-04 季铵碱的 Hoffmann 消除
(3)应用--测定胺的结构
未知胺
季铵盐
季铵碱
烯烃+叔胺
有机化学第二版(高占先)10-13章习题答案

第10章 醛、酮、醌10-1 命名下列化合物。
(1)3-甲基-1-苯基-1-戊酮; (2)2,4,4-三甲基戊醛; (3)1-(1-环已烯基)丁酮; (4)(E )-苯基丙基酮肟; (5)3-丁酮缩乙二醇; (6)2-环已烯酮; (7)三氯乙醛缩二甲醇; (8)2-戊酮苯腙; (9)2,6-萘醌; (10)2,4-已二酮; (11)((E )-间甲基苯甲醛肟。
10-2 写出下列反应的主要产物。
PhCHOHCOONa +浓NaOHHCHO2OH+(Cannizzaro 反应)OZn-Hg / HClHCNH 3OOH COOHO(Clemmensen 还原)H 3CC CH 3OMg 66H 3OH 2SO 4△(CH 3)2C C(CH 3)2OH OH(H 3C)3CC CH 3O(pinacol 重排)(1)(2)(3)(4)+HCHO(Mannich 反应)+HCl(5)(6)O N HCH 2CH 2NOCH 3OCH3CH 3OH(黄鸣龙还原)CO 3Cl+CO 2HCl+(Baeyer-Villiger reaction)ONH 2+PCl 5H NO(Beckmann 重排)O(1) HSCH 2CH 2SH2O(1) Cl 2 / NaOH 3OHO(卤仿反应)(7)(8)(9)(10)CHCl 3+(Wittig reaction)CH 3MgBr +Ph 3(1) CuCl 3(13)(12)(11)O+O(1,4-加成产物)OCHCH 2CH 3O OOHHONCO(双烯合成反应)10-3 比较下列化合物的亲核加成反应活性。
(2)(1)C OCH 3H 3C C CH 3OH 3CC HOCOCH 3H 3C(3)(4)(3)>(1)>(2)>(4)10-4 将下列化合物按烯醇式的含量多少排列成序。
CH 3COCHCOCH 3CH 3COCH 2CH 3(2)(1)PhC H 2C O(3)(4)3CH 3COCH 2COCH 3C CH 3O(1)>(4)>(3)>(2)10-5 指出下列化合物中,哪些能发生碘仿反应?哪些能与饱和NaHSO 3反应?(2)(1)O(3)(4)(5)ICH 2CHOCH 3CH 2CHOC 6H 5COCH 3CH 3CHOCH 3CH 2CH 2OHCH 3CH 22CH 3CH 3CH 23OH(7)(6)(8)O能与饱和NaHSO 3反应的有(1)、(2)、(5)、(8)[脂肪族甲基酮、大多数醛和8个碳以下的脂肪酮能进行此反应]。
2020高中化学竞赛讲义设计—天然产物化学-第三章 生物碱(下)

2020高中化学竞赛讲义天然产物化学2020苏州中学竞赛讲义第三章 生 物 碱(下)㈢成盐(Alk 成盐的机理)绝大多数生物碱可与酸形成盐,对H +(质子)化来说,仲胺、叔胺生物碱成盐时,质子多结合于氮原子。
对以季胺碱、氮杂缩醛、烯胺以及具有涉及氮原子的跨环效应形式存在的生物碱,质子化则往往并非发生在氮原子上。
1.季胺生物碱的成盐:(质子与OH _结合成水)盐遇碱又可复成季胺碱,但对以亚胺盐(immonium salts )形式,如:小檗碱类、苯菲啶类、3,4—二氢异喹啉类等存在的季铵盐,其在酸碱溶液中存在的形式比较特殊。
曾认为通常以季胺型、醛式和氮杂缩醛三种方式平衡存在。
经应用物理分析方法研究结果表明,在碱水液中,以氮杂缩醛形式存在(无醛式)。
2.含氮杂缩醛Alk 的成盐:[质子与RO -结合成H-OR (醇或水)] 这类生物碱与酸作用形成亚胺盐,质子是与RO -结合成醇或水。
N OHOHN +-+X .-+H OH季胺碱盐水NO OHOMe OMeNO OOMe OMeNHO OOMe OMeCHO+.OH-醛式季铵型小檗碱的三种平衡方式氮杂缩醛(醇胺型)3.具有烯胺结构Alk 的成盐:此类Alk 质子化多在β碳上,而非氮原子。
例:吡咯与烯胺不同,因其孤电子对参与芳香体系,氮原子被极化呈正性而排斥电子,故碱性极弱。
但若强行质子化时,质子则加在α碳上。
新士的宁虽有烯胺结构,但与酸成盐时,质子却结合于N 2上,而非β碳。
原因是其分子中N 2处于稠环桥头,受Bredt ’s 规则限制,难于形成亚胺形式盐类。
所以新士的宁分子中N 2类似于叔胺而非烯胺。
同理,阿马林碱虽含氮杂缩醛结构,但与酸成盐时,质子化则直接发生在N 2上。
N C HORN CH H O H X OH 或HOR+X-+R氮杂缩醛生物碱亚胺盐醇或水23N NOCH 2CH 3COOH+斯米生(亚胺盐)(内脂环开裂,质子与COO 结合)-C NCCH αβ+H+烯胺亚胺盐NONHH MeOOCN ON H H MeOOCH+OH二氢奥斯冬宁亚胺盐NHNαβ烯胺吡咯含氮杂缩醛Alk 的成盐(如:阿马林碱)和烯胺结构Alk 的成盐(如:新士的宁),若在分子中,N 原子处于稠环桥头,由于张力较大,N 原子难于形成亚胺盐。
第九章消除反应(07)

E1反应中的碳正离子重排 反应中的碳正离子重排
(CH3)3CCHCH3 OH H+ (CH3)2C=C(CH3)2
+
(CH3)3CCHCH3 OH
+
1) H+ 2) -H2O
(CH3)2C CH3
-H+ CH3
CHCH3
1,2-甲基迁移 甲
CH3 C C CH3
(CH3)2C
C(CH3)2 H
CH3
H Nu: + H H
•
影响E2反应区域选择性的因素: 影响 反应区域选择性的因素: 反应区域选择性的因素 1) 碱的结构
CH3 CH3 CH C CH3 + ROCH3 C CH3 CH3 C CH3 + CH3 CH CH3 CH3 C CH2
CH3 Br
产 物 : 双 键 碳 上 取 代 基较 多
双 键碳 上 取 代 基 较 少
9.1 一般消去反应机理 9.2 消去反应的区域选择性 9.2.1 Zaitsev’s Rule 9.2.2 Hoffmann’s Rule 9.3 E2反应的机理及其立体化学 反应的机理及其立体化学 9.4 EI反应的机理及其立体化学 反应的机理及其立体化学 9.5 E/SN反应的竞争 9.6 E1cb反应 似E1cb反应 反应/似 反应 反应 9.6.1 季铵碱的 季铵碱的Hofman消去机理 消去机理 9.6.2 季铵碱 季铵碱Hofman消去的取向 消去的取向 9.7 Cope消去反应 热消去反应 消去反应(热消去反应 消去反应 热消去反应) 9.8 邻二卤代烷消去 2成碳碳双键 邻二卤代烷消去X 的反应 9.9 邻/偕二卤代烷消去 2成碳碳三 偕二卤代烷消去X 偕二卤代烷消去 键的反应
霍夫曼降解反应

霍夫曼降解反应[编辑]
(重定向自Hofmann降解反应)
霍夫曼降解反应(Hofmann降解)又称霍夫曼重排反应,是指一级酰胺在溴(或氯)和碱的作用下转变为少一个碳原子的伯胺的有机化学反应。
[1][2][3]
这一反应以其发现者奥古斯特·威廉·冯·霍夫曼命名。
其过程为溴和氢氧化钠混合后有部分生成次溴酸钠,次溴酸钠将一级酰胺转化为中间产物异氰酸酯,异氰酸酯水解,放出二氧化碳,同时生成比反应物少一个碳原子的伯胺。
邻氨基苯甲酸在工业上就是通过这个反应制备的。
目录
[隐藏]
• 1 机制
• 2 变化
• 3 参考文献
• 4 参见
机制[编辑]
酰胺氮原子上的氢原子先被溴原子取代,生成N-溴代酰胺,这时氮原子上连接的两个吸电子基使得氮原子上的氢在碱性条件下被解离去,形成负离子,继而重排为异氰酸酯,后者水解并脱羧,得到伯胺。
变化[编辑]
一些反应物可以用来代替溴,如N-溴代琥珀酰亚胺用1,8-二氮杂二环[5.4.0]十一碳-7-烯(DBU)作为生物碱进行反应。
另一个变化是用甲醇钠和甲醇的混合液代替氢氧化钠,以提高产率。
此时中间产物异氰酸酯会和甲醇反应生成易水解和分离的氨基甲酸。
[4]。
有机合成中的 β-消除反应

有机合成中的β-消除反应摘要:本文阐述了消除反应的类型和各类型反应的机理和历程,并讨论了其影响因素。
关键字:β—消除、立体选择、过渡态、碳正离子消除反应是从一个分子中消除两个原子或基团而不被其它原子或基团所置换的反应。
它可以分为三类,若消去的2个原子连在同一个碳原子上,则称为α—消除反应,若2个消去的原子连在相邻的2个碳原子上,则称为β—消除反应,若2个消去的原子连在1,3位碳原子上,则称为γ—消除反应,其中β—消除反应最为重要。
其实质是从相邻的两个原子上消除两个原子或基团,形成一个新的双键或叁键。
β—消除反应包括的反应多,而该类反应涉及的反应条件、反应产物都比较复杂,且消除反应和取代反应常常相伴而行,反应历程也时有变化,因而比较复杂[1]。
但其在实际中有广泛的应用,如卤代烃的消除反应、磺酸酯的消除反应、季铵碱的消除反应[2].接下来本文将对β—消去反应的反应历程和影响因素作简要介绍。
1反应历程分类β—消去反应的历程有三种,即:单分子消除反应机理(E1)、双分子消除反应机理(E2)和碳负离子反应机理(E1cb)[4]。
1.1E1机理单分子消除为2步过程,第一步是离去基团带着一对电子离去,底物成为碳正离子;第二步是碳正离子从β位脱去一个质子,给予碱或溶剂,生成烯键,第一步速率较慢,是决定反应速率的步骤,E1机理中C—X键断裂在前,C(β)一H 键断裂在后,故常伴随碳正离子重排。
单分子消除反应的动力学特征是:速率=K[RX]影响反应快慢的因素有:第二步中生成碳正离子的稳定性,介质是否容易电离和是否易于使离子溶剂化,不同结构的卤代烷烃反应活性难易为1。
RX<2。
RX<3。
RX。
消除反应按E1历程进行时,中间体正碳离子的稳定性决定反应速度,产物的生成发生在第2步,产物的稳定性是决定消除反应择向的主要因素。
在E1反应里,不论作用物性质如何,总是形成双键碳上带有最多烷基的烯烃主产物;所以消除反应按E1历程进行时一般服从规则,但Saytzaff消除反应产物由于空间作用变得不稳定时,消除反应将遵Hoffmann规则1.2E2机理1.2.1双分子消除反应为一步反应,当碱进攻β—H时,β—C—H和α—C—H 同时均等协同地断裂,在过渡状态中5个原子团在同一个平面上,随后在α—碳和β—碳上生成π键。
hoffman反应机理

hoffman反应机理Hoffman反应机理引言:Hoffman反应是一种重要的有机合成反应,常用于合成氨基酸和醇胺等化合物。
该反应以底物的氨基取代基为起始,通过重排反应将其转化为对应的胺化合物。
本文将详细介绍Hoffman反应的机理及其应用。
一、Hoffman反应的机理Hoffman反应的机理主要涉及两个关键步骤:底物的氨基取代基的脱离和氨基重排。
1. 底物的氨基取代基的脱离Hoffman反应一般以氯化胺为底物,首先经过亲核取代反应,底物的氨基取代基(通常是氯或溴原子)会被亲核试剂(如氢氧化钠或氢氧化钾)攻击,从而脱离出底物,形成相应的亲核试剂盐。
2. 氨基重排脱离的氨基取代基会发生重排反应。
这个过程中,氨基的位置会发生改变,通常是通过中间产物的环化、开环或重排等方式实现。
重排反应的具体机理取决于底物的结构和反应条件,常见的机理包括Hofmann消除、Hofmann重排和Hofmann交换等。
二、Hoffman反应的应用Hoffman反应在有机合成中有着广泛的应用。
以下是一些典型的应用示例:1. 氨基酸的合成Hoffman反应可以用于合成氨基酸。
通过选择合适的底物和反应条件,可以将底物中的氨基取代基脱离并发生重排,从而得到目标氨基酸。
2. 醇胺的合成Hoffman反应也可以用于合成醇胺。
通过选择适当的底物和反应条件,可以将底物中的氨基取代基脱离并发生重排,最终得到目标醇胺。
3. 药物合成Hoffman反应在药物合成中也有广泛的应用。
例如,一些抗癌药物的合成中常常涉及到氨基取代基的脱离和重排,Hoffman反应可以有效地实现这些步骤,从而合成所需的药物。
4. 功能性化合物的合成Hoffman反应还可以用于合成各种具有特定功能的化合物,如配体、催化剂和功能性高分子等。
通过选择不同的底物和反应条件,可以实现底物中特定位置的氨基取代基的脱离和重排,从而引入所需的功能基团。
结论:Hoffman反应是一种重要的有机合成反应,通过底物中氨基取代基的脱离和重排,可以合成各种氨基酸、醇胺和其他功能性化合物。
霍夫曼降解

霍夫曼降解1. 3-Aminopicolinic Acid and its Derivatives.Aqueous sodium hypobromite (from bromine, 56 g., and ice-cold 15% sodium hydroxide solution, 350 ml.) was added to a solution of quinolinimide 7 (50 g.) in ice-cold 10% sodium hydroxide solution (1L.). The mixture was keptat room temperature for an hour and then at 85" for a further hour ; after cooling, the pH was brought to 5 with 50% sulphuric acid and the mixture kept at 2" for 48 hr. A small amount of 2-aminonicotinic acid was removed by filtration and the filtrate treated with copper acetate (20 g.) in hot water (400 ml.) containing acetic acid (10 ml.). The precipitated copper salt was collected by filtration, washed with water, and resuspended in water (400 ml.), and the suspension saturated with hydrogen sulphide ; copper sulphide was removed by filtration and the filtrate concentrated, 3-Aminopicolinic acid (26 g. ; 56%), m. p. 210", separated on cooling;a further crop (13 g, ; 28%) of less pure material could beobtained from the mother-liquor by evaporation to dryness.2.霍夫曼降级反应为什么必须在碱性条件,且先低后高、逐步升温呢?3、将6.3g(157.5mmol)NaOH,67mLH2O置于250mL三口瓶中,装上温度计和搅拌器。
有机化学 高占先(第二版)课后答案

有机化学(第二版)课后习题参考答案第一章绪论1-1扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB 拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4)极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9)亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
13-04 季铵碱的 Hoffmann 消除
(3)应用--测定胺的结构
未知胺
季铵盐
季铵碱
烯烃+叔胺
13-04 季铵碱的 Hoffmann 消除
(1)季铵碱的制备
季铵盐与强碱作用时,得到含有季铵碱的平衡混合物
常用湿的氧化银与季铵盐作用促进反应
13-04 季铵碱的 Hoffmann 消除
(2)季铵碱的性质------热分解
季铵碱加热到100-150℃会分解 ①若季铵碱的烃基上没有-H,加热时生成叔胺和醇
②若季铵碱的烃基上有-H,加热时生成叔胺和烯烃
13-04 季铵碱的 Hoffmann 消除
含-H季铵碱加热分解反应历程(双分子消除反应E2)13-Leabharlann 4 季铵碱的 Hoffmann 消除
季铵碱存在多个烃基反应时,-氢被消除的难易次序如下
霍夫曼(Hoffmann)消除:消除反应中含多种-H的季铵碱 主要产物为双键上烷基最少的烯烃
