苦味酸法测定血清肌酐
血清肌酐测定

血清肌酐测定(生化分析仪)(一)检测目的规范血清肌酐(cr)检测实验,确保检测结果的准确性和重复性。
(二)标本米集1.血肌酐测定一般可以采用血清或血浆。
血清应新鲜无溶血;如用血浆,主张用肝素抗凝血浆。
2.稳定性:在4C冰箱可保存3天,在25C以下可保存较长时间。
3.建议使用带分离胶的真空采m管,并及时分离血清。
(三)测定方法1.方法:两点法波长:490-510nm 温度:25C、30C或37C 比色杯光径:1cm 将Ri与R n按1:1混和均匀,配成工作液,工作液预先保温到测试温度。
2.原理:苦昧酸法。
在碱性溶液中,苦味酸与肌酐作用生成橘红色的苦味酸肌酐复合物,在505nm波长监测吸光度,吸光度的速率变化(△ A/ min)与肌酐浓度呈正比。
(五)校准1.校准物的准备与保存,严格按照购置说明执行。
2.校准频率:(1)新仪器设备在开始使用时。
(2)设备进行重要维护保养以及发生故障维修之后。
(3)试剂盒在仪器上28天后。
(4)试剂批号更改后。
(5)更换试剂厂家后。
(6)由室内质控结果决定。
(7)定期校准,可由实验室根据检测系统(仪器与试剂)的情况自行决定校准周期。
(六)质量控制1.质控品:质控品应选择稳定、瓶问差小、基质效应小的物质。
同时,因为是定量检测项目,所以应选择两个不同浓度水平的质控品,这样有利于在不同的医学决定性水平上监测方法的性能。
2.质控方法的选择。
备选的质控规则如下:1 2s(一个质控结果超出i 土 2SD为违背此规则,提示警告)。
13s(一个质控结果超过i 土3SD为违背此规则,提示失控,存在随机误差)。
22s(两个连续质控结果同时超过i 土2SD提示失控,存在系统误差)。
R4s(当同一批内高和低值之间差值超过 4SD提示失控,存在随机误差)。
4 1s(4个连续的质控结果落在i+I SD或i 一 1SD的同一侧,提示存在系统误差,需具体分析)。
10x(10 个连续的质控结果落在靶值的同一侧,提示存在系统误差,需具体分析)。
苦味酸法肌酐测定单点与多点定标的比较

过 率( G F R) 和残余 肾功能 ( R R F ) , 故测定 血清 肌酐浓度 较血 清 尿素浓度能准确地反 映肾小球 功能 , 因而血清 肌酐测定是
临床常规检测 。 肾功能指标之一 。准确测定血 清肌酐 的含量对 临床 肾脏疾病 的诊 断 、 疗效 观察 及预后判断都 有十分重要 的
意义 。
2 结 果
1 . 1 仪器与试剂 : O l y m p u s A U 6 4 0 ,原装奥林 帕斯多项定 标 液, 原装奥林 帕斯肌酐试剂盒 由奥林 帕斯 公司提供 。校 准品 :
单 点 定 标浓 度 为 2 3 3 I x mo l / L ;多 点 定标 的 6点 为 5 8 2 . 5 、
的产 生和排泄较稳定 , 能反映和评估 G F R和 R R F 。故测 定血
血清肌酐测定是 临床常规检测肾功能指标之一 。准确测定血 清肌酐的含量对临床肾脏疾病 的诊断 、疗效观察及预后判 断
清肌酐浓度较 血清尿素浓度能准确地 反映肾小球功能 。因而
通信作者 : 杨军 , E m a i l : 1 0 3 4 7 7 0 6 9 9 @q q . c o n l
4 3 6 . 8、 2 9 1 . 3、 1 4 5 . 6 、 7 2 . 8、 3 6 . 4 l a , mo l / L 。
使用 0 l y m p u s 原装试剂盒检测 3 组肌酐 高值 、中值 、 低 值样 本 , 单点定标与多点定标结 果如下 : 高值组单点较多点定 标 偏低 8 . 8 %, 中值组偏低 0 . 4 %, 低值组偏 高 1 . 7 %; 高值组 和 低值 组经统计 检验差异均有统计学意义( 尸 < 0 . 0 5 ) , 见表 1 。
血清肌酐苦味酸法测定

血清肌酐(Creatine)苦味酸法测定1.实验原理不去除蛋白的Jaffe碱性苦味酸连续监测比色法。
肌酐与苦味酸在碱性条件下形成橙红色复合物,在固定的时间内吸光度增加速率与样品中肌酐浓度呈正比。
肌酐+ 苦味酸肌酐苦味酸复合物2. 标本采集2.1 病人准备:早晨空腹采血(空腹12小时左右),静脉采血。
2.2 类型:血清,肝素血浆,尿液。
3. 标本存放:血清、血浆的稳定性:4~25℃保存可稳定7天;-20℃保存至少可稳定3个月。
尿液的稳定性:20~25℃保存可稳定2天;4~8℃保存可稳定6天;-20℃保存可稳定6个月对尿液用蒸馏水作1:49稀释后检测,结果乘50后报告。
4. 标本运输:常温条件下运输5. 标本拒收的标准:细菌污染的标本不能作测定。
6. 实验材料6.1 上海申能肌酐检测试剂盒(142 1717170 1 试剂1:6×64ml+试剂2:6×16ml)。
6.1.1 试剂组成:试剂1(R1):氢氧化钠0.16mol/L试剂2(R2):苦味酸 4.0mmol/L6.1.2 试剂准备:试剂为即用式。
6.1.3 试剂稳定性与贮存:试剂保存于2~25℃,若无污染,可稳定至失效期。
试剂不可冰冻。
6.1.4 变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。
6.1.5 注意事项:试剂1中含氢氧化钠。
请按以下条例处理:R36/38: 刺激眼睛和皮肤。
S26:如与眼睛接触应立即用大量水冲洗并请医生诊视。
S37/39:戴上手套并采取合适的眼/脸的防护。
S45:如发生事故或感觉不适立即请医生诊视。
试剂2中含苦味酸。
吸入、接触皮肤、吞咽将会中毒。
戴上手套并采取合适的眼/脸的防护。
如与皮肤接触应立即用聚乙二醇400(DAB8)或大量水冲洗。
如情况严重,立即请医生诊视。
使用实验室试剂应采取必要的预防。
6.2 校准品:使用DiaSys公司提供的TruCal U校准品对自动分析仪进行校准,具体参见生化检验校准品和质控品.SOP文件。
肌氨酸氧化酶法与碱性苦昧酸法测定血清肌酐的实验比对

肌氨酸氧化酶法与碱性苦昧酸法测定血清肌酐的实验比对[摘要] 目的评价肌氨酸氧化酶法(简称酶法)、碱性苦味酸法(简称苦味酸法)测定血清肌酐的可靠性。
方法分别采用两种方法测定血肌酐值进行精密度试验,并按美国临床实验室标准化委员会(NCCLS)EP9-A文件进行评估,将测定结果进行相关回归分析,计算两种方法间的偏倚。
结果酶法3个水平的定值质控血清CV日间%分别为3.77%、2.53%、1.23%;苦味酸法3个水平的定值质控血清CV日间%分别为5.23%、4.05%、2.46%。
两种方法测定的血清肌酐浓度,经组内、组间离群值检验后得线性回归方程:Y(苦味酸)=0.9772X(酶法)+5.1911,r2 = 0.9910。
两种方法间各有明显恒定偏倚。
结论苦味酸法特异性不高,易产生交叉污染,但成本低廉,操作简便;肌氨酸氧化酶法特异性高、线性范围宽,抗干扰能力强,是比较理想的方法。
【关键词】肌氨酸氧化酶法;碱性苦味酸法;肌酐1 材料与方法1.1材料与仪器试剂和校准品由浙江伊利康生物技术有限公司提供,定值质控血清由美国贝克曼一库尔特试剂公司提供。
血清样本均来自当日临床病人新鲜血清。
仪器:凯美雅S3600全自动生化分析仪,参数均按厂家要求设置。
1.2方法1.2.1精密度测定按NCCLS精密度评价方法[1],取低、中、高值3份定值质控血清,白天跟随样本作双份检测,连续20天,对结果作统计学分析。
1.2.2线性回归方程采用酶法和碱性苦味酸法分别测定50例患者血清肌酐含量,两种方法测定肌酐浓度经组内、组间离群值检验后得线性回归方程。
1.2.3结果偏倚估计根据酶法测定值分组:I组(0~94μmol/L)24例,Ⅱ组(95~800μmol/L)17例,Ⅲ组(801~1200μmol/L)9例。
2 结果2.1精密度结果见表1。
表1 日间精密度测定结果(单位:μmol/L ,n=20)2.2两种方法相关性方程为:Y(苦味酸)=0.9772X(酶法)+5.1911,r2 = 0.9910。
肌氨酸氧化酶法和苦味酸法测定血清肌酐的比较

肌氨酸氧化酶法和苦味酸法测定血清肌酐的比较【关键词】肌酐;肌氨酸氧化酶法;苦味酸法;方式比较[摘要]目的:评测肌氨酸氧化酶法和苦味酸法测定血清样本肌酐(Cre)的偏倚。
方式:依据美国国家临床实验室标准协会EP9A 文件,天天取临床样本8份,别离用两种方式测定血清样本Cre含量,共测定5 d,记录结果,去除离群点,计算线性回归方程和相关系数,进行偏倚估量。
结果:在测定患者新鲜非黄疸血清样本Cre时,肌氨酸氧化酶法和苦味酸法测定结果的预期相对偏倚在Cre浓度<100 μmol/L时,两种方式的预期偏倚≤-1.8%,酶法的测定结果低于苦味酸法; 当Cre浓度>200 μmol/L时,两种方式的预期偏倚≥11.9%,酶法的测定结果高于苦味酸法,当Cre浓度>500 μmol/L时,两种方式的预期偏倚≥20.1%。
结论:随血清Cre浓度上升,酶法和苦味酸法的测定结果的预期偏倚增加,临床实验室在换用不同仪器或试剂时必需对肌酐测定的不同方式成立不同的参考值范围。
[关键词]肌酐;肌氨酸氧化酶法;苦味酸法;方式比较Measurement of Serum Creatinine by Sarcosine Oxidase and Picric Acid MethodsComparison between Two MethodsAbstract: Objective To determine the bias between two methods for measuring the serum creatinine (CRE). Methods Following the protocol described by the NCCL approved guideline (method comparison and bias estimation using patient samples),40 patient samples were analyzed in 5 operating days, each sample was analyzed in duplicate by both enzymatic assay and Jaffe kinetic assay. The duplicates were assessed for each method within the same run. The coefficient of correlation was calculated and the bias between the two methods was calculated accordingly. Results The bias between the enzymatic assay and Jaffe kinetic assay were -1.8% at 100 μmol/L, 11.9% at 200 μmol/L and 20.1% at 500 μmol/L for creatinine. Conclusion The bias between the two methods increases as the concentration of the serum creatinine increases. New reference range for creatinine should be established when new instrument or new reagent is applied.Key words:Creatinine;Sarcosine oxidase;Picric acid methods; Method comparison血中的肌酐(Cre)由外源性和内源性两类组成,要紧由肾小球滤过,肾小管大体不重吸收。
实验九血清肌酐的测定(碱性苦味酸法)

教研室 生物化学 课程 内容 生物化学检验 专业 07 检验 指导教师 徐燕 学时 3 实验九 含氮化合物测定 ——两点法测定肌酐
教材 生化检验实验 教学 目的 和要 求 教学 内容 教学 重点 难点 教学 媒体 复习 旧课
掌握两点法测定肌酐的原理及操作方法。 两点法测定肌酐 重点:掌握两点法测定肌酐的原理及操作方法。 难点:把握反应时间。 学生动手操作为主,课堂演示为辅 肌酐测定方法 (一)原理 肌酐与碱性苦味酸试剂反应生成黄红色络合物,在 500nm 处选择线性较好 的两个吸光度值,与通过同样处理的标准液比较,即可计算出血中肌酐含量。 肌酐 + 苦味酸 (二)操作步骤 加入物(ml) 碱性 橙红色复合物 标准管 1.5 0.1 0.1 样品管 1.5
教 学 要 求
试剂空白 1.5
教 学 过 程
讲 授 新 课
工作试剂 标准液 样品
混匀,37 水浴 9min,用试剂空白调零,分光光度计 520nm 处,读取标准管 和样品管的吸光度。 (三)结果与分析
CT控制很重要,10℃以下会抑制 Jaffe 反应,温度升高可使碱 性苦味酸溶液显色加深。 课堂 两点法测定肌酐为什么要严格把握反应时间? 提问 课堂 两点法测定肌酐的原理及操作方法。 小节 布置 简述两点法测定肌酐的注意事项。 作业 参考 钱士匀主编.临床生物化学和生物化学检验实验指导.第 2 版,北京:人民卫生 书目 出版社,2003
苦味酸法测定血清肌酐

肌酐(CRE)是人体内肌酸代谢的最终产物, 由肾排出,少部分来自食物,大部分在体内生成, 血肌酐的浓度主要取决于GFR。 血肌酐的测定对中晚期肾疾病临床意义较大。 肌酐测定方法有化学法和酶法。 酶法主要有三种类型:肌氨酸氧化酶法、肌酐氨基 水解酶法和肌酐亚氨基水解酶法。
先读取S1、U1吸光度,5分钟后再读取S2、U2吸光度。
六、计算
血清肌酐(mmol/L)= ΔAU/ΔAS×133μmol/L
参考区间:男性:62-115μ mol/L 女性:53-97μ mol/L
七、注意事项
1.血标本无溶血,应及时处理。 2.工作液开盖混合后,应置2-8度避光保存,稳定期3天。
八、临床意义
肌酐经肾小球滤过后不被肾小管重吸收,通过肾 小管排泄。只有当GFR下降到正常的1/3时,Scr才明 显上升,是反眏GFR减退的后期指标。 增高:见于各种原因引起的肾小球滤过功能减退:各种 肾病,急慢性肾衰竭、重度充血性心力衰竭、心肌炎 等。 降低:见于尿崩症、进行性肌萎缩、白血病、贫血等
一、实验目的
1.掌握血清肌酐的测定原理和方法。 2. 了解肌酐测定的参考范围及临床意义。
二、实验原理
在碱性条件下,血清中的肌酐(Cre) 苦味酸反应,生成橘红色的苦味酸肌酐复合物 。检测505nm波长处吸光度的变化,可知被测 血清中的肌酐的浓度。其反应式如下:
肌酐+碱性苦味酸 OH红- 色物质
血清
——
—— —— 0.15 0.15
133μ mol/L肌酐
标准应用液
——
0.15 0.15 —— ——
生理盐水
0.15
—— —— —— ——
R1
0.75
实验十二去蛋白苦味酸法测定血清肌酐 - 副本

过程
结果计算: 肌酐浓度(umol/L)= (△A测定 / △A标准) ×C标准 (其中△A为吸光度的变化,C标准为标准品浓度。)
注意事项
必须严格的控制反应的时间,以尽量避免 快速或慢速反应假肌酐物质的干扰 溶血产生的红细胞内非特异性物质将干扰 反应 胆红素可引起负偏差。某些全自动生化分 析仪,能设置空白速率参数,能去除胆红 素负干扰。
评价
特异性 血浆中的蛋白质和糖、丙酮、维生素C、丙酮 酸、乙酰乙酸等均能与碱性苦味酸发生非特异 性反应,反应速度稍慢。红细胞中这类物质最 多,约有60%,血浆或血清约20%,尿约5%, 故血清和血浆需制备无蛋白滤液后测定。 回收率 受无蛋白滤液PH影响,滤液PH在3~4.5时,回 收率为85%~90%,PH在2以下时,回收率为 100% 线性范围 肌酐含量在1320μmol/L以内线性良好
速率法和苦味酸法测定 血清肌酐比较
速率法原理
肌酐在肌酸脒基水解酶作用下生成肌氨酸, 肌氨酸在肌氨酸氧化酶作用下生成过氧化氢, 后者在过氧化氢酶作用下与4-氨基安替比林、 ESPAS反应生成呈色产物紫红色醌亚胺,在 546nm处引起吸光度增高,通过监测546nm 处吸光度值的上升来测定肌酐的浓度
过程
试剂
步骤
结果计算
注意事项
源自碱性肌酐苦味酸复合物的最大吸光度在485nm, 过量苦味酸离子存在于反应液中,在波长低于 500nm时会产生明显的吸收。 反应温度以15~25℃为宜,10℃以下,会抑制 Jaffe反应。温度升高,可使碱性苦味酸溶液显色 增深,但测定管较标准管更为明显。 呈色后标准管色泽稳定,但测定管吸光度随时 间延长而增加,可能与血标本中存在的非特异 性物质有关,故在加入显色剂后30分钟内比色 为宜。 苦味酸一定要纯,否则要纯化。若含有杂质, 则使试剂空白吸光度增加而影响测定结果。
肌酐生化方法学

肌酐生化方法学
肌酐(Creatinine)是一种由肌肉代谢产生的废物,通常通过肾脏排出体外。
肌酐生化方法学是用于测定血清或血浆中肌酐浓度的实验方法。
1. 碱性苦味酸法:这是最常用的肌酐测定方法之一。
在碱性条件下,肌酐与苦味酸反应生成红色化合物,通过比色法或分光光度法测定其吸光度,进而计算肌酐浓度。
2. 酶法:利用肌酐酶将肌酐转化为氨和肌酸,然后通过测定氨或肌酸的生成量来计算肌酐浓度。
酶法具有较好的特异性和准确性。
3. 干化学法:使用纸片或试纸等干式试剂,通过颜色变化或比色法来测定肌酐浓度。
这种方法通常用于快速检测,但准确性可能稍低。
4. 高效液相色谱法(HPLC):这是一种分离和分析化合物的技术,可以用于肌酐的定量测定。
HPLC 法具有高分辨率和准确性,但设备和操作相对复杂。
5. 质谱法:利用质谱仪对肌酐进行分析,通过检测肌酐的特定离子或碎片来确定其浓度。
质谱法具有高灵敏度和准确性,但设备昂贵。
在选择肌酐生化方法时,需要考虑实验要求、设备条件和准确性等因素。
不同方法可能在灵敏度、特异性、操作简便性和成本等方面有所差异,因此应根据具体情况进行选择。
无论使用哪种方法,都应遵循标准操作程序,并进行质量控制以确保结果的准确性和可靠性。
临床血清肌酐测定方法、羟苯磺酸钙药物作用及血肌酐测值干扰影响和要点总结

临床血清肌酐测定方法、羟苯磺酸钙药物作用及血肌酐测值干扰影响和要点总结血清肌酐测定方法血清肌酐是评价肾小球滤过功能的重要指标,其检测方法主要有苦味酸法和肌氨酸氧化酶法。
苦味酸法会受到维生素C、丙酮酸、丙酮、乙酰乙酸、葡萄糖、蛋白质、胆红素等多种物质的干扰,不适宜用于黄疸、溶血等情况下患者的血清肌酐测定,特异性较差。
酶法与苦味酸法相比,具有样本量小、速度快、特异性高等优点,使用酶法代替苦味酸法血清肌酐测定。
羟苯磺酸钙羟苯磺酸钙,化学名为2,5-二羟基苯磺酸钙,是广泛应用于临床微血管保护剂,用于治疗糖尿病视网膜病变,具有抑制视网膜微动脉瘤形成和减轻出血渗出等作用。
适应证包括慢性肾功能不全、慢性静脉功能不全、色素沉着性紫癜性皮肤病、白内障、肝脏缺血-再灌注损伤、阻塞性黄疸等。
保护血管药理机制主要体现在以下两个方面: ① 羟苯磺酸钙可增加微血管壁阻力,降低其病理性高通透性,减少出血与渗出;② 羟苯磺酸钙降低血液黏稠度,抑制血小板活化与聚集,防止血栓形成引起血管狭窄或堵塞。
羟苯磺酸钙对酶法检测肌酐干扰当羟苯磺酸钙浓度大于2 μg/ml 时,羟苯磺酸钙浓度越高,对血清肌酐水平负性干扰则越明显。
羟苯磺酸钙干扰血肌酐测值肌酐在肌酐酶的催化作用下生成肌酸,肌酸在酶催化作用下水解生成尿素和肌氨酸,其中肌氨酸经肌氨酸氧化酶催化生成甲醛、甘氨酸、过氧化氢等。
过氧化氢、4-氨基安替比林和2,4,6-三溴-3-羟基苯甲酸在过氧化物酶催化下反应生成可以进行比色反应的紫红色化合物醌亚胺。
羟苯磺酸钙对酶法检测血清肌酐存在干扰,对苦味酸法检测血清肌酐干扰。
使用苦味酸法检测肌酐时,羟苯磺酸钙浓度在 64 μg /ml 以上也不会对结果产生明显干扰,羟苯磺酸钙对苦味酸法检测肌酐基本没有干扰。
要点总结开具血清肌酐检查时,可备注标明患者正在使用羟苯磺酸钙,用于提示在必要时可选择苦味酸法进行重复、多次检测,以提高血清肌酐结果测定的准确性。
苦味酸法测肌酐实验报告

苦味酸法测肌酐实验报告实验目的:通过苦味酸法测定尿液中肌酐的含量,了解肾功能的状况。
实验原理:苦味酸法是利用肌酐与苦味酸在酸性条件下发生化学反应,生成苦味酸肌酐,其红色产物具有可见吸收波长,利用分光光度计测定其吸光度,从而计算出尿液中肌酐的含量。
实验仪器和试剂:分光光度计、离心机、量筒、离心管、试管、吸管、移液枪、苦味酸试剂盒等。
实验步骤:1.收集早晨首次排尿的尿液样本,并进行标号。
2.将尿液离心5分钟,分离出上清液并转移到干净的试管中。
3. 使用移液枪分别取出1ml上清液,分装到两个试管中。
4.分别向两个试管中加入适量的苦味酸试剂,摇匀混合。
5.置于室温下反应15分钟。
6.使用分光光度计设置红色滤光片,将两个试管的吸光度读数记录下来。
7.根据标准曲线,计算出两个试管中肌酐的浓度。
8.比较两个试管中肌酐的浓度,并结合标准值,评估肾功能的状况。
实验结果:样本A:吸光度为0.2样本B:吸光度为0.4实验数据处理:根据标准曲线,对应吸光度0.2的肌酐浓度为10mg/dL对应吸光度0.4的肌酐浓度为20mg/dL。
样本A的肌酐浓度为10mg/dL样本B的肌酐浓度为20mg/dL。
实验结论:根据实验结果,可以得出样本B的肌酐浓度高于样本A,说明样本B 中的肌酐含量较高。
根据肌酐浓度判断,样本A的肾功能正常,而样本B 的肾功能可能存在问题。
进一步的分析还需要参考其他临床指标来评估。
实验注意事项:1.实验中使用的尿液样本需要新鲜、干净。
2.操作过程中避免交叉污染,使用吸管和试管时要小心。
3.实验中的试剂使用前需要根据说明书正确稀释。
4.操作过程中要注意安全,避免试剂溅入眼睛或皮肤。
5.所有仪器和试剂使用完毕后要进行清洗,保持实验环境整洁。
实验改进:1.在实验过程中可以增加对照组,使用已知肌酐浓度的尿液样本,以验证实验结果的准确性。
2.可以进行多次实验重复检测,以提高结果的可靠性。
3.对实验过程中的操作细节和操作顺序进行反复检查和核实,确保实验的精确性和可重复性。
Roche P模块 肌酐(苦味酸)说明书

质控: 质控使用“订单信息”中列出的材料。 可添加其他适用的质控品。 血清/血浆 使用上面列出的未稀释血清质控材料进行 质控。 可添加其他适用的质控品。 尿液 使用上面列出的 Precinorm PUC 和 Precipath PUC 进行质控。 可添加其他适用的质控品。 应根据各实验室的具体要求采用适合的质 控间隔和限值。检测值应在设定的范围 内。若质控值在设定范围外,各实验室应 采取相应措施。 按可用的政府规章和地方法规进行质控。
稀释液 (NaCl)
6µL 144µL
2µL 180µL
10µL 115µL
cobas c 111 系统-检测设定
血清、血浆和尿液应用参数
测定模式
吸光度
Abs.计算模式
动态
反应方向
上升
波长 A/B
512/583 nm
计算结果 第一次/最后一次 21/26
血清/血浆
补偿
-18µmol/L (-0.2mg/dL)
波长(副/主) 反应方向
单位
试剂移液 R1 R3
样本 样本容量
正常 减少 增加
10µL 10µL 10µL
速率法 A
10/27-37-15-23 (STAT 4/12-19)
570/505nm
上升
µmol/L (mg/dL,mmol/L)
稀释 样本稀释
样本
30µL
样本
样本稀释
样本容量
样本
稀释液 (NaCl)
正常
10µL 6µL 144µL
减少
10µL 2µL 180µL
增加
10µL 10µL 115µL
cobas c 311 系统-检测设定 血清和血浆应用参数
肌酐测定试剂盒(苦味酸法)产品技术要求zsbk0

肌酐测定试剂盒(苦味酸法)适用范围:本产品用于体外定量测定人血清中肌酐的浓度。
1.1包装规格液体型试剂1(R1):100mL×1,试剂2(R2):100mL×1,校准品:2mL×1。
1.2主要组成成分试剂1(R1)液体:氢氧化钠 0.32mol/L试剂2(R2)液体:苦味酸 35mmol/L校准品液体:水溶液基质(1个浓度)肌酐校准品定值范围100μmol/L~150μmol/L(每批定值,详见值单) 2.1 外观试剂盒中各组件的外观应满足:2.1.1试剂1(R1)应为无色透明溶液,无杂质、无絮状物,外包装完整无破损。
2.1.2试剂2(R2)应为橘黄色透明溶液,无杂质、无絮状物,外包装完整无破损。
2.1.3校准品应为无色透明溶液,无杂质、无絮状物,外包装完整无破损。
2.2 净含量液体试剂净含量应不少于标示值。
2.3 试剂空白吸光度在波长505nm(480nm~520nm)(光径1cm)处,试剂空白吸光度(A)应≤0.350,试剂空白吸光度变化率(△A/min)应≤0.035。
2.4准确度测定GBW09174,测定结果的相对偏差应不超过±10%。
2.5分析灵敏度对应于浓度为100μmol/L的肌酐所产生的吸光度差值(△A)应在0.011~0.070的范围内。
2.6重复性重复测试高、中、低浓度样本,变异系数(CV)应≤5%。
2.7批间差测试同一样本,批间差(R)应≤5%。
2.8线性范围在[22,880]μmol/L范围内,线性相关系数(r)应≥0.990;在(80,880]μmol/L范围内,线性相对偏差应不超过±10%;在[22,80]μmol/L范围内,线性绝对偏差应不超过±8μmol/L。
2.9试剂稳定性2.9.1效期稳定性原包装的试剂盒在2℃~8℃避光贮存,有效期为16个月。
试剂有效期满后3个月以内,试剂性能应符合2.1、2.3、2.4、2.5、2.6、2.8 的要求。
肌酐(CRE)测定试剂盒(苦味酸法)产品技术要求lideman

肌酐(CRE)测定试剂盒(苦味酸法) 适用范围:本产品用于体外定量测定人血清中肌酐的含量。
1.1包装规格试剂1(R1):2×80mL、试剂2(R2):2×80mL;试剂1(R1):3×60mL、试剂2(R2):3×60mL;试剂1(R1):2×40mL、试剂2(R2):2×40mL;试剂1(R1):2×80mL、试剂2(R2):2×16mL;试剂1(R1):2×60mL、试剂2(R2):2×20mL;试剂1(R1):4×60mL、试剂2(R2):1×60mL;试剂1(R1):1×10mL、试剂2(R2):1×10mL;试剂1(R1):1×60mL、试剂2(R2):1×60mL;试剂1(R1):2×30mL、试剂2(R2):2×30mL;试剂1(R1):3×61mL、试剂2(R2):3×61mL。
校准品(选配):1×3mL。
1.2主要组成成分1.2.1试剂组成表1 试剂组成1.2.2校准品的组成:单水平液体校准品,在水基质中添加肌酐(纯度:大于95%)。
定值范围:(50~300)μmol/L。
注:校准品浓度具有批特异性,具体浓度见标签。
2.1 外观液体双试剂:试剂1(R1)为无色澄清液体,试剂2(R2)为桔黄色澄清液体。
校准品:无色至浅黄色澄清液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 空白吸光度在37℃、(505nm±10%)范围内的波长、1cm光径条件下,试剂空白吸光度应<0.3 ABS。
2.4 分析灵敏度浓度为132.6μmol/L时,吸光度变化范围应在(0.004~0.02)ABS之间。
2.5 线性在(0,2210]μmol/L线性范围内,线性相关系数r2≥0.995。
酶法与苦味酸法检测血清肌酐的相关性
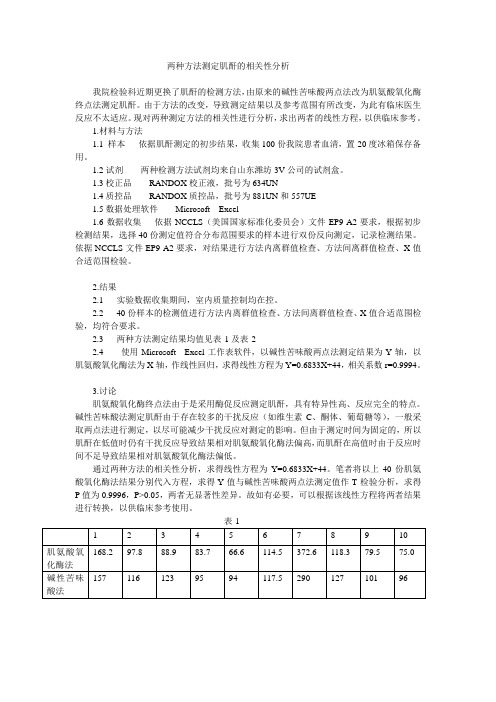
我院检验科近期更换了肌酐的检测方法,由原来的碱性苦味酸两点法改为肌氨酸氧化酶 终点法测定肌酐。由于方法的改变,导致测定结果以及参考范围有所改变,为此有临床医生 反应不太适应。现对两种测定方法的相关性进行分析,求出两者的线性方程,以供临床参考。
1.材料与方法 1.1 样本 依据肌酐测定的初步结果,收集 100 份我院患者血清,置-20 度冰箱保存备 用。 1.2 试剂 两种检测方法试剂均来自山东潍坊 3V 公司的试剂盒。 1.3 校正品 RANDOX 校正液,批号为 634UN 1.4 质控品 RANDOX 质控品,批号为 881UN 和 557UE 1.5 数据处理软件 Microsoft Excel 1.6 数据收集 依据 NCCLS(美国国家标准化委员会)文件 EP9-A2 要求,根据初步 检测结果,选择 40 份测定值符合分布范围要求的样本进行双份反向测定,记录检测结果。 依据 NCCLS 文件 EP9-A2 要求,对结果进行方法内离群值检查、方法间离群值检查、X 值 合适范围检验。
25 229.5
307 205
34 371.7
35 586.5
289 434.5
16
17
18
1165.0 1247.3 1020
853 887.5 753.5
26 228.5
27 210.0
28 528.3
200.5 188.5 391.5
36
37
38
489.4 103.8 70.9
373.5 115 83.5
间不足导致结果相对肌氨酸氧化酶法偏低。
通过两种方法的相关性分析,求得线性方程为 Y=0.6833X+44。笔者将以上 40 份肌氨 酸氧化酶法结果分别代入方程,求得 Y 值与碱性苦味酸两点法测定值作 T 检验分析,求得 P 值为 0.9996,P>0.05,两者无显著性差异。故如有必要,可以根据该线性方程将两者结果 进行转换,以供临床参考使用。
血清肌酐苦味酸法测定

血清肌酐(Creatine)苦味酸法测定1.实验原理不去除蛋白的Jaffe碱性苦味酸连续监测比色法。
肌酐与苦味酸在碱性条件下形成橙红色复合物,在固定的时间内吸光度增加速率与样品中肌酐浓度呈正比。
肌酐+ 苦味酸肌酐苦味酸复合物2. 标本采集2.1 病人准备:早晨空腹采血(空腹12小时左右),静脉采血。
2.2 类型:血清,肝素血浆,尿液。
3. 标本存放:血清、血浆的稳定性:4~25℃保存可稳定7天;-20℃保存至少可稳定3个月。
尿液的稳定性:20~25℃保存可稳定2天;4~8℃保存可稳定6天;-20℃保存可稳定6个月对尿液用蒸馏水作1:49稀释后检测,结果乘50后报告。
4. 标本运输:常温条件下运输5. 标本拒收的标准:细菌污染的标本不能作测定。
6. 实验材料6.1 上海申能肌酐检测试剂盒(142 1717170 1 试剂1:6×64ml+试剂2:6×16ml)。
6.1.1 试剂组成:试剂1(R1):氢氧化钠0.16mol/L试剂2(R2):苦味酸 4.0mmol/L6.1.2 试剂准备:试剂为即用式。
6.1.3 试剂稳定性与贮存:试剂保存于2~25℃,若无污染,可稳定至失效期。
试剂不可冰冻。
6.1.4 变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。
6.1.5 注意事项:试剂1中含氢氧化钠。
请按以下条例处理:R36/38: 刺激眼睛和皮肤。
S26:如与眼睛接触应立即用大量水冲洗并请医生诊视。
S37/39:戴上手套并采取合适的眼/脸的防护。
S45:如发生事故或感觉不适立即请医生诊视。
试剂2中含苦味酸。
吸入、接触皮肤、吞咽将会中毒。
戴上手套并采取合适的眼/脸的防护。
如与皮肤接触应立即用聚乙二醇400(DAB8)或大量水冲洗。
如情况严重,立即请医生诊视。
使用实验室试剂应采取必要的预防。
6.2 校准品:使用DiaSys公司提供的TruCal U校准品对自动分析仪进行校准,具体参见生化检验校准品和质控品.SOP文件。
苦味酸速率法肌酐测定的线性范围及其临床应用评价

苦味酸速率法肌酐测定的线性范围及其临床应用评价摘要目的观察分析苦味酸速率法肌酐测定的线性范围。
方法使用低、高值定值血清,配制不同肌酐浓度的标本,进行测定。
结果肌酐浓度在66.0~512.0 μmol/L范围内检测,线性方程:Y=0.8571X+22.953,相关系数r=0.9973。
结论苦味酸速率法肌酐测定线性范围较小,临床应用需采取措施加以校正。
关键词苦味酸速率法;肌酐测定;线性范围苦味酸速率法肌酐测定在临床实验室具有一定范围的应用,观察分析其测定的线性范围及相关问题,以期与使用者共同探讨。
1 资料与方法1. 1 实验标本英国产RANDOX(Human-Sera分析用人血清基质)定值冻干质量控制血清。
1. 2 仪器OLYMPUS(奥林帕斯)AU-2700全自动生化分析仪。
1. 3 试剂国内某品牌苦味酸速率法肌酐测定试剂盒,R1试剂:0.32 mol/L 氢氧化钠,R2试剂:53.0 mmol/L苦味酸,肌酐标准品浓度:132.6 μmol/L。
1. 4 方法取RANDOX(Human-Sera分析用人血清基质)定值冻干质量控制血清,同一批号的低值血清(肌酐定值浓度:66.0 μmol/L)3瓶,同一批号的高值血清(肌酐定值浓度:512.0 μmol/L)3瓶;严格依照产品说明书使用去离子纯净水5.00 ml,溶解各瓶冻干血清;待其充分溶解后,混匀,备用。
分别将备用的每瓶低、高值血清依照不同比例,进行配制,形成6个系列18份实验标本。
按照由低值向高值的顺序,上机进行肌酐实验检测,具体见表1。
其中,肌酐理论(定)值在400.0 μmol/L以上的标本,使用生理盐水稀释后,再次上机进行测定。
上机主要技术参数:标本30 μl,R1试剂150 μl R2试剂150 μl,主波长520 nm,次波长700 nm,反应时间13~15。
1. 5 统计要求a值在(1±0.10)范围内,相关系数r≥0.975,截距b小于检测上限浓度的5%。
血清肌酐(Crea)测定苦味酸法标准操作程序SOP文件

CALIBRATION METHOD [ LINEAR ]
POINT(3)[ 11 ]
CALIBRATION POINT [ 2 ]
POINT(4)[16]
SPAN POINT [ 2 ]
WAVELENGTH(PRIMARY)[505]
DUPLICATE LIMIT(%) [ 5 ]
11 临床意义
在肌代谢中,内源性肌酐来源于肌酸及肌酸磷酸盐,在肾脏功能正常时,肌酐通过肾小球滤过。在急性/慢性肾性疾病的诊断、治疗以及对肾透析的监测时,肌酐的测定很有意义。尿液中的肌酐浓度可以作为一些分解物(白蛋白、-淀粉酶)排泄的参考物。
1.1 肾病初期血肌酐通常不变,只有肾功能严重损伤时,血清肌酐才增加,故对晚期肾病患者临床意义较大。其值增高2.5~5倍,提示尿毒症可能,增高10倍常见于尿毒症。与血尿素氮同时测定,若二者均增高,示肾严重损害,若尿素氮高而肌酐不高,则常为肾外因素,如胃肠出血,尿路梗阻、高蛋白饮食等。
ABCD医院
生化实验室
文件编号:
ABCD-SOP-04-20
血清肌酐(Crea)测定苦味酸法
版序:ABCD
页码:第1页,共4页
1 测定方法
速率空白补偿法。
2 测定原理
肌酐+苦味酸碱性环境肌酐-苦味酸复合物
在碱性环境中,肌酐与苦味酸形成一种橘黄色的化合物,颜色的深浅与肌酐的浓度成正比。肌酐的测定应用速率空白补偿法,可以有效的清除胆红素的干扰。
SENSITIVITY LIMIT(HIGH) [ 1.1 ]
R.VOLUME(R1) [ 180 ]
S1 ABS(LOW) [ 0 ]
R.VOLUME(R2) [ 0 ]
S1 ABS(HIGH) [ 4000 ]
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
加入物(ml) 空白管
标准管
S1
S2
测定管(U) U1 U2
血清
——
—— —— 0.15 0.15
133μ mol/L肌酐
标准应用液
——
0.15 0.15 —— ——
生理盐水
0.15
—— —— —— ——
R1
0.75
0.75 0.75 0.75 0.75
R2
0.75
0.75 0.75 0.75 0.75
八、临床意义
肌酐经肾小球滤过后不被肾小管重吸收,通过肾 小管排泄。只有当GFR下降到正常的1/3时,Scr才明 显上升,是反眏GFR减退的后期指标。 增高:见于各种原因引起的肾小球滤过功能减退:各种 肾病,急慢性肾衰竭、重度充血性心力衰竭、心肌炎 等。 降低:见于尿崩症、进行性肌萎缩、白血病、贫血等
一、实验目的
1.掌握血清肌酐的测定原理和方法。 2. 了解肌酐测定的参考范围及临床意义。
二、实验原理
在碱性条件下,血清中的肌酐(Cre) 苦味酸反应,生成橘红色的苦味酸肌酐复合物。 检测505nm波长处吸光度的变化,可知被测血 清中的肌酐的浓度。其反应式如下:
肌酐+碱性苦味酸 OH- 红色物质
九、方法学评价
1.化学法:即苦味酸法,该法成本低廉,方法简便, 但试剂具毒性和腐蚀性。
2. 酶法:准确度和灵敏度高,采用两点速率法,适 合于自动生化分析仪检测。
SUCCESS
THANK YOU
2020/1/21
实验五 苦味酸法测定血清肌酐
肌酐(CRE)是人体内肌酸代谢的最终产物, 由肾排出,少部分来自食物,大部分在体内生成, 血肌酐的浓度主要取决于GFR。 血肌酐的测定对中晚期肾疾病临床意义较大。 肌酐测定方法有化学法和酶法。 酶法主要有三种类型:肌氨酸氧化酶法、肌酐氨基 水解酶法和肌酐亚氨基水解酶法。
三、器材
1、主要器具
试管与试管架
微量移液器
三用水浴箱
可见分光光度计
四、试剂
1.试剂:R1:氢氧化钠
R2:苦味酸
工作液:将R1与R2按1:1的比例混合面成。
2.肌酐标准应用液(133μmol/L)
SUCCESS
THANK YOU
2020/1/21
五、操作步骤
取试管5支,按下表操作
混匀后,37度水浴箱放置,2分钟后,波长505nm处,空白管调零,
先读取S1、U1吸光度,5分钟后再读取S2、U2吸光度。
六、计算
血清肌酐(mmol/L)= ΔAU/ΔAS×133μmol/L
参考区间:男性:62-115μmol/L 女性:53-97μmol/L
七、注意事项
1.血标本无溶血,应及时处理。 2.工作液开盖混合后,应置2-8度避光保存,稳定期3天 。
