肌钙蛋白T(cTnT)测定试剂盒(化学发光免疫分析法)产品技术要求taige
肌钙蛋白T(TnT)测定试剂(荧光免疫层析一步法)产品技术要求万孚

1.性能指标
1.1外观检查
外观应平整,标识清晰,各组分齐全,液体无渗漏。
1.2物理检查
膜条宽为 4.0±0.5 mm;液体移行速度应不低于10 mm/min。
1.3准确度
用参考品作为样本进行测定,其测定结果的相对偏差(B ias)不应超过±15%。
1.4最低检出限
应不大于0.03 ng/mL。
1.5线性
在0.03 ng/mL~10 ng/mL 的范围内,线性相关系数r≥0.9900。
1.6精密度
1.6.1批内精密度
用同一批号的试剂分别测定 2 个不同浓度的样本,其测定结果的变异系数(CV)应不大于15%。
1.6.2批间精密度
用三个不同批号的试剂分别测定2 个不同浓度的样本,其测定结果的变异系数(CV)应不大于15%。
超敏心肌肌钙蛋白T(hs-cTnT)测定试剂盒(磁微粒化学发光免疫分析法)产品技术要求puenguangde

超敏心肌肌钙蛋白T(hs-cTnT)测定试剂盒(磁微粒化学发光免疫分析法)适用范围:用于体外定量测定人血浆中心肌肌钙蛋白T(cTnT)的含量。
1.1包装规格50人份、100人份1.2 主要组成成分质控品质控范围批特异,详见标签。
2.1 外观2.1.1 试剂盒各组分应齐全、完整,液体无渗漏;2.1.2 中文包装标签应清晰,无磨损。
2.2 空白限空白限浓度应不高于0.005ng/mL。
2.3 线性在[0.005,10]ng/mL区间内,线性相关系数(r)应不低于0.99,且线性区间[0.005,2.0]ng/mL内,绝对偏差应不超过±0.3ng/mL;线性区间(2.0,10]ng/mL内,相对偏差应不超过±15%。
2.4 重复性分别用高、低浓度的样本各重复检测10次,其变异系数(CV)应不大于10%。
2.5 准确度用Human Cardiac Troponin Complex(NIST SRM2921)国际标准品作为样本进行检测,其测量结果的相对偏差应在±20%区间内。
2.6 分析特异性测定浓度均为1000ng/mL的心肌肌钙蛋白C、心肌肌钙蛋白I、骨骼肌肌钙蛋白I,测定结果应不高于0.005ng/mL。
2.7 溯源性根据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》及有关规定提供校准品的来源、赋值过程及测量不确定度等内容。
校准品溯源至美国国家标准与技术研究院(National Institute of Standards and Technology,NIST)的Human Cardiac Troponin Complex(SRM2921)。
2.8 质控品赋值有效性本试剂盒质控品的测定结果应在质控范围内。
2.9 批间差用3个批号的产品分别检测同一份样本,3批产品间的相对极差(R)应不大于15%。
2.10 稳定性试剂盒在(2~8)℃储存条件下的有效期为12个月,试剂盒在规定的条件下保存,取到效期后的试剂盒进行检测,检验结果应符合2.1、2.2、2.3、2.4、2.5、2.6的规定。
人的肌钙蛋白T(TNT)酶联免疫吸附测定试剂盒 说明书

Uscn Life Science Inc.Wuhan网址:电话:+862784259552传真:+862784259551E-mail:***************人的肌钙蛋白T(TnT)酶联免疫吸附测定试剂盒使用酶联免疫吸附测定试剂盒使用说明说明说明书书产品编号:E1820Hu规格:96T本试剂盒仅供体外研究使用,不用于临床诊断!预期应用本酶联免疫吸附测定试剂盒运用双抗体夹心ELISA 法定量测定人血清、血浆或其它相关生物液体中TnT 含量。
本试剂盒试剂盒未提供但需自备的设备及试剂未提供但需自备的设备及试剂1、450±10nm 滤光片的酶标仪(建议仪器使用前提前预热)2、单道和多道微量加液器及吸头3、稀释样品的EP 管4、蒸馏水或去离子水5、吸水纸6、盛放洗液的容器试剂盒的储存及有效期所有试剂均按试剂瓶标签上所示保存。
请注意,收到试剂盒后请尽快将标准品、检测溶液A 、检测溶液B 以及96孔板保存于-20。
开封后的酶标板要密封加干燥剂后保存于-20,避免潮湿。
有效期为6个月。
实验原理将TnT 抗体包被于96孔微孔板中,制成固相载体,向微孔中依次加入标准品和标本,其中的TnT 与连接于固相载体上的抗体结合,洗板之后加入生物素化的TnT 抗体,将未结合的生物素化抗体洗净后,加入HRP 标记的亲和素,再次彻底洗涤后加入底物(TMB)显色。
TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的TnT呈正相关。
用酶标仪在450nm波长下测定吸光度(值),计算样品浓度。
标本的采集与与保存标本的采集1、血清:将收集于血清分离管的全血标本在室温放置30分钟或4过夜,然后1000g离心20分钟,取上清即可检测,或将上清置于-20或-80保存,但应避免反复冻融。
2、血浆:用EDTA或肝素作为抗凝剂采集标本,并将标本在采集后的30分钟内于2-81000g离心15分钟,取上清即可检测,或将上清置于-20或-80保存,但应避免反复冻融。
肌钙蛋白I测定试剂盒技术要求

肌钙蛋白I测定试剂盒技术要求肌钙蛋白I(cTnI)是心肌细胞特异性的蛋白质,它的释放与心肌损伤和坏死相关。
因此,cTnI的测定对于心肌梗死、心肌炎等心脏疾病的诊断和监测至关重要。
肌钙蛋白I测定试剂盒是一种用于测量血液中cTnI浓度的试剂盒,其中包含了测量所需的试剂和标准品。
1.灵敏度:试剂盒应具备高灵敏度,能够检测到非常低浓度的cTnI。
因为心肌损伤时cTnI释放的浓度可能很低,所以试剂盒需要具备足够高的灵敏度来确保准确的测量结果。
2.特异性:试剂盒需要具备对cTnI的高特异性,即只能有效地识别和测定cTnI而不受其他物质的干扰。
这是为了避免假阳性和假阴性的发生,保证结果的准确性和可靠性。
3.精确性:试剂盒需要具备高精确度,能够提供稳定且一致的测量结果。
这要求试剂盒的反应性和稳定性非常好,不受其他因素的影响,如温度、储存时间等。
4.操作简便:试剂盒的操作应简单易行,不需要复杂的设备和专业人员。
推荐使用简化的步骤和标准化的操作流程,减少用户误操作的可能性。
5.储存和保质期:试剂盒的储存和保质期要求较长,能够在适应不同环境条件下保持试剂的稳定性和活性。
并且在试剂盒使用前后,可以通过储存和保质期的信息确定试剂盒的有效性。
6.经济实用:试剂盒的价格相对较低,并且具有良好的性价比,使其更易于普及和推广使用。
同时,试剂盒的包装也要方便用户使用,减少浪费和交叉污染。
7.文献支持:试剂盒需要具备一定的文献和临床数据支撑,能够证明其有效性和准确性。
此外,厂家还应提供技术支持和培训,以帮助用户正确操作和使用试剂盒。
总结起来,肌钙蛋白I测定试剂盒需要具备高灵敏度、高特异性、高精确性、操作简便、储存稳定、经济实用等特点,能够提供准确可靠的测量结果,为心脏疾病的诊断和监测提供有效工具。
同时,厂家还需要提供技术支持、培训和文献支持,以保证试剂盒的质量和用户的满意度。
高敏肌钙蛋白I测定试剂盒(化学发光免疫分析法)产品技术要求万孚

2性能指标
2.1外观
外观应符合如下要求:
a)磁珠包被物R1摇匀后应为棕褐色悬浊液;静止久后,棕褐色磁珠沉降于底部,上清液应为无色液体;酶标记物R2应为无色液体,无沉淀或絮状物;样本处理液R3应为无色液体;校准品应为外观均匀,成形完整,呈乳白色的冻干品,复溶后较清亮,无浑浊及沉淀;
b)试剂盒各组分应齐全、完整,液体无渗漏;
c)中文包装标签清晰,无磨损。
2.2准确度
将具有溯源性的两个正确度控制品进行检测,检测结果与标定浓度的相对偏差在±10% 范围内。
2.3空白限
空白限不大于0.006ng/mL;
2.4线性
试剂盒在0.01ng/mL~50 ng/mL 区间内,其相关系数(r)的绝对值不低于0.9900。
2.5重复性
变异系数CV≤8%。
2.6批间差
变异系数CV≤10%.
2.7分析特异性
测定浓度均为1000ng/mL 的心肌肌钙蛋白C、心肌肌钙蛋白T、骨骼肌肌钙蛋白I,交叉反应率应≤0.1%。
2.8校准品
2.8.1校准品准确度
测定校准品,C1,C2 测定结果的相对偏差在±10%范围内,C0 测定结果的绝对偏差的绝对值不高于0.006ng/mL。
2.8.2校准品瓶内均一性
校准品C1,C2 瓶内均一性≤8%,C0 的SD≤0.006ng/mL。
2.8.3校准品瓶间均一性
校准品C1,C2 瓶间均一性≤5%,C0 的SD≤0.006ng/mL。
心肌肌钙蛋白T(cTnT)测定试剂盒(电化学发光免疫分析法)产品技术要求lianzhongtaike
心肌肌钙蛋白T(cTnT)测定试剂盒(电化学发光免疫分析法)适用范围:本试剂盒用于体外定量测定人体血清样本中心肌肌钙蛋白T(cTnT)的含量。
1.1包装规格:100人份/盒、200人份/盒。
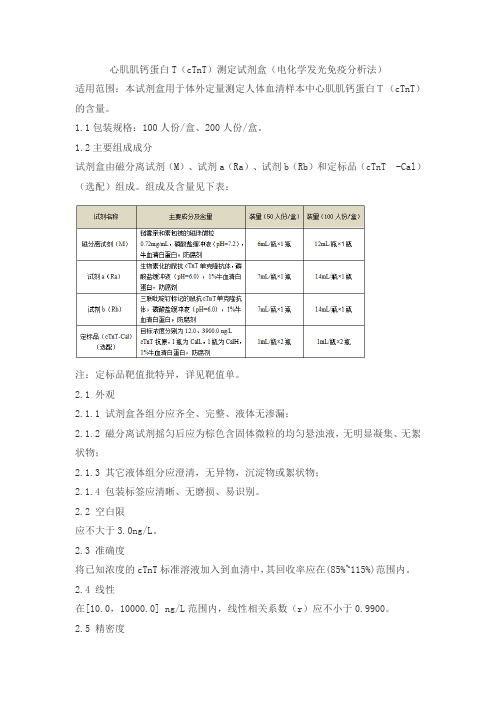
1.2主要组成成分试剂盒由磁分离试剂(M)、试剂a(Ra)、试剂b(Rb)和定标品(cTnT -Cal)(选配)组成。
组成及含量见下表:注:定标品靶值批特异,详见靶值单。
2.1 外观2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物;2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物;2.1.4 包装标签应清晰、无磨损、易识别。
2.2 空白限应不大于3.0ng/L。
2.3 准确度将已知浓度的cTnT标准溶液加入到血清中,其回收率应在(85%~115%)范围内。
2.4 线性在[10.0,10000.0] ng/L范围内,线性相关系数(r)应不小于0.9900。
2.5 精密度2.5.1 重复性在试剂盒的线性范围内,检测高、低两个水平的样品,检测结果的变异系数(CV)应不大于8%。
2.5.2 批间差在试剂盒的线性范围内,用3个批号试剂盒分别检测高、低两个水平的样品,检测结果的变异系数(CV)应不大于15%。
2.6 效期末稳定性本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。
2.7 溯源性依据GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求提供心肌肌钙蛋白T(cTnT)定标品的来源、赋值过程以及测量不确定度等内容,定标品溯源到企业工作校准品。
TNT

肌钙蛋白T用途:用免疫学方法定量测定人血清或血浆中的肌钙蛋白T含量。
电化学发光免疫测定试剂,适用于罗氏Elecsys1010、2010和E170(Elecsys模块)免疫测定分析仪。
概述:心肌来源的肌钙蛋白T(cTnT,分子量39.7kD)是心肌损伤特异的、灵敏的标志。
在急性心肌梗死(AMI)发病后3-4小时,血清cTnT含量升高,并可持续14天之久。
检测血清cTnT对心肌缺血性损伤,如AMI和心肌炎的诊断,以及监测不稳定型心绞痛的病程和危险性评价均有重要意义。
在30%肾功能衰竭的病人血清中,cTnT可升高。
临床资料表明:该类病人患继发性心血管并发症的危险性升高。
Elecsys肌钙蛋白T采用两种心肌特异的单克隆抗体。
用重组人cTnT作为参考标准品,为第3代TnT测试。
原理:采用双抗体夹心法,整个过程18分钟完成。
・ 第1步:15ul标本、生物素化的抗TnT单克隆抗体和钌(Ru)标记的抗TnT单抗混匀,形成夹心复合物。
・ 第2步:加入链霉亲和素包被的微粒,让上述形成的复合物通过生物素与链霉亲和素间的反应结合到微粒上。
・ 第3步:反应混和液吸到测量池中,微粒通过磁铁吸附到电极上,未结合的物质被清洗液洗去,电极加电压后产生化学发光,通过光电倍增管进行测定。
・检测结果由机器自动从标准曲线上查出。
此曲线由仪器通过2点定标校正,由从试剂条形码扫描入仪器的原版标准曲线而得。
试剂:M:链霉亲和素包被的微粒(透明瓶盖),1瓶,6.5ml。
粒子浓度0.72mg/ml,生物素结合能力 470ng生物素/ml粒子。
含防腐剂。
R1:生物素化的抗TnT单克隆抗体(灰盖),1瓶,10ml。
浓度1.5mg/l,磷酸缓冲液0.1mol/l,pH6.0。
含防腐剂。
R2:Ru(bpy)32+标记的抗TnT单克隆抗体(黑盖),1瓶,10ml。
浓度1.2mg/l,磷酸缓冲液0.1mol/l,pH6.0。
含防腐剂。
储存和稳定性:存放在2-8 度,切莫倒置。
超敏肌钙蛋白I测定试剂盒产品技术要求新产业

超敏肌钙蛋白I测定试剂盒产品技术要求新产业1.试剂盒成分:试剂盒应包含超敏肌钙蛋白I检测试剂、质控品、稀释缓冲液等试剂。
2.检测原理:该试剂盒基于化学发光免疫分析法,测定血液中的超敏肌钙蛋白I浓度。
该方法利用特异性抗体与超敏肌钙蛋白I结合,产生荧光信号,通过测定荧光信号的强度来确定样品中超敏肌钙蛋白I的浓度。
3. 灵敏度:试剂盒应具有高灵敏度,能够在低浓度范围内准确测定超敏肌钙蛋白I的浓度。
通常,灵敏度应在1 ng/mL以下。
4.精密度:试剂盒应具有良好的精密度,能够在同一实验条件下反复测定,结果应具有较低的变异性。
精密度可通过重复测定一组质控品来评估。
5.线性范围:试剂盒应具有宽线性范围,能够测定不同浓度范围内的超敏肌钙蛋白I。
一般来说,线性范围应当覆盖从低浓度到高浓度的所有可能浓度。
6.特异性:试剂盒应具有良好的特异性,能够与超敏肌钙蛋白I结合,而不与其他相关蛋白结合。
特异性可以通过与其他蛋白进行交叉反应的实验来评估。
7.储存条件:试剂盒的储存条件应符合通常的实验室要求,通常需要在2-8°C下储存,避免冻结。
8.使用方便性:试剂盒应具有使用方便、操作简单的特点,能够被广泛的临床实验室使用。
试剂盒应提供详细的操作指南,并且包含所有必要的试剂和耗材。
9.技术支持:试剂盒的生产商应提供有效的技术支持,包括现场指导、问题解答和技术培训等。
同时,试剂盒应附带一份完整的说明书,包含使用步骤、注意事项和结果解释等内容。
超敏肌钙蛋白I测定试剂盒的技术要求是确保其在临床实验室中准确、可靠地测定血液中超敏肌钙蛋白I浓度的关键。
通过满足这些技术要求,可以提高心肌梗死的早期诊断和预后评估的准确性,为临床医生提供更好的诊断和治疗决策依据。
肌钙蛋白T测定试剂盒产品技术要求万孚

肌钙蛋白T测定试剂盒产品技术要求万孚1.产品简介:肌钙蛋白T测定试剂盒是一种高灵敏度、高特异性的试剂盒,用于检测肌钙蛋白T水平。
该试剂盒通过化学发光免疫分析法,利用特异性的抗体与肌钙蛋白T结合,生成免疫复合物,进而产生化学发光信号,通过光度计测量信号强度,从而确定样本中肌钙蛋白T的浓度。
2.抗体:该试剂盒中所使用的抗体应为高亲和力、高特异性的肌钙蛋白T抗体。
抗体应经过充分的验证,并能与肌钙蛋白T特异性结合,不与其他相关物质发生非特异性反应。
3.校准品:试剂盒应包含不同浓度的校准品,用于构建标准曲线。
校准品应经过准确测定其肌钙蛋白T浓度,并保证稳定性。
4.灵敏度:试剂盒应具有足够的灵敏度,能够检测出低至0.01 ng/mL的肌钙蛋白T浓度。
5.线性范围:试剂盒应具有宽广的线性范围,能够涵盖生理范围内的肌钙蛋白T浓度变化。
6.重复性:试剂盒应具有良好的重复性,同一样本的重复测定结果应具有较小的变异性。
7.特异性:试剂盒应具有良好的特异性,不受其他相关物质的干扰。
8.稳定性:试剂盒的试剂和材料应具有良好的稳定性,能够保持在规定的储存条件下长期保存。
9.操作简便性:试剂盒的操作步骤应简单明了,能够被普通实验室人员快速掌握并使用。
10.结果解读:试剂盒的结果应能够准确、直接地反映样本中肌钙蛋白T的浓度,并能够被普通实验室人员快速解读。
以上是对肌钙蛋白T测定试剂盒产品技术要求的详细描述,通过满足这些要求,可以确保该产品可以准确、可靠地测定肌钙蛋白T水平,从而在临床诊断和研究中发挥重要作用。
心肌肌钙蛋白I测定试剂盒(荧光免疫层析法)产品技术要求zhongjianantai

心肌肌钙蛋白I测定试剂盒(荧光免疫层析法)
适用范围:本试剂盒用于体外定量检测人血清、血浆或全血样本中心肌肌钙蛋白I(cTnI)的含量。
1.1包装规格:20人份/盒,40人份/盒。
1.2主要组成:
表1 试剂盒产品组成表
2.1 物理检查
2.1.1 外观
外观平整,材料附着牢固,内容齐全,试剂无杂质,外包装完整无破损,标签清晰可辨。
2.1.2 膜条宽度
膜条宽度应满足4.0mm±0.2mm。
2.1.3 液体移行速度
液体移行速度应不低于10mm/min。
2.1.4 样本稀释液
样本稀释液的净含量应不少于标示值,且其pH值为7.0±0.2。
2.2准确度
试剂盒的回收率在85%~115%之间。
2.3线性
在[0.2,50]ng/mL范围内,线性相关系数(r)应不低于0.990。
2.4 重复性
分别测定高、低两个浓度的样本,变异系数(CV)应不高于10.0%。
2.5 批间差
用三个不同批号试剂盒分别测定高、低两个浓度的样本,三个批号试剂盒之间的批间变异系数应不高于15.0%。
2.6 空白限
试剂盒空白限应不大于0.1ng/mL。
2.7校准信息溯源性
校准信息所用工作校准品根据GB/T 21415-2008 《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的规定,溯源至工作校准品,工作校准品通过已上市产品进行赋值。
2.8 稳定性
试剂盒在规定的条件下保存至有效期末,取到效期后两个月内的试剂盒,检测2.2、2.3、2.4、2.6项,结果应符合要求。
心肌标志物6项质控品产品技术要求北京康彻思坦

心肌标志物6项质控品适用范围:本品适用于使用厦门万泰凯瑞生物技术有限公司的心肌肌钙蛋白T 测定试剂盒(化学发光微粒子免疫检测法)、N端脑钠肽前体测定试剂盒(化学发光微粒子免疫检测法)、超敏C反应蛋白测定试剂盒(化学发光微粒子免疫检测法)、心肌肌钙蛋白I测定试剂盒(化学发光微粒子免疫检测法)、肌红蛋白测定试剂盒(化学发光微粒子免疫检测法)和肌酸激酶同工酶测定试剂盒(化学发光微粒子免疫检测法)进行临床检测时的实验室内部质量控制。
1.1 包装规格水平1(复溶体积):1×2mL,10×2mL,30×2mL;水平2(复溶体积):1×2mL,10×2mL,30×2mL;水平3(复溶体积):1×2mL,10×2mL,30×2mL;全水平(复溶体积):水平1 1×2mL,水平2 1×2mL,水平3 1×2mL。
1.2 主要组成成分注:不同批次质控品不能混用;每批次质控品的质控范围见试剂盒内靶值单。
2.1外观试剂(盒)各组分应齐全、完整;标签应清晰,包装无破损。
冻干品应为疏松体,复溶后液体应澄清。
2.2质控品赋值有效性检测结果应在质控范围内。
2.3 均匀性2.3.1瓶间差瓶间变异系数应不高于15%。
2.3.2瓶内均匀性瓶内变异系数应不高于10%。
2.4稳定性2.4.1复溶稳定性原包装质控品在开瓶完全复溶后,置于2℃~8℃条件下保存,放置24小时后进行检测,结果应符合2.2项的规定。
2.4.2 效期稳定性原包装质控品在2℃~8℃的条件下储存,有效期为36个月。
取效期末产品进行检测,结果应符合2.1、2.2、2.3.2项的规定。
人心肌特异性肌钙蛋白T(cTnT)elisa试剂盒使用说明书

人心肌特异性肌钙蛋白T(cTnT)elisa试剂盒使用说明书Elisa kit规格:48孔配置/96孔配置标准品稀释液:1.5ml×1瓶酶标试剂:3 ml×1瓶(48)/6 ml×1瓶(96)【人心肌特异性肌钙蛋白T(cTnT)elisa试剂盒】本试剂仅供研究使用计算:以标准物的浓度为横坐标,OD值为纵坐标,在坐标纸上绘出标准曲线,根据样品的OD值由标准曲线查出相应的浓度;再乘以稀释倍数;或用标准物的浓度与OD值计算出标准曲线的直线回归方程式,将样品的OD值代入方程式,计算出样品浓度,再乘以稀释倍数,即为样品的实际浓度。
试剂盒组成:封板膜:2片(48)/2片(96)说明书:1份密封袋:1个标准品:2700ng/L 0.5ml×1瓶0.5ml×1瓶2-8℃保存酶标包被板: 1×48 1×96 2-8℃保存样品稀释液: 3ml×1瓶 6 ml×1瓶2-8℃保存显色剂A液: 3ml×1瓶 6 ml×1瓶2-8℃保存显色剂B液: 3ml×1瓶 6 ml×1瓶2-8℃保存终止液: 3ml×1瓶6ml×1瓶2-8℃保存浓缩洗涤液:(20ml×20倍)×1瓶(20ml×30倍)×1瓶2-8℃保存实验原理:本试剂盒应用双抗体夹心法测定标本中人心肌特异性肌钙蛋白T(cTnT)水平。
用纯化的人心肌特异性肌钙蛋白T(cTnT)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入心肌特异性肌钙蛋白T(cTnT),再与HRP标记的心肌特异性肌钙蛋白T(cTnT)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的心肌特异性肌钙蛋白T(cTnT)呈正相关。
肌钙蛋白I(cTnI)测定试剂盒(化学发光免疫分析法)产品技术要求taige
肌钙蛋白I(cTnI)测定试剂盒(化学发光免疫分析法)适用范围:本试剂盒主要用于体外定量测定人血清中的肌钙蛋白I(cTnI)含量。
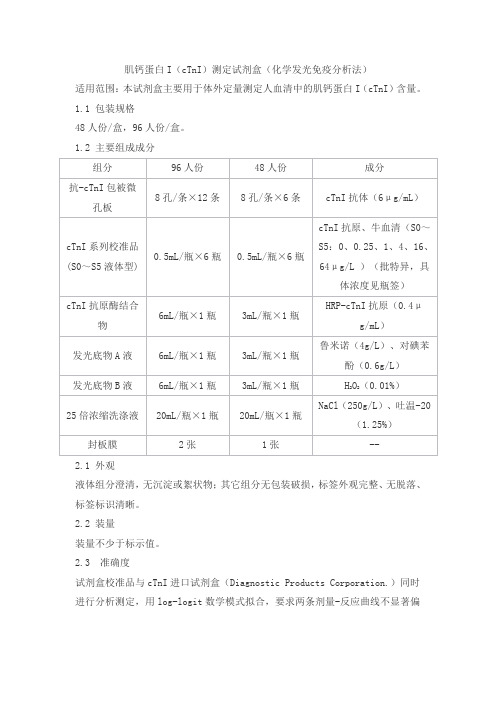
1.1 包装规格48人份/盒,96人份/盒。
1.2 主要组成成分2.1 外观液体组分澄清,无沉淀或絮状物;其它组分无包装破损,标签外观完整、无脱落、标签标识清晰。
2.2 装量装量不少于标示值。
2.3 准确度试剂盒校准品与cTnI进口试剂盒(Diagnostic Products Corporation.)同时进行分析测定,用log-logit数学模式拟合,要求两条剂量-反应曲线不显著偏离平行(t-检验);以cTnI进口试剂盒(Diagnostic Products Corporation.)为对照品,其回收率应在90.0%~110%范围内。
2.4 剂量-反应曲线线性相关系数在[0.25,64]μg/L范围内,用log-logit数学模式拟合,剂量-反应曲线相关系数(r)的绝对值应不小于0.9900。
2.5 精密度2.5.1 重复性以同批次试剂盒,高低两种浓度的质控血清平行测定10次,求其平均值和标准差(SD),批内精密度(CV%)=SD/平均值×100%,重复性(CV%)应不高于15.0%;2.5.2 批间差三种不同批次试剂盒,对同一样品进行重复测定10次,计算各组测定结果的平均值和标准差(SD),批间精密度(CV%)=SD/平均值×100%,批间差(CV%)应不高于20.0%。
2.6 最低检出量应不高于0.250μg/L。
2.7 质控血清测定值应在允许的范围之内。
2.8 特异性cTnI与肌红蛋白、肌钙蛋白T (cTnT)、肌酸激酶同工酶的交叉反应如下:2.9 稳定性2.9.1 热稳定性37℃放置3天,测定结果应符合上述2.1~2.7项要求。
2.9.2 效期稳定性成品试剂盒2~8℃存放6个月后,测定结果应符合上述2.1~2.7项要求。
2.10 校准品溯源性按照GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》要求,该校准品溯源至本公司内部工作校准品,通过与cTnI进口试剂盒(Diagnostic Products Corporation.)比对赋值。
肌钙蛋白 I(cTnI)测定试剂盒(胶乳免疫比浊法)说明书

肌钙蛋白I (cTnI)测定试剂盒(胶乳免疫比浊法)说明书【产品名称】肌钙蛋白I(cTnI)测定试剂盒(胶乳免疫比浊法)【包装规格】a)试剂1:1×15mL 试剂2:1×5mL b)试剂1:2×45mL 试剂2:2×15mL c)试剂1:4×60mL 试剂2:4×20mL d)试剂1:2×60mL 试剂2:2×20mL 【预期用途】用于体外定量测定人血清中肌钙蛋白I 的含量。
肌细胞受损时,肌钙蛋白I (cTnI )立即释放入血,在胸痛发生4-6h 后,血中cTnI 水平超过正常上限,12-24h 达高峰,可持续6~10天之久。
由于cTnI 可检出微小心肌损伤,是公认的快速诊断急性心肌梗死和急性冠脉综合症(ACS )[1]。
测定肌钙蛋白I 常用于心肌细胞受损、急性心肌梗死、急性冠脉综合症的辅助诊断。
【检验原理】样本与胶乳试剂在缓冲液中混合后,其中的肌钙蛋白Ⅰ与胶乳颗粒表面的抗体结合,使相邻的胶乳颗粒彼此交联,发生凝集反应产生浊度变化,该浊度变化与样本中的肌钙蛋白的量成正相关。
【主要组成成分】试剂1主要组分磷酸盐缓冲液30mmol/L聚乙二醇(PEG )0.5%表面活性剂及稳定剂适量试剂2主要组分磷酸盐缓冲液30mmol/L抗人肌钙蛋白(cTnI )抗体乳胶颗粒适量表面活性剂及稳定剂适量注:不同批号试剂盒中各组分未经试验不可互换。
【储存条件及有效期】1.试剂原包装在2~8℃储存,有效期为12个月,生产日期、有效期见标签。
2.开口后的试剂在仪器仓中(2~8℃)可稳定30天。
【适用仪器】艾威德AS-420/AS-660/AS-1200;日立HITACHI 7020型/7060型/7180型/7600型/LABOSPECT 008AS 型;贝克曼AU400/AU480/AU640/AU680/AU2700/AU5400/AU5800/AU5811/AU5821;佳能TBA-FX8/TBA-120FR /TBA-2000FR ;罗氏cobas 8000c 702/cobas 8000c 701/cobas 8000c 502;西门子SIEMENS ADVIA 1800/ADVIA 2400;雅培ABBOTT ARCHITECT c8000/ARCHITECT c16000/ARCHITECT ci8200;西森美康SYSMEX BM6010/C ;科华KHB 卓越310/卓越330/卓越400/卓越450/ZY-1200/ZY-1280;迪瑞CS-240/CS-T300/CS-300B/CS-380/CS-400A/CS-400B/CS-600A/CS-600B/CS-800A/CS-800B/CS-1200/CS-1200ISE/CS-1300B/CS-1400;迈瑞MINDRAY BS-220/BS-330/BS-350E/BS-380/BS-390/BS-400/BS-430/BS-600/BS-800/BS-2000M ;颐兰贝ES-200/ES-380/ES-480;赛诺迈德SUNMATIK-9050型;雷杜Chemray 420;英诺华D280;特康TC6010L ;锦瑞GS400;普康6066。
心肌肌钙蛋白I(cTnI)测定试剂盒(化学发光法)产品技术要求tongxin

心肌肌钙蛋白I(cTnI)测定试剂盒(化学发光法)适用范围:本试剂盒用于体外定量测定人血清或血浆中心肌肌钙蛋白I(cTnI)的含量。
分说明1.1 包装规格96人份/盒1.2 主要组成成分表1 主要组成成分备注:校准品溯源至美国国家标准与技术研究院(National Institute of Standards and Technology,NIST)颁布的有证标准参考物质(SRM 2921),校准品(A~F)目标浓度为0、0.5、1.4、4.0、18.0、45.0ng/ml。
2.1 外观组分齐全、完整,液体无渗漏,微孔板包装袋无破损、漏气现象;包装标签应清晰,易识别。
2.2 装量液体装量应不少于标示值。
2.3 准确度在剂量反应曲线检测范围内,用已知浓度的纯品(源自Hytest公司)做回收试验,其回收率应在85~115%范围内。
2.4 线性在线性范围[0.25,45]ng/ml内,剂量反应曲线相关系数(r)的绝对值应不低于0.9900。
2.5 空白限应不大于0.25ng/ml。
2.6 重复性同一次试验中分别重复检测浓度值为1.35±0.33ng/ml、18.83±3.78ng/ml样本10次,其变异系数(CV)应不大于10.0%。
2.7 批间差用3个批号的试剂盒检测浓度值为1.35±0.33ng/ml、18.83±3.78ng/ml样本,3个批号试剂盒之间的批间变异系数(CV)应不大于15.0%。
2.8 分析特异性测定浓度为1000ng/ml 心肌肌钙蛋白C(Cardiac Troponin C,cTnC),交叉反应率小于0.05%。
测定浓度为1000ng/ml 心肌肌钙蛋白T(Cardiac Troponin T,cTnT),交叉反应率小于0.05%。
测定浓度为1000ng/ml 骨骼肌肌钙蛋白I(Skeletal Troponin I,sTnI),交叉反应率小于0.05%。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
肌钙蛋白T(cTnT)测定试剂盒(化学发光免疫分析法)
适用范围:本试剂盒主要用于体外定量测定人血清中的肌钙蛋白T(cTnT)含量。
1.1 规格
48人份/盒,96人份/盒。
1.2 主要组成成分
2.1 外观
液体组分澄清,无沉淀或絮状物;其它组分无包装破损,标签外观完整、无脱落、标签标识清晰。
2.2 装量
装量不少于标示值。
2.3 准确性
回收率应在90.0%~110%范围内。
2.4 剂量-反应曲线线性相关系数
在[0.25,64]μg/L范围内,用log-logit数学模式拟合,剂量-反应曲线相关系数(r)的绝对值应不小于0.9900。
2.5 精密度
2.5.1 重复性(C.V%)应不高于15.0%;
2.5.2 批间差(C.V%)应不高于20.0%。
2.6 最低检出量
应不高于0.250μg/L。
2.7 质控血清测定值
应在允许的范围之内。
2.8 特异性
cTnT与肌红蛋白、cTnI、肌酸激酶同工酶的交叉反应如下:
2.9 稳定性
2.9.1 37℃放置3天,测定结果应符合上述2.1~2.7项要求。
2.9.2 成品试剂盒2~8℃存放6个月后,测定结果应符合上述2.1~2.7项要求。
2.10 校准品溯源性
按照GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》要求,该校准品溯源至本公司内部工作校准品,通过与湖南隆润达生物技术有限公司的cTnT试剂盒比对赋值。
