硼及其化合物的性质
高中化学竞赛-硼族元素
高中化学奥林匹克竞赛辅导硼族元素一、硼族元素简介硼族元素包括硼(B)、铝(Al)、镓(Ga)、铟(In)、铊(Tl),在周期表中处于第Ⅲ A族。
硼族元素的价电子构型为n s2n p1,除硼外其余元素均为金属元素,金属性随原子序数的增加而增强。
B的半径较小,失去三个电子非常困难,因此硼不能形成简单阳离子B3+,只能通过共用电子对形成共价化合物。
Al、Ga、In、Tl在水溶液中可以形成M3+。
因为惰性电子对效应,Tl3+具有强氧化性。
在硼族元素形成的共价分子中,中心原子最外层只有6个电子,未达到8电子的外层结构,属于缺电子化合物,它们具有一个空p轨道,可以接受孤对电子形成配位键,是强的路易斯酸。
硼族元素的性质二、硼及其化合物1.硼的单质硼的非金属单质以原子晶体形式存在。
单质硼有无定形硼和晶体硼两种,无定形硼为棕色粉末,晶体硼为黑灰色原子晶体。
晶体硼结构较为复杂,其晶体结构单元为12个硼原子组成的正二十面体。
它有20个等边三角形面,12个顶点,硼二十面体通过不同的连接方式形成各种硼的同素异形体。
晶体硼的化学活性较低,无定形硼较活泼。
常温下,硼能与F 2反应,高温下能与N 2、O 2、S 等非金属单质反应。
无定形硼可被热的浓硝酸、浓硫酸氧化成硼酸,也能与强碱作用放出氢气。
2B+N 22BN(与金刚石C 2互为等电子体,是原子晶体) B+3HNO 3(浓)B(OH)3+3NO 2↑2B+2NaOH+2H 2O2NaBO 2+3H 2↑(与Al 的性质相似)2.硼的氧化物及含氧酸硼最重要的氧化物是B 2O 3,熔融B 2O 3能溶解许多金属氧化物,形成具有特征颜色的偏硼酸盐,这个反应用于定性分析,称为硼珠实验:CuO+B 2O 3Cu(BO 2)2(蓝色) NiO+B 2O 3Ni(BO 2)2(绿色) B 2O 3的水化物为硼酸H 3BO 3或B(OH)3。
H 3BO 3是白色的片状晶体,具有片层结构,层和层 之间存在范德华力,容易发生滑动,其中氢键对其结构的形成具有支配的作用。
专题1-1:主族非金属-硼及其化合物(解析版)

系列一 主族非金属专题1 硼及其化合物一、硼及其化合物的性质(1)单质硼有晶态硼和无定形硼两种。
晶体硼呈黑灰色,以正二十面体为基本的结构单元,硬度与金刚石的硬度接近,其导电性差,但它的导电率却随着温度的升高而增大,从而示出与金属导体的不同,化学性质较为惰性。
无定型硼为棕色粉末,,化学性质较为活泼。
(2)常温下,硼稳定,仅与F 2反应,2B + 3F 2 2BF 3(3)点燃条件下,硼在空气中燃烧放出大量的热,4B + 3O 2 =====点燃2B 2O 3,该反应体现出硼氧键的键能很大,因此硼可以从许多稳定的氧化物如SiO 2,P 2O 5中取氧。
在炼钢过程中可以作为去氧剂,3SiO 2+4B =====△3Si+2B 2O 3。
(4)高温时,无定形硼可以同水蒸气作用生成硼酸,2B+6H 2O(g)=====△2B(OH)3+3H 2。
(5)高温时,硼也可以与N 2、S 、卤素等反应,2B + N 2=====高温2BN ,2B + 3S =====高温B 2S 3,2B + 3Cl 2=====高温BCl 3。
(6)硼不溶于非氧化性酸,仅被热的氧化性酸,如浓HNO 3、浓H 2SO 4和王水所氧化:B + 3HNO 3(浓)H 3BO 3 + 3NO 2↑;2B + 3H 2SO 4(浓)2H 3BO 3 + 3SO 2↑(7) 无定形硼与NaOH 有类似硅那样的反应:2B + 6NaOH2Na 3BO 3 + 3H 2↑ (8)可利用金属还原法制得单质硼(通常用Mg 或Al ):B 2O 3+3Mg =====△2B+3MgO 。
二、工业制取硼及其化合物的转化关系(1)转化关系(2)相应步骤涉及的反应①硼镁矿与烧碱溶液反应生成可溶于水的偏硼酸钠(NaBO 2)和Mg (OH )2:2MgO·B 2O 3+2NaOH +H 2O===2NaBO 2+2Mg (OH )2↓向偏硼酸钠溶液中通入CO 2使NaBO 2转化成硼砂:4NaBO 2+CO 2+10H 2O===Na 2B 4O 5(OH )4·8H 2O +Na 2CO 3 ②将硼砂与硫酸反应,得到硼酸:Na 2B 4O 5(OH )4·8H 2O +H 2SO 4===4H 3BO 3+Na 2SO 4+5H 2O③硼酸加热分解得到氧化硼:2H 3BO 3=====△B 2O 3+3H 2O④用镁或铝还原B 2O 3制得硼:B 2O 3+3Mg=====△3MgO +2B⑤硼和NaOH 溶液反应生成NaBO 2(或Na[B (OH )4])和H 2:2B +2NaOH +2H 2O===2NaBO 2+3H 2↑或2B+2NaOH +6H 2O===2Na[B (OH )4]+3H 2↑【习题1】硼酸(H 3BO 3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。
硼

元素序号:5元素符号:B元素名称:硼元素原子量:10.81元素类型:非金属发现人:戴维、盖吕萨克、泰纳发现年代:1808年发现过程:1808年,英国的戴维和法国的盖吕萨克、泰纳,用钾还原硼酸而制得硼。
元素描述:它是最外层少于4个电子的仅有的非金属元素。
其单质有无定形和结晶形两种。
前者呈棕黑色到黑色的粉末。
后者呈乌黑色到银灰色,并有金属光泽。
硬度与金刚石相近。
无定形的硼密度2.3克/厘米3,(25-27℃);晶形的硼密度2.31克/厘米3,熔点2300℃,沸点2550℃,化合价3。
在室温下无定形硼在空气中缓慢氧化,在800℃左右能自燃。
硼与盐酸或氢氟酸,即使长期煮沸,也不起作用。
它能被热浓硝酸和重铬酸钠与硫酸的混合物缓慢侵蚀和氧化。
过氧化氢和过硫酸铵也能缓慢氧化结晶硼。
上述试剂与无定形硼作用激烈。
与碱金属碳酸盐和氢氧化物混合物共熔时,所有各种形态的硼都被完全氧化。
氯、溴、氟与硼作用而形成相应的卤化硼。
约在600℃硼与硫激烈反应形成一种硫化硼的混合物。
硼在氮或氨气中加热到1000℃以上则形成氮化硼,温度在1800-2000℃是硼和氢仍不发生反应,硼和硅在2000℃以上反应生成硼化硅。
在高温时硼能与许多金属和金属氧化物反应,生成金属硼化物。
元素来源:制备方法有:硼的氧化物用活泼金属热还原;用氢还原硼的卤化物;用碳热还硼砂;电解熔融硼酸盐或其他含硼化合物;热分解硼的氢化合物上述方法所得初产品均应真空除气或控制卤化,才可制得高纯度的硼。
元素用途:由于硼在高温时特别活泼,因此被用来作冶金除气剂、锻铁的热处理、增加合金钢高温强固性,硼还用于原子反应堆和高温技术中。
棒状和条状硼钢在原子反应堆中广泛用作控制棒。
由于硼具有低密度、高强度和高熔点的性质,可用来制作导弹的火箭中所用的某些结构材料。
硼的化合物在农业、医药、玻璃工业等方面用途很广。
元素辅助资料:天然含硼的化合物硼砂(Na2B4O7·10H2O)早为古代医药学家所知悉。
硼元素的高考知识点归纳

硼元素的高考知识点归纳硼(B)是一种化学元素,其在化学元素周期表中的原子序数为5。
作为一种主组元素,硼具有许多重要的化学和物理特性,是高中化学学科中重要的一部分内容。
在高考中,对于硼元素的相关知识点的了解和掌握是非常必要的。
本文将对硼元素的高考知识点进行归纳和总结,希望能够帮助读者更好地掌握相关知识。
硼元素的基本性质硼元素是一种典型的准金属元素,具有特殊的物理和化学性质。
硼的原子结构为1s²2s²2p¹。
硼元素的原子半径较小,电负性较高,具有较强的电子亲和能力。
另外,硼元素具有良好的导电性和热导性能,并且对于中子有很好的吸收能力,因此在核能工业中也有一定的应用。
硼元素的同位素硼元素存在两种稳定同位素,分别为硼-10和硼-11。
硼-10的质量数为10,占自然界中硼元素的约20%;硼-11的质量数为11,占自然界中硼元素的约80%。
此外,硼元素还存在一种放射性同位素,即硼-8,其半衰期极短,仅为157 ns。
硼元素的化合物和反应硼元素与氧、氢等多种元素之间能够形成多种化合物。
其中,最重要的化合物之一是硼酸(H3BO3),硼酸是一种弱酸,可溶于水,并具有良好的缓冲和阻燃性能。
此外,硼元素还与碱金属和碱土金属等元素形成金属硼化物,如NaBH4和CaB6等。
这些金属硼化物在化工和材料领域有着广泛的应用。
硼元素的应用硼元素具有广泛的应用价值,在许多领域都有重要的应用。
首先,硼元素在玻璃和陶瓷工业中被用作增强剂和阻燃剂;其次,硼元素也被用于制备特种材料,如硼化硅陶瓷、金属硼化物等;此外,硼元素还在医学、农业和能源等领域有着广泛的应用。
例如,硼中子俘获治疗(BNCT)是一种新型的抗癌治疗方法,利用硼元素对中子的吸收作用,对癌细胞进行热杀伤。
硼元素的历史和发现硼元素的发现和研究历史可以追溯到公元前9世纪的古代文明。
在古代,人们就已经开始使用含硼矿石来制备颜料,如硼砂(硼酸钠)。
然而,直到1808年,英国化学家梅杰(Humphry Davy)才成功地从硼酸中分离出纯净的硼元素。
硼族元素及其化合物

硼族元素及其化合物
一、硼的性质
硼(Boron)是一种族IIIb的元素,在化学元素周期表中第五位,原子序数为5,原子质量为10.81、硼元素是一种半金属元素,具有金属质地,保持着类似硅的结构。
硼具有极强的抗氧化、加热稳定性、腐蚀性,使其有着优良的电性能,适用于电子设备中的导电成份,还拥有稳定的介电性能,是线路板制作的上佳材料。
二、硼的化合物
(1)氢氧化硼
氢氧化硼(H₂BO₃)是硼元素的最常见的化合物。
它是一种无色粉末状的晶体,熔点为350℃,有特殊的稀酸味,非常溶于水,但在碳酸钠、碳酸氢钠水溶液中极难溶解。
氢氧化硼是一种电解质,是用作电缆、电池和电磁浮动的主要材料。
(2)硼酸
硼酸(HBO₂)是硼的重要的化合物之一,其有机半氧化物的形式为
H₃BO₃,通常以白色粉末的形式存在,溶于水,不溶于二氯甲烷,拥有特殊的稀酸性味道。
硼酸有着广泛的应用,主要用作农药、洗涤剂、轻工业中制作消光剂、染料、防腐剂和焊条等。
(3)硼酸钠
硼酸钠(Na₂B₂O₄·2H₂O)是一种水溶性的硼酸盐,主要用作染料、洗涤剂、消光剂、增塑剂、绝缘剂、涂料等。
2020高中化学硼单质及其化合物
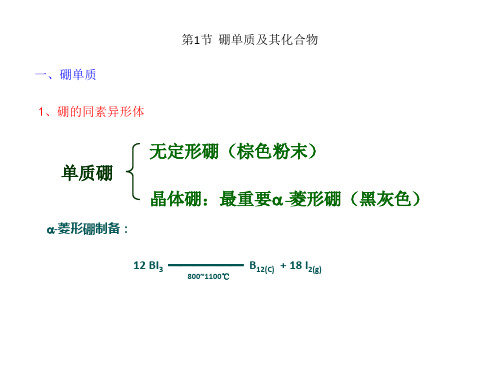
② 水解
火 焰 呈 现 绿 色
含 硼 化 合 物 燃 烧
B2H6 (g) 3H 2O(l) 2H 3BO 3 (s) 6H2 (g)
△ rHm -509.3kJ mol -1 水下火箭燃料
③ 加合反应
B2H6 CO 2[H 3B CO]
B2H6 2NH 3 [BH 2 (NH 3 )2 ] [BH 4 ] 2LiH B2H6 2LiBH 4 2NaH B2H6 2NaBH 4
2 个 B 与 4 个 H 共平面
B2H6分子存在“多中心缺电子键”,即3c-2e bond
Lipscomb(李普斯昆)硼烷成键五要素 1960年代初,Harvard University的William N. Lipscomb提出,1976年获
Nobel Prize in Chemistry.
1.末端 B-H: 2.正常 B-B 键
=
4e 。
4
3
顶部(编号:3、8、9)和底部(编号5、6、11)各3个5B
原子与上一层3个B原子或下一层3个B原子共形成6个正常B-
B 2C-2e键,共用去6×(2/2)e = 6e 。
9
与外部B12 成键共用去4e + 6e = 10 e
10
11
2 6 8
7
12
3、单质硼的化学性质
2 B + 3 F2 = 2 BF3 4 B + 3 O2 = 2 B2O3 2 B + 6 H2O(g) = 2 B(OH)3 + 3 H2↑ 2 B + N2 = 2 BN 2 B + 3 Cl2 = 2 BCl3 2 B + 3 S = B2S3 B + 3 HNO3(浓) = B(OH)3 + 3 NO2↑ 2 B + 3 H2SO4 (浓) = 2 B(OH)3 + 3 SO2↑
硼族元素及其化合物

无机化学
硼族元素及其化合物
氢氧化铝(Al(OH)3)是两性物质,既溶于酸又溶于碱: Al(OH)3+NaOH → NaAlO2+2H2O 2Al(OH)3+6HCl → 2AlCl3+3H2O 氢氧化铝的碱性比酸性略强,故铝盐都易水解。
硼族元素及其化合物
铝的卤化物从氟化物到碘化物,键型由离子键过渡 到共价键,这是因为F-、Cl-、Br-、I-的变形性依次增强, 其中最重要的是AlCl3。无水氯化铝是无色晶体,常温下 有挥发性,经测定其蒸发密度知它的分子式相当于Al2Cl6, 是共价化合物,为双聚分子。AlCl3溶于所有的有机溶剂, 在水中也易溶,因水解作用,其溶液显较强酸性,水解 过程中有碱式盐生成,其水解过程如下:
3. 铝的重要化合物
铝的重要化合物有氧化物、氢氧化物及卤化物。
氧化铝(Al2O3)是一种难熔的且不溶于水的白色粉末, 经灼烧后的氧化铝也不溶于酸。刚玉是存在于自然界中的 结晶氧化铝,其硬度仅次于金刚砂(碳化硅),是很好的 磨料。经特殊处理的氧化铝粉末,疏松多孔,具有很大的 相对表面积,有很强的吸附性能,叫做活性氧化铝,广泛 用作层析工作中的吸附剂。
无机化学
硼族元素及其化合物
硼族元素位于周期表中第ⅢA族,主 要包括硼(B)、铝(Al)、镓(Ga)、 铟(In)、铊(Tl)五种元素。
硼族元素及其化合物
一、 硼族元素通性
硼族元素的价电子层结构为ns2np1,其氧化数为+3 和+1,以+3为主要特征,在+3氧化态时完全是共价化合 物。由于它们价电子层的四个轨道中只有三个电子,价电 子数少于价电子层轨道数,故称为缺电子原子,所形成的 化合物被称为缺电子化合物。因此硼族元素有极强的接受 电子的能力,易形成聚合型分子(如Al2Cl6)和配位键化 合物。表8-19是硼族元素的一些基本性质。
硼及其化合物

硼族元素及其化合物约公元前200年,古埃及、罗马、巴比伦曾用硼沙制造玻璃和焊接黄金。
法国化学家盖·吕萨克用金属钾还原硼酸制得单质硼。
硼在地壳中的含量为0.001%。
硼为黑色或银灰色固体。
晶体硼为黑色,硬度仅次于金刚石,质地较脆。
硼还由于其缺电子性造成其氢化物中硼原子拥有异常高的配位数,使之成为所有元素氢化物中结构最复杂的。
单质硼为黑色或深棕色粉末,熔点2076℃。
沸点3927℃。
单质硼有多种同素异形体,无定形硼为棕色粉末,晶体硼呈灰黑色。
晶态硼较惰性,无定形硼则比较活泼。
单质硼的硬度近似于金刚石,有很高的电阻,但它的导电率却随着温度的升高而增大,高温时为良导体。
硼共有14种同位素,其中只有两个是稳定的。
室温时为弱导电体;高温时则为良导体。
在自然界中主要以硼酸和硼酸盐的形式存在。
晶体结构晶态单质硼有多种变体,它们都以B12正二十面体为基本的结构单元。
这个二十面体由12个B原子组成,20个接近等边三角形的棱面相交成30条棱边和12个角顶,每个角顶为一个B原子所占据。
由于B12二十面体的连接方式不同,键也不同,形成的硼晶体类型也不同。
其中最普通的一种为α-菱形硼。
α-菱形硼是由B12单元组成的层状结构,α-菱形硼晶体中既有普通的σ键,又有三中心两电子键。
许多B原子的成键电子在相当大的程度上是离域的,这样的晶体属于原子晶体,因此晶态单质硼的硬度大,熔点高,化学性质也不活泼。
在α-菱形硼晶格中,每个二十面体通过处在腰部的6个B原子以三中心两电子键与在同一平面内的相邻的6个二十面体连接起来(其中虚线三角形表示三中心两电子键,键距203pm)。
这种二十面体组成的片层,层面结合靠的是二十面体的上下各3 个B原子以6个正常的B-B共价键(即两中心两电子键,键长171pm)同上下两层的6个附近的二十面体相连接,3个在上一层,3个在下一层。
在硼的二十面体结构单元中,B12的36个电子是如下分配的:在二十面体内有13个分子轨道,用去26个电子;每个二十面体同上下相邻的6个二十面体形成6个两中心两电子共价键,用去了6个电子;在二十面体腰部的6个B原子与同平面上周围相邻的6个三中心两电子键,用去了6×2/3=4个电子,结果总电子数是26+6+4=36。
高中化学竞赛辅导无机化学15.1硼及其化合物知识点素材

第十五章 硼族元素Chapter 15 The Boron Family ElementsBoron (B) Aluminum (Al) Gallium (Ga) Indium (In)Thallium (Tl)Electron configuration :n s 2n p 1§15-1 硼及其化合物 Boron and its Compounds一、General Properties1.硼的化学性质与Si 有某些相似之处(对角线相似原则),通常硼呈现+3氧化态,负氧化态的情况很少。
硼与金属形成非化学计量的化合物(nonstoichiometric compounds ),M 4B 、M 2B 、MB 、M 3B 4、MB 2、MB 6等。
(1) B 2O 3与SiO 2都是固态酸性氧化物,Al 2O 3是两性,CO 2是气态酸性; (2) H 3BO 3与H 4SiO 4都是很好的酸; (3) 多硼酸盐与多硅酸盐结构相似;(4) 硼烷、硅烷可形成多种可燃性气态物质,而AlH 3是固态。
2.在自然界中,硼以硼砂(borax ):Na 2B 4O 7·10H 2O,四水硼砂(kernite ):Na 2B 4O 7·4H 2O,天然硼酸 ( sassolite ):H 3BO 3存在。
3.硼在自然界中丰度之所以低,是因为Li He B 734210105+→+n ,所以硼材料可作为核反应堆的减速剂和生物防护。
二、The Simple Substance1.Boron has several allotropic forms. 无定形硼为棕色粉末, The crystals ofboron are black. 高熔沸点(m.p. 2300℃,b.p. 2550℃)单质硼有多种复杂的晶体结构,其中最普通的一种是α - 菱形硼,其基本结构单元为正二十面体的对称几何构型,然后由B 12的这种二十面体的布起来组成六方晶系的α - 菱形硼。
硼化合物的化学性质和应用

硼化合物的配位性
硼化合物的配位能力: 硼原子的电负性较大, 容易与金属离子形成 配位键
硼化合物的配位数: 硼化合物通常具有较 高物的配位模式 :硼化合物的配位模 式多样,可以形成单 齿、双齿、三齿等多 种配位模式
硼化合物的配位稳定 性:硼化合物的配位 稳定性较高,可以稳 定存在于多种环境中
硼化合物在材料科学中的应用
硼合金:用于制造耐高温、 耐磨损的特种合金
硼酸盐:用于制造耐热、耐 腐蚀的特种玻璃和陶瓷
硼纤维:用于制造高强度、 高弹性的复合材料
硼烷:用于制造半导体器件 和太阳能电池
硼化合物在农业领域的应用
硼肥:硼是植物生 长必需的微量元素, 可以促进作物生长 和发育
硼酸:硼酸是一种 重要的农药,可以 防治病虫害
硼砂:硼砂是一种 重要的肥料,可以 提供植物所需的硼 元素
硼酸盐:硼酸盐是 一种重要的肥料, 可以提供植物所需 的硼元素,同时可 以调节土壤酸碱度
未来展望
硼化合物的新应用领域
硼化合物在医药领域的应用
硼化合物在环保领域的应用
硼化合物在电子领域的应用
硼化合物在能源领域的应用
硼化合物的发展趋势和挑战
要应用价值
硼化合物的酸碱性
硼酸:弱酸,可与 碱反应生成硼酸盐
硼酸盐:碱性,可 与酸反应生成硼酸
硼烷:碱性,可与 酸反应生成硼烷酸
硼氢化物:碱性, 可与酸反应生成硼 烷酸
硼化合物的氧化还原性
硼化合物的氧化性:硼酸、硼酸盐等具有较强的氧化性,可以氧化金属、有机物等 硼化合物的还原性:硼氢化物、硼烷等具有较强的还原性,可以还原金属氧化物、有机物等 氧化还原反应:硼化合物的氧化还原反应在化学实验和工业生产中具有重要应用 氧化还原平衡:硼化合物的氧化还原平衡在化学实验和工业生产中具有重要应用
知识点3 硼的化合物

第五章 p 区元素(一)第二节硼族元素5.2.3 硼的化合物硼的氢化物硼烷分类:BnH n+4 和 B n H n+6(少氢硼烷)(多氢硼烷)例: B2H6 B4H10乙硼烷丁硼烷有CH4,但无BH3最简单的硼烷:B2H6其结构并非如右图所示:HHBBHHH H硼烷的结构B:利用 sp3 杂化轨道,与氢形成三中心两电子键。
(氢桥)记作:HH B BHH HH要点:B的杂化方式,三中心两电子键、氢桥。
B4H10分子结构硼烷的性质① 自燃 高能燃料,剧毒(可与氰化氢和光气相比) 空气中允许的最高浓度 0.1 ppm O(g)3H (s)O B (g)3O (g)H B 232262+−→−+含硼化合物燃烧火焰呈现绿色② 水解(g)H 6(s)BO 2H O(l)3H (g)H B 233262+−→−+水下火箭燃料③ 配位反应 263B H 2CO 2[H B CO]+−−→←④ 加合反应4622NaBH H B 2NaH −→−+4622LiBH H B 2LiH −→−+⑤ 与卤素反应 6HCl (l)2BCl (g)6Cl (g)H B 3262+−→−+硼的含氧化合物①三氧化二硼 B2O3原子晶体:熔点460︒C无定形体:软化结构:一般以无定形的状态存在,很难形成晶体,但在高强度退火后也能结晶。
B2O3(无定形)= B2O3(晶体)△r Hθ= - 19.2 kJ·mol-1制备:性质:(1) 溶于水形成HBO2 或H3BO3(2) 能被碱金属及镁铝还原成单质硼(3) 与金属氧化物共熔形成具有特征颜色的玻璃状偏硼酸盐,用于鉴别金属离子。
(4) 与非金属氧化物反应P2O5 + B2O3 = 2 BPO4(两性性质)②硼酸 H3BO3结构:层状结构层内:B sp2杂化有氢键。
层间:范德华力。
∴似石墨,有解离性。
硼酸晶体的片层结构24723324 Na B O2HCl5H O4H BO Na SO++−−→+制备:R.T.微溶于水,T↗,溶解度↗,可用重结晶方法提纯。
硼的性质及用途

世上无难事,只要肯攀登
硼的性质及用途
硼属于非金属元素,但也具有金属性质。
硼的化学性质很活泼,在自然界中呈化合物存在,形成各种硼酸盐及一些含硼硅酸盐、硅铝酸盐矿物。
在高温下硼可以和氧、氮、碳、卤素等元素化合,生成相应的化合物,其中氮化硼、碳化硼在工业上有着特殊的用途。
硼及其化合物广泛地应用于化工、建材、轻工、冶金、纺织、机械、电子、航天、核工业和农业等部门。
在化学工业方面:硼矿是制取硼砂、硼酸和各种硼化物及元素硼的主要原料。
硼砂、硼酸具有去垢、漂白和防腐、消毒作用,用于肥皂、洗涤剂等日用化工和医药的生产上。
在建材和轻工业方面:玻璃和玻璃纤维中加入适量硼砂、硼酸或硼矿物,可提高产品的热稳定性,增加光泽和透明度,增强抗冲击和抗腐蚀性能,用于制造高质量的耐热硼硅酸玻璃、玻璃纤维、光学透镜、各种仪器、药剂、化学用器皿的特种玻璃、绝缘材料和玻璃钢,还用于制造搪瓷。
在冶金工业方面:硼主要用来冶炼硼钢,作合金钢的添加剂。
硼砂具有熔蚀金属氧化物的能力,可用作冶金助熔剂和金属焊接剂。
在机械工业方面:渗硼是一种化学热处理新工艺,它可以提高部件表面的硬度和抗氧化性能。
碳化硼的硬度高,耐热性强,可用来制造切削工具和研磨材料。
在航天工业方面:硼与氢、锂、铍的化合物,可用作高能喷气燃料;用硼与氮、碳、锆、钛的化合物制作的金属陶瓷,用于制造火箭喷嘴、燃烧室的内衬和真空高频电炉的绝缘材料。
在核工业方面:硼的同位素具有强的吸收中子能力,用于制造原子反应堆中的热中子吸收器和调节器,含硼2~4%的钢可作防射线的中子屏,塑料中加入。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
硼及其化合物的性质
1.硼
硼单质有晶体硼和无定形硼两种,晶体硼相当稳定,无定形硼比较活泼,能发生如下反应:
(1)高温下,与N 2、S 、X 2等单质反应,如2B +N 2=====高温2BN 。
(2)高温下同金属反应生成金属硼化物。
(3)赤热下,与水蒸气反应,2B +6H 2O(g)=====△2B(OH)3+3H 2。
(4)与热的浓硫酸或浓硝酸反应,2B +3H 2SO 4(浓)=====△2H 3BO 3+3SO 2↑,B +3HNO 3(浓)=====△
H 3BO 3+3NO 2↑。
2.硼酸(H 3BO 3)
(1)一元弱酸,H 3BO 3+H 2O H ++[B(OH)4]-。
(2)H 3BO 3受热时会逐渐脱水,首先生成偏硼酸(HBO 2),继续升温可进一步脱水生成四硼酸(H 2B 4O 7),更高温度时则转变为硼酸的酸酐(B 2O 3)。
3.硼氢化钠(NaBH 4)
硼氢化钠中的氢元素为-1价,具有还原性,故其可用作醛类、酮类和酰氯类的还原剂:。
4.硼砂(Na 2B 4O 7·10H 2O)
(1)制备:将偏硼酸钠溶于水形成较浓溶液,然后通入CO 2调节pH ,浓缩结晶分离出硼砂:4NaBO 2+CO 2+10H 2O===Na 2B 4O 7·10H 2O +Na 2CO 3。
(2)将硼砂溶于水,用硫酸溶液调节pH ,可析出溶解度小的硼酸晶体:Na 2B 4O 7+H 2SO 4+5H 2O===4H 3BO 3↓+Na 2SO 4。
1.NaBH 4与FeCl 3反应可制取纳米铁:2FeCl 3+6NaBH 4+18H 2O===2Fe +6NaCl +6H 3BO 3+21H 2↑,下列说法正确的是( )
A .该反应中氧化剂只有FeCl 3
B .NaBH 4的电子式为
C .NaBH 4不能与水发生反应
D .该反应中每生成1 mol Fe 转移电子3 mol
答案 B
解析 反应2FeCl 3+6NaBH 4+18H 2O===2Fe +6NaCl +6H 3BO 3+21H 2↑中,FeCl 3中的Fe 由+3价降低到0价,水中部分H 由+1价降低到0价,所以该反应中氧化剂为FeCl 3和H 2O ,A 项错误;NaBH 4由钠离子与BH -4构成,为离子化合物,则其电子式为,B 项正确;NaBH 4中H 为-1价,水中H 为+1价,两者发生归中反应可生成氢气,C 项错误;题述氧化还原反应中,化合价升高的只有NaBH 4中的H ,由-1价升高到0价,可据此判断电子转移数目,每生成1 mol Fe ,消耗3 mol NaBH 4,转移电子12 mol ,D 项错误。
2.按要求回答问题
(1)[2019·全国卷Ⅰ,26(3)]根据H 3BO 3的解离反应:H 3BO 3+H 2O
H ++B(OH)-4,K a =5.81×10-10,可判断H 3BO 3是________酸。
(2)[2015·全国卷Ⅰ, 27(1)(6)]写出Mg 2B 2O 5·H 2O 与硫酸反应的化学方程式:
________________________________________________________________________。
单质硼可用于生产具有优良抗冲击性能的硼钢。
以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程:________________________________________________________。
(3)[2015·安徽理综,27(2)]请配平化学方程式:______NaBO 2+______SiO 2+______Na +______H 2===____NaBH 4+______Na 2SiO 3。
(4)[2014·重庆理综,11(2)]NaBH 4是一种重要的储氢载体,能与水反应得到NaBO 2,且反应前后B 的化合价不变,该反应的化学方程式为___________________________________。
答案 (1)一元弱 (2)Mg 2B 2O 5·H 2O +2H 2SO 4=====△2MgSO 4+2H 3BO 3 2H 3BO 3=====△
B 2O 3+3H 2O 、B 2O 3+3Mg=====△2B +3MgO(点拨:硼酸先高温脱水生成B 2O 3,然后与镁发生置换反应) (3)1 2 4 2 1 2 (4)NaBH 4+2H 2O===NaBO 2+4H 2↑
3.硼、镁及其化合物在工农业生产中应用广泛。
已知硼镁矿的主要成分为Mg 2B 2O 5·H 2O ,硼砂的化学式为Na 2B 4O 7·10H 2O 。
一种利用硼镁矿制取金属镁及粗硼的工艺流程如图所示:
(1)写出硼元素在元素周期表中的位置:___________________________________________。
(2)将硼砂溶于水后,用硫酸调节溶液的pH ≈3.5以制取硼酸(H 3BO 3),该反应的离子方程式为___________________________________________________________________________。
(3)由MgCl2·6H2O制备MgCl2时,一定条件是_____________________________________。
(4)制得的粗硼在一定条件下反应生成BI3,BI3在一定条件下受热分解可以得到纯净的单质硼。
0.200 0 g粗硼制成的BI3完全分解,将生成的I2配制成100 mL碘水,量取10.00 mL碘水于锥形瓶中,向其中滴加几滴淀粉溶液,用0.300 0 mol·L-1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液18.00 mL。
(提示:I2+2S2O2-3===2I-+S4O2-6)滴定终点的现象为_______________________________,该粗硼样品的纯度为________%。
(5)H3BO3[也可写成B(OH)3]可以通过电解NaB(OH)4溶液的方法制备。
工作原理如图所示。
①b膜为__________(填“阴离子”或“阳离子”)交换膜,写出产品室发生反应的离子方程式:_______________________________________________________________,理论上每生成1 mol H3BO3,N室可生成________L(标准状况)气体。
②N室中,进口和出口的溶液浓度大小关系为a%______(填“>”或“<”)b%。
答案(1)第二周期ⅢA族(2)B4O2-7+2H++5H2O===4H3BO3↓(3)在HCl氛围中加热(4)滴加最后一滴Na2S2O3溶液,锥形瓶中溶液蓝色褪去,且半分钟内不恢复原色99(5)①阴离子H++B(OH)-4===H3BO3+H2O11.2②<
解析(3)因MgCl2在蒸干灼烧时会发生水解,其水解的化学方程式为MgCl2+2H2O Mg(OH)2+2HCl,所以为了防止氯化镁水解生成氢氧化镁,需要在HCl氛围中加热。
(4)消耗的Na2S2O3的物质的量为0.300 0 mol·L-1×0.018 L=0.005 4 mol,根据关系式:B~
BI3~3
2I2~3S2O
2-
3
得,n(B)=
1
3n(S2O
2-
3
)=0.001 8 mol,则该粗硼样品中B的物质的量=0.001
8 mol×100 mL
10.00 mL=0.018 mol,则硼的质量为11 g·mol
-1×0.018 mol=0.198 g,该粗硼样品中
硼的质量分数为0.198 g
0.200 0 g×100%=99%。
(5)①产品室可得到H3BO3的原因是M室的H
+穿过阳离子交换膜扩散至产品室,原料室的B(OH)-4穿过阴离子交换膜扩散至产品室,二者反应生成H3BO3,其离子方程式为H++B(OH)-4===H3BO3+H2O,所以b膜应为阴离子交换膜。
阴极的电解液为氢氧化钠溶液,所以N室的电极反应式为2H2O+2e-===H2↑+2OH-,生成1 mol H3BO3时,需要M室和原料室分别转入1 mol H+、1 mol B(OH)-4,则需转移1 mol e-,所以N室可生成0.5 mol氢气,其体积在标准状况下为11.2 L。
②N室溶液中氢氧根离子浓度增大,Na+从原料室通过阳离子交换膜进入N室,故N室进口溶液浓度比出口的小,即a%<b%。
