常见气体制备装置课件
2015届高考化学总复习 第八章 第四节常见气体的制备精讲课件

现象 说明
烧杯中有气泡产生,停 止微热,冷却后导气管 末端形成一段水柱,且 保持一段时间不下降
液面的高度差不变
针对训练
1.某研究性学习小组为合成 1丁醇,查阅资料得知一条 合成路线: 一定条件 CH CH===CH +CO+H ――――→
3 2 2
H2 CH3CH2CH2CHO――――→ Ni,△ CH3CH2CH2CH2OH。 浓H2SO4 CO↑+H O, CO 的制备原理: HCOOH――――→ 并设计 2 △ 出原料气的制备装置。
CuSO4
⑤品红溶液
解析:本题主要通过有机反应考查化学实验的基本方法
和技能。 (2) 考虑到CO 逸出时带有 HCOOH 和 H2O等杂质,因 此需先除去 HCOOH 等蒸气 ——c 中装 NaOH 溶液,再除去水 蒸气 ——d 中装浓 H2SO4 ; a 的作用是利于分液漏斗中液体的 顺利滴下——使压强恒定,b应起到安全瓶的作用——防倒吸。 (3)设计实验检验混合气体的各种成分时,要注意其他气体的 存在对此的干扰,先检验能干扰其他气体检验的气体并除去, 检验气体过程中不能产生未检验的气体。分析问题(3)中提供 的试剂的作用,可先检验水 —— 用④,再用⑤检验 SO2 并用 ①除去 SO2( 因 SO2 干扰丙烯的检验 ) ,然后,用③检验 CO2 , 最后用②检验丙烯,因KMnO4氧化丙烯时要生成CO2。
请填写下列空白: (1) 实验室现有锌粒、稀硝酸、稀盐酸、浓硫酸、 2丙醇,从 中选择合适的试剂制备氢气、丙烯,写出化学反应方程式:
______________________ , _____________________________
______________________________________________。 (2)若用以上装置制备干燥纯净的CO,装置中a和b的作用分别 是 __________________ 、 ________________ ; c 和 d 中盛装的 试剂分别是 ______________ , ________________ 。若用以上
常见气体制备装置归纳

C.CH4 D.NH3
5、设计了四种制备气体的方案:(1) 加热稀硫酸和乙
醇制备乙烯;(2) 加热稀盐酸和二氧化锰制备氯气;
(3)用稀硫酸和大理石制备二氧化碳;(4)用稀硝酸和
硫化亚铁制备硫化氢。不宜采用的方案有哪些?D
A.只有(1)和(2)
B.只有(1)和(3)
C.只有(3)和(4)
图2
图3
图4
图5
图6
gfr
5
(4)启普发生器及简易装置
图7
图8
图9 图10
图11 图12
gfr
6
3、固体+液体或液体+液体加热制气体
①反应容器:试管、烧瓶 ②加液容器:分液漏斗 ③注意事项:见图16、17
图13
图14
图1gf5r
图16
图17
7
二、气体净化装置: 根据净化剂的状态和条件选择
gfr
编 A中物 B中物 C中
号质
质 气体
有关化学方程式
(1) Na2SO3
浓硫酸 SO2
Na2SO3 +H2SO4(浓) ═ Na2SO4 +SO2↑+H2O
(2) Cu
浓硝酸 NO2
Cu + 4HNO3(浓) ═ Cu(NO3)2+ 2NO2↑+2H2O
(3) KMnO4 浓盐酸 Cl2
2KMnO4 + 16HCl ═ 2KCl g+fr 2MnCl2+5Cl2↑+ 8H2O
在瓶E和F之间连接装有干燥剂的装置
gfr
21
7根据下面实验图填空和回答问题:(1)烧瓶中所发生的主
要反应的化学方程式是 2H2SO4(浓)+2Na,Br+MnO2═MnSO4+Br2↑+
+2025届高三化学二轮复习+++第十章+第3讲+常见气体的制备++课件

化学试剂
A
Ca(OH)2+NH4Cl
B
MnO2+HCl(浓)
C
MnO2+KClO3
D
NaCl+H2SO4(浓)
制备的气体 NH3 Cl2 O2 HCl
1
2
3
4
返回目录
第3讲 常见气体的制备
[解析] 由题给装置可知,固体加热,排除B、D项;采用向上排空气法收集气体, NH3的密度比空气小,排除A项。
收集方法 排水法
向上排空气法
向下排空气法
收集的气体不 收集原理 与水反应且难
溶于水
收集的气体密度比空气 收集的气体密度比空气小,
大,且与空气密度相差 且与空气密度相差较大;与
较大;不与空气中的成 空气中的成分反应
分反应
收集装置
返回目录
第3讲 常见气体的制备
示例3 利用上述收集方法收集H2、SO2、O2、CH4、Cl2、CO2、NO、NO2、NH3。
返回目录
第3讲 常见气体的制备
课标要求
核心考点
能根据反应原理选取实 常见气体的制备
验装置制取物质
五年考情
2020 海 南 , T4 ; 2020 江 苏 , T5 ; 2019 海 南 , T17 ; 2019北京,T28
返回目录
第3讲 常见气体的制备
1.高考选择题中常结合气体除杂或收集、物质性质探究等考查气体 制备实验装置的选择、除杂试剂及装置的选择、收集装置的选择 等。综合实验题中常结合物质制备考查气体制备实验原理、气体 净化、尾气处理等,也会以文字叙述的形式考查仪器作用、实验 核心素养对接 方案评价等。 2.预计2025年高考仍会在选择题中考查常见气体制备、气体净化等 的装置选择。综合实验题中会结合气体的制备考查气体制备原 理、性质探究等
中学化学实验中常见气体制备装置归纳

九、尾气处理装置
根据多余气体的性质选择
• 溶液吸收 • 点燃 • 充袋法
易溶于水的要 用防倒吸装置
十.安全装置
通常设计化学实验时,为了保证操作人员的安 全,保障实验如期顺利进行,往往要设置安全装置; 一般在涉及气体的实验中最为常见。涉及到的安全 问题有:
防倒吸(防倒吸装置)、
防堵塞(检验堵塞、防压强过大)、
H2S,NH3,HBr,HI,C2H4 防堵塞(检验堵塞、防压强过大)、
(填“漏气”、“不漏气”或“不能确定”)
防污染(尾气吸收)等安全问题。
B中:—————————— D中:—————————
或“不能确定”)
,判断理由
。
这是一种仅适用于室温下随
3、固体+液体或液体+液体加热制气体 防污染(尾气吸收)等安全问题。
中学化学实验中常见气体制备装置归纳
一、气体发生装置:根据反应物状 态及反应条件选择发生装置
1、固体加热制气体
反应容器:试管
注意事项:粉末状固 体应在试管口放一团 棉花
2、固体+液体不加热制气体 ①反应容器:试管、烧瓶、广口瓶; ②加液容器:长颈漏斗、分液漏斗; ③注意事项:图4、6
图图图图图 23456
把导管伸入水槽的液 面下,手握住试管, 过会儿看到导管口有 气泡冒出,松开手导 管中形成一段水柱, 则证明气密性良好
连接好装置,关闭开关,从漏斗中倒水。漏斗 内外产生液面差,静止一段时间,液面差不变, 证明装置气密性完好。
关闭开关,将干燥管放入盛水的烧杯中, 若干燥管内的液面比烧杯中液面低,且过 一段时间后干燥管内液面保持不变,证明 装置气密性完好。
①关闭图A装置中的止水夹a后,从长颈漏斗
高三化学实验之气体制取复习ppt课件

C.加热氯酸钾和少量二氧化锰,制取氧气
D.加热氯化铵和消石灰混合物,制取氨气
练习精选
1、下列反应适用于实验室制备氧气的是 A
(1)高锰酸钾热分解2KMnO4═K2MnO4+O2+MnO2
(2)硝酸铵热分解2NH4NO3═4H2O+N2+O2
(3)过氧化氢催化分解2H2O2═H2O+O2
(4)二氧化氮热分解2NO2═2NO+O2
常见气体制备
思考:实验室如何制取纯净的氯气?
增加: 除杂装置
饱和食盐水 浓硫酸
思考:
气体的收集装置和净化装置 分别有几种类型?根据什么原 则选择有关装置?
二、收集装置
气体收集装置的设计原则: 根据气体的溶解性、密度及是否与
空气中的成分发生反应
装置类型 排水法 向上排气法 向下排气法
示意图
气体性质 难溶或微溶 密度大于空 密度小于空 于水的气体 气的气体 气的气体
高三化学实验之气体制取复习ppt课件
气体的制备
(一)考纲要求 (二)知识要点复习 (三)部分高考题 (四)随堂练习
今年高考考试说明要求
★ 掌握常见气体实验室制法,包括所用试剂、 仪器、反应原理和收集方法
该装置可用于制备O2、NH3和CH4
2KM 4K n2M O4n M O2n O O 2
湿润的 浓 氢氧 蓝色石 硫 化钠 蕊试纸 酸 溶液 变红
尾气处理:吸收、燃烧、收集
或用贮 气瓶
气体极易溶,防倒吸
安全瓶
洗气瓶的有关装置问题讨论
高考题选摘
从高考题型看,在第Ⅰ卷出现在选择题型 中的主要是基本实验的内容,从气体的制备, 离子的共存与识别,到物质的分离与提纯。
初中常见化学实验装置图归类

中学化学实验中常见气体制备装置归纳一、气体发生装置:根据反应物状态及反应条件选择发生装置气体固体、固体−→−+∆1()()。
在试管口处放一团棉花应注意事项:粉末状固体反应容器:试管21()()()643212、注意事项:见图分液漏斗;加液容器:长颈漏斗、锥形瓶;、广口瓶反应容器:试管、烧瓶气体液体、固体−→−+图2图3图4图5图6()启普发生器及改良4图7图8图9图10图11图12()()()17163213、注意事项:见图加液容器:分液漏斗反应容器:试管、烧瓶气体”液体气体”或“液体液体、“固体−→−+−→−+∆∆图 1图13 图14 图15 图16 图17 二、气体收集装置:根据气体的密度和溶解性选择、排空气法1图18 图19 图20 图21 图22 图23 、排水法2、贮气瓶3三、尾气处理装置:根据多余气体的性质选择气体、在水中溶解性不大的1图27、燃烧或袋装法2(图28、图29)气体:防倒吸。
、在水中溶解性很大的.3图26图24 图25图28 图29图30 图31图32图33图34图35图36图37图38四、气体净化装置:根据净化剂的状态和条件选择图39图40图41图42五、气体性质实验装置:根据反应物的状态及反应的条件选择、常温反应装置1 、加热反应装置2、冷却反应装置3六、排水量气装置:测量气体的体积相平。
中左短水位与右端水位中水相平,图中量器内的水位与水槽注意事项:图5250图43图44图45图46图47图48图49图50图51图52图53[例题]有下列实验装置如图8-1:示意图中A是简易的氢气发生器,B是大小适宜的圆底烧瓶,C是装有干燥剂的U形管,a是旋转活塞,D是装有还原铁粉的反应管,E是装有酚酞的试管。
实验前先检查实验装置的气密性。
实验开始时,先关闭活塞a,并取下烧瓶B;向A中加入一定量适当浓度的盐酸,产生氢气。
经必要的“操作”〔见问题(2)〕后,在导管的出口处点燃氢气,然后如图所示套上烧瓶B,塞紧瓶塞,氢气在烧瓶中继续燃烧,用酒精灯加热反应管D中的还原铁粉,待B中氢气的火焰熄灭后,打开活塞a,气体通过反应管D 进入试管E中,使酚酞试液呈红色。
常见气体制备装置归纳

图15
图16
图17
Hale Waihona Puke 二、气体净化装置: 气体净化装置: 根据净化剂的状态和条件选择
三、气体的干燥
液态干燥剂
装 置 常见干燥 剂 可干燥 气体 不可干燥 气体 洗气瓶 长进短出) (长进短出)
固态干燥剂
干燥管 大进小出) (大进小出)
浓硫酸
H2,O2,Cl2SO2, CO,N2,CH4 H2S,NH3,HBr ,HI,C2H4
图2
图3
图4
图5
图6
(4)启普发生器及简易装置 )
图7
图8
图9
图10
图11
图12
3、固体+液体或液体 液体加热制气体 、固体 液体或液体 液体或液体+液体加热制气体
①反应容器:试管、烧瓶 反应容器:试管、 ②加液容器:分液漏斗 加液容器: ③注意事项:见图16、17 注意事项:见图 、
图13
图14
• • • 溶液吸收 点燃 充袋法
易溶于水的要 用防倒吸装置
饱 和 食 盐 水
无水CaCl2
O2,Cl2,HCl,SO2, H2, CO,N2,CH4 NH3
碱石灰
H2,O2,N2, CH4,NH3 HX,H2S,SO2, CO2,NO2, Cl2
四、气体收集装置
根据气体的密度和溶解性选择
1. 排空气法
图18
图19
图20
图21 图22
图23
2.排水法 排水法
五、尾气处理装置 根据多余气体的性质选择
中学化学实验中 常见气体制备装置归纳
一、气体发生装置:根据反应物状 气体发生装置: 态及反应条件选择发生装置
1、固体加热制气体 、 反应容器:试管 反应容器: 注意事项:粉末状固 注意事项: 体应在试管口放一团 棉花
常见气体的制备有装置图ppt课件

② 向试管中加入一定量碳酸钙固体
;
向试管中到入过量的稀硝酸,并迅速盖上带铜丝
③ 和导管的橡皮塞
;
④ 待反应完全后,将右边导管插入试管内接近液面 ;
⑤ 将铜丝插入到溶液中
;
⑥用注射器向试管内推入氧气(或空气)
精选ppt课件2021
33
⑵推入氧气或空气的目的是 检验生成的NO ,
⑶分别将等质量的铜片与等体积均过量的浓硝酸、
精选ppt课件2021
28
[例1]:
(1)在没有现成的CO2气体发生器的情况下,请你选用下 图中的部分仪器,装配成一个简易的、能随开随用、随关
随停的CO2气体发生装置。应选用的仪器是(填入仪器的
编号)
。
(2)若用上述装置制取CO2气体,而实验室只有稀硫酸、 浓硝酸、水、块状纯碱、块状大理石,比较合理的方案应
精选ppt课件2021
19
• 3.2 装置的分类
(1)排水(液)法
精选ppt课件2021
20
• 3.2 装置的分类
(2)向上排空气法
收集比空气 重的气体
精选ppt课件2021
21
• 3.2 装置的分类
(3)向下排空气法
收集比空气 轻的气体
精选ppt课件2021
22
• 3.2 装置的分类
(4)其他 贮气瓶、贮气袋
D.(1) (2) (3)(4)
精选ppt课件2021
39
6、(2000全国)实验室可用氯气与金属反应制备无水三氯化铁,
稀硝酸反应,所得到的溶液前者成绿色,后者成
蓝色, 某同学提出这可能是铜离子浓度差异形成
的,你同意这种看法吗? 不同意 (填“同意”或 “不同意”),原因是铜片质量相同,溶液体积相同;,
(完整版)初中化学常见气体制备的装置及方法
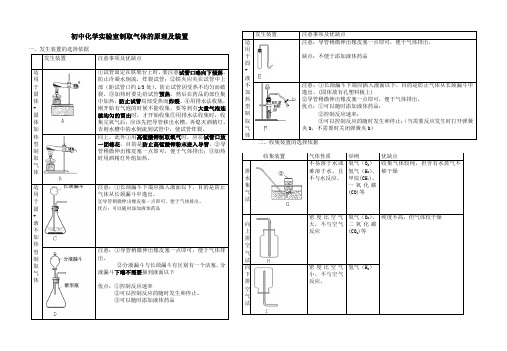
初中化学实验室制取气体的原理及装置一、发生装置的选择依据二、收集装置的选择依据发生装置 注意事项及优缺点 适用于固+液不加热型制取气体 注意:导管稍微伸出橡皮塞一点即可,便于气体排出。
缺点:不便于添加液体药品 注意:①长颈漏斗下端应插入液面以下,目的是防止气体从长颈漏斗中逸出。
(固体放有孔塑料板上) ②导管稍微伸出橡皮塞一点即可,便于气体排出。
优点:①可以随时添加液体药品; ②控制反应速率; ③可以控制反应的随时发生和停止;(当需要反应发生时打开弹簧夹b ,不需要时关闭弹簧夹b )发生装置注意事项及优缺点适用于固体+固体加热型制取气体①试管固定在铁架台上时,要注意试管口略向下倾斜,防止冷凝水倒流,炸裂试管;②铁夹应夹在试管中上部(距试管口约1/3处),防止试管因受热不均匀而破裂。
③加热时要先给试管预热,然后在药品的部位集中加热,防止试管局部受热而炸裂。
④用排水法收集,刚开始有气泡的时候不能收集,要等到有大量气泡连续均匀的冒出时,才开始收集⑤用排水法收集时,收集完氧气后,应该先把导管移出水槽,再熄灭酒精灯。
否则水槽中的水倒流到试管中,使试管炸裂。
同上,此外①用高锰酸钾制取氧气时,应在试管口放一团棉花,目的是防止高锰酸钾粉末进入导管。
②导管稍微伸出橡皮塞一点即可,便于气体排出;③加热时用酒精灯外焰加热。
适用于固+液不加热型制取气体注意:①长颈漏斗下端应插入液面以下,目的是防止气体从长颈漏斗中逸出。
②导管稍微伸出橡皮塞一点即可,便于气体排出。
优点:可以随时添加液体药品注意:①导管稍微伸出橡皮塞一点即可,便于气体排出。
②分液漏斗与长颈漏斗有区别有一个活塞,分液漏斗下端不需要插到液面以下优点:①控制反应速率②可以控制反应的随时发生和停止。
③可以随时添加液体药品 收集装置 气体性质 举例 优缺点 排水集气法 不易溶于水或难溶于水,且不与水反应。
氧气(O 2) 氢气(H 2)、甲烷(CH 4)、一氧化碳(CO)等 收集气体较纯,但含有水蒸气不够干燥 向上排空气法密度比空气大,不与空气反应 氧气(O 2)、二氧化碳(CO 2)等纯度不高,但气体较干燥 向下排空气法密度比空气小,不与空气反应。
2015届陕西考化学ppt复习课件【第16讲】常见气体制备与收集

【注意事项】(1)若使用长颈漏斗,长颈漏斗导管 下端应伸入液体药品的液面以下。(2)块状固体应 大小适当,不能太小,防止反应剧烈不易控制。
气体收集装置
1.排空气集气法 所收集的气体不与空气中的任何成分反应,且密度与空 气相差较大的,采用排空气法收集。密度比空气大的气 体,用向____排空气法(如O2、CO2),密度比空气小的气 体用向____排空气法(如H2)。 上 下
解析:本题考查实验室制取气体的操作,难度较小。(1)实验室用高锰酸 钾制取氧气需在加热的条件下才能进行反应,分析图中仪器可知缺少酒精 灯;在实验时,由于试管中原先就有空气,因此刚开始冒出的气泡不能收 集,只有等气泡连续均匀地放出时,才可以收集;反应的化学方程式为 △ K MnO +MnO +O ↑。(2)①已提供的药品中已有稀盐酸, 2KMnO4 ===== 2 4 2 2 再补充含碳酸钙的大馏水润湿的紫花,通入二氧化碳后,由于二氧化碳能够与水反应生成 碳酸,碳酸能使紫色石蕊试液变成红色,故将观察到紫花变红的实验现象。
[答案](1)酒精灯 连续均匀地放出 2KMnO4 K2MnO4+MnO2+O2↑ (2)①
△ =====
画图要求:A装置中用实线画液面;用虚线画液 体;画气泡;画固体;液体不超过容积的二分之一;长颈 漏斗末端要伸入液面以下;导管插过橡胶塞少许;橡胶塞 部位不画导管;胶皮管要涂黑。②紫花变红(合理即可)
2.排水集气法 不溶于水或难溶于水的气体可用 ________ 收集 ( 如 H2 、 O2 排水法 、CO、CH4等)。CO2不能用排水集气法收集。最佳收集时 间:当导管口气泡连续且均匀放出时。 3.检验与验满 (1) 检验 O2 :将带火星的木条伸入集气瓶中 , 木条复燃; 检验CO2:将燃着的木条伸入集气瓶中,木条熄灭。 (2)验满O2:将带火星的木条放到集气瓶口,木条复燃; 验满CO2:将燃着的木条放到集气瓶口,木条熄灭。
化学常见气体的制备方法总结(超经典)[优质ppt]
![化学常见气体的制备方法总结(超经典)[优质ppt]](https://img.taocdn.com/s3/m/af698650a45177232f60a279.png)
反应装置
-----常用装置
1、气体发生装置
思 考:
气体制备的发生装置有几种类型?如何选择气 体的发生装置? 气体发生装置的基本类型:
A、固体反应物(加热)
B、固液反应物(不加热) C、固(液)液反应物(加热)
气体发生装置的设计原则:
根据反应原理、反应物状态和反应所需条 件等因素来选择反应装置。
A、固体反应物(加热) 注意事项:
气体溶于水,内部气压变小,水在
大气作用下被吸入漏斗,使得液面与漏斗口脱离,水又回到烧杯
6、实验室里可按下图所示的装置干燥、储存气体R, 多余的气体可用水吸收,则R是 D A.NO2 B.HCl
C.CH4 D.NH3
7、分别由下列四组物质制取气体。①浓盐酸和
MnO2②(NH4)2Cl和Ca(OH)2 ③NaCl和H2SO4(浓)
CO2,Cl2,HCl
H2,NH3
下面是课外兴趣小组的同学设计的各种尾气吸收装置:
a b c d
e
f
I
g
h
从实验安全和环境保护的角度考虑,若用于吸收HCl气体(装置中的液体为水,
固体为碱石灰),应选用的装置是________a_____d_____ e h
4、常见除尾气装置
A、 燃烧法 如CH4、C2H4、C2H2、H2、CO等。
试管 酒精灯
(1)试管口应略向下倾斜 (2)试管夹夹在试管的中上部
导管 (3)药品应平铺于试管底部
(4)导管不宜伸入试管过长
(5)实验开始时先检验装置的气密性
铁架台 (6)加热时,先预热且应用外焰加热
该装置可用于制备 O2、NH3和CH4
2KM 4K n2M O4n M O2n O O 2
高三常见气体制备吸收装置

大家好
10
[例5]铜与浓硝酸反应和铜与稀硝酸反应,产物
不同,实验现象也不同。
⑴某课外活动小组为了证明并观察到铜与稀
硝酸反应的产物为NO,设计了如左图所示
的实验装置。请你根据他们的思路,选择下
列药品,完成该实验,并叙述实验步骤。
药品:稀硝酸、稀盐酸、锌粒、碳酸钙固体
步骤:①检查装置的气密性;
② 向试管中加入一定量碳酸钙固体
(4)若烧杯是干燥的,不能用此装置来收集的 气体是___。
【答】(1) ②④⑦⑧ (2)①③⑥,A
(3)①②③④⑥⑧,B (大家4好)⑥
9
[例4]:
某集气瓶中充满了HI气体,试设计一个装置表 示:将这种气体排出烧瓶,并粗略证明它确实是HI 气体,写出有关反应的离子方程式。
【答】:往装有气体的瓶中注入浓磷酸,使气体排出, 用盛有适量水的烧杯吸收排出的气体(玻璃管下端接一个 倒置漏斗),一段时间以后,取少量烧杯中的溶液,测得 PH值小于7;加入用硝酸酸化的硝酸银溶液,如发现有黄 色沉淀生成,则可说明原气体是HI气体。
4、尾气处理装置
▪总原则 ▪(1)有毒、污染环境的气体不能直接排放。 ▪(2)尾气吸收要选择合适的吸收剂和吸收装置。
•直接吸收:Cl2、H2S、NO2 防倒吸:HCl、NH3、SO2 •常用吸收剂:NaOH溶液,硫酸铜溶液 ▪(3)可燃性气体且难用吸收剂吸收:燃烧处理或袋装。
大家好
1
4、尾气处理装置
(1)若烧瓶是干燥的,则由A口进气,在B口可收集的气体 有(用数字表示,下同)________________.
(2)若烧瓶充满水,可收集的气体有________,这时气体 由________口进入。
(3)若在烧瓶内装入浓硫酸进行干燥气体,则 可用此装置的气体有____________,这时气体 由________口进入。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
无水CaCl2
O2,Cl2,HCl,SO2, H2, CO,N2,CH4 NH3
碱石灰
H2,O2,N2, CH4,NH3 HX,H2S,SO2, CO2,NO2, Cl2
五、气体收集装置 根据气体的密度和溶解性选择 1. 排空气法
图18
图19
图20
图21 图22
图23
2.排水法
储气装置
六、气体性质实验装置 根据反应物的状态及反应的条件选择
②恒压式
原理是使分液漏斗与烧瓶内气 压相同,保证漏斗中液体顺利 流出。
⑴实验前如何检查装置的气密性?
⑵点燃氢气前必须进行 操作,进行该操作的方法是
⑶写出B、D中分别发生的化学反应方程式: B中:—————————— ⑷C中所盛干燥剂的名称是
。
D中:————————— 。
;该干燥剂的作用是
通常设计化学实验时,为了保证操作人员的安 全,保障实验如期顺利进行,往往要设置安全装置; 一般在涉及气体的实验中最为常见。涉及到的安全 问题有: 防倒吸(防倒吸装置)、
防堵塞(检验堵塞、防压强过大)、
防爆炸(验纯,操作顺序)、
防污染(尾气吸收)等安全问题。
防堵塞装置
(2)防堵塞安全装置
①液封式
原理是流动的气体若在前方受阻, 锥形瓶内液面下降,玻璃管中水 柱上升
图2
图3
图4
图5
图6
(4)启普发生器及简易装置
图7
图8
图9
图10
图11
图12
3、固体+液体或液体+液体加热制气体
①反应容器:试管、烧瓶 ②加液容器:分液漏斗
③注意事项:见图16、17
图13
图14
图15
图16
图17
二、装置气密性检验
饱 和 食 盐 水
例1、用示意图中的简易装置可以进行气体的发生和收集。
例:根据右图描述回答下列问题: ①关闭图A装置中的止水夹a后,从长颈漏斗 向试管中注入一定量的水,静置后如图所示 试判断:A装置是否漏气? (填“漏气”、“不漏气”或“不能确定”) ②关闭图B装置中的止水夹a后,开启活塞b, 水不断往下滴,直至全部流入烧瓶。试判断: B装置是否漏气?(填“漏气”、“不漏气” 或“不能确定”) ,判断理由 。 ①不漏气 ②不能确定;不管装置是否 漏气,烧瓶内气压与漏斗上 方的气压相等,水在重力作 用下可完全流入。
1.常温反应装置
Байду номын сангаас
2.加热反应装置
七、冷凝装置
八、排水量气装置:测量气体的体积
注意事项:
为减小误差, 读数时1、2 装置量筒内外 液面在同一水 平线,3装置 左右管水面在 同一水平线
九、尾气处理装置
根据多余气体的性质选择
• • • 溶液吸收 点燃 充袋法
易溶于水的要 用防倒吸装置
十.安全装置
5.2《中学化学实验中 常见气体制备装置》
中学化学实验中 常见气体制备装置 归纳
一、气体发生装置:根据反应物状 态及反应条件选择发生装置
1、固体加热制气体
反应容器:试管
注意事项:粉末状固 体应在试管口放一团 棉花
2、固体+液体不加热制气体
①反应容器:试管、烧瓶、广口瓶;
②加液容器:长颈漏斗、分液漏斗; ③注意事项:图4、6
二、装置气密性检验
饱 和 食 盐 水
二、装置气密性检验
二、装置气密性检验
二、装置气密性检验
三、气体净化装置: 根据净化剂的状态和条件选择
四、气体的干燥
液态干燥剂
装 置 洗气瓶 (长进短出)
固态干燥剂
干燥管 (大进小出)
常见干燥 剂
可干燥 气体 不可干燥 气体
浓硫酸
H2,O2,Cl2SO2, CO,N2,CH4 H2S,NH3,HBr ,HI,C2H4
实验前应如何检查该装置的气密性?
把导管伸入水槽的液 面下,手握住试管, 过会儿看到导管口有 气泡冒出,松开手导 管中形成一段水柱, 则证明气密性良好
连接好装置,关闭开关,从漏斗中倒水。漏斗 内外产生液面差,静止一段时间,液面差不变, 证明装置气密性完好。 关闭开关,将干燥管放入盛水的烧杯中, 若干燥管内的液面比烧杯中液面低,且过 一段时间后干燥管内液面保持不变,证明 装置气密性完好。
