最新【知情同意书模板】知情同意书格式.doc
最新知情同意书格式

知情同意书格式1、标题:双方单位名称事由,协议书三部分组成。
2、正文:条款内容1、同意目的2、同意目的责任3、协议的时间和期限4、同意目的条款和酬金{价格明确总额大写必须明确货币种类}5、履行条款期限6、违反条款的责任处理7、落款{签署}8、签署日期知情同意书研究批准文号:受试者姓名:身份证号:·联系电话:住址:尊敬的受试者:您将被邀请参加一项临床研究,本知情同意书提供给您一些信息,在您决定是否参加这项研究之前,请尽可能仔细阅读以下内容。
它可以帮助您了解该项研究以及为何要进行这项研究,研究的程序和期限,参加研究后可能给您带来的益处、风险和不适。
如果您愿意,您也可以和您的亲属、朋友一起讨论,或者请医生给予解释,帮助您做出决定。
一、研究背景和研究目的研究背景:(包括该药物或医疗器械国内、国外研究进展)本研究目的:简要说明研究要达到的最终目标(评价新药物或新医疗器械的安全性及有效性)二、研究简介关于此项临床研究的基本资料(包括本研究是否已通过伦理委员会审核、研究概况、主要研究内容、过程与期限、检查操作等)。
研究概况(本研究将在医院科(或研究中心)进行,预计有名受试者自愿参加,受试者入选条件、告知受试者可能被分配到研究的不同组别等。
)(本研究已经得到批准,伦理委员会已经审议此项研究是遵从赫尔辛基宣言原则,符合医疗道德的。
)主要研究内容:过程与期限:检查操作:三、哪些人不宜参加研究根据不同研究目的和研究药物规定的人群,另外还有1)正参加其它临床研究的患者;2)研究人员认为其它原因不适合临床研究者。
四、如果参加研究将需要做什么?您是合格的纳入者,您可自愿参加研究,签署知情同意书。
如您不愿参加本项研究,我们将按您的病情和意愿给予其它适当的处理。
2、若您自愿参加研究,将按以下步骤进行:简单叙述受试者分配流程,告知受试者可能被分配到研究的不同组别、给药方法(药物:剂量、疗程、使用说明和注意事项、药物生产厂家和批号;采用的治疗和诊断仪器:生产厂家、生产企业许可证、注册证号等)受试者到医院进行检查和随访的时间、次数、注意事项。
知情同意书模板格式

知情同意书模板格式一、引言知情同意书是医学伦理中非常重要的一个环节,它用于保护患者的知情权、选择权和隐私权,确保患者对医疗措施有充分的了解并自愿接受相关治疗。
本文将介绍知情同意书的模板格式,以便读者了解如何正确填写知情同意书。
二、模板格式知情同意书通常包括以下内容:1. 患者基本信息:包括姓名、年龄、联系方式等。
2. 医疗措施描述:详细说明将要实施的医疗措施,包括名称、目的、风险、副作用等。
3. 医学背景:简要介绍患者的健康状况、既往病史、当前症状等。
4. 风险和利益:列出实施医疗措施可能带来的风险和利益,以供患者权衡。
5. 隐私保护:说明医疗机构将如何保护患者的隐私,包括数据收集、存储和使用等方面的规定。
6. 签名和日期:患者需要在同意书上签名和注明日期。
以下是一个知情同意书的模板:[患者姓名]:本人,[患者姓名],愿意接受[医疗机构名称]实施的[医疗措施名称]的医学治疗。
在此,本人充分了解并接受以下内容:1. 我/我们将对您/我进行[医疗措施名称],该措施的目的是[具体目的],可能存在的风险和副作用包括[具体列举]。
2. 我/我们已简要介绍了我的/我的健康状况和既往病史,包括[具体列举]。
3. 在实施该医疗措施的过程中,我/我们将采取必要的措施来保护我的隐私,包括数据收集、存储和使用等方面的规定。
4. 我/我们已充分了解并接受实施该医疗措施可能带来的风险和副作用,同时也意识到该措施可能带来的利益。
我已认真权衡了这些利弊,并自愿接受该医疗措施。
在此,本人声明:我已阅读并理解上述内容,我/我们自愿接受该医疗措施,并愿意承担由此产生的所有风险和副作用。
我/我们有权拒绝任何违反我意愿的医疗措施。
本人签名:______________ 日期:______________三、注意事项填写知情同意书时,需要注意以下几点:1. 真实性和准确性:患者应如实填写个人资料和健康状况,以便医疗机构更好地提供服务。
2. 充分告知:医疗机构应充分告知患者医疗措施的风险和利益,以便患者做出明智的决策。
知情同意书模板

1.手术知情同意书模版手术知情同意书尊敬的患者:您好!根据您目前的病情,您有此手术适应症,医师特向您详细介绍和说明如下内容:术前诊断、手术名称、手术目的、术中拟使用高值医用耗材和仪器、术中或术后可能出现的并发症、手术风险及替代医疗方案等。
帮助您了解相关知识,作出选择。
等,应重新履行告知并签署知情同意书。
2、建议此知情同意书采用一式两份,患者方留存一份。
2.特殊检查知情同意书模板特殊检查知情同意书尊敬的患者:您好!根据您目前的病情,您有该检查的适应症,根据《医疗机构管理条例实施细则》的规定,特殊检查是指有一定危险性,可能产生不良后果的检查;由于患者体质特殊或者病性危笃,可能对患者产生不良后果和危险的检查;临床试验性检查;收费可能对患者造成较大经济负担的检查。
医师特向您详细介绍和说明如下内容:特殊检查项目名称、目的、费用、可能出现的并发症、风险及替代医疗方案,帮助您了解相关知识,作出选择。
注:建议此知情同意书采用一式两份,患者方留存一份。
3.特殊治疗知情同意书模板特殊治疗知情同意书尊敬的患者:您好!根据您目前的病情,您有该治疗的适应症,根据《医疗机构管理条例实施细则》的规定,特殊治疗是指有一定危险性,可能产生不良后果的治疗;由于患者体质特殊或者病性危笃,可能对患者产生不良后果和危险的治疗;临床试验性治疗;收费可能对患者造成较大经济负担的治疗。
医师特向您详细介绍和说明如下内容:特殊治疗项目名称、目的、费用、可能出现的并发症、风险及替代医疗方案,帮助您了解相关知识,作出选择。
注:1、以治疗为目的,需先履行检查的,可在此告知书中一并填写。
2、建议此知情同意书采用一式两份,患者方留存一份。
腹股沟疝手术知情同意书尊敬的患者:您好!根据您目前的病情,您有此手术适应症,医师特向您详细介绍和说明如下内容:术前诊断、手术名称、手术目的、术中拟使用高值医用耗材和仪器、术中或术后可能出现的并发症、手术风险及替代医疗方案等。
知情同意书范本.doc
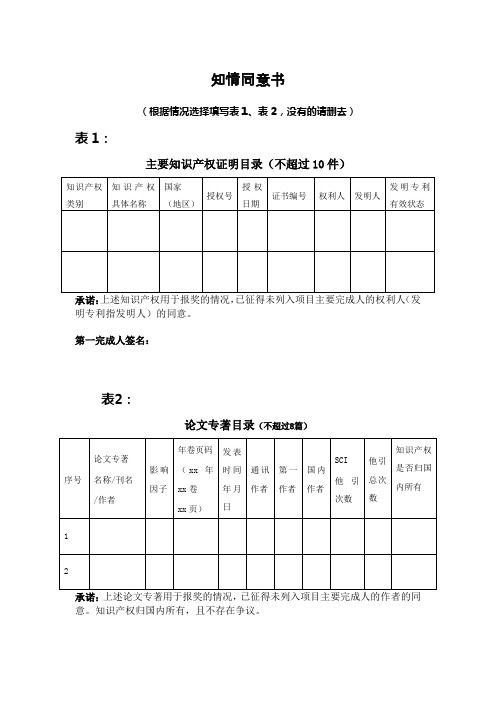
序号
论文专著
名称/刊名
/作者
影响因子年卷页码(x年xx卷xx页)发表时间年月日
通讯作者
第一作者
国内作者
SCI
他引次数
他引总次数
知识产权是否归国内所有
1
2
承诺:上述论文专著用于报奖的情况,已征得未列入项目主要完成人的作者的同意。知识产权归国内所有,且不存在争议。
第一完成人签名:
知情同意书
(根据情况选择填写表1、表2,没有的请删去)
表1:
主要知识产权证明目录(不超过10件)
知识产权类别
知识产权具体名称
国家
(地区)
授权号
授权日期
证书编号
权利人
发明人
发明专利有效状态
承诺:上述知识产权用于报奖的情况,已征得未列入项目主要完成人的权利人(发明专利指发明人)的同意。
第一完成人签名:
表2:
知情同意书模板(医疗)

知情同意书模板(医疗)
[医疗机构名称]
[医疗机构地址]
[日期]
受试者:[受试者姓名]
诊疗项目:[详细描述诊疗项目]
我同意参加上述诊疗项目,并确认已经充分了解以下内容:
1. 目的:参与该诊疗项目的目的、可能的益处以及可能的风险和副作用。
2. 风险和副作用:我已被告知这种诊疗项目可能带来的风险和副作用,包括但不限于:[详细描述可能的风险和副作用]。
3. 代价和费用:我了解参与该诊疗项目可能产生的费用,并同意承担这些费用。
4. 自愿参与:我确认自愿参与该诊疗项目,而非被强迫、诱导或滥用权力。
5. 回收权:我了解我有权在任何时间停止参与该诊疗项目,并可以收回我的同意。
6. 隐私和保密:我同意医疗机构可以保存、处理并保密与该诊疗项目相关的个人信息。
7. 法律责任:我了解医疗机构将尽力保护我的权益,但无法对可能发生的意外事件和不良后果承担责任。
8. 联络方式:我已了解医疗机构提供的联系方式,在需要时可与他们取得联系。
本知情同意书代表我自愿参与该诊疗项目,并确认我已经充分理解其中的内容。
我已经有机会询问并获得满意的答复。
受试者签名:__________________________ 日期:_____________________
见证人签名:__________________________ 日期:_____________________。
知情同意书模板(人力资源调查)

知情同意书模板(人力资源调查)
尊敬的先生/女士:
您好!为了确保企业经营的正常顺利,我们需要进行一些必要的人力资源调查。
在此,我们诚挚邀请您参与此次调查,并且在明确了解调查内容和目的后予以同意。
我们郑重承诺,在此次人力资源调查过程中,会严格遵守相关法律法规,并保护您的隐私权。
我们承诺不会将您的个人信息用于任何与本次调查无关的目的,并采取适当的安全措施,保障您的信息安全。
此次调查不会涉及到与您的薪酬待遇、家庭状况、政治、个人隐私等敏感信息的采集。
我们只会就与工作相关的事项进行调查。
您可以放心,您的个人信息将被严格保密,仅限于有关人力资源管理人员和相关领导层查看。
请您在签署前认真阅读以下声明:
1. 我已充分了解此次调查的目的、范围和方式,并愿意自愿参与。
2. 我明确知晓此次调查不会泄露与薪酬待遇、家庭状况、政治、个人隐私等敏感信息。
3. 我同意将个人信息供给有关人力资源管理人员和相关领导层
进行查看,并保证所提供的信息的真实性和准确性。
4. 我了解,如果我对此次调查有任何疑问、担忧或不愿参与,
我有权拒绝参与或提出异议,不会因此受到任何不利待遇。
我愿意参与此次人力资源调查,并接受上述声明所述的规定。
签名:________________________
日期:________________________
感谢您的配合与支持!
此知情同意书的一方拥有原件,另一方则保留副本。
学生实习知情同意书【模板】

附件2
学生实习知情同意书
(校内导师适用)
**大学法学院:
本人系级(本科生□法学法硕研究生□法律硕士研究生□)学生(姓名)的校内导师,已经知悉并同意该生于年月日至年月日期间在(实习单位名称)参加专业实习活动的申请。
我已经完全阅读我院关于学生专业实习的相关规章制度,并充分了解此次活动可能存在的各种风险。
我将按照学院专业实习相关规章制度的要求充分履行职责,以保证该生能够按照学院专业实习相关规章制度的目标要求顺利完成本次实习活动。
校内导师签章:
年月日
实习学生确认签字:
年月日。
家长同意知情书(模板)

家长同意知情书(模板)
尊敬的老师:
我是一名本科生的家长,我的孩子就读于XXXXX级XXX专业。
我已经知道了学校的放假时间为XXX年X月XX 日至XX月X日,并且学生在放假期间原则上不得留校。
然而,由于XXXXXX原因,我知道我的孩子需要申请延长留校时间(或者提前返校),我已经同意并签署了知情同意书。
我知道我的孩子将在X月XX日至X月XX日期间延长留校(或者提前返校),并承诺在此期间遵守学校规定,注意人身安全,并且每天至少与我联系一次。
如果遇到特殊情况,我会及时和学院辅导员老师联系,以确保我的孩子度过一个安全愉快的假期。
最后,我在此留下我的联系方式(手机),以便老师和学院随时与我取得联系。
谢谢您的关注和支持。
学生(签字):
家长(签字):
联系方式(手机):。
知情同意书模板范文

知情同意书模板范文英文回答:Informed Consent Form Template.[Your Name][Your Address][City, State, Zip Code][Email Address][Phone Number][Date][Recipient's Name][Recipient's Address][City, State, Zip Code]Dear [Recipient's Name],。
I, [Your Name], hereby provide my informed consent to participate in [Name of the study or research project]. I have been fully informed about the purpose, procedures, potential risks, benefits, and any alternative options associated with this study.I understand that my participation in this study is voluntary, and I have the right to withdraw my consent at any time without any consequences or penalty. I also understand that my withdrawal from the study will notaffect my relationship with [Name of the institution or organization conducting the study].I have been informed that my personal information and data collected during the study will be kept confidential and will only be used for the purpose of this research. Any publication or presentation of the results will be done ina way that ensures my anonymity and confidentiality.I acknowledge that I have had the opportunity to ask questions and have received satisfactory answers regarding the study. I understand that I can contact [Contact Person's Name] at [Contact Person's Email Address] or [Contact Person's Phone Number] if I have any further questions or concerns.By signing below, I confirm that I have read and understood the information provided in this informed consent form. I voluntarily agree to participate in [Name of the study or research project] and give my consent for the collection and use of my data for research purposes.Participant's Signature: _______________________。
(完整word)知情同意书模板

知情同意书模板:1.“科研项目中需涉及病人或正常人血液、尿液标本采集”受试者须知模版2.“科研项目中涉及病人组织标本采集"受试者须知模板3.“新药临床试验”受试者须知模版知情同意书(ICF Template)“科研项目中需涉及病人或正常人血液、尿液标本采集”受试者须知模版(括号内斜体字部分需根据课题不同情况自行填写)方案名称:方案编号:KY2009-×××(“×××”为伦理审查委员会首次受理号)方案版本号:01,2009年×月×日(“01”为版本序号,随版本更新而依次递增)知情同意书版本号:01,2009年×月×日(“01”为版本序号,随版本更新而依次递增)研究机构:主要研究者(负责研究医师):您将被邀请参加一项临床研究.本知情同意书提供给您一些信息以帮助您决定是否参加此项临床研究。
请您仔细阅读,如有任何疑问请向负责该项研究的研究者提出。
您参加本项研究是自愿的.本次研究已通过本研究机构伦理审查委员会审查。
研究目的:背景意义(包括国内、国外研究进展)――语言要求通俗易懂。
研究过程:(包括主要研究内容、预期参加的受试者人数、过程与期限、随访的次数、需何种检查操作、告知受试者可能被分配到试验的不同组别等――语言要求通俗易懂)。
(例如:如果您同意参与这项研究,我们将对每位受试者进行编号,建立病历档案。
在研究过程中我们需要采集一些您的标本,将由专业人员为您取样,例如从您的胳膊上抽取静脉血毫升,或留取尿液毫升,共需次.您的样品仅用于研究。
)风险与不适:对于您来说,所有的信息将是保密的。
您的样本采集将严格按照无菌要求操作,标本的采集可能会有一些非常小的风险,包括短暂的疼痛、局部青紫,少数人会有轻度头晕,或极为罕见的针头感染.受益:通过对您的标本进行检测将有助于对疾病作出诊断,为您的治疗提供必要的建议,或为疾病的研究提供有益的信息。
知情同意书模板 知情同意书格式(最新)

我们将要开展一项(研究题目),因您患有(疾病名称)(或:因您患有(疾病名称)并将接受(治疗名称)),且您的具体情况符合该研究的入组条件,因此,我们想邀请您参加该项研究。
本知情同意书将向您介绍本研究的目的、步骤、获益、风险、不便以及您的权益等,请仔细阅读后慎重做出是否参加研究的决定。
当研究者向您说明和讨论知情同意书时,您可以随时提问并让他/她向您解释您不明白的地方。
您可以与家人、朋友以及您的经治大夫讨论之后再做决定。
若您目前正参加其他临床研究,请务必告知您的研究医生或者研究人员。
本项研究的项目负责人是(姓名,单位),研究资助方或研究资金来源是(名称)。
若为多中心研究,请同时列出组长单位。
1. 为什么进行这项研究?简要描述本项研究的背景和目的。
(此部分需由研究者根据项目特点,用通俗易懂的语言作介绍)结合研究内容,紧密围绕对疾病的认识水平/诊断现状/治疗现状等简要介绍研究背景; 结合研究背景和研究题目适当解释研究目的。
首次使用的英文缩写前须有中文注释。
对于本研究使用的(包括对照)药物、生物制品、诊断试剂、医疗器械,请明确说明哪些是国家食品药品监督管理局已批准上市的,哪些是研究性的(包括已在国外批准上市,国内尚未批准的进口药;或国外批准上市,国内正在仿制,尚未批准的,都要明确描述),如果是药品/生物制品、或医疗器械等,要简略介绍其主要作用(效果)、主要副作用。
如果有前期临床试验结果,也可一并简单介绍。
同时还必须对对照产品进行介绍,包括疗效和副作用。
如果您将开展的是有关诊疗技术的研究,例如外科术式或者诊断程序,请明确说明它是研究性的。
2.哪些人将被邀请参加这项研究?简要描述本项研究受试人群的特点,以通俗易懂的语言描述受试者的纳入和排除标准。
3. 多少人将参与这项研究?如果是多中心临床研究,请注明研究机构/医疗机构的数目。
本研究共计划招募( )名受试者,其中我中心将招募()名受试者。
4. 该研究是怎样进行的?描述研究方法和具体研究步骤,包括研究期限(包括筛选阶段,试验阶段及随访阶段)、受试者分组、随机和双盲的设置(应用通俗语言介绍什么是随机和双盲、随机比例)、干预措施(包括分组后每组的给药种类、给药方法;或各组不同的治疗器械、治疗方法。
制度知情同意书模板

制度知情同意书模板尊敬的[姓名/单位名称]:您好!为了保护您的权益,确保您充分了解和同意[相关项目/活动/制度]的相关规定,特制定本知情同意书。
请您在仔细阅读、充分理解后,签字确认并遵守以下内容:一、项目/活动/制度概述1.1 本[项目/活动/制度]是由[主办方/组织者]主办,旨在[目的和意义]。
1.2 本[项目/活动/制度]的实施时间为[开始时间]至[结束时间]。
1.3 本[项目/活动/制度]的地点为[具体地点]。
二、参与者的权利与义务2.1 参与者享有以下权利:(1)获得[项目/活动/制度]相关的信息、培训和指导;(2)参与[项目/活动/制度]的决策和监督;(3)获得[项目/活动/制度]所提供的服务和资源;(4)提出意见和建议,并对[项目/活动/制度]进行评价;(5)在[项目/活动/制度]中享有平等的机会和待遇。
2.2 参与者需履行以下义务:(1)遵守国家法律法规、[项目/活动/制度]的相关规定和纪律;(2)如实提供个人信息,并确保其真实、准确和完整;(3)积极参与[项目/活动/制度]的各项工作和活动;(4)尊重其他参与者,维护[项目/活动/制度]的和谐氛围;(5)按照约定使用[项目/活动/制度]所提供的资源和设施。
三、隐私保护3.1 [主办方/组织者]承诺保护参与者的个人信息和隐私,除法律法规另有规定外,不得向第三方透露。
3.2 [主办方/组织者]将采取合理措施确保参与者的个人信息安全,防止泄露、损毁或丢失。
四、风险提示4.1 参与者应充分了解并同意,[项目/活动/制度]存在一定的风险和不确定性,可能影响参与者的权益。
4.2 [主办方/组织者]将尽力确保[项目/活动/制度]的顺利进行,但对于不可抗力、意外事件等无法预见、无法避免和无法克服的情况,不承担责任。
4.3 参与者应自行评估自身的能力和条件,谨慎参与[项目/活动/制度],并在遇到困难和问题时,及时寻求帮助和解决方案。
五、退出和解除协议5.1 参与者有权在[项目/活动/制度]开始前退出,但需提前通知[主办方/组织者]。
知情同意书模板

知情同意书模板方案名称:知情同意书版本号:1.0,20XX年X月X日研究机构:主要研究者:患者姓名:患者姓名缩写:患者地址:患者:尊敬的(先生/女士):我们在此邀请您作为受试者参加一项临床试验。
本知情同意书提供应您一些信息以帮忙您决定是否参加此项临床试验。
请您用必然的时间仔细阅读下面的内容,如有不清楚的问题或术语,可以与有关医师进行讨论。
您参加本项研究是完全自愿的。
本次研究已通过北京肿瘤病院伦理委员会审查。
1.研究布景:布景意义(包罗国内、国外研究进展)一一语言要求通俗易懂,鼓励以图表、漫画等形式。
2.研究目的:3.研究过程:(包罗主要研究内容、预期参加的受试者人数、过程与期限、随访的次数、需何种查抄操作、告知受试者可能被分配到试验的不同组别等一一语言要求通俗易懂)。
如果您的研究设计为“随机分组〃、〃抚慰剂对照〃、和“双盲〃,请向受试者解释其定义。
〃随机分组〃暗示您会被随机地分配到一个治疗组中,以减少偏差。
您有1/2的时机接受,1/2的时机接受,具体的分组会通过计算机程序随机确定。
无论是您还是您的大夫均不克不及选择您接受哪种药物。
这样可以包管以公正的方式对研究药物进行评估。
“抚慰剂对照〃暗示研究中会使用一种看起来很像真实的样子的“安慰剂〃,实际上该抚慰剂不含有任何活性研究药物。
“双盲〃暗示您、您的研窕大夫均不知道您接受的是还是抚慰剂片。
这样可以包管参与本试验性研究的每一个人都能够公平的评价药物的平安性和有效性。
但在紧急情况下,如果您的大夫确定对知道您是服用还是抚慰剂片非常重要的话,您的大夫可以了解。
4.需要您配合的事项:为了能使本项研究顺利和成功开展,请您配合以下事项:•遵照研究者安排服药、接受查抄。
•在与研究大夫确认之前,您不克不及够随意改变您目前的治疗或者开始任何新的治疗。
•需要您告知研究大夫有关您健康的问题,甚至是您认为不是很重要的问题。
•需要您告诉研究大夫您在参加研究前和研究中使用的除研究用药以外的其它所有药物(包罗中草药)。
知情同意书模板模版

使用说明为了更好地方便您的理解和使用,发挥本文档的价值,请在使用本模版之前仔细阅读以下说明:本模版为根据一般情况制定或编写的常规模版;使用过程中请根据结合您的客观实际情况作出必要的修改和完善;本文档为word格式,您可以放心修改使用。
希望本文档能够对您有所帮助!!!感谢使用知情同意书模板第一部分受试者须知我们将要开展一项(研究题目),您的情况可能符合该项研究的入组条件,因此,我们想邀请您参加该项研究。
本知情同意书将向您介绍该研究的目的、步骤、获益、风险、不便或不适等,请仔细阅读后慎重做出是否参加研究的决定。
当研究人员向您说明和讨论知情同意书时,您可以随时提问并让研究人员向您解释您不明白的地方。
您可以与家人、朋友以及您的医生讨论之后再做决定。
若您目前正参加其他临床研究,请告知研究人员。
本项研究的项目负责人是(姓名,单位),本项研究的申办方/资助方是(单位)。
备注:若为多中心研究,请同时列出组长单位项目负责人和本中心的项目负责人。
请说明研究申办方/资助方,或研究资金来源和名称,如“国家自然科学基金”。
若研究为企业资助,请说明申办方的名称。
为什么进行这项研究?简要描述本项研究的目的和背景。
备注:1.对于本研究使用的(包括对照)药物或医疗器械,请明确说明哪些是国家食品药品监督管理局已批准上市的,哪些是研究性的,并对“研究性”进行说明,例如,“研究性”指本研究的药物、器械仍处于研究阶段,其使用还未得到国家食品药品监督管理局批准。
对研究用药或器械避免使用“药品”、“治疗”或“疗法”等字眼,应描述为“研究药物”、“研究步骤”、“研究过程”等。
2. 研究背景描述应尽量使用通俗易懂的语言。
哪些人将被邀请参加这项研究?简要描述本项研究受试人群的特点。
备注:以简明易懂的语言概括性描述受试者的纳入和排除标准,避免照搬方案。
多少人将参与这项研究?本研究计划招募名受试者。
备注:如果是多中心临床研究,请注明研究机构的数目,同时说明本研究中心计划招募的受试者人数。
知情同意书模板(社会调查)

知情同意书模板(社会调查)知情同意书模板 (社会调查)
我,________ [调查对象的姓名],完全了解并理解以下内容,并且自愿同意参与本次社会调查。
背景和目的
本社会调查的背景和目的是________ [简要说明社会调查的目的和意义]。
调查内容和方式
本次社会调查将涉及的内容和方式包括但不限于:
1. __________ [描述调查内容1]
2. __________ [描述调查内容2]
3. __________ [描述调查内容3]
...
风险和保密
在参与本次社会调查过程中,可能存在一定的风险,如
__________ [列举可能的风险]。
我已充分了解这些风险,并愿意承担相应责任。
此外,我保证将本次社会调查的内容和结果保密,并不会将其泄露给任何未经授权的第三方。
参与权利
作为调查对象,我享有以下权利:
1. 在任何时间点,有权选择中断或终止参与本次社会调查,而无需提供理由。
2. 有权拒绝回答任何与隐私或个人信息相关的问题。
3. 有权要求获得本次社会调查的结果或分析报告。
自愿参与和知情同意
我自愿参与本次社会调查,并且在提供自身信息和回答问题前,已充分了解并理解本知情同意书的内容。
我确认,在签署本知情同意书之前,已经获得了解答我所提问
题的机会,并且对本次社会调查的目的、内容、方式、风险、保密、参与权利等进行了详细询问。
本知情同意书自双方签字生效,并在调查结束后终止。
---
调查对象(签字): __________
日期: __________。
患者病情知情同意书【范本模板】

患者病情知情同意书
姓名:性别:科别:床号:住院号:
尊敬的患者:
患者住院治疗的过程就是医护人员与患者共同合作,一起与疾病斗争的过程,为使您及家属对疾病有个初步的认识和了解,以便更好地理解和配合医护人员为治愈疾病所采取的诊断和治疗措施,同时也充分尊重您的知情决定权,主管医生就以下几个问题与您或您的家属谈话.
一、诊断:
二、可能出现的并发症和合并症:
三、治疗方案及可能出现的不良后果:
四、必须的检查项目(主要指大金额及特殊检查):
五、病情可能的转归:
治愈、好转、无变化、恶化、死亡
六、需患者及家属配合的内容:
1。
积极配合医生治疗;
2。
住院期间不准外出,外出如发生意外,后果自负。
经治医生签字:签字时间:年月日
患者或委托代理人陈述:
医师已详细告知我病情、可能出现的并发症、治疗方案及可能出现的不良后果、必须检查项目及其目的、病情可能转归、需患者及家属配合的内容等,对我的病情我已完全了解,对可能出现的并发症、不良后果、疾病转归等均理解。
患者签字:签字时间:年月日
特殊情况下,患者的监护人、近亲属、授权委托人请在此处签字:
签字: 签字时间: 年月日
与患者关系:。
知情同意书模板(医疗)

知情同意书模板(医疗)[患者姓名]本书是为了确保 [患者姓名](以下简称“患者”)在进行医疗诊疗和治疗过程中能够充分了解相关信息,自主选择,并明确同意相关医疗行为和风险而编写的。
在您签署本知情同意书之前,我们将向您详细介绍医疗诊疗和治疗的目的、方法和可能的风险。
请您在仔细阅读并充分理解以下内容后,签署本知情同意书,表示您已明确同意。
1. 医疗诊疗和治疗目的详细描述医疗诊疗和治疗的目的和预期效果。
2. 医疗诊疗和治疗方法对医疗诊疗和治疗过程中采用的具体方法进行详细说明。
3. 风险和不确定性列举可能存在的风险和不确定性,包括但不限于身体损伤、疾病恶化等。
4. 替代选择描述可能存在的医疗诊疗和治疗的替代选择,并说明其优缺点。
5. 知情同意的自愿性明确表达患者签署本知情同意书的自愿性,并强调可以随时撤销同意。
6. 知情同意的理解患者确认已充分了解医疗诊疗和治疗的目的、方法、风险及可能的替代选择,并已提出相应问题,得到令其满意的答复。
7. 知情同意的签署患者在明确理解医疗诊疗和治疗的相关信息之后,应签署本知情同意书。
8. 被委托人签署在患者无能力或未满法定年龄的情况下,其法定监护人或依法取得患者监护权的人应签署本知情同意书。
9. 监护人同意的撤销若被委托人在签署本知情同意书后,患者取得明确自主决策能力,且能够真实表达自己意愿时,患者可撤销委托人的知情同意。
10. 其他事项可根据具体情况补充相关医疗法律条款或其他需要明确的事项。
请您在签署本知情同意书之前,再次仔细阅读并确保充分理解上述内容。
如果您有任何疑问,您可以随时向医疗团队提出。
感谢您的合作![医疗机构名称] [日期]。
患者知情同意书模板范文

患者知情同意书模板范文尊敬的患者/患者家属:您好!在我们开始相关医疗活动之前,有些重要的事情得跟您唠唠,就像朋友之间交底一样。
一、病情状况。
咱先说说您(患者)现在的情况。
您这身体呀,就像一辆有点小毛病的汽车(这么说您可别介意哈,就是方便理解)。
您现在得的[具体疾病名称]呢,就好比汽车发动机某个零件有点磨损,导致整个车的运行不太顺畅。
我们医生呢,就像是汽车修理工,得想办法把您这“发动机”修好。
不过呢,这病可不是那种一下子就能弄好的小问题。
它可能会让您觉得[描述一些疾病带来的不适症状,比如老是头疼,就像有个小锤子在脑袋里时不时敲一下;或者浑身没力气,就像背着个重重的壳]。
而且这个病在治疗过程中可能还会出现一些变化,就像天气一样,有时候晴空万里,有时候突然就乌云密布了。
比如说,病情可能会突然加重一点,不过您也别太担心,这就像汽车在修理的时候可能会发现一些新的小毛病一样,我们医生都会有应对的办法。
二、建议的治疗方案。
那针对您的情况,我们想了这么个治疗方案,就像给汽车制定修理计划一样。
# (一)治疗方法。
我们打算采用[具体治疗方法,如药物治疗、手术治疗等]。
要是药物治疗呢,就像是给您的身体注入一些小小的“修理工”,这些药物会在您的身体里跑来跑去,找到那些出问题的地方,然后想办法修复。
但这过程中可能会有点小“副作用”,就像这些小“修理工”有时候可能会不小心在其他地方捣鼓出一点小动静。
比如说,可能会让您觉得有点恶心,或者胃口不太好,就像您吃多了东西不消化的那种感觉。
要是手术治疗呢,这就像是对汽车进行一次大检修。
我们得把您身体里有问题的部分“拆开”,然后把坏掉的“零件”修好或者换一个新的。
不过手术可是个大事情,就像大检修汽车一样,有一定的风险。
手术过程中可能会出现出血的情况,这就像汽车修理的时候不小心弄破了油管一样,不过我们医生会在旁边盯着,一旦有这种情况就会马上处理。
术后呢,您还得有个恢复期,就像汽车修好后还得磨合一段时间一样。
知情同意书(模板)

知情同意书知情同意书•知情告知页尊敬的先生/女士:经医生检查您已被确诊为XXX,我们诚挚邀请您参加由XXX有限公司发起XXX。
一、研究背景疾病介绍XXX是严重威胁XXXXX。
国内外的治疗情况XXX研究药物的介绍XX类药物是广泛应用于XXX,属于化学药品XX类。
二、临床研究项目介绍本研究为XX试验。
本研究由XX有限公司发起,计划完成试验的XX患者不少于XX例,计划最多入组XX例,预计在全国XX家中心开展,XX医院作为组长单位。
主要目的是观察XX患者中的安全性。
三、哪些人适合参加研究满足全部入选标准方可入选:(1)受试者充分了解试验目的、性质、方法以及可能发生的不良反应,自愿参加研究,并在研究程序开始前签署知情同意书;(2)XX符合下列条件之一的受试者将不得入选试验:(1)对XX有过敏史者;(2)XXX;(3)研究者判断不适宜参加本项临床研究的受试者。
四、临床研究的流程1、签署知情同意书;2、进行临床研究的入组筛选;3、如您满足XXX试验流程包含的具体内容如下:筛选期研究医生将与您一起阅读这份知情同意书。
试验期经研究者判断您可以入选本研究后,我们会分配给您一个受试者随机编号XXXXXX。
五、受试者的责任和义务如果您选择参加本研究,请您如实地告诉研究医生有关自身病史和当前身体状况的真实情况,告诉研究医生自己是否曾参与其他研究,或目前正参与的其他研究。
在研究期间,您需要按时到医院访视、接受检查;您需要向医生报告在研究过程中您身体和精神方面的任何改变,无论这种改变是否与研究有关。
请您务必告知您的医生您目前正在使用以及在研究期间使用的任何其它药物,不得使用受限制的药物。
研究期间,请您不要使用任何其他抗肿瘤治疗的药物,如需其他治疗,请事先与您的医生联系,以获得正规医学指导。
如果您选择参加本研究,我们希望您能够坚持完成全部研究过程。
此外,在您参加试验之前,试验期间,您需要注意以下事项:在开始药物治疗前XXX。
六、可能的受益您将可能从本项研究中受益,此种受益包括您的病情可能获得改善,同时您的参与也将为评价该药物的安全性和有效性做出贡献,使更多的患者获得更好的治疗,在此,我们向您表示感谢。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
【个人简历范文】
知情同意书格式
1、标题双方单位名称事由,协议书三部分组成。
2、正文条款内容
1、同意目的
2、同意目的责任
3、协议的时间和期限
4、同意目的条款和酬金{价格明确总额大写必须明确货币种类}
5、履行条款期限
6、违反条款的责任处理
7、落款{签署}
8、签署日期
知情同意书
研究批准文号受试者姓名
身份证号·联系电话
住址
尊敬的受试者
您将被邀请参加一项临床研究,本知情同意书提供给您一些信息,在您决定是否参加这项研究之前,请尽可能仔细阅读以下内容。
它可以帮助您了解该项研究以及为何要进行这项研究,研究的程序和期限,参加研究后可能给您带来的益处、风险和不适。
如果您愿意,您也可以和您的亲属、朋友一起讨论,或者请医生给予解释,帮助您做出决定。
一、研究背景和研究目的
研究背景(包括该药物或医疗器械国内、国外研究进展)
本研究目的简要说明研究要达到的最终目标(评价新药物或新医疗器械的安全性及有效
性)
二、研究简介
关于此项临床研究的基本资料(包括本研究是否已通过伦理委员会审核、研究概况、主要研究内容、过程与期限、检查操作等)。
研究概况
(本研究将在医院科(或研究中心)进行,预计有名受试者自愿参加,受试者入选条件、告知受试者可能被分配到研究的不同组别等。
)
(本研究已经得到批准,伦理委员会已经审议此项研究是遵从赫尔辛基宣言原则,符合医疗道德的。
)
主要研究内容
过程与期限
检查操作
三、哪些人不宜参加研究
根据不同研究目的和研究药物规定的人群,另外还有1)正参加其它临床研究的患者;2)研究人员认为其它原因不适合临床研究者。
四、如果参加研究将需要做什么?
1.在您入选研究前,医生将询问、(记录您的病史,并进行检查。
您是合格的纳入者,您可自愿参加研究,签署知情同意书。
如您不愿参加本项研究,我们将按您的病情和意愿给予其它适当的处理。
2、若您自愿参加研究,将按以下步骤进行
简单叙述受试者分配流程,告知受试者可能被分配到研究的不同组别、给药方法(药物剂量、疗程、使用说明和注意事项、药物生产厂家和批号;采用的治疗和诊断仪器生产厂家、生产企业许可证、注册证号等)
受试者到医院进行检查和随访的时间、次数、注意事项。
3、作为受试者需要您配合的其它事项
您必须按医生和您约定的随访时间带着来医院就诊(随访阶段,医生可能通过电话、登门的方式了解您的情况)。
对您的随访非常重要,因为医生将判断您接受的治疗是否真正起作用,并及时对您进行指导。
您必须按医生指导用药,并请您及时、客观地填写您的用药记录。
您在每次随访时都必须归还未用完的药物及其包装,并将正在服用的其它药物带来,包括您有其它合并疾病须继续服用的药物。
在研究期间您不能使用治疗的其它药物。
如您需要进行其它治疗,请事先与您的研究医生取得联系。
关于饮食、生活起居有如下规定
五、参加研究可能的受益
写明受试者可能获得的受益尽管已经有证据提示有满意的疗效,但这并不能保证对您肯定有效。
本研究所采用的也不是治疗的唯一的方法。
如对您的病情无效,您可以向医生询问有可能获得的替代治疗方法。
六、参加研究可能出现的不良反应、风险和不适、不方便
告知参加研究可能出现的不良反应(已预知及未预知)、研究过程中的检查等可能造成的风险和不适、不方便,并明确表明对其的处理方案和可能的补偿方案。
例如果在研究期间您出现任何不适,或病情发生新的变化,或任何意外情况,不管是否与研究有关,均应及时通知您的医生,他/她将对此作出判断并给予适当的医疗处理。
您在研究期间需要按时到医院随访,做一些检查,这些占用您的一些时间,也可能给您造成麻烦或带来不方便。
七、费用
告知受试者诊断和治疗过程中哪些费用可免,哪些需要自己负担;
告知受试者出现不良反应时,申办者是否负担处理不良反应的费用和患者可能获得的赔偿。
如(医生将尽全力预防和治疗由于本研究可能带来的伤害。
如果在临床研究中出现不良事件,被证实确实与临床研究有关。
申办者将按照我国相关法律或指导原则的规定,对与研究相关的损害提供诊断治疗的费用及相应的经济赔偿)。
对于您同时合并的其它疾病所需的治疗和检查,将不在免费的范围之内。
参加本研究的报酬。
八、个人信息及医疗记录的保密
有关您身份的记录都是保密的,您的姓名不会出现在病例记录表、任何相关研究报告和公开出版物中。
您的医疗记录(研究病历/CRF、化验单等)将完整地保存在您所就诊的医院。
医生会将化验检查结果记录在您的住院或门诊病历上。
在必要情况下只有研究者、申办者、监查员、伦理委员会和药品监督管理部门有权查阅您所有的研究记录资料。
我们将在法律允许的范围内,尽一切努力保护您个人医疗资料的隐私。
您有权在研究期间,随时了解与自己有关的信息资料。
九、怎样获得更多的信息?
在研究过程中,如果您有任何与本项研究有关的疑问或不理解的事情,您随时可向负责研究的医师提出。
您的医生将给您留下他/她的电话号码以便能回答您的问题。
联系人(研究者或有关人员姓名)电话号码
如果在研究过程中有任何重要的新信息,可能影响您继续参加研究的意愿时,您的医生将会及时通知您。
十、可以自愿选择参加研究或中途退出研究
是否参加研究完全取决于您的意愿。
您可以拒绝参加此项研究,或在研究过程中的任何时间退出本研究,这都不会影响您和医生间的关系,不会因退出遭到歧视或报复,不会影响您的医疗待遇与权益。
出于对您的最大利益考虑如果您需要其它治疗,或者您没有遵守研究计划,或者发生了与研究相关的损伤或者有任何其它原因,研究医师可以终止您继续参与本项研究。
如果您因为任何原因从研究中退出,您可能被询问有关您使用研究药物的情况。
如果医生认为需要,您也可能被要求进行相关实验室检查和体格检查。
十一、现在该做什么?
是否参加本项研究由您自己(和您的家人)决定。
在您做出参加研究的决定前,请尽可能向你的医生询问有关问题,直至您对本项研究完全理解。
感谢您阅读以上材料。
如果您决定参加本项研究,请告诉您的医生,他/她会为您安排一切有关研究的事务。
请您保留这份资料。
我已经阅读了上述有关本研究的介绍,而且有机会就此项研究与医生讨论并提出问题。
我提出的所有问题都得到了满意的答复。
我知道参加本研究可能产生的风险和受益。
我知晓参加研究是自愿的,我确认已有充足时间对此进行考虑,而且明白
1、我可以随时向医生咨询更多的信息。
2、我可以随时退出本研究,而不会受到歧视或报复,医疗待遇与权益不会受到影响。
3、如果因病情变化我需要采取其它治疗,我会在事先征求医生的意见,或在事后如实告诉医生。
4、如果我没有遵守研究计划,或者发生了与研究相关的损伤或者有任何其它原因,研究医师可以终止我继续参与本项研究。
我将获得一份经过签名并注明日期的知情同意书副本。
最后,我决定同意参加本项研究,并保证尽量遵从医嘱。
受试者姓名________________________ 受试者签名_________________________
签字日期______ 年________月________日联系电话,手机
三、医生声明
我确认已向受试者充分解释了本项研究的详细情况,包括其权益以及可能的受益和风险,并给其一份签署过的知情同意书副本。
研究者姓名______________________ 研究者签名_________________________
日期______ _年________月________日工作电话,手机*******
(注如果受试者不识字时尚需见证人签名,如果受试者无行为能力时则需法定代理人签名)。
