有机化学-红外光谱共20页文档
合集下载
红外光谱(最全最详细明了)课件

THANKS
感谢观看样ຫໍສະໝຸດ 制备固体样品液体样品
气体样品
注意事项
研磨成粉末,与KBr混合 压片或涂在ZnSe窗片上
。
稀释在适当的溶剂中, 涂在CaF2或ZnSe窗片
上。
通过干燥管进入光谱仪 。
避免样品中的水分和二 氧化碳干扰,确保样品
纯净。
实验操作
打开红外光谱仪电源,预热 稳定。
调整仪器至最佳状态,如光 路对中、调零等。
对实验操作的要求
总结词
红外光谱实验操作需要一定的技巧和经验,以确保结 果的准确性和可靠性。
详细描述
红外光谱实验涉及到样品的制备、仪器操作和谱图解析 等多个环节。每个环节都需要一定的技巧和经验,以确 保结果的准确性和可靠性。例如,在样品的制备过程中 ,需要选择合适的制样方法,以获得均匀、平整的样品 ;在仪器操作中,需要正确设置参数,以保证谱图的质 量;在谱图解析中,需要具备丰富的经验和专业知识, 以准确解析谱图特征。因此,进行红外光谱实验的人员 需要经过专业培训和实践经验的积累。
红外光谱(最全最详细 明了)课件
contents
目录
• 红外光谱基本原理 • 红外光谱与分子结构的关系 • 红外光谱的应用 • 红外光谱实验技术 • 红外光谱的局限性
01
红外光谱基本原理
红外光谱的产生
分子振动
分子中的原子或分子的振动,导致偶 极矩变化。
偶极矩变化
辐射吸收
分子吸收特定波长的红外光,导致振 动能级跃迁。
02
01 03
放入样品,记录光谱。
实验结束后,关闭仪器,清 理样品。
04
05
注意事项:保持室内温度和 湿度的稳定,避免仪器受到
红外吸收光谱讲课文档

CH
NH OH
2800-3000cm-1
3000-3600cm-1
第十二页,共72页。
分子中基团的基本振动形式
伸缩振动 亚甲基:
弯曲振动
亚甲基
第十三页,共72页。
影响峰位变化的因素
❖ (1) 内部因素
❖ ① 电子效应 ❖ 1)诱导效应:由于取代基具有不同的电负性,通过静电诱导
作用,引起分子中电子分布的变化,从而引起键力常数的变化, 改变了基团的特征频率,这种效应通常称为诱导效应。
(3)炔烃
❖ 末端炔烃的C-H伸缩振动一般在3300 cm-1处出现
强的尖吸收带。
❖
一取代:2150~2100cm-1
❖ C≡C伸缩振动
❖
二取代:2270~2150cm-1
第二十九页,共72页。
(4)芳烃
❖ vC-H:3100~3000cm-1 ❖ γC-H:面外弯曲振动在900~650cm-1,反映苯环上取代
动光谱,简称振转光谱。
❖ 分子在未受光照射之前,能量处于最低能级, 称之为基态。
❖ 当分子受到红外光的辐射,产生振动能级的跃迁, 在振动时伴有偶极矩改变者就吸收红外光子,形 成红外吸收光谱。
第三页,共72页。
区域 λ(μm)
σ(cm-1 )
能级跃迁类型
近红外 0.ቤተ መጻሕፍቲ ባይዱ5~2.5 13330~4000 OH 、NH及CH键倍频吸收区
❖ (2) 照射分子的红外光的频率与分子某种振动的频率相 同时(红外=振),分子吸收能量后,才能产生跃迁,在 红外谱图上出现相应的吸收带。
第五页,共72页。
❖ 已知任何分子就其整个分子而言,是呈电中性 的,但由于构成分子的各原子因价电子得失的 难易,而表现出不同的电负性,分子也因此而 显示不同的极性。
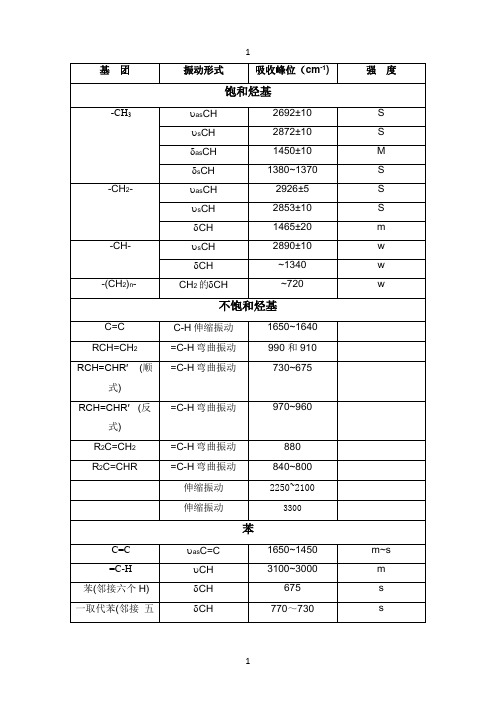
(完整word版)红外光谱各基团出峰位置
CH
810~750
s
725~680
m
五取代(孤H)
CH
870
s
1,3,5三取代(孤H)
CH
865~810
s
730~675
s
羟基
OH
OH(游离)
3600
m(尖)
OH(締合)
3300
s(宽)
C-OH(伯醇)
C-O
1050
s(宽)
C-OH(仲醇)
C-O
1100
s(宽)
C-OH(叔醇)
C-O
1150
s(宽)
2250~2100
伸缩振动
3300
苯
C=C
asC=C
1650~1450
m~s
=C-H
CH
3100~3000
m
苯(邻接六个H)
CH
675
s
一取代苯(邻接 五个H)
CH
770~730
s
710~690
s
邻二取代苯(邻接四个H)
CH
770~730
s
对二取代苯(邻接二个H)
CH
860~800
s
间二取代苯(邻接三个
较特征
酸酐(RCO)2O
C=O
1880~1800
S
C-O-C
1800~1750
S
1170~1050
S
酰胺(RCONH2)
C=O
1690~1650
S(酰胺Ⅰ峰)
N-H
3500~3050
m
N-H
1650~1620
m(酰胺Ⅱ峰)
硝基
R-NO2
asNO2
1560~1545
810~750
s
725~680
m
五取代(孤H)
CH
870
s
1,3,5三取代(孤H)
CH
865~810
s
730~675
s
羟基
OH
OH(游离)
3600
m(尖)
OH(締合)
3300
s(宽)
C-OH(伯醇)
C-O
1050
s(宽)
C-OH(仲醇)
C-O
1100
s(宽)
C-OH(叔醇)
C-O
1150
s(宽)
2250~2100
伸缩振动
3300
苯
C=C
asC=C
1650~1450
m~s
=C-H
CH
3100~3000
m
苯(邻接六个H)
CH
675
s
一取代苯(邻接 五个H)
CH
770~730
s
710~690
s
邻二取代苯(邻接四个H)
CH
770~730
s
对二取代苯(邻接二个H)
CH
860~800
s
间二取代苯(邻接三个
较特征
酸酐(RCO)2O
C=O
1880~1800
S
C-O-C
1800~1750
S
1170~1050
S
酰胺(RCONH2)
C=O
1690~1650
S(酰胺Ⅰ峰)
N-H
3500~3050
m
N-H
1650~1620
m(酰胺Ⅱ峰)
硝基
R-NO2
asNO2
1560~1545
红外光谱图文课件PPT

红外光谱可以监测化学反应过程中分 子结构的动态变化,有助于理解反应 机理。
04
红外光谱实验技术
Байду номын сангаас
样品制备技术
01
02
03
固体样品制备
将样品研磨成粉末,然后 与KBr混合压制成透明片 或与Ge晶片接触测量。
液体样品制备
将液体样品涂在CaF2或 NaCl晶片上,或使用液膜 法测量。
气体样品制备
将气体样品通过吸收池, 利用适当的吸收剂吸收后 进行测量。
红外光谱的表示方法
谱图
红外光谱图是以波长为横坐标,以透 射比或吸光度为纵坐标绘制的图谱。
峰的位置与强度
特征峰与峰带
特征峰是指特定官能团对应的吸收峰, 峰带则是由多个特征峰组成的区域, 可以反映分子中存在的官能团及其结 构特征。
峰的位置表示特定波长的红外光被吸 收,峰的强度则反映该波长下分子振 动的程度。
红外光谱图文课件
目录
• 红外光谱基本概念 • 红外光谱与分子结构的关系 • 红外光谱的应用 • 红外光谱实验技术
01
红外光谱基本概念
红外光谱的产生
分子振动
分子中的原子或分子的振动会产 生能量变化,当这些变化与红外 光相匹配时,光被吸收,形成红 外光谱。
分子振动类型
分子振动主要有伸缩振动和弯曲 振动两种类型,伸缩振动是指原 子沿键轴方向的往复运动,弯曲 振动则是指分子构型的变化。
02
仪器维护
定期对仪器进行校准和维护,确保测量准确性。
03
安全防范措施
了解并遵守实验室安全规定,避免直接接触有毒有害物质;在操作过程
中注意防止气体泄漏和火灾事故的发生;实验结束后,应按照实验室规
定正确处理废弃物。
04
红外光谱实验技术
Байду номын сангаас
样品制备技术
01
02
03
固体样品制备
将样品研磨成粉末,然后 与KBr混合压制成透明片 或与Ge晶片接触测量。
液体样品制备
将液体样品涂在CaF2或 NaCl晶片上,或使用液膜 法测量。
气体样品制备
将气体样品通过吸收池, 利用适当的吸收剂吸收后 进行测量。
红外光谱的表示方法
谱图
红外光谱图是以波长为横坐标,以透 射比或吸光度为纵坐标绘制的图谱。
峰的位置与强度
特征峰与峰带
特征峰是指特定官能团对应的吸收峰, 峰带则是由多个特征峰组成的区域, 可以反映分子中存在的官能团及其结 构特征。
峰的位置表示特定波长的红外光被吸 收,峰的强度则反映该波长下分子振 动的程度。
红外光谱图文课件
目录
• 红外光谱基本概念 • 红外光谱与分子结构的关系 • 红外光谱的应用 • 红外光谱实验技术
01
红外光谱基本概念
红外光谱的产生
分子振动
分子中的原子或分子的振动会产 生能量变化,当这些变化与红外 光相匹配时,光被吸收,形成红 外光谱。
分子振动类型
分子振动主要有伸缩振动和弯曲 振动两种类型,伸缩振动是指原 子沿键轴方向的往复运动,弯曲 振动则是指分子构型的变化。
02
仪器维护
定期对仪器进行校准和维护,确保测量准确性。
03
安全防范措施
了解并遵守实验室安全规定,避免直接接触有毒有害物质;在操作过程
中注意防止气体泄漏和火灾事故的发生;实验结束后,应按照实验室规
定正确处理废弃物。
红外光谱最全最详细明了

CH3-CO-CH3 CH2Cl-CO-CH3 CI-CO-CH3 Cl-COCl F-CO-F
υC=O 1715
1724
1806
1828 1928
第31页/共108页
(2)共轭效应(C效应): 共轭效应要求共轭体系有共平面性。
共轭效应使共轭体系的电子云密度平均化,键长也平均 化,双键略有伸长,单键略有缩短。
如乙酰乙酸乙酯有酮式和烯醇式结构,两者的吸收皆能 在红外谱图上找到,但烯醇式的υC=O较酮式υC=O弱,说 明稀醇式较少。
CH3-CO-CH2-COO-C2H5 υC=O 1738(s),1717(s)
CH2-C(OH)=CH-COOC2H5 υC=O与υC=C在1650cm-1(w) υOH3000cm-1
C=C 1780
1646
CH2
1611
CH2
1566
CH2
1641 cm-1
1678
1657
1651 cm-1
第37页/共108页
(5)氢键的影响:氢键的形成,往往使伸缩振动频率移向 低波数,吸收强度增强,并变宽;形成分子内氢键时影响很 显著。
O OH
H OO
υC=O ( cm-1)
O
O
1676,1673; 1675,1622
第15页/共108页
问题:C=O 强;C=C 弱;为什么?
吸收峰强度跃迁几率偶极矩变化
吸收峰强度 偶极矩的平方
偶极矩变化——结构对称性;
对称性差偶极矩变化大吸收峰强度大
符号:S (strong)
M (medium) W (weak)
B (broad)
Sh (sharp)
红外吸收峰强度比紫外吸收峰小2~3个数量级;
红外光谱(最全_最详细明了)、、ppt课件

M (medium) W (weak)
B (broad)
Sh (sharp)
红外吸收峰强度比紫外吸收峰小2~3个数量级;
精选PPT课件
17
精选PPT课件
18
1.2 红外光谱仪及实验方法
(1)仪器类型与结构
两种类型:色散型 干涉型(傅立叶变换红外光谱仪)
精选PPT课件
19
1. 内部结构
日本岛津公司的 DT-40 FT-IR
环内双键,张力越大,伸缩振动频率越低, 但是环丙烯例外。 环外双键,张力越大,伸缩振动频率越高。
精选PPT课件
37
环内双键的吸收频率, 对环的大小很敏感, 吸收频率随 环内角的变小而降低,环丁烯(内角90 o) 达最小值, 继续 变小至环丙烯(内角60 o)吸收频率反而升高.
C=C 1650
CH2
精选PPT课件
29
某一基团的特征吸收频率,同时还要受到分子结构 和外界条件的影响。
同一种基团,由于其周围的化学环境不同,其特征吸 收频率会有所位移,不是在同一个位置出峰。
基团的吸收不是固定在某一个频率上,而是在一个范围 内波动。
精选PPT课件
30
1.3.1 外部条件对吸收位置的影响
(1)物态效应:同一个化合物固态、液态和气态的红外光谱 会有较大的差异。如丙酮的υC=O,汽态时在1742cm-1,液态 时1718cm-1,而且强度也有变化。
共轭效应使共轭体系的电子云密度平均化,键长也平均 化,双键略有伸长,单键略有缩短。
共轭体系容易传递静电效应,常显著地影响基团的吸 收位置及强度。
共轭体系有“π-π”共轭和“P-π”共轭。
基团与吸电子基团共轭(受到-C效应),使吸收频率 升高;与给电子基团共轭(受到+C效应)使基团吸收频 率降低。
《红外光谱》PPT课件

)
(cm-1) = 104 / λ (μ m)
纵坐标:吸光度(A)或透光率(T) 多以百分透光率T%来表示
*
T = I / I0 (遵守Lambert-Beer定律
)
A = lg (1 / T)
IR中,“谷”越深(T越小),吸光 度越大,吸收强度越强。
*
二、红外光谱基本原理
满足两个条件: (1)辐射能满足物质产生振动能级跃迁所需的能量; (2)伴随净的偶极矩的变化。
*
对称伸缩振动s 非对称伸缩振动as 剪式振动
面内摇摆
*
面外摇摆
扭曲振动
分子振动自由度
研究多原子分子时,常把复杂振动分解为许多简单的基本振动, 这些基本振动数目称为分子的振动自由度,简称分子自由度。
原子在三维空间的位置可用x,y,z表示,即3个自由度。
含N个原子的分子,分子自由度的总数为3N个。
分子总的自由度3N=平动自由度+转动自由度+振动自由度
非线性分子:3N-6 (平动3、转动3) 线性分子:3N-5 (平动3、转动2)
*
峰位、峰数与峰强
(1)峰位 化学键的力常数K越大,原子折合质量越小,键的
振动频率越大,吸收峰将出现在高波数区(短波长区);反之, 出现在低波数区(高波长区)。
(2)峰数 峰数与分子自由度有关。无瞬间偶极距变化时, 无红外吸收。
(3)瞬间偶基距变化大,吸收峰强;键两端原子电负性相差越 大(极性越大),吸收峰越强。
(4)由基态跃迁到第一激发态,产生一个强吸收峰,基频峰。
(5)由基态跃迁到第二激发态或更高激发态,产生的弱的吸收 峰,倍频峰。
*
影响吸收谱带位置的主要因素(内部因素)
1. 诱导效应(I效应)
(cm-1) = 104 / λ (μ m)
纵坐标:吸光度(A)或透光率(T) 多以百分透光率T%来表示
*
T = I / I0 (遵守Lambert-Beer定律
)
A = lg (1 / T)
IR中,“谷”越深(T越小),吸光 度越大,吸收强度越强。
*
二、红外光谱基本原理
满足两个条件: (1)辐射能满足物质产生振动能级跃迁所需的能量; (2)伴随净的偶极矩的变化。
*
对称伸缩振动s 非对称伸缩振动as 剪式振动
面内摇摆
*
面外摇摆
扭曲振动
分子振动自由度
研究多原子分子时,常把复杂振动分解为许多简单的基本振动, 这些基本振动数目称为分子的振动自由度,简称分子自由度。
原子在三维空间的位置可用x,y,z表示,即3个自由度。
含N个原子的分子,分子自由度的总数为3N个。
分子总的自由度3N=平动自由度+转动自由度+振动自由度
非线性分子:3N-6 (平动3、转动3) 线性分子:3N-5 (平动3、转动2)
*
峰位、峰数与峰强
(1)峰位 化学键的力常数K越大,原子折合质量越小,键的
振动频率越大,吸收峰将出现在高波数区(短波长区);反之, 出现在低波数区(高波长区)。
(2)峰数 峰数与分子自由度有关。无瞬间偶极距变化时, 无红外吸收。
(3)瞬间偶基距变化大,吸收峰强;键两端原子电负性相差越 大(极性越大),吸收峰越强。
(4)由基态跃迁到第一激发态,产生一个强吸收峰,基频峰。
(5)由基态跃迁到第二激发态或更高激发态,产生的弱的吸收 峰,倍频峰。
*
影响吸收谱带位置的主要因素(内部因素)
1. 诱导效应(I效应)
有机化合物的红外光谱PPT课件

1
vCH 2890cm-1。 (3)醛氢的 vC-H 与δCH 的倍频产生费米共振,出现双峰:
2840 、 2720cm-1。
(4)环丙烷的 vC-H 在3060cm-1附近,随着环的增大,频
率下降至3000cm-1以下。
第12页/共90页
烃类化合物中,vC-H频率与C原子杂化状态
有关,杂化C原子的s成分比例越高,其电负性越
第53页/共90页
1820
1820cm-1附近的弱峰为δ=CH2(面外)的
倍频峰,可帮助鉴定 C=CH2结构。
第54页/共90页
700
970
第55页/共90页
1820 1650
990 910
965
第56页/共90页
(2)芳氢的弯曲振动吸收峰
芳氢的δ面内吸收峰位于1250~950cm-1,有 5~6个中、弱吸收带,应用较少。
指纹区:
1300~600cm-1
第1页/共90页
特定的基团具有类似的吸收带,这种吸收(带)称为特征吸收,其振动频率称 为特征频率或基团频率(group frequency)。它是与一定的结构单元相联系的 振动频率。
同一类型的基团在不同物质中所处的化学环境各不相同,因此其基团频率有一 定的差别。这种差别常常能反映出结构上的特点。
本书将中红外区分为七个区段。
第2页/共90页
一、 红外光谱的七个重要区段
1. O-H、N-H 伸缩振动区。
2. Y-H 伸缩振动区(Y=C、S、B、P 等)。
3. 三键及累积双键伸缩振动区。
4. C=O伸缩振动区。
5. C=C伸缩振动区。
6. C-H面内弯曲振动、C-O及C-N伸缩振
动区。
第3页/共90页
vCH 2890cm-1。 (3)醛氢的 vC-H 与δCH 的倍频产生费米共振,出现双峰:
2840 、 2720cm-1。
(4)环丙烷的 vC-H 在3060cm-1附近,随着环的增大,频
率下降至3000cm-1以下。
第12页/共90页
烃类化合物中,vC-H频率与C原子杂化状态
有关,杂化C原子的s成分比例越高,其电负性越
第53页/共90页
1820
1820cm-1附近的弱峰为δ=CH2(面外)的
倍频峰,可帮助鉴定 C=CH2结构。
第54页/共90页
700
970
第55页/共90页
1820 1650
990 910
965
第56页/共90页
(2)芳氢的弯曲振动吸收峰
芳氢的δ面内吸收峰位于1250~950cm-1,有 5~6个中、弱吸收带,应用较少。
指纹区:
1300~600cm-1
第1页/共90页
特定的基团具有类似的吸收带,这种吸收(带)称为特征吸收,其振动频率称 为特征频率或基团频率(group frequency)。它是与一定的结构单元相联系的 振动频率。
同一类型的基团在不同物质中所处的化学环境各不相同,因此其基团频率有一 定的差别。这种差别常常能反映出结构上的特点。
本书将中红外区分为七个区段。
第2页/共90页
一、 红外光谱的七个重要区段
1. O-H、N-H 伸缩振动区。
2. Y-H 伸缩振动区(Y=C、S、B、P 等)。
3. 三键及累积双键伸缩振动区。
4. C=O伸缩振动区。
5. C=C伸缩振动区。
6. C-H面内弯曲振动、C-O及C-N伸缩振
动区。
第3页/共90页
有机化学波谱-红外

多聚体 游离
0.01mol/L
多聚体
游离 二聚体
0.1mol/L
1.0 mol/L
不同浓度 环己醇的 IR光谱
h: 环张力的影响
当环有张力时, 环内各键削弱(C-C键成弯曲键, P电 子成分增高), 键角的缩小使双键性减弱, 环内双键伸
缩振动频率下降, 而环外双键伸缩振动频率增高.
化合物
ν
C=C
/cm-1
弯曲振动
1000650cm-1
R1CH=CHR2(反式) 980~960cm-1(vs) R1CH=CHR2(顺式) 730~665cm-1(m, 宽) (特征性弱) 三取代乙烯 850~790cm-1(m) (特征性弱)
例1: 1-己烯的红外光谱图(KBr压片法)
例2: 环己烯的红外光谱图(KBr压片法)
c: 光速, 3×1010cm/s K: N· m-1 µ:原子质量单位为单位
影响吸收频率的因数
(1). 键的力常数K的影响. 化学键键能越大↑ 力常数越大↑ 振动频率↑
a: 成键方式的影响
键类型 力常数 ν /cm-1 2150 1650 1200
C C
C C
C C
b: 振动类型的影响
振动类型 ν /cm-1
红外光谱
1600~3700cm-1 官能团吸收区
吸收峰密集, 难以 辨认, 但如同人的 指纹一样, 化合物 结构上的细微变 化都有反映 <1600cm-1 指纹区
C-C, C-N, C-O伸缩振动 及弯曲振动
2500~3700cm-1
2100~2400cm-1
1600~1800cm-1
Y-H 伸缩振动区 (O-H, N-H, C-H)
常见有机化合物的红外光谱讲课文档

2. 芳环骨架ν(C=C):1600 cm-1和1500 cm-1
所以,芳烃的存在可由3030、1600、1500cm-1 的谱带来判断
第二十页,共34页。
22002222//11//1144
500 cm-1
特征:υC=C 在1600、1580cm-1 , 1500、1450cm-1 出现1~4个峰,可看作两组
特征:甲酸酯1180cm-1,乙酸酯1240cm-1,丙酸以上的酯1190cm-1 ,甲酯1165cm-1
第二十九页,共34页。
22002222//11//1144
(5) 酰胺
酰胺的特征频率: 酰胺结构中既有羰基又有氨基
酰胺的特征频率主要包括:
① ν(N-H)伸缩振动:
(ⅰ) 伯胺:3500cm-1、3400cm-1出现双峰 ( 游离态 )
第十四页,共34页。
C H 3300 cm-1
22002222//11//1144
(2) C=C 伸缩振动 (1680-1630 cm-1 )
反式烯 三取代烯 四取代烯
R1
H
CC
H
R2
R1
R3
CC
R2
H
R1
R3
CC
R2
R4
顺式烯
R1
R2
CC
H
H
乙烯基烯
R1
H
CC
H
H
亚乙烯基烯 R 1 C C H
R2
谱峰数目只与取代情况有关 而与取代基种类无关。
4. Ar-H变形振动的倍
频吸收峰
2000~1650cm-1出现由 2~6个峰组成的特征峰 群,此倍频区峰的形状 与特定的取代类型相关 联。
第二十三页,共34页。
有机化合物波谱分析红外

分子对称性的影响
----结构对称的分子在发生对称伸缩振动过程中△μ=0,无吸收峰,
对称性差的分子振动吸收时偶极矩变化大,吸收峰强。
振动形式的影响 -----不对称>对称as >s,伸缩振动>弯曲振动>δ
2)跃迁几率:倍频峰的强度主要取决于跃迁几率
15
第十五页,课件共61页
第二章 红外光谱(Infrared spectra IR) (四) 影响IR吸收的因素
23
第二十三页,课件共61页
第二章 红外光谱(Infrared spectra IR)
3、空间效应(steric effect)
(4)环张力
环内双键C=C伸缩振动频率随环张力的增大而降低,
而C-H向高波数位移
C=C 1646 cm–1 1611 cm–1 =C-H 3017 cm–1 3045 cm–1
C═O(游离)1676 cm–1
1673 cm–1
OH(游离)3615~3605 cm–1
形成分子内氢键,谱带变宽,波数降低,但强度基本不增。 ∵形成氢键,使-O—H+键拉长,偶极矩增加,出现宽峰。
25
第二十五页,课件共61页
第二章 红外光谱(Infrared spectra IR)
稀溶液(游离状态),OH3650~3600cm-1 浓度增加(氢键),OH3515cm-1(二聚体),3350cm-1 (多聚体)
乙醇在 不同浓
度下分
子间氢
键的影 响
26
第二十六页,课件共61页
第二章 红外光谱(Infrared spectra IR)
5、互变异构:峰位移
乙酰乙酸乙酯的酮式与烯醇式异构体
(A)酮型
C=O 1738 cm–1 C=O 1717 cm–1
----结构对称的分子在发生对称伸缩振动过程中△μ=0,无吸收峰,
对称性差的分子振动吸收时偶极矩变化大,吸收峰强。
振动形式的影响 -----不对称>对称as >s,伸缩振动>弯曲振动>δ
2)跃迁几率:倍频峰的强度主要取决于跃迁几率
15
第十五页,课件共61页
第二章 红外光谱(Infrared spectra IR) (四) 影响IR吸收的因素
23
第二十三页,课件共61页
第二章 红外光谱(Infrared spectra IR)
3、空间效应(steric effect)
(4)环张力
环内双键C=C伸缩振动频率随环张力的增大而降低,
而C-H向高波数位移
C=C 1646 cm–1 1611 cm–1 =C-H 3017 cm–1 3045 cm–1
C═O(游离)1676 cm–1
1673 cm–1
OH(游离)3615~3605 cm–1
形成分子内氢键,谱带变宽,波数降低,但强度基本不增。 ∵形成氢键,使-O—H+键拉长,偶极矩增加,出现宽峰。
25
第二十五页,课件共61页
第二章 红外光谱(Infrared spectra IR)
稀溶液(游离状态),OH3650~3600cm-1 浓度增加(氢键),OH3515cm-1(二聚体),3350cm-1 (多聚体)
乙醇在 不同浓
度下分
子间氢
键的影 响
26
第二十六页,课件共61页
第二章 红外光谱(Infrared spectra IR)
5、互变异构:峰位移
乙酰乙酸乙酯的酮式与烯醇式异构体
(A)酮型
C=O 1738 cm–1 C=O 1717 cm–1
