圆二色谱
cd圆二色谱

cd圆二色谱
CD圆二色谱(Circular Dichroism Spectroscopy)是一种用于研究生物分子结构和构象的实验技术。
它主要基于物质对不同的圆偏振光的吸收差异,通过测量对左旋和右旋圆偏振光的吸收来获取信息。
CD圆二色谱广泛应用于蛋白质、核酸、多肽等生物大分子的结构和构象分析。
通过测量样品在紫外可见光谱范围内的圆二色性,可以获取关于其二级结构、螺旋、折叠状态、聚集形式等信息。
在CD圆二色谱实验中,使用CD光谱仪来测量样品吸收的圆二色性。
该仪器发送出圆偏振光,样品对左旋和右旋圆偏振光的吸收程度不同,进而形成不同的CD谱。
通过解析和解释CD谱,可以了解样品分子结构的特征。
CD圆二色谱是一种非破坏性、快速、灵敏的技术,可以用于分析溶液态和固态样品,包括纯样品、混合物和复杂体系。
它在生物化学、生物物理、药物研发等领域有广泛应用,提供了对生物分子结构和构象的研究和解析。
需要注意的是,解释CD圆二色谱结果需要具备相关的专业知识和经验。
圆二色谱和旋光谱概述

圆二色谱和旋光谱概述圆二色谱(circular dichroism spectroscopy,CD)是一种测量分子对具有不同方向旋转的圆偏振光吸收差异的技术。
它通过测量由物质吸收的左旋和右旋圆偏振光的差异,来研究物质的结构和构象。
圆二色谱的基本原理是Kirchhoff定律的直接应用,即分子的吸收光谱是由对电磁场的响应所导致的。
当吸收的光谱与光的旋转相耦合时,出现左旋和右旋圆二色效应。
圆二色谱实验通常通过使用圆偏振光源、样品和检测器组成。
光源通常是通过一个线性偏振器和一个相位均匀的偏振光源来产生的。
样品通常是通过溶液或薄膜的形式存在。
检测器用于测量透射或反射样品的圆二色信号。
测量得到的数据可以表示为贝尔系数,即偏振光旋转的绝对角度。
根据光谱的形状和幅度,可以分析物质的构象和结构。
旋光谱(optical rotation spectroscopy)是测量物质在其中一种溶剂中的光学旋转角度的技术。
它根据物质对线性偏振光的旋转效应研究物质的手性性质。
旋光谱原理是基于贝尔定律,该定律描述一个物质中的旋转既取决于溶液中物质的浓度,又取决于物质本身的旋转率。
旋光谱实验通常使用旋光仪进行测量。
旋光仪由一个光源、走样器、检测器和读数装置组成。
在实验中,光线通过一系列光学元件(如偏振器和波片)来形成线偏振光,然后通过待测物质样品,最后到达检测器。
读数装置可测量旋转对应的光强度变化,并通过校准数据来计算旋转角度。
圆二色谱和旋光谱在许多领域有着广泛的应用。
在有机化学中,它们被广泛用于研究手性分子、构象分析和反应动力学等。
在生物化学和生物物理学中,它们被用于研究蛋白质和核酸的结构和功能。
此外,圆二色谱和旋光谱还被应用于药物发现、金属络合物分析和环境监测等领域。
总之,圆二色谱和旋光谱是两种常用的分析技术,用于研究物质的光学性质和结构。
它们的基本原理和实验方法都是通过测量物质对光的旋转效应来实现的。
这些技术广泛应用于化学、生物学和医药等领域,为科学家研究和理解物质的性质和行为提供了重要工具。
圆二色谱的介绍

圆二色谱的介绍圆二色性circulardichroism对R和L两种圆偏振光吸收程度不同的现象。
这种吸收程度的不同与波长的关系称圆二色谱,是一种测定分子不对称结构的光谱法。
在分子生物学领域中主要用于测定蛋白质的立体结构,也可用来测定核酸和多糖的立体结构。
光是一种电磁波。
假如用电矢量来表示,光的前进就是由矢量端点在一特定的平面里沿正弦波运动的轨迹。
对于自然光讲,正弦波振动的平面是随机的。
如有一束光,它所有的电矢量的振动平面都是相互平行的,这种光称为平面偏振光。
有一种特殊的情况,光前进的过程中电矢量绕前进轴转动,若电矢量的绝对值不变,则运动轨迹的投影是一个圆,这时就变成圆偏振。
面对光前进的方向看去,电矢量端点的圆运动可以是顺时针方向的,也可以是逆时针方向的,因此圆偏振有R与L两种。
假如L与R两束圆偏振光在一起辐射,强度、速度、频率和位相都相同,它们就会叠合成一束平面偏振光。
如波长λ的L光和R光的光强度相等,在光学各向异性物质中传播某一距离后,它们的综合光将变成椭圆偏振光,椭圆的长轴处于两个圆偏振的电矢量相叠合的地方。
假如两个圆偏振的传播速度也不相同,而所经的途径与上述相同,则叠合的椭圆偏振光的长轴与上面所述的椭圆偏振光的长轴相夹θ角(图1)。
由不对称分子组成的物质是光学各向异性的,即L与R两束圆偏振光在这类物质中的传播速度不相等。
假如光学各向异性物质在某一波长λ有吸收,那将在该时对L光和R光有不同的吸收,如该物质的吸光率是A,而对L光和R光的吸光率是AL和AR,AL和AR的差ΔA=AL-AR,称为圆二色性。
从(图2)可看出,因光吸收不同而产生的椭圆的形状与ΔA有直接的关系。
θ称为椭圆值,也是一种定量描述圆二色性的单位。
在条件相同的情况下,θ=3300ΔA。
在蛋白质分子中,肽链的不同部分可分别形成α-螺旋、β-折叠、β-转角等特定的立体结构。
这些立体结构都是不对称的。
蛋白质的肽键在紫外185~240纳米处有光吸收,因此它在这一波长范围内有圆二色性。
圆二色谱

圆二色谱圆二色谱是一种特殊的吸收普,它对手性分子的构象十分敏感,因此它是最重要的光谱实验之一。
手性是物质结构中的重要特征,即具有不能重叠的三维镜像对映异构体,它们的分子式完全相同,但其中原子或原子基团在空间的配置不同,互为镜像。
凡手性分子都具有光学活性,即可使偏振光的振动面发生旋转。
许多有机物和络合物都具有手性,它们的对映异构体物理化学性质(熔点、沸点、旋光度、溶解度、分子式等)几乎完全相同,但它们的旋光方向相反,生理作用大不相同。
生物基础分子一般都具有手性,也都具有光学活性。
在对生物分子手性的研究中,发现了令人惊异至今不解的对称性破缺现象,那就是在自然界中,氨基酸有L型和D型两种对映异构体,天然糖也有L糖和D糖两种糖。
但在生物体中,组成蛋白质的20种氨基酸,除最简单的甘氨酸不具有手性外,其余都是L型的,而生物体核酸中的糖环则都是D型的。
生物体中这种对称性破缺现象是有特殊意义的自然现象。
手性分子都具有光学活性。
当单色左旋与右旋的圆偏振光通过某一种手性样品时,该样品对左、右旋圆偏振光的吸收不同,这叫做圆二色性。
其差值△A=△AL一△AR称为圆二色值,按波长扫描就得到了圆二色谱(CD谱)。
利用法拉第效应,在外加磁场作用下,许多原来没有光学活性的物质也具有了光学活性,原来可测出CD谱的在磁场中CD信号将增大几个量级。
这种条件下即可测得磁圆二色谱(MCD谱)。
CD和MCD是特殊的吸收谱,它们比一般的吸收谱弱几个量级,但由于它们对分子结构十分敏感,因此近十几年来,CD和MCD 已成为研究分子构型和分子间相互作用的最重要的光谱实验之一。
利用CD和MCD 研究生物大分子和药物分子,具有重要的科学意义和实用价值。
基本定义和原理一束平面偏振光通过光学活性分子后,由于左、右圆偏振光的折射率不同,偏振面将旋转一定的角度,这种现象称为旋光,偏振面旋转的角度称为旋光度。
朝光源看,偏振面按顺时针方向旋转的,称为右旋,用“+”号表示;偏振面按逆时针方向旋转的,称为左旋,用“-”号表示。
圆二色谱原理

圆二色谱原理
圆二色谱是一种用来研究化合物结构和手性性质的重要分析方法。
它利用了分子对圆偏振光的吸收和散射的特性,通过测量样品对左旋和右旋圆偏振光的吸收差异来获取信息。
在这篇文档中,我们将详细介绍圆二色谱的原理和应用。
圆二色谱的原理可以简单地理解为分子结构对圆偏振光的选择性吸收。
当圆偏振光通过手性分子时,分子的结构和构型会决定它们对左旋和右旋圆偏振光的吸收差异。
这种差异可以通过检测样品对左旋和右旋圆偏振光的吸收强度来测量,从而得到有关分子结构和手性性质的信息。
在实际的圆二色谱实验中,常用的仪器是圆二色光谱仪。
它包括一个光源、样品室、检测器和数据处理系统。
光源发出线偏振光,经过样品后变成圆偏振光,然后被检测器检测。
通过改变样品室中的样品和检测器的位置,可以测量不同波长下的圆二色光谱,从而获取更为详细的信息。
圆二色谱在化学、生物化学、药学等领域有着广泛的应用。
在药学中,圆二色谱可以用来研究药物的手性纯度和药效学,帮助药物研发和质量控制。
在生物化学中,圆二色谱可以用来研究蛋白质和核酸的结构和构象变化,有助于理解生物大分子的功能和活性。
在化学领域,圆二色谱也可以用来研究手性催化剂和手性配体的性质,为有机合成提供重要的信息。
总之,圆二色谱作为一种重要的分析方法,具有广泛的应用前景和重要的理论意义。
通过对分子对圆偏振光的选择性吸收的测量和分析,可以获取有关分子结构和手性性质的信息,为化学和生物领域的研究提供重要的支持和帮助。
希望本文对圆二色谱的原理和应用有所帮助,谢谢阅读!。
CD圆二色谱解读:探索生物大分子结构之谜

CD圆二色谱解读:探索生物大分子结构之谜一、圆二色谱的神秘面纱圆二色谱(Circular Dichroism,简称CD)是一种光谱学方法,用于研究生物大分子(如蛋白质和核酸)的结构。
它的原理是基于生物大分子对左旋和右旋偏振光的吸收差异。
这种差异反映了生物大分子的立体结构,因此,CD圆二色谱被广泛应用于生物制药分析领域。
二、CD圆二色谱的工作原理CD圆二色谱的工作原理是基于生物大分子的手性。
手性是一种物质的基本性质,表现为对左旋和右旋偏振光的吸收差异。
生物大分子(如蛋白质和核酸)都具有手性,因此,通过测量其对左旋和右旋偏振光的吸收差异,可以获取其立体结构信息。
三、CD圆二色谱的应用CD圆二色谱的应用非常广泛,主要用于生物大分子的结构研究。
例如,通过CD圆二色谱,我们可以确定蛋白质的二级结构,包括α-螺旋、β-折叠和随机卷曲等。
此外,CD圆二色谱还可以用于研究蛋白质的热稳定性、酶活性、配体结合等性质。
四、CD圆二色谱的优势CD圆二色谱的优势在于其简单、快速和无损。
首先,CD圆二色谱的操作简单,只需要将样品溶解在适当的溶剂中,然后通过光谱仪进行测量。
其次,CD圆二色谱的测量速度快,一般只需要几分钟就可以完成。
最后,CD圆二色谱是一种无损检测方法,不会对样品造成损害,因此,可以用于研究生物大分子的动态过程。
五、CD圆二色谱的挑战与未来尽管CD圆二色谱具有许多优势,但也面临一些挑战。
例如,CD圆二色谱对样品的浓度和纯度要求较高,对于浓度低或杂质多的样品,可能无法获得准确的结果。
此外,CD圆二色谱只能提供生物大分子的平均结构信息,无法获取其具体的三维结构。
然而,随着科技的进步,我们有理由相信,CD圆二色谱的应用将更加广泛。
例如,通过结合其他技术(如核磁共振和X射线晶体学),我们可以获取生物大分子的更详细的结构信息。
此外,通过改进光谱仪的设计和优化测量方法,我们可以提高CD圆二色谱的灵敏度和准确性。
图1。
百泰派克生物科技——生物制品表征,多组学生物质谱检测优质服务商。
蛋白的圆二色谱

蛋白的圆二色谱蛋白的圆二色谱是一种用于研究蛋白结构的分析技术。
它利用蛋白分子中的手性分子结构,即氨基酸残基的旋光性,来研究蛋白的结构和构象变化。
圆二色谱常用于研究蛋白的二级结构、折叠和稳定性。
一、圆二色谱的基本原理蛋白分子是由氨基酸残基组成的,其中大部分的氨基酸残基都是手性分子。
这意味着它们在光学方面展现出非对称性,表现为旋光性。
圆二色谱利用蛋白分子中的手性分子结构,即氨基酸残基的旋光性,来研究蛋白的结构和构象变化。
圆二色谱是通过测量不同波长下蛋白分子对左旋圆偏振光和右旋圆偏振光的吸收差异来实现的。
当圆偏振光与分子中的手性分子结构相互作用时,会发生旋光现象,使得左旋圆偏振光和右旋圆偏振光在分子中表现出不同的旋光性。
当光分子与分子中存在旋光性的物质互作用时,光波的振动方向会旋转一个角度,由于物质的旋光性质不同,光波振动方向旋转的角度也不同。
在圆二色谱中,会测量样品对左旋偏振光和右旋偏振光吸收光谱的差异,即圆二色性。
这种差异的大小和方向与样品中手性分子结构的数量和方向有关。
因此,圆二色谱可以用来测量蛋白质中氨基酸残基的旋光性,也可以测量蛋白质分子中不同二级结构之间的圆二色性差异。
二、圆二色谱在蛋白质结构研究中的应用圆二色谱是一种常用的技术,用于研究蛋白质结构和构象变化的。
以下是圆二色谱在蛋白质结构研究中的应用:1.测量蛋白质的二级结构蛋白质的二级结构是指蛋白质分子中独立的α-螺旋、β-折叠等二级结构单元的和其它形式的线性结构的组合。
不同的二级结构单元具有不同的光学活性,并且对圆偏振光具有不同的圆二色性。
因此,通过圆二色谱可以测量蛋白质分子中各种二级结构单元的含量和分布,并且可以动态地跟踪蛋白质分子中二级结构的形成和变化。
2.测量蛋白质分子折叠状态通过圆二色谱还可以测量蛋白质的折叠状态。
我们知道,在不同的环境下,蛋白质分子的折叠状态是不同的。
例如,当蛋白质分子在近体系或在高温、低温等条件下受到变性的影响时,其细胞或组织的功能将会受到严重的影响。
圆二色谱

0
TM-36 aqueous
-5
TM-36 + TFE
-10
MRE MRE
Effect of 50% TFE on a monomeric peptide
0
peptide in water
peptide in 50% TFE
-5
-10
-15
TFE
-20
-25
-30
-35
200
210
220
230
240
+ band (nm) 192
195
220-230 (weak) 180-190 (strong) 190
205 210-230 weak
200
212
估算蛋白质α螺旋含量
仅适合α含量较高的蛋白质!
If we measure the CD signal for a protein of unknown structure we can find its proportion of 2ndry structures
圆偏振光(Circular polarized light)
振幅保持不变,而方向周期变化, 电场矢量绕传播方向螺旋前进
圆偏振光
朝光源看, 电场矢量方向按顺时针方向旋转的,称为右圆偏振光; 电场矢量方向按逆时针方向旋转的,称为左圆偏振光。
圆二色性(circular dichroism, CD)
¾ 光学活性分子对左、右圆偏振光的吸收也不 同,使左、右圆偏振光透过后变成椭圆偏振 光,这种现象称为圆二色性。
wavelength in nm
-15
-20
-25
-30
TFE
-35
圆二色谱原理

圆二色谱原理
圆二色谱是一种用于分析物质结构和对手性化合物的光学活性的技术。
它是利用物质对左右旋光的吸收差异来进行分析的,对于手性分子的研究具有非常重要的意义。
在圆二色谱的原理中,主要涉及到两个概念,旋光度和比旋度。
旋光度是指物质溶液对圆偏振光旋转的程度,它是圆二色谱分析的基础。
当圆偏振光通过手性分子溶液时,由于分子的对称性不同,左旋光和右旋光会被不同程度地吸收,从而导致光的旋转。
这种旋转的程度就是旋光度,通常用角度表示。
比旋度是指单位长度内的旋光度,它是一个物质的固有性质,与浓度和物质的性质有关。
可以通过比旋度来判断物质的对手性程度,从而进行对手性分析。
圆二色谱的原理是基于这两个概念的。
当圆偏振光通过样品溶液时,左旋光和右旋光会被不同程度地吸收,从而形成一个圆二色信号。
通过检测这个信号的强度和波长,就可以得到样品的圆二色谱图谱。
在图谱中,不同的吸收峰代表不同的对手性分子,通过比较不同样品的圆二色谱图谱,可以进行对手性分析和结构分析。
圆二色谱的应用非常广泛,特别是在药物研发和生物化学领域。
通过圆二色谱分析,可以确定化合物的对手性纯度,从而保证药物
的有效性和安全性。
此外,圆二色谱还可以用于蛋白质的结构分析,对于研究生物大分子的结构和功能具有重要意义。
总之,圆二色谱是一种非常重要的分析技术,它通过测量物质
对圆偏振光的吸收差异来进行对手性分析和结构分析。
在化学、药
物和生物领域都有着广泛的应用前景,对于推动科学研究和技术发
展具有重要意义。
圆二色谱分析结果怎么看?
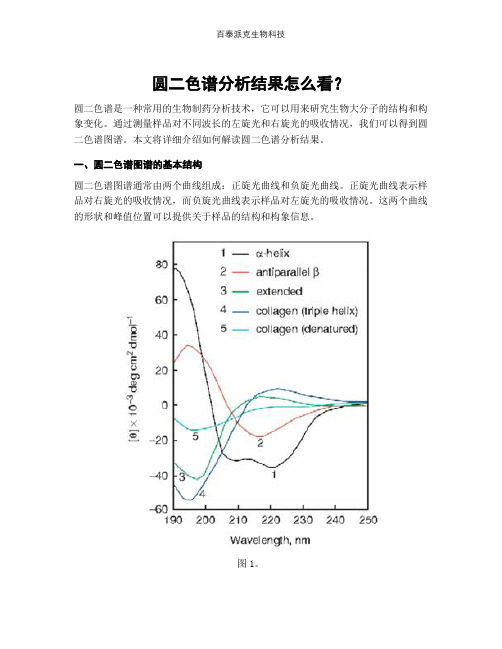
圆二色谱分析结果怎么看?圆二色谱是一种常用的生物制药分析技术,它可以用来研究生物大分子的结构和构象变化。
通过测量样品对不同波长的左旋光和右旋光的吸收情况,我们可以得到圆二色谱图谱。
本文将详细介绍如何解读圆二色谱分析结果。
一、圆二色谱图谱的基本结构圆二色谱图谱通常由两个曲线组成:正旋光曲线和负旋光曲线。
正旋光曲线表示样品对右旋光的吸收情况,而负旋光曲线表示样品对左旋光的吸收情况。
这两个曲线的形状和峰值位置可以提供关于样品的结构和构象信息。
图1。
二、峰值位置的解读圆二色谱图谱中的峰值位置可以告诉我们样品的二级结构信息。
一般来说,α-螺旋结构在190-200 nm处会出现负峰,而β-折叠结构在210-220 nm处会出现正峰。
通过观察峰值位置的变化,我们可以推断样品的二级结构变化。
三、峰值强度的解读除了峰值位置,圆二色谱图谱中的峰值强度也是解读样品结构的重要指标。
峰值强度反映了样品对旋光的吸收程度,强度越高表示吸收越强。
通过比较不同样品的峰值强度,我们可以判断它们的结构差异。
四、色谱图形的解读除了峰值位置和峰值强度,圆二色谱图谱的整体形状也提供了有关样品结构的信息。
例如,如果图谱呈现出对称的双峰形状,那么可能存在一种手性结构。
而如果图谱呈现出单峰形状,那么样品可能是非手性的。
五、结构变化的解读通过比较不同条件下的圆二色谱图谱,我们可以观察到样品结构的变化。
例如,当样品在不同温度下进行测量时,我们可以观察到峰值位置的变化,从而推断样品的热稳定性。
类似地,通过比较不同pH值下的圆二色谱图谱,我们可以了解样品的酸碱稳定性。
圆二色谱分析结果的解读需要考虑峰值位置、峰值强度、峰形、色谱图形和对比分析等因素。
通过综合分析这些指标,我们可以得出关于样品结构特征、纯度和质量变化情况的重要信息。
圆二色谱作为一种重要的分析技术,在生物制药领域具有广泛的应用前景。
百泰派克生物科技——生物制品表征,多组学生物质谱检测优质服务商。
圆二色谱总结

圆二色谱总结圆二色谱是一种常用于研究分子结构和性质的重要工具,特别是在物理、化学、生物学以及材料科学等领域。
它利用偏振光通过样品时产生的圆偏振光变化来测量样品的光谱特性。
以下是关于圆二色谱的一些总结:1.圆二色谱的定义和原理圆二色谱(Circular Dichroism,CD)是一种测量左旋和右旋偏振光通过样品后的透过率差别的技术。
当偏振光通过一个含有手性分子的样品时,它会发生旋光,即偏振面会旋转。
通过测量旋光度,可以确定分子的手性及其结构。
2.圆二色谱的应用圆二色谱被广泛应用于各种科学领域。
例如,在生物学中,CD被用于研究蛋白质和DNA的结构和动力学。
在化学中,它被用于研究有机化合物的手性和分子结构。
在材料科学中,CD被用于研究纳米材料和功能材料的光学特性。
3.圆二色谱的优势和局限性圆二色谱有以下几个优势:(1)灵敏度高:可以检测到样品中微小的旋光度变化,从而可以研究分子结构和动力学。
(2)分辨率高:可以区分不同的手性分子,这对于研究分子结构和手性之间的关系非常重要。
(3)无损检测:不会对样品造成破坏,因此可以用于研究生物样品和其他易损坏的样品。
然而,圆二色谱也存在一些局限性:(1)需要大量的样品:通常需要大量的样品才能获得可靠的CD谱图。
(2)需要专业的技术人员:需要进行CD测量的实验需要专业的技术人员进行操作和维护。
4.圆二色谱的发展趋势近年来,圆二色谱技术不断发展,出现了许多新的技术和发展趋势,如:(1)高精度CD测量技术:随着技术的进步,现在可以获得更高的测量精度和分辨率,从而能够更深入地研究分子的结构和动力学。
(2)CD与其他谱图的联用技术:可以将CD与其他谱图技术联用,如红外光谱、核磁共振谱等,从而可以从多个角度研究分子的结构和性质。
(3)CD在生物医学中的应用:CD可以用于研究生物分子的结构和动力学,从而可以应用于生物医学领域,如药物筛选、疾病诊断和治疗等。
(4)CD在材料科学中的应用:通过CD可以研究纳米材料、功能材料的光学特性,为材料科学的发展提供新的工具。
圆二色谱

旋光色散与圆二色性
叠加原理
¾ 一束自然光可以分解或看作两束相互垂直而没有相位关系
的平面偏振光的加和。
¾ 平面偏振光可以分解成两束相位相等而旋转方向相反的
圆偏振光的加和。 ¾ 当振幅相等,并同步的左、右圆偏振光相加,则产生平面
偏振光;如果这两束圆偏振光的振幅不等则产生椭圆偏 振光(elliptically polarized light)
圆二色性(circular dichroism, CD)
¾ 光学活性分子对左、右圆偏振光的吸收也不 同,使左、右圆偏振光透过后变成椭圆偏振 光,这种现象称为圆二色性。
圆二色性的表示
¾ 吸收(率)差 Δε = εL - εR ΔA = AL – AR
¾ 椭圆度θ,摩尔椭圆度[θ] θ=2.303(AL – AR)/4 [θ] = 3298(εL - εR)≈3300 (εL - εR) 在蛋白质研究中,常用平均残基摩尔椭圆度
Determination of Protein Concentration
¾ Good Methods: 1. Quantitative amino acid composition 2. Determination of backbone amide groups using the microbiuret method. 3. Determination of moles of tyrosine using difference spectroscopy under denaturing conditions. 4. Determination of total nitrogen.
at the effect of trifluoroethanol (TFE) dimer to single helices
圆二色谱和蛋白质结构

圆二色谱和蛋白质结构圆二色谱和蛋白质结构是生物化学和生物物理领域的重要研究内容。
下面我将分别介绍圆二色谱和蛋白质结构,并对它们之间的关系进行分析。
一、圆二色谱圆二色谱是一种用于研究光学活性分子的技术,特别适用于研究具有手性(非对称)结构的分子,如蛋白质、核酸等。
它通过测量样品对不同波长的左旋光和右旋光的吸收差异,来揭示分子的结构和构象变化。
1.工作原理:圆二色谱是基于电磁波的旋转偏振现象。
当线偏振光通过手性分子时,会被分子中的电荷或色团激发,并发生旋转。
左旋光和右旋光被分子旋转的方向和程度不同,导致它们在吸收光谱上呈现出镜像对称的吸收峰。
2.分析应用:-蛋白质结构研究:圆二色谱可以提供蛋白质的次级结构信息,如α-螺旋、β-折叠等。
通过测量蛋白质在不同波长下的圆二色光谱,可以了解蛋白质中氨基酸残基的空间排列和构象变化。
-药物研发:圆二色谱可以用于研究药物与蛋白质相互作用的机制,包括药物结合位点、结合力强度等,有助于药物设计和优化。
二、蛋白质结构蛋白质是生命体中最重要的分子之一,其结构决定了它们的功能。
蛋白质的结构层次可分为四个级别:一级结构、二级结构、三级结构和四级结构。
1.一级结构:一级结构指的是蛋白质的氨基酸序列,也就是由多个氨基酸组成的线性链。
氨基酸之间通过肽键连接。
2.二级结构:二级结构是指蛋白质中局部区域的稳定空间结构,包括α-螺旋和β-折叠。
α-螺旋是螺旋形状的结构,由氢键稳定;β-折叠是折叠形状的结构,由氢键连接。
3.三级结构:三级结构是指蛋白质整体的立体构象,包括各个二级结构之间的空间排列和折叠方式。
这种结构通常由氢键、离子键、范德华力等相互作用稳定。
4.四级结构:四级结构是指由多个蛋白质链或亚单位组成的复合物。
多个蛋白质链通过非共价键(如离子键、范德华力等)相互作用而形成功能完整的蛋白质。
5.蛋白质折叠与功能:蛋白质的特定结构决定了它们的功能。
正确的折叠使蛋白质能够具备生物活性,而错误的折叠可能导致蛋白质失去功能,甚至引发疾病,如变态反应、神经退行性疾病等。
圆二色谱相互作用

圆二色谱相互作用是指在分子或晶体中存在对称性破缺时,分子或晶体表现出的旋转性选择性吸收和散射现象。
圆二色谱是一种分析化学方法,用于研究物质分子结构、手性性质以及分子中的分子间相互作用。
在圆二色谱中,通过测量样品溶液或固体样品对左右旋光的吸收差异,可以得到含有手性中心的分子的绝对构型以及分子间相互作用的信息。
在分子或晶体中,圆二色谱相互作用的产生与分子中存在旋转对称性破缺有关。
这种旋转对称性破缺可以由手性分子自身的手性中心引起,也可以由分子的排列方式或溶剂分子的取向引起。
圆二色谱相互作用包括圆二色吸收和圆二色散射。
圆二色吸收是指物质对左旋光和右旋光的选择性吸收现象。
左旋光和右旋光的圆偏振光在分子或晶体中的吸收度不同,导致圆二色吸收谱的出现。
圆二色吸收谱可以提供有关分子结构、手性性质以及分子间相互作用的信息。
圆二色散射是指物质对左旋光和右旋光的选择性散射现象。
左旋光和右旋光的圆偏振光在分子或晶体中的散射方向和强度不同,产生圆二色散射效应。
圆二色散射谱可以用于研究物质的聚集状态、分子间相互作用以及分子的旋转和振动模式等信息。
总之,圆二色谱相互作用是一种应用于化学和物理领域的分析方法,通过测量物质对左旋光和右旋光的选择性吸收和散射,提供有关分子结构、手性性质以及分子间相互作用的信息。
圆二色谱是用于蛋白质结构研究的什么方法?

圆二色谱是用于蛋白质结构研究的什么方法?蛋白质是生物体内重要的功能分子,其结构决定了其功能。
因此,研究蛋白质的结构对于理解生物体内的生命过程具有重要意义。
在蛋白质结构研究领域,圆二色谱是一种常用的方法,它能够提供关于蛋白质的二级结构信息。
本文将详细介绍圆二色谱的原理、应用以及其在蛋白质结构研究中的重要性。
1. 圆二色谱的原理圆二色谱是一种光谱技术,利用圆偏振光与物质相互作用时的光学旋光现象来研究物质的结构。
当圆偏振光通过具有手性的分子时,其振动方向会发生旋转,这种旋转现象被称为光学旋光。
圆二色谱通过测量样品对圆偏振光的吸收差异来获得物质的圆二色信号。
2. 圆二色谱的应用2.1 蛋白质结构研究蛋白质的结构对其功能起着至关重要的作用。
圆二色谱可以提供关于蛋白质的二级结构信息,包括α-螺旋、β-折叠等。
通过测量蛋白质在不同波长下的圆二色信号,可以得到蛋白质的CD谱图,进而推断出蛋白质的二级结构组成。
图1。
2.2 药物研发圆二色谱在药物研发中也有广泛的应用。
许多药物是通过与蛋白质相互作用来发挥作用的,因此了解药物与蛋白质的相互作用机制对于药物研发至关重要。
圆二色谱可以用来研究药物与蛋白质的相互作用,从而帮助科学家理解药物的作用机制,优化药物设计。
2.3 生物医学研究圆二色谱在生物医学研究中也有广泛的应用。
例如,研究蛋白质的折叠和变性过程、研究蛋白质的构象变化等。
这些研究对于理解蛋白质的功能以及与疾病的关联具有重要意义。
3. 圆二色谱在蛋白质结构研究中的重要性圆二色谱作为一种非破坏性的分析方法,能够提供关于蛋白质的二级结构信息,对于蛋白质结构研究具有重要意义。
首先,圆二色谱可以帮助科学家了解蛋白质的二级结构组成。
蛋白质的二级结构决定了其功能,因此了解蛋白质的二级结构对于理解其功能具有重要意义。
其次,圆二色谱可以用来研究蛋白质的构象变化。
蛋白质的构象变化与其功能密切相关,通过圆二色谱可以监测蛋白质在不同条件下的结构变化,从而揭示蛋白质的功能调控机制。
圆二色谱 标准

圆二色谱是一种用于推断非对称分子构型和构象的光谱技术。
具体来说,圆二色谱的原理是光学活性物质对组成平面偏振光的左旋和右旋圆偏振光的吸收系数(ε)是不相等的,即具有圆二色性。
如果以不同波长的平面偏振光的波长λ为横坐标,以吸收系数之差Δε=εL-εR为纵坐标作图,得到的图谱即是圆二色光谱,简称CD。
由于△ε有正值和负值之分,所以圆二色谱也有呈峰的正性圆二色谱和呈谷的负性圆二色谱。
在紫外可见光区域测定圆二色谱与旋光谱,其目的是推断有机化合物的构型和构象。
圆二色谱的应用非常广泛,包括但不限于生物大分子的二级结构研究、蛋白质折叠和构象研究、DNA/RNA反应、酶动力学研究、光学活性物质纯度测量以及药物定量分析等。
圆二色谱 样品浓度

圆二色谱样品浓度圆二色谱是一种分析化学技术,用于测量样品中的物质浓度。
它基于圆二色现象,即样品吸收线偏振光时,会在旋光性分子存在时发生旋光现象。
圆二色谱可以通过测量旋光角度来确定样品中旋光性分子的浓度。
下面将详细介绍圆二色谱的原理、方法和应用。
圆二色谱的原理是基于光在介质中传播时,电磁波的振动方向可能发生旋转的现象。
对于具有对显性旋光性分子,它们的分子结构中存在着旋光性中心,可以使光中的电磁波振动方向发生旋转。
这种旋光性分子对偏振光有选择地吸收不同方向的电磁波,导致通过溶液的偏振光的偏振方向发生改变。
圆二色谱实验中,常用的光源是紫外可见光源,例如汞灯或钨灯。
样品通常是溶液,可以通过旋转片使入射光是偏振光,然后传播过样品后,通过旋转片使出射光也是偏振光。
这样,通过旋转片的旋转,可以测量样品对不同偏振方向的光的吸收情况。
圆二色谱的测量是用圆二色谱仪进行的。
圆二色谱仪通常由光源、光栅、单色器、样品室、探测器等部分组成。
光源发出的光经过光栅和单色器分光,然后通过样品室中的样品,进入探测器中进行测量。
探测器会将接收到的光信号转换为电信号,经过处理后,可以得到样品的吸光度和旋光度的数据。
根据旋光度和吸光度,可以计算出样品中旋光性分子的浓度。
圆二色谱在科学研究和工业生产中有广泛的应用。
在生物化学和生物技术领域,圆二色谱可以用于研究蛋白质、核酸、糖等生物分子的结构和性质。
通过测量蛋白质的圆二色谱,可以了解其二级结构(α-螺旋、β-折叠等)和反应过程中的构象变化。
在药物研发中,圆二色谱可以用来研究药物与蛋白质的相互作用,推测药物的运输、代谢和毒性等信息。
在食品行业,圆二色谱可以用于检测食品中的旋光性分子,如蔗糖、氨基酸等。
这些旋光性分子可以用来判断食品的纯度和质量。
在工业领域,圆二色谱可用于研究工业催化剂中有机分子的结构和活性,以及研究环境中的污染物浓度。
此外,圆二色谱还可以用于研究草药的成分和功效,甚至用于酒类的品质鉴定。
圆二色谱结构含量计算

圆二色谱结构含量计算一、圆二色谱的原理圆二色谱是通过对右旋圆偏振光和左旋圆偏振光在样品中的吸收和散射进行测量,来获得分子的空间结构信息的一种方法。
根据分子的手性,它们能够使通过它们的圆偏振光产生不同旋光的能力也是不同的。
圆二色谱是在紫外光区(180-350 nm)和可见光区(350-750 nm)范围内进行测量的。
二、圆二色谱的仪器在进行圆二色谱结构含量计算之前,我们需要使用一台圆二色谱仪来进行实验。
圆二色谱仪通常包括光源、单色器、样品室、检测器和计算机等部件。
光源会发出连续的线偏振光,然后经过单色器选择出所需的波长范围的光。
样品室中会放置样品,样品可以是溶液、晶体或固体。
光线通过样品时,其右旋和左旋圆偏振光成分会发生吸收和散射,并被检测器检测到。
最后,计算机会处理检测到的光信号,并生成圆二色谱。
三、圆二色谱结构含量计算方法圆二色谱含量计算方法主要有两种:单一比例法和贡献系数法。
1.单一比例法单一比例法是根据不同立体异构体产生的旋光值之间的比例关系来计算分子结构含量的。
首先,我们需要制备含有不同立体异构体的纯化合物,然后分别测量它们的圆二色谱光谱。
接下来,我们可以使用以下公式来计算每种立体异构体的含量:C=(R-R0)/(R1-R0)其中,C为立体异构体的含量,R为测量到的旋光值,R0为一个基准异构体的旋光值,R1为另一种异构体的旋光值。
2.贡献系数法贡献系数法是通过建立分子结构与旋光值之间的线性关系,并使用多元线性回归进行计算的。
首先,我们需要制备含有不同立体异构体的纯化合物,并测量它们的圆二色谱光谱。
然后,我们需要通过量子化学计算获得这些异构体的分子结构参数。
接下来,我们将旋光值作为因变量,分子结构参数作为自变量进行多元线性回归分析。
最后,通过回归系数可以得到每种立体异构体的贡献系数,从而计算出其含量。
三、圆二色谱在结构含量计算中的应用圆二色谱结构含量计算方法广泛应用于研究生物分子的立体化学结构。
圆二色谱方法

圆二色谱方法一、基础知识介绍圆二色谱是一种用于研究分子旋光性的光谱技术,通过测量样品在圆偏振光照射下的吸收光谱,可以获得关于分子手性、构象和动态行为等信息。
圆二色谱广泛应用于化学、生物学、药学等领域。
二、实验原理当左旋圆偏振光和右旋圆偏振光以一定比例混合时,形成椭圆偏振光。
当这种椭圆偏振光通过手性分子时,左旋和右旋偏振光会被不同吸收,导致透射光的强度和旋光性发生变化。
通过测量透射光的强度和旋光性,可以获得样品的圆二色谱。
三、实验步骤1.准备样品:制备适当浓度的样品溶液,确保样品在手性环境中。
2.安装仪器:将样品放入圆二色谱仪器的样品池中,确保密封良好。
3.设定参数:设置实验参数,如波长范围、扫描速度等。
4.开始实验:启动仪器,开始测量样品的圆二色谱。
5.数据分析:处理实验数据,提取相关信息。
四、数据分析在圆二色谱实验中,通过测量透射光的强度和旋光性,可以绘制出样品的圆二色谱图。
通常情况下,圆二色谱图以波长为横坐标,以旋光度差值ΔOD(或ΔA)为纵坐标。
通过分析圆二色谱图的峰位、峰形和峰强等信息,可以推断出样品的构象、手性和动态行为等。
五、影响因素影响圆二色谱实验结果的因素很多,主要包括温度、浓度、溶剂极性等。
这些因素可能会影响分子的构象和手性,从而影响实验结果。
因此,在实验过程中需要控制这些因素,以确保实验结果的准确性。
六、应用领域圆二色谱方法在多个领域中有着广泛的应用,例如:在手性识别与拆分领域中,可以用于检测手性化合物的纯度;在化学反应监控领域中,可以用于研究化学反应的机理和动力学;在生物学领域中,可以用于研究生物分子的结构和功能等。
七、实验注意事项1.在实验过程中要保持恒温,避免温度波动对实验结果的影响。
2.确保样品的浓度和纯度符合要求,避免杂质干扰实验结果。
3.正确选择溶剂和浓度,以确保分子处于合适的构象状态。
4.在数据分析过程中要注意峰位的准确性,避免由于仪器噪声等因素引起的误差。
八、展望随着科技的不断发展和进步,圆二色谱方法的应用前景也越来越广泛。
圆二色谱的介绍

圆二色谱的介绍圆二色性circulardichroism对R和L两种圆偏振光吸收程度不同的现象。
这种吸收程度的不同与波长的关系称圆二色谱,是一种测定分子不对称结构的光谱法。
在分子生物学领域中主要用于测定蛋白质的立体结构,也可用来测定核酸和多糖的立体结构。
光是一种电磁波。
假如用电矢量来表示,光的前进就是由矢量端点在一特定的平面里沿正弦波运动的轨迹。
对于自然光讲,正弦波振动的平面是随机的。
如有一束光,它所有的电矢量的振动平面都是相互平行的,这种光称为平面偏振光。
有一种特殊的情况,光前进的过程中电矢量绕前进轴转动,若电矢量的绝对值不变,则运动轨迹的投影是一个圆,这时就变成圆偏振。
面对光前进的方向看去,电矢量端点的圆运动可以是顺时针方向的,也可以是逆时针方向的,因此圆偏振有R与L两种。
假如L与R两束圆偏振光在一起辐射,强度、速度、频率和位相都相同,它们就会叠合成一束平面偏振光。
如波长λ的L光和R光的光强度相等,在光学各向异性物质中传播某一距离后,它们的综合光将变成椭圆偏振光,椭圆的长轴处于两个圆偏振的电矢量相叠合的地方。
假如两个圆偏振的传播速度也不相同,而所经的途径与上述相同,则叠合的椭圆偏振光的长轴与上面所述的椭圆偏振光的长轴相夹θ角(图1)。
由不对称分子组成的物质是光学各向异性的,即L与R两束圆偏振光在这类物质中的传播速度不相等。
假如光学各向异性物质在某一波长λ有吸收,那将在该时对L光和R光有不同的吸收,如该物质的吸光率是A,而对L光和R光的吸光率是AL和AR,AL和AR的差ΔA=AL-AR,称为圆二色性。
从(图2)可看出,因光吸收不同而产生的椭圆的形状与ΔA有直接的关系。
θ称为椭圆值,也是一种定量描述圆二色性的单位。
在条件相同的情况下,θ=3300ΔA。
在蛋白质分子中,肽链的不同部分可分别形成α-螺旋、β-折叠、β-转角等特定的立体结构。
这些立体结构都是不对称的。
蛋白质的肽键在紫外185~240纳米处有光吸收,因此它在这一波长范围内有圆二色性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
圆二色谱
圆二色谱是一种特殊的吸收普,它对手性分子的构象十分敏感,因此它是最重要的光谱实验之一。
手性是物质结构中的重要特征,即具有不能重叠的三维镜像对映异构体,它们的分子式完全相同,但其中原子或原子基团在空间的配置不同,互为镜像。
凡手性分子都具有光学活性,即可使偏振光的振动面发生旋转。
许多有机物和络合物都具有手性,它们的对映异构体物理化学性质(熔点、沸点、旋光度、溶解度、分子式等)几乎完全相同,但它们的旋光方向相反,生理作用大不相同。
生物基础分子一般都具有手性,也都具有光学活性。
在对生物分子手性的研究中,发现了令人惊异至今不解的对称性破缺现象,那就是在自然界中,氨基酸有L型和D型两种对映异构体,天然糖也有L糖和D糖两种糖。
但在生物体中,组成蛋白质的20种氨基酸,除最简单的甘氨酸不具有手性外,其余都是L型的,而生物体核酸中的糖环则都是D型的。
生物体中这种对称性破缺现象是有特殊意义的自然现象。
手性分子都具有光学活性。
当单色左旋与右旋的圆偏振光通过某一种手性样品时,该样品对左、右旋圆偏振光的吸收不同,这叫做圆二色性。
其差值△A=△AL一△AR称为圆二色值,按波长扫描就得到了圆二色谱(CD谱)。
利用法拉第效应,在外加磁场作用下,许多原来没有光学活性的物质也具有了光学活性,原来可测出CD谱的在磁场中CD信号将增大几个量级。
这种条件下即可测得磁圆二色谱(MCD谱)。
CD和MCD是特殊的吸收谱,它们比一般的吸收谱弱几个量级,但由于它们对分子结构十分敏感,因此近十几年来,CD和MCD 已成为研究分子构型和分子间相互作用的最重要的光谱实验之一。
利用CD和MCD 研究生物大分子和药物分子,具有重要的科学意义和实用价值。
基本定义和原理
一束平面偏振光通过光学活性分子后,由于左、右圆偏振光的折射率不同,偏振面将旋转一定的角度,这种现象称为旋光,偏振面旋转的角度称为旋光度。
朝光源看,偏振面按顺时针方向旋转的,称为右旋,用“+”号表示;偏振面按逆时针方向旋转的,称为左旋,用“-”号表示。
为了揭示物质的旋光性,菲涅耳作了如下的假设,线偏振光在旋光晶体中沿光轴传播时,分解成了左旋和右旋圆偏振光,它们的传播速度略有不同,或者说它们的折射率不同,经过旋光晶片后产生了附加的相位差,从而使出射的合成线偏振光的振动面有了一定角度的偏转。
如果旋光物质对特定波长的入射光有吸收,而且对左旋和右旋圆偏振光的吸收能力不同,那么在这种情况下,不仅左旋和右旋圆偏振光的传播速度不同,而且振幅也不同,随着时间的推移,左右旋圆偏振光的合成光振动矢量的末端,将循着一个椭圆的轨迹移动。
这就是说,由速度不同振幅也不同的作右旋圆偏振光叠加所产生的不再是线偏振光,而是椭圆偏振光,这种现象称为圆二色性.
旋光度:α = [α]lc [α]是旋光物质的比旋光率,单位是度•厘米2 • 10克-1对同一物质,[α]值与波长有关,旋光率与波长的关系称为旋光色散(Optical rotatory dispersion, ORD)。
旋光色散常用摩尔比旋[Φ]表示: [Φ] = [α]*M/100
圆二色性可用吸收率差和椭圆度来表示:
吸收(率)差 :ε∆ = εL - εR
∆A = AL – AR
椭圆度θ,摩尔椭圆度[θ]
θ=2.303(AL – AR)/4
[θ] = 3298(εL - εR)≈3300 (εL - εR)
旋光色散和圆二色是同时产生的,他们包括同样的分子结构信息,并且可以由Kronig-Krammers转换方程相互转换。
圆二色仪原理
光弹调制器由调制头和控制器组成,调制头主要由一块适当的透光材料(例如熔石英或氟化钙等)附着在压电传感器上组成。
利用光弹效应,它能使线偏振光变成高频振荡的左旋圆偏振光和右旋圆偏振光。
这样当同步辐射线偏振光由单色器单色化后,进人样品室通过光弹调制器的调制头时,就变成了高频振荡(如50kHz)的左旋和右旋圆偏振光,会聚于样品中心。
若是手性样品,则对左、右旋圆偏振光的吸收不同。
为了检测到这种非常微弱的圆二色信号,我们重新设计制造了微弱信号前置放大器,采用多级选频,交、直流分路放大的原理,使CD信
号由拜V级提高到mV级,信噪比大大改善,再通过锁相放大器就采集到稳定的CD信号。
对不同波长,样品的CD值也不同,由步进电机控制单色器进行波长扫描,就得到了该样品的CD谱。
利用计算机数据自动采集系统,可将所需数据采集存储起来,也可实时在记录仪上画出CD曲线,供进一步分析用。
圆二色谱应用
圆二色光谱仪通过测量生物大分子的圆二色光谱从而得到生物大分子
的二级结构,是简便和快捷的获得生物大分子结构的手段之一。
可应用于蛋白质折叠﹑蛋白质构象研究 ,DNA/RNA 反应 , 酶动力学 , 光学活性物质纯度测量 , 药物定量分析。
天然有机化学与立体有机化学 , 物理化学 , 生物化学与宏观大分子 , 金属络合物 , 聚合物化学等相关的科学研究。
随着人们对生命科学的日益关注,分析化学的深入发展将越来越重视和加强生物分析。
特别是人类基因测序工程完成后,因生物、医学上的需要,使与蛋白质的相关研究成为生物分析中的重要课题。
目前,确定蛋白质构象最准确的方法是X-射线晶体衍射,但对结构复杂、柔性的生物大分子蛋白质来说,得到所需的晶体结构较为困难。
二维、多维核磁共振技术能测出溶液状态下较小蛋白质的构象,可是对分子量较大的蛋白质的计算处理非常复杂。
相比之下,圆二色光谱是研究稀溶液中蛋白质构象的一种快速、简单、较准确的方法。
1969年,Greenfield最早用CD光谱数据估计了蛋白质的构
象[3],相关的研究方法陆续有报道。
特别是近十几年来,用远紫外圆二色数据分析蛋白质二级结构,不但在计算方法和拟合程序上有了极大地发展,而且随着X 射线晶体衍射与核磁共振技术的提高,越来越多的蛋白质的精确构象得到测定,
为CD数据的拟合提供了更精确的数据库。
另外有人还发现用CD光谱研究蛋白质三级结构具有独特优点,发展了用远紫外CD光谱辨认蛋白质三级结构的方法及相关程序;此外,近紫外圆二色作为一种灵敏的光谱探针,可反映蛋白质中芳香氨基酸残基、二硫键微环境的变化。
CD光谱技术作为研究溶液状态下蛋白质或多肽构象的一种重要手段,已受到研究者的广泛关注。
圆二色光谱分区
圆二色光谱紫外区段(190 - 240nm ),主要生色团是肽链,这一波长范围的 CD 谱包含着生物大分子主链构象的信息。
在近紫外区(240 - 300nm ),
占支配地位的生色团是芳香胺基侧链,这一区域可以给出“局域”侧链间相互作用的信息。
在波长大于 300nm 的区域,包括可见区域,对 CD 的贡献来自含有金属离子的生色团,这一波段的 CD 谱对金属离子的氧化态、配位态及链-链相互作用均是敏感的。
圆二色光谱对全α、 α /β和变性蛋白质的准确度为100%,对α + β的准确度为85%,对全β的准确度为75%。
对多肽的判断较差!
园二色谱技术发展得较早,成为立体化学研究的重要手段之一。
但此项技术是以可见及近紫外作为入射光源,这就要求被研究的手性分子要具有发色基团,通过对发色基团的研究来获得分子结构信息,因此它只能提供分子局部的结构信息。
这一缺点大大地限制了此项技术的应用范围。
参考文献:
1 Nicholas C Price.Circular Dichroism: Studies of Proteins. ENCYCLOPEDIA OF LIFE SCIENCES. Nature Publishing Group 2001 :1-4.
2 沈星灿,梁宏,何锡文等.园二色谱分析蛋白质构象的方法及研究进展.分析化学评述与进展,2004,32(3):388-394
3 曲世鸣,张鲁殷,薛玉章.园二色性对旋光现象的影响.大学物
理,2001,20(12):18-19
4 王渭,李崇慈,赵南生.BSRF园二色谱研究进展.光谱学与光谱分析,1996,16(1):25-28
5 lIU Tao, RUAN Wen-Juan, MAN Jing etc. CD Spectroscopic Study on the Molecular Recognition of Chiral Salen-Metal Complexes. CHINESE JOURNAL OF CHEMISTRY,2003,21:751-755
6 林波海.蛋白质二级结构的真空紫外园二色性研究.生物化学与生物物理进展,1994,21(1):67-69
7 赵南明,周海梦.生物物理学.高等教育出版社,施普林格出版社.330-344。
