有机化合物的标准热力学数据
乙二醇物性数据

乙二醇物性数据乙二醇是一种常用的有机化合物,化学式为C2H6O2,也被称为1,2-乙二醇或者乙二醇。
乙二醇具有许多重要的物性,包括物理性质、化学性质和热力学性质。
下面将详细介绍乙二醇的物性数据。
1. 物理性质:- 外观:乙二醇是一种无色、粘稠的液体。
- 气味:乙二醇具有轻微的甜味。
- 熔点:乙二醇的熔点约为-13℃。
- 沸点:乙二醇的沸点约为197℃。
- 密度:乙二醇的密度约为1.113 g/cm³。
- 折射率:乙二醇的折射率约为1.431。
- 溶解性:乙二醇可溶于水、醇类、醚类和酮类溶剂。
2. 化学性质:- 氧化性:乙二醇在氧气存在下可以被氧化为乙醛和乙酸。
- 还原性:乙二醇可以被还原为乙醇。
- 酸碱性:乙二醇是一种中性物质,不具有酸碱性。
- 可燃性:乙二醇是可燃物质,其燃烧产生二氧化碳和水。
3. 热力学性质:- 热容:乙二醇的热容约为2.51 J/g·K。
- 热导率:乙二醇的热导率约为0.25 W/m·K。
- 蒸发潜热:乙二醇的蒸发潜热约为245 kJ/mol。
- 燃烧热:乙二醇的燃烧热约为1363 kJ/mol。
- 热膨胀系数:乙二醇的热膨胀系数约为0.0006 1/℃。
4. 安全性:- 乙二醇具有一定的毒性,长期暴露或者高浓度接触可能对健康造成危害。
- 乙二醇具有刺激性,接触皮肤和眼睛可能引起刺激和炎症。
- 乙二醇具有易燃性,应避免与明火和高温接触。
以上是关于乙二醇物性数据的详细介绍。
乙二醇是一种广泛应用于化工、医药、塑料等领域的化合物,了解其物性数据对于正确使用和处理乙二醇至关重要。
在使用乙二醇时,务必遵守相关的安全操作规程,确保人身安全和环境安全。
环己烷比热容

环己烷比热容标题:环己烷的比热容:研究与应用简介:本文将探讨环己烷的比热容及其相关研究和应用领域,从理论和实验角度介绍环己烷的热性质以及其在化学、工程等领域中的重要性。
正文:比热容是描述物质热性质的一个重要参数,它代表了单位质量的物质在温度变化下吸收或释放的热量。
对于研究和应用领域而言,了解不同物质的比热容对于设计和优化过程至关重要。
本文将聚焦于环己烷这一常见有机化合物的比热容特性。
环己烷,化学式C6H12,是一种无色液体,常用作溶剂和燃料。
它具有低粘度、低毒性和较高的沸点,因此在化学和工程领域中被广泛应用。
了解环己烷的比热容可以帮助我们更好地理解其热力学行为,并为相关领域的设计和过程优化提供依据。
环己烷的比热容可以通过实验测定获得。
研究者通常使用差示扫描量热仪等热分析仪器来测量在不同温度下环己烷的热量变化。
通过测量物质在不同温度下吸收或释放的热量,可以绘制出热容-温度曲线。
这些数据对于工程热力学计算、储能系统设计以及燃烧过程模拟等领域非常有用。
环己烷的比热容随温度的变化而变化。
一般而言,在低温下,环己烷的比热容较低,随着温度的升高,比热容也逐渐增加。
这是因为在低温下,分子振动和转动受到限制,热运动的自由度较低,因此吸热能力有限。
而随着温度升高,分子热运动的自由度增加,吸热能力也随之增强,导致比热容增加。
环己烷的比热容对于许多应用具有重要意义。
例如,在化学反应的热力学计算中,准确地了解反应物和产物的比热容可以帮助确定反应的热平衡和热效应。
在工程领域,了解环己烷的比热容可以用于设计和优化热交换设备、燃烧系统和储能系统。
此外,环己烷的比热容也对于材料科学和热物性研究有重要意义。
总结起来,环己烷的比热容是描述该有机化合物热性质的重要参数。
通过实验测定和理论计算,我们可以了解其在不同温度下的吸热能力变化规律。
这对于化学、工程等领域的研究和应用具有重要意义,并为相关领域的设计和优化提供了基础数据。
请注意,本文不涉及任何侵权争议,不包含敏感词或其他不良信息,且与标题一致。
丙酮的汽化潜热值表

丙酮的汽化潜热值表全文共四篇示例,供读者参考第一篇示例:【丙酮的汽化潜热值表】丙酮,化学式为C3H6O,是一种挥发性有机化合物,也被称为丙酮酸甲酯。
丙酮具有特殊的物理性质,在室温下为无色液体,易挥发,有强烈的刺激性气味。
丙酮在化工、药剂、染料等行业中得到广泛应用。
丙酮的汽化潜热是指单位质量的丙酮从液态转变为气态所需要吸收的热量。
汽化潜热值是丙酮热学性质的重要参数之一,对于工程设计、燃烧研究等领域具有重要意义。
下面将介绍一份关于丙酮的汽化潜热值表,以供参考:|温度(℃)|汽化潜热值(kJ/kg)||-------|-------------||0 |28.63 ||10 |28.59 ||20 |28.54 ||30 |28.49 ||40 |28.44 ||50 |28.38 ||60 |28.32 ||70 |28.26 ||80 |28.19 ||90 |28.12 ||100 |28.04 |从上表可以看出,丙酮的汽化潜热值随温度的升高而逐渐减小。
在0℃下,丙酮的汽化潜热值为28.63 kJ/kg,随着温度升高到100℃时,汽化潜热值降至28.04 kJ/kg。
这表明在不同温度下,丙酮的汽化潜热值有所变化,工程设计和燃烧研究需要考虑到温度对汽化潜热值的影响。
丙酮的汽化潜热值是在标准大气压下测定得出的,不同压力条件下丙酮的汽化潜热值可能会有所变化。
在实际应用中,需要根据具体的研究对象和工程需求选择适当的汽化潜热值数据。
丙酮的汽化潜热值是其热学性质的重要参数之一,对于工程设计、燃烧研究等领域具有重要意义。
通过建立准确的汽化潜热值表,可以更好地指导相关研究和工程实践,为丙酮的应用提供更加科学的依据。
希望以上信息对您有所帮助。
第二篇示例:丙酮,又称丙酮醛,是一种常见的有机化合物,化学式为(CH3)2CO。
它是一种易挥发的液体,有着特殊的香味。
丙酮以其广泛的用途而闻名,被广泛运用于溶剂、清洁剂、油漆等领域。
南开大学高等有机化学课件第四章有机反应机理的研究和描述

Ea ln k ln A RT
R: 气体常数, A: 频率因数,
在不同温度下测速率常数, 可计算出 Ea: Arrhenius活化能
Ea ΔH RT ΔS Ea log k 10 .753 log T 4.576 4.576T
4.3.1 简单速率表达式的积分形式
正常情况下动力学数据用微分方程的积分形式来处理:
如简单的一级反应和二级反应:
1 C0 一级级反 : k ln( ) t C 1 b0(a) 二级反应 : k (a0 - b0)ln t a0(b)
a, b, c: 时间t时浓度
a0, b0, c0: 起始浓度
一些反应速率方程积分形式的推导:
4.2 动力学数据(Kinetic Data)
动力学数据使我们能更详细地洞察反应机理。用跟踪反 应物消失和产物出现的方法可以测定某一个反应的速度。波 谱技术提供了一个迅速又连续地监测浓度变化的方法,因而 往往被用来测量反应进行的程度。总之,任何与一种反应物 或产物的浓度有关而且能被测量的性质,都可利用来测定反 应速度。 动力学研究的目的是为了在反应物和催化剂的浓度以及 反应速度之间建立定量关系。
k1[A][B] [C] k -1
d[D] k1 k2[C] k2 [A][B] kobs.[A][B] dt k -1
大多数反应不止一步, 可以参考一些重要的多步反应例子来得出动 力学表达式, 例如在决速步之前可以有一个快速平衡:
ROH + H+
+ ROH2
快 k1 k -1
_
ROH2 RBr +H2O
计算出一个反应的自由能变化,就使反应平衡位置的计算有了 可能,也就指出了某一化学过程的可实现性。 有兴趣的反应大多数发生在溶液中,任何这种反应的焓、熵和 自由能都与溶剂介质有关。 但是,热力学数据并不能说明是否存在一个能量上有利的潜在 反应途径,即反应速度上的情报。因此,深入了解反应机理以及 有机反应进行是中间所经各步的速度和能量要求是极为重要的。
热力学数据

/data/2006/0822/article_4750.htm国外的.这是在线免费查热力学的数据库./show/download/shtml/014965.shtml这个则是150页的许多种有机物的热力学数据./化学数据库7KMWeWFuZ2Rvbmd5dQ==Ir0z---清风小木虫1. 化合物毒性相关数据库Toxnet /2毒性物质与健康和环境数据库/efdb/TSCA TS.htm3. 急性毒性数据库/data/acute/acute.html4. SpectraOnline,Galact /SpectraOnline/Default_ie.htm5. 药物使用指南,USP DI /medlineplus/druginformation.html6。
美国常用药物索引库RxList /7. 有机化合物光谱资料库系统http://www.aist.go.jp/RIODB/SDBS/menu-e.html8. NIST的Chemistry WebBook /chemistry/9. 化合物基本物性库10. 化学物质热力学数据/databases/key1.html11. 溶剂数据库SOLV-DB /solvdb.htm12. 三维结构数据库NCI-3D /nci3d/13. 有机合成手册数据库/14. Beilstein Abstracts /databases/belabs15. 有机合成文献综述数据库/ ... als/info/index.html16. 预测LogP和LogW /17. 物性、质谱、晶体结构数据库http://factrio.jst.go.jp/18. 网上光谱资料库/SpectraOnline/Default_ie.htm19. 中国科学院学位论文数据库/cgrs全球实用化学化工期刊和数据库网址资源名称:AIChE(美国化学工程师协会)资源地址:/获取途径:部分资源可免费查阅资源名称:American Chemical Society(美国化学学会网站)资源地址:/获取途径:大部分资源可免费查阅,34种期刊(/about.html)全部免费阅览全文。
乙二醇物性数据

乙二醇物性数据引言概述:乙二醇(Ethylene Glycol)是一种常用的有机化合物,具有广泛的应用领域,如化工、医药、塑料等。
了解乙二醇的物性数据对于工程设计和生产过程中的操作非常重要。
本文将详细介绍乙二醇的物性数据,包括密度、熔点、沸点、粘度和热容等五个方面。
一、密度:1.1 乙二醇的密度随温度的变化规律:根据实验数据,乙二醇的密度随温度的增加而减小。
具体来说,当温度从0摄氏度增加到25摄氏度时,乙二醇的密度从1.113 g/cm³减小到1.110 g/cm³。
1.2 乙二醇的密度与浓度的关系:乙二醇的密度与其浓度密切相关。
普通情况下,乙二醇的浓度越高,其密度也越大。
例如,当乙二醇的浓度为50%时,其密度约为1.125 g/cm³。
1.3 乙二醇的密度对于工程设计的影响:乙二醇的密度是工程设计中重要的参数之一,它对于计算流体的体积和质量具有重要影响。
在设计乙二醇的输送管道或者储罐时,需要准确考虑其密度变化,以确保操作的安全和高效。
二、熔点:2.1 乙二醇的熔点与纯度的关系:乙二醇的熔点与其纯度密切相关。
较高纯度的乙二醇熔点较低,纯度越高,熔点越低。
普通来说,乙二醇的熔点约为-13摄氏度。
2.2 乙二醇的熔点与外界条件的影响:乙二醇的熔点受外界条件的影响较小。
在常温下,乙二醇处于固态,需要加热至熔点以上才干变为液态。
2.3 乙二醇的熔点在工业应用中的重要性:乙二醇的熔点在工业应用中具有重要意义。
例如,在低温环境下,乙二醇可以用作防冻剂,其低熔点使得其在低温下仍能保持液态,起到防冻的作用。
三、沸点:3.1 乙二醇的沸点与压力的关系:乙二醇的沸点与压力密切相关。
普通来说,乙二醇的沸点随着压力的增加而升高。
在常压下,乙二醇的沸点约为197摄氏度。
3.2 乙二醇的沸点与纯度的关系:乙二醇的沸点与其纯度密切相关。
较高纯度的乙二醇沸点较高,纯度越高,沸点越高。
3.3 乙二醇的沸点对于工程设计的影响:乙二醇的沸点是工程设计中需要考虑的重要参数之一。
化合物物性查询网站

1.物性数据(/data.xls)该数据库是浏览型数据库,含有470多种纯组分的物性数据,如分子量、冰点、沸点、临界温度、临界压力、临界体积、临界压缩、无中心参数、液体密度、偶极矩、气相热容、液相热容、液体粘度、反应标准热、蒸气压、蒸发热等。
2.热力学性质(/~jrm/thermot.html)该站点可查294种组分的热力学性质,还可以根据Peng Robinson状态方程计算纯组分或混合物的性质:包括气液相图、液体与气体密度、焓、热容、临界值、分子量等数据。
3.标准参考数据库化学网上工具书(/chemistry/)该数据库是一种检索型数据库,检索方法非常简单,可通过化学物质名称、分子式、部分分子式、CAS 登记号、结构或部分结构、离子能性质、振动与电子能、分子量和作用进行检索,可检索到的数据包括分子式、分子量、化学结构、别名、CAS登记号、气相热化学数据、凝聚相热化学数据、液态常压热容、固态常压热容、相变数据、汽化焓、升华焓、燃烧焓、燃烧熵、各种反应的热化学数据、溶解数据、气相离子能数据、气相红外光谱、质谱、紫外/可见光谱、振动/电子能及其参考文献。
4.美国标准技术研究所物理网上工具书(/)该站点包括物性常数、原子光谱数据、分子光谱数据、离子化数据、χ-射线、γ-射线数据、放射性计量数据、核物理数据及其它数据库。
5.sigma-aldrich手册(/saw ... +Bulk?EditDocument)该数据库是一种可检索数据库,可通过产品名称、全文、分子式、CAS登记号等进行检索,检索的结果包括产品名称、登记号、分子式、分子量、贮存温度、纯度、安全数据等。
6.美国国立医学图书馆毒性化学物质数据(HSDB)/servlets/simple-search?1.5.0可通过化学物质名称/别名、CAS登记号、化学物质名称的一部分进行检索,检索结果包括化学物质名称、登记号、同义词、分子式、RTECS号、运输方式、所含杂质等数据。
化工热力学常用数据手册

常用数据手册D. R. Lide,“CRC Handbook of Chemistry and Physics”,77th ed.,ChemicalRubber Co,该手册是美国化学橡胶公司(Chemical Rubber Co,简称CRC)出版的一部著名化学和物理学科的工具书。
它初版于1913年,以后逐年改版,内容不断完善更新。
该手册资料丰富,查阅方便,为人们提供了可靠的常用基础数据。
全书由目录、正文、附录和索引组成,正文分16个部分。
其中:第3部分是有机化合物的物理常数。
主要内容是有机化合物的物理常数表,收录了1.5万多种有机化合物的物理常数。
第4部分是元素和无机化合物的性质。
主要内容为元素和各种化合物的物理和化学性质、无机化合物的物理常数表。
第5部分是热力学、电化学和动力学。
主要内容有化学物质的标准热力学性质、某些有机化合物的燃烧焓、无机化合物的融化焓、电解质水溶液的当量导电率、电解质的溶解焓等。
第6部分是流体的性质,汇集了流体的各种物理和化学数据。
主要内容有流体的热物理性质、蒸气压、气体在水中的溶解度、某些化合物的临界常数、沸点、熔点、无机物和有机物的气化焓、共沸混合物、流体的粘度等。
第7部分是生物化学和营养。
第8部分是分析化学,包括试剂的制备、酸碱盐的标准溶液、有机分析试剂、酸碱指示剂、荧光指示剂、电化次序、酸碱在水溶液中的解离常数,溶解度表等。
J. A. Dean; “L ange’s Handbook of chemistry”,14th ed,McGraw-Hill New York,1992这是一本著名的化学数据手册,1934年发行第一版。
正文以表格形式为主,共分为11个部分。
其中有(9)热力学性质和(10)物理性质。
每一部分的前面有目次表,书末有主题索引。
该手册的第13版有中译本,名为《兰氏化学手册》,由尚久方等翻译,1991年3月科学出版社出版。
R. C. Reid et.al.,“The properties of Gases and Liquids,” Fourth ed.,McGraw-Hill,New York,1987该书共分11个部分:(1)物理性质的估算;(2)纯组分常数,包括临界性质、偏心因子、沸点、熔点及偶极矩;(3)纯气体的PVT关系;(4)混和物的容积性质;(5)热力学性质;(6)理想气体热力学性质;(7)纯液体的蒸气压和蒸发焓;(8)多组元系统的流体相平衡;(9)粘度;(10)导热系数;(11)表面张力。
苯酚的热力学数据

苯酚的热力学数据苯酚是一种芳香族非合成双萜类有机化合物,它主要用于制造染料、工业润滑剂和医药等,它也被用作芳香剂成分。
由于苯酚具有广泛的应用,因此对苯酚的热力学数据的研究对于更好地理解它的结构和特性具有重要意义。
苯酚的热力学数据大致可以分为三部分:一、熔点苯酚的熔点在比较宽的温度范围内,其熔点取决于苯酚的结构,熔点和相关定质事件的活化能之间存在着密切的关系。
一般来说,苯酚的熔点范围大约为5-90℃,取决于它的结构,但也可以通过化学反应调节。
二、沸点苯酚具有较高的沸点,一般在110-180℃。
其中,沸点的高低取决于所采用的苯酚的结构,它的结构越复杂,其沸点也越高,因此,在实际应用中,苯酚可以在一定温度范围内制备成不同的结构,以提高特定性能。
三、热分解温度苯酚的热分解温度一般为320-420℃,其分解温度可以根据拆分率和拆分产物的构型来进行控制,以获得最佳性能。
热分解温度高的苯酚可以在高温条件下得到更高的分解比例。
四、燃烧温度苯酚的燃烧温度约为450-600℃,这是由于苯酚的分子结构密度和氧化性质决定的,苯酚的燃烧温度越高,其安全性越高,可以更好地保护环境和人类健康。
以上是关于苯酚的热力学数据的主要介绍,热力学数据在苯酚的合成、利用和应用中占据着重要地位,因此,对苯酚的热力学数据的研究对更好地提高它的应用价值至关重要。
另外,苯酚的热力学性质也可以用来区分不同结构式的苯酚,从而实现特定性能的优化。
最重要的是,苯酚的热力学数据也可以帮助我们更好地了解苯酚的结构特性,从而实现有效合成和利用,为合成苯酚的化学反应提供可行方案。
总之,对苯酚的热力学数据的深入研究,可以为苯酚的结构和特性的研究提供更多有价值的信息,以期实现更高效,更安全的应用。
热力学数据

附录Ⅳ若干种热力学数据表1.单质和无机物物质适用温度范围/KAg0 042.71225.48 23.975.284-0.25293~1234-506.14 -437.09 167.36-30.56 -10.82 121.71 65.57Al(s)0 028.31524.35 20.67 12.38273~931.7Al(g)313.80 273.2 164.553-1669.8 -2213.160.98679.0 92.3837.535-26.86127~1937-3434.98 -3728.53 239.3 259.4 368.57 61.92 -113.47298~1100111.88482.396175.02130.71 3.109 245.455 35.99 37.200.690-1.188300~1500C(金刚石) 1.896 2.8662.4396.079.1213.22 -6.19 ~1200C(石墨)0 05.6948.6617.154.27-8.79298~2300CO(g)-110.525 -137.285 198.01629.14227.6 5.0290~2500-393.511 -394.38 213.7637.1244.149.04-8.54298~2500Ca(s)0 0 41.63 26.27 21.92 14.64 273~673-62.8 -67.8 70.2 62.34 68.6 11.88 -8.66 298~720-1206.87 -1128.70 92.8 81.83 104.52 21.92 -25.94 298~1200-795.0 -750.2 113.8 72.63 71.88 12.72 -2.51 298~1055CaO(s)-635.6 -604.2 39.7 48.53 43.834.52-6.52298~1800-986.5 -896.89 76.1 84.5(硬石膏)-1432.68 -1320.24 106.7 97.65 77.49 91.92 -6.561273~1373 -167.456 -131.168 55.10Cu(s)0 0 33.32 24.47 24.564.18-1.201 ~1357CuO(s)-155.2 -127.1 43.51 44.4 38.79 20.08 298~1250-166.69 -146.33 100.8 69.8 62.34 23.85 298~12000 0 203.5 31.46 34.691.84-3.35273~2000 0 27.15 25.23 17.28 26.69 273~1041-747.68 -673.84 92.8 82.13 48.66 112.1 298~885FeO(s)-266.52 -244.3 54.0 51.1 52.806.242-3.188273~1173-822.1 -741.0 90.0 104.6 97.74 17.13 -12.887298~1100-117.1 -1014.1 146.4 143.42 167.03 78.91 -14.88 298~1100(续表)物质适用温度4 00 0130.69528.8329.08-0.842.0300~15000 0144.88429.228.5770.8791.958298~1500HBr(g)-36.24 -53.22 198.6029.1226.155.861.09298~1600HBr(aq)-120.92 -102.8080.7 1HCl(g)-92.311 -95.265186.78629.1226.534.61.90298~2000HCl(aq)-167.44 -131.1755.1 0-698.7 -623.37 191.2Hl(g)-25.94 -1.32 206.4229.1226.325.940.92298~1000-241.825 -228.577188.82333.57130.1211.30273~2000-285.838 -237.14269.94075.296-291.850 (-234.03) (39.4)-187.61 -118.04 102.2682.2 9-20.146 -33.040 205.7533.9729.2915.69273~1300-811.35 (-866.4) 156.85 137.57 -811.32-885.75 -752.99 126.8662.242 19.34 260.6036.8 70 0191.59829.1226.874.27273~2500-46.19 -16.603 192.6135.6529.7925.48-1.665273~1400NO(g)89.860 90.37210.30929.86129.583.85-0.59273~150033.85 51.86 240.5737.942.938.54-6.7481.55 103.62 220.1038.745.698.62-8.54273~5009.660 98.39 304.42 79.083.8930.7514.92.51 110.5 342.4 108.0O(g)247.521 230.095161.06321.930 0205.13829.3731.463.39-3.77273~2000142.3 163.45 237.738.1 5-229.940 -157.297-10.53 9S(单斜)0.29 0.09632.5523.6414.929.08368.6~392S(斜方)0 0 31.922.614.9826.11273~368.6(g)124.94 76.08 227.7632.5536.111.09273~2000S(g)222.80 182.27167.825-3.51-395.18 -370.40 256.3450.757.3226.86 -13.05273~900-907.51 -741.90 17.2 2.有机化合物在指定温度范围内恒压热容可用下式计算物质适用温度范围/K烃类-74.847 50.827 186.3035.71517.45160.461.117-7.205298~1500226.748 209.200200.92843.92823.4685.768-58.34215.870298~150052.283 68.157 219.56 43.564.197154.59-81.09016.815298~1500-84.667 -32.821 229.6052.654.936182.259-74.85610.799298~150020.414 62.783 267.05 63.893.305235.86-117.60022.677298~1500-103.847 -23.391 270.02 73.51-4.799307.311-160.15932.748298~1500-0.13 71.60 305.71 85.652.540344.929-191.28441.664~1500-6.99 65.96 300.94 78.918.774342.448-197.32234.271298~1500-11.17 63.07 296.59 87.828.381307.541-148.25627.284298~1500-16.90 58.17 293.70 89.127.084321.632-166.07133.497298~1500-126.15 -17.02 310.23 97.450.469385.376-198.88239.996298~1500-134.52 -20.79 294.75 96.82-6.841409.643-220.54745.739298~150082.927 129.723 269.31 81.67 -33.899471.872-298.34470.835298~150049.028 124.597 172.35 135.77 59.50 255.01 281~353-123.14 31.92 298.51 106.27 -67.664679.452-380.76178.006298~1500-167.19 -0.09 388.85 143.093.084565.786-300.36962.061298~1500-198.82 -4.08 295.89 194.9349.999 122.388 319.86 103.76 -33.882557.045-342.37379.873298~150018.995 122.207 352.86 133.26 -14.811591.136-339.59074.697~1500-24.439 110.495 246.48 187.917.238 118.977 357.80 127.57 -27.384620.87-363.89581.379298~1500-25.418 107.817 252.17 183.317.949 121.266 352.53 126.86 -25.92460.670-350.56176.877298~1500(续表)物质适用温度范围/K -24.426 110.244 247.36 183.7含氧化合物-115.90 -110.0 220.2 35.3618.8258.379-15.606291~1500-362.63 -335.69 251.1 54.4 30.67 89.20-34.539300~700-201.17 -161.83 237.8 49.4 20.42 103.68-24.64~700-238.57 -166.15 126.8 81.6-166.36 -133.67 265.8 62.831.054121.457-36.577298~1500-487.0 -392.4 159.8 123.4 54.81 230-436.4 -381.5 293.4 72.4 21.76 193.09 -76.78 300~700-277.63 -174.36 160.7 111.46 106.52 165.7 575.3 283~348-235.31 -168.54 282.1 71.120.694-205.38-99.809300~1500-248.283 -155.33 200.0 124.73 55.61 232.2 298~320-216.69 -152.2 296.00 75.322.472201.78-63.521298~1500-273.2 -116.47 253.1 170.7 290-384.55 -245.5 170.7 155.2 卤代烃-82.0 -58.6 234.29 40.7914.90396.2-31.552273~800-88 -59 270.62 51.38 33.47 65.3 273~800-131.8 -71.4 202.9 116.3-100 -67 296.48 65.8129.506148.942-90.713273~800-139.3 -68.5 214.43 131.75 97.99 111.71 273~330-106.7 -64.0 309.41 85.51116.3 -198.2 197.5 145.6含氮化合物(待续)见网页(fulu4b2s2.html)(续表)物质适用温度范围/K78.87 159.9 179.1 140.2 29335.31 153.35 191.6 199.6 338.28 -1068.6 2022.1 278~34815.90 146.36 244.3 185.4 293本附录数据主要取自Handbook of Chemistry and Physics ,70 th Ed.,1990;Editor John A.Dean ,Lange's Handbook of Chemistry ,1967。
4-氰基-3-羟基丁酸乙酯生成焓

4-氰基-3-羟基丁酸乙酯生成焓让我们了解一下4-氰基-3-羟基丁酸乙酯的结构和性质。
这是一个有机化合物,化学式为C6H9NO3。
它的结构中含有一个羟基和一个氰基,分子中还有一个乙酯基。
这个化合物常用于医药领域,具有一定的药理活性。
生成焓,也称为反应焓,是指一定反应条件下反应物转变为产物时释放或吸收的热量。
对于4-氰基-3-羟基丁酸乙酯的生成焓,我们需要了解它的合成过程以及反应热量的计算方法。
4-氰基-3-羟基丁酸乙酯的合成通常可以通过酯化反应来实现。
酯化反应是一种有机化学反应,通常涉及醇和酸酐的反应,生成酯和水。
具体到这个化合物的合成过程,可以使用乙醇和4-氰基-3-羟基丁酸反应得到4-氰基-3-羟基丁酸乙酯。
在这个反应过程中,乙醇作为醇试剂,4-氰基-3-羟基丁酸作为酸酐试剂,它们发生酯化反应,生成目标化合物4-氰基-3-羟基丁酸乙酯,并伴随着水的生成。
此外,这个反应过程是一个放热反应,反应过程中会释放热量。
生成焓的计算通常可以通过燃烧实验来确定。
在燃烧实验中,将一定量的化合物完全燃烧,测量产生的热量,根据燃烧产物的生成物的物质量和生成焓的定义,可以计算出反应的生成焓。
对于4-氰基-3-羟基丁酸乙酯的生成焓,可以通过燃烧实验来测定。
除了燃烧实验,生成焓的计算还可以通过其他方法来确定,如利用反应的热力学数据计算。
热力学数据指的是反应过程中各种物质的热力学参数,如标准生成焓、标准反应焓等。
通过这些数据,可以计算出反应的生成焓。
4-氰基-3-羟基丁酸乙酯的生成焓是指在一定条件下,通过酯化反应合成该化合物时释放或吸收的热量。
生成焓的计算可以通过燃烧实验或利用热力学数据来确定。
这个化合物在医药领域有一定的应用价值,深入了解其生成焓可以为相关领域的研究提供参考。
物理化学原理在有机化学教与学中的应用(共2篇)

物理化学原理在有机化学教与学中的应用(共2篇)本文从网络收集而来,上传到平台为了帮到更多的人,如果您需要使用本文档,请点击下载按钮下载本文档(有偿下载),另外祝您生活愉快,工作顺利,万事如意!第1篇:物理化学原理在有机化学教与学中的应用有机化学教与学中常常涉及化合物的稳定性判断,分析和讨论有机分子的稳定性是有机化学的重要内容之一,因为物理有机化学的反应性与其稳定性是密切相关的。
可燃物质B的标准摩尔燃烧焓是指在标准压力下,反应温度时,单位量的物质B完全燃烧为同温下的指定产物时的标准摩尔焓变,用符号表示为ΔcHθm(B,相态,T),下标“c”和“m”分别表示燃烧和反应进度为1mol。
燃烧产物指定为:该化合物中C变为CO2(g),H变为H2O(l),S变为SO2(g),N变为N2(g),Cl成为HCl(水溶液),金属成为游离状态。
燃烧焓可以很精确地测量,它是重要的热化学数据。
本文以烷烃、环烷烃和烯烃的稳定性为例,介绍燃烧焓在有机化学中的应用。
一、烷烃同分异构体的相对热化学稳定性烷烃和所有其他碳氢化合物一样,都是可燃的。
烷烃完全燃烧,生成CO2(g)和H2O(l),并放出大量的热:CnH2n+2+O2(g)→nCO2(g)+(n+1)H2O(l)ΔrHθm(T)=Δc Hθm(CnH2n+2,T)燃烧焓的测定数据表明:直链烷烃分子每增加一个CH2,其燃烧焓数值的增加基本上是一个定值,即约为-·mol-1。
例如,甲烷、乙烷、丙烷和丁烷标准摩尔燃烧焓分别为-·mol-1、-·mol-1、-·mol-1和-·mol-1。
利用烷烃异构体燃烧焓的大小可以推测烷烃异构体的相对热化学稳定性。
在烷烃的同分异构体中,支链烷烃的燃烧焓比直链烷烃大。
支链越多,燃烧焓越大。
实验数据表明:在烷烃异构体中,支链最多的燃烧焓最大,也最稳定。
烷烃异构体燃烧时生成的产物相同,均为CO2(g)和H2O(l),反应消耗O2(g)的量和生成产物的量也相同。
化工热力学常用数据手册

常用数据手册D. R. Lide,“CRC Handbook of Chemistry and Physics”,77th ed.,ChemicalRubber Co,该手册是美国化学橡胶公司(Chemical Rubber Co,简称CRC)出版的一部著名化学和物理学科的工具书。
它初版于1913年,以后逐年改版,内容不断完善更新。
该手册资料丰富,查阅方便,为人们提供了可靠的常用基础数据。
全书由目录、正文、附录和索引组成,正文分16个部分。
其中:第3部分是有机化合物的物理常数。
主要内容是有机化合物的物理常数表,收录了1.5万多种有机化合物的物理常数。
第4部分是元素和无机化合物的性质。
主要内容为元素和各种化合物的物理和化学性质、无机化合物的物理常数表。
第5部分是热力学、电化学和动力学。
主要内容有化学物质的标准热力学性质、某些有机化合物的燃烧焓、无机化合物的融化焓、电解质水溶液的当量导电率、电解质的溶解焓等。
第6部分是流体的性质,汇集了流体的各种物理和化学数据。
主要内容有流体的热物理性质、蒸气压、气体在水中的溶解度、某些化合物的临界常数、沸点、熔点、无机物和有机物的气化焓、共沸混合物、流体的粘度等。
第7部分是生物化学和营养。
第8部分是分析化学,包括试剂的制备、酸碱盐的标准溶液、有机分析试剂、酸碱指示剂、荧光指示剂、电化次序、酸碱在水溶液中的解离常数,溶解度表等。
J. A. Dean; “L ange’s Handbook of chemistry”,14th ed,McGraw-Hill New York,1992这是一本著名的化学数据手册,1934年发行第一版。
正文以表格形式为主,共分为11个部分。
其中有(9)热力学性质和(10)物理性质。
每一部分的前面有目次表,书末有主题索引。
该手册的第13版有中译本,名为《兰氏化学手册》,由尚久方等翻译,1991年3月科学出版社出版。
R. C. Reid et.al.,“The properties of Gases and Liquids,” Fourth ed.,McGraw-Hill,New York,1987该书共分11个部分:(1)物理性质的估算;(2)纯组分常数,包括临界性质、偏心因子、沸点、熔点及偶极矩;(3)纯气体的PVT关系;(4)混和物的容积性质;(5)热力学性质;(6)理想气体热力学性质;(7)纯液体的蒸气压和蒸发焓;(8)多组元系统的流体相平衡;(9)粘度;(10)导热系数;(11)表面张力。
环己酮氧化到己二酸的热力学数据,含平衡常数

环己酮氧化到己二酸的热力学数据,含平衡常数1 环己酮和己二酸的性质环己酮(C6H10O)和己二酸(C6H10O4)都是有机化合物,它们在化学性质上表现出明显的不同。
环己酮是一种酮类化合物,其分子中含有一个碳酰基。
而己二酸是一种二元酸,其分子中含有两个羧基官能团。
这两种化合物都具有一定的热稳定性和化学稳定性。
2 环己酮的氧化反应环己酮可发生氧化反应,将其氧化为己二酸。
环己酮的氧化反应需要催化剂存在,一般使用催化剂为二氧化锰(MnO2),高锰酸钾(KMnO4)或某些金属催化剂。
环己酮的氧化反应可以分为两步进行。
首先,环己酮被氧化为环己酮酸,然后进一步氧化为己二酸。
反应式如下:环己酮+ 1/2 O2 → 环己酮酸环己酮酸+ 1/2 O2 → 己二酸氧化反应中的反应物是环己酮和氧气,产物是己二酸,而催化剂则促进了反应的进行。
3 热力学数据环己酮氧化为己二酸是一个放热反应。
该反应的热力学数据如下:反应热ΔH0 = -1673 kJ/mol标准生成焓ΔHf0 = -1264 kJ/mol标准摩尔熵S°= 250 J·K-1·mol-1平衡常数K= 1.038×10^13反应热是反应过程中释放的热量。
反应热为负数说明反应为放热反应,反之则为吸热反应。
而标准生成焓则是反应生成产物的热效应。
标准生成焓为负数说明反应的生成物热稳定性高。
标准摩尔熵则涉及到反应物和产物的分子结构和运动方式,是反应的另一个重要热力学参数。
平衡常数则是反应在平衡态下反应物浓度和产品浓度之比。
4 反应机理由于环己酮的结构中含有一个碳酰基,因此,它会与氧气发生加成反应生成环己酮酸。
这是氧化反应的第一步。
环己酮酸之后再发生另一轮加成反应,加上氧气进一步氧化生成己二酸。
反应过程如下:1. 环己酮被氧气加成生成环己酮酸,反应式为:C6H10O + 1/2 O2 → C6H10O32. 环己酮酸被氧气再次加成,氧气中的两个氧原子分别被加到环己酮酸分子的两个碳上生成己二酸,反应式为:C6H10O3 + 1/2 O2 → C6H10O45 应用和意义环己酮氧化为己二酸是一种重要的有机氧化反应,具有广泛的应用前景。
乙二醇物性数据

乙二醇物性数据乙二醇(Ethylene Glycol)是一种常用的有机化合物,化学式为C2H6O2。
它是一种无色、无臭、粘稠的液体,在许多工业和消费品中广泛应用。
乙二醇具有许多重要的物性数据,下面将详细介绍乙二醇的几个关键物性数据。
1. 密度(Density):乙二醇的密度是指单位体积内所含质量的大小。
普通情况下,乙二醇的密度为1.113 g/cm³。
这意味着在标准温度和压力下,每立方厘米的乙二醇质量为1.113克。
2. 沸点(Boiling Point):乙二醇的沸点是指在标准大气压下,乙二醇从液态转变为气态的温度。
乙二醇的沸点约为197°C。
这个高沸点使得乙二醇在许多应用中作为溶剂和冷却剂非常实用。
3. 熔点(Melting Point):乙二醇的熔点是指在标准大气压下,乙二醇从固态转变为液态的温度。
乙二醇的熔点约为-13°C。
这个相对较低的熔点使得乙二醇在低温应用中具有重要的作用,例如作为防冻剂和制冷剂。
4. 折射率(Refractive Index):乙二醇的折射率是指光线在乙二醇中传播时的折射程度。
乙二醇的折射率通常在1.431至1.432之间。
折射率的测量可以用于确定乙二醇的纯度和浓度。
5. 粘度(Viscosity):乙二醇的粘度是指其内部阻力对流体流动的妨碍程度。
乙二醇的粘度通常在15至20毫帕·秒之间。
粘度的测量对于乙二醇在润滑剂和化工工艺中的应用非常重要。
6. 热导率(Thermal Conductivity):乙二醇的热导率是指其传导热量的能力。
乙二醇的热导率约为0.25 W/(m·K)。
这个相对较高的热导率使得乙二醇在热交换和冷却应用中具有良好的性能。
7. 比热容(Specific Heat Capacity):乙二醇的比热容是指单位质量乙二醇在吸收或者释放热量时所需的能量。
乙二醇的比热容约为2.42 J/(g·K)。
《化工设计》第二节基本物性数据资料

1
Tr
例题:P53
热容—一定量物质温度升高一度所需的热量。 单位:SI:kJ/(kg 〃 K) ;kJ/(kmol〃K) CGS: cal/(g〃℃); cal/(gmol〃℃ ) (一) 理想气体的热容 1.理想气体的热容与温度的关系 公式:Cp0=a + bT + cT2 + dT3
获取物性数据的方法主要有以下几种: (1)查手册或文献资料;
《化学工程手册》、《化工工艺设计手
册》、《无机盐工业手册》、《石油化
工基础数据手册》、《氮肥工业设计手
册》、《小型合成氨厂设计手册》、
《纯碱工业》等。
(2)估算; (3)用实验直接测定。 当查手册或文献资料得不到所需数据时,估算 和用实验直接测定两法应首选估算法。 目前,应用计算机储存、检索和推算物性数据 日益增多。相应建立了物性数据库,可通过计 算机自动检索或估算所要求的数据。
0V m 推导过程:PV=nRT= M RT M RT
MP M 即: RT RT P M M kg / m 3 0.08206 273 .15 / 1 22.4
涉及到的单位问题:
R:0.08206(atm·m3)/(kmol·K); P:1atm;T:273.15K
(一)有机物临界常数的估算( Lydersen基团贡献法)
TC
0.567 T T
2
Tb
P C
0.34 P
M
2
VC 40 V
例题:见WORD论文
(二)无机化合物临界常数的估算 无机化合物及非金属元素(正常沸点与临界温 度之间的比例有关联式),即:
第二章有机热载体及其热力学性质分析

第二章有机热载体及其热力学性质分析有机热载体即热传导液,习惯称做导热油、热媒等。
有机热载体加热技术是伴随现代工业而产生、发展的。
在我国,20世纪80年代以来,有机热载体加热技术的应用领域迅速扩展,显现出巨大的发展潜力。
作为传热介质,有机热载体无论从使用性能还是安全性能角度都有着同于水、水蒸气和一般石化产品的特殊性能要求和检测方法[1]。
2.1 有机热载体的发展概况导热油又称传热油,正规名称为热载体油(GB/T4016-83),英文名称为Heat transfer oil,所以也称热导油,热煤油等。
20世纪初,随着工业的发展,传统的加热方式已不能满足要求,人们开始在传热工艺中使用矿物油产品如机械油、汽缸油作为热载体以代替水或者蒸汽。
20世纪30年代,美国DOW 化学公司研制的合成化学品(联苯-联苯醚),不仅使加热工艺安全可靠,而且介质温度可达400℃,标志着有机热载体的商品化产品的问世。
在工业生产中,常见的热载体有无机热载体和有机热载体之分。
典型的无机热载体有水及蒸汽、熔盐、液态金属(如汞)等。
有机热载体,在化学类别上属于有机化学物质。
水及蒸汽是最常用的无机热载体,虽然廉价而且稳定,但在100℃以上蒸汽压力迅速升高,压力越高设备投资成本就会越大,操作要求就会越高。
因此,大多都在200℃以下使用。
溶盐和液态金属可分别在400℃~500℃和500℃~800℃的高温范围内使用,但投资昂贵,不易广泛使用。
有机热载体一般在200℃~400℃温度范围使用。
由于其具有使用温度范围宽、操作压力低、控温精度高、对设备无腐蚀等优点,现已成为除水及蒸汽以外使用最广、用量最大的传热介质[1]。
2.2 有机热载体的主要性能要求导热油是一种热量的传递介质,由于其具有加热均匀,调温控制温准确,能在低蒸汽压下产生高温,传热效果好,节能,输送和操作方便等特点,近年来被广泛应用于各种场合,而且其用途和用量越来越多。
但是我们在实际运行过程中还要特别注意有机热载体的热稳定性、氧化安定性、低温流动性、传热性、蒸发性、安全性等一些性能要求,不然不仅会达到我们的运行要求,而且还会造成无法估计的损失,甚至造成更大的安全事故。
有机化合物标准热力学数据
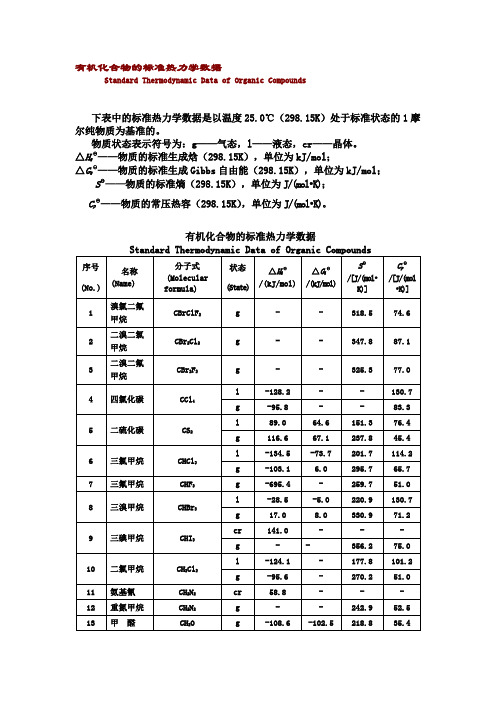
SΘ——物质的标准熵(298.15K),单位为J/(mol•K);
CpΘ——物质的常压热容(298.15K),单位为J/(mol•K)。
有机化合物的标准热力学数据
Standard Thermodynamic Data of Organic Compounds
有机化合物的标准热力学数据
Standard Thermodynamic Data of Organic Compounds
下表中的标准热力学数据是以温度25.0℃(298.15K)处于标准状态的1摩尔纯物质为基准的。
物质状态表示符号为:g——气态,l——液态,cr——晶体。
△HfΘ——物质的标准生成焓(298.15K),单位为kJ/mol;
-
-
-
g
180.6
-
-
-
75
丙炔
C3H4
g
184.9
-
-
-
76
丙二烯
C3H4
g
190.5
-
-
-
77
咪唑
C3H4N2
cr
58.5
-
-
-
78
丙烯酸
C3H4O2
l
-383.8
-
-
145.7
79
丙腈
C3H5N
l
15.5
-
-
119.3
g
51.5
-
-
-
80
三硝酸甘油酯
C3H5N3O9
l
-370.9
-
-
-
g
-270.9
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
△ Gf
Θ
SΘ
/[J/(mol K)] 318.5 347.8 325.3 151.3 237.8 201.7 295.7 259.7 220.9 330.9 356.2
C pΘ
/[J/(mol K)] 74.6 87.1 77.0 130.7 83.3 76.4 45.4 114.2 65.7 51.0 130.7 71.2 75.0 101.2 51.0
l g cr g l l g g cr g g cr
-236.2 -196.6 -503.3 228.2 -283.7 -67.9 -47.5 -212.0 -821.7 -723.7 79.2 -94.1 14.6 37.3 -223.4 -273.8 -243.5 -467.2 -442.1 -162.5 -510.5 31.4 64.3 -92.0 52.5 -191.8 -166.2 -77.8 -52.6 -484.5 -432.8
(State) /(kJ/mol) g g g l g l g l g g l g cr g l g -128.2 -95.8 89.0 116.6 -134.5 -103.1 -695.4 -28.5 17.0 141.0 -124.1 -95.6
/(kJ/mol)
64.6 67.1 -73.7 6.0 -5.0 8.0 -
58.8 -108.6 -424.7 -378.6 -59.4 -35.5 -81.9 -12.3 14.7 -74.4 -254.0 -113.1 -74.7 -159.0 -333.6 -239.1 -201.5 -46.4 -22.3 -47.3 -22.5 54.0 94.3 -50.6 -280.8 -202.8 -497.9 -820.5 -658.9 -43.6 -8.1
47 48 49 50
乙酰氟 乙酰碘 氯乙酸 乙 腈
C2H3FO C2H3IO C2H3ClO2 C2H3N
51 52 53
异氰酸甲 酯 乙 乙 烯 醛
C2H3NO C2H4 C2H4O
54
环氧乙烷
C2H4O
55
乙
酸
C2H4O
�
三氯乙腈 四氯乙烯 三氯乙酰 氯 六氯乙烷 三氟乙腈 四氟乙烯 氯乙炔 三氯乙烯
36 37 38 39 40 41 42 43
三氯乙醛 三氯乙酸 乙炔 氯乙酰氯 乙烯酮 乙二醛 草 酸
C2HCl3O C2HCl3O2 C2H2 C2H2Cl2O C2H2O C2H2O2 C2H2O4 C2H3Br
151.0 43.9 51.8 91.0 55.5 59.4 53.7 117.0 67.8 91.4 52.2 43.6 89.0 55.3 88.0 47.9 123.3 66.5
溴乙烯
44
氯乙烯
C2H3Cl
l g
45 46
乙酰溴 乙酰氯
C2H3BrO C2H3ClO
l l g l g l cr l g l g l g l g l g
52.5 35.4 99.0 42.4 40.8 37.5 126.0 44.1 35.3 106.6 57.3 157.3 81.1 43.9 90.5 50.3 102.1 50.1 134.9 71.1 96.1 143.4 198.2 77.9 80.5 54.3 124.4 80.3
15 16 17 18 19 20 21 22 23 24
210.7 -48.3 81.8 53.6 -208.0 -205.8 77.2 81.7 68.4 -127.6 -132.8 -11.8 -13.0 -389.9 -374.5
200.9 247.6 109.8 275.8 264.0 200.8 295.1 149.6 245.1 219.6 160.2 263.7 153.9 242.5 159.8 282.5
-102.5 -361.4 -26.3 -50.3 -14.4 -6.8 -43.4 -166.6 -162.6 -7.7 -9.3 35.7 32.7 180.0 187.0 3.0 -
242.9 218.8 129.0 246.4 234.6 222.9 163.2 254.1 186.3 171.8 275.0 217.1 126.8 239.8 169.2 255.2 150.2 242.9 165.9 278.8 336.6 266.9 237.3 298.1 300.1 242.0 228.4 324.8
CpΘ——物质的常压热容(298.15K) ,单位为 J/(molK).
有机化合物的标准热力学数据 Standard Thermodynamic Data of Organic Compounds
序号 (No.) 1 2 3 名称 (Name) 溴氯二氟 甲烷 二溴二氯 甲烷 二溴二氟 甲烷 四氯化碳 分子式 (Molecular formula) CBrClF2 CBr2Cl2 CBr2F2 状态 △ Hf
4
CCl4
5
二硫化碳
CS2
6 7 8
三氯甲烷 三氟甲烷 三溴甲烷
CHCl3 CHF3 CHBr3
9
三碘甲烷
CHI3
10
二氯甲烷
CH2Cl2
177.8 270.2
11 12 13 14
氨基氰 重氮甲烷 甲 甲 醛 酸
CH2N2 CH2N2 CH2O CH2O2
cr g g l g l g g g l g g l l g l cr l g l g l g l g g l l cr g cr g g l g
有机化合物的标准热力学数据
Standard Thermodynamic Data of Organic Compounds
下表中的标准热力学数据是以温度 25.0℃(298.15K)处于标准状态的 1 摩 尔纯物质为基准的. 物质状态表示符号为:g——气态,l——液态,cr——晶体. △HfΘ——物质的标准生成焓(298.15K),单位为 kJ/mol; △GfΘ——物质的标准生成 Gibbs 自由能(298.15K),单位为 kJ/mol; SΘ——物质的标准熵(298.15K),单位为 J/(molK);
溴甲烷 氯甲烷 氟甲烷 碘甲烷 甲 烷
CH3Br CH3Cl CH3F CH3I CH4 CH3NO CH3NO2 CH3NO3 CH4N2O
甲酰胺 硝基甲烷 硝酸甲酯 脲 甲 醇Fra bibliotekCH3OH
25
甲硫醇
CH3SH
26
甲
胺
CH5N
27 28 29 30 31 32 33 34 35
甲
肼
CH6N2 C2Cl3N C2Cl4 C2Cl4O C2Cl6 C2F3N C2F4 C2HCl C2HCl3
