第九章讲义层析法
层析原理和使用方法

层析原理和使用方法
层析原理主要是利用不同物质在物理或化学性质上的差异,通过这些差异实现混合物中各组分的分离。
具体来说,层析技术包括但不限于吸附层析、分配层析、离子交换层析和凝胶过滤等方法。
使用方法:层析技术主要包括柱层析和薄层层析两种形式。
柱层析是将固定相装入柱内,使样品沿着一个方向移动而分离的方法。
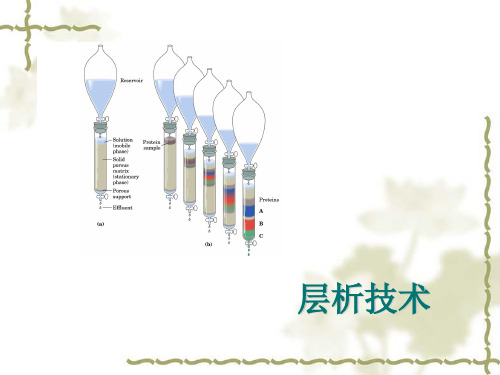
在操作时,先在圆柱管中填充不溶性基质形成固定相,然后将样品加到柱子上,用特殊溶剂洗脱,溶剂组成流动相,在样品从柱子上洗脱下来的过程中实现分离。
薄层层析则是将适当粘度的固定相均匀铺在薄板上,点样后,用流动相展开,从而实现分离。
薄层层析法分离色素[讲义]
![薄层层析法分离色素[讲义]](https://img.taocdn.com/s3/m/0dbcce0e2379168884868762caaedd3383c4b52c.png)
实验八色素的分离(层析法)一、目的要求1.掌握薄层板的制备及薄层层析的操作方法。
2.掌握吸附剂活度测定的原理及方法。
3. 掌握偶氮苯和苏丹红(III)的分离方法二、实验原理薄层层析是将吸附剂或者支持剂(有时加入固化剂)均匀地铺在一块玻璃上,形成薄层。
把欲分离的样品点在薄层板的一端,然后将点样端浸入适宜的展开剂中, 在密闭的层析缸中展开,使混合物得以分离的方法。
由于层析在薄层上进行故而得名。
薄层层析是一种微量、快速的层析方法。
它不仅可以用于纯物质的鉴定,也可用于混合物的分离、提纯及含量的测定,还可以通过薄层层析来摸索和确定柱层析时的洗脱条件。
薄层层析根据作为固定相的支持物不同,分为薄层吸附层析(吸附剂)、薄层分配层析(纤维素、硅胶、硅藻土)、薄层离子交换层析(离子交换剂)、薄层凝胶层析(分子筛凝胶)等。
薄层层析中以吸附薄层为多用,吸附薄层中常用的吸附剂为氧化铝和硅胶(氧化铝的活化温度为150℃-160℃,硅胶的活化温度为105℃-110℃)。
吸附薄层主要是利用吸附剂对样品中各成分吸附能力不同,及展开剂对它们的解吸附能力的不同,使各成分达到分离。
分配薄层层析在展开过程中,各成分在固定相和流动相之间作连续不断的分配,由于各成分在两相间的分配系数不同,因而可以达到相互分离的目的。
薄层层析选择展开剂视被分离物的极性及支持剂的性质而定。
如果薄层层析所用的支持剂是吸附剂,在同一吸附剂上,不同化合物的吸附性质有如下规律:1.饱和碳氢化合物不易被吸附;2.不饱和碳氢化合物易被吸附,分子中双键愈多,则吸附得愈紧密;3.当碳氢化合物被一个功能基取代后,吸附性增大。
吸附性较大的化合物,一般需用极性较大的溶剂才能推动它。
选择展开剂的另一个依据是溶剂的极性大小。
极性大的化合物需用极性大的展开剂,极性小的化合物需用极性小的展开剂。
一般情况下,先选用单一展开剂如苯、氯仿、乙醇等,如发现样品个组分的R值较大,可改用或加入适量极性小的展开剂如石油醚等。
层析法

硅胶吸附柱色谱技术实际应用色谱法,又称层析法.是一种以分配平衡为机理的分配方法.色谱体系包含两个相,一个是固定相,一个是流动相.当两相相对运动时,反复多次的利用混合物中所含各组分分配平衡性质的差异,最后达到彼此分离的目的.色谱法从发明到现在已有八十多年的历史.它是纯化和分离有机或无机物的一种方法.色谱法按固定相的状态可分为柱色谱.平板色谱和棒色谱三种而实验室中最常用的是柱层析和薄层层析,以及它们之间的配合应用.[1]柱层析[2]1 吸附色谱地原理在一定条件下,硅胶与被分离物质之间产生作用,这种作用主要是物理和化学作用两种.物理作用来自于硅胶表表面与溶质分子之间的范德华力.化学作用主要是硅胶表面的硅羟基与待分离物质之间的氢键作用.2操作步骤2.1 硅胶准备[3]硅胶一般选用250-400目(即40-63μm直径的硅胶颗粒),根据ΔRf选用硅胶的用量.2.2 实验仪器准备一支玻璃色谱柱,一个铁架台,烧杯,锥形瓶,径口直径较大的玻璃漏斗,一支玻璃棒,2.3 装柱[4]2.3.1 吸附剂的加入①干法:将吸附剂一次加入色谱管,振动管壁使其均匀下沉,然后沿管壁缓缓加入开始层析时使用的流动相,或将色谱管下端出口加活塞,加入适量的流动相,旋开活塞使流动相缓缓滴出,然后自管顶缓缓加入吸附剂,使其均匀地润湿下沉,在管内形成松紧适度的吸附层。
操作过程中应保持有充分的流动相留在吸附层的上面。
②湿法:将吸附剂与流动相混合,搅拌以除去空气泡,徐徐倾入色谱管中,然后再加入流动相,将附着于管壁的吸附剂洗下,使色谱柱表面平整。
俟填装吸附剂所用流动相从色谱柱自然流下,液面将柱表面相平时,即加试样溶液.2.3.2试样的加入①将试样溶于层析时使用的流动相中,再沿色谱管壁缓缓加入。
注意勿使吸附剂翻起。
或将试样溶于适当的溶剂中。
与少量吸附剂混匀,再使溶剂挥发去尽后使呈松散状;将混有试样的吸附剂加在已制备好的色谱柱上面。
如试样在常用溶剂中不溶解,可将试样与适量的吸附剂在乳钵中研磨混匀后加入。
层析(包括:吸附层析、分配层析、离子交换层析、亲和层析等)

2、层析法是目前广泛应用的一种分离技术, 是分离各种生物大分子的主要手段之一,是 利用不同物质理化性质的差异而建立起来的 技术。
3、40年代:两位英国科学家Martin和 Synge发明了分配色谱(层析),他们首先 提出了色谱塔板理论,获得了1952年的诺 贝尔化学奖。由此,层析技术成为分离生化 物质的关键技术。
将适当的高分子有机吸附剂制成薄 膜,以类似纸层析方法进行物质的 分离
凝胶层析
(gel chromatography)
凝胶排阻层析(gel exclusion chromatography) 分子筛层析(molecular sieve chromatography) 凝胶过滤(gel filtration) 凝胶渗透层析(gel permeation chromatography)
❖ K值小表示某溶质在流动相中浓度 大,故在洗脱液中出现较早
❖ 有相似的K值,则表明两组分层析峰 会发生重叠,分离效果差
分配系数主要与下列因素有关: ①被分离物质本身的性质 ②固定相和流动相的性质 ③层析柱的温度。
不同的层析机理,其K值函义不同:
❖ 吸附层析中K值表示吸附平衡常数 ❖ 分配层析中K值表示分配系数 ❖ 离子交换层析中K表示交换常数 ❖ 亲和层析中K表示亲和常数。
凝胶层析的定义:
凝胶是一种具有 多孔、网状结构的 分子筛。利用这种 凝胶分子筛对大小、 形状不同的分子进 行层析分离,称凝 胶层析 。
葡聚糖一凝、胶凝(胶d的ex种tra类n和)性质 聚丙烯酰胺凝胶(polyacrylamide) 琼脂糖凝胶(agarose) Sephacryl Superdex 聚苯乙烯凝胶
• 排阻极限代表一种凝胶能有效分离的最大分子量, 大于这种凝胶的排阻极限的分子用这种凝胶不能得 到分离
五种层析方法和原理

五种层析方法和原理五种层析方法和原理1. 列点 1•新华字典定义:层析方法是一种通过分析物质内部不同成分在不同条件下的分布情况,从而推断物质组成、性质和结构的方法。
•原理:层析方法基于物质成分在固定相和流动相之间的分配行为。
固定相通常是固体或涂覆在固体上的物质,而流动相则是向上或向下流动的溶剂。
2. 列点 2•薄层层析法:–原理:薄层层析法是一种将样品溶解在溶剂中后涂覆在薄层板的表面上,然后通过毛细作用将溶剂上升至薄层表面,样品成分分离的方法。
根据样品成分的亲疏水性质和与固定相的相互作用,不同成分会以不同的速度在薄层板上移动,从而实现分离。
–应用:薄层层析法常用于化学品分析、食品检测和药物分析等领域。
3. 列点 3•气相层析法:–原理:气相层析法是利用气体(流动相)和涂覆在固体或涂覆在固体上的涂层(固定相)之间的分配作用,使样品成分在涂层上分离的方法。
样品经过蒸发后进入气化室,在高温和惰性气体的作用下,样品成分分解为气体状态,然后进入色谱柱,通过不同成分与固定相的相互作用,实现分离。
–应用:气相层析法广泛应用于环境监测、食品安全检测和生物医药领域。
4. 列点 4•液相层析法:–原理:液相层析法是通过溶液中样品成分与固定相之间的相互作用,实现样品分离的方法。
当溶液通过柱子时,样品成分会根据其与固定相的相互作用力的强度和性质不同,在固定相上停留的时间也不同,从而实现分离。
–应用:液相层析法广泛应用于药物分析、食品检测和环境监测等领域。
5. 列点 5•离子交换层析法:–原理:离子交换层析法利用带电粒子(离子)之间的静电相互作用,在一定条件下,使样品中的离子与固定相中的带电粒子发生相互作用,从而实现分离。
不同离子会在不同条件下被吸附或释放,从而实现分离。
–应用:离子交换层析法常用于水质分析、药物分析和环境监测等领域。
通过以上列点方式,我们对五种层析方法的原理和应用作了简要的介绍。
这些层析方法在不同领域的分析和检测中扮演重要角色,为我们获取准确的数据和信息提供了有效手段。
9.4 层析分离法 PPT课件

第四节 层析分离法
9.4.1 柱层析法
9.4.2 平面层析法
2019/1/11
9.4.1 柱层析法
1. 吸附柱层析法
以吸附剂为固定相(硅胶、氧化铝和活性炭等)。 根据试样的性质、吸附剂的活性和流动相的极性这 三种因素来选择适宜的条件。 被分离的组分极性较强,应选择吸附性能较弱的吸 附剂,同时选择极性较强的洗脱剂;或反之。 吸附柱层析法可用于芳香族化合物的分离、倍半萜 类烯物的分离等。
装置简单、操作简便。
常作为一种不挥发高沸点有机物、生物大分子混合物 的有效、快速、简便的分离分析手段而被应用。
平面层析法与其他色谱分离有着相同或相似的分离机 理。
2019/1/11
平面层析法
纸层析和薄层层析流 动相的移动是依靠毛细作 用。 将试样点在色谱滤纸 或层析板的一端,并将该 端浸在作为流动相的溶剂 (常称之为展开剂)中, 随着溶剂向上的移动,经 过试样点时,带动试样向 上运动。
2019/1/11
凝胶柱层析法
应用 生化领域,如蛋白质、氨基酸、核酸、肽类等生物物 质的分离和制备; 抗菌素的分离、纯化,肝炎病毒的分离等; 高聚物的相对分子质量和分子质量分布测定。
2019/1/11
9.4.2 平面层析法
平面层析法(planar chromatography)主要包括薄层层 析法和纸层析法两大类。 薄层层析:将固定相涂布于平面载板上。 纸层析:直接以滤纸作为固定相。
2019/1/11
缺点:
• 缺点: 分离效率较低,不适用于挥发性试 样分离。定性定量不便。 • 应用:平板色谱法在染料、农药、医药、 有机酸碱类化合物、糖类化合物、氨基酸、 蛋白质及中草药中有效成分的分离分析中经 常被使用。也可以用于无机离子的分离。还
层析理论及技术

29
Biochemistry experiment 8
2012-7-7
凝胶柱的选择
30
Biochemistry experiment 8
2012-7-7
凝胶的前处理
a. 溶胀:称取适量凝胶干粉,用约10倍蒸馏水 浸泡24小时以上,待凝胶充分溶胀后,倾去 上层悬浮物及蒸馏水。 b. 碱洗:用0.5 M NaOH 溶液浸泡半个小时,然 后用蒸馏水洗至中性。 c. 酸洗:用0.5 M HCl 溶液浸泡半个小时,然 后用蒸馏水洗至中性。 d. 平衡:用起始缓冲液浸泡凝胶,直至凝胶液 pH与起始缓冲液相同。
根据层析分离机制
根据操作形式不同
4
按层析过程的机理分类:
5
Biochemistry experiment 8
2012-7-7
离子交换层析法原理
利用离子交换剂对各种离子的亲和力不同。 特点:利用带有相反电荷的颗粒之间具有 引力作用 固定相:带有大量电荷的离子交换剂 流动相:具有一定pH值和一定离子强度的 电解质溶液 常采用柱层析 洗脱方法:增加离子强度、改变pH值。
32 Biochemistry experiment 8 2012-7-7
上柱、洗脱、收集
a. 如图装好层析装置,打开下端出 口,使溶液流出至刚好达到凝胶 胶面 b. 沿柱壁缓慢加入2ml样品,打开下 端出口,使样品溶液流出至刚好 达到凝胶胶面,再取少量起始缓 冲液洗涤柱壁。 c. 打开起始缓冲液阀门,连续洗脱。 d. 用自动部分收集器自动或手动收 集,合并同一高峰各管。
31 Biochemistry experiment 8 2012-7-7
装柱
a. 将层析柱垂直固定,加入适 量溶剂排走空气。 b. 将平衡好的凝胶搅匀,连续 倾入柱中,待其自然沉降至 1/4~1/3高时打开下端出口, 让溶剂慢慢流出,继续侵入 凝胶至沉降到所需高度。装 柱时要注意操作压。 c. 用3-5倍柱床体积的起始缓冲 液走柱,使交换剂充分平衡, 柱床稳定。
层析法-理论ppt课件

方法:
(1) oligo(dT)-纤维素层 析柱法
(2) oligo(dT)-纤维素液 相结合离心法
(3)磁珠分离法
oligo(dT)-纤维素层析柱法
磁 珠 分 离 法
配体与载体结合
(固相化)
亲和层析
装柱
的基本过程
(亲和层析柱)
解吸附 洗柱
亲和吸附
(生物高分子与配体专一结合)
配体与载体的联接方法
固定相——滤纸上的吸附水 流动相——溶剂(乙醇、丙醇、丙酮及与水不相溶
的溶剂)
分离示意图
层 析 纸
层析缸
溶剂前沿
y x2
x1 起始线
(原点)
展开剂
Rf > 0.02 ,A 、B可分离. 与标样比较可定性鉴定
. 如果两种氨基酸的迁移速率相近,
或者氨基酸的Rf值相同,如何来分
离?
氨基酸的Rf值
展开剂 正丁醇+吡啶+水
名称
分离原理
固定相只能与一种待分离
亲和层析法 组份专一结合,以此和无 亲和力的其它组份分离
层析法的分类
• 按操作形式不同分类
名称
操作形式
柱层析法 固定相装于柱内,使样品沿着 一个方向前移而达分离
纸层析法 用滤纸作液体的载体,点样后 用流动相展开,使各组份分离
将适当的高分子有机吸附剂制成 薄膜层析法 薄膜,以类似纸层析方法进行物
加入样品 层析后
实验:胡萝卜的 柱层析分离法
柱层析示意图
薄层吸附层析
( Thin layer absorption chromatography)
薄层吸附层析是将吸附剂 均匀地在玻璃板上铺成薄层, 再把样品点在薄层板上,点样 的位置靠近板的一端。然后将 板的这端浸入适当的溶剂(流 动相)中,使溶剂在薄层板上 扩散,并在此过程中通过吸附 →解吸→再吸附→再解吸的反 复进行,而将样品各个组分分 离出来。
《生物学层析法》课件

实际应用案例
食物颜料分离
层析法可用于鉴定和分离食物中 的色素。
药物分析
层析法可以分离和测定药物中的 不同成分。
环境分析
层析法可用于环境样品中污染物 的分离和检测。
优势和局限性
1 优势
简单易操作,分离效果好,广泛应用度较慢,分离效率受到样品性质和实验条件的限制。
常见错误和注意事项
《生物学层析法》PPT课 件
层析法是一种在生物学研究中常用的分离和分析技术。本课件将介绍层析法 的概念与原理,基本步骤,不同类型的层析法,实际应用案例,优势和局限 性,常见错误和注意事项,最后进行总结。
概念与原理
层析法是一种分离和分析技术,通过不同物质在固定相和流动相中的分配系数差异,实现混合物的分离。
基本步骤
1
样品加载
将待分离的混合物加载到层析柱或层析纸上。
2
流动相流动
通过柱床或层析纸,使流动相在不同组分间逐渐分离。
3
收集分离物
按照需要,逐段收集分离得到的组分。
不同类型的层析法
薄层层析法
将样品涂抹在薄层介质上进 行分离。
柱层析法
通过柱床进行样品的分离。
气相层析法
通过气相站和液相站将混合 物分离。
错误
1. 选择错误的固定相和流动相。 2. 加载样品过多或过少。 3. 不仔细观察分离结果。
注意事项
• 准备好合适的实验器材。 • 注意实验室安全。 • 根据需要进行进一步分析和确认。
总结与结束语
层析法是一种重要的生物学实验技术,通过分离混合物的不同成分,为生物学研究提供了有力工具。掌握层析 法的原理和操作技巧,将可以更好地实施生物学实验和开展科学研究。
常见层析法

层析技术的应用一、层析技术的原理和分类(一)层析技术的原理层析法是目前广泛应用的一种分离技术。
本世纪初俄国植物学家M。
Tswett发现并使用这一技术证明了植物的叶子中不仅有叶绿素还含有其它色素。
现在层析法已成为生物化学、分子生物学及其它学科领域有效的分离分析工具之一。
层析法是利用不同物质理化性质的差异而建立起来的技术.所有的层析系统都由两个相组成:一是固定相,它或者是固体物质或者是固定于固体物质上的成分;另一是流动相,即可以流动的物质,如水和各种溶媒。
当待分离的混合物随溶媒(流动相)通过固定相时,由于各组份的理化性质存在差异,与两相发生相互作用(吸附、溶解、结合等)的能力不同,在两相中的分配(含量对比)不同,而且随溶媒向前移动,各组份不断地在两相中进行再分配。
与固定相相互作用力越弱的组份,随流动相移动时受到的阻滞作用小,向前移动的速度快.反之,与固定相相互作用越强的组份,向前移动速度越慢。
分部收集流出液,可得到样品中所含的各单一组份,从而达到将各组份分离的目的.(二)层析法分类见表16-5~7(三)层析法的特点与应用表16—5 按两相所处状态分类层析法是根据物质的理化性质不同而建立的分离分析方法.根据层析峰的位置及峰高或峰面积,可以定性及定量。
层析法与光学、电学或电化学仪器连用,可检测出层析后各组份的浓度或质量,同时绘出层析图。
层析仪与电子计算机联用,可使操作及数据处理自动化,大大缩短分析时间。
由于层析法具有分辨率高、灵敏度高、选择性好、速度快等特点,因此适用于杂质多、含量少的复杂样品分析,尤其适用于生物样品的分离分析。
近年来,已成为生物化学及分子生物学常用的分析方法。
在医药卫生、环境化学、高分子材料、石油化工等方面也得到了广泛的应用。
表16—6 按层析原理分类名称分离原理吸附层析法组份在吸附剂表面吸附固定相是固体吸附剂,各能力不同分配层析法各组份在流动相和静止液相(固相)中的分配系数不同离子交换层析法固定相是离子交换剂,各组份与离子交换剂亲和力不同凝胶层析法固定相是多孔凝胶,各组份的分子大小不同,因而在凝胶上受阻滞的程度不同亲和层析法固定相只能与一种待分离组份专一结合,以此和无亲和力的其它组份分离表16—7 按操作形式不同分类名称操作形式柱层析法固定相装于柱内,使样品沿着一个方向前移而达分离薄层层析法将适当粘度的固定相均匀涂铺在薄板上,点样后用流动相展开,使各组份分离纸层析法用滤纸作液体的载体,点样后用流动相展开,使各组份分离薄膜层析法将适当的高分子有机吸附剂制成薄膜,以类似纸层析方法进行物质的分离二、层析法实验技术(一)凝胶层析法凝胶层析又称分子筛过滤、排阻层析等。
常见层析法

层析技术的应用一、层析技术的原理和分类(一)层析技术的原理层析法是目前广泛应用的一种分离技术。
本世纪初俄国植物学家M.Tswett发现并使用这一技术证明了植物的叶子中不仅有叶绿素还含有其它色素。
现在层析法已成为生物化学、分子生物学及其它学科领域有效的分离分析工具之一。
层析法是利用不同物质理化性质的差异而建立起来的技术。
所有的层析系统都由两个相组成:一是固定相,它或者是固体物质或者是固定于固体物质上的成分;另一是流动相,即可以流动的物质,如水和各种溶媒.当待分离的混合物随溶媒(流动相)通过固定相时,由于各组份的理化性质存在差异,与两相发生相互作用(吸附、溶解、结合等)的能力不同,在两相中的分配(含量对比)不同,而且随溶媒向前移动,各组份不断地在两相中进行再分配.与固定相相互作用力越弱的组份,随流动相移动时受到的阻滞作用小,向前移动的速度快。
反之,与固定相相互作用越强的组份,向前移动速度越慢。
分部收集流出液,可得到样品中所含的各单一组份,从而达到将各组份分离的目的。
(二)层析法分类见表16—5~7(三)层析法的特点与应用表16-5 按两相所处状态分类层析法是根据物质的理化性质不同而建立的分离分析方法.根据层析峰的位置及峰高或峰面积,可以定性及定量。
层析法与光学、电学或电化学仪器连用,可检测出层析后各组份的浓度或质量,同时绘出层析图.层析仪与电子计算机联用,可使操作及数据处理自动化,大大缩短分析时间.由于层析法具有分辨率高、灵敏度高、选择性好、速度快等特点,因此适用于杂质多、含量少的复杂样品分析,尤其适用于生物样品的分离分析。
近年来,已成为生物化学及分子生物学常用的分析方法。
在医药卫生、环境化学、高分子材料、石油化工等方面也得到了广泛的应用。
表16-6 按层析原理分类名称分离原理吸附层析法组份在吸附剂表面吸附固定相是固体吸附剂,各能力不同分配层析法各组份在流动相和静止液相(固相)中的分配系数不同离子交换层析法固定相是离子交换剂,各组份与离子交换剂亲和力不同凝胶层析法固定相是多孔凝胶,各组份的分子大小不同,因而在凝胶上受阻滞的程度不同亲和层析法固定相只能与一种待分离组份专一结合,以此和无亲和力的其它组份分离表16—7 按操作形式不同分类名称操作形式柱层析法固定相装于柱内,使样品沿着一个方向前移而达分离薄层层析法将适当粘度的固定相均匀涂铺在薄板上,点样后用流动相展开,使各组份分离纸层析法用滤纸作液体的载体,点样后用流动相展开,使各组份分离薄膜层析法将适当的高分子有机吸附剂制成薄膜,以类似纸层析方法进行物质的分离二、层析法实验技术(一)凝胶层析法凝胶层析又称分子筛过滤、排阻层析等.它的突出优点是层析所用的凝胶属于惰性载体,不带电荷,吸附力弱,操作条件比较温和,可在相当广的温度范围下进行,不需要有机溶剂,并且对分离成分理化性质的保持有独到之处。
层析(色谱)技术课程讲义(45页)

层 析 仪 器
层 析 仪 器
紫外检测器
记录仪
泵
收集器
层析柱
第一节 概 述
有关历史和专有名词
色谱法是一种物理或物理化学的分 离分析方法.它的分离原理是:混合物 中各组分在两相间进行分配,其中一相 是不动的,称为固定相 (stationaryphase);另一相是携带混 合物流过固定相的,称为流动相 (mobilephase)。
位。
28
HPLC方法,多采用紫外检测器,若使 用荧光检测器或电化学检测器,可使灵敏 度提高2~3个数量级.对剂量较小、体内 浓度较低的药物可使用荧光或电化学检测 器,但不是所有的物质都有荧光,不能产 生荧光的药物可经衍生化作用形成带荧光 化合物,再用荧光检测器检测,电化学检 测器只能检测具有氧化还原性的药物.
薄层色谱法能合理选择固定相,这种方 法 是 在 1938 年 由 Izmailov 和 Shraiber 首 先 使 用的,50年代末Stahl首次提出薄层色谱法这 个名词。
4
1941 年 Martin 和 Synge 因 对 色 谱 法 的 贡献而获得诺贝尔奖 。1952年Martin 和 James 发 表 了 第 一 篇 气 相 色 谱 法 的 论 文 。 从1952年到60年代,气相色谱法发展很快。
8
三、按实验操作形式分类
1.柱色谱法 将固定相装于柱管内构成色谱柱,色谱过程 在柱内进行。按色谱柱的不同又可分为填充 柱、毛细管柱及微填充柱色谱。气相色谱法、 高效液相色谱法均属于柱色谱范围。
2.纸色谱法 用纸作为支持物(固定相),点样后,用流动 相展开,以达到分离检测的目的。
3.薄层色谱法 将固定相涂铺在玻璃板上,按纸色谱法操作。
层析法

層析法z國立臺灣大學化學系,大學化學實驗一暨實驗二,第二版,國立臺灣大學出版中心:台北,民國九十五年。
z版權所有,若需轉載請先徵得同意;疏漏之處,敬請指正。
z臺大化學系普化教學組葉芝嵐助教、佘瑞琳講師,2009年4月14日。
一、目的:利用管柱層析(column chromatography)及薄層層析法(thin layer chromatography,TLC)來分離及辨別混合物。
二、實驗技能:學習萃取、管柱層析及薄層層析等實驗技能。
三、原理:層析法(chromatography)是利用化合物在靜相與流動相之間的分配差異以分離混合物的方法。
層析法依據靜相(stationary phase)與流動相(mobile phase)之不同,分為管柱層析、薄層層析、氣液層析(gas liquid chromatography,GC)等。
薄層層析是吸附性色層分析的一種,將吸附劑如矽膠或礬土均勻塗佈在鋁片、膠片或玻璃板上形成薄層,作為層析靜相,再將混合物試樣點附在此薄層靜相上,以液體展開劑作為流動相,透過毛細作用由下往上移動。
由於不同的化合物與靜相之吸附力和流動相間溶解度的差異,當展開劑上升、流經所吸附的試樣點時,吸附力弱的物質移動快,吸附力強的移動慢。
由於各種物質移動的速率不同,使混合物最後在靜相薄層上分開,達到分離目的。
一個化合物在層析片上上升的高度與展開劑上升高度的比值,是化合物在該分析條件下的特性參數,稱為R f值。
利用R f值,可以判斷兩化合物是否為相同的化合物。
除了可用來判斷兩化合物是否為相同,或是不同,也可用於決定混合物中至少含有多少種成分物、作為管柱層析沖提劑選擇的參考,或用來檢視分離純化方法的離析成效,還可以追蹤化學反應的進行程度。
管柱層析是在直立的玻璃管柱中,裝填已經用沖提劑潤濕的吸附性固態填充物,例如矽膠或礬土,作為靜相,要分離的混合物由管柱頂端載入,再以液態沖提劑(eluent)作為流動相,利用化合物與靜相之間的吸附力及化合物與沖提劑間溶解度的差異,造成各成分物被沖提的速率不同,而達到區帶分離的目的。
层析法

理论塔板数
一个色谱柱的理论塔板有多少? Martin和Synge计算了硅酸柱的理论塔板并求得一 个理论塔板数的高度为0.002厘米
1厘米的层析柱=1/0.002=500个理论塔板 20厘米的层析柱上可进行10000次分配 1厘米分馏柱=20个理论塔板 20厘米的分馏柱上只能分配400次
理论塔板数的意义:比较层析柱的分离效率
第三节 蛋白质的精分离
第四节 蛋白质的纯化
色谱法 (层析法)(chromatography)
色谱法是由俄国化学家茨维特于1903年创建的。他 将含有叶绿素的石油醚提取液通过装有氯化钙的柱 子,发现叶绿素被分为不同颜色的区带,故将此法 称为色谱法(chromatography) Chromatography这个词字面意思是“color writing” 色谱法 与层析法
Martin
Synge
1941年 色谱塔板理论, 液-液分配色谱 1952年 诺贝尔化学奖
1958年 Golay
毛细管柱气相色谱
1959年 Porath, Flodin
60年代中期
凝胶过滤色谱
高压液相色谱
1981年
Jorgenson
毛细管电泳法
基本原理
色谱由两部分组成:固定 相(solid phase)和流动 相(mobile phase)。由 于样品中各组分物理化学 性质有差别,故在固定相 (solid phase)和流动相 (mobile phase)中的分 布不同,在色谱柱中的移 动速度也不同,经过一定 的时间便可获得分离
为什么?
阶段洗脱(stepwise elution)
采用间断地增加盐离子 强度的方式进行洗 脱,是一种不连续的洗 脱
优点:洗脱速度相对比 梯度洗脱快
层析法概述

第五章 层析法5.1 层析法概述5.2 柱层析5.3 平面层析 5.1 层析法概述前述各种分离方法,都属于经典分离法。
如前所述,这些方法利用被分离组分的某种差异,在许多情况下,可以收到很好的分离效果,然而它们有一个严重的局限性:被分离组分之间必须具有质的差异(例如,溶解与不溶解,吸附与不吸附……等等);如果仅是量的差异(例如,溶解度大与溶解度小,吸附性强与吸附性弱……等),这些方法常常难以收效。
而层析法则是一类与上述经典分离方法具有本质差异的分离手段,它尤其适用于彼此性质差异较小的混合组分的分离,并能获得高效分离结果。
在层析法中通常具有固定相和流动相,进行分离时,该二相处于相对运动状态;被分离的各组分,由于其结构性质的差异,导致它们对上述两相的亲和力各不相同,由此也导致它们在两相中的迁移速度产生差别;当这些组分在相对运动的两相中反复分配时,其迁移速度的差异,经反复累积,必然使其相互间的距离不断扩大,从而导致最终实现分离;如果该层析是在层析柱中进行,则可见到被分离各组分所形成的层析谱带,处于层析柱中由上到下的不同位置(下图A ),如果是在某层析平面上进行,也可见到它们处于平面中的前后不同位置(下图B ),因而达到分离目的。
图A 柱层析示意图: 图B 平面层析示意图:常规方法难以分离的成分,常可借层析法得以分离,一般能够得到单体成分;甚至同分异构体,有时也能获得很好地分离。
欲获得某种高纯度的天然药物成分,而常规方法又难以实现时,层析法不失为一种值得考虑的有效方法,尤其是在天然产物混合成分的检测分析中,该法更为有效和实用。
层析法按流动相不同,可分为气相层析和液相层析:气相层析(GC ),流动相为气体; 液相层析(LC ),流动相为液体。
液相层析分类如下页表1所示。
表1 液 相 层 析 法 分 类分离前分离后 -------------------------分离前 分离后5.2 柱层析5.2.1 吸附层析5.2.2 分配层析5.2.3 离子交换层析5.2.4 凝胶层析5.2.5 层析法的选择应用5.2.1 吸附层析5.2.1.1基本原理 3 个5.2.1.2基本操作 6 个主要步骤5.2.1.3 常用方法 4 种5.2.1.1基本原理一、吸附层析3 原理1. 利用(被分离成分间的)吸附性差异进行分离。
各类层析色谱分析技术完全讲解
层析介质与生物大分子的关系
大孔径的,亲水性好的球形材料。 多糖类凝胶层析介质最常用
Sephadex
Sepharose Bio-Gel
缺点:刚性差,不耐压,分离时间长
层析介质的性能
层析介质的形状:球形,不定形 技术指标
粒度大小:粒度小,分离效果好,但流速慢
均匀度:均匀,流速快,峰值集中 机械强度:强度高,流速快,保留值小,柱效高 理化性质:稳定,非特异性吸附少,亲水性好,耐酸碱和有机溶剂 吸附容量:单位质量或体积的层析介质吸附流动相中溶质的质量。
流动相
流动相
缓冲溶液:根据待分离物质的性质(等电点、极
无机化合物:无机盐类、无机酸类、络合物类等 有机化合物:烷烃类、有机酸和有机胺类、杂环类 生物大分子:核酸和核苷酸类、蛋白质、酶及肽类、多 活体生物:
糖及寡糖类、激素类 病毒、细菌、细胞器等
分析的参数
常见的层析分离法分析技术,是以混合物中分离 单一成分,制备一定量的产品为主,以分析鉴定 化合物的性质,获得分析参数为辅。
原理
根据物料中各组分对固定相(吸附剂) 的吸附程度不 同,以及其在相应的流动相(溶剂)中溶解度的差异 来实现。经反复的吸附—解吸—再吸附—再解吸的 过程,达到分离目的。 无化学键引入,只存在相对较弱的氢键力、范德华 力和偶极力相互作用。
吸附力的产生
吸 附
吸附:任何两相都可以形成界面,其中一相的 物质或溶解在其中的溶质在另一相表面上发生 密集行为。
薄层层析法
纸层析法
薄膜层析法
第09章疏水层析ppt课件

Water molecules
Hydrophobic ligand
Sample application
1. Equilibration
2. Sample application
3. Washing 4. Elution
Hydroptrix
Proteins
Washing out unbound material
R代表疏水配基,M代表基质。调节两种反 应物的比例可控制介质的配基密度
偶联至基质的常见配基类型
(A)丁基 (B)辛基 (C)苯基 (D)新戊基
对某些蛋白而言,上述有些配基与其结合力 太强,洗脱有时需用有机溶剂,有变性风险;具 中等疏水的高分子配基(如聚乙二醇和聚丙三醇等) 不仅可提供足够的结合力,且避免了上述缺点。
工作pH范围为3-13,清洗pH范围为2-14,工作 的最大速度是600cm/h,配基结合量为每 ml50μmol正辛烷基,疏水性中等,适合各种蛋 白的分离和纯化。
⒊ Phenyl Sepharose 6 Fast Flow
工作pH范围为3-13,清洗pH范围为2-14, 工作的最大速度是600cm/h配基结合量为每ml 40 μmol苯基Phenyl,疏水性最强,载量高, 适合含芳香族配体的生物分子的预处理,
▪ 硫酸钠是一种非常好的盐析试剂,但是在 高浓度下,蛋白稳定性的问题可能会阻碍 它的应用。
图22 不同盐对选择性的影响:按顺序增大洗脱体积洗脱: 细胞色素C、溶菌酶、核糖核酸酶A、α-糜蛋白酶原。
▪ 如果目的分子洗脱得太晚或根本不洗脱, 或者不能更换到不同的填料,尝试使用50% 的盐浓度结合。
▪ 有些蛋白在高盐浓度下开始沉淀。起始缓 冲液中的盐浓度需要降低以避免在运行中 的沉淀。重复的以小量上样也能帮助避免 由于沉淀引起的产量丢失。
层析技术讲义

层析技术讲义层析法又称色层分析法或色谱法(Chromatography),它是在1903-1906年由俄国植物学家M. Tswett首先系统提出来的。
他将叶绿素的石油醚溶液通过CaCO3管柱,并继续以石油醚淋洗,由于CaCO3对叶绿素中各种色素的吸附能力不同,色素被逐渐分离,在管柱中出现了不同颜色的谱带或称色谱图(Chromatogram)。
当时这种方法并没引起人们的足够注意,直到1931年将该方法应用到分离复杂的有机混合物,人们才发现了它的广泛用途。
随着科学技术的发展以及生产实践的需要,层析技术也得到了迅速的发展。
为此作出重要贡献的当推英国生物学家Martin和Synge。
他们首先提出了色谱塔板理论。
这是在色谱柱操作参数基础上模拟蒸馏理论,以理论塔板来表示分离效率,定量的描述、评价层析分离过程。
其次,他们根据液-液逆流萃取的原理,发明了液-液分配色谱。
特别是他们提出了远见卓识的预言:一、流动相可用气体代替液体,与液体相比,物质间的作用力减小了,这对分离更有好处;二、使用非常细的颗粒填料并在柱两端施加较大的压差,应能得到最小的理论塔板高(即增加了理论塔板数),这将会大大提高分离效率。
前者预见了气相色谱的产生,并在1952年诞生了气相色谱仪,它给挥发性的化合物的分离测定带来了划时代的变革;后者预见了高效液相色谱(HPLC)的产生,在60年代末也为人们所实现,现在HPLC已成为生物化学与分子生物学、化学等领域不可缺少的分析分离工具之一。
因此, Martin和Synge于1952年被授予诺贝尔化学奖。
如今的色层分析法经常用于分离无色的物质,已没有颜色这个特殊的含义。
但色谱法或色层分析法这个名字仍保留下来沿用。
现在我们简称为层析法或层析技术。
层析法的最大特点是分离效率高,它能分离各种性质极相类似的物质。
而且它既可以用于少量物质的分析鉴定,又可用于大量物质的分离纯化制备。
因此,作为一种重要的分析分离手段与方法,它广泛地应用于科学研究与工业生产上。
层析技术简单介绍及其应用

层析法的主要介绍及其应用1.层析法的概念层析法又称色谱法[1].色层法或层离法(Chromatography),是一种应用很广的分离分析方法。
1903年,俄国的植物学家M,C.UBeT在研究分离植物色素过程中,首先创造了色谱法,这是一种根据化合物的不同结构和不同的物理,化学特性,从而具有不同吸附性能的原理,以分离混合物中的化学成分的一种物理化学分离方法,最初用于有色物质,之后应用于大量的无色物质。
色谱法的名称虽然仍然沿用,但已失去原来的含义。
层析法和其他分离方法比较,具有分离效率高,操作又不太麻烦的优点。
因此,层析法的应用越来越广,对于近代化学科学的发展有巨大的影响。
在制药、化工、农业、医学等方面都有着广泛的应用。
2.层析法的历史及原理层析法的历史1903年3月21日俄国植物学家茨维特(Michael Tswett,1872-1919)在华沙自然科学学会生物学会议上发表了“一种新型吸附现象及其在生化分析上的应用”研究论文,介绍了一种应用吸附原理分离植物色素的新方法,并首先认识到这种层析现象在分离分析方面有重大价值。
1906年他在德国植物学杂志发表文章,首次命名上述分离后色带为色谱图,称此方法为色谱法(Chromatography)。
1907年在德国生物学会年会上,展示过带有色带的分离柱管和纯化过的植物色素溶液。
茨维特被世人公认为色谱创始人。
德籍奥地利化学家R.Kuhn 等利用他的方法在纤维状氧化铝和碳酸钙的吸附柱上将过去一个世纪以来公认为单一的结晶状胡萝卜素分离成a 和b 两个同分异构体,并由所取得的纯胡萝卜素确定出了其分子式。
Kuhn正是由于在维生素和胡萝卜素的离析与结构分析中取得了重大研究成果而获得了1938年诺贝尔化学奖.1952年,Martin和James发表第一篇气液色谱论文,首次用气体作流动相,配合微量酸碱滴定,发明了气相色谱,它给挥发性化合物的分离测定带来了划时代的革命。
2.2层析法的原理层析Chromatography(色谱),利用混合物中各组分的物理化学性质间的差异(溶解度、分子极性、分子大小、分子形状、吸附能力、分子亲合力等) ,使各组分在支持物上集中分布在不同区域,借此将各组分分离。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
二.层析展开技术
层析过程包括: ①加样 ②展开(*) ③分部收集
层析过程的关键是色谱的展开, 具体方法有以下三种:
➢ 洗脱分析法 ➢ 前流分析法 ➢ 顶替分析法
1.洗脱分析法
将混合物(样品)尽量浓缩,使体积 缩小,然后引入色谱柱上部,并用溶剂 洗脱,洗脱剂可以是原来溶解混合物的 溶剂,也可选用另外的溶剂。
第九章层析法
9.1 概述
层析用于物质的分离始于二十世纪初。
1903年,俄国植物学家向填充碳酸钙的柱 中注入植物色素的石油醚萃取物,然后用石油 醚冲洗,发现柱中出现数条相互分离的色带, 层析法的命名就是由此发现开始的。层析又称 色谱或色层。
层析分离精度高、设备简单、 操作方便。
它是获得高纯度产物最有效的 技术。
一.塔板理论
塔板理论假定 层析柱是不连续
的,是由N个相同
大小的混合接触 器串联而成。
大多数塔板理论模型所共有的假设:
① 吸附过程是热力学上可逆的; ② 在相间,溶质的质量传递阻力
可以忽略不计,也就是说溶质 的分布平衡可瞬间达到; ③ 洗脱液连续通过板;
④ 在相邻板之间没有返混;对于第j
级,溶质的质量平衡方程为: Q ccj 1Q ccjV m ctj V s q tj (9-10)
色谱法按照不同的标准可以分成不同的类型:
Hale Waihona Puke 固相的阻滞作用是由不同的机理产生的, 其中包括相的变化、相的分配、在溶液中 的分子筛效应或电场作用。
相变化是指溶质从液相传递到固相,如 吸附;相分配是指溶质从一个液相迁移到 另一个液相,溶质始终保持在液相中。
按照层析过程的机制,层析技术又可 进一步分类。
K1 Kd1
K2 Kd2
(9-8)
(5) 分离度或分辨率Rs
一个固定相在分离两种物质时,如果两 种物质的洗脱曲线重叠,则无法用分离因 子来描述,必须用分离度来解释,其定义 为:
R s0.(5 t(R W 1 1 tR W 2)2) (N 94 1/-29() 1)1 ( K K 22)
式中N为理论板数;W为峰宽。
称保留时间)与死时间τ(τ=Vm/Qe)通
过下面的方程式关联在一起:
tR(1K)
(9-7)
容量因子是吸附剂对一种溶质亲 和力的量度,对于给定的溶质,容量 因子越低,它从柱中流出得越早。
(4) 分离因子或选择性α
在给定的层析系统中,混合物各组
分的每一个参数都有一个特定的值。 这个系统分离任何两种溶质1和2的能力 可用分离因子或选择性α来表示,它是 峰与峰之间分离时间的一个量度:
时间。
Rf值与分布系数有关,可通过
下面的式子关联:
Rf
1
1Kd(Vs /Vm)
(9-3)
式中Vs和Vm分别为固定相和流动相
的总体积。
(2) 溶出体积VR
定义为溶质的最大浓度区从柱中流 出时已流出的流动相体积。
它与分配系数的关系是:
VRVmKdVs
(9-4)
一种溶质流出色谱柱所需的时间
(滞留时间)与VR的关系是:
9.2 层析分离过程理论
有效层析分离的两个条件:
1. 分离因素或选择性要足够高,即溶质的平均 迁移速度(或保留时间)应相差较大;
2. 保留时间的控制与溶质在固定相和流动 相之间分配的热力学平衡有关,通过固定相 和流动相的适当选择可以改善峰的分离。
2. 色层的末端弥散应保证减至最低程度,从而 使两个连续色带的重叠范围达到最小限度。
洗脱分析法能使 各组分分层且分离 完全,层与层间隔 着一层溶剂。
如果溶质迁移速 率不同,它们将以 分离带的形式从柱 中排出。
2.前流分析法
将混合物溶液连续通 过色谱柱,只有吸附力 最弱的组分以纯品状态 最先自柱中流出,其他 各组分都不能达到分离。 色谱图呈阶梯式,在分 析吸附平衡和确定等温 线时很有用。
3.顶替分析法
利用一种吸附力比 各被吸附组分都强的物 质来洗脱,这种物质称 为顶替剂。
此法处理量较大, 且各组分分层清楚,但 层与层相连,故不能将 组分完全分离。
三.层析分离中的有关术语
在层析过程中,所有的溶质都被同 一流动速度的移动相运送,并且可逆 地向固定相迁移,由于在固定相上面 它们所消耗的时间不同,所以其总的 迁移速率各不相同。
tR
VR vA
VR Qe
(9-5)
式中υ为洗脱剂的空塔速度;A为柱的 截面积;Qe为洗脱剂的流量。
(3) 容量因子K
容量因子K是衡量色谱柱对分离组
分保留能力的重要参数,它意味着
在固定相和移动相中溶质数量的比 例大小:
KcqVVms Kd
(1)
式中ε为床的孔隙率。
(9-6)
容量因子把溶质的滞留时间(或
层析过程中,溶质在固定相和移
动相之间存在着一个动力学分配平衡,
可用分配系数Kd来表示,其定义是溶
质在固定相中的浓度q与移动相中浓 度c之比:
Kd q/c
(9-1)
对于每个溶质,分配系数Kd值
反映了它消耗在固定相上的时间,
也反映了它在柱中的停留程度。
描述溶质的层析行为的参数:
(1) 阻滞因素Rf
式中Vs和Vm分别为该级中固定相和移
动相的体积;
⑤ 平衡等温线是线性的(Kd=常数);
色层的扩张起因于弥散和流体力学效应 以及溶质在流动相和固定相之间质量传递 的限制(实际上,层析分离过程是在一个 不平衡状况下进行的)。
可以通过控制操作参数的办法来进一步 改善分离特性,主要是洗脱剂的速率和颗 粒的直径,它们将影响色层的扩展。
层析分离的理论
塔板理论或反应器串联模型 速率理论或质量平衡模型
一.层析中的基本概念及其分类
基本概念
层析是根据混合物中,溶质在 互不混溶的两相之间分配行为的差 别,引起移动速度的不同而进行分 离的方法。
互不相溶的两相分别称为固定相和流 动相。
固定相可以是固体或者是包埋在惰性 固体中的液体,而流动相可以是气体(气 相色谱,GC)或液体(液相色谱,LC),这 取决于两相物理性质的结合,色谱过程有 气-液、气-固、液-液、液-固色谱。
定义为溶质的迁移速度和一个理想标准 物质(既不吸着也不溶解)的迁移速度之比, 实际上这个理想标准物质一般是指洗脱剂 或移动相。
当标准物质沿柱移动L长度时,
移动相所需的时间为tm,而溶质所 需的时间更长,为(tm+ ts),即 滞留时间tR,因此阻滞因素为:
Rf
tm (tm ts )
(9-2)
式中ts为溶质在固定相中消耗的
