(2020年7月整理)《中华人民共和国药典》四部 通则0921崩解时限检查法.doc
0101片剂(2020版中国药典四部)

0101 片剂片剂系指原料药物或与适宜的辅料制成的圆形或异形的片状固体制剂。
中药还有浸膏片、半浸膏片和全粉片等。
片剂以口服普通片为主,另有含片、舌下片、口腔贴片、咀嚼片、分散片、可溶片、泡腾片、阴道片、阴道泡腾片、缓释片、控释片、肠溶片与口崩片等。
含片系指含于口腔中缓慢溶化产生局部或全身作用的片剂。
含片中的原料药物一般是易溶性的,主要起局部消炎、杀菌、收敛、止痛或局部麻醉等作用。
舌下片系指置于舌下能迅速溶化,药物经舌下黏膜吸收发挥全身作用的片剂。
舌下片中的原料药物应易于直接吸收,主要适用于急症的治疗。
口腔贴片系指粘贴于口腔,经黏膜吸收后起局部或全身作用的片剂。
口腔贴片应进行溶出度或释放度(通则0931) 检查。
咀嚼片系指于口腔中咀嚼后吞服的片剂。
咀嚼片一般应选择甘露醇、山梨醇、庶糖等水溶性辅料作填充剂和黏合剂。
咀嚼片的硬度应适宜。
分散片系指在水中能迅速崩解并均匀分散的片剂。
分散片中的原料药物应是难溶性的。
分散片可加水分散后口服,也可将分散片含于口中吮服或吞服。
分散片应进行溶出度(通则0931)和分散均匀性检查。
可溶片系指临用前能溶解于水的非包衣片或薄膜包衣片剂。
可溶片应溶解于水中,溶液可呈轻微乳光。
可供口服、外用、含漱等用。
泡腾片系指含有碳酸氢钠和有机酸,遇水可产生气体而呈泡腾状的片剂。
泡腾片不得直接吞服。
泡腾片中的原料药物应是易溶性的,加水产生气泡后应能溶解。
有机酸一般用枸橼酸、酒石酸、富马酸等。
阴道片与阴道泡腾片系指置于阴道内使用的片剂。
阴道片和阴道泡腾片的形状应易置于阴道内,可借助器具将其送入阴道。
阴道片在阴道内应易溶化、溶散或融化、崩解并释放药物,主要起局部消炎杀菌作用,也可给予性激素类药物。
具有局部刺激性的药物,不得制成阴道片。
阴道片应进行融变时限检查(通则0922)。
阴道泡腾片还应进行发泡量检查。
缓释片系指在规定的释放介质中缓慢地非恒速释放药物的片剂。
缓释片应符合缓释制剂的有关要求(指导原则9013)并应进行释放度(通则0931)检查。
崩解时限检查法

目的:建立崩解时限检查法的标准操作程序,规范崩解时限检查法的操作范围:适用于崩解时限检查法职责:检验科主管、检验员规程:1 简述1.1 本法(中国药典2000年版二部附录X A)适用于片剂(包括普通片,薄膜衣片,糖衣片,肠溶衣片及泡腾片),胶囊剂(包括硬胶囊剂,软胶囊及肠溶胶囊剂),以及丸剂的溶散时限检查.凡规定检查溶出度,释放度或融变时限的制剂,不再进行崩解时限检查。
1.2 片剂口服后,需经崩散,溶解,才能为机体吸收而达到治疗目的;胶囊剂的崩解是药物溶出及被人体吸收的前提,而囊壳常因所用囊材的质量,久贮或与药物接触等原因,影响溶胀或崩解;尺剂中不含有崩解剂,故在水中不是崩解而是逐渐溶散,且基质的种类与尺剂的溶解性能有密切关系,为控制产品质量,保证质量,保证疗效,药内规定本检查项目。
1.3 本检查法中所称“崩解”,系指固体制剂于规定条件下在检查时限内全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶囊壳外,应通过筛网。
2 仪器与用具2.1 崩解仪(见中国药典2000年版二部附录X A的仪器装置)。
2.2 滴丸剂专用吊篮,按2.1项下所述仪器装置,但不锈钢丝筛网的筛孔内径改为0.425mm。
2.3 烧杯1000ml2.4 温度计,分度值1℃3试药与试液3.1人工胃液(供办胶囊剂和以明胶为基质的滴丸剂检查用),取稀盐酸16.4ml,加水约800ml与胃蛋白酶10g,摇匀后,加水稀释成1000ml,即得.临用前制备。
3.2人工肠液(从肠溶胶囊剂检查用)取磷权二氢钾6.8g,加水500ml使溶解,用0.4%氢氧化钠溶液调节pH值至6.8;另取胰酶10g,加水适量使溶解,将两液混合后,加水稀释成1000ml,即得,临用前制备。
4 操作方法4.1 将吊篮通过上端的不锈钢轴悬持于金属支架上,浸入1000ml烧杯中,并调节吊篮位置使共下降时筛网距烧杯底部25mm,烧杯内盛有温度为37±1℃的水(或规定的溶液),调节液面高度使吊篮上升时筛网在液面下15mm处.除另有规定外,取药片6片,分别置上述吊篮的玻璃管中,每管各加1片,立即启动崩解仪进行检查。
新药典4部

编号 9000
9001 9011 9013 9015 9101 9102 9103 9203 9204 9205 9206 9601 9621 9622 9901
通则名称 指导原则 原料药物与制剂稳定性试验指导原则 药物制剂人体生物利用度和生物等效性试验指导原则 缓释、控释和迟释制剂指导原则 药品晶型研究及晶型质量控制指导原则 药品质量标准分析方法验证指导原则 药品杂质分析指导原则 药物引湿性指导原则 药品微生物实验室质量管理指导原则 微生物鉴定指导原则 药品洁净实验室微生物监测和控制指导原则 无菌检查用隔离系统验证指导原则 药用辅料功能性指标研究指导原则 药包材通用要求指导原则 药用玻璃材料和容器指导原则 国家药品标准物质制备指导原则
口腔贴片应进行溶出度(通则0931)或释放度(通则9031)检查 分散片应进行溶出度(通则0931)和分散均匀性检查 缓释片应符合缓释制剂的有关要求(通则9013)并进行释放度(通则0931)
检查 肠溶片除另有规定外,应进行释放度(通则0931)检查 除冷冻干燥法制备的口崩片外,口崩片应进行崩解时限检查(通则0921)。
除另有规定外,片剂应进行以下相应检查 【重量差异】 【崩解时限】
崩解时限检查法(通则0921) 凡规定检查溶出度、释放度的片剂,一般不再进行崩解时限检查 【分散均匀性】 照崩解时限检查法(通则0921)检查,不锈钢丝网的筛孔内径为710μm,水 温为15~25℃;取供试品6片,应在3分钟内全部崩解并通过筛网。 【微生物限度】 照非无菌产品微生物限度检查:微生物计数法(通则1105)和控制菌检查法 (通则1106)及非无菌药品微生物限度标准(通则1107)检查,应符合规定。
2020版中国药典—羟丙甲纤维素空心胶囊国家药用辅料标准

羟丙甲纤维素空心胶囊本品系由羟丙甲纤维素加辅料制成的空心硬胶囊。
【性状】本品呈圆筒状,系由可套合和锁合的帽和体两节组成的质硬且有弹性的空囊。
囊体应光洁、色泽均匀、切口平整、无变形、无异臭。
本品分为透明(两节均不含遮光剂)、半透明(仅一节含遮光剂)、不透明(两节均含遮光剂)三种。
【鉴别】(1)取本品1.0g,加沸水100ml,使用25mm 长的磁力搅拌子搅拌使溶解,应有悬浊液形成。
搅拌下冷却至10℃,溶液应澄清或略有浑浊,如澄清,取溶液为供试品溶液,如浑浊,取适量,每分钟2500 转速下离心2 分钟,取上清液为供试品溶液。
(2)取鉴别(1)项下供试品溶液0.1ml,加90%的硫酸溶液9ml,振摇,水浴加热3 分钟,立即冰浴冷却,小心加入茚三酮试液0.6ml,振摇,室温放置,溶液应先呈红色,并在100 分钟内变成紫色。
(3)精密量取鉴别(1)项下供试品溶液50ml,置于烧杯中,加水50ml,磁力搅拌,加热,升温速度为2∼5℃/min,记录溶液形成浑浊时的温度,絮凝温度应高于50℃。
【检查】松紧度取本品10 粒,用拇指与食指轻捏胶囊两端,旋转拔开,不得有粘结、变形或破裂,然后装满滑石粉,将帽、体套合并锁合,逐粒于1m 的高度处直坠于厚度为2cm 的木板上,应不漏粉;如有少量漏粉,不得超过1 粒。
如超过,应另取10 粒复试,均应符合规定。
脆碎度取本品50 粒,置表面皿中,移入盛有硝酸镁饱和溶液的干燥器内,置25±1℃ 恒温24 小时,取出,立即分别逐粒放入直立在木板(厚度2cm)上的玻璃管(内径为24mm,长为200mm)内,将圆柱形砝码(材质为聚四氟乙烯,直径为22mm,重20g±0.1g)从玻璃管口处自由落下,视胶囊是否破裂,如有破裂,不得超过2 粒。
崩解时限取本品6 粒,装满滑石粉,照崩解时限检查法(通则0921)胶囊剂项下的方法,加挡板进行检查,各粒均应在15 分钟内崩解,除破碎的胶囊壳外,应全部通过筛网。
崩解时限检查法
4.3.1硬胶囊剂或软胶囊剂 ,除另有规定外,取供试品6粒,按上述装置与方法(漂浮在液面的胶囊剂可加挡板)检查。硬胶囊剂应在30分钟内、软胶囊剂应在1小内全部崩解并通过筛网(囊壳碎片除外)。软胶囊剂可改在人工胃液中进行检查。如有1粒不能完全崩解,应另取6粒按上述方法复试,均应符合规定。
4.3.2肠溶胶囊剂,除另有规定外,取供试品6粒,按上述装置与方法(漂浮在液面的胶囊剂 可加挡板)检查。先在盐酸溶液(9→1000)中检查2小时,每粒的囊壳均不得有裂缝或崩解现象;继将吊篮取出,用少量水洗涤后,每管各加挡板一块,再按上述方法在磷酸盐缓冲液(PH6.8)中进行检查,1小内应全部崩解并通过筛网(囊壳碎片除外)。如有1粒不能完全崩解,应另取6粒复试,均应符合规定。
文件名:崩解时限检查法
制定人:
制定日期:
分发份数:3
审核人:
审核日期:
颁发部门:GMP办
批准人:
批准日期:
生效日期:
分发至:质量保证部、质监科、质量检验中心
1.目的:规范崩解时限的检查方法,以保证检验结果的准确性。
2.范围:崩解时限的检查。
3.责任:质量保证部、质监科、质量检验中心、检验操作人员。
4.内容:
4.2.2检查法 将吊篮通过上端不锈钢轴悬挂于金属支架上,浸入1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37℃±1℃的水,调节水位高度使吊篮上升时筛网在水面下15mm处。
4.2.2.1除另有规定外,取供试品6片,分别置上述吊篮的玻璃管中,启动崩解仪进行检查,药材原粉片各片均应在30分钟内全部崩解;浸膏(半浸膏)片、糖衣片各片均应在1小时内全部崩解。如有1片不能完全崩解,应另取6片复试,均应符合规定。
崩解时限检查法(通则0921)培训试题及答案

依据:中国药典分析检测技术指南(2017年7月)崩解时限检查法(通则0921)培训试题及答案2018.09姓名:成绩:一、单选题(每题4分,共24分)A、取稀盐酸16.4ml,加水约800ml与胃蛋白酶10g,摇匀后,加水稀释成1000ml,即得。
B、取稀盐酸10ml,加水约800ml与胃蛋白酶16.4g,摇匀后,加水稀释成1000ml,即得。
C、取胃蛋白酶10g,加水约800ml,摇匀后,加水稀释成1000ml,即得。
D、取稀盐酸16.4ml,加水约800ml,摇匀后,加水稀释成1000ml,即得。
2、人工肠液是:。
(B)A、稀盐酸B、磷酸盐缓冲液(含胰酶)C、胃蛋白酶水溶液D、磷酸盐缓冲液(不含胰酶)3、介质用量:调节液面高度使吊篮上升时筛网在液面下mm处。
(C)A、5B、10C、15D、20A、30℃±5℃B、30℃±2℃C、20℃±2℃D、20℃±5℃5、在测试过程中,烧杯内的水温应保持在:。
(C)A、20℃±5℃B、30℃±5℃C、37℃±1℃D、37℃±5℃6、在结果判定时,除另有规定外,如有1片(粒)不能完全崩解,应另取片(粒)复式,均应符合规定。
(D)A、3B、4C、5D、6二、多选题(每题4分,共16分)1、崩解时限记录包括:。
(ABCD)A、仪器型号、制剂类型B、测试条件C、介质配制D、崩解或溶散时间2、2015版药典规定了胶囊剂包括:。
(ABC)A、硬胶囊剂B、软胶囊剂C、肠溶胶囊剂D、滴丸剂3、2015版药典规定了片剂包括:。
(ABCD)A、口服普通片、薄膜衣片、糖衣片B、肠溶衣片、肠溶片C、含片、舌下片、可溶片D、泡腾片、口崩片4、在崩解时限检查方法与仪器发展的历史中,出现的检查方法和仪器包括:。
(ABCD)A、手工法B、吊篮式崩解仪C、介质流动的崩解仪D、溶解性总固体崩解仪三、判断题(每题4分,共20 分)1、崩解时限检查法是一项重要的常规检测方法,是注射剂质量监控的重要手段。
0103胶囊剂(2020版中国药典四部)

0103 胶囊剂胶囊剂系指原料药物或与适宜辅料充填于空心胶囊或密封于软质囊材中制成的固体制剂。
胶囊剂可分为硬胶囊和软胶囊。
根据释放特性不同还有缓释胶囊、控释胶囊、肠溶胶囊等。
硬胶囊(通称为胶囊)系指采用适宜的制剂技术,将原料药物或加适宜辅料制成的均匀粉末、颗粒、小片、小丸、半固体或液体等,充填于空心胶囊中的胶囊剂。
软胶囊系指将一定量的液体原料药物直接密封,或将固体原料药物溶解或分散在适宜的辅料中制备成溶液、混悬液、乳状液或半固体,密封于软质囊材中的胶囊剂。
可用滴制法或压制法制备。
软质囊材一般是由胶囊用明胶、甘油或其他适宜的药用辅料单独或混合制成。
缓释胶囊系指在规定的释放介质中缓慢地非恒速释放药物的胶囊剂。
缓释胶囊应符合缓释制剂(指导原则9013)的有关要求,并应进行释放度(通则0931)检查。
控释胶囊系指在规定的释放介质中缓慢地恒速释放药物的胶囊剂。
控释胶褒应符合控释制剂(指导原则9013)的有关要求,并应进行释放度(通则0931)检查。
肠溶胶囊系指用肠溶材料包衣的颗粒或小丸充填于胶囊而制成的硬胶囊,或用适宜的肠溶材料制备而得的硬胶囊或软胶囊。
肠溶胶囊不溶于胃液,但能在肠液中崩解而释放活性成分。
除另有规定外,肠溶胶囊应符合迟释制剂(指导原则9013)的有关要求,并进行释放度(通则0931)检查。
胶囊剂在生产与贮藏期间应符合下列有关规定。
一、胶囊剂的内容物不论是原料药物还是辅料,均不应造成囊壳的变质。
二、小剂量原料药物应用适宜的稀释剂稀释,并混合均匀。
三、硬胶囊可根据下列制剂技术制备不同形式内容物充填于空心胶囊中。
(1)将原料药物加适宜的辅料如稀释剂、助流剂、崩解剂等制成均匀的粉末、颗粒或小片。
(2)将普通小丸、速释小丸、缓释小丸、控释小丸或肠溶小丸单独填充或混合填充,必要时加入适量空白小丸作填充剂。
(3)将原料药物粉末直接填充。
(4)将原料药物制成包合物、固体分散体、微囊或微球。
(5)溶液、混悬液、乳状液等也可采用特制灌囊机填充于空心胶囊中,必要时密封。
查阅并记录片剂崩解时限检查方法及标准

查阅并记录片剂崩解时限检查方法及标准查阅并记录片剂崩解时限检查方法及标准1. 引言片剂崩解时限检查是药品质量控制中不可或缺的一环。
正确而准确地评估片剂崩解时限可以为药品生产企业提供重要的质量保证。
在本文中,我们将深入探讨片剂崩解时限检查的方法和标准,以帮助读者更好地理解这一重要的质量控制指标。
2. 片剂崩解时限的定义和意义片剂崩解时限是指在一定的试验条件下,药物通过崩解释放活性成分所需的时间。
正确评估片剂崩解时限可以验证药物是否按照设计要求释放活性成分。
片剂崩解时限还可以衡量药物的生物利用度和治疗效果。
3. 片剂崩解时限检查方法(1)理论基础片剂崩解时限检查方法主要基于药典规定,其中包括中国药典、美国药典等。
这些药典为片剂崩解时限提供了详细的试验条件和评估指标。
(2)试验条件片剂崩解时限检查通常需要在模拟生理条件下进行。
常见的试验条件包括温度、溶液pH值、搅拌速度等。
这些条件的选择应基于药物的特性和适应对象。
(3)试验设备常用的片剂崩解时限检查设备包括崩解度仪、电子天平、恒温槽等。
这些设备可以提供稳定和准确的试验条件。
(4)试验步骤片剂崩解时限检查的试验步骤包括样品准备、试验条件设定、试验操作、数据记录等。
通过严格按照试验步骤进行操作,可以准确评估片剂崩解时限。
4. 片剂崩解时限的评估标准(1)国家标准不同国家和地区对于片剂崩解时限的评估标准可能存在差异。
中国药典对于常见药物的崩解时限给出了具体的评估标准,生产企业应根据国家标准进行评估。
(2)药企自主标准一些大型药企可能根据自身需求和技术水平制定了更为严格的片剂崩解时限评估标准。
这些标准可以更好地满足企业的质量控制需求。
5. 个人观点和理解片剂崩解时限是药品质量控制过程中非常重要的一项指标。
通过准确评估片剂崩解时限,可以保证药物的质量和疗效。
片剂崩解时限还可以为药企提供重要的质量控制数据和生产指导。
在实际操作中,我认为需灵活运用片剂崩解时限检查方法和标准。
中药制剂的常规检查技术—崩解时限检查法

➢ 适用剂型 丸剂(除大蜜丸)、片剂、滴丸剂(溶散)、胶囊剂等。
➢ 检查意义 在一定程度上可以间接反映药品的生物利用度。
➢ 检查原理 崩解仪、人工模拟胃肠道蠕动、规定溶剂、规定时限内能否崩解或溶散,并全 部通过筛网。
【注】检查溶出度、释放度、融变时限(栓剂、阴道片等)或分散均匀性的制剂 ,不再进行崩解时限检查。
01
目录
01
水分测定法
02
崩解时限检查法
03
相对密度测定法
04 重(装)量差异检查法
05
其他常规检查法
崩解时限检查法
一、概述
➢ 1、崩解(溶散)的定义 系指口服固体制剂于规定条件和时间内崩解(溶散)成碎粒,并全部通过筛网
(不溶性包衣材料或破碎的胶囊壳除外)。
➢ 2、 崩解(溶散)时限 《中国药典》(四部)特性检查法规定的允许崩解或溶散的最长允许时间。
(三)崩解篮法
1. 仪器与试剂 升降式支架、崩解篮、1000ml烧杯、温度计(分度值1℃)、水等。
2. 操作方法 将不锈钢管固定于支架上,浸入1000ml烧杯中,杯内盛有温度为
37℃±1℃的水约900ml,调节水位高度使不锈钢管最低位时筛网在水 面下15mm±1mm。启动仪器。取本品1片,置上述不锈钢管中进行检 查,应在60秒种内全部崩解并通过筛,可作符合规定论。重复测定6片, 均应符合规定。如有1片不符合规定,应别取6片复试,均应符合规定。
➢ 检查原理 崩解仪、人工模拟胃肠道蠕动、规定溶剂、规定时限内能否崩解或溶散,并全 部通过筛网。
【注】检查溶出度、释放度、融变时限(栓剂、阴道片等)或分散均匀性的制剂 ,不再进行崩解时限检查。
➢ 测定方法 吊篮法:大多数药品的崩解时限检查采用此法。 烧杯法:该法检查崩解时限仅适用于泡腾片。 崩解篮法:该法检查崩解时限仅适用于口崩片。
中国药典崩解时限检查法

中国药典崩解时限检查法中国药典2010年版--崩解时限检查法硬胶囊剂或软胶囊剂的崩解时限按上述装置与⽅法检查,如胶囊漂浮于液⾯,可加挡板1块。
硬胶囊剂应在30分钟内全部崩解,软胶囊剂应在1⼩时内全部崩解。
如有1粒不能完全崩解,应另取6粒,搜集整理按上述⽅法复试,均应符合规定。
软胶囊剂可改在⼈⼯胃液中进⾏检查。
肠溶胶囊剂按上述装置与⽅法,先在盐酸溶液(9→1000)中检查2⼩时,每粒的囊壳均不得有裂缝或崩解现象;继将吊篮取出,⽤少量⽔洗涤后,每管各加⼊挡板1块,再按上述⽅法,改在⼈⼯肠液中进⾏检查,1⼩时内应全部崩解。
如有1粒不能完全崩解,应另取6粒,按上述⽅法复试,均应符合规定。
庄⼦云:“⼈⽣天地之间,若⽩驹过隙,忽然⽽已。
”是呀,春秋置换,⽇⽉交替,这从指尖悄然划过的时光,没有⼀点声响,没有⼀刻停留,仿佛眨眼的功夫,半⽣已过。
⼈活在世上,就像暂时寄宿于尘世,当⽣命的列车驶到终点,情愿也罢,不情愿也罢,微笑也罢,苦笑也罢,都不得不向⽣命挥⼿作别。
我们⽆法挽住时光的脚步,⽆法改变⼈⽣的宿命。
但我们可以拿起⽣活的画笔,把⾃⼰的⼈⽣涂抹成⾊彩靓丽的颜⾊。
⽣命如此短暂,岂容随意挥霍!只有在该⾟勤耕耘的时候播洒汗⽔,⼀程风⾬后,⼈⽣的筐篓⾥才能装满硕果。
就算是烟花划过天空,也要留下短暂的绚烂。
只有让这仅有⼀次的⽣命丰盈充实,才不枉来尘世⾛⼀遭。
雁过留声,⼈过留名,这⼀趟⼈⽣旅程,总该留下点⼉什么!⽣活是柴⽶油盐的平淡,也是⾏⾊匆匆的奔波。
⼀粥⼀饭来之不易,⼀丝⼀缕物⼒维艰。
前⾏的路上,有风也有⾬。
有时候,风⾬扑⾯⽽来,打在脸上,很疼,可是,我们不能向⽣活低头认输,咬⽛抹去脸上的⾬⽔,还有泪⽔,甩开脚步,接着向前。
我们需要呈现最好的⾃⼰给世界,需要许诺最好的⽣活给家⼈。
所以,⽣活再累,不能后退。
即使⽣活赐予我们⼀杯不加糖的苦咖啡,皱⼀皱眉头,也要饮下。
⼈⽣是⼀场跋涉,也是⼀场选择。
我们能抵达哪⾥,能看到什么样的风景,能成为什么样的⼈,都在于我们的选择。
新药典4部

内容和药用辅料品种正文。
详情如下:
编号 0100
0101 0102 0103 0200 0251 0261 0291 0301 0400 0401 0402 0406
通则名称 制剂通则
片剂 注射剂 胶囊剂 其他通则 药用辅料 制药用水 国家药品标准物质通则 一般鉴别试验 光谱法 紫外-可见光光度法 红外分光光度法 原子吸收分光光度法
除另有规定外,取供试品10个,照各品种项下规定的方法,分别测定每一个 单剂以标示量为100的相对含量,求其均值X和标准差S以及标示量与均值之 差的绝对值A(A=|100-X|)
若A+2.2S≤L,则供试品的含量均匀度符合规定; 若A+S>L,则不符合规定; 若A+2.2S>L,且A+S≤L,则应另取供试品20个复试。复试判定较2010版药典规
对于难溶性药物制成的口崩片,还应进行溶出度检查(通则0931),对于经 肠溶材料包衣的颗粒制成的口崩片,还应进行释放度检查(通则0931) 除另有规定外,非包衣片应符合片剂脆碎度检查法(通则0932) 根据原料药物和制剂的特性,除来源于动、植物多组分且难以建立测定方法 的片剂外,溶出度、释放度、含量均匀度等应符合要求。
ⅥG黏度测定法
ⅦA电位滴定法与永停滴定法 ⅦB非水溶液滴定法
0800 0900
编号
0801 0821 0831 0832 0861
0901 0902 0903 0904 0921 0923 0931 0941 0942 0982
通则名称 限量检查法 氯化物检查法 重金属检查法 干燥失重测定法 水分测定法 残留溶剂测定法 特性检查法 溶液颜色检查法 澄清度检查法 不溶性微粒检查法 可见异物检查法 崩解时限检查法 片剂脆碎度检查法 溶出度与释放度测定法 含量均匀度检查法 最低装量检查法 粒度和粒度分布测定法
崩解时限检查法的操作流程

崩解时限检查法的操作流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!崩解时限检查法的操作流程一、准备工作阶段。
在进行崩解时限检查之前,需要做好充分的准备工作。
崩解时限检查法标准操作规程(2020版药典)

崩解时限检查法标准操作规程目的:建立崩解时限检查法标准操作规程。
范围:适用于崩解时限检查法标准操作规程职责:QC检验员对本标准的实施负责执行标准:《中国药典》2020年版四部第129页通则0921规程:1简述1.1本法(中国药典2020年版四部通则0921)适用于片剂(包括普通片、薄膜衣片、糖衣片、)、胶囊剂(包括硬胶囊剂、软胶囊剂)。
1.2 片剂口服后,需经崩散、溶解,才能为机体吸收而过到治疗目的;胶囊剂的崩解是药物溶出及被人体吸收的前提,而囊壳常因所用囊材的质量,久贮或与药物接触等原因,影响溶解或崩解,为控制产品质量,保证疗效,规定本检查项目。
1.3本检查法中所称“崩解”,系指固体制剂于规定条件下在检查期限内全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶囊壳外,都应通过筛网。
2仪器与用具2.1六管崩解仪2.2烧杯2.3温度计分度值1℃3试药与试液3.1人工胃液取稀盐酸16.4ml,加水约800ml与胃蛋白酶10g,摇匀后,加水稀释成1000ml,即得。
临用前制备。
4操作方法4.1将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸入1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37±1℃的水(或规定的溶液),调节液面高度使吊篮上升时筛网在液面下15mm处。
除另有规定外,取药片6片,分别置上述吊篮的玻璃管中,每管各加1片,立即启动崩解仪进行检查。
4.2片剂4.2.1普通片按 4.1项下方法检查,全粉片各片均应在30分钟内全部崩解;浸膏(半浸膏)片、糖衣片各片均应在1小时内全部崩解。
如有一片不能完全崩解,应另取6片复试,均应符合规定。
4.2.2薄膜衣片按4.1项下方法,并可改在盐酸溶液(9-1000)中进行检查,各片均应在1小时内崩解。
4.3胶囊剂除另有规定外,取供试品6粒,分别置吊篮的玻璃管中,每管各加1粒,按4.1项下方法检查(若供试品漂浮在液面,应加档板),硬胶囊应在30分钟内全部崩解。
崩解时限-整理

崩解时限检查法一简述1.本法系用于检查口服固体系剂在规定条件下的崩解状况。
2.除还有规定外,凡规定检查溶出度、开释度、融变时限或分别平均性的制剂,不再进行崩解时限检查。
3.崩解系指口服固体系剂在规定条件下所有崩解溶散或成碎粒,除不溶性包衣资料或破裂的胶襄壳外,应所有经过筛网。
若有少许不可以经过筛网,但已软化或轻质上漂且无硬心者,可作切合规定论。
4.溶液配制磷酸盐缓冲液( pH 6.8)取 0.2mol/L 磷酸二氢钾溶液 250ml,加 0.2mol/L 的氢氧化钠溶液 118ml,用水稀释至 1000ml,摇匀,即得。
人工胃液:取稀盐酸 16.4ml,加水约 800ml 与胃蛋白酶 10g,摇匀后,加水稀释成 1000ml,即得。
人工肠液,即磷酸盐缓冲液(含胰酶)(pH 6.8)取磷酸二氢钾 6.8g,加水 500ml 使溶解,用 0.1mol/L 的氢氧化钠溶液调理pH 值至 6.8;另取胰酶 10g,加水适当使溶解,将两液混淆后,加水稀释至1000ml,即得。
二装置主要采纳起落式崩解仪,主要构造为一能起落的金属支架与下端镶有筛网的吊篮,并附有挡板。
起落的金属支架上下挪动距离为55±2mm,来回频次为每分钟30? 32 次三检查方法1.将吊篮经过上端的不锈钢轴悬挂于支架上,浸入1000ml烧杯中,并调理吊篮地点使其降落至低点时筛网距烧杯底部25mm,烧杯内盛有温度为37 ±1°C 的水,调理水位高度使吊篮上涨至高点时筛网在水面下15mm 处,吊篮顶部不行淹没于溶液中。
2.除还有规定外,取供试品6 片(粒),分别置上述吊篮的玻璃管中,启动崩解仪进行检查。
各片(粒)均应切合规定。
若有 1 片(粒)不切合规定,应另取 6 片(粒)复试,均应切合规定。
四不一样制剂种类的崩解实验要求剂型溶液挡板崩解时间特别状况一般各片均应在若有 1 片不可以完整崩水 37 ±1°C×15min 内所有解,应另取 6 片复试,片剂崩解均应切合规定中药各片均应在浸膏水 37 ±1°C√1h 内所有崩假如供试品黏附挡板,片解应另取 6 片,不加挡板中半浸各片均应在按上述方法检查,应符药水 37 ±1°C√1h 内所有崩合规定膏片片解若有 1 片不可以完整崩全粉各片均应在解,应另取 6 片复试,水 37 ±1°C√30min 内所有均应切合规定片崩解化药水 37 ±1°C各片均应在假如供试品黏附挡板,薄膜→1000盐×30min 内所有应另取 6 片,不加挡板9薄片酸溶液崩解按上述方法检查,应符膜中药水 37 ±1°C各片均应在合规定片若有 1 片不可以完整崩薄膜9→ 1000 盐√1h 内所有崩解,应另取 6 片复试,片酸溶液解均应切合规定化药水 37 ±1°C各片均应在假如供试品黏附挡板,糖衣9→ 1000 盐×1h 内所有崩应另取 6 片,不加挡板糖片酸溶液解按上述方法检查,应符衣中药水 37 ±1°C各片均应在合规定片若有 1 片不可以完整崩糖衣9→ 1000 盐√1h 内所有崩解,应另取 6 片复试,片酸溶液解均应切合规定硬胶中药胶各粒均应在以明胶为基质的软胶水 37 ±1°C囊加30min 内所有囊可改在人工胃液中囊胶化药胶崩解进行检查囊软胶囊若漂各粒均应在若有 1 粒不可以完整崩水 37 ±1°C浮于液1h 内所有崩解,应另取 6 粒复试,囊面可加解均应切合规定各片均不该若有 1 片不切合规定,在 10min 内含片水± °×应另取 6 片复试,均应37 1C所有崩解或切合规定熔解舌下各片均应在若有 1 片不可以完整崩水 37 ±1°C×5min 内所有解或熔解,应另取6片崩解并熔解片复试,均应切合规定可溶水 20±5 °C×各片均应在若有 1 片不可以完整崩片3min 内所有解或熔解,应另取6崩解并熔解片复试,均应切合规定肠溶片不加档板1在盐酸溶液(9→1000)中检查 2h 每片均不得有裂痕、崩解、融化拿出吊篮,用少许水清洗加入挡板2放入磷酸盐缓冲液( pH6.8)中检查1h 内应所有崩解。
《中国药典》2020年版四部通则历次增修订目录(共计25批))

0102 注射剂.pdf 0104颗粒剂.pdf 0106 鼻用制剂.pdf
0108 丸剂.pdf 0121贴剂.pdf 0122贴膏剂.pdf 1101无菌检查法-第三次征求意见稿.pdf 9206无菌检查用隔离系统验证指导原则-第三次征求意见稿.pdf 灭菌用生物指示剂指导原则-第三次征求意见稿.pdf 生物指示剂耐受性检查法指导原则-第三次征求意见稿.pdf 1105微生物计数法-第二次征求意见稿.pdf 1121 抑菌效力检查法-第二次征求意见稿.pdf 1143 细菌内毒素检查法-第二次征求意见稿.pdf 1213 硫酸鱼精蛋白效价测定法-第二次征求意见稿.pdf 9203药品微生物实验室质量管理指导原则-第二次征求意见稿.pdf 0109-软膏剂、乳膏剂.pdf 0183-煎膏剂(膏滋).pdf 0184胶剂.pdf 9001 原料药物与制剂稳定性试验指导原则.pdf 9014 微粒制剂指导原则.pdf 0105 眼用制剂.pdf 0107 栓剂.pdf 0111 吸入制剂.pdf 0112 喷雾剂.pdf 0113 气雾剂.pdf 0119 涂膜剂.pdf 0181 合剂.pdf 0182 锭剂.pdf 0185 酒剂.pdf 0187 露剂.pdf 0188 茶剂.pdf 1431 生物检定统计法.pdf DNA测序技术指导原则.pdf 标准核酸序列建立指导原则.pdf 9013 缓释、控释和迟释制剂指导原则-第二次公示稿.pdf 1101- 无菌检查法(第二次征求意见稿).pdf
0123 口服溶液剂 口服混悬剂 口服乳剂.pdf 0124 植入剂.pdf 0125 膜剂.pdf 0126 耳用制剂.pdf 0127 洗剂.pdf 0128 冲洗剂.pdf 0129 灌肠剂.pdf
0512 高效液相色谱法 0601 相对密度测定法振荡型密度计法(第二次征求意见稿)
《中华人民共和国药典》四部 通则0921崩解时限检查法.doc

0921 崩解时限检查法本法系用于检查口服固体制剂在规定条件下的崩解情况。
崩解系指口服固体制剂在规定条件下全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶襄壳外,应全部通过筛网。
如有少量不能通过筛网,但已软化或轻质上漂且无硬心者,可作符合规定论。
除另有规定外,凡规定检查溶出度、释放度、融变时限或分散均匀性的制剂,不再进行崩解时限检查。
一、片剂仪器装置采用升降式崩解仪,主要结构为一能升降的金属支架与下端镶有筛网的吊篮,并附有挡板。
升降的金属支架上下移动距离为55mm±2mm,往返频率为每分钟30〜32次。
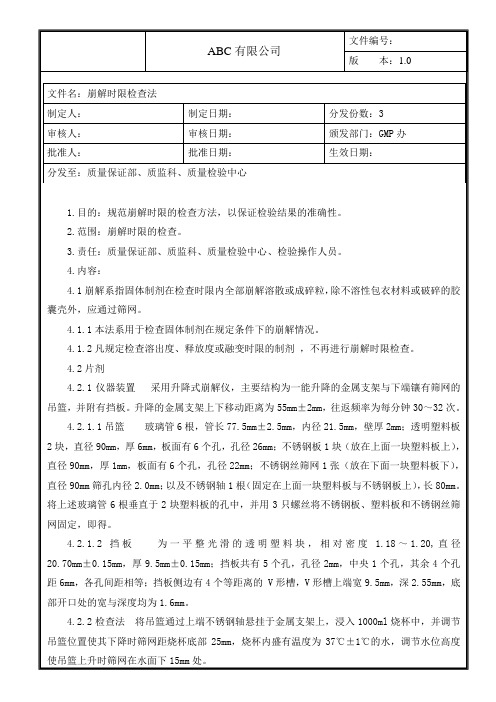
(1) 吊篮玻璃管6根,管长77.5mm± 2.5mm,内径21.5mm,壁厚2mm;透明塑料板2块,直径90mm,厚6mm,板面有6个孔,孔径26mm;不锈钢板1块(放在上面一块塑料板上),直径90mm ,厚lmm,板面有6个孔,孔径22mm;不锈钢丝筛网1张(放在下面一块塑料板下),直径90mm,筛孔内径2.0mm;以及不锈钢轴1根(固定在上面一块塑料板与不锈钢板上),长80mm。
将上述玻璃管6根垂直置于2块塑料板的孔中,并用3只螺丝将不锈钢板、塑料板和不锈钢丝筛网固定,即得(图1)。
(2) 挡板为一平整光滑的透明塑料块,相对密度1.18〜1.20,直径20.7mm±0.15mm,厚9.5mm±0.15mm;挡板共有5个孔,孔径2mm,中央1个孔,其余4个孔距中心6rmn,各孔间距相等;挡板侧边有4个等距离的V形槽,V形槽上端宽9.5mm,深2.55mm,底部开口处的宽与深度均为1.6mm(图2)。
检査法将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸人1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37°C ±1".的水,调节水位高度使吊篮上升时筛网在水面下15mm处,调节吊篮顶部不可浸没于溶液中。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
0921 崩解时限检查法
本法系用于检查口服固体制剂在规定条件下的崩解情况。
崩解系指口服固体制剂在规定条件下全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶襄壳外,应全部通过筛网。
如有少量不能通过筛网,但已软化或轻质上漂且无硬心者,可作符合规定论。
除另有规定外,凡规定检查溶出度、释放度、融变时限或分散均匀性的制剂,不再进行崩解时限检查。
一、片剂
仪器装置采用升降式崩解仪,主要结构为一能升降的金属支架与下端镶有筛网的吊篮,并附有挡板。
升降的金属支架上下移动距离为55mm±2mm,往返频率为每分钟30〜32次。
(1) 吊篮玻璃管6根,管长77.5mm± 2.5mm,内径21.5mm,壁厚2mm;透明塑料板2块,直径90mm,厚6mm,板面有6个孔,孔径26mm;不锈钢板1块(放在上面一块塑料板上),直径90mm ,厚lmm,板面有6个孔,孔径22mm;不锈钢丝筛网1张(放在下面一块塑料板下),直径90mm,筛孔内径2.0mm;以及不锈钢轴1根(固定在上面一块塑料板与不锈钢板上),长80mm。
将上述玻璃管6根垂直置于2块塑料板的孔中,并用3只螺丝将不锈钢板、塑料板和不锈钢丝筛网固定,即得(图1)。
(2) 挡板为一平整光滑的透明塑料块,相对密度1.18〜1.20,直径20.7mm±0.15mm,厚9.5mm±0.15mm;挡板共有5个孔,孔径2mm,中央1个孔,其余4个孔距中心6rmn,各孔间距相等;挡板侧边有4个等距离的V形槽,V形槽上端宽9.5mm,深2.55mm,底部开口处的宽与深度均为1.6mm(图2)。
检査法将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸人1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37°C ±1".的水,调节水位高度使吊篮上升时筛网在水面下15mm处,调节吊篮顶部不可浸没于溶液中。
除另有规定外,取供试品6片,分别置上述吊篮的玻璃管中,启动崩解仪进行检查,各片均应在15分钟内全部崩解。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
中药浸膏片、半浸膏片和全粉片,按上述装置吊篮的玻璃管中,启动崩解仪进行检查,全粉片各片均应在30分钟内全部崩解;浸膏(半浸膏)片各片均应在1个小时内全部崩解。
如有供试品黏附挡板,应另取6片,不加挡板按上述方法检查,应符合规定。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
薄膜衣片,按上述装置与方法检査,并可改在盐酸溶液(9—1000)中进行检查,化药薄膜衣片应在30分钟内全部崩解。
中药薄膜衣片,则每管加挡板1块,各片均应在1个小时内全部崩解,如有供试品黏附挡板,应另取6片,不加挡板按上述方法检查,应符合规定。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
糖衣片,按上述装置与方法检查,化药糖衣片应在1个小时内全部崩解。
中药糖衣片则每管加挡板1块,各片均应在1个小时内全部崩解,如有供试品黏附挡板,应另取6片,不加挡板按上述方法检查,应符合规定。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
肠溶片,按上述装置与方法,先在盐酸溶液(9— 1000)中检査2小时,每片均不得有裂缝、崩解或软化现象;然后将吊篮取出,用少量水洗涤后,每管加人挡板1块,再按上述方法在磷酸盐缓冲液(PH6.8)中进行检查,1小时内应全部崩解。
如有1片不能
完全崩解,应另取6片复试,均应符合规定。
结肠定位肠溶片,除另有规定外,按上述装置照各品种项下规定检查,各片在盐酸溶液(9→1000)及pH6.8以下的磷酸盐缓冲溶液中均应不得有裂缝、崩解或软化现象;在PH7.5~8.0的磷酸盐缓冲液中1小时内应完全崩解。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
含片,除另有规定外,按上述装置和方法检査,各片均不应在10分钟内全部崩解或溶化。
如有1片不符合规定,应另取6片复试,均应符合规定。
舌下片,除另有规定外,按上述装置和方法检査,各片均应在5分钟内全部崩解并溶化。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
可溶片,除另有规定外,水温为20℃±5℃,按上述装置和方法检査,各片均应在3分钟内全部崩解并溶化。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
泡腾片,取1片,置250ml烧杯中(内有200ml温度为20℃±5℃的水)中,即有许多气泡放出,当片剂或碎片周围的气体停止逸出时,片剂应溶解或分散在水中,无聚集的颗粒剩留。
除另有规定外,同法检查6片,各片均应在5分钟内崩解。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
口崩片,除另有规定外,照下述方法检查。
仪器装置主要结构为一能升降的支架与下端镶有筛网的不锈钢管。
升降的支架上下移动距离为10mm±1mm,往返频率为每分钟30次。
崩解篮不锈钢管,管长3 0m m ,内径13. 0mm,不锈钢筛网(镶在不锈钢管底部)筛孔内径710微米(图3) 。
检查法将不锈钢管固定于支架上,浸入1000ml杯中,杯内盛有温度为3 7 *C ± 1*C 的水约900ml,调节水位髙度使不锈钢管最低位时筛网在水面下15mm士1m m。
启动仪器。
取本品1 片,置上述不锈钢管中进行检査,应在6 0秒钟内全部崩解并通过筛网,如有少量轻质上漂或黏附于不锈钢管内壁或筛网,但无硬心者,可作符合规定论。
重复测定6片,均应符合规定。
如有1 片不符合规定,应另取6 片复试,均应符合规定。
二、胶囊剂
硬胶囊剂或软胶囊剂,除另有规定外,取供试品6粒,按片剂的装置与方法(如胶囊漂浮于液面,可加挡板)检査。
硬胶囊应在30分钟内全部崩解,软胶囊应在1小时内全部崩解。
软胶囊可改在人工胃液中进行检査。
如有1粒不能完全崩解,应另取6粒复试,均应符合规定。
肠溶胶囊剂,除另有规定外,取供试品6粒,按上述装置与方法,先在盐酸溶液
(9—1000)中不加挡板检査2小时,每粒的囊壳均不得有裂缝或崩解现象;继将吊篮取出,用少量水洗涤后,每管加人挡板,再按上述方法,改在人工肠液中进行检查,1小时内应全部崩解。
如有1粒不能完全崩解,应另取6粒复试,均应符合规定。
结肠肠溶胶囊剂,除另有规定外,取供试品6粒,按上述装置与方法,先在盐酸溶液(9—1000)中不加挡板检査2小时,每粒的囊壳均不得有裂缝或崩解现象;将吊篮取出,用少量水洗涤后,再按上述方法,在磷酸盐缓冲液(pH6. 8)中不加挡板检查3小时,每粒的囊壳均不得有裂缝或崩解现象;续将吊篮取出,用少量水洗涤后,每管加人挡板,再按上述方法,改在磷酸盐缓冲液(PH7. 8)中检查,1小时内应全部崩解。
如有1粒不能完全崩解,应另取6粒复试,均应符合规定。
三、滴丸剂
按片剂的装置,但不锈钢丝网的筛孔内径应为0.425mm;除另有规定外,取供试品6粒,按上述方法检查,应在30分钟内全部溶散,包衣滴丸应在1小时内全部溶散。
如有1粒不能完全溶散,应另取6粒复试,均应符合规定。
以明胶为基质的滴丸,可改在人工胃液中进行检査。
【附注】
人工胃液取稀盐酸16. 4ml ,加水约800ml与胃蛋白酶10g ,摇匀后,加水稀释成1000ml,即得。
人工肠液即磷酸盐缓冲液(含胰酶)(pH 6.8)(通则8004)。
