中华人民共和国药典2010年版
2010版中国药典知识
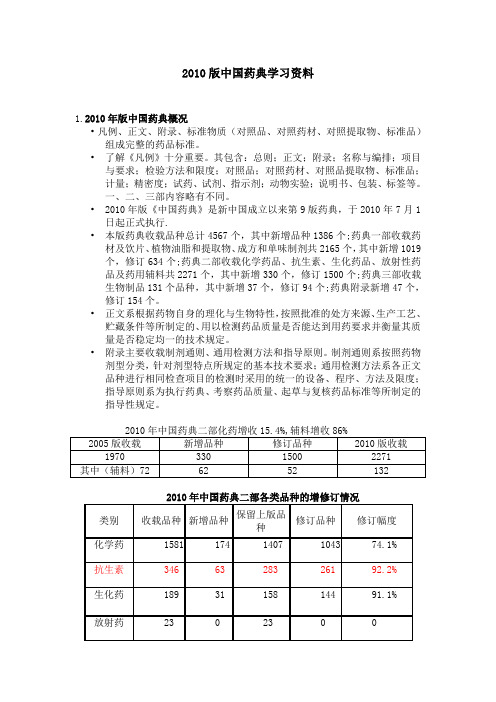
2010版中国药典学习资料1.2010年版中国药典概况•凡例、正文、附录、标准物质(对照品、对照药材、对照提取物、标准品)组成完整的药品标准。
•了解《凡例》十分重要。
其包含:总则;正文;附录;名称与编排;项目与要求;检验方法和限度;对照品;对照药材、对照品提取物、标准品;计量;精密度;试药、试剂、指示剂;动物实验;说明书、包装、标签等。
一、二、三部内容略有不同。
•2010年版《中国药典》是新中国成立以来第9版药典,于2010年7月1日起正式执行.•本版药典收载品种总计4567个,其中新增品种1386个;药典一部收载药材及饮片、植物油脂和提取物、成方和单味制剂共2165个,其中新增1019个,修订634个;药典二部收载化学药品、抗生素、生化药品、放射性药品及药用辅料共2271个,其中新增330个,修订1500个;药典三部收载生物制品131个品种,其中新增37个,修订94个;药典附录新增47个,修订154个。
•正文系根据药物自身的理化与生物特性,按照批准的处方来源、生产工艺、贮藏条件等所制定的、用以检测药品质量是否能达到用药要求并衡量其质量是否稳定均一的技术规定。
•附录主要收载制剂通则、通用检测方法和指导原则。
制剂通则系按照药物剂型分类,针对剂型特点所规定的基本技术要求;通用检测方法系各正文品种进行相同检查项目的检测时采用的统一的设备、程序、方法及限度;指导原则系为执行药典、考察药品质量、起草与复核药品标准等所制定的指导性规定。
凡例的增修订情况•新版药典凡例进行了重大修订:•1)、首次在凡例中设置总则一节。
增加了“总则”一节,将中国药典中最重要、最原则、最通用、最基础的内容集中阐明,并且做到一、二、三部之凡例的体例、结构的一致性。
内容在保留特点的基础上也基本一致。
•2)、首次明确药典制定颁布依据。
新版药典凡例总则之一明确“《中华人民共和国药典》简称《中国药典》。
《中国药典》依据《中国人民共和国药品管理法》组织制定和颁布实施”。
《中华人民共和国药典》2010年版

附件《中华人民共和国药典》2010年版第三增补本目录一部新增品种1.三七伤药胶囊2.三七伤药颗粒3.女珍颗粒4.小儿七星茶口服液5.小儿肺咳颗粒6.小柴胡胶囊7.开胸顺气胶囊8.五苓胶囊9.止痛化癥片10.牛黄化毒片11.牛黄净脑片12.六君子丸13.心脑康片14.四物颗粒15.乐脉丸16.乐脉片17.乐脉胶囊18.外感风寒颗粒19.花红胶囊20.芪参胶囊21.克感利咽口服液22.抗炎退热片23.抗栓再造丸24.补肾养血丸25.补肾益脑丸26.补益地黄丸27.苦参片28.枇杷止咳软胶囊29.刺五加胶囊30.刺五加颗粒31.肾宝合剂32.肾宝糖浆33.肾康宁颗粒34.明目地黄丸(浓缩丸)35.金莲花颗粒36.栀芩清热合剂37.胃安胶囊38.胃疡灵颗粒39.香砂胃苓丸40.复方杏香兔耳风颗粒41.姜黄消痤搽剂42.养阴清肺口服液43.津力达颗粒44.桔梗冬花片45.柴连口服液46.柴黄口服液47.钻山风糖浆48.通窍鼻炎胶囊49.通窍鼻炎颗粒50.桑菊感冒丸51.银翘散52.康尔心胶囊53.康妇软膏54.康莱特软胶囊55.清肺化痰丸56.清热解毒片57.脾胃舒丸58.感冒清热咀嚼片59.感冒清热胶囊60.缩泉胶囊修订品种1.丹参2.灵芝3.楮实子4.蕲蛇5.二至丸6.七味铁屑丸7.小金丸8.元胡止痛片9.止痛化癥胶囊10.牛黄降压片11.乌鸡白凤丸12.心脑康胶囊13.百令胶囊14.灯盏细辛注射液15.芪苈强心胶囊16.辛夷鼻炎丸17.刺五加片18.金水宝胶囊19.保妇康栓20.桂龙咳喘宁胶囊21.健脑安神片22.脂脉康胶囊(降脂灵胶囊)23.黄连上清颗粒24.银黄颗粒25.康妇消炎栓26.葛根芩连丸(葛根芩连微丸)27.感冒清热颗粒新增附录1.附录ⅩⅧ J 中药材DNA条形码分子鉴定法指导原则修订附录1.附录Ⅵ E 甲醇量检查法2.附录ⅩⅧ G 药品微生物实验室质量管理指导原则二部新增品种1.乙胺吡嗪利福异烟片(Ⅱ)2.厄贝沙坦3.厄贝沙坦片4.厄贝沙坦分散片5.厄贝沙坦胶囊6.水杨酸软膏7.甘氨双唑钠8.注射用甘氨双唑钠9.司他夫定10.地高辛口服溶液11.齐多夫定12.齐多夫定注射液13.齐多拉米双夫定片14.坎地沙坦酯15.妥布霉素地塞米松眼膏16.妥布霉素地塞米松滴眼液17.青蒿素哌喹片18.苯扎贝特胶囊19.拉米夫定20.拉米夫定片21.果糖22.注射用果糖23.帕司烟肼24.依达拉奉25.依达拉奉注射液26.乳果糖浓溶液27.注射用甲磺酸加贝酯28.注射用吡拉西坦29.注射用盐酸纳洛酮30.复方蒿甲醚片31.盐酸西替利嗪胶囊32.盐酸吡硫醇注射液33.盐酸阿普林定34.盐酸阿普林定片35.盐酸班布特罗36.盐酸班布特罗片37.恩曲他滨38.恩曲他滨胶囊39.棓丙酯40.注射用棓丙酯41.硝酸咪康唑阴道片42.硝酸咪康唑阴道软胶囊43.硝酸咪康唑阴道泡腾片44.碘佛醇45.碘佛醇注射液46.磷酸咯萘啶47.磷酸咯萘啶注射液48.二氧化碳49.门冬氨酸50.门冬酰胺51.马来酸52.牛磺酸53.甘氨酸54.丙氨酸55.色氨酸56.麦芽酚57.谷氨酸钠58.果糖59.组氨酸60.亮氨酸61.氧化钙62.酪氨酸63.精氨酸64.缬氨酸65.磷酸修订品种1.壬苯醇醚栓2.双氢青蒿素3.双氢青蒿素哌喹片4.本芴醇5.丙氨酰谷氨酰胺注射液6.左炔诺孕酮炔雌醚片7.甲状腺片8.甲状腺粉9.生长抑素10.注射用生长抑素11.头孢克肟分散片12.司他夫定胶囊13.对氨基水杨酸钠14.对氨基水杨酸钠肠溶片15.注射用对氨基水杨酸钠16.地塞米松磷酸钠注射液17.钆喷酸葡胺注射液18.异福片19.异福胶囊20.异福酰胺片21.异福酰胺胶囊22.克林霉素磷酸酯23.吡嗪酰胺24.吡嗪酰胺片25.吡嗪酰胺胶囊26.吲哚菁绿27.利福平28.利福昔明干混悬剂29.谷氨酰胺颗粒30.尿促性素31.阿法骨化醇软胶囊32.阿莫西林舒巴坦匹酯片33.青蒿琥酯34.青蒿琥酯片35.注射用青蒿琥酯36.奈韦拉平37.奈韦拉平片38.注射用苯磺顺阿曲库铵39.注射用奥硝唑40.复方莪术油栓41.绒促性素42.盐酸乙胺丁醇片43.盐酸乙胺丁醇胶囊44.盐酸西替利嗪滴剂45.格列本脲46.替米沙坦47.葡萄糖酸钙氯化钠注射液48.氯化钙注射液49.氯雷他定片50.醋酸曲普瑞林注射液51.磷酸伯氨喹52.磷酸伯氨喹片53.磷酸哌喹54.磷酸哌喹片55.无水亚硫酸钠56.亚硫酸氢钠57.麦芽糊精58.DL-苹果酸59.L-苹果酸60.DL-酒石酸61.富马酸62.醋酸新增附录1.附录ⅪⅩ S 药用辅料功能性指标研究指导原则修订附录1.附录Ⅵ G 黏度测定法2.附录Ⅸ B 澄清度检查法3.附录Ⅹ A 崩解时限检查法4.附录Ⅹ K 锥入度测定法5.附录Ⅻ D 肝素生物测定法6.附录ⅩⅨ F 药品杂质分析指导原则7.附录ⅩⅨ Q 药品微生物实验室质量管理指导原则三部新增品种1.注射用红色诺卡氏菌细胞壁骨架索引中文索引1.一部2.二部3.三部英文索引1.二部2.三部。
2010版中国药典一部word版电子书

2010版中国药典一部word版电子书中国药典沿革1953年版(第一版) 1949年10月1日中华人民共和国成立后,党和政府十分关怀人民的医药卫生保健工作,当年11月卫生部召集在京有关医药专家研讨编纂药典问题。
1950年1月卫生部从上海抽调药学专家孟目的教授负责组建中国药典编纂委员会和处理日常工作的干事会,筹划编制新中国药典。
1950年4月在上海召开药典工作座谈会,讨论药典的收载品种原则和建议收载的品种,并根据卫生部指示,提出新中国药典要结合国情,编出一部具有民族化、科学化,大众化的药典。
随后,卫生部聘请药典委员49人,分设名词、化学药、制剂、植物药、生物制品、动物药、药理、剂量8个小组,另聘请通讯委员35人,成立了第一届中国药典编纂委员会。
卫生部部长李德全任主任委员。
1951年4月24日至28日在北京召开第一届中国药典编纂委员会第一次全体会议,会议对药典的名称、收载品种、专用名词、度量衡问题以及格式排列等作出决定。
干事会根据全会讨论的意见,对药典草案进行修订,草案于1952年底报卫生部核转政务院文教委员会批准后,第一部《中国药典》1953年版由卫生部编印发行。
本版药典共收载品种531种,其中化学药215种植物药与油脂类65种,动物药13种,抗生素2种,生物制品25种,各类制剂211种。
1957年出版《中国药典》1953年版增补本。
1963年版(第二版) 1955年卫生部组建第二届药典委员会,聘请委员49人,通讯委员68人,此届委员会因故未能开展工作。
1957年卫生部组建第三届药典委员会,聘请委员80人,药学专家汤腾汉教授为这届委员会主任委员(不设通讯委员),同年7月28日至8月5日在北京召开第一次全体委员会议,卫生部李德全部长做了药典工作报告,特别指出第一版《中国药典》未收载广大民众习用的中药的缺陷。
会议在总结工作的基础上,通过了制订药典的原则,讨论了药典的性质和作用,修改了委员会章程,并一致认为应把合乎条件的中药收载到药典中。
中国药典2010年版二部解析

附录II 附录 药用辅料
残留溶剂、微生物限度或无菌应符合要求 注射用药用辅料的热原或细菌内毒素、无菌等应 符合要求
附录IV 附录 A 紫外-可见分光光度法 紫外 可见分光光度法
高氯酸钬溶液校正双光束仪器波长 校正波长的允许误差:紫外光区±1nm,500nm 附近±2nm 吸收峰波长应在该品种项下规定的波长±2nm以 内,并以吸光度最大的波长作为测定波长 当溶液pH值对测定结果有影响时,应将供试品 溶液和对照品溶液的pH值调成一致{研究注意}
附录VII A 附录 电位滴定法与永停滴定法
滴定终点确定的作图法分为一阶导数法 [(∆E/∆V)-V曲线]的极值和二阶导数法 [(∆2E/∆V2)-V曲线]曲线过零时的对应体积 滴定终点确定的二阶导数法还可采用曲线过零前、 后两点坐标的线性内插法计算: V0=V+∆V×a/(a+b)
附录VIII H 附录 重金属检查法
附录IX 附录 C 不溶性微粒检查法
应用对象:静脉用注射剂(溶液型、注射用无菌 粉末、注射用浓溶液)及静脉注射用无菌原料药 【原:溶液型静脉用注射剂】{应用范围扩大} { } 光阻法仪器一般要求:测量粒径范围为“2~ 100µm”,检测微粒浓度为“0~10000个/ml” 【原:测量粒径范围为“2~50µm”,检测微 粒浓度为“0~5000个/ml”】
附录I 附录 B 注射剂
注射剂所用原辅料应从来源及工艺等生产环节进行严格 控制并应符合注射用的质量要求 供注射用的非水性溶剂,应严格限制其用量,并应在品 种项下进行相应的检查 除另有规定外,容器应足够透明,以便内容物的检视{性 状、可见异物检查法} 注射剂必要时应进行相应的安全性检查,如异常毒性、 过敏反应、溶血与凝聚、降压物质、热原或细菌内毒素 等,均应符合规定 注射剂所用辅料,在标签或说明书中应标明其名称
2010年版《中华人民共和国药典》产地趁鲜加工品种

2010年版《中华人民共和国药典》产地趁鲜加工品种序号品名规格
1 巴戟天生段
2 "菝葜" 生片
3 白蔹生片
4 柏子仁生净
5 川木通生片
6 地榆生片
7 滇鸡血藤生片
8 颠茄草生段
9 丁公藤生片
10 粉萆薢生片
11 粉葛根厚片
12 佛手生片
13 茯苓生片
14 茯苓皮生净
15 干姜生片
16 高良姜生段
17 葛根小块
18 功劳木生片
19 钩藤生段
20 狗脊厚片
21 广东紫珠生段
22 桂枝厚片
23 何首乌生块
24 虎杖厚片
25 槲寄生生段
26 黄山药生片
27 黄藤生段
28 鸡血藤生片
29 金钱白花蛇生净
30 苦参厚片
31 苦杏仁生净
32 狼毒生片
33 两面针生片
34 绵萆薢生片
35 片姜黄厚片
36 桑寄生生段
37 桑枝生片
38 三奈生片
39 山楂生片
40 山茱萸生净
41 商陆生片
42 首乌藤(夜交藤)生段
43 桃枝生段
44 土茯苓薄片
45 乌药生片
46 香橼生片
47 野木瓜生段
48 益母草生段
49 皂角刺生段
50 浙贝母厚片
51 紫苏梗生段。
2010版中华人民共和国药典临床用药须知

2010版中华人民共和国药典临床用药须知出版社:中国医药科技出版社2011年7月出版1.《化学药和生物制品》定价:750.00元2《中成药》定价:650.00元3《中药饮片》定价:580.00元规格:全三卷定价:1980元优惠价:1380元《中华人民共和国药典临床用药须知》(以下简称《临床用药须知》是《中华人民共和国药典》(以下简称《中国药典》)配套标准图书之一,将于2011年6月由中国医药科技出版社正式出版发行。
2010年版《临床用药须知》由第九届药典委员会医学专业委员会、中医专业委员会组织全国范围内各学科具有丰富专业知识、工作严谨的医药学权威专家,根据临床用药经验并结合国内外公认的资料编写。
本版在前几版基础上做了大胆探索和创新,明确《临床用药须知》为药典服务,防范药典收载品种的盲目性和随意性,做到覆盖《国家基本药物》、《国家基本医疗保险和工伤保险药品目录》及临床常用药品,达到信息广博、内容丰富、与时俱进、科学合理、经典实用、准确权威的总目标。
该书内容科学、详实,论述严谨、有序,紧密结合临床实际,具有较高的实用性和权威性。
一、体例更趋合理为了指导临床应用和适应近年来药品迅速发展的形势,2010年版《临床用药须知》分为三卷。
1、《临床用药须知》化学药和生物制品卷是在前四版的基础上,结合我国临床用药的实际情况进行了充实、修订和完善,使其更具科学性、实用性。
全书共收载药品1350余种(按原料药计),比上一版增加了30%,除《中国药典》2010年版(二部)所收载品种外,尚包括部分药典未收载,但国家已正式批准生产且临床应用广泛的品种,并根据需要新增了部分临床广泛应用的进口药品的相关信息。
2、《临床用药须知》中药成方制剂卷是在2005版《临床用药须知》中药卷的基础上进行修订编写而成,本书增加了总论内容,回顾了从先秦到民国不同历史时期中成药的发展历史,着重介绍了中华人民共和国成立以来中成药事业蓬勃发展的光辉历程;在总论中还介绍了中成药的命名分类组成、常用剂型、用法用量、使用注意、不良反应等内容,并重点从辨证合理用药、配伍合理用药、安全合理用药、依法合理用药四个方面,系统地介绍了指导临床安全、有效、科学使用中成药的理论和方法。
中华人民共和国药典-2010版

2010年版中华人民共和国药典-全三部作者:国家药典委员会丛书名:中华人民共和国药典-2010年版【ISBN】:9787506744379出版社:中国医药科技出版社出版日期:2010年1月1日包装:大16开精装3卷总定价:1498.00优惠价:1100元内容简介:2010年版药典的鲜明特色:更新与淘汰并举、收载品种大幅增加。
药品检测项目和检测方法增加、标准提高,因而在药品安全性和质量可控性方面有更高、更多、更大提升。
二部中采用高效液相色谱法进行含量测定或用于有关物质检查的品种有近千个,系统适用性要求也更为合理,个别品种采用了分离效能更高的离子色谱法,检测器使用种类也更加多样。
中药标准有突破和创新,尤其在过去比较薄弱的中药材和中药饮片标准的新增和修订方面,如本版《中国药典》一部中动物药蛇类、植物药川贝母等,都采用了PCR检测方法。
新版药典在凡例、品种的标准要求、附录的制剂通则等方面均有较大的变化和进步。
在广泛吸取国内外先进技术和实验方法的基础上,附录内容与目前国际对药品质量控制的方法和技术力求一致,进一步发挥《中国药典》的国际影响力。
新版药典在坚持科学、实用、规范、药品安全性、质量可控性和标准先进性的原则下,力求覆盖国家基本药物目录品种和社会医疗保险报销药品目录品种。
顶尖专家扛鼎之作。
本版《中国药典》是在第九届药典委员会的精心组织下,聘请全国医药行业323位一流专家、投入巨额资金、历时两年编制而成,集中体现了当前我国药品标准工作的最新发展成果。
《中国药典》是国家监督管理药品质量的法定技术标准。
2010年版《中国药典》分为三部出版,一部为中药,二部为化学药,三部为生物制品。
各部内容主要包括凡例、标准正文和附录三部分,其中附录由制剂通则、通用检测方法、指导原则及索引等内容构成。
药典二部收载化学药品、抗生素、生化药品、放射性药品以及药用辅料等。
药典三部收载生物制品。
新版药典在凡例、品种的标准要求、附录的制剂通则和检验方法等方面均有较大的改进和发展,特别是对药品的安全性、有效性和质量可控性方面尤为重视。
中国药典2010年版
年版截图:中国药典20102010版中国药典word版pdf版exe版电子书2010版中国药典word版pdf版exe版电子书中国药典2010年版一部正文一枝黄花(p3)YizhihuanghuaSOLIDAGINIS HERBA本品为菊科植物一枝黄花Solidago decurrens Lour.的干燥全草。
秋季花果期采挖,除去泥沙,晒干。
【性状】本品长30~lOOcm。
根茎短粗,簇生淡黄色细根。
茎圆柱形,直径0.2~0.5cm;表面黄绿色、灰棕色或暗紫红色,有棱线,上部被毛;质脆,易折断,断面纤维性,有髓。
单叶互生,多皱缩、破碎,完整叶片展平后呈卵形或披针形,长1~9cm,宽0.3~1.5cm;先端稍尖或钝,全缘或有不规则的疏锯齿,基部下延成柄。
头状花序直径约0.7cm,排成总状,偶有黄色舌状花残留,多皱缩扭曲,苞片3层,卵状披针形。
瘦果细小,冠毛黄白色。
气微香,味微苦辛。
【鉴别】 (1)叶表面观:上表皮细胞多角形,垂周壁略呈念珠状增厚。
下表皮细胞垂周壁波状弯曲,气孔不定式,略下陷。
非腺毛有两类:表皮非腺毛由3个细胞组成,壁薄,顶端1个细胞常萎缩成鼠尾状,较小;叶缘非腺毛睫毛状由3~7个细胞组成,壁稍厚,长180~500μm。
(2)取本品粉末2g,加石油醚(60~90℃)50ml,超声处理30分钟,放冷,滤过,弃去石油醚液,药渣挥干溶剂,加70%乙醇30ml,加热回流1小时,放冷,滤过,滤液蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。
另取一枝黄花对照药材2 g,同法制成对照药材溶液。
再取芦丁对照品,加甲醇制成每1ml含0.5mg的溶液,作为对照品溶液。
照薄层色谱法(附录ⅥB)试验,吸取供试品溶液5~10μl、对照药材溶液和对照品溶液各5μl,分别点于同一以含4%磷酸氢二钠溶液制备的硅胶G薄层板上,以乙酸乙酯-甲醇-甲酸-水(8:1:2010版中国药典word版pdf版exe版电子书1:1)为展示剂,展开,取出,晾干,喷以3%三氯化铝乙醇溶液,晾干,置紫外光灯(365nm)下检视,供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的荧光斑点。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
丛书名:中华人民共和国药典-2010年版【ISBN】:9787506744379
作者:国家药典委员会
出版社:中国医药科技出版社
出版日期:2010年1月1日
包装:大16开精装3卷
总定价:1498.00
优惠价:1100元
内容简介:
2010年版药典的鲜明特色:
更新与淘汰并举、收载品种大幅增加。
药品检测项目和检测方法增加、标准提高,因而在药品安全性和质量可控性方面有更高、更多、更大提升。
二部中采用高效液相色谱法进行含量测定或用于有关物质检查的品种有近千个,系统适用性要求也更为合理,个别品种采用了分离效能更高的离子色谱法,检测器使用种类也更加多样。
中药标准有突破和创新,尤其在过去比较薄弱的中药材和中药饮片标准的新增和修订方面,如本
版《中国药典》一部中动物药蛇类、植物药川贝母等,都采用了PCR检测方法。
新版药典在凡例、品种的标准要求、附录的制剂通则等方面均有较大的变化和进步。
在广泛吸取国内外先进技术和实验方法的基础上,附录内容与目前国际对药品质量控制的方法和技术力求
一致,进一步发挥《中国药典》的国际影响力。
新版药典在坚持科学、实用、规范、药品安全性、质量可控性和标准先进性的原则下,力求覆盖国家基本药物目录品种和社会医疗保险报销药品
目录品种。
顶尖专家扛鼎之作。
本版《中国药典》是在第九届药典委员会的精心组织下,聘请全国医药行业323位一流专家、投入巨额资金、历时两年编制而成,集中体现了当前我国药品标准工作的最新发展成果。
《中国药典》是国家监督管理药品质量的法定技术标准。
2010年版《中国药典》分为三部出版,一部为中药,二部为化学药,三部为生物制品。
各部内容主要包括凡例、标准正文和附录三部分,其中附录由制剂通则、通用检测方法、指导原则及索引等内容构成。
药典二部收载化学药品、抗生素、生化药品、放射性药品以及药用辅料等。
药典三部收载生物制品。
新版药典在凡例、品种的标准要求、附录的制剂通则和检验方法等方面均有较大的改进
和发展,特别是对药品的安全性、有效性和质量可控性方面尤为重视。
新版药典在继承前版药典的基础上,做了大量发展和创新性的工作。
新增与淘汰并举,收载品种大幅增加提高药品标准就意味着优胜劣汰。
2010年版《中国药典》在2005年版的基础上,做了大幅度的增修
订和新增品种的工作。
本版药典共收载品种4615种,新增1358种。
一部收载品种2136种,其中新增990种、修订612种;
二部收载品种2348种,其中新增340种、
修订1500种;
三部收载品种131种,其中新增28种、修订103种。
药用辅料标准新增130多
种。
附录其中药典一部新增14个、修订54个;药典二部新增15个、修订70个;药典三部新增18个、修订38个。
