关于2010年版《中国药典》第二增补本品种的公示
关于2010年版《中国药典》第二增补本品种的公示

关于2010年版《中国药典》第二增补本品种的公示
更新日期: 2012年4月9日下午3:42
29 乳癖消颗粒
30 参苓白术丸
31 参苓白术颗粒
32 季德胜蛇药片
33 金匮肾气丸
34 金匮肾气片
35 保和片
36 保和颗粒
37 冠心苏合胶囊
38 复方丹参胶囊
39 活血止痛胶囊
40 胃苏颗粒
41 茵栀黄颗粒
42 香砂养胃丸(浓缩丸)
43 消炎利胆胶囊
44 消炎利胆颗粒
45 益母草片
46 益母草胶囊
47 通宣理肺颗粒
48 速效救心丸
49 接骨七厘片
50 清开灵颗粒
51 蛇胆川贝液
52 银黄片
53 颈舒颗粒
54 黄连上清胶囊
55 黄连上清颗粒
56 普乐安片
57 普乐安胶囊
58 舒筋活血丸
59 舒筋活血片
60 橘红片
61 橘红胶囊
2、新增品种
序号品种名称
1 金嗓清音丸
2 保济口服液
3 脉安颗粒
4 健脾生血颗粒。
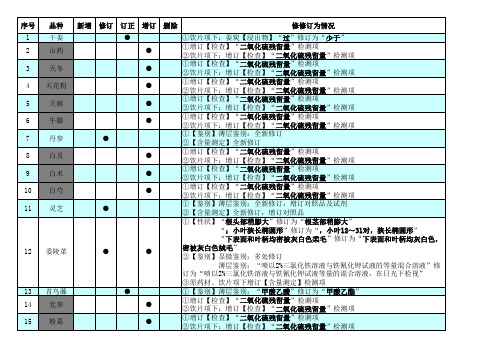
《中国药典》2010版第二增补本一部中药材修改品种明细
12
委陵菜
●
●
13 14 15
首乌藤 党参 粉葛
● ● ●
16 17
黄连 酸枣仁
● ●
①【含量测定】“不得少于7.0%”修订为“含小檗碱(C20 H17 NO4 )不得少于7.0%” ①饮片项下:“酸枣变(2010版勘误) 原药材及饮片检测项改动较大 原药材及饮片检测项改动较大 原药材及饮片检测项改动较大 原药材及饮片检测项改动较大 原药材及饮片检测项改动较大 原药材检测项改动较大 原药材及饮片检测项改动较大 原药材及饮片检测项改动较大 原药材及饮片检测项改动较大 原药材检测项改动较大
需新申购 / / / / / / / / / / 半乳糖对照品、木糖对照 品
原药材及饮片检测项改动较大
/
整体检测方法无改变(2010版勘误) 原药材及饮片检测项改动较大 原药材及饮片检测项改动较大
/ / /
整体检测方法无改变 饮片检测项改动较大
/ /
序号 1 2 3 4 5 6 7 8 9 10 11
品种 干姜 山药 天冬 天花粉 天麻 牛膝 丹参 白及 白术 白芍 灵芝
新增 修订 订正 增订 删除 ● ● ● ● ● ● ● ● ● ● ●
修修订为情况 ①饮片项下:姜炭【浸出物】“过”修订为“少于” ①增订【检查】“二氧化硫残留量”检测项 ②饮片项下:增订【检查】“二氧化硫残留量”检测项 ①增订【检查】“二氧化硫残留量”检测项 ②饮片项下:增订【检查】“二氧化硫残留量”检测项 ①增订【检查】“二氧化硫残留量”检测项 ②饮片项下:增订【检查】“二氧化硫残留量”检测项 ①增订【检查】“二氧化硫残留量”检测项 ②饮片项下:增订【检查】“二氧化硫残留量”检测项 ①增订【检查】“二氧化硫残留量”检测项 ②饮片项下:增订【检查】“二氧化硫残留量”检测项 ①【鉴别】薄层鉴别:全新修订 ②【含量测定】全新修订 ①增订【检查】“二氧化硫残留量”检测项 ②饮片项下:增订【检查】“二氧化硫残留量”检测项 ①增订【检查】“二氧化硫残留量”检测项 ②饮片项下:增订【检查】“二氧化硫残留量”检测项 ①增订【检查】“二氧化硫残留量”检测项 ②饮片项下:增订【检查】“二氧化硫残留量”检测项 ①【鉴别】薄层鉴别:全新修订,增订对照品及试剂 ②【含量测定】全新修订,增订对照品 ①【性状】“根头部稍膨大”修订为“根茎部稍膨大” “;小叶狭长椭圆形”修订为“,小叶12~31对,狭长椭圆形” “下表面和叶柄均密被灰白色柔毛”修订为“下表面和叶柄均灰白色, 密被灰白色绒毛” ②【鉴别】显微鉴别:多处修订 薄层鉴别:“喷以2%三氯化铁溶液与铁氰化钾试液的等量混合溶液”修 订为“喷以2%三氯化铁溶液与铁氰化钾试液等量的混合溶液,在日光下检视” ③原药材、饮片项下增订【含量测定】检测项 ①【鉴别】薄层鉴别:“甲酸乙酸”修订为“甲酸乙酯” ①增订【检查】“二氧化硫残留量”检测项 ②饮片项下:增订【检查】“二氧化硫残留量”检测项 ①增订【检查】“二氧化硫残留量”检测项 ②饮片项下:增订【检查】“二氧化硫残留量”检测项
2010年版药典(二部)增修订内容及新增品种-截止到第7批

目录1.关于2010年版药典(二部)增修订内容及新增品种(第一批)的公示·········22.关于2010年版药典(二部)增修订内容及新增品种(第二批)的公示·········23.关于2010年版药典(二部)增修订内容及新增品种(第三批)的公示·········24.2010年版药典(二部)增补本增修订内容-第四批·········································35.2010年版药典增补本拟新增品种公示-第四批·················································56.2010年版药典(二部)增补本增修订内容(第五批)··································77.附件:2010年版药典增补本拟新增品种公示-第五批·········································98.附件:关于2010年版药典(二部)增补本的公示(第六批)····························99.关于2010年版药典(二部)增补本的公示(第七批)·································101.关于2010年版药典(二部)增修订内容及新增品种(第一批)的公示更新日期:2010年6月12日上午10:22我委现将2010年版药典(二部)增修订内容及新增品种(第一批)进行公示,增修订内容见附件。
2010年版药典(二部)增修订介绍

各论的增修订情况(1):名称与性状
溶解度( 原料药)
对收录溶剂进行了适当的取舍,原则是首选标准中用到的 溶剂及重结晶溶剂;选择常用试剂,考虑环保因素;对于 难溶的样品,应考虑特殊溶剂,如酸性溶液和碱性溶液或 二甲基亚砜和二甲基甲酰胺等对试验有帮助的溶剂。
今后应加强对多晶型药物不同晶型溶解度的考察。
2271个
330个
1941个
1500个
76.1%
其中,由于未找到样品而未修订的品种有345个,占保留上版品种17.5%
例:注射用盐酸阿糖胞苷
项目 鉴别 2005年版 2项 酸度 干燥失重 ---检查 ---2010年版 3项(+LC) 酸度 水分 溶液的澄清度 有关物质
------含量测定 UV吸收系数法
174
63 31 0 268
1407
283 158 23 1871
化学药中由于未找到样品而未修订的品种有306个,占保留上版品种21.8%
2010年版与2005年版药典主要项目收载情况比对表
增修订项目 红外光谱鉴别 有关物质 残留溶剂 渗透压摩尔浓度 溶出度或释放度 含量均匀度 无菌检查方法 细菌内毒素 原料 2005年版 530 2010年版 580
(2)制剂:一般收2-3个鉴别,以化学反应、色谱和紫外光谱鉴别为
主,部分制剂采用了红外光谱鉴别。根据辅料对样品提取结果的影响 不同,采用了全谱比较或限定特征波数两种方式。
各论的增修订情况(2):鉴别
化学反应
要选用反应明显、专属性较强的方法,且试剂易得、毒 性较低。毒性大的、放射性强的、有悖于环保的,删除。
• 各论的增修订情况(4):有效性检查
• 各论的增修订情况(5):含量测定
2010年版药典(二部)增修订内容及新增品种(第三批)

征求意见稿2010 年版药典(二部)增修订内容及新增品种公示(第三批)一、增修订品种诺氟沙星胶囊[订正]【检查】其他 应符合胶囊剂项下有关的各项规定(附录Ⅰ E)。
盐酸甲氯芬酯[订正]【检查】有机酸 第4行“消耗氢氧化钠滴定液(1.0mol/L)不得过0.54ml”改为“消耗氢氧化钠滴定液(0.1mol/L)不得过0.54ml”。
富马酸亚铁咀嚼片 [订正] 【鉴别】(1)第1行“取本品,除去包衣后,研细,取细粉适量(约相当于富马酸亚铁2g)”改为“取本品细粉适量(约相当于富马酸亚铁2g)”硫唑嘌呤片 [订正]【检查】有关物质 第4行“供试品溶液色谱图中如有与对照品溶液色谱图中6-巯基嘌呤峰……”改为“供试品溶液色谱图中如有与对照品溶液(1)色谱图中6-巯基嘌呤峰……”。
卡莫司汀 [订正]【检查】干燥失重 第2行“60℃减压干燥至恒重……”改为“减压干燥至恒重……吸收性明胶海绵 [修订] 【检查】甲醛 取本品10片,剪碎,混合均匀,精密称取0.5g,加水100ml,浸泡2小时,并时时振摇,吸取上清液 1.0ml,加变色酸试液20ml,摇匀,加塞,置水浴中加热30分钟,放冷,照紫外-可见分光光度法(附录Ⅳ A),在570nm 的波长处测定吸光度,与征求意见稿0.003%(W/V)标准甲醛溶液1.0ml 同法制成的对照液比较,吸光度不得更大(0.6%)。
注射用盐酸甲氯芬酯[修订]【检查】溶液的澄清度 “取本品,每支加水5ml 溶解后,溶液应澄清……”改为“取本品,加水溶解并稀释制成每1ml 中约含50mg 的溶液,溶液应澄清……”。
叶酸[增订]【检查】有关物质 取本品约100mg ,精密称定,置100ml 量瓶中,加氨试液约1ml 使溶解,用流动相稀释至刻度,摇匀,作为供试品溶液。
精密量取适量,加流动相定量稀释制成每1ml 中约含1μg 的溶液作为对照溶液。
取蝶酸10mg ,置100ml 量瓶中,加0.1mol/L 磷酸钠溶液5ml 与供试品溶液10ml ,用流动相溶解并稀释至刻度,摇匀,照含量测定项下的色谱条件,取10μl 注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的20%。
2010年药典第二增补本

2010年药典第二增补本2010年药典第二增补本是中华人民共和国卫生部制定的医药领域的重要规范性文件,全称为《中华人民共和国药典-药品行业标准-药典增补本(2010年)第二部》。
这本药典增补本是在原有2010年药典的基础上进行修订和增补而成,为医药行业的规范发展和药品质量的保证起到了重要的作用。
首先,2010年药典第二增补本对于药品的规格和质量标准做出了详细的规定。
药品对于人们的生命健康至关重要,因此药品的质量必须得到严格的控制和保证。
增补本对于常用的药品进行了规格和质量标准的明确,从原材料的选择、生产工艺的控制到最终产品的质量检测等方面进行了全面的规定。
这对于提升药品的质量和可靠性具有十分重要的意义。
其次,2010年药典第二增补本对于公共卫生和个人健康也起到了积极的作用。
药品的规范使用和正确用药对于人们的健康至关重要,特别是在公共卫生事件和突发疫情等情况下,正确用药更是关系到整个社会的健康和稳定。
增补本对于药品的使用说明、禁忌和注意事项进行了详细的规定,确保了药品的正确使用,避免了因为错误使用导致的不良反应和副作用。
更重要的是,增补本还对药品的储存和运输等环节进行了规范,避免了药品质量受到损害的可能。
此外,2010年药典第二增补本还推动了医药行业的技术创新和科学发展。
药典是医药行业的基础性文件,其质量要求和技术规范的更新对于新药开发和现有药品的改进至关重要。
增补本对于一些新药的质量标准进行了修订和增补,使得这些新药能够更好地适应市场需求,并保证了其安全性和有效性。
此外,增补本还对一些已有药品的质量标准进行了调整和完善,使得这些药品能够更好地适应现实临床需求。
总而言之,2010年药典第二增补本是医药领域的重要规范性文件,其规定的药品规格和质量标准能够确保药品的安全性和有效性。
增补本对于公共卫生和个人健康也起到了积极的作用,确保了药品的正确使用和储存运输,避免了不良反应和药品质量受到损害的可能。
此外,增补本还推动了医药行业的技术创新和科学发展,为新药开发和现有药品的改进提供了可靠的依据。
中国药典2010年版第一、二增补本目录

菝葜 菊苣 甜瓜子 猪胆粉 商陆 续断 绵马贯众 棕榈 蛤蚧 蓖麻子 蒲公英 槐角 满山红 酸枣仁 蜘蛛香 辣椒 灯盏花素 肿节风浸膏 莪术油 二十五味珍珠丸 二母安嗽丸 十香返生丸 三九胃泰颗粒 大川芎口服液 山香圆片 千柏鼻炎片 川芎茶调丸 川芎茶调散 小儿七星茶颗粒 小儿退热颗粒 小儿腹泻宁糖浆 天舒胶囊 云南白药胶囊 云香祛风止痛酊(云香精) 牛黄上清片 牛黄蛇胆川贝液 牛黄清心丸(局方) 牛黄解毒片 牛黄镇惊丸 片仔癀 分清五淋丸 丹红化瘀口服液 丹桂香颗粒 风痛安胶囊 风湿马钱片 乌灵胶囊 六合定中丸
三七伤药片 三九胃泰胶囊 女金丸 小儿退热合剂(小儿退热口服液) 天和追风膏 天麻丸 五福化毒丸 中风回春片 中华跌打丸 牛黄上清丸 牛黄降压片 六味地黄颗粒 心血宁片 双黄连口服液 玉屏风胶囊 石斛夜光丸 龙胆泻肝丸 再造生血片 西瓜霜润喉片 百合固金丸 伤痛宁片 壮骨关节丸 灯盏生脉胶囊 导赤丸 妇科十味片 利肝隆颗粒 利胆片 辛夷鼻炎丸 启脾丸 阿胶补血膏 附子理中丸 板蓝根颗粒 刺五加片 郁金银屑片 金果含片 金果饮 金振口服液 金银花露 乳癖消片 乳癖消胶囊 骨仙片 复方川贝精片 复方丹参滴丸 复方石韦片 复方鱼腥草片 复方鲜竹沥液 保妇康栓
奥硝唑胶囊 奥硝唑葡萄糖注射液 注射用奥硝唑 蒙脱石 蒙脱石分散片 蒙脱石散 羧苄西林钠 注射用羧苄西林钠 醋酸去氨加压素 醋酸去氨加压素注射液 醋酸曲普瑞林 醋酸曲普瑞林注射液 注射用磷酸川芎嗪 二丁基羟基甲苯 十八醇 十六醇 十六十八醇 山梨酸钾 马来酸(顺丁烯二酸) 口服补液盐酸(Ⅰ) 右旋糖酐40葡萄糖注射液 甲磺酸酚妥拉明 注射用甲磺酸酚妥拉明 尼可刹米注射液 丝裂霉素 地高辛片 呋喃唑酮 阿昔洛韦 阿昔洛韦滴眼液 非诺贝特 非诺贝特片 非诺贝特胶囊 乳糖酸红霉素 炔雌醚 单硝酸异山梨酯缓释片 枸橼酸铋钾胶囊 精蛋白重组人胰岛素注射液 盐酸克林霉素 盐酸格拉司琼注射液 盐酸氨溴索口服溶液 盐酸胺碘酮注射液 格列本脲 格列齐特片(Ⅱ) 葡萄糖 无水葡萄糖 葡萄糖氯化钠注射液 硬脂酸红霉素
药典第二增补本

药典第二增补本近日,国家药典委发布了《中国药典》2010版第二增补本,共收载新增品种288个,修订或订正品种160个,其中中药材及饮片二氧化硫残留量限度标准收入到增补本内,规定中药材及饮片(矿物来源的中药材除外,下同)中亚硫酸盐残留量(以二氧化硫计)不得过150mg/kg,山药、牛膝、粉葛、天冬、天麻、天花粉、白及、白芍、白术、党参等10种中药材及其饮片中亚硫酸盐残留量(以二氧化硫计)不得过400mg/kg国家药典委关于《中国药典》2010年版第二增补本有关增修订内容的说明根据《药典委员会章程》和国家药品标准发展的要求,为适应药品研发、生产、检验、应用以及监督管理等方面的需要,国家药典委员会及时对国家药品标准进行增修订和订正,出版《中国药典》增补本。
增补本与现行版《中国药典》具有同等的法定地位。
自2010年10月1日《中国药典》2010年版执行以来,按照《中国药典》2015年版编制大纲所确定的内容,我委于2012年出版了第一增补本。
前一阶段我委经过广泛征求意见,进一步提出了增修订内容,通过药典委员会相关专业委员会审定并经网上公示,编制了《中国药典》2010年版第二增补本。
第二增补本共收载新增品种288个,修订或订正品种160个。
其中,一部新增75个(成方制剂75个),修订或订正102个(药材17个、成方制剂85个);二部新增210个(化学药204个、辅料6个),修订或订正42个(化学药37个、辅料5个);三部新增3个(预防类1个、治疗类2个),三部修订或订正16个(预防类11个、治疗类5个)。
对《中国药典》2010年版的附录也进行了增修订,其中一部增订5个、修订或订正9个;二部增订5 个、修订或订正6个;三部增订3个、修订或订正2个。
其中,中药材及饮片二氧化硫残留量限度标准已收载进第二增补本(有关情况说明见附件)。
第二增补本的修订内容采用全文刊载方式,变动部分辅以“■ ■”标记,并分别以[修订]、[订正]、[增订]和[删除]予以标识,以利于广大药学工作者及时掌握标准修订内容和方便使用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
31
参苓白术颗粒
32
季德胜蛇药片
33
金匮肾气丸
34
金匮肾气片
35
保和片
36
保和颗粒
37
冠心苏合胶囊
38
复方丹参胶囊
39
活血止痛胶囊
40
胃苏颗粒
41
茵栀黄颗粒
42
香砂养胃丸(浓缩丸)
43
消炎利胆胶囊
44
消炎利胆颗粒
45
益母草片
46
益母草胶囊
47
通宣理肺颗粒
48
速效救心丸
49
接骨七厘片
50
清开灵颗粒
增加小蜜丸
41
益母草颗粒
增加无糖型规格
42
逍遥丸
增加小蜜丸规格
43
清开灵胶囊
增加每粒装0.40g规格。
44
清火栀麦片
增加薄膜衣规格
45
清眩丸
增加小蜜丸规格。
46
清瘟解毒丸
增加小蜜丸规格
47
羚羊清肺丸
增加小蜜丸标准
48
银杏叶胶囊
修订性状
50
麻仁滋脾丸
增加小蜜丸规格
53
黄连羊肝丸
增加小蜜丸规格
54
黄藤素片
增加薄膜衣每片重0.26g的规格。
34
复方鱼腥草片
增加薄膜衣每片重0.35g
35
复方鲜竹沥液
增加每支20ml(无蔗糖)规格,甜菊素加入量改为“适量”。
36
祖师麻片
功能与主治有变更
37
穿龙骨刺片
增加薄膜衣每片重0.5g的规格。
38
骨仙片
增加薄膜衣每片重0.41g规格
39
柴胡舒肝丸
增加小蜜丸规格
40
益母丸
增加薄膜衣规格和大片规格
55
琥珀抱龙丸
增加小蜜丸规格。
56
疏风定痛丸
增加小蜜丸规格
57
舒肝丸
增规格
58
葛根芩连片
增加薄膜衣每片重0.3g
59
跌打丸
增加小蜜丸规格
60
锁阳固精丸
增加小蜜丸规格
61
新清宁片
增薄膜衣
62
腰痛宁胶囊
更正相似度,后附马钱子粉标准
63
精制冠心片
增加薄膜衣规格。
64
藿香正气口服液
修订【鉴别】4
10
元胡止痛颗粒
11
内消瘰疬丸
12
双黄连胶囊
13
天王补心丸(浓缩丸)
14
牛黄解毒软胶囊
15
牛黄解毒胶囊
16
四神片
17
归脾合剂
18
正天丸
19
生脉颗粒(党参方)
20
伤科接骨片
21
妇科千金胶囊
22
血府逐瘀丸
23
血脂康胶囊
24
防风通圣颗粒
25
护肝胶囊
26
护肝颗粒
27
补中益气颗粒
28
附子理中片
29
乳癖消颗粒
30
11
党参
药材及其饮片品种项下增加“二氧化硫残留量”检查
项目,限度为“二氧化硫残留量不得超过400 mg/kg”。
12
粉葛
药材及其饮片品种项下增加“二氧化硫残留量”检查
项目,限度为“二氧化硫残留量不得超过400 mg/kg”。
三、修订中药材
序号
品种名称
修订项目
1
大血藤
修订【鉴别】2
2
山药
药材及其饮片品种项下增加“二氧化硫残留量”检查
项目,限度为“二氧化硫残留量不得超过400 mg/kg”。
3
干姜
修订饮片【浸出物】
4
天冬
药材及其饮片品种项下增加“二氧化硫残留量”检查
项目,限度为“二氧化硫残留量不得超过400 mg/kg”。
8
白及
药材及其饮片品种项下增加“二氧化硫残留量”检查
项目,限度为“二氧化硫残留量不得超过400 mg/kg”。
9
白术
药材及其饮片品种项下增加“二氧化硫残留量”检查
项目,限度为“二氧化硫残留量不得超过400 mg/kg”。
10
白芍
药材及其饮片品种项下增加“二氧化硫残留量”检查
项目,限度为“二氧化硫残留量不得超过400 mg/kg”。
15
伤痛宁片
增薄膜衣规格
16
再造生血片
增加薄膜衣规格
17
妇科十味片
增加薄膜衣每片重0.33g的规格。
18
导赤丸
增加水蜜丸每10丸重1g规格
19
百合固金丸
增加小蜜丸规格
20
西瓜霜润喉片
增无蔗糖规格
21
利肝隆颗粒
增加无蔗糖规格。
22
启脾丸
增加小蜜丸规格。
23
阿胶补血膏
增加每瓶装100g规格。
24
附子理中丸
关于2010年版《中国药典》第二增补本品种的公示
更新日期: 2012年4月9日下午3:42
2010年版《中国药典》第二增补本名单
一、新增中成药
1、基本药物品种已完成公示
序号
品种名称
1
小儿消积止咳口服液
2
川芎茶调片
3
川芎茶调颗粒
4
丹栀逍遥丸
5
乌鸡白凤胶囊
6
云南白药气雾剂
7
云南白药酊
8
云南白药膏
9
元胡止痛滴丸
5
天花粉
药材及其饮片品种项下增加“二氧化硫残留量”检查
项目,限度为“二氧化硫残留量不得超过400 mg/kg”。
6
天麻
药材及其饮片品种项下增加“二氧化硫残留量”检查
项目,限度为“二氧化硫残留量不得超过400 mg/kg”。
7
牛膝
药材及其饮片品种项下增加“二氧化硫残留量”检查
项目,限度为“二氧化硫残留量不得超过400 mg/kg”。
增加小蜜丸规格
25
刺五加片
增加薄膜衣每片重0.26g、0.3g的规格。
26
板蓝根颗粒
增加每袋装3g(无蔗糖,相当于饮片7g)规格。
27
郁金银屑片
增加薄膜衣规格
28
金果含片
增加薄膜衣片
29
金果饮
增加无蔗糖规格。
30
金银花露
增加无蔗糖规格。
31
保和丸
增加小蜜丸规格
32
保胎丸
增加小蜜丸规格
33
复方川贝精片
51
蛇胆川贝液
52
银黄片
53
颈舒颗粒
54
黄连上清胶囊
55
黄连上清颗粒
56
普乐安片
57
普乐安胶囊
58
舒筋活血丸
59
舒筋活血片
60
橘红片
61
橘红胶囊
2、新增品种
序号
品种名称
1
金嗓清音丸
2
保济口服液
3
脉安颗粒
4
健脾生血颗粒
二、修订中成药
序号
品种名称
修订项目
1
九味羌活颗粒
增加无蔗糖规格。
2
十全大补丸
增小蜜丸规格
3
三七伤药片(薄膜衣片)
增薄膜衣规格
4
女金丸
增加小蜜丸规格。
5
小儿咽扁颗粒
增2g规格
6
小活络丸
增水蜜丸
7
中风回春片
增加薄膜衣规格
8
中华跌打丸
增加小蜜丸规格
9
乌鸡白凤丸增制丸10源自五福化毒丸增小蜜丸规格
11
双黄连口服液(浓缩型)
增规格
12
天麻丸
增小蜜丸规格
13
牛黄上清丸
增加小蜜丸规格
14
龙胆泻肝丸
增加小蜜丸规格
