酚的分类和命名
有机化学 第7章-2
——生成氧盐 生成氧盐—— 生成氧盐
(2)醚键断裂 伯烷基醚: 伯烷基醚:
CH3CH2CH2OCH3 CH3CH2CH2OCH3 HI H CH3CH2CH2OH CH3I AgNO3 AgI I
SN2
有机分析中用此法测定甲氧基的含量(Zeisel测 有机分析中用此法测定甲氧基的含量(Zeisel测 定法)。 定法)。 芳基混醚: 芳基混醚: OH CH3 I O CH3 HI 叔丁基醚: 叔丁基醚:
——酚的物理性质 酚的物理性质—— 酚的物理性质
酚的结构 酚分子中,酚羟基的氧原子是sp2杂化 杂化, 酚分子中,酚羟基的氧原子是 杂化,形成
p-π共轭作用。由于共轭作用的影响,氧原子上的电子云密 π共轭作用。由于共轭作用的影响, 度向苯环转移,从而使C-O键较难断裂;同时使苯环上的电 键较难断裂; 度向苯环转移,从而使 键较难断裂 子云密度增高,有利于亲电取代反应。 子云密度增高,有利于亲电取代反应。
O
O
CH2 CH CH2 O Cl
3-氯-1,2-环氧丙烷
O
1,4 -环氧丁 烷 1,4 -二氧六 环 ( 二恶烷 ) (四氢呋喃)
(HTF) )
——命名 命名—— 命名
(二)物理性质 沸点:醚分子间不能形成氢键,沸点较低。 沸点:醚分子间不能形成氢键,沸点较低。 溶解度: 与水可形成分子间氢键, 溶解度: 与水可形成分子间氢键,有一定水 溶性。 能与水互溶. 溶性。HTF能与水互溶. 能与水互溶
第二节
酚
羟基直接与芳环相连的化合物为酚 羟基直接与芳环相连的化合物为酚,与侧链 相连为芳醇 芳醇。 相连为芳醇。 (一)酚的分类和命名 分类: 根据芳环上羟基的数目, 分类: 根据芳环上羟基的数目,酚可分为一元酚
第十章+酚

•
-COOH
-Cl
-NO2
11.3.2 芳环上的亲电取代反应 • 羟基是强的邻对位定位基,使苯环活化。 羟基是强的邻对位定位基,使苯环活化。 酚很容易发生卤化。 (1)卤化反应 酚很容易发生卤化。 )卤化反应—酚很容易发生卤化
•苯酚与溴水作 苯酚与溴水作 生成2,4,6用 , 生成 三溴苯酚白色 沉淀 •溴水过量,生成黄色 溴水过量, 溴水过量 的四溴苯酚析出
Cl + 2 NaOH
350~370℃,20MPa ℃ Cu催化剂 催化剂
ONa
注意反应 条件! 条件!
+ NaCl + H 2O
ONa + HCl
OH + NaCl
• 当卤原子的邻位或对位有强的吸电子基时,水解反应 当卤原子的邻位 对位有强的吸电子基时 邻位或
容易进行。 容易进行。
11.4.3 从芳磺酸制备
酚与水分子之间的氢键
酚与酚分子之间的氢键
第一节
二、酚的化学性质
酚
亲核取代反应 亲电取代反应 O H 酸性
11.3 酚的化学性质 11.3.1 酚羟基的反应 键容易离解。 (1)酚的酸性 )酚的酸性——O-H键容易离解。 键容易离解 • 极高的亲电反应活性 极高的亲电反应活性——O-H基对苯环的供电性。 基对苯环的供电性。 基对苯环的供电性
OH
CH2CH=CH2 *
Claisen重排在有机合成上具有较大价值: Claisen重排在有机合成上具有较大价值: 重排在有机合成上具有较大价值
* OCH2CH=CH2 H3CO
△
OH H3CO CH2CH=CH2 *
邻丁子香酚
(3)酯的生成 ) • 酚与酸酐或酰氯作用可得
有机化学-酚

O2N
NO2 OH NO2
0.25
(CH3)3CCH2
CH2C(CH3)3 CH2C(CH3)3
酸性极弱
pka
2,与三氯化铁的显色反应 , 多数酚能与三氯化铁溶液反应生成紫, 多数酚能与三氯化铁溶液反应生成紫,蓝,绿,棕 等颜色的化合物. 此反应可用于酚类的鉴定) 等颜色的化合物.(此反应可用于酚类的鉴定) 苯酚与三氯化铁溶液作用显紫色. 苯酚与三氯化铁溶液作用显紫色. 与三氯化铁溶液的显色反应并不限于酚,凡 与三氯化铁溶液的显色反应并不限于酚, 具有烯醇式结构的化合物( 具有烯醇式结构的化合物(—C=C—)也有此反 ) 应. OH
(1)卤代反应
酚在中性或碱性溶液中卤化,得到2,4,6酚在中性或碱性溶液中卤化,得到2,4,6-三卤苯酚 2,4,6
Br
OH + Br2Br BrOH白色(2)硝化反应 )
OH
OH
+ HNO3(20%)
-H2O 室温
NO2
+ HO
OH OH O2N NO2 NO2
NO2
+ HNO3
浓H2SO4
+ H2O
OH
O
+ H+
pKa≈10
OH + NaOH
ONa
+H2O
苯酚的酸性比碳酸弱, 苯酚的酸性比碳酸弱,它不能溶于碳酸氢钠 溶液;在苯酚钠的溶液中通入 溶液;在苯酚钠的溶液中通入CO2,可使苯酚游 离析出. 离析出.
ONa + CO + H O 2 2 OH
+NaHCO3
苯环上的取代基对酚酸性强弱的影响
OH OH
4-甲基苯酚
CH3 SO3H
酚

(四) 维生素E 又名生育酚,是一种天然存在的酚。自然界有多 种异构体( a、 、、 等),其中 a-生育酚的生 理活性最高,其结构为:
CH3 H3C HO CH3 O CH3 CH3 CH3 CH3
维生素E是一种自由基的清除剂或抗氧化剂,以 减少自由基对机体的损害。临床上用以治疗先 兆流产和习惯流产,及延缓老年早衰和记忆力 减退。
OH
稀 HNO3
OH NO2 +
OH
浓 HNO3
OH
OH O2N
NO2
NO2
NO2
又名:苦味酸,烈性炸药,也可作为染料(黄色)
3)磺化反应:
OH OH
浓H2SO4
SO3H
发烟 H2SO4
OH SO3H SO3H
OH
SO3H
(三)酚的氧化反应
OH
K2Gr2O7 + H2SO4
O
对苯醌(黄褐色)
OH
OH HO CH3
区别于: 2,4 –二甲基苯酚
CH3 H3C OH
2,4-二羟基甲苯
OH
OH
OH
OH
Cl
NO2
2,4,6-三硝基 苯酚(苦味酸)
CH3
5-甲基-1-萘酚
3-氯苯酚 苯酚 (石炭酸) 间氯苯酚
OH
OH
OH
O2N NO2
NO2
CH3
间-甲苯酚 3-甲苯酚
OH
1-萘酚(a-萘酚)
HO
第二节
酚
OH
羟基直接与芳环相连的化合物称为酚
OH
CH2CH3
OH
OH CH
一、酚的分类
1、根据芳环的不同可分为:苯酚、萘酚、蒽酚等。
酚和胺
OH
OH
-CH2- -CH2- -CH2- -CH2-
H
CH2=O H
CH2OH H
-CH2- -CH2- -CH2- -CH2-
OH
OH
OH
OH
CH2O, C6H5OH H+orOH-
OH
OH
OH
OH
-CH2- -CH2- -CH2- -CH2-
CH2
CH2
-CH2- -CH2- -CH2- -CH2-
§12-6 酚和胺
一、酚和胺的概念、分类、和命名
1、概念
(1)酚又称苯酚,羟基跟苯环直接相连的化合物;或,苯环上
的氢被羟基取代所生成的化合物;也可以看成水分子中的氢被苯 环取代形成的化合物。
苯酚的结构式和结构模型
OH
醇与酚的区别
比例模型
球棍模型
OH
苯酚
CH2 OH
苯甲醇
OH
环己醇
(2)胺:氨分子中氢原子被烃基取代而形成的化合物。
N CH3 CH3
N,N-二甲基苯胺
③复杂的胺:以烃基为母体,把氨基作为取代基命名
NH2 CH3CH CHCH2CH3
CH3 2-甲基-3-氨基戊烷
CH3 CH3CHCHNHCH3
CH3
2-甲基-3-甲氨基丁烷
④ 季铵盐和季铵碱:命名同无机铵类化合物。如:
[(CH3)3NC2H5]+Br-
溴化三甲基乙基铵
二甲胺
CH3NHC2H5
甲乙胺
CH3 C2H5 N CH(CH3)2
甲乙异丙胺
②N-取代芳香胺(即N上的氢被取代的苯胺):
一般以苯胺为母体,但要标明烃基与N相连。复杂的也可以
酚的分类和命名

(3)磺化 ——苯酚与浓硫酸作用,生成羟基苯磺酸 ——温度不同,可得到不同的一元取代产物(原因:低温为热力学控制,高温为动力学控制) ——继续磺化可得到二磺化物。
(4)傅瑞德尔—克拉夫茨反应 ——由 Nhomakorabea酚羟基的影响,酚容易发生烷基化和酰基化反应 ——烷基化时多不用AlCl3作催化剂,原因:酚羟基与三氯化铝形成配合物,使它失去催化能力。 ——二六四抗氧剂是重要的抗氧化剂和食品防腐剂
3 .从芳卤衍生物制备取代苯酚:首先在高温、高压下与碱作用成酚钠,再在硫酸作用下生成取代酚(Dow法): 评价 氯苯难进行,有强吸电子基团时吸进行亲核取代反应 4 .从芳胺制备 实验室常用 5 .从煤焦油分馏所得酚油中分离
15.6.8 酚的化学性质 概况 ——与醇有相似之处,但大多数反应与芳环有关。酚的反应既可在羟基上,也可在芳环上 ——由于苯环的影响,O-H键易断裂,酚羟基的酸性较强,但Ph-O键较不易断裂 ——注意三氯化铁的显色反应 ——羟基是较强的邻位定位基,使苯环活化,故酚的亲电取代反应较易进行
取代基对酸性的影响 ——苯环上连有供电子基时,取代苯氧负离子电荷增加,不稳定,酸性减弱 ——苯环上连有吸电子基时,取代苯氧负离子电荷降低,更稳定,酸性增强 ——示例:对甲苯酚酸性(pKa=10.14)比苯酚弱;对硝基苯酚的酸性(pKa=7.15)比苯酚强,2,4,6﹣三硝基苯酚(苦味酸)的酸性(pKa=0.71)与无机酸接近。
2. 芳环上的反应 概况 羟基是较强的邻对位定位基,可使苯环活化,酚的(亲电)取代反应比苯容易的多(苯酚溴化速率比苯快1011倍) (1)卤化 酚易与卤素反应。例,苯酚与过量溴水反应生成2,4,6﹣三溴苯酚的白色沉淀
应用 ——反应灵敏,并能定量完成,常用于酚的定性和定量分析,可检验出10mg·L-1的酚含量。(含酚污水的检测) ——卤化反应在低温或非极性溶性中,控制卤素用量,可得到一卤代酚或二卤代酚: ——水溶液中,pH=10时,与Cl2可得三氯苯酚,在三氯化铁存在下,可进一步氯化成五氯苯酚——灭钉螺药物,橡胶制品的杀菌剂
酚

酚: 羟基(―OH)直接与苯环相连的化合物
一 酚的分类和命名
(一)分类
1、按酚羟基所连芳香环分:
OH
OH
苯酚
β-萘酚
按酚羟基的数目分:
一元酚:
OH CH3
O2 N OH
二元酚:
OH
OH
OH OH
OH
OH
多元酚:
OH OH
HO OH
单宁
(二)
酚的命名
1、结构简单的酚 结构简单且芳环上连有R- , RO- , -X , -NO2 , -NH2等取代基的酚的命 名是在“酚”字前面加上苯环名称,以 此作为母体, 再冠以取代基的位次, 数 目和名称。
练习: 用化学方法区分 苯酚,乙醇,甲苯酚
溴水
苯酚
三氯化铁
苯酚,甲苯酚
白色沉淀
颜色变化
苯酚在较低的温度和非极性溶剂中(如CS2或 CCl4)进行卤代,则可得到一溴苯酚,且以对位产 物为主。
OH 2Br 2
CS2
OH
OH
Br
0℃
Br
33%
67%
(2) 硝化
苯酚的硝化在室温下即可进行,但因苯酚 易被氧化,故产率较低。
OH +
O
OH HNO3 (20%)
25℃
OH NO2 +
O
H
N
O O HO
O
N O HO
NO2
O
N
分子内氢键,熔 点较低。
分子间氢键,熔 点较高。
可用水蒸气蒸馏将二者分开。
(3) 磺化
OH
H2SO4(98%)
OH SO3H +
OH
H2SO4(98%)
酚的命名和化学性质

酚的命名和化学性质work Information Technology Company.2020YEAR酚的命名和化学性质一、命名1、只有酚OH 时,称为酚、二酚…2、-NO2,-X,-R作取代基,酚为母体3、取代基氧化度>酚OH,则酚OH作取代基氧化度=碳氧间形成的价键数O=C=O -C-O(H) -C- C-OHO O(-COOH,-CHO,-SO3H等→合体作母体,类别为苯甲酸、苯甲醛、苯磺酸等) 例题:1、OH2、OC2H5OH3、OH3C2H54、OHCH3 5、OHOHC2H5NO26、C2H5CH37、OHNO2NO2NO28、COOHOH9、CHOOCH310、OHCH3 11、CH2OH解:1、α-萘酚 2、邻乙氧基苯酚 3、3-甲基-5-乙基苯酚4、5-甲基-2-萘酚5、2-乙基-5-硝基-1, 4-苯二酚6、1-甲基-6-乙基萘7、2,4,6-三硝基苯酚(苦味酸) 8、邻羟基苯甲酸(水杨酸)9、4-羟基-2-甲氧基苯甲醛 10、对甲苯酚 11、苯甲醇(苄醇)二、酚的结构特点(一)酚中羟基直接与芳基相连,彼此存在着电子效应。
以苯酚为例:1、酚羟基对苯基的电子效应为+C >-I ,使环上ρe ↑,亲电活性↑,后取代进入邻对位;2、酚羟基与苯基存在共轭使C-O 键强↑,酚OH 难取代(有别于醇);3、酚羟基与苯基的p-π共轭使O-H 键极性↑,H +易离去而显一定酸性,且产生的Ph-O - 也因共轭而稳定性↑,因此酚的酸性>醇。
(二)酚存在烯醇结构,可与FeCl 3发生显色反应。
(三)酚因具有稳定的芳香共轭体系而可以以烯醇结构存在。
三、酚的化学性质 (一)弱酸性1、苯酚酸性>醇,可与氢氧化钠反应:C 6H 5OH +NaOHC 6H 5ONa +H 2O(石碳酸,酸性小于碳酸)2、苯酚酸性<碳酸,因此在酚钠中通入水和二氧化碳可惜出酚:ONa OH NaHCO 3+CO 2++H 23、苯酚可溶于NaOH ,不可溶于NaHCO 3,籍此可区别苯酚与其他有机酸。
化学 第二节酚
OH ︱ ︱ 凡是含有烯醇式结构(-C=C-)的化合物都能与三氯化 铁产生颜色。一般认为生成下列有色配合离子。 36 OH + FeCl3 Fe( )6 + 6H+ + 3ClO
3.氧化反应
酚很容易氧化,例如苯酚久贮,可因与空气中氧接 触而氧化。由无色至呈粉红色,红色以致深褐色。 O OH
K2Cr2O7 H2SO4
216 197 279分解
245 281 286
0.2 2.2 1.3
45.1 123 8
三、酚的化学性质
苯酚的结构: p,π–共轭体系 0.142 nm
109° H
O
sp2杂化
由于 p-π 共轭,使C-O键比醇分子中的C-O键更难 断裂; O-H键的极性显著提高,而增加了质子的离解能力; 同时由于氧原子上电子密度降低,它接受质子的能 力减弱; 芳环上电子密度增大,使亲电取代反应更易发生。
⑶当酚的芳环上连有斥电子基时,酸性减弱;连有吸电 子基时酸性增强。 如: OH
CH3 pKa 10.2 OH NO2 NO2 10.00 OH NO2 O2N NO2 0.38 8.48 OH NO2 OH
OH
Cl
pKa
7.22
4.09
2.与三氯化铁反应
大多数酚和三氯化铁溶液反应生成有色配合物,颜色从 绿到蓝、紫、红等。可用于鉴别酚类。例: 化合物 苯酚 对甲苯酚 邻苯二酚 生成颜色 紫 蓝 绿 化合物 间苯二酚 1,2,3-苯三酚 α -萘酚 生成颜色 紫 红 紫色沉淀
1.酸性
OH + H2O
+ O- + H3 O pKa = 10.00
⑴酚>醇
OH + NaOH ONa + H2O
酚(1)

Pericyclic Reactions
邻位被占则重排到对位,事实上是发生两次重排
OH
OCH3
(CH3)2SO HNO 4 HNO 3 3 H2SO H2SO 4 4
O OCH3
HNO3 H2SO4
OH
HI
?
对苯醌 O NO2
NO2
应用——保护酚羟基 ONa + Br
Cu
O
二苯醚
3 成酯和酯的反应
Pka 9.98 -I,+C
9.65 -I
10.21 -I,+C
带甲氧基的化合物比较特殊。 对位上共轭和诱导反向,共轭给诱导吸。而 首先,间位存在邻位效应,将使酸性增强。 共轭强于诱导,因此给电子,酸性变弱。间 位只有诱导吸电子,酸性变强。 (确切机理暂不明,了解即可)
比较下列取代酚的酸性:
A
B
C
酚
ArOH
Vitamin-E
一、分类和命名
二、酚的结构
三、反应
酚的酸性;酚芳环上的取代反应;酚酯的形 成和Fries重排;酚醚的形成和Claisen重排; 与三氯化铁的显色反应;Reimer-Timann
四、制备
一、分类和命名
(一)分类 sorts
苯酚
萘酚 根据酚羟基的个数也可分为一元酚、二元酚 和多元酚
将下列化合物按酸性大小排列
OH
④
OH
② NO2
OH
③ Br
CH2OH
⑤
OH
①
NO2
OH
⑥
SO3H
2 成醚和醚的反应
( 1) Williamson Ether Synthesis
(2) 克莱森重排
酚的命名汇总

OCH3 + HI OH + CH3I
ONa
+ Br
Cu 210 C
O
4、成酯:须与酸酐或酰氯作用,才能生成酯。
OH
+
OH COOH
+
(CH3CO)2O
浓 H2SO4
OCOCH3
或 CH3COCl
Cl
O C
CH3
H+
O
O C
CH3
COOH
邻羟基苯甲酸 (俗:水扬酸)
乙酰水杨酸(俗:阿斯匹林)
.OH
H+ N+ O OO
O-
O
+
N+ O-O N+ O-
OH O2N NO2 NO2 >
OH NO 2 NO 2
OH
OH
>
NO 2
~
NO2
OH
OH
>
NO2
OH
>
CH 3
2、与三氧化铁的显色反应
苯酚
蓝紫 色 邻苯二 对苯二酚 酚 暗绿色结 深绿色 晶 对甲 苯酚 蓝色
1,2,4-苯三酚
蓝绿色
连苯三酚
淡棕红色
6ArOH+FeCl3
[Fe(OAr)6]
3-
+ 3 Cl 6 H + +
除酚类外,凡具有烯醇式结构的化合物与FeCl3 也都有显色反应
C C OH
3、成醚
ONa + (CH3)2SO4
ONa +
75%
OCH3 + CH3OSO3Na
O CH3
CH3I
说明:(1)苯甲醚(俗名:大茴香醚)——配制香料
酚

+ H+
p-π共轭稳定苯氧负离子 应用:分离提纯
OH
NaOH
ONa H+
OH
OH
68
取代酚的酸性
G
O
G NH2 CH3 CH3O H Cl Br I NO2 pKa10.46 10.26 10.21 10.0 9.38 9.35 9.30 7.16
酸性增强
吸电子基使苯氧负离子稳定性提高,酸性增强 给电子基使苯氧负离子稳定性降低,酸性减弱
CS2或CCl4 0℃
HO
2.硝化反应
Br + HBr 80~84%
NO2
OH HNO3/CHCl3 15℃
OH + O2N
30%~40%
OH 15%
应用水蒸气蒸馏分离
82
O H
+ ON
O
O + ON
H O
O H
N
-O
O
分子内氢键,水溶性小, 挥发性大,水蒸气蒸馏分离
OH CO CH3
83
4
3.磺化反应
对甲苯乙醚
99
结构比较复杂的化合物,可将醚当作烃的 烷氧基取代物命名
CH3 CH3CH CHCH3
OCH3
Cl
OCH2CH3
1-乙氧基-4-氯环己烷
2-甲基-3-甲氧基丁烷
100
环醚:常以俗名来命名或按环氧烷命名
O
O
O
环氧乙烷 1,2-环氧丙烷 1,2-环氧丁烷
OO O
1,4-二氧六环 四氢呋喃(THF) (二噁烷)
69
OH NO2
O2N
OH NO2
NO2
NO2
pKa 4.09
第十一章 酚和醌
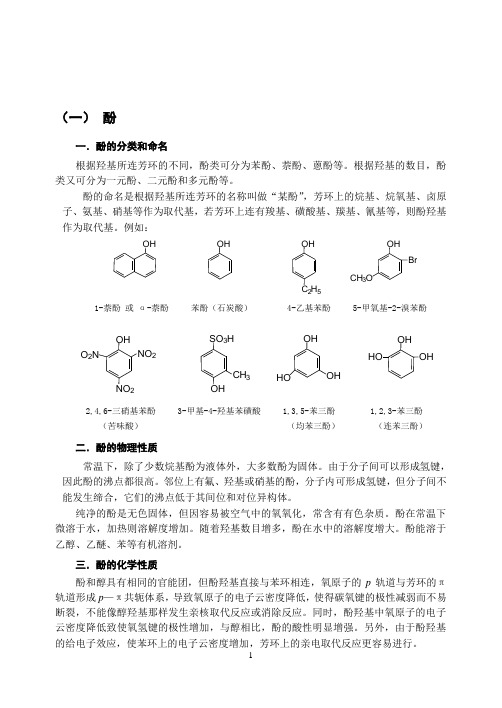
(一) 酚一.酚的分类和命名根据羟基所连芳环的不同,酚类可分为苯酚、萘酚、蒽酚等。
根据羟基的数目,酚类又可分为一元酚、二元酚和多元酚等。
酚的命名是根据羟基所连芳环的名称叫做“某酚”,芳环上的烷基、烷氧基、卤原子、氨基、硝基等作为取代基,若芳环上连有羧基、磺酸基、羰基、氰基等,则酚羟基作为取代基。
例如:1-萘酚 或 α-萘酚 苯酚(石炭酸) 4-乙基苯酚 5-甲氧基-2-溴苯酚2,4,6-三硝基苯酚 3-甲基-4-羟基苯磺酸 1,3,5-苯三酚 1,2,3-苯三酚 (苦味酸) (均苯三酚) (连苯三酚)二.酚的物理性质常温下,除了少数烷基酚为液体外,大多数酚为固体。
由于分子间可以形成氢键,因此酚的沸点都很高。
邻位上有氟、羟基或硝基的酚,分子内可形成氢键,但分子间不能发生缔合,它们的沸点低于其间位和对位异构体。
纯净的酚是无色固体,但因容易被空气中的氧氧化,常含有有色杂质。
酚在常温下微溶于水,加热则溶解度增加。
随着羟基数目增多,酚在水中的溶解度增大。
酚能溶于乙醇、乙醚、苯等有机溶剂。
三.酚的化学性质酚和醇具有相同的官能团,但酚羟基直接与苯环相连,氧原子的p 轨道与芳环的π轨道形成p —π共轭体系,导致氧原子的电子云密度降低,使得碳氧键的极性减弱而不易断裂,不能像醇羟基那样发生亲核取代反应或消除反应。
同时,酚羟基中氧原子的电子云密度降低致使氧氢键的极性增加,与醇相比,酚的酸性明显增强。
另外,由于酚羟基的给电子效应,使苯环上的电子云密度增加,芳环上的亲电取代反应更容易进行。
OH OH OH 2H 5OHBrCH 3OOHOHOHNO 2O 2N2SO 3H CH 3HOOHHOOH苯酚中p-π共轭示意图综上所述,酚的主要化学性质可归纳如下:1.酸性酚类化合物呈酸性,大多数酚的pKa 都在10左右,酸性强于水和醇,能与强碱溶液苯酚的酸性比碳酸弱,能溶于碳酸钠溶液,但不能溶于碳酸氢钠溶液,在苯酚钠的溶液中通入二氧化碳能使苯酚游离出来。
有机化学第二版第11章酚和醌

本章主要内容
1. 酚的构造、分类与命名. 2. 酚的制备方法与重要的酚. 3. 酚的化学性质及结构对性质的影响. 4. 苯醌的结构特点与性质. 5. 萘醌、蒽醌的结构特点与应用.
编辑ppt
(一)酚
11.1 酚的结构、分类和命名
◆ 酚是羟基(-OH)直接和苯环相连的化合物,官能 团为酚羟基.
Br
ArN2Cl H3+O ArOH
N2HSO4
H3+O
△ Br
OH Br
编辑ppt
1.如何从苯出发合成间苯二酚?
2.从萘出发合成 -萘酚及其衍生物?
H+
H
165℃
编辑ppt
11.3 酚的物理性质
◆酚大多数为结晶固体,微溶于水。 ◆酚分子中含有羟基,酚分子间、酚与水分子间有
氢键缔合,其沸点和溶点高于质量相近的烃. ◆邻、间、对苯二酚的熔、沸点渐高.
与羟胺反应
苯 醌 单 肟 ( wo) 与 对 亚硝基苯酚的互变
编辑ppt
互变异构体
(4)还原反应 ☺对苯醌与对苯二酚可通过还原与氧化反应互变。
(黄色) 熔点 116℃
醌氢醌(暗绿色) 171 ℃
无色
☺对苯醌与对苯二酚可生成分子络合物,称为醌氢醌,
其缓冲溶液可用作标准参比电极。
☺对苯二酚的水溶液中加入FeCl3,溶液先呈绿色,再 变棕色,最后也析出暗绿色的醌氢醌晶体。
◆碱催化先形成苯氧负离子,苯氧负离子比苯酚有 更强的亲核性.
编辑ppt
羟甲基苯氧负离子
3.醛过量时形成羟甲基较多的中间产物:
2,4--二羟甲基苯酚
2,6--二羟甲基苯酚
4.酚过量时形成不含羟甲基的中间产物:
有机化学 徐寿昌(第二版)第十一章

OH +
Na2CO3
X
利用醇、酚与NaOH和NaHCO3反应性质的不同,可鉴别和分离酚和醇。 练习:P159 一、8
酚的性质
•酚酸性的比较:
当苯环上连有吸电子基团时,酚的酸性增强; 连有供电子基团时,酚的酸性减弱。
有机化学
吸电子基团(硝基)使羟 基氧上负电荷更好地离域 移向苯环(诱导和共轭效 应),生成更稳定的对硝 基苯氧负离子,酸性增强
酚的构造、分类和命名
一元酚 二元酚
三元酚
有机化学
酚的构造、分类和命名 *带有优先序列取代基的命名:
有机化学
-COOH, -SO3H, -COOR, -COX, -CONH2, -CN, -CHO, >C=O, -OH(醇), -OH(酚), -SH, -NH2, >NH, 叁键,-C=C-, OR, -SR, -R, -X, -NO2
SO3H
OH
Cl
对羟基苯磺酸
SO3 H
HO CH3
4-甲基-5-羟基-2-氯苯磺酸
酚的构造、分类和命名
OH CH3
2-甲基苯酚
有机化学
HO
COOH
OH
O2N
CHO OH
4-羟基苯甲酸 对羟基苯甲酸
6-硝基-1-萘酚
2-羟基苯甲醛 邻羟基苯甲醛(水杨醛)
酚的制法
有机化学
从异丙苯制备
+ CH3CH=CH2 H2SO4
酚的性质
邻硝基苯酚和对硝基苯酚可用 水蒸气蒸馏方法分开
邻硝基苯酚分子形成分 子内六元环的螯和物, 对硝基苯酚只能通过分 子间的氢键缔和。
有机化学
酚的性质
下列化合物哪些能形成分子内氢键?
酚类命名 (1)

互变异构
CH2CH=CH2
OH CH2CH=CH2
如果邻位有取代基,重排将继 续到对位
完成下列反应
OCH2CH=CHCH3
OH CH3 CHCH=CH2
H3C
OCH2
OCH2CH=C(CH3)2
Cl
CH3
H3C
OH
H2C
OH
Cl
CH3
CH2CH=C(CH3)2
4、成酯:须与酸酐或酰氯作用,才能生成酯。
OH + CH3I
ONa + Br
Cu
210 C
O
Claisen 重排
OCH2CH=C* H2 200 0C
OH C*H2CH=CH2
H3C
OCH2CH=C* H2
H3C
CH3
200 0C
OH CH3
CH2CH=CH2* 相当于进行了两次Claisen 重排
Claisen重排反应历程
O
O
O H
(二)酚
一、 酚的命名
酚的命名一般根据芳烃结构的不同称为“某酚”, 并注明酚羟基的位次。
OH
OH
OH
苯酚
β-萘酚(2-萘酚)
α-蒽酚
通常作为主官能团的优先顺序为: COOH,SO3H,COOR,COX,CONH2,CN,CHO, C=O,OH(醇),OH(酚),SH,NH2, OR, C C , C=C, R,X,NO2
O Br
Br Br
黄色
用途:苯酚的定性检验和定量测定。
OH + Br2
CS2 5℃ 或CCl4
Br
OH
2)硝化反应
OH
混酸 O2N
OH
第7.2节 酚

酚ห้องสมุดไป่ตู้FeCl 酚与FeCl3显色反应机理一般认为是在溶液中 生成配合离子缘故。 生成配合离子缘故。
6C6H5OH + FeCl3 苯酚 H3[Fe(OC6H5)6] + 3HCl 六苯氧根络铁酸 蓝紫色
凡具有烯醇式结构的化合物 都有这一显色反应
OH C C OH
显色反应可鉴别酚类和具有烯醇型结构的化合物。 显色反应可鉴别酚类和具有烯醇型结构的化合物。 酚类和具有烯醇型结构的化合物
非极性溶剂 低温下
2.硝化 .
异构体
邻-硝基苯酚和对-硝基苯酚之间的分离? 硝基苯酚和对-硝基苯酚之间的分离?
低温 低极性溶剂
主要产物 61%
3. 磺化
反应在室温下进行时, 反应在室温下进行时,主产物
反应在100℃进行时, 反应在100℃进行时,主产物 100℃进行时
(四) 氧化反应 四
OH O N a 2 C r 2 O 7 /H 2 SO 4 OH O OH
甲苯酚(m-甲苯酚 甲苯酚) 间-甲苯酚 甲苯酚 甲苯酚
OH OCH3 Cl Cl 2-甲氧基苯酚
OH Cl Cl
OH O2N NO2
Cl 五氯苯酚
NO2 2,4,6-三硝基苯酚 (苦味酸)
CH 3
(3) 当分子中含有一个 当分子中含有一个-CH3,酚 羟基又在1个以上时, 羟基又在1个以上时,常以甲苯为 母体。例如: 母体。例如:
作
Book P111
(作业本) 作业本) 4(单)、5(双)、6、8 单、 双、 、 10(写出相关方程式) (写出相关方程式)
业
(自己做) 4(双)、5(单)、 7、9 自己做) 双 、 单 、 、
取代酚的酸性
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CH3CH2OH —
浓H2SO4,170 0C CH2=CH2 或Al2O3,360 0C
浓H2SO4,140 0C 或Al2O3,260 0C
CH3CH2—O—CH2CH3
在糖代谢过程中,羟基可与相邻碳原子脱水而成烯基。
H—CH—COOH HO —C—COOH
CH2—COOH
柠檬酸
-H2O +H2O
•伯醇、仲醇、叔醇的通式
伯醇 R-CH2-OH
R
仲醇
CH
OH
R’
R”
叔醇 R’—C—OH R
按
一元醇 CH3—OH
甲醇
含
羟
二元醇 CH2—OH
乙二醇基 的 数C2—OH CH2—OH目
多元醇 CH —OH
丙三醇
CH2—OH
* 2.醇的命名 对于一元醇,系统命名规则为:
1.选择含-OH的最长碳链为主链,支链 为取代基;
2.编号:保持-OH位次最小,羟基位次 标在醇前面,命为“某醇”;
3.侧链或其它基团的名称、数目和位 次写在羟基位次之前。
CH3CH2CH2CH2OH CH3CHCH2CH3
1-丁醇( 伯醇) 2-丁醇( 仲醇)
OH CH3 - CH - CH2 - OH 2-甲 基-1-丙 醇
CH3
- CH - CH - CH3 3-苯 基-2-丁醇 CH3 OH
羧酸
例如:乙醇是伯醇,可氧化(脱去两个氢原 子),而乙醛可进一步氧化成乙酸。
H CH3-C-O H
H 乙醇
H [O] CH3 -C= O
-H2O
乙醛
OH [O] CH3 -C= O
乙酸
仲醇可氧化生成相应的酮
R’ R-C-O H
H 仲醇
[O]
-H2O
O R-C—R’
酮
例如:2—丙醇是仲醇,可氧化(脱去两个氢原子) 生成丙酮。
3.对含有其它取代基的酚,如是一元酚,仍以 酚作为母体,其他基作为取代基来命名;如 是多元酚,则用芳香烃为母体,将酚性羟基 作为取代基来命名。
二、酚的化学性质
1.弱酸性:苯酚俗称“石炭酸”,酸性弱于
H2CO3。 *
苯 酚:Ka=1.28×10-10 H2CO3:Ka=4.3×10-7
CH—SH CH—SH
CH2—S CH—S
+2H+
CH—OH
HgC2+H2—OH
Hg
第二节 酚
• 苯环上的氢原子被羟基取代的化合物称 为酚。
• 酚的通式:Ar-OH
一、酚的分类和命名
(一)酚的分类
1.羟基与苯环碳相连为苯酚;与萘环碳相连为 萘酚。
萘酚
-萘酚
-萘酚
2.根据酚性羟基的数目,可分为一元酚、二元 酚、三元酚等。含有两个或两个以上酚性羟基 的统称为多元酚。
成烯烃。 *
—C—C—
催化剂 —C=C— + H2O
H OH 醇
烯
(2)分子间脱水:醇与浓硫酸或氧化铝等催化剂 共热,可发生分子间脱水而形成醚。
乙醚就是用乙醇和浓硫酸共热制得的。
CH3CH2OH + HO—CH2CH3
浓硫酸
CH3CH2—O—CH2CH3 + H2O
140 0C
反应条件对脱水方式 的影响:
CH3 CH3-C-O H
H 2—丙醇
[O]
-H2O
O CH3-C—CH3
丙酮
糖代谢中,乳酸(-羟基丙酸)在乳酸脱氢酶 催化下,可脱氢氧化生成丙酮酸。丙酮酸在乳酸脱 氢酶催化下,还可加2H重新还原成乳酸。
OH CH3-C-COOH
H
O
-2H
CH3-C—COOH
+2H
2、脱水反应
(1)分子内脱水(消除反应):醇类在适当催 化剂存在下,其碳氧键可断裂;同时,在碳原 子上消除一个氢原子。分子内失去一分子水而形
CH—COOH C—COOH CH2—COOH
顺乌头酸
3、酯化反应:醇类的羟基可以与含氧无机酸或有
机羧酸脱水成酯。 *
OH
OH
R—OH + H—O—P=O
-H2O
+H2O
OH 磷酸
R—O—P=O OH 磷酸酯
O R—O—H + HO—C—R’
有机羧酸
-H2O +H2O
O R’—C—O—R
有机酸酯
例如:甘油与磷酸可脱去一分子水而酯化成甘油酯。
CH2=CHCH2OH 2-丙烯-1-醇
二、醇的化学性质
H R-C O H
H
醇性羟基具有氧化脱氢、酯化、脱 水等重要性质。
1、氧化和脱氢反应: *
在氧化剂存在下,伯醇氧化生成相应 的醛,醛可继续氧化生成羧酸。
H R-C-O H
H 伯醇
H [O] R-C= O
-H2O 醛
OH [O] R-C= O
CH2—OH CH —OH + CH2—OH
OH H—O—P = O
OH
甘油
-H2O +H2O
CH2—OH CH—OH OH CH2—O—P=O
OH
1-磷酸甘油酯 -磷酸甘油酯
例如:乙醇与乙酸脱去一分子水,酯化成乙酸 乙酯。该反应是可逆的
O
O
CH3CH2—O H + HO —C—CH3
CH3—-HC2O—O—CH2CH 3 +H2O
三、医学上常见的醇*
1.甲醇 CH3OH:又名木精。 2.乙醇C2H5OH:俗名酒精。 3.丙三醇 CH2—CH—CH2:俗称甘油。
OH OH OH 4.苯甲醇C6H5CH2OH:又称苄醇。
5.硫醇(R—SH):—SH称为巯基,是硫醇的功能基。 CH3SH 甲硫醇 C2H5SH 乙硫醇
临床上利用硫醇(二巯基丙醇,简称BAL)与重金属盐能形成稳定的不 溶性盐的性质,把硫醇作为某些重金属中毒的解毒剂。
1,2-苯二酚 1,3-苯二酚 1,2,3-苯三酚
邻-苯二酚
间-苯二酚
连-苯三酚
(二)酚的命名*
1.对不含其它取代基的一元酚和多元酚,通常 以酚作母体,在酚名前用阿拉伯数字标出羟 基位次,并保持最小。
2.二元酚可用邻、间、对分别表示1,2位、1, 3位、1,4位;三元酚可用连、均、偏分别表 示1,2,3位、1,3,5位、1,2,4位。
•多元醇的命名:
尽可能选择包含多个羟基在内的碳链作为主链, 按所含羟基数目而称某二醇、某三醇,并在醇的 名字前标明各羟基的位次。
CH2OH
CH2OH CH2OH
乙二醇
CHOH
丙三醇, 又名:甘油
CH2OH
CH2OH CHOH
1,2-丙二醇
CH3
不饱和醇的命名: 主链应包含羟基和双键或三键在内,羟基的位 次应比双键或三键为小。
第一节 醇
❖ 醇是脂肪烃、脂环烃或芳香烃侧链上的氢原 子被羟基取代而成的化合物。
• 醇的通式:R-OH Ar-CH2-OH
一、醇的分类与命名
1.醇的分类
CH3
按 饱和醇 羟 基 所 不饱和醇 连 烃 基 脂环醇 不 同
芳香醇
CH3 - C - OH
叔醇
CH3
CH2=CH-CH2-OH
伯醇
OH
仲醇
CH2 OH
