有机化学 刑其义版 考题选编和答案PPT课件
有机化学-邢其毅课件(全)

供电子诱导效应(+ I):
O
COO
(CH 3)3C
(CH 3)2CH
CH3CH2
CH3
H
§有机化学反应的类型和试剂的分类
一、共价键的断裂方式:
1、 均裂:成键的一对电子平均分给两个原子或原子 团。均裂生成的带单电子的原子或原子团称为自由基, 或游离基。
自由基不带电荷,呈电中性。有很高的化学活性。 自由基反应:通过共价键的均裂而进行的反应。
键矩:极性共价键正或负电荷中心的电荷(q)与两 个电荷中心之间的距离(d)的乘积叫键矩(u)。
化学键的极性:以键矩又称偶极矩()来量度。
偶极矩是向量,带有方向性,一般以“ ”来表示,
箭头表示从正电荷到负电荷的方向。
Cl
多原子分子的偶极矩是分子中各个 键的偶极矩的向量和。 H Br
μ = 2.60 × 10-30 C.m
有机化学的任务
1.发现新现象(新的有机物,有机物的新的来源、 新的合成方法、合成技巧,新的有机反应等) 2.研究新的规律(结构与性质的关系,反应机理等) 3.提供新材料 (提供新的高科技材料,推动国民经 济和科学技术的发展) 4.探索生命的奥秘(生命与有机化学的结合)。
6、 学习有机化学的要求
1)、认真听课,作好笔记。 2)、勤思考、多提问,再理解的基础上记忆。 3)、学完每章,应归纳、总结。掌握该章的重点、难 点和规律。 4)、按时独立的完成作业。 5)、参阅有关的资料(参考书、杂志)。 6)、重视有机实验,以实验促进学习。
键角反映了分子的空间形象。 键矩和键的极化性反映了分子的化学反应活性,并影 响它们的物理性质。
键能:气态时原子A和原子B结合成1molA-B双原子分子(气 态)所放出的能量。通常键能愈大,键愈牢固。
邢其毅有机化学.ppt

25
• 离去基团和α氢原子必须处于反式共平面状态
使H-C-C-X四个原子在同一个平面上只有两种可能的情况
• 一种是分子取对交叉构象,进行 反式消除, • 一种是分子取重叠构象,进行顺 式消除.
对交又构象比较稳定,故卤代烷的E2消除是反式消除(anti elimination).
机理进行.
19
• 偶极溶剂有利SN2反应
在质子溶剂中进行SN2反应时, • 由于溶剂化作用,有利于离去基团的离去, • 由于亲核试剂可以被溶剂分子所包围,因此必须付出能量,先在亲 核试剂周围除掉一部分溶剂分子,才能使试剂接触底物而进行反应。 最后的影响是两种作用的共同结果.
在偶极溶剂中反应时, • 对于负离子很少溶剂化,亲核试剂一般可以不受偶极溶剂分子包围,
弱
4
若两个或多个试剂的碱性大小和可极化性大小的顺序是 相反的,亲核性大小主要取决于哪一个因素则与溶剂有关
同一族的元素,由上至下碱性减小,可极化性增大
5
溶剂对碱性和亲核性的影响
碱性决定亲核性
可极化性决定亲核性决定
6
溶剂对碱性和亲核性的影响
原因:
可极化性受溶剂的影响 不大,但碱性与溶剂的 关系很大
31
6.9.2 E2反应和SN2反应的并存与竞争
卤代烃放在碱性体系中加热,常常 会得到亲核取代和消除两种产物
32
E2机理
SN2机理
• 试剂亲核性强、碱性弱、体积小时,有利于SN2反应. • 试剂碱性强、浓度大、体积大、反应温度高时有利于E2反3应3
6. 10. E1反应
单分子消除反应用E1表示. E表示消除反应.1代表单分子 过程 • 大多数卤代烃在碱作用下的消除反应都是按E2机理进行的 • 三级卤代烷在无碱存在时的消除反应却是按E1机理进行的.
基础有机化学(邢其毅、第三版)第七章PPT

邻对位致 钝定位基
特点:
a. 都是邻对位定位基;
b.含有氧、氮原子,虽然电负性较大,产 生吸电 子的诱导效应,但是孤对电子可 以通过共轭效应共轭到环上,环上电子 云密度加大,亲电反应活性提高;
c.卤素等电负性太大,使环上电子云密度 下降,亲电反应活性下降, 但在反应过 程中可以通过共轭效应将孤对电子共轭 到环上而稳定中间体,仍是邻对位定位基
AlCl3
CH2
2
+ CH2Cl2
AlCl3
CH
3
+ CHCl3
AlCl3
C
4
+ CCl4
Cl
e. 质子酸可以催化烯烃或醇 进行付氏烷基化反应 H2SO4 + CH3CH=CH2
O O + CH3CH2CH2OHH2SO4
CHCH3 CH3
f. 如果苯环上有比卤素更强的吸电子基团,不反应
COCH3
CH2CH2CH2CH3
CH3
CHCH2CH3
CH3 C - CH3 CH3
c. 易发生多烷基化,反应不易停留在一取代 在强催化剂条件下可以发生歧化反应;
CH3
CH3
AlCl3 + CH3Br
0C
AlCl3, 0 C
CH3
2 CH3Br
CH3
CH3
CH3
CH3
CH3
2
AlCl3
CH3
+ CH3
d.多芳基化:—与多卤代烷的反应;
CH3
CH3
CH3
CH3
CH3
CH3
b.p. 144 C
139 C
138 C 偶极矩μo>μm>μp
吉林大学课件-基础有机化学(邢其毅、第三版)第16章PPT

第十六章碳水化合物概述§16.1 葡萄糖的结构一、开链结构C 6H 12O 61. HI -P 还原生成正己烷直链结构2. 与乙酸酐反应消耗5mol酸酐五个羟基3. 与HCN反应生成一元α-羟基腈一个羰基4. 与溴水反应生成一元羧酸一个醛基FischerFischer确定葡萄糖结构1. HNO3氧化得到旋光性的葡萄糖二酸(1)与(7)不符合2. 葡萄糖降解后得到(-)阿拉伯糖,用HNO3氧化得到旋光性二酸(2)、(5)与(6)不符合3. (-)阿拉伯糖升级后得到(+)葡萄糖和(+)甘露糖,二者氧化后得到旋光性糖二酸(8)不符合CH2OHHO H原来化合物,如果有另外一种己醛糖氧化生成葡萄糖二酸,则(+)葡萄糖的结构为(二、环状结构1.变旋光现象:常温水中重结晶:m.p. 145 °C,[α]D=+112 °110°C重结晶m.p. 150 °C,[α]D=+19 °放置,比旋光度逐渐变成+52.7 °2. 形成糖苷时, 只与1mol甲醇反应3. 不与NaHSO3反应HO H H OH HHO H 3CH 2OHOH H 旋转C4-C5§H§CHO COOHOHO H Br2, H2O HO HCHOCNHH OHOH§16.4 二糖和多糖一、二糖1. 麦芽糖C11H22O11水解:生成2分子葡萄糖可用α-葡萄糖苷酶水解还原糖变旋现象:[α]D =+168°[α]D=+112°变为[α]D=+136°HOH HHO H二、多糖淀粉Mw:30 000~50 000纤维素Mw:1000 000~1200 000。
基础有机化学(邢其毅、第三版)第八章PPT

§8 .卤代烃8.1 卤代烃的分类及命名8.2 化学性质I ---亲核取代反应8.3 化学性质II---亲核取代反应机理 8.4 化学性质III -消除反应8.5 化学性质IV --与金属反应8.6 化学性质V --还原反应8.7 总结8.1 卤代烃的分类及命名1、分类:A.按含卤原子的个数分类a.单卤代b.多卤代B.按卤原子所连的碳分类a. 1°(伯)卤代烷b. 2°(仲)卤代烷c. 3°(叔)卤代烷2、命名:B.8.2 化学性质I ---A.CH3CH2ONa CH CH CH OCH CH CH CH CH BrWillimenson法合成醚C.酸解反应1o or 2D.氨(胺)解反应E.氰解反应8.3 化学性质II---亲核取代反应机理SS N2反应特点:亲核试剂沿C-X键轴背面进攻,然 a.后再断裂C-X键;b.过渡态有五个基团,中心原子由 sp3杂化转化为sp2杂化;排斥力加 大,空间影响显著;c.反应后构型发生翻转;d.亲核试剂的亲核性强对反应有利。
SSS N1反应特点:C-X键首先断裂形成碳正离子;a.b.过渡态为平面结构,中心原子由sp3杂化转化为sp2杂化;c.亲核试剂可以从碳正离子两侧与之结合,生成等量的对映体,即发生消旋化d. 与亲核试剂的亲核能力无关。
S8.4Saytzerff规则:生成取代较多的烯烃B,消除反应机理及立体化学E2机理2, E2消除反应立体化学CH CH在稳定的构象中消除反式共平面的Ph3, SOH亲1. 与Na的反应A. Wurtz反应:2.绝对乙醚或THF RX (or PhX ) + MgRMgX (or PhMgX ) + HY RH(or PhH)+MgXOHTHFd.H+O RMgX (or PhMgX ) +8.6 化学性质V ---总结总结1.伯卤代烃易发生取代反应,叔卤代烃易发生消除反应;2.一级卤代烃,烯丙基(苄基)卤代烃按照S N2机理;三级卤代烃,烯丙基(苄基)卤代烃按照S N1机理;3.S N2构型反转;S N1外消旋化;4.格氏试剂用于合成各种醇。
基础有机化学(邢其毅、第三版)第一章PPT

NO2
NO2
NO2
CH3
+NO2 O-
CH3 H
NO2
CH3 H
NO2
CH3 H
NO2
CH3 H
NO2
CH3
CH3
+NO2 p-
H
NO2
CH3
CH3
H
NO2
H
NO2
CH3
H
NO2
CH3
+NO2 m-
CH3
H NO2
CH3
H NO2
CH3
CH3
H NO2
H NO2
NO2
+NO2 m-
NO2
H NO2
蛋白质,糖 (生物化学基础)
周环反应
硝基化合物, 胺,腈 (含氮有机物)
负碳离子机理 羧酸及衍生物 (酯, 酰卤, 酰胺, 酸酐)
亲核加成
醛, 酮
醇,酚,醚
卤代烷 亲核取代,消除反应 芳香烃 亲电取代 烯烃,炔烃,二烯烃 亲电加成 烷烃 自由基机理
§1.3 有机化学反应的分类
1.按反应类型分类:
不饱和度:使化合物变成开链的饱和烃, 理论上所需的氢分子的个数
3 H2
H2
2 H2
H2
C.消除反应:
由不饱和度相对较低的化合物变成不饱 和度相对较高的化合物的反应。
Br OH-
OH H2SO4
D.重排反应:
仅仅是碳骨架发生变化的反应
OCH2-CH=CH2
OH
CH2-CH=CH2 Claisen重排反应
CH2=CH-CH=CH2 ↔CH2-CH=CH-CH2
-
+
-+
↔CH2-CH=CH-CH2 ↔ CH2-CH-CH=CH2
基础有机化学(邢其毅、第三版)第2章PPT

§2. 烷烃§2.1 烷烃的结构及同分异构B、σ键的特点a, 沿键轴方向重叠b, 电子云成筒型分布c, 可以任意旋转C、化学键的有关概念a,键角: 键与键之间的夹角, 甲烷C-H键角109.5°b,键长: 成键原子核之间的距离, C-H 0.11nmc,键能: 断裂(形成)一个化学键所需要(放出)的能量, C-H 439.3 kJ/mol2.烷烃的结构A. 甲烷的结构B. 烷烃的结构每个碳都以四面体形式存在如:CH COCH与CH CH CHOB.同系物与同系列CH4中的H被-CH3取代CH3CH3CH3CH3中的H被-CH3取代CH3CH2CH3形成一个可以用C n H2n+2表示的系列 这样一系列的化合物称为同系列。
同系列中每个化合物之间互称同系物。
§2.2 烷烃的命名1.普通命名法:正-异-表示在第二个碳上有一个甲基支链。
新-把所有的烷烃都看作是甲烷的衍生物,选级别最高的碳作为甲烷的母碳,称为某某甲烷。
碳的分级及烷基的命名碳的分级:1级碳(伯碳)-与一个碳相连2级碳(仲碳)-与两个碳相连3级碳(叔碳)-与三个碳相连4级碳(季碳)-与四个碳相连C, H原子的分类与一个碳相连的碳称为一级碳,伯碳,1°C, 上面的氢为1°H;与两个碳相连的碳称为二级碳,仲碳,2°C, 上面的氢为2°H;与三个碳相连的碳称为三级碳,叔碳,3°C, 上面的氢为3°H;与四个碳相连的碳称为四级碳,季碳,4°C如:烷基的命名烷基:烷烃去掉一个氢所剩的含一个自由价的部分3.系统命名法(C.最小§2.3 烷烃的异构现象1、碳链异构C6H142. 构象异构b,锯架式:D,构象与分子能量的关系b,丁烷:§2.4 烷烃的物理性质感官性质物理性质物理常数烷烃状态C1~C4 气体C5~C16 液态各种油汽油C17以上固态煤油柴油润滑油§2.5 化学键的断裂与有机反应类型§2.6 烷烃的化学性质2.裂解:A.热裂解:>750℃R -R’→R -H + R’-HB.催化裂解:在催化剂作用下,在<450 ℃3.卤代:烷烃与卤素(重点是Cl2和Br2)在光或热作用下反应生成卤代烃的反应A.卤代反应选择性:氯代-1°:2°:3°H=1 : 3.8 : 5溴代-1°:2°:3°H=1 : 82 : 1600事实:a,丙烷卤代:CHB,活性及选择性1)活性:反应的难易程度对于烷烃:3°H > 2°H > 1°H > CH4; 对于卤素: F2>>Cl2>Br2>>I22)选择性: 反应部位的专一程度Br > Cl为什么?应用:C.机理:room temperature CH.4.烷烃的其它反应A,硝化R-H + HNO3→R -NO2+ H2O B,磺化R -H + H2SO4→RSO3H + H2O§2.7 卤代反应选择性的理论解释1) 过渡态: 反应历程中能量最高的状态2)活化能: 反应物到过渡态的能量(山有多高)活化能高反应速率小(山高爬的慢) 3) Hammond假设:过渡态的结构与近的一边类似2,溴代及氯代反应的过渡态a,过渡态更接近于左侧中间体的性质; b,CH3CH2CH3中1°H : 2°H = 6 : 2; 取代1°H更为有利;c,但CH3CH.CH3比CH3CH2CH2.稳定, 取代2°H有利。
吉林大学课件-基础有机化学(邢其毅、第三版)第13章PPT

OH NH2
Ph CH3 Ph C C CH3 -N2
OH N2+
Ph CH3 Ph C C CH3
OH
Ph
CH3
Ph C C CH3 -H+ Ph C COPh
OH CH3
CH3
OH
O HCN 1)LiAlH4 2)H2O
NaNO2 HCl
CH2NH2
O
2. 仲胺
R2NH
HCl NaNO2
R2N-N=O
PhNH-NHPh 氢化偶氮苯
PhNH-NHPh H+
H2N
NH2 70%
NH NH H+
NH2 NH2
反
应;
H2N
H
H
H2N
NH2 2+
H
H
NH2
H3C NH HN CH3
NH HN CH3
H3C H+ H2N
H3C H+ H2N
NH2 CH3
NH2
§13.3 重氮盐及其化学性质
(CH3)3CCH=CH2 + CH3OH
20%
80%
叔丁基体积大,羟基进攻β-H受阻,故进攻 甲基,发生SN2反应
CH3
CH3
H3C C CH CH2 N CH3
CH3 H
CH3
OH-
四、酰化反应
RNH2 + R'COX RNH2 + (R'CO)2O
R'CONHR + HCl R'CONHR + R'COOH
N C2H5
CH2CH=CH2
CH3
N C2H5 H2C=HCH2C
邢其毅版基础有机化学第二版--绪论有机化合物的命名ppt课件
3 CH2CH
CH3 CH3
若多原子基团的第一个连接原子相 同,则比较与它相连的其它原子,先 比较原子序数最大的原子,再比较第
CH2CH 2
CH3 CH2Cl
二大的,依次类推。若第二层次的原 子仍相同,则沿取代链依次相比,直
至比出大小为至。
Cl H
H H
CH
CH
OH
H
H
CH H
CC H
CC H
C HH H
3 命 名: 中文名称: 2,3,5-三甲基-4-丙基辛烷
英文名称: 2,3,5-trimethyl-4-n-propyloctane
最新版整理ppt
21
123
4
5
6
7
实
765
4
3
2
1
例
CH3CH2CH CH CH2 CH CH3
三
CH3 5CH2
CH3
6CH CH3
7CH3
1 确定主链:有两根等长的主链,侧链数均为三个。
异丁基 (iso)
最新版整理ppt
13
C H 3 C H 3 C H 2 C
C H 3
三级戊基 (Tert or t )
C H 3 H 3 CC
C H 3
三级丁基
C H 3 H 3 CCC H 2
C H 3
新戊基 (neo)
最新版整理ppt
14
*3 顺序规则 各种原子或取代基按先后次序排列的规则称为顺序规则。
H 3C C H C H 2 C H 2 C H 3 C H 3
CH3CHCH2CH2CH2CH3 CH3
键线式
OH
最新版整理ppt
有机化学课件邢其毅
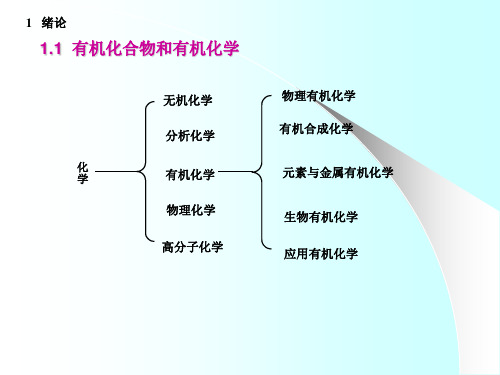
常见有机基团
中文名称
化学式
英文代号 中文名称
化学式
英文代号
甲基 丙基 丁基 叔丁基
CH3CH3CH2CH2CH3CH2CH2CH2-
(CH3)3C-
Methyl n-Propyl n-Butyl t-Butyl
vinyl propenal
Ar-
1 绪论
1.3 有机化合物的命名原则
1.3.1 有机化合物的系统命名法 1.3.1.2 化合物书写
1 书写时根据主链碳原子数目的多少进行命名。当主链碳原子数在10以内时,分 别用甲,乙,丙,丁,戊,己,庚,辛,壬,癸表示;当主链碳原子数超过10时,则直接用中 文数字表示。
的其它部分,这种作用称为诱导效应(inductive effect)。常用“I”表示 。
δδCδ
δCδ
δ
C
δCl
γ
β
α
●诱导效应通过化学键传递时,随着传递的化学键增多,诱导效应迅速减弱。 ●诱导效应是一种永久效应,它影响化合物的分子极性。 ●诱导效应的比较标准是氢原子。
给电子效应:用“+I”表示;吸电子基效应:用“-I”表示。
1 根据化合物中所含官能团的情况,确定母体.
2 选取含母体官能团的最长碳链作为主链
3 主链碳原子上其它支链全部作为取代基
4 用文字表达命名
1 绪论
1.3 有机化合物的命名原则
1.3.1 有机化合物的系统命名法
母体选择顺序(排在前面的优先)为:
-+NR3(铵) -COOH(羧酸) -SO3H(磺酸) -COOR(酯) -COX(酰卤) -CONH2(酰胺) -CN(腈) -CHO(醛) -COR(酮) -OH(醇,酚) -NH2 (胺) -R(烷基) -OR(烷氧基)
有机化学刑其义版考题选编和答案

二、填空题
填空题1 填空题3 填空题5 填空题7 填空题9
填空题2 填空题4 填空题6 填空题8 填空题10
1.化合物A的分子式为C3H6Cl2,且氯化时只能给出一种三氯
代烃。则A的结构式是
。
答案: (CH3)2CCl2
2. 化合物蔗糖的哈武斯透视式是
。
答案:
C H 2O H O
OH
OH OH O
7. 写出下列化合物的中英文名称。
CH3
H3C
N+ CH3 OH-
CH2CH3
答案: 中文名称:氢氧化乙基三甲基铵 英文名称: ethyltrimethylammonium hydroxide
8. 写出下列化合物的中英文名称。
H3CH2C
CH2CH3 N+ CH2CH3 Br-
CH2CH3
答案: 中文名称:溴化四乙铵 英文名称:tetraethylammonium bromide
Cl H
Cl
H
CH3
CH3
五、完成反应式题
完成反应式题1 完成反应式题3 完成反应式题5 完成反应式题7 完成反应式题9 完成反应式题11 完成反应式题13 完成反应式题15 完成反应式题17 完成反应式题19 完成反应式题21
完成反应式题2 完成反应式题4 完成反应式题6 完成反应式题8 完成反应式题10 完成反应式题12 完成反应式题14 完成反应式题16 完成反应式题18 完成反应式题20 完成反应式题22
题目类型 1. 给出结构简式,写出化合物的中文名称。 2. 给出结构简式,写出化合物的英文名称。 3. 给出化合物的中文名称或英文名称,写出化合物的结构简式。
考查内容 (1)母体烃的名称,官能团字首、字尾的名称,基的名称。 (2)选主链的原则,编号的原则,取代基排列次序的原则。 (3)名称的基本格式。 (4)确定R、S、Z、E、顺、反的原则。 (5)桥环和螺环化合物的命名原则。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
H O H 2 C O
H O
C H 2 O H O H
3. 核酸的基本结构单元是
。
答案:D-核糖、D-2-脱氧核糖、腺嘌呤、鸟嘌呤、 胸腺嘧啶、脲嘧啶、胞嘧啶、磷酸。
4.有一个羰基化合物,分子式为C5H10O,核磁共振谱只
有二个单峰,其结构式是
。
答案: (CH3)3CCHO
5. 下列化合物的优势构象式为
答案: C
8. 下面反应的产物是
N
H 2 O 2
(A )
N
NO2
H N O 3
(B )
P C l3NO2 NNO2(C )
N
(D )
O 2N
N
答案: B
说明:第一步是喹啉氧化成N-氧化物;第二步是喹啉N-氧化物硝化,由 于N-氧化物中的氧具有电子储存库的作用,因此亲电取代反应在杂环上进 行,基团主要进入N的对位;第三步是N-氧化物的还原。
15% H 2O 2
OH H 3O +
C H 3C O O H
5. 适宜作呋喃和吡咯的磺化试剂的是 (A)浓硫酸 (B)浓硫酸+浓硝酸 (C)稀硫酸 (D)吡啶三氧化硫加合物
答案: D 说明:呋喃在酸性条件下易开环,吡咯在酸性条件下 易聚合。所以呋喃和吡咯进行磺化反应时要用温和的 非质子的磺化试剂。
4 . 下列四种制酚的方法,哪种是经过苯炔中间体机理进行的?
SO 3Na
OH
NaOH
HCl
(A )
300oC
Cl
OH
NaOH Cu
HCl
(B )
300oC 28M Pa
+N NH SO 3-
OH
(C )
H 3O +
Br (D )
Mg 无 水THF
(C H 3O )3B -80oC
H 3O +
答案:B
答案:D 说明:葡萄糖和甘露糖是一对C2差向异构体 ,所以(A) 和(B)均不对。葡萄糖是醛糖,果糖是酮糖,不是差 向异构体,所以(C) 也不对。正确答案是D。
3. 下列哪种条件可得酚酯 (A)羧酸+酚(酸或碱催化) (B)酰氯+酚(碱催化) (C)酯交换 (D)腈+酚+水
答案:B 说明:酚有酸性,酚羟基氧的电子对与苯环共轭,在酸 性条件下酚不能发生酯化和酯交换反应。在碱性条件下, 酚形成酚盐,酚盐负离子进攻酰氯的羰基碳,经加成消除机理形成酚酯。因此正确答案是(B) 。
(七)考题选编和答案
题目选自考卷,多数题为容易题和中等难度的题, 也有较难的题。展示题目和答案的目的是让学生了解:
1.考题的类型; 2.考题的难度; 3.应如何复习书本知识; 4.建立解各类题目的基本思路; 5.掌握答题的基本要求。 所选题目不多,不可能覆盖所有的知识点,只能起 一个示范作用,希望同学举一反三。
构是
。
答案:
C H 3 C H 2 C H C H 2 O H
C H = C H 2
10. 以质量计,无水乙醇含乙醇
。
答案:99.5%
三、结构和命名题
结构和命名题1 结构和命名题3 结构和命名题5 结构和命名题7 结构和命名题9 结构和命名题11
结构和命名题2 结构和命名题4 结构和命名题6 结构和命名题8 结构和命名题10 结构和命名题12
(D)环庚三烯正离子
答案:C
说明:上述化合物中,只有吡喃环不含封闭的环状
的(4n+2)电子的共轭体系,即不符合(4n+2)规则,
所以吡喃无芳香性。
2. 下列叙述正确的是 (A)葡萄糖和甘露糖是一对互变异构体 (B)葡萄糖和甘露糖是一对C1差向异构体 (C)在碱性条件下,葡萄糖和果糖能经差向异构化互变 (D)在碱性条件下,葡萄糖和甘露糖能经差向异构化互变
题目类型
一、选择题 二、填空题 三、结构和命名题 四、立体化学题 五、完成反应式题 六、反应机理题 七、测结构题 八、合成题
一、选择题
选择题1 选择题3 选择题5 选择题7 选择题9
选择题2 选择题4 选择题6 选择题8 选择题10
1. 下列化合物没有芳香性的是
(A)吡啶
(B)环戊二烯负离子
(C)吡喃
题目类型 1. 给出结构简式,写出化合物的中文名称。 2. 给出结构简式,写出化合物的英文名称。 3. 给出化合物的中文名称或英文名称,写出化合物的结构简式。
二、填空题
填空题1 填空题3 填空题5 填空题7 填空题9
填空题2 填空题4 填空题6 填空题8 填空题10
1.化合物A的分子式为C3H6Cl2,且氯化时只能给出一种三氯
代烃。则A的结构式是
。
答案: (CH3)2CCl2
2. 化合物蔗糖的哈武斯透视式是
。
答案:
C H 2 O H O
O H
O H O H O
6.下列化合物有芳香性的是
(A)六氢吡啶
(B)四氢吡咯
(C)四氢呋喃
(D)吡啶N-氧化物
答案:D
说明:上述化合物中,只有吡啶N-氧化物含有封闭的 环状的(4n+2)电子的共轭体系,即符合(4n+2)规则。
所以正确选项为(D)。
7. 室温条件下,除去少量噻吩的方法是加入浓硫酸,震荡,分 离。其原因是 ( A )苯易溶于浓硫酸 ( B )噻吩不溶于浓硫酸 ( C )噻吩比苯易磺化,生成的噻吩磺酸溶于浓硫酸 ( D )苯比噻吩易磺化,生成的苯磺酸溶于浓硫酸
9. 萜类化合物在生物体内是下列哪种化合物合成的? (A)异戊二烯 (B)异戊烷 (C)异戊醇 (D)乙酸
答案: D
说明:尽管萜类化合物在组成上含有异戊二烯结构单元,但其在 生物体内是由乙酰类化合物合成的(乙酸在体内经过酶的作用, 转变成活化的乙酸,再经生物体内的反应转变而成)所以正确选 项是(D)。
。
H 3C
H
答案:
H
C H 3 H
6. 实验室中常用溴的四氯化碳溶液鉴定烯键,该反应
属于
。
答案: 亲电加成反应
7. 氢溴酸与3,3-二甲基-1-丁烯加成生成2,3-二甲基-2-
溴丁烷。该反应的反应过程中发生了
重排。
答案: 碳正离子
8. 2,3-丁二醇跟高碘酸反应得到
。
答案: CH3CHO
9. 分子式为 C6H12O 的手性醇,经催化氢化吸收一 分子氢后得到一个新的非手性醇。则该醇的可能结
10. 橙花油醇的构造式为(CH3)2C=CHCH2CH2C(CH3)=CHCH2OH,它 属于
(A)单萜
(B)半萜
(C)倍半萜
(D)双萜
答案:A
说明:绝大多数萜类化合物分子中的碳原子数是异戊二 烯五个碳原子的倍数,所以萜类化合物可以按碳原子数 分类。含10个碳原子即两个异戊二烯结构单元是单萜, 所以正确选项是(A)。
