氧化还原反应第一课时课件
合集下载
氧化还原反应第一课时省名师优质课赛课获奖课件市赛课一等奖课件

如 KMnO4、浓硫酸、HNO3 等。 ④过氧化物:如___H_2_O_2_、__N_a_2_O_2 ____。
17
(2)常见旳还原剂
①金属单质,如: Al、Fe、Zn 等。 ②某些非金属单质,如_H__2、__C___等。 ③低价态金属阳离子,如_F_e_2_+____等。 ④元素处于低价态时旳氧化物,如_C_O______等。
<H2O2<I-<SO2,则下列反应不能发生旳是 ( A
) A.H2O2+H2SO4=SO2↑+O2↑+22 H2O B.2Fe3++SO2+2H2O=2Fe2++4 SO +4H+ C.SO2+I2+2H2O=H2SO4+2HI D.Cl2+SO2+2H2O=H2SO4+2HCl
14
判断正误
(1)在反应 KIO3+6HI===KI+3I2+3H2O 中,每生成
HCl 被氧化,K2Cr2O7被还原。
氧化还原反应表达措施: 标电子转移方向和数目——双线桥法
1.箭头由反应物指向生成物旳同种元素
2.箭头上注明得失字样及电子数目
• 在黑火药旳爆炸反应
2KNO3+S+3C=K2S+N2↑+3CO2↑中, 化合价升高旳元素是 ,得C 电子旳原子
是
,N被、S还原旳元素是 ,N、发S 生氧
化反应旳物质是
C。
氢化钠(NaH)是一种生氢剂,可发生如下反应:NaH +H2O=NaOH+H2↑对这一反应旳描述正确旳是
A.NaH是氧化剂 B.NaH是氧化产物 C.NaOH是还原产物 D.氧化产物与还原产物旳质量比是1:1 答案:D
9
下列物质转化需要加入还原剂才干实现旳是
A.SO32- →SO2 C.Na→Na+
17
(2)常见旳还原剂
①金属单质,如: Al、Fe、Zn 等。 ②某些非金属单质,如_H__2、__C___等。 ③低价态金属阳离子,如_F_e_2_+____等。 ④元素处于低价态时旳氧化物,如_C_O______等。
<H2O2<I-<SO2,则下列反应不能发生旳是 ( A
) A.H2O2+H2SO4=SO2↑+O2↑+22 H2O B.2Fe3++SO2+2H2O=2Fe2++4 SO +4H+ C.SO2+I2+2H2O=H2SO4+2HI D.Cl2+SO2+2H2O=H2SO4+2HCl
14
判断正误
(1)在反应 KIO3+6HI===KI+3I2+3H2O 中,每生成
HCl 被氧化,K2Cr2O7被还原。
氧化还原反应表达措施: 标电子转移方向和数目——双线桥法
1.箭头由反应物指向生成物旳同种元素
2.箭头上注明得失字样及电子数目
• 在黑火药旳爆炸反应
2KNO3+S+3C=K2S+N2↑+3CO2↑中, 化合价升高旳元素是 ,得C 电子旳原子
是
,N被、S还原旳元素是 ,N、发S 生氧
化反应旳物质是
C。
氢化钠(NaH)是一种生氢剂,可发生如下反应:NaH +H2O=NaOH+H2↑对这一反应旳描述正确旳是
A.NaH是氧化剂 B.NaH是氧化产物 C.NaOH是还原产物 D.氧化产物与还原产物旳质量比是1:1 答案:D
9
下列物质转化需要加入还原剂才干实现旳是
A.SO32- →SO2 C.Na→Na+
公开课氧化还原反应第一课时课件

0
0
+1-1
H2 + Cl2 === 2 H Cl
电子对偏向,化合价降低,被还原
化合价升降的原因:电子的偏移
[结论] 氧化还原反应的实质是: 发生了电子的转移(得失或偏移)
元素化合价和电子得失的关系
化合价升高,被氧化
0
0
+1 -1
2Na + Cl2 = 2NaCl
离子化合物: 元素化合价数
= 该元素一个原子得失电子数
得到2e -,化合价降低,被还原 失去1e -,化合价升高,被氧化
0
-1
+1
Cl2 + H2O = HCl + HClO
双箭号跨过等号, 从反应物指向生成物, 起止为同一元素。
注明失去或得到 电子的总数,叙述要 完整。
得到1e -,化合价降低,被还原
课堂练习
用双线桥表示同种元素的电子得失。
失去 2e-,化合价升高,被氧化
+4
-1 +2
0
MnO2 + 4 HCl = MnCl2 + Cl2 + 2H2O
得 到2e-,化合价降低,被还原
. 氯 元素化合价升高,被 氧化 (填“氧化”或 “还原”),氧发化生 (填“氧化”或“还原”锰)
反应; .
元素还化原合价降低,被 (填
“氧化”或“还还原原”),发生
(填“氧化”
或“还原”)反应。
化合价降低的反应 得到电子的反应 (或电子对偏向)
化合价升高降 得失电子同时发生
低同时发生
(得失电子总数相等)
有化合价升降的 反应
有电子转移的反应
特征(表现)
本质
四、表示氧化还原反应的方法
氧化还原反应ppt课件

化合价降低,被还原,发生还原反应
+2
0 高温 0
+4
2CuO + C = 2Cu + CO2
有氧参与的反应
化合价升高,被氧化,发生氧化反应
一、氧化还原反应
凡有元素化合价升降的化学反应都是氧化还原反应。
化合价降低,被还原,发生还原反应
+1
0
0
+2
无氧参与的反应
化合价升高,被氧化,发生氧化反应
(2019·抚顺高一期末)下列化学反应中,不属于氧化还原反应的是
解析 A项,氧化性:Z2>W2,不符合题给信息,反应不能发生; B项,氧化性:Z2>X2,符合题给信息,反应能发生; C项,氧化性:Y2>W2,不符合题给信息,反应不能发生; D项,氧化性:X2>Z2,不符合题给信息,反应不能发生。
二、氧化性、还原性强弱比较
(3)根据反应的难易(反应条件)比较下列物质的氧化性强弱
√A.CaCO3+2HCl===CaCl2+CO2↑+H2O
B.Fe+CuSO4===Cu+FeSO4 高温
C.Fe2O3+3CO===== 2Fe+3CO2 D.2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
判断正误
(1)氧化还原反应中一定有氧元素的得失(× ) (2)氧化还原反应中得电子的物质发生还原反应(√ ) (3)氧化还原反应中所有元素的化合价都一定发生变化(× ) (4)一个反应中可以只有元素化合价升高,而无元素化合价降低(× ) (5)有单质参加的反应一定是氧化还原反应(× )
②Fe+S
△ =====
FeS
可判断氧化性:氯气__>__硫。
1.下列微粒:①Al3+ ②Cl- ③N2 ④S2- ⑧MnO-4 。既具有氧化性又具有还原性的是
+2
0 高温 0
+4
2CuO + C = 2Cu + CO2
有氧参与的反应
化合价升高,被氧化,发生氧化反应
一、氧化还原反应
凡有元素化合价升降的化学反应都是氧化还原反应。
化合价降低,被还原,发生还原反应
+1
0
0
+2
无氧参与的反应
化合价升高,被氧化,发生氧化反应
(2019·抚顺高一期末)下列化学反应中,不属于氧化还原反应的是
解析 A项,氧化性:Z2>W2,不符合题给信息,反应不能发生; B项,氧化性:Z2>X2,符合题给信息,反应能发生; C项,氧化性:Y2>W2,不符合题给信息,反应不能发生; D项,氧化性:X2>Z2,不符合题给信息,反应不能发生。
二、氧化性、还原性强弱比较
(3)根据反应的难易(反应条件)比较下列物质的氧化性强弱
√A.CaCO3+2HCl===CaCl2+CO2↑+H2O
B.Fe+CuSO4===Cu+FeSO4 高温
C.Fe2O3+3CO===== 2Fe+3CO2 D.2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
判断正误
(1)氧化还原反应中一定有氧元素的得失(× ) (2)氧化还原反应中得电子的物质发生还原反应(√ ) (3)氧化还原反应中所有元素的化合价都一定发生变化(× ) (4)一个反应中可以只有元素化合价升高,而无元素化合价降低(× ) (5)有单质参加的反应一定是氧化还原反应(× )
②Fe+S
△ =====
FeS
可判断氧化性:氯气__>__硫。
1.下列微粒:①Al3+ ②Cl- ③N2 ④S2- ⑧MnO-4 。既具有氧化性又具有还原性的是
氧化还原反应课件第1课时课件
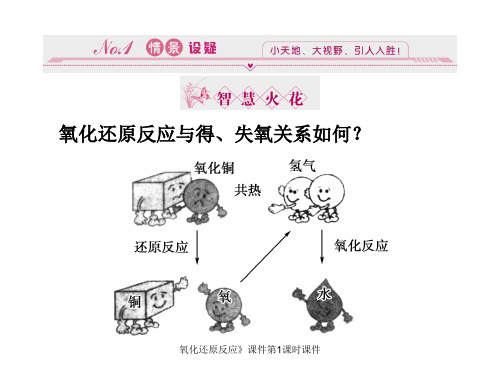
氧化还原反应》课件第1课时课件
(2)分析下列反应的化学方程式,是氧化还原 反应的用单线桥法标出电子转移的方向和数 目。 ①BaCl2+Na2SO4===BaSO4↓+2NaCl ________________________________, ②Fe+2HCl===FeCl2+H2↑ ____________________________________。
失去
6×2e-↑
答案: C
氧化还原反应》课件第1课时课件
热点实验 探究氧化还原反应在生活中的应用
[探究举例] (1)人体血红蛋白中含有Fe2+,如
果误食亚硝酸盐,会使人中毒,因为亚硝酸盐 会使Fe2+转变成Fe3+,生成高铁血红蛋白而丧 失与O2结合的能力,服用维生素C可缓解亚硝 酸盐的中毒,这说明维生素C具有________。
氧化还原反应》课件第1课时课件
氧化还原反应中电子转移的表示 (1)分析下列反应的化学方程式,是 氧化还原反应的用双线桥法标出电子转移的方 向和数目,指出被氧化和被还原的元素。 ① 2Na+Cl2=点==燃==2NaCl ______________________________________, ②NaOH+HCl===NaCl+H2O ___________________________________。
氧化还原反应》课件第1课时课件
得氧和
化合价 电子转移观
失氧观点 升降观点
点
反 氧 化 应
得氧的反应
化合价升高 的反应
失去(或偏 离)电子的
反应
还 原 反 应
失氧的反应
化合价降低 的反应
得到(或偏 向)电子的
反应
氧化还原反应》课件第1课时课件
得失(或偏
(2)分析下列反应的化学方程式,是氧化还原 反应的用单线桥法标出电子转移的方向和数 目。 ①BaCl2+Na2SO4===BaSO4↓+2NaCl ________________________________, ②Fe+2HCl===FeCl2+H2↑ ____________________________________。
失去
6×2e-↑
答案: C
氧化还原反应》课件第1课时课件
热点实验 探究氧化还原反应在生活中的应用
[探究举例] (1)人体血红蛋白中含有Fe2+,如
果误食亚硝酸盐,会使人中毒,因为亚硝酸盐 会使Fe2+转变成Fe3+,生成高铁血红蛋白而丧 失与O2结合的能力,服用维生素C可缓解亚硝 酸盐的中毒,这说明维生素C具有________。
氧化还原反应》课件第1课时课件
氧化还原反应中电子转移的表示 (1)分析下列反应的化学方程式,是 氧化还原反应的用双线桥法标出电子转移的方 向和数目,指出被氧化和被还原的元素。 ① 2Na+Cl2=点==燃==2NaCl ______________________________________, ②NaOH+HCl===NaCl+H2O ___________________________________。
氧化还原反应》课件第1课时课件
得氧和
化合价 电子转移观
失氧观点 升降观点
点
反 氧 化 应
得氧的反应
化合价升高 的反应
失去(或偏 离)电子的
反应
还 原 反 应
失氧的反应
化合价降低 的反应
得到(或偏 向)电子的
反应
氧化还原反应》课件第1课时课件
得失(或偏
化学人教版高中必修1高一化学《氧化还原反应》课件-PPT

还原剂:反应中失电子的物质,表现还原性,具 有还原能力,起还原作用。
2、氧化产物:还原剂失电子被氧化对应生成物 还原产物:氧化剂得电子被还原对应生成物 氧化剂(有氧化性)--→还原产物 还原剂(有还原性)--→氧化产物
一、常见的氧化剂和还原剂
1.常见氧化剂
(1)部分非金属单质:如 、Cl2 等O。2
CaCO3 高温 CaO+CO2
(否)
2KClMO△n3O2 2KCl+3O2
(是)
CaO+H2O Ca(OH) 2
(否)
C+O2 点燃 CO2
(是)
CuO+H△2
Cu+H2O
(是)
3C+Fe2O3 高温 2Fe+3CO2
(是)
HCl+NaOH NaCl+H2O
(否)
2HCl+CaCO3 CaCl2+H2O+CO2(否)
(2)含有高价态元素的化合物:如
HNO3、 KMnO、4 FeC等l3。
H2、SO4
2.常见还原剂 (1)活泼的金属单质,如 (2)某些非金属单质,如
Al Zn Fe
、H2 、C 等。 、 C等O。 SO2
(3)某些非金属氧化物,如 、 等。
要点一 氧化性、还原性强弱的判断
1.根据氧化还原反应方程式进行判断 在同一反应中 氧化性:氧化剂>氧化产物;还原性:还原剂>还 原产物; 如:Fe+H2SO4===FeSO4+H2↑ 氧化性:H2SO4>FeSO4,还原性:Fe>H2
四 “双线桥”法
Mg + Cl2 = MgCl2
步骤:
1.标出变价元素的化合价
2、氧化产物:还原剂失电子被氧化对应生成物 还原产物:氧化剂得电子被还原对应生成物 氧化剂(有氧化性)--→还原产物 还原剂(有还原性)--→氧化产物
一、常见的氧化剂和还原剂
1.常见氧化剂
(1)部分非金属单质:如 、Cl2 等O。2
CaCO3 高温 CaO+CO2
(否)
2KClMO△n3O2 2KCl+3O2
(是)
CaO+H2O Ca(OH) 2
(否)
C+O2 点燃 CO2
(是)
CuO+H△2
Cu+H2O
(是)
3C+Fe2O3 高温 2Fe+3CO2
(是)
HCl+NaOH NaCl+H2O
(否)
2HCl+CaCO3 CaCl2+H2O+CO2(否)
(2)含有高价态元素的化合物:如
HNO3、 KMnO、4 FeC等l3。
H2、SO4
2.常见还原剂 (1)活泼的金属单质,如 (2)某些非金属单质,如
Al Zn Fe
、H2 、C 等。 、 C等O。 SO2
(3)某些非金属氧化物,如 、 等。
要点一 氧化性、还原性强弱的判断
1.根据氧化还原反应方程式进行判断 在同一反应中 氧化性:氧化剂>氧化产物;还原性:还原剂>还 原产物; 如:Fe+H2SO4===FeSO4+H2↑ 氧化性:H2SO4>FeSO4,还原性:Fe>H2
四 “双线桥”法
Mg + Cl2 = MgCl2
步骤:
1.标出变价元素的化合价
氧化还原反应的概念ppt课件

(1) 2Al
高温
+ Fe2O3
2Fe + Al2O3
(2)Cl2 + 2NaOH
NaCl + NaClO + H2O
(3) MnO2 + 4HCl Δ MnCl2 + 2H2O + Cl2↑
失2×3e-,化合价升高,被氧化
0 +3 高温 0 +3
(1) 2Al + Fe2O3
2Fe + Al2O3
氧化性、还原性的强弱取决于物质得失电子的难易程度, 与得失电子数目的多少无关。
1.根据反应方程式来比较 “强” 制“弱”
氧化性: 氧化剂﹥氧化产物 还原性: 还原剂﹥还原产物
例1:根据下列三个氧化还原反应: (1)2 Fe3+ + 2 I- = 2Fe2+ + I2 (2)2 Fe2+ + Cl2 = 2 Fe3+ + 2Cl- 试比较:
得2×3e-,化合价降低,被还原
氧化剂: Fe2O3 还原产物: Fe
还原剂:Al 氧化产物: Al2O3
失1×e-,化合价升高,被氧化
0
(2)Cl2 + 2NaOH
-1
+1
NaCl + NaClO + H2O
得1×e-,化合价降低,被还原
氧化剂、还原剂:Cl2
还原产物:NaCl 氧化产物:NaClO
+17
Cl-
NaCl
Na+ Cl-
NaCl的形成过程示意图
12
3.从电子转移的角度认识氧化还原反应
• 金属与非金属的反应
得到2×1个电子,化合价降低2×1
《第三节_氧化还原反应》第一课时PPT课件

△
D.Ca(OH)2+CO2=CaCO3 + H2O
2、下列叙述正确的是( BD )
A、在氧化还原反应中,失去电子的物质,所含元 素化合价降低 B、凡是有元素化合价升降的化学反应都是氧 化还原反应 C、在氧化还原反应中一定所有的元素化合价 都发生变化 D、氧化还原反应的本质是电子的转移(得失 或偏移)
分层训练2:选做题
1.某元素在化学反应中由化合态(化合物) 变为游离态(单质),则该元素( C ) A.一定被氧化 B.一定被还原 C.可能被氧化,也可能被还原 D.以上都不是 2.下列变化属于氧化反应的是( BD ) A.Fe2O3 Fe B.Zn ZnCl2 C.Na2CO3 CO2 D.Al Al2O3
化合价变化本质原因分析2: 0 0 点燃 +1 -1 以HCl形成为例 H2 + Cl2 = 2HCl
H
+1
+17
Cl
HCl
共 用 电 子 对
+1
+17
化合价变化的原因:
共用电子对的偏移
+1 -1
H
Cl
H
偏离
Cl
偏向
元素化合价变化的本质原因: 电子的得失 共用电子对的偏移 氧化还原反应的本质: 电子的转移 电子的转移
化 学 反 应
氧化还原反应(有元素化合价升降) 非氧化还原反应(无元素化合价升降)
练习
判断下列反应哪些属于氧化还原反应,并 指出其属于哪种基本反应类型?
点燃
(1) 2Mg + O2 =2MgO √ 化合反应 (2) H2O + SO2 = H2SO3 × (3) 2KClO3 = √ △ 2KCl+3O2↑ △ 分解反应 × (4) Cu(OH)2 = CuO + H2O (5) Fe + 2HCl = 2FeCl2 + H2↑ √ 置换反应 (6) Fe + CuSO4 = FeSO4 + Cu √ 复 (7) Na2CO3 + 2HCl=2NaCl + H2O + CO2↑ × 分 (8) BaCl2 + Na2CO3 = BaCO3 ↓+ 升高 化合价 降低
D.Ca(OH)2+CO2=CaCO3 + H2O
2、下列叙述正确的是( BD )
A、在氧化还原反应中,失去电子的物质,所含元 素化合价降低 B、凡是有元素化合价升降的化学反应都是氧 化还原反应 C、在氧化还原反应中一定所有的元素化合价 都发生变化 D、氧化还原反应的本质是电子的转移(得失 或偏移)
分层训练2:选做题
1.某元素在化学反应中由化合态(化合物) 变为游离态(单质),则该元素( C ) A.一定被氧化 B.一定被还原 C.可能被氧化,也可能被还原 D.以上都不是 2.下列变化属于氧化反应的是( BD ) A.Fe2O3 Fe B.Zn ZnCl2 C.Na2CO3 CO2 D.Al Al2O3
化合价变化本质原因分析2: 0 0 点燃 +1 -1 以HCl形成为例 H2 + Cl2 = 2HCl
H
+1
+17
Cl
HCl
共 用 电 子 对
+1
+17
化合价变化的原因:
共用电子对的偏移
+1 -1
H
Cl
H
偏离
Cl
偏向
元素化合价变化的本质原因: 电子的得失 共用电子对的偏移 氧化还原反应的本质: 电子的转移 电子的转移
化 学 反 应
氧化还原反应(有元素化合价升降) 非氧化还原反应(无元素化合价升降)
练习
判断下列反应哪些属于氧化还原反应,并 指出其属于哪种基本反应类型?
点燃
(1) 2Mg + O2 =2MgO √ 化合反应 (2) H2O + SO2 = H2SO3 × (3) 2KClO3 = √ △ 2KCl+3O2↑ △ 分解反应 × (4) Cu(OH)2 = CuO + H2O (5) Fe + 2HCl = 2FeCl2 + H2↑ √ 置换反应 (6) Fe + CuSO4 = FeSO4 + Cu √ 复 (7) Na2CO3 + 2HCl=2NaCl + H2O + CO2↑ × 分 (8) BaCl2 + Na2CO3 = BaCO3 ↓+ 升高 化合价 降低
氧化还原反应ppt课件

VS
拉瓦锡 1743~1794 (法)
弗兰克兰 1825~1899(英)
1852年,弗兰克兰在研究金属有化合物时提出化合价的概念,并逐步得到完善后,人们把化合价升高的反应叫做氧化反应,把化合价降低的反应叫做还原反应。
得失氧的视角
化合价的视角
氧化还原反应
环节一:宏观视角,认识氧化还原反应的特征
元素水平——化合价升降的视角
氧化还原反应
环节三:宏观辨识,归纳氧化还原反应和四大基本反应类型的关系
反应前后物质的类别和数目
反应前后有无元素化合价的变化
氧化还原反应
环节三:宏观辨识,归纳氧化还原反应和四大基本反应类型的关系
氧化还原反应
非氧化还原反应
本节小结
得氧、失氧
元素(宏观视角)
元素化合价升降
电子(微观视角)
电子转移(电子得失或共用电子对的偏移)
物质水平——得失氧的视角
在一个反应中同时发生
氧化还原反应
狭义
一种物质得到氧发生氧化反应,同时另一种物质失去氧发生还原反应的反应叫氧化还原反应。
氧化还原反应
环节一:宏观视角,认识氧化还原反应的特征
元素水平——化合价升降的视角
1774年,拉瓦锡创立氧化学说(既燃烧是物质与氧气的反应)推翻了流行千年的燃素说,以解释燃烧等实验现象,指出动物的呼吸实质上是缓慢氧化。
化合价升高,
化合价降低,
氧化还原反应
环节一:宏观视角,认识氧化还原反应的特征
元素水平——化合价升降的视角
氧化还原反应
非氧化还原反应
无元素化合价变化
有元素化合价变化
氧化还原反应的特征
氧化还原反应
环节一:宏观视角,认识氧化还原反应的特征
拉瓦锡 1743~1794 (法)
弗兰克兰 1825~1899(英)
1852年,弗兰克兰在研究金属有化合物时提出化合价的概念,并逐步得到完善后,人们把化合价升高的反应叫做氧化反应,把化合价降低的反应叫做还原反应。
得失氧的视角
化合价的视角
氧化还原反应
环节一:宏观视角,认识氧化还原反应的特征
元素水平——化合价升降的视角
氧化还原反应
环节三:宏观辨识,归纳氧化还原反应和四大基本反应类型的关系
反应前后物质的类别和数目
反应前后有无元素化合价的变化
氧化还原反应
环节三:宏观辨识,归纳氧化还原反应和四大基本反应类型的关系
氧化还原反应
非氧化还原反应
本节小结
得氧、失氧
元素(宏观视角)
元素化合价升降
电子(微观视角)
电子转移(电子得失或共用电子对的偏移)
物质水平——得失氧的视角
在一个反应中同时发生
氧化还原反应
狭义
一种物质得到氧发生氧化反应,同时另一种物质失去氧发生还原反应的反应叫氧化还原反应。
氧化还原反应
环节一:宏观视角,认识氧化还原反应的特征
元素水平——化合价升降的视角
1774年,拉瓦锡创立氧化学说(既燃烧是物质与氧气的反应)推翻了流行千年的燃素说,以解释燃烧等实验现象,指出动物的呼吸实质上是缓慢氧化。
化合价升高,
化合价降低,
氧化还原反应
环节一:宏观视角,认识氧化还原反应的特征
元素水平——化合价升降的视角
氧化还原反应
非氧化还原反应
无元素化合价变化
有元素化合价变化
氧化还原反应的特征
氧化还原反应
环节一:宏观视角,认识氧化还原反应的特征
人教版化学必修一2.3氧化还原反应优秀课件PPT

( 6)被还原的元素是__H_2_S_O_4中__的__S_元__素_,
(7)1molFeS参加反应,转移电子____3___mol。
勤学勤练:
2S2- + SO32- + 6H+ = 3S↓+ 3H2O
氧化剂:__S_O_3_2_-
还原剂:__S_2_- ___
氧化产物:_S______ 还原产物:_S______
每生成1molS转移电子__1_._3_3___mol
(三)常见的氧化剂和还原剂
元素的化合价分成最高价,最低价和中间价态,元 素的最高价只有: 氧化性 最低价只有:还原性 中 间价态: 既有氧化性又有还原性 金属的化合价只 有: 正价 所以金属单质只有: 还原 性。非金属 的最高化合价一般等于 最外层电子数 最低化合价一 般等于:最高化合价-8 但是氟元素的化合价一般只 有:负一价 所以F2只有: 氧化性。
重要的氧化剂、还原剂
氧化剂
具体物质
(1)活泼非金属单质 O3、Cl2、Br2、O2
(2)高价的氧化物 NO2、CO2、MnO2
(3)高价的含氧酸 HClO、浓H2SO4、HNO3
(4)高价的盐
KMnO4、KClO3、FeCl3
(5)过氧化物
Na2O2、H2O2等
还原剂
具体物质
(1)活泼金属单质 Na、Al、Zn、Fe
记忆方法:失高氧、得低还,若说“剂” 两相反。 氧化剂本身被还原,还原剂本身被氧化。
(二)氧化还原反应中电子转移的表示方法
双线桥法 线上标出得失电子的情况及价的升降、被氧
化或被还原等内容。
1氧、化M剂nO是2:+4MHnCO2l(浓) 还原剂Cl是2↑:+MHnCCll2+2H2O 氧化产物是:Cl2 还原产物是:MnCl2 氧化剂和还原剂的物质的量之比是:_1_:__2__。 每生成2.24LCl2(标况),转移__0_._2_mol电子。
(7)1molFeS参加反应,转移电子____3___mol。
勤学勤练:
2S2- + SO32- + 6H+ = 3S↓+ 3H2O
氧化剂:__S_O_3_2_-
还原剂:__S_2_- ___
氧化产物:_S______ 还原产物:_S______
每生成1molS转移电子__1_._3_3___mol
(三)常见的氧化剂和还原剂
元素的化合价分成最高价,最低价和中间价态,元 素的最高价只有: 氧化性 最低价只有:还原性 中 间价态: 既有氧化性又有还原性 金属的化合价只 有: 正价 所以金属单质只有: 还原 性。非金属 的最高化合价一般等于 最外层电子数 最低化合价一 般等于:最高化合价-8 但是氟元素的化合价一般只 有:负一价 所以F2只有: 氧化性。
重要的氧化剂、还原剂
氧化剂
具体物质
(1)活泼非金属单质 O3、Cl2、Br2、O2
(2)高价的氧化物 NO2、CO2、MnO2
(3)高价的含氧酸 HClO、浓H2SO4、HNO3
(4)高价的盐
KMnO4、KClO3、FeCl3
(5)过氧化物
Na2O2、H2O2等
还原剂
具体物质
(1)活泼金属单质 Na、Al、Zn、Fe
记忆方法:失高氧、得低还,若说“剂” 两相反。 氧化剂本身被还原,还原剂本身被氧化。
(二)氧化还原反应中电子转移的表示方法
双线桥法 线上标出得失电子的情况及价的升降、被氧
化或被还原等内容。
1氧、化M剂nO是2:+4MHnCO2l(浓) 还原剂Cl是2↑:+MHnCCll2+2H2O 氧化产物是:Cl2 还原产物是:MnCl2 氧化剂和还原剂的物质的量之比是:_1_:__2__。 每生成2.24LCl2(标况),转移__0_._2_mol电子。
氧化还原反应ppt课件

氧化还原反应 非氧化还原反应
化学反应按照不同的分类方法可以分为不同 的反应,四大基本反应类型与氧化还原反应 什么关系?
随堂检测
1. 回答下列问题:
① CO2+C 高温 2CO ③ C+H2O(g) 高温 CO+H2 ⑤ CaCO3 高温 CaO+CO2↑
② CaO+H2O===Ca(OH)2 ④ 2H2O 电解 2H2↑+O2↑
00
2Na+Cl2
+1 -1
2NaCl
化合价降低,还原反应
化合价升降的原因:电子的得失
三、从电子转移的角度认识氧化还原反应
微观探析:以H2与Cl2反应为例
H +1 1
都可得1个e-
Cl +17 2 8 7
化合价升高,氧化反应
共用电子对
00
H2+Cl2
点燃
+1 -1
2HCl
化合价降低,还反应
化合价升降的原因:共用电 子对的偏移(偏离或偏向)
一、从得失氧的角度认识氧化还原反应
根据初中学过的氧化反应和还原反应的知识,分析以下反应:
得到氧
2Cu+O2
2CuO
➢ 铜: 得__到__氧变成了氧化铜,发生 氧___化_反应,被氧气_氧___化。
一、从得失氧的角度认识氧化还原反应
根据初中学过的氧化反应和还原反应的知识,分析以下反应:
得到氧
2CuO+H2
还原反应
化合价升高
0 +2
Fe+ CuSO4
+2
0
FeSO4+Cu
化合价降低 ➢ Fe元素:化合价升高,发生氧化反应,被氧化。
➢ Cu元素:化合价降低,发生还原反应,被还原。 虽没有物质得氧、失氧,但反应前后却有元素化合价的变化。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化合价升高
高温 0
氧化反应
+4
C + 2CuO
物质失氧
= Cu + CO2 ↑
化合价降低
还原反应
氧化反应:物质所含元素的化合价升高的反应。 还原反应:物质所含元素的化合降价低的反应。
0
+2
+2
0
Fe + CuSO4 = FeSO4 + Cu
属于氧化还原反应。
并非只有得氧、失氧才是氧化还原反应,凡 是有化合价升降的化学反应都是氧化还原反应。
1.金属与非金属的反应(钠与氯气反应)
e-
Na+ Cl-
失去
2e-
化合价升高 被氧化
2Na
0
0
+
Cl2 =
得到
2NaCl
化合价降低 被还原
+1 -1
2e-
氧化反应:原子失去电子,化合价升高,被氧化
还原反应:原子得到电子,化合价降低,被还原
2.非金属与非金属的反应(氢气与氯气的的反应)
0
0
+1 -1
H2 + Cl2 = 2HCl
氧化反应:原子偏离电子的过程 还原反应:原子偏向电子的过程
总结:氧化还原反应
初步认识 判断依据 本质
氧化反应 得氧的反应
还原反应 失氧的反应
化合价升高的 化合价降低的 反应 反应 失去(或偏离) 电子的过程 得到 (或偏向) 电子的过程
课后作业:思考氧化还原反应与四种基 本反应类型有什么关系?并尝试画出其交 叉分类示意图。
按化合价变化情况
{
氧化还原反应(反应前后化合价发生变化)
非氧化还原反应(反应前后化合价不发生变化)
判断下列反应类型:CO2+Ca(OH)2=CaCO3+H2O
Na2O + H2O = 2 NaOH
2Fe + 3Cl2 = 2FeCl3
点燃
CaO + CO2 = CaCO3
㈢从电子转移角度分析 上述反应化合价为什么发生了变化? (发生氧化还原反应的本质)
氧化反应:物质得到氧的反应 还原反应:物质失去氧的反应
氧化反应和还原反应 是否是独立发生?
物质得氧
氧化反应
C + 2CuO
物质失氧Biblioteka 高温= Cu + CO2↑
还原反应
结论:氧化反应和还原反应是同时发生的。
㈡从化合价变化角度分析 以上反应除了有得氧失氧的变化外,还有其 他的什么变化吗?
物质得氧
0 +2
氧化还原反应
Fe2O3 + 3CO = 2Fe + 3CO2
属于上述基本反应类型中的哪一类? 化合反应?分解反应?置换反应?复分解 反应?
小结:四种基本反应类型并不是都包 含了所有的反应。
㈠从物质得氧、失氧角度分析
氧化反应
点燃
C+O2 =CO2
C得到氧 变成了CO2 CuO失去
高温
还原反应 C + 2CuO = Cu + 了氧变成 CO2 ↑ 了Cu
