第一章 有机化学绪论
有机化学第一章绪论

脑白金(Melatonine)
MeO
CH2 CH2 NHAc N H
感冒药物
快克,康泰克,白加黑,康必得,速效感冒胶囊,泰诺 主要成份为对乙酰氨基酚
H N O
HO
CH3
对乙酰氨基酚
对乙酰氨基酚能抑制前列腺素的合成而产生解热作用
药物:
HO H
NO2
NO2
H NHCOCHCl 2 CH2OH
H Cl2CHCONH
(b) 碳原子的sp2杂化
(b) 碳原子的sp2杂化
120 120
府视图
(c) 碳原子的sp杂化
(b) 碳原子的sp杂化
(3) 分子轨道理论 (molecular orbital theory)
分子轨道(MO):由原子轨道线性组合而成。 成键电子在整个分子轨道中运动。
+
+
节面
反键轨道
φ1
He Ne Ar Kr Xe
Cs
Fr
Ba
Ra
La
Ac
Hf
Rf
Ta
Db
W
Sg
Re
Bh
Os
Hs
Ir
Mt
Pt
Uun
Au
Uuu
Hg
Uub
Tl
Pb
Uuq
Bi
Po
At
Rn
Ce Th
Pr Pa
Nd U
Pm
Sm
Eu
Am
Gd
Cm
Tb Bk
Dy Cf
Ho Es
Er Fm
Tm Md
Yb No
Lu Lr
Np
Pu
有机物和无机物的区別
有机化学-1 第一章 绪论

C-H键键能 (423+439+448+347)/4=414 kj/mol 键键能=( 键键能
2003-2008年 2003-2008年
2009年至今 2009年至今
1999-2003年 年 化学(师范类) 化学(师范类) 2003-2008年 年 有机合成 2009年至今 2009年至今 有机化学
安徽师范大学 理学学士 中国农业大学 理学博士 中科院大连化物所 博士后
第一章 绪论
§ 1-1 有机化学的产生和发展 § 1-2 有机化合物的分类 §1-3 有机化合物结构式的表达方式 §1-4 现代共价键理论 §1-5 共价键的断裂和有机反应的类型
4,键的极性和极化性 ,
两个不同原子形成共价键时, 两个不同原子形成共价键时,将使键产生极性 不同原子形成共价键时
δ H δ Cl H C m H Cl C =3.57X10
-30
=3.57X10-30 C m Cl
极化性:键的极性大小取决于成键的两原子电负性 极化性:
的差值,与外界条件无关, 永久的性质 的差值,与外界条件无关,是永久的性质
H3C NH2 N O
O
硝羟硝
S OH 硝磺羧 O
§1-3 有机化合物结构式的表达方式
H H C H C H H C C H CH3CHCH2CH3 CH3
农学考研之有机化学 第一章 绪论

第一节有机化合物和有机化学有机化学是化学的一个分支,它是研究有机化合物的来源、制备、结构、性能、应用以及有关理论和方法学的科学。
有机化合物的主要特征是含有碳原子,即都是含碳化合物,因此有机化学就是研究碳化合物的化学。
但少数碳的氧化物(如二氧化碳、碳酸盐等)和氰化合物(如氢氰酸、硫氰酸等),仍归属无机化合物范畴。
一、有机化学的发展有机化学作为一门科学是在十九世纪产生的,但有机化合物在生活中和生产中的应用由来已久。
最初是从天然产物中提取有效成分。
例如:从植物中提取染料、药物、香料等。
在十八世纪末,已经得到了许多纯粹的化合物如酒石酸、柠檬酸、乳酸、尿素等。
这些化合物有许多共同性质,但与当时从矿物来源得到的化合物相比,则有明显的区别。
在十九世纪初曾认为这些化合物是在生命力的作用下生成的,有别于从无生命中的矿物中得到的化合物。
因此叫做有机化合物,后者叫做无机物。
有机化合物早期的定义是“来自有生命机体的物质内”简称“有机物”。
这是因为,在化学发展的前期,无机物被大量合成,而有机物只能从动植物体获得。
如1769年从葡萄汁中取得纯的酒石酸;1773年从尿中取得尿素;1780年从酸奶中取得乳酸;1805年从鸦片中取得吗啡等。
因此,人们认为有机物是与生命现象密切相关的,是生物体内一种特殊的、神秘的“生命力”作用下产生的,只能从生物体内得到,不能人工合成。
这就是瑞典化学权威Berzelius为代表的“生命力”学说的观点。
由于人们认识局限性和对权威的迷信,“生命力”学说统治化学界达半个世纪之久,严重阻碍了有机化学的发展。
1828年德国化学家韦勒(F.W hler)将氰酸铵的水溶液加热得到了尿素:氰酸铵可以从无机物NH4Cl和氰酸钾(或银)反应生成。
此后,许多化学家也在实验室用简单的无机物做为原料,成功地合成了许多其他有机物。
如1845年colbe合成了醋酸;1854年Berthelot合成了油脂类物质等。
在大量的科学事实面前,化学家摒弃了“生命力”学说,加强了有机化合物的人工合成实践,促进了这门科学的发展。
有机化学 第1章 绪论

第一章 绪 论
【本章重点】
共价键的形成及共价键的属性、诱导效应。 【必须掌握的内容】 1. 有机化合物及有机化学。 2. 有机化合物构造式的表示方法。 3. 共价键的形成——价键法(sp3、sp2 sp杂化、σ键与π 键)和分子轨道法。 4. 共价键的基本属性及诱导效应。 5. 共价键的断键方式及有机反应中间体。 6. 有机化合物的酸碱概念。
2Cl·
△H = +242kJ / mol (
双原子分子键能也就是键的离解能;多原子分子 同类型共价键的键能,是各个键离解能的平均值。
如: CH4 +435.1 ·CH +443.5 ·CH2 +443.5 ·CH +338.9 而CH
4 3
离解能△H(kJ / mol) ·CH3 + H· ·CH2 ·CH ·C ·C + H· + H· +物通过蒸馏、结晶、吸附、
萃取、升华等操作孤立出单一纯净的有机物。
[结构] 对分离出的有机物进行化学和物理行为的了解
,阐明 其结构和特性。
[反应和合成] 从某一有机化合物(原料)经过一系列反
应转化成一已知的或新的有机化合物(产物)。
§有机化合物的特点
有机化合物的特点通常可用五个字概括: “多、燃、低、难、慢”。
△H = (435.1 + 443.5 + 443.5 + 338.9)= 1661 kJ / mol 故甲烷C-H 键的键能为:1661 / 4 = 415.3 kJ / mol 键能是指破坏或形成某一个共价键所需的平均能量。 一般来说,有机分子的键能越小,键就越活泼;键能越 大,键就比较稳定。
4. 键的极性与偶极矩 由两个电负性不同的原子组成共价键时,由 于成键的两个原子对价电子的吸引力不同,使成 键电子云在两个原子间的分布不对称,造成共价 键的正负电荷中心不重合形成极性键。
医用有机化学课件-第一章绪论(临床)

手性分子定义
不能与其镜像重合的分子。
判断方法
观察分子中是否存在手性 碳原子,若存在则分子具 有手性。
手性碳原子定义
连有四个不同基团的碳原 子。
对映异构体和非对映异构体区别
01
02
03
对映异构体
具有完全相同的物理性质 和不同的化学性质,如旋 光性、溶解性等。
非对映异构体
具有不同的物理性质和化 学性质,如沸点、熔点、 极性等。
胺类化合物的官能团,具有碱 性,可以参与酰化、烷基化等 反应。
酮基(>C=O)
酮类化合物的官能团,具有还 原性,可以参与加成、缩合等 反应。
有机反应类型和机理简介
取代反应
有机分子中的某些原子或原子团 被其他原子或原子团所取代的反 应。如酯化反应、卤代反应等。
重排反应
有机分子中的原子或原子团发生 位置重排的反应。如频哪醇重排、 贝克曼重排等。
利用立体异构原理研究蛋白质 、核酸等生物大分子的三维结 构及功能。
生物医学成像技术
利用某些具有特定立体构型的 分子作为造影剂,提高医学成
像技术的分辨率和准确性。
Part
06
医用有机化学发展趋势和挑战
新型有机合成方法和技术应用
1 2
高效、高选择性合成方法
发展高效、高选择性的有机合成方法,提高合成 效率和产物纯度,降低副产物生成。
Part
03
碳原子结构与性质
碳原子结构特点及杂化方式
碳原子结构特点
碳原子具有四个价电子,可以形 成四个共价键,是构成有机化合 物的基本骨架。
杂化方式
碳原子在形成共价键时,其价电 子可以进行sp、sp2、sp3等杂化 方式,从而形成不同形状和性质 的有机分子。
《有机化学》第一章 绪论

Sp3杂化
2P
2S 6C
2P 跃迁 2S
杂化
Sp3杂化轨道
Sp2杂化
2P 2S 6C
2P 跃迁 2S
杂化
Sp2杂化轨道
Sp2和sp3杂化轨道的形状大体相似,只是由于s成分的 逐渐增多,形状较胖,电负性较大。
Sp杂化
2P 2S 6C
2P 跃迁 2S
杂化
Sp杂化轨道
判断杂化类型的方法(第2和3章重点讲)
第一节 有机化学(Organic chemistry)发展概况
Organic一词的意思是有机的、有生命的 , 因此,有机化合物的最初定义是指来源于 动、植物体的物质 。
甘蔗------制取蔗糖; 大米或果汁----酿制酒精 植物油和草木灰共融--------制成肥皂 米醋------乙酸等称为有机物,形成“生命力论”
共价键 C--C C=C C—O C—N C--Br
键能 347.3 611 359.8 305. 4 284.5
3、键角(bond angle) 有机分子中二个共价键之间的夹角,称为键角。
4、键的极性和分子的极性
当两个相同的原子或原子团形成共价键时,由 于其电负性相同,因此成键电子云对称地分布 在两个原子周围,分子的正、负电荷中心重合, 这种键称为非极性共价键。
=dq 偶极矩的单位为德拜(Debye, Debye.Peter 荷兰物理学家), 简写为D。1D=10-8cm 10-10静电单位。
双原子分子的极性就是其键的极性,多原子分子 的极性是各个价键极性的矢量和。偶极矩是矢量,方向 从正电荷中心指向负电荷中心,可书写如下:
δ+
H
-
Cl
偶极矩 u=q•d
由于青霉素的发现和大量生产,拯救了千百万 肺炎、脑膜炎、脓肿、败血症患者的生命,及时 抢救了许多的伤病员。青霉素的出现,当时曾轰 动世界。为了表彰这一造福人类的贡献,弗莱明、 钱恩、弗罗里于1945年共同获得诺贝尔医学和生 理学奖。
有机化学 chap1-绪论

1848年—— 含碳化合物的化学 1854年
油脂
有机物 × 无机物
1874年—— 碳氢化合物及其
衍生物的化学
维勒(德国)
2020年4月17日星期五
NH4OCN(氰酸铵)
△
O NH2–C–NH2(尿素)
《有机化学》
有机化学——碳化合物的化学
1、与人类关系密切
凭什么一个C
就能成为一门 独立学科?
2、数量众多
生命科学 材料科学 环境科学 化学生物学 能源、工业、农业 ...... 等方面
1901~1998年,诺贝尔化学奖共90项,其中有机化学方面的 化学奖55项,占化学奖61%
2020年4月17日星期五
《有机化学》
1989年美国Harvard大学kishi教授等完成海 葵毒素(palytoxin) 的全合成。
Constitution(构造):指组成分子的原子或基团相互 连接的顺序。如C2H4Cl2有CH2ClCH2Cl和CH3CHCl2
2020年4月17日星期五
《有机化学》
Configuration(构型):指组成分子的原子或基团的固 有空间排列,其排列状态的改变,必须靠共价键的断 裂和新的化学键的形成。
化合 物
醛、酮 CH3–CHO CH3-C-CH3 O 羧酸和羧酸衍生物 CH3–COOH CH3-C-Cl
生 含氮 硝基化合物 CH3–NO2
物 化合
胺
CH3–NH2
物 重氮和偶氮化合物
–+N2HSO4-
杂环化合物 O 2020年4月17日星期五
S
《有机化学》
四、有机物结构表示方式——构造式 表示无机物——分子式——组成(H2O) 构造式——分子中原子的连接方式和次序。
《有机化学》第1章_绪论(高职高专 )

1.1 有机化合物和有机化学
一.有机化学(Organic Chemistry)的发展
① 1806年,Berzelius首先提出“有机化学” 概念;无机化学. ② 生命力学说:有机化合物只能来源于有机体(organic) 。 ③ 1828年, F.Wöhler从无机物氰酸铵人工合成了有机物尿素,突 破生命力学说约束,促进有机化学发展并成为一门单独学科。
特殊的共价键组成决定了上述特点。
石墨的晶体结构(sp2)
Graphite
金刚石的晶体结构(sp3)
足球烯erical
有机化合物结构上存在同分异构现象:
一.同分异构现象 分子式相同而结构相异因而其性质也各异的不同 化合物,称为同分异构体,这种现象叫同分异构现象。
A:B A·+ B·
例如:
Cl : Cl (光照) Cl·+ Cl· CH4 + Cl · CH3 ·+ H : Cl
例如: 乙醇和二甲醚(官能团异构)
CH3CH2OH CH3OCH3
CH3 CH3CHCH3
丁烷和异丁烷(碳链异构)
CH3CH2CH2CH3
原子数目和种类越多,同分异构体数越多.
碳架异构 构造异构 同分异构 立体异构 构型异构 位置异构
(丁烷与异丁烷) (1-丁烯与2-丁烯)
官能团异构 (二甲醚与乙醇) 构象异构
(2)键角(方向性):任何一个两价以上的原子,与其它原 子所形成的两个共价键之间的夹角. (3)键能 :气态原子A和气态原子B结合成气态A-B分子 所放出的能量,也就是气态分子A-B离解成A和B两个 原子(气态)时所吸收的能量.
(泛指多原子分子中几个同类型键的离解能的平均值).
◆离解能:某个共价键离解所需能量.
有机化学知识点

有机化学知识点第⼀章绪论⼀、有机化合物定义:碳氢化合物及其衍⽣物。
但是有局限性,如:NaHCO3、H2CO3、HCN是⽆机物;CCl4、:CCl2是有机物。
⼆、共价键的种类和特点键的极化:由于外加电场作⽤⽽使共价键极性发⽣改变的现象。
键的极化度:共价键发⽣极化的难易程度。
三、共价键的键参数1.键长:成键的2个原⼦原⼦核之间的距离。
常⽤单位为pm、nm。
(1pm=1×10-12m,1nm=1×10-10m)2.键⾓:分⼦中1个原⼦与另外2个原⼦形成的共价键之间的夹⾓。
单位为°。
3.键能:AB键的离解能是指当以共价键结合的双原⼦分⼦AB(⽓态)断裂成A原⼦和B 原⼦(⽓态)时,所吸收的能量。
双原⼦分⼦——键的离解能就是其键能;多原⼦分⼦——键能是同类型键的离解能的平均值。
4.键的极性:2个相同原⼦形成的共价键,没有极性,为⾮极性共价键;2个不同原⼦形成的共价键,由于原⼦的电负性不同,电⼦云靠近电负性较⼤的原⼦⼀端,使其带部分负电荷,⽽电负性较⼩的原⼦⼀端带部分正电荷,从⽽使共价键具有极性,为极性共价键。
电负性之差∝键的极性。
共价键的极性⼤⼩⽤偶极距(µ)表⽰,µ既有⼤⼩,⼜有⽅向(由正指向负)。
µ∝键的极性。
分⼦的极性既与共价键的极性有关,也与分⼦的结构有关。
四、同分异构现象分⼦式相同,但是结构不同,从⽽性质不同的现象。
五、有机化合物的分类1.按碳链结合⽅式分类1)开链化合物(⼜称为脂肪族化合物)2)碳环化合物(根据碳环中碳原⼦的成键⽅式不同,⼜可分为脂环族化合物和芳⾹族化合物)3)杂环化合物(环中的⾮碳原⼦称为杂原⼦)2.按官能团分类官能团——分⼦中⽐较容易发⽣反应的原⼦或原⼦团六、有机化合物的表⽰⽅法(了解) 1.结构式 2.结构简式 3.键线式七、有机化合物的反应类型1.按反应历程分类1)游离基反应(⼜称为⾃由基反应,共价键发⽣均裂)2)离⼦型反应(共价键发⽣异裂)2.按反应历程分类1)取代反应(分⼦中的原⼦或原⼦团被其他原⼦或原⼦代替的反应)2)加成反应(有机物与另⼀种物质作⽤⽣成1种产物的反应)3)聚合反应(由低分⼦结合成⾼分⼦的反应)4)消除反应(从1个有机物分⼦中消去1个简单分⼦⽽⽣成不饱和化合物的反应)5)重排反应(有机物因为⾃⾝稳定性差,在⼀定因素影响下,分⼦中的某些基团发⽣转移或分⼦中碳⾻架发⽣改变的反应)第⼆章饱和烃⼀、碳原⼦杂化轨道的类型⼆、有机物中C的杂化类型与共价键的构成三、烷烃(通式为C n H 2n +2,n≥1;官能团为C -C 键)1.同分异构现象 1)碳链异构2)构象异构(属于⽴体异构)2.烷烃分⼦中的碳氢原⼦的类型☆碳原⼦ 1)伯碳原⼦(只与1个碳直接相连的碳原⼦)2)仲碳原⼦(与2个碳直接相连的碳原⼦)3)叔碳原⼦(与3个碳直接相连的碳原⼦)4)季碳原⼦(与4个碳直接相连的碳原⼦)☆氢原⼦ 1)伯氢原⼦(伯碳原⼦上的氢原⼦)2)仲氢原⼦(仲碳原⼦上的氢原⼦)3)叔氢原⼦(叔碳原⼦上的氢原⼦)3.烷烃的命名 1)普通命名法(适⽤于结构简单的烷烃)碳原⼦数≤10C 的⽤“天⼲+烷”;>10C 的⽤ “中⽂数字+烷”;为区分异构体使⽤“正)、新()”。
有机化学-绪论(药学)

有机化合物和有机化学的现代定义:
有机化合物(organic compounds) — 含碳的化合物 有机化学(organic chemistry)是研究有机化合物 的结构、性能和合成方法的一门科学。
CO32-、CO2、CO、CN-、OCN-、SCN-等由于 其性质与无机物相似,习惯上仍列为无机物
: : ·· : : ··
·· · 4 H + ·C·
H·CHH···H
or
H H—C—H
H
共价键的形成过程
H·+ ·H
H·+ ·Cl:
y
y
:: ::
·· H H or H—H 电子云重叠区,吸引着 两个原子核,形成稳定 体系
H ··Cl: or H—Cl
y
x H(1s)
x Cl(2p)
x H—Cl
路易斯结构式:
H HC H
H
H
H
HC CH H C C H
Lewis 的共价键理论的优缺点: 优点:比较正确的反映了离子键和共价键的区别。 不足:没有揭示共价键的真正本质。
配位共价键:形成共价键的一对电子是由成 键的两个原子中的一个原子提供。配位键通常 用箭头 表示,指示从提供电子的原子指向 接受电子的原子。
H
109.5o
H
C
H
H
有机化合物构造式的表达方式:
凯库勒式
结构简式
H3C CH CH2 CH3
H HH HH HC C C C C H
HH HHH
CH2 CH3
CH3CHCH2CH2CH2CH3 CH3
键线式
OH
2.路易斯结构式
路易斯结构式: 用共用电子的点来表示共价 键的结构式.
徐寿昌有机化学第一章绪论

①在发展原子论方面,他发现了几种新元素:铈、 硒、钍。他还提出了新 的元素符号体系,沿用至今。
②在电化学方面,贝采利乌斯1814年提出了电化二元论:
③在有机化学方面,贝采利乌斯在1806年最早提出“有机化学”这个名称。 他发现了外消旋酒石酸,认识到同分异构现象,并命名。1835年他发现了 催化作用,并命名。
2. 易燃烧 3. 熔、沸点低,热稳定性差
室温(r.t room temperature)下,多数有机物为气体、液体或
低熔点的固体。因为有机分子间的引力主要为范德华力(Verder Waals Force),结合较弱。
4. 难溶于水,易溶于有机溶剂 5. 原子间主要以共价键结合 6. 反应速度慢,易发生副反应
拉瓦锡,法国化学家。1743年8月26日生于 巴黎,1794年5月8日卒于巴黎。1763年获法学 士学位,并取得律师开业证书,后转向研究自然 科学。21岁时从事地质学研究,后又转为学习 化学。1765年他当选为巴黎科学院候补院士。
1772年,拉瓦锡任皇家科学院副教授, 1778年提升为正教授。拉瓦锡是近代化学奠基 人之一。1774年10月,发现氧。1783年拉瓦锡 将水滴在加热的炮筒上,产生了氢气,他和H. 卡文迪什的工作确证了水不是一种元素,而是 氢和氧的化合物。1789年拉瓦锡写了《化学概 要》一书,书中为元素下了一个定义:“凡是 简单的不能分离的物质,才可以称为元素。” 他还认为少量存在的物质不是元素,例如他认 为黄金就不是元素,这也是错误的。
杂化
激发
2Px 2Py 2Pz 2s
SP3杂化轨道
杂化轨道类型:SP3 SP2
SP
几何图形:正四面体 ;平面三角形 ;直线型。
二)、分子轨道理论
大学化学《有机化学 绪论》课件

本章提纲
1.1 有机化学的产生和发展 1.2 有机化学的成就
1 学科建设 2 学术成就 3 研究思路
1.1 有机化学的产生和发展
1773年 由尿中得到了尿素。 1805年 由鸦片中得到了第一个生物碱——吗啡。 1806年Berzelius J(柏则里)首先引用“有机化学”,同时提出“生命力” 学说。 1828年Wöhler F(魏勒)用无机物氰酸铵合成了尿素。 1845年Kolbe H(柯尔柏)合成了醋酸 1848年Gmelin L(葛美林)提出“有机化学是研究碳的化学”。 1854年Berthelot M(柏塞罗)合成了油脂, Butlerov A(布特列洛夫) 合成H4CNO
NH4CNO 氰酸铵
O
H2NCNH2
尿素
Kolbe H的工作(1845年)
C + 2S CS2 + 3 Cl2
CS2 Fe
CCl4 + S2Cl2
2 CCl4
C2Cl4 + 2 Cl2
C2Cl4 + 2 H2O + Cl2
CCl3COOH + 3 HCl
CCl3COOH + 3 H2
CH3COOH + 3 HCl
1.2 有机化学的成就
1 学科建设
1 制备了上千万种的化合物 1928年(第一个),1990年(1000万种), 1999年(2443万种) 。
2 建立了一套系统鉴定和测定有机化合物的方法。 吗啡(1805年)发现,历经150年才测出它的结构,现在使用先进的 仪器,几个月、几天、几个小时就可以测定一个化合物的结构。
材料化学 由无机材料发展为无机、有机材料并重,将来有机材料将会占主导地位。
有机化学-汪小兰
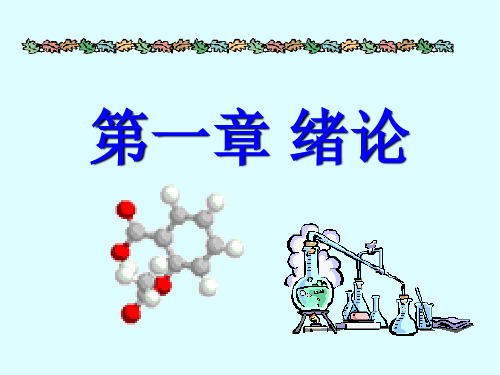
(2)碳原子的SP2杂化
2S 2Px 2Py 2Pz 激发
2Px 2Py 2Pz
2S
杂化
SP2
2Pz
SP2杂化轨道
乙烯的分子模型
每个SP2轨道由1/3S和2/3P轨道杂化组成,3个SP2轨道 在同一平面,轨道间的夹角为120°。
(3)碳原子的SP杂化
2S 2Px 2Py 2Pz 激发
2Px 2Py 2Pz
巯基
磺酸基
C2H5SH C6H5SH C6H5SO3H
乙硫醇 苯硫酚 苯磺酸
想一想 试指出结构式中官能团的名称
HO
酚羟基
H2N
氨基
N C CH3 HO
酰胺键
扑热息痛
杂环
N
SO2NH S
磺胺噻唑
磺酰胺基 -SO2-NOH-
(二)按碳架分类
1、链状化合物 (又称脂肪族)
CH3 CH2 CH2 CH3 CH3 CH2 CH2 CH2OH
4、键的极性与极化性
非极性键 (1)键的极性
极性键
H H Cl Cl
δδ
δδ
H2C Cl H Cl
组成共价键两原子电负性
(2)分子的极性 差值越大键的极性越大
Cl
Cl
Cl
C Cl
Cl
无极性
HCH H
有极性
(3)键的极化性
共价键在外电场的作用下,键的极性发生变化 称键的极性。键的极性用极化度来度量,它表 示成键电子被成键原子核约束的相对程度。极 化性与成键原子的体积、电负性和键的种类有 关外,与外电场的强度也有关系。如:
C、C间 三键相连
CC
C、C间首 位相连成环
CC CC
有机化学 第一章 第1章 绪 论

第1章绪论一、有机化学和有机化合物人类对有机化合物(organic compound)的认识,最初主要基于实用的目的。
例如,用谷物酿酒和食醋;从植物中提取染料、香料和药物等。
到18世纪末,已经得到了一系列纯粹的化合物,例如酒石酸、柠檬酸、乳酸、苹果酸等。
这些从动植物来源得到的化合物具有许多共同的性质,但与当时从矿物来源得到的化合物相比,则有明显的区别。
由于受到生产力水平的限制,在18世纪末到19世纪初,曾认为这些化合物是由动植物有机体内的“生命力”影响而形成的,故有别于从没有生命的矿物中得到的化合物。
将前者称为有机化合物,后者称为无机化合物。
“生命力”学说曾一度阻碍了有机化学的发展,尤其是减缓了有机合成的前进步伐。
给予“生命力”学说的第一次沉重打击是1928年德国年轻的化学家乌勒(Friedrich Wöhler,1802~1882)首次从无机化合物氰酸铵合成了有机化合物尿素,这也是有机合成的开端。
NH4OCN-→NH2CONH2氰酸铵尿素尿素的人工合成,突破了无机化合物与有机化合物之间的绝对界限,不仅动摇了“生命力”学说的基础,开创了有机合成的道路,而且启迪了人们的哲学思想,有助于生命科学的发展。
德国化学家拜尔(Adolf von Beyer,1835~1917)与他人合作,1870年首次合成了靛蓝。
由于他对靛蓝及其衍生物的深入研究而荣获1905年诺贝尔化学奖。
与此同时,人们又合成了大量的有机化合物。
至此,“生命力”学说彻底破产了。
此后,人们还合成了成千上万种与日常生活密切相关的染料、药品、香料、炸药等有机物。
在一个“老的自然界”旁,再放上一个远远超过它的“新的自然界”。
这也是为什么要将有机化学(organic chemistry)单独作为一个化学分支的原因之一。
因此,有机化学是直到18世纪末才开始发展起来的一门科学。
在19世纪初期,由于测定物质组成的方法的建立和发展,在测定许多有机化合物的组成时发现,它们都含有碳,是碳的化合物。
有机化学第一章 绪论

双原子分子:键能=离解能 例如:Cl2 Cl. + Cl. E=242KJ/mol. 多原子分子:键能=平均离解能,例如 :
CH4 CH3 CH2 CH CH4
CH3 + H
435.1KJ/mol
CH2 + H D2= 443.5KJ/mol
CH + H D3= 443.5KJ/mol
2020/3/2
四、有机化学的重要性 有机化学是许多现代科学技术的基础:
生命科学(生物化学,分子生物学等) 医药学(药物化学,病理学,生化分析等) 农业(农业化学,农用化学品等) 石油(石油化工等) 材料科学(高分子化学,功能材料等) 食品(食品化学,营养学,添加剂等) 日用化工(染料,涂料,化装品等)
2020/3/2
§1-3 诱导效应 一、定义
当两个原子形成共价键时、两个成键原子的 电负性大小不同,成键原子的电子云的分布偏向 电负性大的一方,产生极性共价键。例如:
δδδδ + δδδ + δδ + δ + δ CH3 CH2 CH2 CH2 Cl
由于极性键C-Cl 的影响,使得C1带部分正 电核,C2带更少的部分正电核,C3带更更少的 正电核,这种现象称为诱导效应。
C + H D4= 338.9KJ/mol
C + 4H
H=
D1+D2
4
+D3 + D4=
415.25KJ/mol
2020/3/2
4、共价键的偶极矩:在共价键中,由于成键的 两个原子的电负性大小不同,使得成键的电子云 偏向电负性大的一端,电负性大的原子具有部分 负电核δ-,电负性小的原子具有部分正电核δ+。 由此定义偶极矩:µ=q.d
有机化学-第一章绪论
4. 有机化合物结构测定
[化学方法] 官能团分析、化学降解及合成
[物理方法] 红外(IR)、紫外(UV)、核磁(NMR)、质谱 (MS)、气液色谱和X衍射等。
非常重要,先自学
如何学习有机化学
• 1 . 理解与记忆相结合,学好前几章的基础 内容,打好基础。
• 2 . 多作习题,多练习,多思考。 • 3 . 课后及时复习,巩固所学内容。 • 4 . 及时总结、比较前后所学内容之异同,
迄今已知的化合物已达几千万种(主要通过 人工合成 ),其中绝大多数是有机化合物。
4、有机化合物的特征
1)同分异构现象 2)分子组成复杂 VB12:C63H90N14PCo
C63H90N14PCo
4、有机化合物的特征
1)同分异构现象 2)分子组成复杂 VB12:C63H90N14PCo 3)熔、沸点低,易燃 4)难溶、反应速度慢 5)副反应多
以减少记忆量。 • 5 . 记化学反应式时,重点记忆官能团的转
化。
lewis酸碱反应形成配位键,产生加合物。
lewis 酸 + lewis 碱
加合物
BF3 + O(CH2CH3)2
F CH2CH3 F BO
F CH2CH3
B(CH3)3 + NH3
H3C H CH3 B N H
H3C H
•lewis酸具有亲电性,lewis碱具有亲核性。
常见的lewis酸:
BF3 AlCl3 SO3 FeCl3 SnCl4 ZnCl2 H+ Ag+ Ca2+ Cu2+ . . . . . .
2、机体的代谢过程,同样遵循有机化学 反应的活性规律。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一章 绪论 一、选择
1. 首次利用无机物合成尿素的科学家是( )。
A. 柏则里
B. 魏勒
C. 路易斯
D. 克莱门森 2. 下列路易斯结构错误的是( )。
A.
H 3C
C
B.
H 3C
CH
C.
H 3C
2 D.
N O
O 3. 根据路易斯结构, CO 分子中氧原子带有( )。
A . 正电荷 B. 负电荷 C. 不带电荷 D. 带未成对电子 4. 下列化合物的路易斯结构式出现正负电荷分离情况的是( )。
A. CO B. H 2O C. CH 2=CH 2 D. CH 3OH 5. 下列离子碱性最强的是( )。
A. F -
B. Cl -
C. Br -
D. I - 6. 下列化合物中含sp 2和sp 3杂化碳原子的是( )。
A. CH 2=CHCH 3
B. 乙炔
C. CH 2=CH-CH=CH 2
D. H 2C=C=CH 2 7. 下列化合物酸性最强的是( )。
A. HF
B. HCl
C. HBr
D. HI 8. 碳原子sp 2杂化轨道间的夹角是( )。
A. 90o B. 109.5o C. 120o D.180o 9. 共价键异裂产生( )。
A. 自由基
B. 碳正离子
C. 碳负离子
D. B 或C 10. 共价键均裂产生
A .正离子 B. 负离子 C.自由基 D.稳定的分子 11. 属于非极性分子的是( )。
A. CH 3Cl
B. CH 2Cl 2
C. CHCl 3
D. CCl 4 12. 下列化合物极性最大的是( )。
A. CCl 4
B. CH 4
C. CH 2=CH 2 D . CH 3Cl 13. 下列化合物属于路易斯酸的是( )。
A. NH 3
B. AlCl 3
C. CH 3CH 2O -
D. CH 3OCH 3 14. 属于路易斯碱的是( )。
A. AlCl 3
B. BF 3
C. FeCl 3
D. CH 3OCH 3
15. 下列化合物中所有碳原子均采取SP 2杂化的是( )。
A. CH 2=CHCH 3
B. 乙炔
C. CH 2=CH-CH=CH 2
D. H 2C=C=CH 2 16. 按共价键断裂方式的不同,有机反应类型可分为( )。
A .自由基反应和离子型反应 B.自由基反应和亲电反应 C.离子型反应和亲电反应 D. 离子型反应和亲核反应
17. 所有碳原子处于同一平面的分子是( )。
A.
CH 3CH=CHCH 2CH 3C H 2CH C CH C H 2CH CH 2CH 3CH 2CH
3A. B.C. D. B. 3CH=CHCH 2CH 3C H 2CH C CH C
H 2CH CH 2CH
3CH 2CH 3A. B.C. D. C.
3CH=CHCH 2CH 3
C H 2CH
C
CH C H 2CH CH 2CH 3CH 2CH 3
A.
B.C. D.
D.
3CH=CHCH 2CH 3
C H 2CH C
CH
C H 2CH CH 2CH 3CH 2CH 3A. B.C. D.
18. 下列碳原子的杂化状态仅为sp 2的化合物是( )。
A.
A
B C D E
CH 3CH CH 2C CH
CH CH 2
B.
B
C D E CH 3CH CH 2C CH CH CH 2 C.
B C D E CH 3CH
CH 2C CH CH CH 2 D.
B
C
D E CH 3CH CH 2
C CH
CH CH 2
19. 下列化合物属于非极性分子的是( )。
A.
CH 3CH 2
OH C H 3O CH 3
C H 3
CH COOH NH 2
C C Cl
H
H Cl
A. B.
C. D. B.
H CH 2OH C H 3O CH 3C H 3CH COOH NH 2C C
Cl H H Cl A.
B.C. D. C.
H 3CH 2
OH
C H 3O CH 3
C H 3CH COOH 2
C C Cl
H
H Cl
A.
B.C. D. D.
H 3CH 2OH C H 3O CH 3
C H 3
CH COOH
NH 2
C C
Cl
H H A. B.C. D.
20. 具有sp 和sp 2
杂化碳原子的化合物是( )。
A. B. C. D.
二、简答
1. 下列哪个化合物能与氯负离子结合?为什么? CH 4(甲烷)AlCl 3(三氯化铝)
2. 有机化合物的反应类型有几种? 答案 一、选择
1.B
2.D
3.A
4.A
5.A
6.A
7.D
8.C
9.D 10.C 11.D 12.D 13.B 14.D 15.C 16.A 17.B 18.C 19.D 20.C 二、简答
1. 三氯化铝能与氯负离子结合。
因为三氯化铝是路易斯酸,氯负离子是路易斯碱,两者能发生酸碱中和反应。
2. 按共价键的断裂方式不同,有机反应主要分为两种类型。
一种是共价键均裂的自由基反应;另一种是共价键异裂的离子型反应。
