配位化学习题(答案参考)
配位化学补充习题及答案

配位化学补充习题:1. 画出下列配合物和配合离子的几何结构:(a) [Pt(en)2]2+;(b) 顺-二水二草酸合铁(III)离子;(c) 反-二氯二联吡啶;(d) 四碘合汞(II)离子;(e) [Mo(en)3]3+;(f) 五氨一氯合钒(II)离子;(g) 顺-二氨二硫氰酸根合钯(II)。
2. Co(NH3)5(SO4)Br有两种异构体,一种为红色,另一种为紫色。
两种异构体都可溶于水形成两种离子。
红色异构体的水溶液在加入AgNO3后生成AgBr沉淀,但在加入BaCl2后没有BaSO4沉淀。
而紫色异构体具有相反的性质。
根据上述信息,写出两种异构体的结构表达式。
3. 某一锰的配合物是从溴化钾和草酸阴离子的水溶液中获得的。
经纯化并分析,发现其中含有(质量比)0.0% 锰,28.6% 钾,8.8% 碳和29.2% 溴。
配合物的其它成分是氧。
该配合物水溶液的电导性与等摩尔浓度的K4[Fe(CN)6]相同。
写出该配合物的化学式,用方括号表示配位内界。
4. 下列化合物中,中心金属原子的配位数是多少?中心原子(或离子)以什么杂化态成键?分子或离子的空间构型是什么? Ni(en)2Cl2, Fe(CO)5,[Co(NH3)6]SO4, Na[Co(EDTA)].5. 硫酸亚硝酸根五氨合钴(III)的化学式是(1)___________;(NH4)3[CrCl2(SCN)4]的学名是(2)____________;6 判断题:( (1)配位键都是由金属离子接受电子对形成的;(2)多数配离子能存在于水溶液中;(3)含两个配位原子的配体称螯合体;(4)通常情况下外轨型配合物的配位原子比内轨型配合物的配位原子的电负性大。
7. 选择题:(1)下列说法正确的是()。
(a)只有金属离子才能作为配合物的形成体;(b)配位体的数目就是形成体的配位数;(c)配离子的电荷数等于中心离子的电荷数;(d)配离子的几何构型取决于中心离子所采用的杂化轨道类型。
配位化学复习题及答案

配位化学复习题及答案配位化学是无机化学的一个重要分支,它研究金属离子与配体形成配位化合物的过程和性质。
以下是一些配位化学的复习题及答案,供参考:一、选择题1. 什么是配位化合物?A. 含有金属离子的化合物B. 含有配体的化合物C. 金属离子与配体通过配位键结合形成的化合物D. 只含有金属元素的化合物答案:C2. 配位化合物中的配位键是由什么构成的?A. 金属离子和非金属离子之间的离子键B. 金属离子和配体之间的共价键C. 金属离子提供的空轨道和配体提供的孤对电子D. 配体之间的共价键答案:C3. 下列哪个不是常见的配体?A. 水分子B. 氨分子C. 二氧化碳分子D. 硫氰酸根离子答案:C4. 配位数是指什么?A. 配体的数量B. 配位化合物中的金属离子数量C. 与中心金属离子直接相连的配体数量D. 配位化合物中的总原子数量答案:C5. 什么是内界和外界?A. 内界是配体,外界是金属离子B. 内界是金属离子,外界是配体C. 内界是配位化合物的中心,外界是配位化合物的外围D. 内界和外界都是配体答案:B二、填空题6. 配位化合物的化学式通常表示为[M(L)_n]^z+,其中M代表______,L代表______,n代表______,z代表______。
答案:中心金属离子;配体;配位数;电荷数7. 配位化合物的几何构型取决于配位数,例如,四面体、平面正方形、八面体等。
当配位数为4时,常见的几何构型是______。
答案:四面体8. 配位化合物的稳定性可以通过______来衡量,它与配体的电子供体能力有关。
答案:配位常数9. 配位化合物的光学活性是由于分子的______性造成的。
答案:手性10. 在配位化学中,硬酸和硬碱倾向于形成______,而软酸和软碱倾向于形成______。
答案:硬配位键;软配位键三、简答题11. 简述什么是配位化学中的“软硬酸碱理论”?答案:软硬酸碱理论是由R. P. Pearson提出的,它根据中心金属离子和配体的相对电负性差异,将它们分为硬酸、软酸、硬碱和软碱。
配位化学习题答案

配位化学习题答案【篇一:配位化学及答案】ss=txt>配位化学一.(12分)配位化合物a是单核配合物分子,由11个原子组成;微热后失重11.35%得到b;b进一步加热又失重26.66%(相对b)得到金属c;b极难溶于水,不溶于乙醇、乙醚,能溶于盐酸。
a有2种异构体a1、a2,其中a2能与草酸盐反应得到一种式量比a略大的配合物分子d(a1无相似反应)1.写出a、b、c的化学式;2.写出b溶于盐酸后产物的名称;3.试画出a1、a2、d的结构,并比较a1、a2在水中溶解性的大小。
4.a还有若干种实验式相同的离子化合物。
它们每个还满足如下条件:是由分立的、单核的离子配合物实体构成的;仅含1种阳离子和1种阴离子。
(1)符合上述条件的离子化合物的精确的分子式有多少种。
(2)其中1种与agno3反应(摩尔比1︰2)得到两种组成不同的配合物,写出反应的化学方程式。
二.(7分)某Ⅷ族不活泼金属a溶于足量的王水生成b的溶液(a的含量为47.60%);将so2通入b的溶液中,得到c的溶液(a的含量为57.56%)。
已知b、c的组成元素完全相同,且阴离子所带电荷也相同。
1.通过计算推理,确定a的元素符号;2.写出所涉及反应的化学方程式。
3.画出b、c阴离子的空间构型。
三.(11分)太阳能发电和阳光分解水制氮,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面。
下图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带(未充填电子的分子轨道构成的能级最低的能带)与价带(已充填价电子的分子轨道构成的能级最高的能带)+子、h为空穴。
瑞士科学家最近发明了一种基于上图所示原理的廉价光电化学电池装置,其半导体电极由2个光系统串联而成。
系统一由吸收蓝色光的wo3纳米晶薄膜构成;系统二吸收绿色和红色光,由染料敏化的tio2纳米晶薄膜构成。
在光照-下,系统一的电子(e)由价带跃迁到导带后,转移到系统二的价带,再跃迁到系统二的导带,然后流向对电极。
配位化学试题及答案

配位化学试题及答案一、选择题(每题2分,共10分)1. 配位化学中,配体与中心原子通过什么键结合?A. 离子键B. 共价键C. 配位键D. 氢键答案:C2. 以下哪个不是配位化合物的特点?A. 含有配位键B. 含有金属离子C. 含有非金属离子D. 含有配体答案:C3. 配位化学中,配位数指的是什么?A. 配体的数量B. 中心原子的电荷数C. 配体的电荷数D. 配体的价电子数答案:A4. 以下哪种配位化合物的几何构型是八面体?A. [Co(NH3)6]3+B. [Fe(CN)6]4-C. [Ni(CO)4]D. [PtCl6]2-答案:B5. 配位化学中,内球络合物与外球络合物的区别是什么?A. 配体的种类不同B. 配位键的数目不同C. 配位键的强度不同D. 配位键的类型不同答案:C二、填空题(每题2分,共10分)1. 在配位化学中,中心原子与配体之间的键被称为________。
答案:配位键2. 配位化合物的化学式中,通常用方括号表示________。
答案:配位离子3. 配位化学中,配体与中心原子之间的键角通常小于________。
答案:180度4. 配位化合物的命名中,配体的名称通常放在中心原子的名称________。
答案:之前5. 配位化学中,配体的配位能力与其________有关。
答案:电子密度三、简答题(每题5分,共10分)1. 简述配位化学中的配位键形成机制。
答案:配位键的形成机制是指配体向中心原子提供孤对电子,而中心原子提供空轨道,两者通过共享电子对形成配位键。
2. 描述一下配位化学中的几何异构现象。
答案:在配位化学中,几何异构是指具有相同化学式但不同空间排列的配位化合物。
例如,[Co(NH3)4Cl2]Cl·H2O可以存在两种不同的几何异构体:顺式和反式。
四、计算题(每题10分,共20分)1. 已知一个配位化合物的化学式为[Cu(NH3)4]SO4,计算其中心原子Cu的氧化态。
配位化学 课后习题答案

配位化学课后习题答案配位化学是化学中的一个重要分支,研究的是金属离子与配体之间的相互作用及其形成的配合物的性质。
在配位化学中,学生常常需要通过课后习题来巩固所学的知识。
本文将为大家提供一些配位化学课后习题的答案,希望能够帮助大家更好地理解和掌握这门学科。
1. 以下哪种配体不是双电子供体?答案:氨(NH3)。
氨分子中的氮原子只能提供一个孤对电子,因此它是单电子供体。
2. 以下哪种配体不是双电子受体?答案:氯(Cl-)。
氯离子中的氯原子已经满足了八个电子,不具有受体性质。
3. 对于配合物[M(H2O)6]2+,其中M代表金属离子,该配合物的配位数是多少?答案:6。
配位数是指一个金属离子周围配位体的数量,根据该配合物的化学式可知,M周围有6个水分子配位,因此配位数为6。
4. 对于配合物[Co(NH3)5Cl]Cl2,其中Co的氧化态是多少?答案:+3。
根据化学式可知,配合物中的氯离子带有-1的电荷,而Cl2带有-2的电荷,因此配合物中的Co离子需带有+3的电荷,即Co的氧化态为+3。
5. 以下哪个配体是取代型配体?答案:CN-。
取代型配体指的是能够替代配位体与金属离子形成配合物的配体,而CN-正是一种常见的取代型配体。
6. 以下哪种配合物是八面体构型?答案:[Fe(CN)6]4-。
八面体构型是指配合物中金属离子周围八个配位体呈八面体排列的结构,而[Fe(CN)6]4-正是一个典型的八面体配合物。
7. 对于配合物[PtCl4]2-,该配合物的配位键是哪种类型?答案:配位键是配体与金属离子之间的化学键,对于[PtCl4]2-,其中的Pt与Cl之间的配位键是配位键。
8. 以下哪个配合物是高自旋配合物?答案:[Fe(H2O)6]2+。
高自旋配合物是指配合物中金属离子的自旋多重度较高的配合物,而[Fe(H2O)6]2+中的Fe离子具有高自旋状态。
9. 对于配合物[Cu(NH3)4(H2O)2]2+,其中的配体是哪个?答案:配体是指与金属离子形成配合物的非金属离子或分子,对于该配合物,配体是NH3和H2O。
配位化学考研试题及答案

配位化学考研试题及答案一、选择题(每题2分,共20分)1. 下列哪项是配位化学中配体的特征?A. 能够提供孤对电子B. 能够接受孤对电子C. 能够提供空轨道D. 能够接受空轨道答案:A2. 在配位化合物中,中心离子或原子的电荷数与配位数的乘积称为?A. 配位数B. 配位数C. 配位能力D. 配位价答案:D3. 配位化合物的几何构型通常由什么决定?A. 中心离子的大小B. 配体的类型C. 配位数D. 以上都是答案:D4. 配位化合物的稳定性主要取决于什么?A. 配体的类型B. 中心离子的电荷C. 配位数D. 配位化合物的几何构型答案:A5. 配位化合物中,配体与中心离子之间的键被称为?A. 离子键B. 共价键C. 配位键D. 金属键答案:C6. 下列哪种类型的配体是硬酸?A. 氨B. 硫氰酸根C. 碘离子D. 溴离子答案:A7. 硬碱和硬酸之间的相互作用被称为?A. 软相互作用B. 硬相互作用C. 软硬相互作用D. 非相互作用答案:B8. 配位化学中,哪种类型的配体可以提供多个孤对电子?A. 单齿配体B. 双齿配体C. 多齿配体D. 桥联配体答案:C9. 配位化合物中,中心离子的氧化态通常由什么决定?A. 配体的类型B. 中心离子的电子构型C. 配位数D. 配位化合物的几何构型答案:B10. 配位化学中,哪种类型的配体可以作为桥联配体?A. 单齿配体B. 双齿配体C. 多齿配体D. 所有类型的配体答案:C二、填空题(每题2分,共20分)1. 配位化合物中,中心离子或原子的电荷数与配位数的乘积称为配位价。
2. 配位化合物的稳定性主要取决于配体的类型。
3. 硬碱和硬酸之间的相互作用被称为硬相互作用。
4. 配位化合物中,中心离子的氧化态通常由中心离子的电子构型决定。
5. 配位化合物的几何构型通常由配位数决定。
6. 配位化学中,多齿配体可以作为桥联配体。
7. 配位化合物中,配体与中心离子之间的键被称为配位键。
配位化学试题及答案

配位化学试题及答案一、选择题(每题2分,共10分)1. 下列哪项不是配位化合物的特点?A. 含有中心原子或离子B. 含有配位键C. 含有离子键D. 含有配体答案:C2. 配位化合物的几何构型通常由什么决定?A. 配体的电荷B. 配体的数目C. 配体的电子排布D. 中心原子的氧化态答案:B3. 配位化学中,路易斯碱是指什么?A. 能够提供电子的分子或离子B. 能够接受电子的分子或离子C. 能够提供空轨道的分子或离子D. 能够接受空轨道的分子或离子答案:B4. 下列哪种配体是单齿配体?A. 乙二胺(en)B. 1,3-丙二胺(pn)C. 环己二胺(cn)D. 四齿配体答案:A5. 配位化合物的命名中,配体的名称通常放在什么位置?A. 中心原子的前面B. 中心原子的后面C. 配位化合物的前面D. 配位化合物的后面答案:A二、填空题(每题2分,共10分)1. 配位化学中,中心原子或离子与配体之间形成的化学键称为______。
答案:配位键2. 一个中心原子或离子最多可以与______个配体形成配位键。
答案:63. 配位化合物的配位数是指______。
答案:中心原子或离子周围配体的数量4. 配位化合物的命名中,配体的数目通常用希腊数字表示,其中“二”表示______。
答案:二5. 配位化合物的命名中,配体的电荷通常用罗马数字表示,其中“Ⅱ”表示______。
答案:+2三、简答题(每题5分,共20分)1. 简述什么是内界和外界,并举例说明。
答案:内界是指配位化合物中中心原子或离子与配体形成的配位单元,外界是指配位单元以外的部分。
例如,在[Co(NH3)6]Cl3中,[Co(NH3)6]是内界,Cl3是外界。
2. 什么是螯合配体?请举例说明。
答案:螯合配体是指能够通过多个配位点与中心原子或离子形成配位键的配体。
例如,乙二胺(en)可以与金属离子形成螯合配位化合物。
3. 配位化合物的稳定性与哪些因素有关?答案:配位化合物的稳定性与中心原子或离子的电荷、配体的类型、配位数以及配体与中心原子或离子之间的配位键强度等因素有关。
化学_朱文祥_第3章配位化学-习题答案
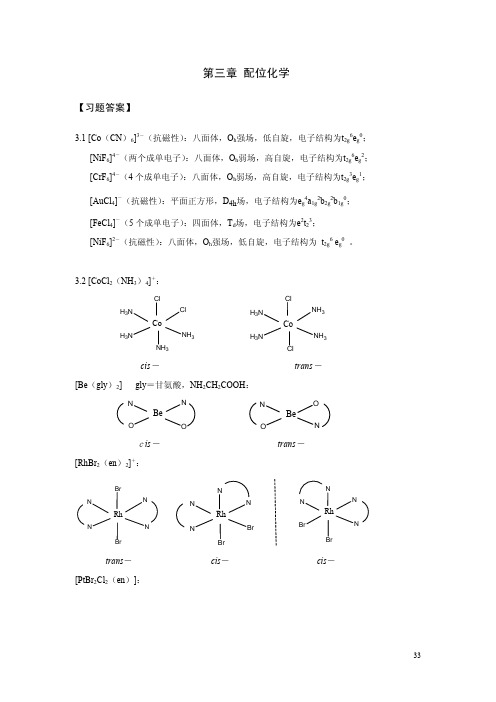
CoCl42-为正四面体构型。由于正四面体场的分裂能较小,所以(e)CoCl42-为高自旋。
3.6 配离子中的配体均为弱场配体,一般为高自旋构型。但是Co3+为d6组态,其与水分子配 位时产生的分裂能略大于电子成对能,因此(c)Co(H2O)63+为低自旋构型。
3.7 (c)的论述正确。F-为弱场配体,晶体场分裂能Δ小,CoF63-因采取高自旋构型而呈顺 磁性。
3.8 (b)Fe(H2O)62+产生Jahn-Teller效应。
3.9
H3N H3N
NO2 NH3
Co
NO2
NO2
mer-
H3N O2N
NO2
Co
NH3
NH3 NO2
fac-
3.10 具有平面四边形结构的配合物为(c)PtCl42—。
3.11 (a)4CoCl2· 6H2O + 4NH4Cl + 20NH3 + O2 → 4[Co(NH3)6]Cl3 + 26H2O (b)K2Cr2O7 + 7 H2C2O4 → 2K[Cr(C2O4)2(H2O)2]+ 6CO2 + 3H2O
3.17 粉红色固体用AgNO3溶液滴定时迅速生成 3 mol AgCl沉淀,说明 3 个Cl-在外界,粉红 色固体的化学式为 [Co(NH3)5(H2O)]Cl3,即三氯化五氨•一水合钴(Ⅲ)。受热外界的 1 个Cl-进入内界占据所失水分子的配位位点,因此紫色固体的化学式为 [CoC(l NH3)5]Cl2, 即二氯化一氯·五氨合钴(III)。
配位化学习题及答案(1)

配位化学习题及答案(1)配位化学练习题一. 是非题1.配合物的配位体都是带负电荷的离子,可以抵消中心离子的正电荷。
2+2+ 2+2.[Cu(NH)] 的积累稳定常数β是反应[Cu(NH)]+NH,[Cu(NH)] 的平33332333衡常数。
3. 配位数是中心离子(或原子) 接受配位体的数目。
4. 配离子的电荷数等于中心离子的电荷数。
5. 配合物中由于存在配位键,所以配合物都是弱电解质。
θ6. 根据稳定常数的大小,即可比较不同配合物的稳定性,即K愈大,该配合物 f 愈稳定。
7.对同一中心离子,形成外轨型配离子时磁矩大,形成内轨型配合物时磁矩小。
3+8.Fe(?) 形成配位数为 6 的外轨型配合物中,Fe 离子接受孤对电子的空轨道32 是spd。
9. 中心离子的未成对电子数越多,配合物的磁矩越大。
10. 配离子的配位键越稳定,其稳定常数越大。
二. 选择题1. 下列叙述正确的是()A.配合物由正负离子组成B.配合物由中心离子(或原子) 与配位体以配位键结合而成C. 配合物由内界与外界组成D. 配合物中的配位体是含有未成键的离子2.下面关于螯合物的叙述正确的是( )A、有两个以上配位原子的配体均生成螯合物B、螯合物和具有相同配位原子的非螯合物稳定性相差不大C、螯合物的稳定性与环的大小有关,与环的多少无关 D 、起螯合作用的配体为多齿配体,称为螯合剂,,,,,,,, ,,,, 3.已知lgAgNH=7.05,,21.7 ,=7.57 ,lgAgCNlgAgSCN,,, ,,,,,,,,232222,,,,2 ,,,,,,3,,,,=13.46; 当配位剂的浓度相同时,AgCl在哪种溶液中的溶解度lgAgSO,,,,,2232 ,,1最大( )A.NH?HOB. KCNC. NaSOD. NaSCN 322234.为了保护环境,生产中的含氰废液的处理通常采用FeSO法产生毒性很小的配 4 合物是( )3, A 、Fe(SCN) B、Fe(OH) 363, C 、Fe(CN) D、Fe [(Fe(CN)] 2 665.下列说法中错误的是()A.在某些金属难溶化合物中,加入配位剂,可使其溶解度增大3+3+B.FeNaFFe 在溶液中加入后,的氧化性降低3-C.[FeF] 在溶液中加入强酸,也不影响其稳定性 63+D.[FeF] 在溶液中加入强碱,会使其稳定性下降 66.对于一些难溶于水的金属化合物,加入配位剂后,使其溶解度增加,其原因是()A.产生盐效应B.配位剂与阳离子生成配合物,溶液中金属离子浓度增加C. 使其分解D. 阳离子被配位生成配离子,其盐溶解度增加7. 下列分子或离子能做螯合剂的是( )-A. HN-NH B. CHCOO C. HO-OH D.HNCHCHNH 22 322228.配位数是()A.() 中心离子或原子接受配位体的数目B.() 中心离子或原子与配位离子所带电荷的代数和C.中心离子(或原子) 接受配位原子的数目D.中心离子(或原子)与配位体所形成的配位键数目9. 关于配合物,下列说法错误的是( )A. 配体是一种可以给出孤对电子或π键电子的离子或分子B. 配位数是指直接同中心离子相连的配体总数C. 广义地讲,所有金属离子都可能生成配合物D. 配离子既可以存在于晶体中,也可以存在于溶液中210.分子中既存在离子键、共价键还存在配位键的有( )3+AlCl A. B. C.[Co(NH)]Cl D. NaSOKCN3633243+11.下列离子中,能较好地掩蔽水溶液中Fe离子的是( )- ---A.F B.Cl C. Br D. I12. 下列说法中错误的是()A. B. 配合物的形成体通常是过渡金属元素配位键是稳定的化学键C.D. 配位体的配位原子必须具有孤电子对配位键的强度可以与氢键相比较13. 下列命名正确的是()A. [Co(ONO)(NH)Cl]Cl ?III 亚硝酸根二氯五氨合钴()352B.[Co(NO)(NH)] ?III 三亚硝基三氨合钴()2333C.[CoCl(NH)]Cl ?III 氯化二氯三氨合钴()233D.[CoCl(NH)]Cl ?III 氯化四氨氯气合钴()23414.影响中心离子(或原子)配位数的主要因素有()A. 中心离子(或原子)能提供的价层空轨道数B.空间效应,即中心离子(或原子)的半径与配位体半径之比越大,配位数越大C.配位数随中心离子(或原子) 电荷数增加而增大D.以上三条都是15.下列说法中正确的是()A. 配位原子的孤电子对越多,其配位能力就越强B. 电负性大的元素充当配位原子,其配位能力就强C.能够供两个或两个以上配位原子的多齿配体只能是有机物分子D.内界中有配位键,也可能存在共价键16.C oCl?5NH?HO已知某化合物的组成为,其水溶液显弱酸性,加入强碱并加332AgNO热至沸,有氨放出,同时产生三氧化二钴的沉淀; 加于另一份该化 3 AgClAgNO合物的溶液中,有沉淀生成,过滤后,再加入而无变化,但加 3AgCl热至沸又产生沉淀,其重量为第一次沉淀量的二分之一,故该化合物的化学式为()A.[CoCl(NH)]Cl?HOB.[Co(NH)HO]Cl235235233C.[CoCl(NH)]Cl?HOD.[CoCl(NH)]Cl?NH?HO 3522234323+17.Fe 离子能与下列哪种配位体形成具有五元环的螯合离子() --2- A. CO B.CHCOCHCOCH C. HNCHCHNHD.OOCCHCOO 24323222222-18. 下列各配合物具有平面正方形或八面体的几何构型,其中CO 离子作为螯合 3剂的是( )+ + A.[Co(NH)CO]B.[Co(NH)CO]353333C.[Pt(en)CO]D.[Pt(en)( NH)CO] 33319.下列配离子能在强酸性介质中稳定存在的是( )3,2 ,3,2, ,,,,,,AgSONiNHFeCOHgCl232433244A. B. C.; D.。
配位化学答案

(四)配位化学答案一.(12分)配位化合物A 是单核配合物分子,由11个原子组成;微热后失重11.35%得到B ;B 进一步加热又失重26.66%(相对B )得到金属C ;B 极难溶于水,不溶于乙醇、乙醚,能溶于盐酸。
A 有2种异构体A 1、A 2,其中A 2能与草酸盐反应得到一种式量比A 略大的配合物分子D (A 1无相似反应)1.写出A 、B 、C 的化学式;2.写出B 溶于盐酸后产物的名称;3.试画出A 1、A 2、D 的结构,并比较A 1、A 2在水中溶解性的大小。
4.A 还有若干种实验式相同的离子化合物。
它们每个还满足如下条件:是由分立的、单核的离子配合物实体构成的;仅含1种阳离子和1种阴离子。
(1)符合上述条件的离子化合物的精确的分子式有多少种。
(2)其中1种与AgNO 3反应(摩尔比1︰2)得到两种组成不同的配合物,写出反应的化学方程式。
答案:1.A :Pt(NH 3)2Cl 2(1.5分) B :PtCl 2(1分) C :Pt (1分)2.四氯合铂(Ⅱ)酸(1分)3.A 1:PtNH 3H 3N Cl(1分) B :Pt Cl H 3N H 3N(1分) D :Pt O H 3N H 3N O O O (1.5分) 在水中溶解度较大的是A 2(1分)4.(1)4种([Pt(NH 3)4]重+、[Pt(NH 3)3Cl]+与[Pt(NH 3)Cl 3]-、[PtCl 4]2-组合)(1分)(2)[Pt(NH 3)4][PtCl 4]+2AgNO 3=Ag 2[PtCl 4]+[Pt(NH 3)4](NO 3)2(2分二.(7分)某Ⅷ族不活泼金属A 溶于足量的王水生成B 的溶液(A 的含量为47.60%);将SO 2通入B 的溶液中,得到C 的溶液(A 的含量为57.56%)。
已知B 、C 的组成元素完全相同,且阴离子所带电荷也相同。
1.通过计算推理,确定A 的元素符号;2.写出所涉及反应的化学方程式。
配位化合物(习题参考答案)
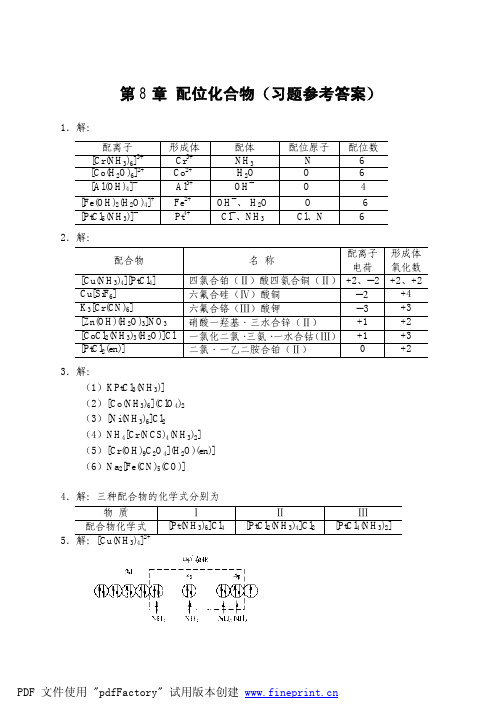
K fψ ([FeF6 ] 3− ) K fψ ([Fe (NCS) 2 ] )
= 8.91×10 10
K ψ 很大,故该反应向右进行。
*13.解: (1)[Ni(CN)4]2− + 2e− 对于电极反应:Ni2+ + 2e−
2+ ψ 2+ 2+ − ψ 2−
Ni + 4CN− Ni
E (Ni /Ni) = E (Ni /Ni) + (0.0592 V / 2) lg c( Ni 2 + ) / c ψ
{c ([Cu (NH ) ] )} {c (Cu )} { c (NH ) }
3 4 2+
x
4
=
0.050 − x = 2.09×1013 4 x( 2.8 + 4 x )
0.050 =2.1×1013, x =3.9×10−17 4 x (2.8)
c([Cu(NH3)4]2+) ≈0.050 mol·L−1,c(NH3·H2O) ≈2.8 mol·L−1 若在此溶液中加入 0.010 mol NaOH(s),即:c(OH− ) = 0.50 mol·L−1
ψ J = 3.9×10−17 × (0.50)2 = 9.8×10−18 > K sp (Cu (OH)2)
故有 Cu (OH)2 沉淀生成。 9.解: 设 1.0 L 6.0 mol·L−1NH3·H2O 溶解 x mol AgI, 则 c([Ag(NH3)2]+) = x mol·L−1 (实 际上应略小于 x mol·L−1)c(I− ) = x mol·L−1 AgI(s) + 2NH3·H2O −1 平衡浓度/(mol·L ) 6.0 − 2 x [Ag(NH3)2]+ + I− + 2H2O x x
配位化学习题答案

配位化学习题答案
配位化学学习题答案
在配位化学中,配位化合物是由中心金属离子和周围的配体组成的。
学习配位
化学需要掌握一定的理论知识和解题技巧。
下面是一些配位化学学习题的答案,希望能帮助大家更好地理解和掌握这一知识点。
1. 问题:写出以下配位化合物的配体名称和化学式:
(a) [Co(NH3)6]Cl3
(b) K4[Fe(CN)6]
(c) [Cu(H2O)4]SO4
答案:
(a) 配体名称:氨
化学式:[Co(NH3)6]Cl3
(b) 配体名称:氰化物
化学式:K4[Fe(CN)6]
(c) 配体名称:水
化学式:[Cu(H2O)4]SO4
2. 问题:计算以下配位化合物的配位数和配体的数量:
(a) [Pt(NH3)4]Cl2
(b) [Co(en)3]Cl3
(c) [Ni(CN)4]2-
答案:
(a) 配位数:4
配体数量:4
(b) 配位数:6
配体数量:3
(c) 配位数:4
配体数量:4
3. 问题:根据配位化合物的性质,判断以下说法的正误:
(a) 配位化合物的颜色与中心金属离子的电子构型有关。
(b) 配位化合物的稳定性与配体的配位能有关。
(c) 配位化合物的磁性与中心金属离子的自旋态有关。
答案:
(a) 正确
(b) 正确
(c) 正确
通过以上学习题的答案,我们可以看到配位化学涉及到配体的命名、配位数的计算以及配位化合物的性质等多个方面。
希望大家在学习配位化学的过程中能够多加练习,加深对这一知识点的理解和掌握。
配位化学习题及答案

配位化学习题及答案
配位化学学习题及答案
配位化学是化学中一个重要的分支,涉及到配合物的结构、性质和反应等方面。
以下是一些配位化学的学习题及答案,希望能帮助大家更好地理解这一领域的
知识。
1. 什么是配合物?
答案:配合物是由中心金属离子和周围的配体组成的化合物。
配体通常是能够
提供一个或多个孤对电子给中心金属离子的分子或离子。
2. 什么是配位数?
答案:配位数是指一个中心金属离子周围配体的数量。
例如,对于[Fe(CN)6]4-
这个配合物来说,铁离子的配位数为6。
3. 什么是配位键?
答案:配位键是指中心金属离子和配体之间的化学键。
这种键通常是由配体中
的孤对电子和中心金属离子形成的。
4. 什么是配位化合物的立体化学?
答案:配位化合物的立体化学涉及到配体和中心金属离子之间的空间排布。
这
种排布对于配合物的性质和反应有很大的影响。
5. 什么是配合物的分子结构?
答案:配合物的分子结构是指配体和中心金属离子之间的空间排布。
这种排布
可以通过X射线衍射等方法来确定。
通过以上学习题及答案,我们可以更好地理解配位化学这一领域的知识。
希木
大家能够通过学习不断提高自己的化学水平,为将来的科研和工作打下坚实的
基础。
(四)配位化学答案

(四)配位化学答案一.(12分)配位化合物A 是单核配合物分子,由11个原子组成;微热后失重11.35%得到B ;B 进一步加热又失重26.66%(相对B )得到金属C ;B 极难溶于水,不溶于乙醇、乙醚,能溶于盐酸。
A 有2种异构体A1、A2,其中A2能与草酸盐反应得到一种式量比A 略大的配合物分子D (A1无相似反应)1.写出A 、B 、C 的化学式;2.写出B 溶于盐酸后产物的名称;3.试画出A1、A2、D 的结构,并比较A1、A2在水中溶解性的大小。
4.A 还有若干种实验式相同的离子化合物。
它们每个还满足如下条件:是由分立的、单核的离子配合物实体构成的;仅含1种阳离子和1种阴离子。
(1)符合上述条件的离子化合物的精确的分子式有多少种。
(2)其中1种与AgNO3反应(摩尔比1︰2)得到两种组成不同的配合物,写出反应的化学方程式。
答案:1.A :Pt(NH3)2Cl2(1.5分) B :PtCl2(1分) C :Pt (1分)2.四氯合铂(Ⅱ)酸(1分)3.A1:Pt NH 3H 3NCl (1分) B :Pt Cl H 3N H 3N Cl(1分) D :Pt O H 3N H 3N O O O (1.5分)在水中溶解度较大的是A2(1分)4.(1)4种([Pt(NH3)4]重+、[Pt(NH3)3Cl]+与[Pt(NH3)Cl3]-、[PtCl4]2-组合)(1分)(2)[Pt(NH3)4][PtCl4]+2AgNO3=Ag2[PtCl4]+[Pt(NH3)4](NO3)2(2分二.(7分)某Ⅷ族不活泼金属A 溶于足量的王水生成B 的溶液(A 的含量为47.60%);将SO2通入B 的溶液中,得到C 的溶液(A 的含量为57.56%)。
已知B 、C 的组成元素完全相同,且阴离子所带电荷也相同。
1.通过计算推理,确定A 的元素符号;2.写出所涉及反应的化学方程式。
3.画出B 、C 阴离子的空间构型。
(完整版)配位化学习题

配位化合物(01)1.历史上记录的第一种人工合成的配位化合物是( D )A.硫酸六氨合钴(II)B.普鲁士蓝C.硫酸四氨合铜(II)D.氯化二氨合银(I)2.配位化学的奠基人是( D)A.阿仑尼乌斯B.路易斯C.鲍林D.维尔纳3.下列说法中错误的是( C)A 配合物的形成体通常是过渡金属元素B 配键是稳定的化学键C 配键的强度可以和氢键相比较D 四面体配合物中,不存在顺反几何异构现象4.下列说法中正确的是(D )A 配位原子的孤电子对越多,其配位能力就越强B 电负性大的元素充当配位原子,其配位能力也强C CH3-C-OH配体是双齿配体D 在[Cu(en)2]2+中,Cu2+的配位数是412.下列说法中错误的是(D )A.对于Ni2+来说,当配位数为6时,无论是强场或弱场配体本位,只能采用SP3d2杂化B.对Ni2+来说,当本位数为4时,随配体的不同可采取dsp2或SP3杂化C.无论中心离子杂化轨道是d2sp2或SP3d2,其构型均为八面体形D.配合物中,由于存在配键,所以配合物都是弱电解质13.下列配体的本位能力的强弱次序为(B )->NH3>NCS->H2O>X-->NH3>NCS->H2O>X-C.X->H2O>CH->NH3>NCS-D.X->CN->H2O>NH3>NCS-14.在配位分子3KNO2.Co(NO3)2中,配位数为(D )A 3B 4C 5D 627.1 共价键和配位共价键的区别是什么?在NH4+离子中分别有多少个共价键和配位共价键?如何对其进行区分?解配位共价键是指一对电子由两个原子共享,且此电子是由其中的一个原子提供的;共价键是指一对共用电子对,一旦形成这两种键就没有区别。
在NH4+离子中有四个共价键,其中有一个是配位共价键。
27.4 求下列配位化合物的中心原子的配位数分别是多少?(a) [Mo(CN)8]4-中的钼(b)Cu(en)22+中的铜(en为乙二胺)解(a) 8 (b) 427.7 指出下列各金属中心离子的特征配为数:(a) CuⅠ(b) CuⅡ(c)AlⅢ(d) CoⅢ(e) ZnⅡ(f) FeⅡ(g) FeⅢ(h) AgⅠ。
配位化学习题答案
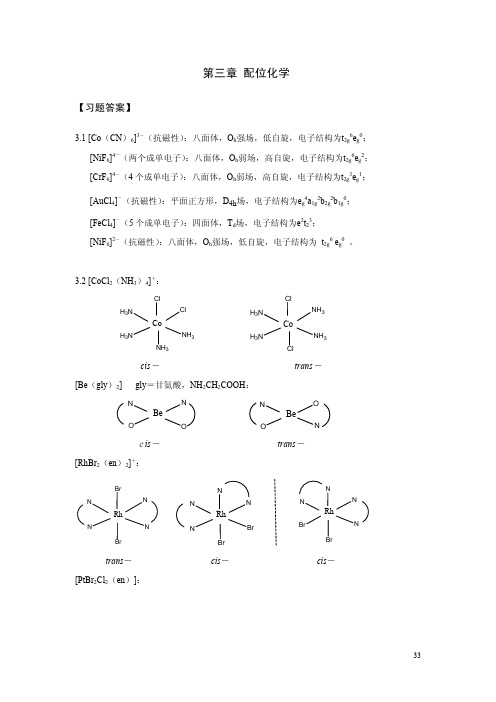
第三章 配位化学【习题答案】3.1 [Co (CN )6]3-(抗磁性):八面体,O h 强场,低自旋,电子结构为t 2g 6e g 0;[NiF 6]4-(两个成单电子):八面体,O h 弱场,高自旋,电子结构为t 2g 6e g 2; [CrF 6]4-(4个成单电子):八面体,O h 弱场,高自旋,电子结构为t 2g 3e g 1; [AuCl 4]-(抗磁性):平面正方形,D 4h 场,电子结构为e g 4a 1g 2b 2g 2b 1g 0;[FeCl 4]-(5个成单电子):四面体,T d 场,电子结构为e 2t 23;[NiF 6]2-(抗磁性):八面体,O h 强场,低自旋,电子结构为 t 2g 6 e g 0 。
3.2 [CoCl 2(NH 3)4]+:ClNH 3H 3NH 3NCoClNH 3NH 3NH 3H 3NH 3NCoClClcis - trans -[Be (gly )2] gly =甘氨酸,NH 2CH 2COOH :NONOBeONN O Becis - trans - [RhBr 2(en )2]+:NNNNRhBrBrNBrNNRhNNNNBrRhNBrtrans - cis - cis - [PtBr 2Cl 2(en )]:BrBrNNPtClClClNNPtBrBrBrClNNPtBrClBrClNNPtBr[Ir (C 2O 4)2Cl 2]3-:OOOOIrClOClOOIrOClOClOOIrOCltrans - cis - cis - [Cr (gly )3]:NOONCrNONOONCrNON ON OCrN ON ON OCrNOmer - mer - fac - fac - [Pt (gly )2]:NONOPtONNO Ptcis - trans -3.3 [M (A -B )2]为旋光活性的,说明它的结构为四面体:ABBA M A BBA M[M (A -B )2X 2]为旋光活性的,说明它的结构为cis -八面体A BB XM A XA BB XM A X3.4 Ti 3+为d 1组态,在O h 弱场中的跃迁为2T 2g → 2E g ,对应谱图中的吸收峰。
配位化学习题(答案参考)

配位化学习题(答案参考)配位化合物(01)1.历史上记录的第一种人工合成的配位化合物是( D )A.硫酸六氨合钴(II)B.普鲁士蓝C.硫酸四氨合铜(II)D.氯化二氨合银(I)2.配位化学的奠基人是( D)A.阿仑尼乌斯B.路易斯C.鲍林D.维尔纳3.下列说法中错误的是( C)A 配合物的形成体通常是过渡金属元素B 配键是稳定的化学键C 配键的强度可以和氢键相比较D 四面体配合物中,不存在顺反几何异构现象4.下列说法中正确的是(D )A 配位原子的孤电子对越多,其配位能力就越强B 电负性大的元素充当配位原子,其配位能力也强C CH3-C-OH配体是双齿配体D 在[Cu(en)2]2+中,Cu2+的配位数是412.下列说法中错误的是(D )A.对于Ni2+来说,当配位数为6时,无论是强场或弱场配体本位,只能采用SP3d2杂化B.对Ni2+来说,当本位数为4时,随配体的不同可采取dsp2或SP3杂化C.无论中心离子杂化轨道是d2sp2或SP3d2,其构型均为八面体形D.配合物中,由于存在配键,所以配合物都是弱电解质13.下列配体的本位能力的强弱次序为(B )/doc/5016026078.html,->NH3>NCS->H2O>X-/doc/5016026078.html,->NH3>NCS->H2O>X-C.X->H2O>CH->NH3>NCS-D.X->CN->H2O>NH3>NCS-14.在配位分子3KNO2.Co(NO3)2中,配位数为(D )A 3B 4C 5D 627.1 共价键和配位共价键的区别是什么?在NH4+离子中分别有多少个共价键和配位共价键?如何对其进行区分?解配位共价键是指一对电子由两个原子共享,且此电子是由其中的一个原子提供的;共价键是指一对共用电子对,一旦形成这两种键就没有区别。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
配位化合物(01)
1.历史上记录的第一种人工合成的配位化合物是( D )
A.硫酸六氨合钴(II)
B.普鲁士蓝
C.硫酸四氨合铜(II)
D.氯化二氨合银(I)
2.配位化学的奠基人是( D)
A.阿仑尼乌斯
B.路易斯
C.鲍林
D.维尔纳
3.下列说法中错误的是( C)
A 配合物的形成体通常是过渡金属元素
B 配键是稳定的化学键
C 配键的强度可以和氢键相比较
D 四面体配合物中,不存在顺反几何异构现象
4.下列说法中正确的是(D )
A 配位原子的孤电子对越多,其配位能力就越强
B 电负性大的元素充当配位原子,其配位能力也强
C CH3-C-OH配体是双齿配体
D 在[Cu(en)2]2+中,Cu2+的配位数是4
12.下列说法中错误的是(D )
A.对于Ni2+来说,当配位数为6时,无论是强场或弱场配体本位,只能采用SP3d2杂化
B.对Ni2+来说,当本位数为4时,随配体的不同可采取dsp2或SP3杂化
C.无论中心离子杂化轨道是d2sp2或SP3d2,其构型均为八面体形
D.配合物中,由于存在配键,所以配合物都是弱电解质
13.下列配体的本位能力的强弱次序为(B )
->NH3>NCS->H2O>X-
->NH3>NCS->H2O>X-
C.X->H2O>CH->NH3>NCS-
D.X->CN->H2O>NH3>NCS-
14.在配位分子3KNO2.Co(NO3)2中,配位数为(D )
A 3
B 4
C 5
D 6
27.1 共价键和配位共价键的区别是什么?在NH4+离子中分别有多少
个共价键和配位共价键?如何对其进行区分?
解配位共价键是指一对电子由两个原子共享,且此电子是由其中的一个原子提供的;共价键是指一对共用电子对,一旦形成这两种键就没有区别。
在NH4+离子中有四个共价键,其中有一个是配位共价键。
27.4 求下列配位化合物的中心原子的配位数分别是多少?
(a) [Mo(CN)8]4-中的钼(b)Cu(en)22+中的铜(en为乙二胺)
解(a) 8 (b) 4
27.7 指出下列各金属中心离子的特征配为数:(a) CuⅠ(b) CuⅡ(c)AlⅢ
(d) CoⅢ(e) ZnⅡ(f) FeⅡ(g) FeⅢ(h) AgⅠ。
解(a) 2 (b)4 (c)6 (d) 6,有时为4 (e) 4 (f) 6 (g) 6 (h) 2
27.9 标明下列各配位离子的电荷数:(a)[FeⅢ(CN)6]
(b)[PtⅣ(NH3)3(H2O)Cl2] (c)[CrⅢ(NH3)2(H2O)2Cl2]
(d)[PdⅡ(en)Cl2] (e)AlⅢ(H2O)2(OH)4]
解(a) 3- (b) 2+ (c) 1+ (d) 0 (E) 1-
7.NH4[Cr(NCS)4(NH3)2]的正确名称是(D )
A 顺一二(三苯基膦).二氯合铂(ⅱ)
B 反一二(三苯基膦).二氯合铂(ⅱ)
C 反一二氯.二(三苯基膦)合铂(ⅱ)D顺一二氯.二(三苯基膦)合铂(ⅱ)
8.NH4[Cr(NCS)4(NH3)2]的正确名称是(B )
A 四(硫氰酸根).二氨全铬(ⅲ)酸铵
B 四(异硫氰酸根).二氨全铬(ⅲ)酸铵
C 四(异硫氰酸根).二氨全铬酸(1-)铵 D.四(硫氰酸).二氨全铬(ⅲ)酸铵
27.19 给下列各化合物命名:(a)[FeCl2(H2O)4]+(b)[Pt(NH3)2Cl2]
(c)[CrCl4(H2O)2]-
解(a)四水二氯合铁(Ⅲ)离子(b)二氯二氨合铂(Ⅱ)(c)二水四
氯合铬(Ⅲ)离子
27.20给下列各化合物命名(其中en=乙二胺,py=吡啶):
(a)[Co(NH3)5Br]SO4 (b)[Cr(en)2Cl2]Cl (c)[Pt(py)4][PtCl4]
(d)K2[NiF6] (e)K3[Fe(CN)5CO] (f)CsTeF5
解(a)硫酸一溴五氨合钴(Ⅲ)
(b)氯化二氯二乙二胺合铬(Ⅲ)
(c)四氯合铂(Ⅱ)化四吡啶合铂(Ⅱ)
(d)六氟合镍(Ⅳ)化钾
(e)一羰基五氰合铁(Ⅱ)化钾
(f)五氟合碲(Ⅳ)化铯
27.21 写出下列各化合物的化学式:
(a)亚硝酸一溴三氨合铂(Ⅱ)
(b)一水二氯二乙二胺合钴(Ⅱ)
(c)溴化一硫酸五氨合钴(Ⅲ)
(d)硫氟合铂(Ⅳ)化二钾
(e)氯化二溴四水合铬(Ⅲ)
(f)七氟合锆(Ⅳ)化三氨
解(a)Pt(NH3)3Br]NO2(b)[Co(en)2Cl2]·H2O (c)[Co(NH3)5SO4]Br
(d)K2PtF6(e)[Cr(H2O)4Br2]Cl (f)(NH4)3[ZrF7]
27.22 给下列各化合物命名:(a)[Co(en)2(CN)2]ClO3(b)K4[Co(CN)6]
(c)[Ni(NH3)6]3[Co(NO2)6]2
解(a)氯酸二氰二乙二胺合钴(Ⅲ)
(b)六氰合钴(Ⅱ)化钾
(c)六硝基合钴(Ⅲ)化六氨合镍(Ⅱ)
27.23写出下列各化合物的化学式:(a)二氯四氨合铑(Ⅲ)离子(b)
四羟基六水合铝(Ⅲ)离子(c)四氯合锌(Ⅱ)离子(d)硝
酸铝(e)四铝二氨合铬(Ⅲ)化六氨合钴(Ⅲ)
解(a)[Rh(NH3)4Cl2]+(b)[Al(H2O)2(OH)4]-(c)[ZnCl4]2- (d)Al(NO3)3
(e)[Co(NH3)6][Cr(NH3)2Cl4]3
27.24写出下列各化合物的化学式:(a)溴化六氨合钴(Ⅲ)(b)四铝
合锌(Ⅱ)化二溴四氨合钴(Ⅲ)(c)二铝二氨合铂(Ⅱ)
解(a)[Co(NH3)6]Br3(b)[Co(NH3)4Br2]2[ZnCl4] (c)Pt(NH3)2Cl2]
27.25给下列各离子命名:(a)[PdBr4]2-(b)[CuCl2]-(c)[Au(CN)4]-
(d)[AlF6]3-(e)[Cr(NH3)6]3+(f)[Zn(NH3)4]2+(g)[Fe(CN)6]3-
解(a)四溴合铅(Ⅱ)络离子(b)二氯合铜(Ⅰ)络离子(c)四氰合
金(Ⅲ)络离子(d)六氟合铝(Ⅲ)络离子(e)六氨合铬(Ⅲ)络离子
(f)四氨合锌(Ⅱ)络离子(g)六氰合铁(Ⅲ)络离子。
