片剂的制备和质量检查
药品生产技术《片剂的质量检查、处方设计及举例》

片剂的质量检查、处方设计及举例一、片剂的质量检查〔一〕外观性状片剂外观应完整光洁,色泽均匀,有适宜的硬度和耐磨性,除另有规定外,对于非包衣片,应符合片剂脆碎度检查法的要求,防止包装、贮运过程中发生磨损或破碎。
〔二〕重量差异片重差异过大,意味着每片中主药含量不一,对治疗可能产生不利影响。
糖衣片的片芯应检查重量差异并符合规定,包糖衣后不再检查重量差异。
薄膜衣片应在包薄膜衣后检查重量差异并符合规定。
检查法:取供试品2021精密称定总重量,求得平均片重后,再分别精密称定每片的重量,每片重量与平均片重相比拟〔凡无含量测定的片剂,每片重量应与标示片重比拟〕,超出重量差异限度的不得多于2片,并不得有1片超出限度1倍。
凡规定检查含量均匀度的片剂,一般不再进行重量差异检查。
〔三〕脆碎度仪器装置:内径约为286mm,深度为39mm,内壁抛光,一边可翻开的透明耐磨塑料圆筒〔见图〕,筒内有一自中心向外壁延伸的弧形隔片〔内径为80mm±1mm,内弧外表与轴套外壁相切〕,使圆筒转动时,片剂产生滚动。
圆筒固定于水平转轴上,转轴与电动机相连,转速为每分钟25转±1转。
每转动一圈,片剂滚动或滑动至筒壁或其他片剂上。
检查法:片重为或以下者取假设干片,使其总重约为;片重大于者取10片。
用吹风机吹去脱落的粉末,精密称重,置圆筒中,转动100次。
取出,同法除去粉末,精密称重,减失重量不得过1%,且不得检出断裂、龟裂及粉碎的片。
【经典】最正确选择题在进行脆碎度检查时,片剂的减失重量不得超过%%『正确答案』C〔四〕崩解时限崩解系指口服固体制剂在规定条件下全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶囊壳外,应全部通过筛网,但已软化或轻质上漂且无硬心者,可作符合规定论。
凡规定检查溶出度、释放度或融变时限的制剂,不再进行崩解时限检查。
1咀嚼片、缓、控释片,不需要作崩解时限检查。
2标准:〔五〕溶出度或释放度检查根据?药典?的有关规定,溶出度检查用于一般的片剂,而释放度检查适用于缓释控释制剂,其主要原因在于:崩解度检查并不能完全正确地反映主药的溶出速度和溶出程度以及机体的吸收情况。
片剂制备实验报告doc

片剂制备实验报告篇一:实验报告2:片剂的制备及质量考察药剂学实验实验报告实验二片剂的制备及质量检查一、实验目的和要求1. 掌握湿法制粒压片法与干法制粒压片法的制备工艺2. 掌握片剂的质量检测方法(硬度、崩解时限、脆碎度、片重差异等)3. 熟悉单冲压片机的结构及其使用方法二、实验内容和原理 1. 实验内容(1)单冲压片机的使用实验1:单冲压片机的安装与拆卸了解单冲压片机的原理,结构,装、卸方法及使用中注意事项。
(2)湿法制粒压片法制备片剂实验2:维生素C片剂的制备以维生素C、淀粉、糊精、柠檬酸、硬脂酸镁等为原料,通过湿法制粒压片法制备维生素C片剂。
(3)片剂的质量检查实验3:检查自制维生素C片剂质量使用硬度计、脆碎度测定仪、崩解时限测定仪等对自制维生素的硬度、脆碎度、崩解时限、片重差异等进行检查。
2. 实验原理(请根据实验教材自己补充,包括湿法制粒压片法的工艺流程,常用辅料及其特性,湿法制粒压片法制备过程中的常见问题及其解决方法,药典规定的片剂的质量检查项目等。
)三、主要仪器设备1. 实验材料:维生素C、淀粉、糊精、柠檬酸、乙醇、硬脂酸镁等。
2. 设备与仪器:单冲压片机、硬度计、脆碎度测定仪、崩解时限测定仪、天平、尼龙筛(20目、100目),吹风机、搪瓷托盘、烘箱等。
四、实验步骤、操作过程(根据实验过程填写,必须列出处方)五、实验结果与分析1.简述维生素C片剂制备过程中所发生的问题,分析产生原因,说明解决方法。
2.将所制维生素C片剂的质量考察结果填写于以下表格中,对其质量进行评估,对所发生的质量问题进行分析并说明解决方法。
表1 外观、硬度、抗张强度表2 崩解时间崩解时间 (min)表3 片重差异表4 片剂脆碎度的测定结果试验前重量(g) 试验后重量(g)批号片数脆碎度(%)篇二:片剂实验报告篇一:实验报告2:片剂的制备及质量考察药剂学实验实验报告实验二片剂的制备及质量检查一、实验目的和要求1. 掌握湿法制粒压片法与干法制粒压片法的制备工艺2. 掌握片剂的质量检测方法(硬度、崩解时限、脆碎度、片重差异等)3. 熟悉单冲压片机的结构及其使用方法二、实验内容和原理 1. 实验内容(1)单冲压片机的使用实验1:单冲压片机的安装与拆卸了解单冲压片机的原理,结构,装、卸方法及使用中注意事项。
6.片剂的制备及质量检查

6.片剂的制备及质量检查实验目的:1.通过片剂制备,掌握湿法制粒压片的工艺过程。
2.掌握单冲压片机的基本构造、使用方法。
3.掌握片剂的质量检查方法。
实验原理:片剂系指药物与适宜的辅料均匀混合,通过制剂技术压制而成片状的固体制剂。
片剂是医疗中应用最广泛的剂型之一,它具有剂量准确,质量稳定。
服用方便、成本低等优点。
片剂由药物和辅料二部分组成。
辅料是指片剂中除主药外一切物质的总称,亦称赋形剂,为非治疗性物质。
加入辅料的目的是使药物在制备过程中具有良好的流动性和可压性;有一定的黏结性;遇体液能迅速崩解、溶解、吸收而产生疗效。
辅料应为“惰性物质”,性质稳定,不与主药发生反应,无生理活性,不影响主药的含量测定,对药物的溶出和吸收无不良影响。
但是,实际上完全惰性的辅料很少,辅料对片剂的性质甚至药效有时可产生很大的影响,因此,要重视辅料的选择。
片剂中常用的辅料包括填充剂、润湿剂、黏合剂、崩解剂及润滑剂等。
通常片剂的制备包括制粒压片法和直接压片法二种,前者根据制颗粒方法不同,又可分为湿法制粒压片和干法制粒压片,其中湿法制粒压片较为常用。
湿法制粒压片适用于对湿热稳定的药物。
其一般工艺流程如下:整个流程中各工序都直接影响片剂的质量。
主药和辅料首先必须符合规定要主药辅药(填充剂或吸收剂、崩解剂)混合粉料加润湿剂软材过筛湿颗粒干燥干颗粒(测定含量、水分)整粒加润滑剂(外加崩解剂)压片求,特别是主药为难溶性药物时,必须有足够的细度,以保证与辅料混匀及溶出度符合要求。
主药与辅料是否充分混合均匀与操作方法也有关。
若药物量小,与辅料量相差悬特时,用递加稀释法(配研法)混合,一般可混合得较均匀,但其含量波动仍然较大;而用溶剂分散法,即将量小的药物先溶于适宜的溶剂中,再与其它成分混合,往往可以混合得很均匀,含量波动很小。
颗粒的制造是制片的关键。
湿法制粒,欲制好颗粒,首先必须根据主药的性质选好粘合剂或润湿剂,制软材时要控制粘给剂或润湿的用量,使之“握之成团,轻压即散”,并握后掌上不沾粉为度。
片剂的制备及质量的考察
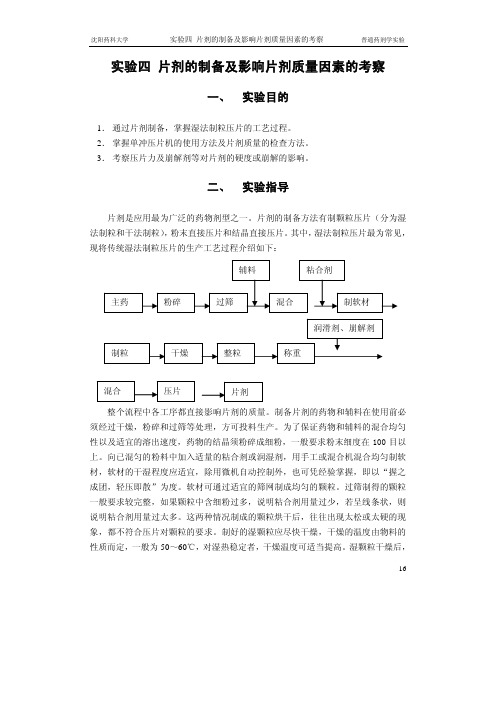
实验四片剂的制备及影响片剂质量因素的考察一、实验目的1.通过片剂制备,掌握湿法制粒压片的工艺过程。
2.掌握单冲压片机的使用方法及片剂质量的检查方法。
3.考察压片力及崩解剂等对片剂的硬度或崩解的影响。
二、实验指导片剂是应用最为广泛的药物剂型之一。
片剂的制备方法有制颗粒压片(分为湿法制粒和干法制粒),粉末直接压片和结晶直接压片。
其中,湿法制粒压片最为常见,现将传统湿法制粒压片的生产工艺过程介绍如下:整个流程中各工序都直接影响片剂的质量。
制备片剂的药物和辅料在使用前必须经过干燥,粉碎和过筛等处理,方可投料生产。
为了保证药物和辅料的混合均匀性以及适宜的溶出速度,药物的结晶须粉碎成细粉,一般要求粉末细度在100目以上。
向已混匀的粉料中加入适量的粘合剂或润湿剂,用手工或混合机混合均匀制软材,软材的干湿程度应适宜,除用微机自动控制外,也可凭经验掌握,即以“握之成团,轻压即散”为度。
软材可通过适宜的筛网制成均匀的颗粒。
过筛制得的颗粒一般要求较完整,如果颗粒中含细粉过多,说明粘合剂用量过少,若呈线条状,则说明粘合剂用量过太多。
这两种情况制成的颗粒烘干后,往往出现太松或太硬的现象,都不符合压片对颗粒的要求。
制好的湿颗粒应尽快干燥,干燥的温度由物料的性质而定,一般为50~60℃,对湿热稳定者,干燥温度可适当提高。
湿颗粒干燥后,1617需过筛整粒以便将粘结成块的颗粒散开,同时加入润滑剂和需外加法加入的崩解剂并与颗粒混匀。
整粒用筛的孔径与制粒时所用筛孔相同或略小。
压片前必须对干颗粒及粉末的混合物进行含量测定,然后根据颗粒所含主药的量计算片重。
()测得值干颗粒中主药百分含量标示量每片应含主药量片重=根据片重选择筛目与冲膜直径,其之间的常用关系可参考表1。
根据药物密度不同,可进行适当调整。
表1 根据片重可选的筛目与冲膜的尺寸筛目数片重 冲膜直径 (mg) 湿粒 干粒 (mm)50 18 16-20 5-5.5100 16 14-20 6-6.5150 16 14-20 7-8200 14 12-16 8-8.5300 12 10-16 9-10.5500 10 10-12 12制成的片剂需按照中国药典规定的片剂质量标准进行检查。
片剂的生产工艺及质量检测培训教材

对不合格的片剂进行标识、隔离和处理,防止不合格品流入市场。
06
片剂的包装与储存
BIG DATA EMPOWERS TO CREATE A NEW
ERA
包装材料的选择
包装材料应具备足够的阻隔性能,如 防潮、防氧化、防紫外线等,以确保 片剂的稳定性和有效期。
根据片剂的特性和用途,选择适当的 包装材料和形式,如泡罩包装、铝箔 包装等。
存储与运输
对原辅料的存储和运输进行管理 ,保持适当的温度和湿度条件, 防止损坏和污染。
制程质量控制
工艺流程
制定详细的工艺流程,明确各工序的操作要 求和标准,确保生产过程中的质量控制。
设备维护与校准
定期对生产设备进行维护和校准,确保设备 性能稳定,符合生产要求。
成品质量控制
检验标准
制定严格的成品检验标准,包括外观、尺寸、重量、硬度等指标,确保产品质量符合规 定。
含量均匀度检测
总结词
含量均匀度检测是检查片剂中药物分布 的均匀程度。
VS
详细描述
含量均匀度检测通常采用高效液相色谱法 等分析方法,对片剂中的药物含量进行测 定。如果含量均匀度不符合标准要求,则 说明片剂中药物分布不均匀,可能影响药 物的疗效和安全性。
04
片剂的生产设备
BIG DATA EMPOWERS TO CREATE A NEW
ERA
片剂的定义
总结词
片剂是一种药物制剂,是将药物与适宜的辅料通过压制或融合技术制成的一种 固体制剂。
详细描述
片剂是一种广泛使用的药物剂型,其外观、形状、大小和颜色等特征可根据不 同药物和生产工艺进行定制。片剂具有剂量准确、使用方便、稳定性好等优点 。
片剂的特点
药剂学实验——片剂的制备与质量检查

实验六 片剂的制备及质量检查
润滑剂 黏合剂 崩解剂
润滑剂 崩解剂
主
药粉
碎混 和
制 制干 整 软湿
混压
辅 料
过 筛
合
材 粒燥 粒 填充
合 挥发
片
剂
物
湿法制粒压片工艺流程
实验六 片剂的制备及质量检查
实验内容与操作
➢实验材料与设备 实验材料:蓝淀粉、糖粉、糊精、淀粉、50%乙 醇、硬脂酸镁等 实验器材:单冲压片机、药筛、搪瓷盆、片剂崩 解仪、不同冲头和冲模(模圈)
实验六 片剂的制备及质量检查
➢实验内容与操作
1.空白片的制备 操作
2.空白片质量检查
操作
实验六 片剂的制备及质量检查
实验报告
实验六 片剂的制备及质量检查
思考题
1.制湿粒之前过两次筛的目的是什么?如果不 过筛会出现什么问题? 2.造成片剂重量差异和崩解时限检查不合格 的主要原因是什么?ຫໍສະໝຸດ 实验六 片剂的制备及质量检查
实验目的 实验指导 实验内容与操作 实验报告 思考题
实验六 片剂的制备及质量检查
实验目的
初步掌握湿法制粒压片的过程的技术 会分析片剂处方的组成和各种辅料在压片 过程中的作用 正确使用单冲压片机 熟悉处片重差异、崩解时限的检查方法
实验六 片剂的制备及质量检查
实验指导
片剂(tablets)系指药物与适宜的辅料混匀压制 而成的圆片状或异形片状的固体制剂(见图6-1)
片剂的质量检查项目

片剂的质量检查项目1. 引言片剂是一种常见的药物制剂形式,它们由活性成分和辅助成分经过一系列工艺步骤制成。
为了确保片剂的质量和安全性,需要进行一系列的质量检查项目。
本文将详细介绍片剂的质量检查项目。
2. 片剂外观检查片剂外观检查是最基本也是最直观的一个检查项目。
通过目测和触摸片剂,可以初步判断其是否符合质量要求。
以下是常见的外观检查项目:•外观:片剂应呈现出统一、均匀、光滑、无裂纹、无破损等特征。
•形状:片剂应具有规定的形状,如圆形、椭圆形、长方形等。
•颜色:片剂应具有统一的颜色,无明显色差或变色。
•表面润滑度:片剂表面应具有适当的润滑性,以便于吞咽。
•厚度:片剂数量应符合规定,并且厚度应均匀。
3. 片剂重量和尺寸检查片剂重量和尺寸的检查是确保每个片剂在制造过程中符合质量要求的重要步骤。
以下是常见的重量和尺寸检查项目:•平均重量:随机选取一定数量的片剂,称重并计算其平均重量。
平均重量应符合规定范围。
•厚度:使用卡尺测量片剂的厚度,厚度应符合规定范围。
•直径:使用卡尺测量片剂的直径,直径应符合规定范围。
4. 片剂硬度和破碎性检查片剂硬度和破碎性的检查是评估片剂在生产、包装和使用过程中是否具有足够的强度和稳定性。
以下是常见的硬度和破碎性检查项目:•硬度:使用硬度计测量片剂在一定压力下的硬度。
硬度应符合规定范围。
•破碎性:通过模拟实际使用情况,在一定高度下自由落体使得片剂受力并观察其是否破裂。
破碎性应符合规定要求。
5. 片剂含量和释放度检查片剂含量和释放度的检查是评估片剂中活性成分的含量和释放效果的重要指标。
以下是常见的含量和释放度检查项目:•含量一致性:通过取样并使用适当的方法测定片剂中活性成分的含量。
含量应符合规定范围。
•释放度:使用离体溶出装置模拟片剂在人体消化道中的溶出过程,测定活性成分的溶出度。
释放度应符合规定要求。
6. 片剂稳定性检查片剂稳定性的检查是评估片剂在储存期间是否能够保持其质量和有效性的重要指标。
片剂的制备与质量检查

项 目 任 务 书一、项目描述二、材料清单序号 各种材料清单数量 备注 1 2 3 4 5 6 78 9 10 11说明:以上为一名学生所需材料项目 3.3片剂的制备与质量检查班级:制药083提出问题如何制备阿司匹林片?阿司匹林片的全程分析包括哪些内容?任务分析1.熟悉片剂制备的基本工艺过程,掌握湿法制粒压片的一般工艺。
2.掌握片剂质量检查方法。
3.学会分析片剂处方的组成和各种辅料在压片过程中的作用。
4.了解阿司匹林片剂的质量检查5.掌握两步中和滴定法的原理及操作方法 相关知识及资料片剂系指药物与适宜的辅料均匀混合,通过制剂技术压制而成片状的固体制剂。
主要供口服。
它是临床应用最广泛的剂型之一,具有剂量准确、质量稳定、服用方便、成本低等优点。
片剂的制备方法主要包括湿法制粒压片、干法制粒压片和直接压片法二种,其中湿法制粒压片较为常用。
湿法制粒压片适用于对湿热稳定的药物。
三、项目实施过程(一)任务分析:通过本模块的学习,学生明确1. 能按生产指令进行压片操作2.能进行压片机的清洁与维护3.能对压片过程中出现不合格片进行判断,并能找出原因同时提出解决方法4. 能按生产指令进行包衣操作并能对包衣片进行质量判断找出不合格原因同时提出解决方案5. 能对包衣机进行清洁与维护。
6. 根据中国药典要求,检查阿司匹林肠溶片质量(二)任务实施要求:1. 查找资料,了解阿司匹林的药理作用,阿司匹林的化学及物理性质,并在课业报告中加以描述。
2. 设计药剂处方,其内容包括:确定阿司匹林的浓度;选择附加剂,并确定比例和附加剂的使用量。
药剂处方和处方说明为课业报告内容。
3. 思考并设计配制方法,并预先考虑应该注意的事项。
4. 在药物制剂技术实验室完成药剂的配制。
在课业报告中详细描述配制过程。
5. 选择包装容器,并设计药品标签。
6.将片剂包装,并贴上自己手工绘制的药品标签。
7. 学会阿司匹林片的含量分析8.每个小组选一个学生代表将本组的工作情况向其他小组同学介绍。
片剂质量检查的主要内容

片剂质量检查的主要内容
片剂质量检查是指对制备好的片剂进行质量评估和控制的过程。
它是药企保证片剂产品符合药典要求以及满足临床应用需要的重要
环节。
主要内容包括以下几个方面:
1. 外观检查:外观是片剂的首要指标之一,也是患者接受药品的第一印象。
外观检查包括片剂的形状、颜色、气味、质地等方面。
通过仔细观察片剂的外观特征,可以初步判断片剂是否符合质量要求。
2. 尺寸和重量检查:片剂的尺寸和重量对于患者的服用体验和剂量控制非常重要。
质量检查中需要测量片剂的长度、厚度和直径,并比较与规定要求是否相符。
同时还需要测量片剂的重量,确保每片剂的剂量准确。
3. 含量测定:片剂的含量测定是评估片剂质量的重要指标。
含量测定一般通过药物分析方法,如高效液相色谱法、紫外分光光度法等进行。
通过测定片剂中有效成分的含量,可以确保每片剂的药物剂量在规定范围内。
4. 溶出度测定:溶出度是评价片剂释放药物速度和程度的重要指标。
溶出度测定可以通过体外溶出度试验来进行,通过测定片剂中药物在一定时间内溶出的百分比,评估片剂的药物释放性能。
5. 片剂硬度测定:片剂的硬度直接影响其在包装和患者服用过程中的耐受性。
硬度测定可以通过药物硬度计来进行,按一定压力测试片剂的硬度值。
合格的片剂应具有足够的硬度以保持其完整性,并能够方便地分割成均匀的剂量。
总之,片剂质量检查的主要内容涵盖了外观、尺寸和重量、含量、溶出度以及硬度等方面的评估。
这些检查内容的合格与否直接关系到片剂的质量和疗效,对于确保片剂的安全性和有效性具有重要意义。
片剂的质量检查项目有哪些

片剂的质量检查项目有哪些片剂是广泛应用于医药行业的一种制剂,其特性是以壁式片剂的形式出现,这种制剂生产时需要控制好大量的参数,为的是最大限度的减少误差因素,同时确保片剂质量如一。
在生产过程中,需要进行严格的质量检查,以确保片剂的安全性及有效性。
本文将介绍片剂的质量检查项目,旨在为消费者提供健康的片剂,保障患者的健康。
1. 料检查原料检查是片剂生产过程中不可缺少的一环,其目的是检查原料的质量和安全性,以确保片剂质量如一。
原料检查涉及的内容包括:(1)药物原料的属性及有效成分的质量检查,如检查药物原料的外观、颜色、比重和含有量等。
(2)原料药物的有效成分检查,如检查药物原料中有效成分的含量、形态等。
(3)原料药物的毒性检查,如检查药物小白鼠的皮肤反应、毒性试验、全血毒性试验等。
2.艺检查工艺检查是控制片剂质量的重要环节,其旨在保证片剂的安全性及有效性。
工艺检查涉及的内容包括:(1)制剂工艺检查,如检查片剂的过程管理、控制及相关记录等。
(2)相关材料的检查,如检查抗菌剂、抗过敏物质、添加剂和填料等。
(3)产品的性能检查,如检查片剂的悬浮度、微生物的计数、药物的有效成分含量等。
3.量检查批量检查是控制片剂质量的最后环节,其旨在保证片剂的稳定性及安全性。
批量检查涉及的内容包括:(1)批量片剂检查,如检查片剂的形状或粒度、湿度、包装标签和相关文件等。
(2)批量片剂性能检查,如检查药物有效成分的含量、悬浮度、溶出度等。
(3)片剂的有效试验,如检查细胞毒性、体外溶出度、药物的活性度等。
以上就是片剂的质量检查项目,其主要包括原料检查、工艺检查和批量检查三部分。
任何一步质量检查出现问题,都会影响最终片剂产品的质量安全。
因此,严格根据要求,完成上述质量检查,以最大限度保证片剂的安全性及有效性,同时保护消费者的健康权益。
片剂的质量检查实验报告

片剂的质量检查实验报告片剂的质量检查实验报告1. 引言片剂是一种常见的药物制剂形式,广泛应用于临床治疗中。
为了确保片剂的质量和安全性,质量检查实验是必不可少的环节。
本报告旨在介绍片剂的质量检查实验以及实验结果的分析。
2. 实验目的本次实验的目的是对片剂进行质量检查,包括外观检查、药物含量测定、溶解度测定和稳定性评价。
3. 实验方法3.1 外观检查外观检查是片剂质量检查的首要步骤。
我们对样品进行了外观观察,包括颜色、形状、大小、光泽等方面的评估。
3.2 药物含量测定药物含量测定是评估片剂药物含量是否符合规定标准的重要指标。
我们采用了高效液相色谱法(HPLC)对样品进行分析,测定片剂中活性成分的含量。
3.3 溶解度测定溶解度是评价片剂的溶解性能的指标之一。
我们采用了溶出度仪对样品进行溶解度测定,以评估片剂在不同介质中的溶解情况。
3.4 稳定性评价稳定性评价是评估片剂在储存期间质量变化的重要指标。
我们将样品置于不同条件下,包括高温、高湿和光照等,进行稳定性测试,以模拟片剂在实际使用环境中的情况。
4. 实验结果与讨论4.1 外观检查结果经过外观检查,样品的颜色均匀一致,形状规整,无明显破损或变形,光泽良好,符合片剂的外观要求。
4.2 药物含量测定结果药物含量测定结果显示,样品中的活性成分含量均在规定范围内,符合片剂的质量标准。
这表明样品制备工艺和质量控制符合要求。
4.3 溶解度测定结果溶解度测定结果显示,样品在不同介质中的溶解度良好,符合片剂的溶解性能要求。
这意味着片剂可以在胃肠道中迅速溶解,提高药物的吸收效果。
4.4 稳定性评价结果稳定性评价结果显示,样品在高温、高湿和光照条件下均未出现明显的质量变化,符合片剂的稳定性要求。
这表明样品在储存期间可以保持良好的质量和药效。
5. 结论通过对片剂的质量检查实验,我们得出以下结论:- 样品的外观符合片剂的外观要求;- 样品中的活性成分含量符合片剂的质量标准;- 样品在不同介质中的溶解度良好,符合片剂的溶解性能要求;- 样品在储存期间保持了良好的稳定性。
片剂—片剂的制备(药物制剂技术)
维生素C片
【质量检查】 [崩解时限检查] 按药典现定采用升降式片剂崩解仪测 定片剂的崩解时限。测定时,取供试药片6片置吊篮 玻璃管中,于37±1℃的恒温水中,按每分钟30-32 次作上下移动,各片均应在规定时间内全部港散或崩 解成碎粒,并通过筛网。如残存有小颗粒不能全部通 过筛网时,应另以6片复试,并在每管加入药片后随 即加人挡板各1块,依法检查,均应符合规定。
200g (主药) 80g (填充剂)
120g (填充剂) 4g (稳定剂)
适量 (润湿剂) 3g (润滑剂)
400g
维生素C片
【制备工艺】 取维生素C、乳糖、糊精混合均匀,将酒石酸溶 于
50%乙醇中再加入搅拌混匀,制软材,通过18-20目 筛,制湿颗粒,在60℃-70℃干燥,干粒水分应控制 在15%以下,颗粒过筛(同制粒相同目筛)整粒,筛 出细粉,加硬脂酸镁混合均匀,然后与干颗粒混匀, 压片质粒包装即可。
维生素C片
【质量检查】 [重量差异] 取供试品20片,精密称定总重量,求得平 均片重后,再分别精密称定每片的重量,每片重量与 平均片重相比较(凡有标示片重的片剂,每片重量与 标示片重相比较),超出限度的不得多于2片,并不 得有1片超出限度一倍。
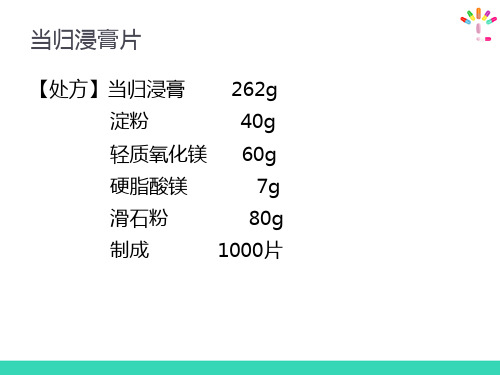
当归浸膏片
【处方】当归浸膏 262g
淀粉
40g
轻质氧化镁 60g
硬脂酸镁
7g
滑石粉
80g
制成
1000片
当归浸膏片
【制备工艺】 取浸膏加热(不用直火)至60℃~70℃,搅拌使熔化 ,将轻质氧化镁、滑石粉(60g)及淀粉依次加入混 匀,分铺烘盘上,于60℃以下干燥至含水量3%以下 。然后将烘干的片(块)状物粉碎成14目以下的颗粒 ,最后加入硬脂酸镁、滑石粉(20g)混匀,过12目 筛整粒,压片、质检、包糖衣。
片剂全检实验报告

片剂全检实验报告一、实验目的及背景片剂是一种常见的固体制剂形式,广泛应用于药物治疗中。
片剂的制备需要保证其质量符合国家相关标准,包括药物含量、溶解度、质地等指标。
因此,本实验旨在通过对片剂样品进行全面检验,评估其质量合格程度,并找出可能的不合格因素。
二、实验仪器与试剂仪器:1. 片剂研磨机2. pH计3. 紫外-可见光分光光度计4. 电子天平5. 超声波溶解仪试剂:1. pH标准缓冲溶液2. 纯水3. 醋酸乙酯4. 硫酸钠5. 氯化钠6. 丙酮7. 多巴胺标准溶液三、实验步骤及结果1. 药物含量检验1. 取适量片剂样品称重,粉碎并过筛,称取0.1g溶解于醋酸乙酯中,定容至100ml。
2. 使用紫外-可见光分光光度计测定药物溶液在321nm处的吸光度,并与多巴胺标准曲线进行比对计算出样品中药物的含量。
2. 包衣膜厚度测定1. 取适量片剂样品,用片剂研磨机研磨成细粉。
2. 使用电子天平测定粉末的质量,并计算得出单位质量下的平均颗粒数。
3. 将粉末置于显微镜下观察,测量皮尔表面数,并计算得出包衣膜厚度。
3. 溶解度测定1. 取适量片剂样品,将其放入超声波溶解仪中,加入适量的pH标准缓冲溶液。
2. 开始超声溶解,直至可清晰看到片剂完全溶解。
4. 质地评价1. 取适量片剂样品,用手触摸表面,记录其表面光滑度、粘稠度等感觉指标。
2. 使用pH计对其进行酸碱性检测。
四、结果与分析1. 药物含量检验结果显示,片剂样品中药物的含量为Xmg/g,符合国家标准。
2. 包衣膜厚度测定结果为Xum,符合国家标准。
3. 片剂样品的溶解度测试结果显示,样品在pH=X的缓冲液中完全溶解,并符合国家标准。
4. 质地评价结果显示,片剂样品表面光滑,无明显粘稠度,pH值介于x~x之间。
五、结论通过对片剂样品进行全面检验,结果表明该片剂样品的药物含量、包衣膜厚度、溶解度和质地指标均符合国家相关标准,质量合格。
本实验方法可为片剂样品的全面检验提供一种有效的方案。
片剂制备实验报告

片剂制备实验报告篇一:实验报告2:片剂的制备及质量考察药剂学实验实验报告实验二片剂的制备及质量检查一、实验目的和要求1. 掌握湿法制粒压片法与干法制粒压片法的制备工艺2. 掌握片剂的质量检测方法(硬度、崩解时限、脆碎度、片重差异等)3. 熟悉单冲压片机的结构及其使用方法二、实验内容和原理 1. 实验内容(1)单冲压片机的使用实验1:单冲压片机的安装与拆卸了解单冲压片机的原理,结构,装、卸方法及使用中注意事项。
(2)湿法制粒压片法制备片剂实验2:维生素C片剂的制备以维生素C、淀粉、糊精、柠檬酸、硬脂酸镁等为原料,通过湿法制粒压片法制备维生素C片剂。
(3)片剂的质量检查实验3:检查自制维生素C片剂质量使用硬度计、脆碎度测定仪、崩解时限测定仪等对自制维生素的硬度、脆碎度、崩解时限、片重差异等进行检查。
2. 实验原理(请根据实验教材自己补充,包括湿法制粒压片法的工艺流程,常用辅料及其特性,湿法制粒压片法制备过程中的常见问题及其解决方法,药典规定的片剂的质量检查项目等。
)三、主要仪器设备1. 实验材料:维生素C、淀粉、糊精、柠檬酸、乙醇、硬脂酸镁等。
2. 设备与仪器:单冲压片机、硬度计、脆碎度测定仪、崩解时限测定仪、天平、尼龙筛(20目、100目),吹风机、搪瓷托盘、烘箱等。
四、实验步骤、操作过程(根据实验过程填写,必须列出处方)五、实验结果与分析1.简述维生素C片剂制备过程中所发生的问题,分析产生原因,说明解决方法。
2.将所制维生素C片剂的质量考察结果填写于以下表格中,对其质量进行评估,对所发生的质量问题进行分析并说明解决方法。
表1 外观、硬度、抗张强度表2 崩解时间崩解时间 (min)表3 片重差异表4 片剂脆碎度的测定结果试验前重量(g) 试验后重量(g)批号片数脆碎度(%)篇二:片剂实验报告篇一:实验报告2:片剂的制备及质量考察药剂学实验实验报告实验二片剂的制备及质量检查一、实验目的和要求1. 掌握湿法制粒压片法与干法制粒压片法的制备工艺2. 掌握片剂的质量检测方法(硬度、崩解时限、脆碎度、片重差异等)3. 熟悉单冲压片机的结构及其使用方法二、实验内容和原理 1. 实验内容(1)单冲压片机的使用实验1:单冲压片机的安装与拆卸了解单冲压片机的原理,结构,装、卸方法及使用中注意事项。
《药剂学》片剂的制备及质量检查实验

《药剂学》片剂的制备及质量检查实验一、实验目的1.通过片剂制备,掌握湿法制粒压片的工艺过程。
2.掌握单冲压片机的使用方法3.掌握片剂四用测定仪的使用方法及片剂的硬度、崩解时限检查方法。
二、基本概念与实验原理:概念:片剂系指药物与适宜的辅料均匀混合后,通过制剂技术压制而成的圆片状或其他异型片状的固体制剂。
配制环境要求:粉碎、过筛、混合、制粒、干燥、压片、包装等生产操作环境D 级制法:湿法制粒压片法、干法制粒压片法、直接压片法。
湿法制粒压片的生产工艺:主药、辅料粉碎、过筛、混合---加粘合剂制软材----过筛制粒----颗粒干燥---测定含量、水分---整粒、称重---加润滑剂和外加崩解剂,计算片重,选择冲模---安装机器,压片。
制粒:物料混匀后,加入适量粘合剂制成软材(以用手握之可成团块,手指轻压时又能散裂而不成粉状为度),用手挤压过筛,所得颗粒应无长条、块状物及细粉。
大量生产时通过颗粒机滚筒(或括板)的挤压,使软材通过筛孔,制得湿颗粒。
应根据药物和辅料的性质选用适宜温度尽快干燥。
干燥后颗粒往往结团粘连,需进行过筛整粒,最后加入润滑剂等辅料,混匀后即可压片。
质量检查:按《中国药典》2010年附录.制剂通则.片剂.进行检查,应符合规定。
单冲压片机的主要构造及压片动作:单冲压片机的安装与调节:首先装好下冲头,旋紧模板固定螺丝。
旋动片重调节器,使下冲在较低的部位。
再将冲模装入模板,旋紧固定螺丝,然后仔细地将模板装在机座上(冲头的尖端锋利部位,易被撞碎而损坏,故在整个装拆过程中都应小心)。
调节出片调节器,使下冲头上升到恰与模圈相齐平。
再装上冲头并旋紧固定螺丝。
转动压力调节器,使上冲处在压力低的部位,缓慢地用手摇转压片机的转轮使上冲头逐渐下降,观察其是否正好在冲模的中心位置。
如不在中心位置,应上升冲头(不得将上冲头强硬地冲入冲模模孔,更不应使上下冲相撞)。
此外,稍微松动一点模孔固定螺丝,移动位置直到上冲头恰在冲模模孔的中心位置为止,旋紧固定螺丝,装好加料斗的全部装置,并加入颗粒。
片剂的生产工艺及质量检测培训

片剂的生产工艺及质量检测培训引言片剂是一种常见的药物制剂形式,它通过将药物颗粒或粉末与其他成分混合,并在一定的工艺条件下,制成平坦、圆形或其他形状的片固体。
片剂能够方便患者服用、保存和运输,因此在医药领域得到广泛应用。
本文将重点介绍片剂的生产工艺以及相关的质量检测方法和要求。
片剂生产工艺1. 原料准备片剂的制备过程中,需要准备药物原料以及辅料。
药物原料包括活性成分,而辅料则包括填充剂、粘合剂和润滑剂等。
其中,填充剂用于提供药片的体积,粘合剂用于粘结药物成分,而润滑剂用于减少药片之间的摩擦。
2. 混合与均匀原料准备完毕后,需要将药物原料及辅料混合均匀。
混合的目的是保证各种原料之间的均匀分布,确保每一片剂中含有相同的药物成分。
3. 压片混合均匀后的药物颗粒或粉末,通过压片机的作用产生压力,使其成形成片剂。
压片机通过对粉末施加一定的压力,使其在模具中形成一定的形状和尺寸。
同时,压片机还可以根据需要给药片加上凹槽或凸字形状,以便患者更方便地分割药片。
4. 干燥压片完成后,药片需要在一定的温度和湿度条件下进行干燥。
干燥的目的是去除药片中的水分,防止药片发生变形、变质或变硬。
5. 包装干燥后的药片需要进行包装。
包装的目的是保护药片免受外界环境的影响,并延长其有效期。
常见的片剂包装形式包括铝箔袋、塑料瓶和泡罩等。
片剂质量检测1. 外观检查外观检查是片剂质量检测的首要步骤。
通过目视观察,检查片剂的形状、颜色、表面是否平整,并排除外部污染等因素。
2. 尺寸和重量检测尺寸和重量是判断片剂质量的重要指标。
常用的检测方法包括使用卡尺测量片剂的直径和厚度,并使用天平称量片剂的重量。
这些指标需要满足一定的范围要求,以确保片剂的一致性。
3. 药物含量测定药物含量测定是片剂质量检测中的关键环节。
常用的方法有高效液相色谱法(HPLC)、紫外分光光度法和质谱法等。
这些方法可以准确测量片剂中的药物含量,并与规定的药物含量标准进行比较。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
药学院 药剂学科
一、实验目的
1、掌握片剂的制备工艺流程及其操作要点。 2、熟悉片剂的质量要求,掌握片重差异、崩解时限、 硬度等常规质量检查方法。 3、掌握压片操作方法,了解压片机的基本结构及其使 用与保养
二、实验指导
片剂系指将药物与适宜的辅料通过制剂技术 制成的片状制剂。
片剂的制法分为直接压片、干法制粒压片和 湿法制粒压片。除对湿、热不稳定的药物之 外,多数药物采用湿法制粒压片。
4、硬度和脆碎度 采用孟山都(Monsanto)硬度计测定 硬度,一般能承受30-40N的压力即认为硬度合格。采 用罗许(Roche)脆碎仪测定,减失重量不得超过1%。
五、思考题
1、制备APC片剂过程中,怎样避免乙酰水 杨酸分解?
2、压制APC片时,应选用何种润滑剂?
10
工艺流程图
质量检查
1、片剂外观 应完整光洁,色泽均匀,有适宜的硬度。
2、重量差异 取本品20片,精密称定。每片重量与平均 片重相比较,超出重量差异限度(平均片重小于 0.3g±7.5%,平均片重0.3g以上±5.0%)的药片不得多 于2片,并不得有1片超出限度一倍。
质量检查
3、崩解时限 采用升降式崩解仪。取片剂6片,分别置 于吊篮的玻璃管中,启动崩解仪进行检查,应在规定时 间内全部通过筛网。如有1片不能完全溶散,应另取6片 复试,均应符合规定。
淀粉浆的制备:冲浆法、煮浆法
实验内容
复方乙酰水杨酸片(复方阿司匹乙酰水杨酸(粒状结晶)
22.7
对乙酰氨基酚(细粉)
16.2
咖啡因(细粉)
3.5
淀粉
6.6
淀粉浆(17%)
适量
滑石粉
5%
〔制法〕对乙酰氨基酚、咖啡因与淀粉混匀,加 淀粉浆制成均匀的软材,通过14~1 6目筛制粒, 湿粒70℃干燥,测定含水量。干颗粒过12~14目 筛整粒。将此颗粒与乙酰水杨酸结晶混合,加入 滑石粉后,充分混匀,压片。
