分光光度法测定聚乙二醇水溶液浓度
快速检测聚乙烯醇水溶液浓度的适用方法

快速检测聚乙烯醇水溶液浓度的适用方法现有的聚乙烯醇水溶液浓度的检测耗时较长,严重制约着化工生产过程中数据传递的及时性。
本课题给出聚乙烯醇水溶液高、中、低浓度的快速检测方法。
标签:聚乙烯醇;浓度;碘/碘化钾溶液;折光率;微波1 引言聚乙烯醇是一种典型的水溶性高分子聚合物,广泛应用于纺织、化工、材料、生物等领域。
使用过程都是配制成一定浓度的水溶液,分析聚乙烯醇水溶液浓度的准确和及时性成了保证生产稳定的前提。
现行的分析方法都是将聚乙烯醇水溶液放在105℃的烘箱中进行干燥,低浓度树脂液需要3小时左右,高浓度树脂液需要10小时以上,极大地限制了分析数据及时指导生产作用。
为此,建立一种快速准确分析聚乙烯醇水溶液浓度的方法势在必行,利用聚乙烯醇水溶液的折光性、与碘结合产生络合物、以及微波的快速渗透性可以很好的建立不同聚乙烯醇水溶液的快速分析方法。
2 检测原理2.1 低浓度聚乙烯醇水溶液的检测原理低浓度的聚乙烯醇水溶液在硼酸存在的条件下会与碘生成稳定的蓝绿色化合物,该有色化合物的颜色深度与水中PV A含量呈线性正比,且在670nm的波长下有最大吸收值,为此通过配制系列浓度的标准聚乙烯醇水溶液,在此波长下测定其吸光度值并建立标准曲线,即可得到聚乙烯醇水溶液的浓度值。
2.2 中浓度聚乙烯醇水溶液的检测原理折光率是有机化合物最重要的物理常数之一,尤其是对于聚乙烯醇水溶液,在一定浓度范围内(一般为10%~15%),随着聚乙烯醇水溶液中聚乙烯醇含量的不断变化,其折光率也随着呈现线性变化。
为此,将浓度和对应的折光率建立标准曲线即可以快速准确测得中浓度聚乙烯醇水溶液的浓度值。
2.3 高浓度聚乙烯醇水溶液的检测原理高浓度聚乙烯醇水溶液(一般浓度大于25%),常规干燥方法一般是在150℃的烘箱中干燥10小时以上才能达到恒重且易焦化。
微波是一种穿透力强的电磁波,它能穿透物体的内部,向被加热介质内部辐射微波电磁场,推动其极化分子的剧烈运动,使分子相互碰撞、摩擦而生热。
007聚乙二醇400检验标准操作规程

聚乙二醇-400检验标准操作规程1范围本标准建立了辅料聚乙二醇400的检验标准操作规程。
本标准适用于辅料聚乙二醇400的检验。
2 职责质量部按本标准进行检验。
3 规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款《中华人民共和国药典》 2010年版二部《微生物限度检查标准操作规程》编号《聚乙二醇400质量标准》编号4 操作规程4.1试剂与试药乙醇、乙醚、邻苯二甲酸酐的吡啶溶液、氢氧化钠滴定液(0.5mol/L)、酚酞的吡啶溶液(1→100)、磷酸盐标准缓冲液(PH6.86)、苯二甲酸标准缓冲液(PH4.00)、2号浊度标准液、黄色2号标准比色液、标准砷溶液、盐酸溶液(9→1000)、稀醋酸、氨试液、硫酸、浓过氧化氢溶液、盐酸5ml。
4.2仪器与设备凯氏烧瓶、比重瓶、平氏黏度计、恒温水浴锅、温度计、秒表、精密酸度计、烧杯、碱式滴定管、纳氏比色管、坩埚、试管、高温电阻炉、铁架台、250ml具塞锥形瓶、三角锥形瓶、天平、砷盐测定装置、毛细管(内径为0.8mm)。
4.3检验项目4.3.1 性状4.3.1.1作方方法(1)取本品,在明亮光线下,用目测和鼻闻法检测;再用水、乙醇、乙醚溶解。
(2)相对密度取本品,依法操作(《中国药典》2010版二部附录Ⅵ A比重瓶法)。
a、取洁净、干燥并精密称定重量的比重瓶,装满供试品(温度应低于20℃或个品种项下规定的温度)后,装上温度计(瓶中应无气泡),置20℃的水浴中放置若干分钟,使内容物的温度20℃,用滤纸除去溢出侧管的液体,立即盖上罩。
然后将比重瓶自水浴中取出,再用滤纸将比重瓶外面擦干净,精密称定,减去比重瓶的重量,求得供试品的重量后,将供试品倒出,洗净比重瓶,装满新沸过的冷水,再照上法测得同一温度时水的重量,按下式计算记得。
b、取洁净、干燥并精密称定重量的比重瓶,装满供试品(温度应低于20℃或个品种项下规定的温度)后,插入中心有毛细孔的瓶塞,用滤纸将从塞孔中溢出的液体擦干,置20℃恒温水浴中,放置数分钟,随着供试液温度上升,多余的液体将不断从塞孔溢出,随时用滤纸将瓶塞顶端擦干,待液体不再由塞孔溢出,迅速将比重瓶自水浴中取出,照上述a法,自“再用滤纸将比重瓶的外面擦净”起,依法测定,即得。
分光光度法测定纳滤膜对聚乙二醇的截留率

分光光度法测定纳滤膜对聚乙二醇的截留率摘要:利用分光光度法可以准确且便捷的测定不同分子量聚乙二醇(PEG)水溶液的浓度;而利用不同分子量的聚乙二醇水溶液可以检测过滤膜的分离性能。
本文在利用分光光度法测定聚乙二醇水溶液的实验基础上,初步研究了纳滤膜对不同分子量聚乙二醇的截留率。
关键词:分光光度法聚乙二醇纳滤膜截留率Determination of Nanofiltration Membrane Rejection Coefficient of Polyethylene Glycol by Spectrophotometry①Abstract:It is convenient and accurate for determination for different molecular weight polyethylene glycol(PEG) aqueous solution concentration by spectrophotometry. And we can use this method to determine the separation performance of the filter membranes. This paper research the rejection coefficient for the different molecular weight polyethylene glycol of nanofiltration membrane, which is based on the experiments for determination for polyethylene glycol aqueous solution concentration by spectrophotometry.Key words:spectrophotometry;polyethylene glycol(PEG);nanofiltration membrane;rejection coefficient材料是当代工业三大支柱之一,在名目众多的新材料中,功能膜近年来备受业界学者关注;而分离膜则是研究相对深入,应用最为广泛的功能膜。
聚乙二醇测定

聚乙二醇的测定一.药剂:碘 I2 氯化钡BaCl2 1000mg/L聚乙二醇(PEG)400 600 800 1000 2000 (分子量)碘化钾碘:0.05mol/L(I 原子量126.9 分子量253.8)氯化钡:5%(质量)分子量208.23二.实验步骤:100mg/L的PEG:取100ml的1000mg/L PEG400(400 600 800 1000 2000)于1L 的容量瓶,定容。
碘溶液:1.269g的碘单质溶于100mL水中。
氯化钡:5g的氯化钡溶于100mL水中。
三.实验操作分别取100mg/L的PEG 2.0 4.0 6.0 8.0 10mL于五只50mL的容量瓶中,纯水定容。
分别为4.0 8.0 12 16 20mg/L的PEG。
分别移去5mL纯水和以上五个溶液与比色管中(6只消解管)分别加入1.0mL的0.05mol I2溶液,再分别加入1.2mL的5%BaCl2 定容10mL(分别用移液器移取 2.8mL纯水) 溶液PEG浓度为0.0 2.0 4.0 6.0 8.0 10mg/L15min后在610nm的波长下测试。
4567891011121314151617181920212223242526272829303132世界脏到羞耻,谁有资格说难过。
创伤,也是一种成熟的象征。
你知道被迷惑,说明你尚且清醒,当你不知道迷惑时,才是最可怜的。
狂妄的人有救,自卑的人没法救。
伤害别人并不能掩盖自己的缺点,不过是自欺欺人罢了。
内心各种小心算计,心中不坦白,表达颠三倒四,五官又怎么端正。
多讲点笑话,以幽默的态度处事,这样子日子会好过一点。
活在别人的赞扬与掌声中,终究会成为一个敏感脆弱的人。
沉默是毁谤最好的答覆。
对人恭敬,无私奉献的爱心,让你拥有一切。
仇恨的心无法被治愈,只有宽容才能化解仇恨,饶过别人就是饶过自己。
接受眼前的现实,你才能超越现实。
聚乙二醇6000检验原始记录

取样日期
取样量
规 格
/
剂 型
/
检品来源
检验依据
企业标准JD-STB1066
检验项目
操作内容
结果/结论
7、环氧乙烷
和二氧六环
检验日期:检验人:
仪器:电子天平编号:;
试液:0.001%乙醛溶液配制:
;
8.1色谱条件
色谱仪:编号:
检测器:编号:
顶空进样器:编号:
色谱柱:聚二甲基硅氧烷为固定液
进样口温度:150℃
试液:浊度标准储备液批号:;
取本品g,加水50ml溶解后,溶液浊度0.5号浊度标准液;溶液颜色黄色号标准比色液。
检验日期:;检验人:;
□是□否
符合规定
4.炽灼残渣
仪器:电子天平、编号:;
箱式电阻炉、编号:;
取洁净坩埚于℃箱式电阻炉中恒重,加样品,于电炉上缓缓炽灼至完全炭化,放冷,加硫酸ml使湿润,继续在电炉上加热至硫酸蒸气除尽后,于℃箱式电阻炉中炽灼完全灰化至恒重。
空白溶液:同样品操作
取上述两种溶液,照《紫外-可见分光光度法检验标准操作规程》测定,在567nm波长处测定吸光度,并用空白溶液进行校正。
结果:供试品溶液的吸光度对照溶液的吸光度。
检验日期:;检验人:;
□是□否符合规定
检验员/日期: 复核员/日期:
编号:JD-RSGB1066-3
检验操作记录
品 名
聚乙二醇6000
取本品g、g,置100ml量瓶中,加水溶解并稀释至刻度,摇匀,用毛细管内径为1.0mm的平氏黏度计,照《黏度检验标准操作规程》(第一法)测定;温度:℃
T1= T2=
计算:
检验日期:;检验人:;
聚乙二醇的检测及其在切割分子量表征中的应用

聚乙二醇的检测及其在切割分子量表征中的应用陈佳萍;陆雯洁;徐伟燕;贾志舰;王灵辉【摘要】The molecular weight cut-off (MWCO) of membrane is a very important and usually characterized by measuring the concentration of model solutes with different molecular weights (MWs) in permeate and retentate.Polyethylene glycols (PEGs) are wildely used as the model solutes in ultrafiltration and nanofiltration process,for the diverse MWs,narrow MW distribution and low price.Therefor,determing PEG concentration accuratly and quickly is meaningful.Several analytic methods were introduced,including spectrophotometry,total organic carbon analysis,liquid chromatography,radiometric analysis and soon.Meanwhile,these mothods were compared with each other for MWCO determination.%切割分子量是分离膜的一个重要参数,一般通过一系列不同分子量物质的过滤实验,对比原液和滤液的浓度得到.聚乙二醇(PEG)具有分子量规格齐全、分子量分布窄和价格便宜等优点,是超滤膜和纳滤膜切割分子量测定的常用基准物质.因此,快速、准确地测定PEG溶液浓度具有重要的意义.本文介绍了不同PEG浓度检测方法的原理,包括分光光度法、总有机碳分析法、液相色谱法和放射性分析法等,并结合切割分子量的表征进行了比较.【期刊名称】《膜科学与技术》【年(卷),期】2017(037)003【总页数】5页(P112-116)【关键词】聚乙二醇;检测;分离膜;切割分子量【作者】陈佳萍;陆雯洁;徐伟燕;贾志舰;王灵辉【作者单位】宁波工程学院,宁波315211;宁波工程学院,宁波315211;宁波工程学院,宁波315211;宁波工程学院,宁波315211;宁波工程学院,宁波315211【正文语种】中文【中图分类】O65自20世纪60年代以来,微滤、反渗透、超滤、纳滤、透析及气体分离等膜分离技术相继迅速发展,被广泛应用于饮用水制备、食品工业、制药工业、生物制品加工、石油化工和工业废水处理等领域中[1].在这些新型过滤分离膜产品的开发过程中,其分离性能的测定至关重要,其中一个关键参数是切割分子量.切割分子量是指膜对某种特定溶质截留率达到90%以上时的最小分子量,一般可以通过一系列已知分子量的基准物质的截留率进行测定.对于超滤膜和纳滤膜来说,基准物质有蛋白质、聚乙二醇(PEG)、葡聚糖、染料分子和纳米粒子等[2].合适的基准物质应该具有与膜的作用力弱、分子量均一和易检测等特点.PEG是一种水溶性高分子,其可以通过阴离子聚合法制备,分子量分布窄,此外还具有与膜作用力弱、分子量规格齐全(从200到20 000 g/mol,甚至20 000 g/mol以上)、价格低廉、化学性质稳定等优点,是表征纳滤和超滤膜切割分子量的合适基准物[3].截留率是通过对比原液和滤液中待测物质的浓度得到的,因此,快速而准确地测定溶液中PEG浓度具有极大的意义.蛋白质和染料分子可以通过紫外 - 可见分光光度计测定浓度,盐类可以通过电导率测得浓度,而PEG即无特征的紫外-可见吸收峰,也无离子电导性,因此无法直接通过分光光度法或电导率法快速测定.文献报道的PEG测试方法比较多,但缺乏明确的机理解释,且叫法比较混乱.本文对PEG测试方法进行系统归纳,并结合其在切割分子量表征中的应用进行优缺点分析,以期为PEG测定方法的选择提供指导.1 分光光度法分光光度法是通过测定被测物质在特定波长处的吸收度,对该物质进行定量分析的方法.由于PEG在紫外 - 可见光区域没有可以用来定量的特征吸收峰,所以需先用化学试剂进行显色,再测定吸光度.文献报道的显色剂主要有两种,碘试剂和Dragendorff试剂(以下简称D试剂).1.1 碘试剂碘试剂的组成一般包括碘、碘化钾和BaCl2,其显色原理如图1所示.图1中示意的是最简单情况,实际上Ba2+可以与多个O络合,PEG链可以络合多个Ba2+.PEG通过氧原子与水溶液中的Ba2+发生络合,再与I3-形成红棕色的复合物.该复合物的最大吸收波长在510 nm左右,而I3-的最大吸收波长在350 nm,所以能够根据该复合物的吸光度进行PEG浓度的定量.Ba2+与PEG有强的络合能力[4],可以增加I3-的络合量,从而提高了检测灵敏度.该方法的检测范围一般在40~200 mg/L之间.图1 PEG与碘试剂的显色原理示意图Fig.1 Chromogenic mechanism of PEG(polyethylene glycol) with I2 reagent除了Ba2+外,也可以使用其它具有络合能力的物质.比如使用硼酸为络合剂时,PEG的浓度检测限可以下降到2~20 mg/L,且依旧保持良好的线性关系[5].由于碘显色法所使用的试剂较为常见,测试过程也较为简单,所以其作为检测滤液中PEG浓度的研究报道较多[6-8].需要注意的是,PEG与碘的络合物稳定性较差,容易形成沉淀,而且PEG分子量越大,浓度越高,络合物越不稳定.因此,在测试的时候,一方面要严格控制测试的时间,另一方面要控制PEG的检测浓度,防止出现沉淀.1.2 D试剂D试剂常用于生物碱的检测,其由A液和B液混合而成,A液成分是次硝酸铋和乙酸,B液为KI水溶液,A液和B液混合时生成BiI4-,这是D试剂的有效成分.PEG与D试剂的显色原理如图2所示,图中只示意最简单情况,实际上PEG链可以结合多个H+.在酸性条件下,PEG与H+作用而带正电,其再与BiI4-作用,生成桔红色的PEG - BiI4-复合物,该复合物的最大吸收波长为510 nm.国家海洋局行业标准HY/T 050—1999 中空纤维超滤膜测试方法[9]中,规定使用D试剂显色法检测PEG的浓度,很多国内外实验室[10-12]也使用D试剂显色法.倪澄峰等[13]考察了D试剂用量、存放条件、缓冲溶液用量以及显色时间等因素对PEG溶液吸光度的影响,得出按照行标要求进行测试的必要性和依据.图2 PEG与D试剂的显色原理示意图Fig.2 Chromogenic mechanism of PEG with Dragendorff reagentD试剂的配制中,经常会由于混合液的pH升高,生成BiI3和BiOI沉淀,这会干扰吸光度的测定,使得标准曲线线性较差.贾志谦等[14]对D试剂的配制进行了改良,改用HAc或HCl溶液进行稀释,发现能很好地抑制沉淀生成,标准曲线的线性也得到了提高.1.3 其它显色剂除了上述I3-和BiI4-两种阴离子显色剂外,也可以使用其它具有紫外或可见光吸收的阴离子,如苦味酸[15]、Co(SCN)42-[16]和Fe(SCN)63-[17]等.这些阴离子与PEG形成的复合物在水中是沉淀,不能直接进行吸光度测定,需要通过有机溶剂(如二氯甲烷或氯仿等)定量萃取出来,然后再进行吸光度检测.以上方法已经用于水、尿液和血液中PEG的检测,但是在切割分子量表征上的应用还未见报道,这主要是由于增加了有机溶剂萃取操作.2 总有机碳(TOC)分析法TOC分析法的原理是水溶液中的有机物在高温和催化剂的作用下完全分解为CO2,通过检测CO2的含量,得到溶液中的有机碳总量,如果已知有机物的分子式,则可以进一步计算出该有机物的浓度.可以看出,TOC并不仅仅局限于PEG浓度的测定,还能够测定几乎所有有机物的水溶液,所以该方法在分离膜切割分子量的测定上有较大的优势.相比于分光光度法来说,TOC法具有快速、自动化、稳定、精确度高、且影响因素较少等优点,但成本相对较高[18].许多单位和国内外实验室[19-20]采用TOC分析仪来测定分离膜的切割分子量.卞晓云等[21]通过TOC法系统考察了PEG的超滤过程,解释了PEG超滤过程中的分离现象,并得出了超滤机制的内在因素.由于TOC法能检测出水溶液中的全部有机物,而并不能特异性区分PEG和其它有机物,因此,为了得到准确的PEG浓度,需要确保溶液中无其它有机物杂质.这要求配制用的水不含有机污染物,同时要对膜进行充分清洗,避免膜内有机添加剂和溶剂等的溶出而造成滤液污染.3 液相色谱法液相色谱法是一种分离和分析方法,依据物质与色谱柱作用力的不同,在不同时间洗脱而实现分离,并利用检测器实现洗脱组分的浓度测定.根据分离机理,液相色谱有多种类型,如根据尺寸排阻原理的体积排阻色谱(SEC),根据分离物质与非极性柱子之间分配作用的反相色谱(RPC).检测器的种类较多,如最常见的紫外检测器,由于PEG在紫外区域没有特征吸收峰,所以一般使用示差折光检测器(RID)和蒸发光散射检测器(ELSD)这两种通用型的检测器.在色谱图中,检测信号的高度或者峰面积与对应物质的浓度是成正比的,通过测定标准曲线,就能关联浓度与检测信号的关系.SEC和RPC在PEG浓度检测上的应用比较多.3.1 SECSEC法进行切割分子量测定时有两种膜过滤模式,单组分过滤和多组分过滤.单组分过滤指进行截留过滤用的溶液中只含有一种分子量的PEG,前面讨论的测试过程都是使用这个过滤模式.该模式下,对原液和滤液进行SEC测试后,利用曲线中PEG峰的峰高比或者峰面积比,可以计算得到截留率.多组分过滤指过滤用的原液中含有多个分子量的PEG.由于SEC具有分离作用,原液和滤液的SEC曲线中会出现多个峰,分别对应于混合溶液中不同分子量的PEG,通过对比相应峰的峰高或峰面积,就得到各个分子量PEG的截留率.可以明显看出,使用多组分过滤模式时,一次过滤实验就能得到截留率与分子量的关系曲线,大大节省了实验时间.事实上,由于SEC法测试成本较高,样品检测时间较长(一般在40 min),主要用于多组分过滤模式[22-24].该模式也存在着一些缺点,比如混合液中的大分子组成可能会堵塞膜孔,使得小分子难以通过膜孔,截留率增大[25],此外,SEC的测试精度较低,对于分子量小于300的PEG难以测定[26].3.2 RPCRPC用于切割分子量的测定时,也有单组分过滤[27]和多组分过滤[28]两种模式,其优势也在于多组分过滤模式上.RPC根据样品的极性差别进行分离,而不同分子量PEG之间的极性差别较小,特别当PEG分子量较大时,极性端羟基的贡献非常小,极性差别更小,分离非常困难.为了实现好的分离效果,需要对流动相组成进行严格而细致地调控.这也说明了RPC更适用于小分子量PEG(分子量小于1 000)的检测,这对纳滤膜来说是充分的.Li等[29]以PEG为基准物质,使用RPC/ELSD进行了有机纳滤实验,发现PEG峰基线平整,而且灵敏度高,认为RPC结合ELSD检测器是非常强大的测定PEG截留率的方法,并且可以扩展为其它有机物的截留表征.Rohani等[28]用C - 8柱结合ELSD检测器研究了PEG的色谱分离效果,发现当分子量在106~1 646之间时,分离精度非常高,谱峰之间仅有一个PEG重复单元的差别,而且峰形与峰间距都非常好,同时进行了商用纳滤膜和超滤膜的水相过滤实验,得到的切割分子量与厂家标示值较接近.4 其它方法除了以上三大类测试方法外,还有其它的报道,但是在分离膜中的应用较少,以下只是作简单介绍.4.1 RID法当溶质与溶剂的折光指数(RID)不同时,溶液的折光指数与溶质浓度成正比,这是RID的检测原理.RID通常具有非常高的灵敏度,而且重复性好.前面提到的色谱结合RID法,主要是针对多组分过滤模式下的检测,而对于单组分过滤模式来说,样品无需经过色谱柱,因此可以直接由RID测得PEG浓度[30].然而,该方法在切割分子量表征上的报道却很少,这一方面可能由于RID的价格比较贵,另一方面滤液中可能会含有膜的溶出物,使得测试结果发生偏差,特别是当截留率高的时候,误差更大.4.2 光干涉法PEG溶液的浓度不同时,经过溶液的平行光干涉点位置也会不同,干涉点位移的大小与浓度成正相关.该方法需用到光干涉仪,测试方法较简单,但是测量误差较大,在0~100 mg/L内甚至达到±5%[31].4.3 重量法在Ba2+的作用下,PEG与沉淀剂形成一定组成的沉淀,经过滤和干燥后,通过沉淀质量就能对PEG进行定量,沉淀剂主要有硅钨酸和磷钼酸[32].该方法测试时间长,而且精度也不高.4.4 放射性分析PEG与133Ba2+在水溶液中发生络合,再与dicarbolide([(C2B9H11Cl2)2Co]-)定量形成复合物,该复合物用有机溶剂萃取后,测定放射性,根据标准曲线得出PEG的浓度[33].4.5 原子吸收法PEG与硫氰酸根金属离子配合物,如Co(SCN)42-和Zn(SCN)42-等,发生配位反应,定量形成复合物,该复合物用有机溶剂萃取,再利用原子吸收法得到复合物中的金属离子含量,再反推得到PEG浓度[34-35].5 小结PEG的检测对象可以分为两类,单组成PEG溶液和多组成PEG溶液.要得到分离膜的切割分子量,需要进行多次单组成PEG溶液或者单次多组成PEG溶液的截留实验.多组成PEG溶液的检测需要结合色谱,该方法能快速得到切割分子量,但存在着大分子量PEG干扰结果、仪器测试精度偏低等问题.单组成PEG溶液过滤模式下,测试时间较长,但能避免不同分子量PEG间的干扰问题.PEG的测定方法较多,根据原理主要可以分为3大类:(1) 利用PEG的物理性质与浓度的定量关系,如RID法和光干涉法等;(2) 根据PEG的元素组成,如TOC法;(3)通过PEG与特定试剂的反应转化为可测定的复合物,如分光光度法、放射性分析法、原子吸收法和重量法等.以上方法各有优缺点,TOC法操作简单、精度高;分光光度法试剂便宜、准确性好.目前来说,在分离膜切割分子量的表征中,相对优势比较明显的,文献报道比较多的PEG测定方法是TOC法与分光光度法中的碘试剂法和D试剂法.参考文献:[1] 徐又一, 徐志康. 高分子膜材料[M]//北京:化学工业出版社, 2005.[2] 潘献辉, 王晓楠, 张艳萍, 等. 超滤膜截留性能检测用基准物质研究与应用进展[J]. 膜科学与技术, 2013, 33(2): 104-108.[3] 汪多仁. 聚乙二醇的应用与合成进展[J]. 化学工业与工程技术, 2000, 21(5): 21-23.[4] Yanagida S, Takahashi K, Okahara M. Metal-ion complexation of noncyclic poly(oxyethylene) derivatives. II. PMR studies of the complexation with alkali and alkaline-earth metal cations[J]. Bull Chem Soc Japan, 1978, 51(5): 1294-1299.[5] 俞建君. 对碘沉淀法测定聚乙二醇浓度的改进[J]. 过滤与分离, 2008, 18(4): 43-45.[6] 武少华, 何宏, 袁淑琴, 等. 氯化钡法及其在聚砜超滤膜性能测定中的应用[J]. 水处理技术, 1995(4): 193-197.[7] Chen Q, Yu P P, Huang W Q, et al. High-flux composite hollow fiber nanofiltration membranes fabricated through layer-by-layer deposition of oppositely charged crosslinked polyelectrolytes for dye removal[J]. J Membr Sci, 2015, 492: 312-321.[8] Li Y F, Su Y L, Li J Y, et al. Preparation of thin film composite nanofiltration membrane with improved structural stability through the mediation of polydopamine[J]. J Membr Sci, 2015, 476: 10-19.[9] 国家海洋局. HY/T 050—1999 中空纤维超滤膜测试方法[S]. 北京, 1999.[10] Han J N, Yang D L, Zhang S H, et al. Effects of dope compositions on the structure and performance of PPES hollow fiber ultrafiltration membranes[J]. J Membr Sci, 2009, 345(s1/2): 257-266.[11] Vatanpour V, Esmaeili M, Farahani M. Fouling reduction and retention increment of polyethersulfone nanofiltration membranes embedded by amine-functionalized multi-walled carbon nanotubes[J]. J Membr Sci, 2014, 466: 70-81.[12] Safarpour M, Khataee A, Vatanpour V. Preparation of a novel polyvinylidene fluoride (PVDF) ultrafiltration membrane modified with reduced graphene oxide/titanium dioxide (TiO2) nanocomposite with enhanced hydrophilicity and antifouling properties[J]. Ind Eng Chem Res, 2014, 53(34): 13370-13382.[13] 倪澄峰, 安树林, 邓利华, 等. D试剂法超滤膜截留聚乙二醇的研究[J]. 膜科学与技术, 2016, 36(1): 109-113.[14] Jia Zhiqian, Tian Chunai. Quantitative determination of polyethylene glycol with modified Dragendorff reagent method[J]. Desalination, 2009, 247(1/3): 423-429.[15] Favretto L, Tunis F. Determination of polyoxyethylene alkylphenyl ether non-ionic surfactants in waters[J]. Analyst, 1976, 101(1200): 198-202.[16] Calzolari C, Favretto L, Tunis F. Determination of polyoxyethylene p-t-nonylphenyl ethers in pomades[J]. Analyst, 1974, 99: 171-177.[17] 韩润平, 尹建四. 用硫氰铁铵 - 氯仿体系光度法测定尿样中的聚乙二醇 -600[J]. 光谱学与光谱分析, 1999, 19(3): 478-480.[18] 周晨, 陆晓峰, 侯铮迟, 等. 分光光度法和总有机碳法对超滤膜截留性能测定的比较[J]. 膜科学与技术, 2011, 31(5): 34-39.[19] Zhang G J, Song X, Ji S L, et al. Self-assembly of inner skin hollow fiber polyelectrolyte multilayer membranes by a dynamic negative pressure layer-by-layer technique[J]. J Membr Sci, 2008, 325(1): 109-116.[20] Laakso T, Kallioinen M, Pihlajamäki A, et al. Polyelectrolyte multilayer coated ultrafiltration membranes for wood extract fractionation[J]. Sep Purif Technol, 2015, 156(2): 772-779.[21] 卞晓云, 刘文强, 杨刚, 等. 聚乙二醇超滤过程的考察及模型化分析[J]. 南京工业大学学报:自然科学版, 2012, 34(5): 12-15.[22] Schlichter B, Mavrov V, Chmiel H. Comparative characterisation of different commercial UF membranes for drinking water production[J]. J Water Supply: Res Technol-AQUA, 2000, 49(6): 321-328.[23] Yanagishita H, Nakane T, Takatsu S, et al. Study on evaluation of ultrafiltration membranes (Ⅱ). Membrane characterization of molecular weight cut-off by PEG solutions[J]. Membrane, 1990, 15(2): 56-61. [24] Causserand C, Rouaix S, Akbari A, et al. Improvement of a method for the characterization of ultrafiltration membranes by measurements of tracers retention[J]. J Membr Sci, 2004, 238(1/2): 177-190.[25] Tam C, Tremblay A. Membrane pore characterization-comparison between single and multicomponent solute probe techniques[J]. J Membr Sci, 1991, 57(2): 271-287.[26] Trägårdh G. Proceedings of the symposium on membrane technologycharacterization methods for ultrafiltration membranes[J]. Desalination, 1985, 53(1): 25-35.[27] Yoo J, Kim J, Kim Y, et al. Novel ultrafiltration membranes prepared from the new miscible blends of polysulfone with poly(1-vinylpyrrolidone-co-styrene) copolymers[J]. J Membr Sci, 2003, 216(1/2): 95-106.[28] Rohani R, Hyland M, Patterson D. A refined one-filtration method for aqueous based nanofiltration and ultrafiltration membrane molecular weight cut-off determination using polyethylene glycols[J]. J Membr Sci, 2011, 382(1/2): 278-290.[29] Li X F, Monsuur Fred, Denoulet Bart, et al. Evaporative light scattering detector: Toward a general molecular weight cutoff characterization of nanofiltration membranes[J]. Anal Chem, 2009, 81(5): 1801-1809.[30] Lin J, Ladisch M, Patterson J, et al. Determining pore size distribution in wet cellulose by measuring solute exclusion using a differential refractometer[J]. Biotechnol Bioeng, 1987, 29(8): 976-81.[31] 高来宝, 陶庆泰. 用光干涉法测定极稀聚乙二醇水溶液的浓度[J]. 水处理技术, 1986(3):47-49.[32] Oliver J, Preston C. Estimation of non-ionic detergents[J]. Nature, 1949, 164(3): 242-243.[33] Seluck P, Krtil J, Rais J. A radiometric method for the determination of PEG - 1000 concentration[J]. J Radioanal Nucl Chem, 1985, 94(3): 177-184.[34] Anderson N, Girling J. Determination of polyoxyethylene non-ionic surfactants at trace levels[J]. Analyst, 1982, 107(1276): 836-838.[35] Françclois M, Wim J, Johan K. Determination of nonionic surfactants in water by atomic absorption spectrometry[J]. Inter J Environ Anal Chem, 1985, 19(2): 155-164.。
非分配示踪剂和分配示踪剂浓度检测方法

非分配示踪剂和分配示踪剂浓度检测方法作者:侯长利来源:《科技创新导报》2011年第21期摘要:准确测量示踪剂浓度是决定示踪剂技术成败的关键因素。
本文分别采用分光光度法和气相色谱法测得了非分配示踪剂硫氰酸钾和分配示踪剂正丁醇的浓度标准曲线,并得到了回归公式。
室内岩心流动实验表明,该浓度测试方法是可靠的。
关键词:硫氰酸钾正丁醇井间示踪剂油田中图分类号:TP2 文献标识码:A 文章编号:1674-098X(2011)07(c)-0116-01井间示踪剂法测定油层剩余油饱和度是应用色谱原理来实现的。
亲油的分配示踪剂和亲水的非分配示踪剂在流动过程中发生分离,其浓度峰值到达地面产生一个时间差,这种时间差与剩余油饱和度有定量关系。
因此准确测量示踪剂浓度非常重要。
不同油田由于其地层水和岩石物性等各方面的差异,选择的示踪剂也不同。
本文针对大庆油田南二区试验区选用的硫氰酸钾和正丁醇,结合大庆油田地层水的实际情况,给出了一套测量井间示踪剂浓度的方法。
1 硫氰酸根离子浓度的定量分析方法1.1 原理水溶液中的与生成血红色络合物,反应式如下:(1)此血红色络合物的最大吸收峰在455nm处。
此反应可以用于测定微量离子。
为了保证配制的溶液中的铁以形式存在,以及达到必要的PH值。
则应用具有强氧化性的硝酸将氧化为。
1.2 仪器与试剂100mg/L的标准溶液;25%的硝酸溶液;5%的溶液;721型分光光度计;50ml容量瓶;5ml移液管。
1.3 测试方法采用分光光度法[1]测定的浓度。
在固定液层厚度及入射光的波长和强度下,测定一系列不同浓度标准溶液的吸光度,以吸光度为纵坐标,标准溶液浓度为横坐标作图,得到工作曲线。
1.3.1 标准曲线的绘制用移液管分别吸取标准溶液0.5,1.0,2.0,3.0,4.0,5.0,6.0,7.0ml于八只50ml容量瓶中,加入Fe3+溶液5ml,用蒸馏水稀释至刻度,摇匀,放置15min,用2cm的比色皿,以不加SCN的空白试液作为参比溶液,用分光光度计分别测其吸光度。
007聚乙二醇400检验标准操作规程

聚乙二醇-400检验标准操作规程1范围本标准建立了辅料聚乙二醇400的检验标准操作规程。
本标准适用于辅料聚乙二醇400的检验。
2 职责质量部按本标准进行检验。
3 规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款《中华人民共和国药典》 2010年版二部《微生物限度检查标准操作规程》编号《聚乙二醇400质量标准》编号4 操作规程4.1试剂与试药乙醇、乙醚、邻苯二甲酸酐的吡啶溶液、氢氧化钠滴定液(0.5mol/L)、酚酞的吡啶溶液(1→100)、磷酸盐标准缓冲液(PH6.86)、苯二甲酸标准缓冲液(PH4.00)、2号浊度标准液、黄色2号标准比色液、标准砷溶液、盐酸溶液(9→1000)、稀醋酸、氨试液、硫酸、浓过氧化氢溶液、盐酸5ml。
4.2仪器与设备凯氏烧瓶、比重瓶、平氏黏度计、恒温水浴锅、温度计、秒表、精密酸度计、烧杯、碱式滴定管、纳氏比色管、坩埚、试管、高温电阻炉、铁架台、250ml具塞锥形瓶、三角锥形瓶、天平、砷盐测定装置、毛细管(内径为0.8mm)。
4.3检验项目4.3.1 性状4.3.1.1作方方法(1)取本品,在明亮光线下,用目测和鼻闻法检测;再用水、乙醇、乙醚溶解。
(2)相对密度取本品,依法操作(《中国药典》2010版二部附录Ⅵ A比重瓶法)。
a、取洁净、干燥并精密称定重量的比重瓶,装满供试品(温度应低于20℃或个品种项下规定的温度)后,装上温度计(瓶中应无气泡),置20℃的水浴中放置若干分钟,使内容物的温度20℃,用滤纸除去溢出侧管的液体,立即盖上罩。
然后将比重瓶自水浴中取出,再用滤纸将比重瓶外面擦干净,精密称定,减去比重瓶的重量,求得供试品的重量后,将供试品倒出,洗净比重瓶,装满新沸过的冷水,再照上法测得同一温度时水的重量,按下式计算记得。
b、取洁净、干燥并精密称定重量的比重瓶,装满供试品(温度应低于20℃或个品种项下规定的温度)后,插入中心有毛细孔的瓶塞,用滤纸将从塞孔中溢出的液体擦干,置20℃恒温水浴中,放置数分钟,随着供试液温度上升,多余的液体将不断从塞孔溢出,随时用滤纸将瓶塞顶端擦干,待液体不再由塞孔溢出,迅速将比重瓶自水浴中取出,照上述a法,自“再用滤纸将比重瓶的外面擦净”起,依法测定,即得。
聚乙二醇标准及检验方法

聚乙二醇标准及检验方法聚乙二醇根据平均分子量的不同分为许多种,这里只涉及四种即聚乙二醇200、400、600和800。
一、聚乙二醇2001、物性乙二醇200是一种无色黏稠液体。
有轻微特殊气味。
略有吸湿性。
溶于水和丙酮。
相对密度 1.127。
凝固点-15℃。
黏度(99℃)4.3μm2/s,【粘度(mm2/s,40℃) 21-24】。
闪点(开杯)177℃。
2、检查a、平均分子量取本品约1.2g,精密称定,置干燥的250ml 具塞锥形瓶中,精密加邻苯二甲酸酐的吡啶溶液(取邻苯二甲酸酐14g ,溶于无水吡啶100ml 中,放置过夜,备用)25ml,摇匀,置沸水浴中,加热30~60分钟,取出冷却,精密加入氢氧化钠滴定液(0.5mol/L)50ml,以酚酞的吡啶溶液(1→100)为指示剂,用氢氧化钠滴定液(0.5mol/L)滴定至显红色,并将滴定的结果用空白试验校正。
供试量(g) 与4000的乘积,除以消耗氢氧化钠滴定液(0.5mol/L)的容积(ml),即得供试品的平均分子量,应为190~210。
b、酸度取本品1.0g,加水20ml溶解后,依法测定(附录Ⅵ H),pH值应为4.0~7.0 。
C、溶液的澄清度与颜色取本品5.0g,加水50ml溶解后,溶液应澄清无色;如显浑浊,与2号浊度标准液(附录Ⅸ B)比较,不得更浓;如显色,与黄色2号标准比色液(附录Ⅸ A第一法)比较,不得更深。
d、乙二醇与二甘醇取乙二醇与二甘醇各50mg,置100ml 量瓶中,加水稀释至刻度,摇匀,作为对照溶液;另取本品4.0g,置10ml量瓶中,加水稀释至刻度,摇匀,作为供试品溶液。
取上述溶液,照气相色谱法〔附录Ⅴ E〕,以硅藻土为载体,山梨醇为固定相,在柱温160 ℃测定。
精密量取试品溶液与对照溶液各2μl,注入气相色谱仪,记录色谱图;按内标发以基线构成的面积称峰面积。
根据面积计算含量。
含乙二醇与二甘醇均不得过0.25%(g/g)。
聚乙二醇6000检验操作规程

聚乙二醇6000检验操作规程1 目的:建立聚乙二醇6000检验操作规程。
2 适用范围:适用于聚乙二醇6000检验操作。
3 职责:检验人员对本规程的实施负责。
4 规程:4.1 编制依据:《中国药典》2010年版二部P1244。
4.2 质量指标:见《聚乙二醇6000质量标准》。
4.3 仪器与用具:PH计、电子天平、电阻炉。
4.4 试药与试液:乙醚、乙醇、吡啶溶液、氢氧化钠滴定液(0.5mol/L)。
4.5 操作方法:4.5.1 性状:本品为白色蜡状固体薄片或颗粒状粉末;略有特臭。
本品在水或乙醇中易溶,在乙醚中不溶。
凝点:取本品,照《凝点检查操作规程》测定,本品的凝点为53-58℃。
黏度:取本品25.0g,置100ml量瓶中,加水溶解并稀释至刻度,摇匀,用毛细管内径为1.0mm的平氏黏度计,按《黏度检查操作规程》第一法测定,在40℃时的运动黏度为10.5-16.5mm2/S。
羟值:本品的羟值为16-22。
4.5.2 鉴别4.5.2.1 化学反应:取本品0.05g,加稀盐酸溶液5ml和氯化钡试液1ml,振摇,滤过,在滤液中加入10%磷钼酸溶液1ml,产生黄绿色沉淀。
4.5.2.2 化学反应:取本品0.1g,置试管中,加入硫氰酸钾和硝酸钴各0.1g,混合后,加入二氯甲烷5ml,溶液呈蓝色。
4.5.3 检查4.5.3.1 平均分子量:取本品约12.5g,精密称定,置干燥的250ml具塞锥形瓶中,加入吡啶25ml,加温使溶解,放冷,精密加入邻苯二甲酸酐的吡啶溶液(取邻苯二甲酸酐14g,溶于无水吡啶100ml中,放置过夜,备用)25ml,摇匀,置沸水浴中,加热30-60分钟,取出冷却,精密加入氢氧化钠滴定液(0.5mol/L)50ml,以酚酞的吡啶溶液(1→100)为指示剂,用氢氧化钠滴定液(0.5mol/L)滴定至显红色,并将滴定的结果用空白试验校正。
供试量(g)与4000的乘积,除以消耗氢氧化钠滴定液(0.5mol/L)的容积(ml),即得供试品的平均分子量,平均分子量应为5400-7800。
聚乙二醇6000检验操作规程

聚乙二醇6000检验操作规程1 目的:建立聚乙二醇6000检验操作规程。
2 适用范围:适用于聚乙二醇6000检验操作。
3 职责:检验人员对本规程的实施负责。
4 规程:4.1 编制依据:《中国药典》2010年版二部P1244。
4.2 质量指标:见《聚乙二醇6000质量标准》。
4.3 仪器与用具:PH计、电子天平、电阻炉。
4.4 试药与试液:乙醚、乙醇、吡啶溶液、氢氧化钠滴定液(0.5mol/L)。
4.5 操作方法:4.5.1 性状:本品为白色蜡状固体薄片或颗粒状粉末;略有特臭。
本品在水或乙醇中易溶,在乙醚中不溶。
凝点:取本品,照《凝点检查操作规程》测定,本品的凝点为53-58℃。
黏度:取本品25.0g,置100ml量瓶中,加水溶解并稀释至刻度,摇匀,用毛细管内径为1.0mm的平氏黏度计,按《黏度检查操作规程》第一法测定,在40℃时的运动黏度为10.5-16.5mm2/S。
羟值:本品的羟值为16-22。
4.5.2 鉴别4.5.2.1 化学反应:取本品0.05g,加稀盐酸溶液5ml和氯化钡试液1ml,振摇,滤过,在滤液中加入10%磷钼酸溶液1ml,产生黄绿色沉淀。
4.5.2.2 化学反应:取本品0.1g,置试管中,加入硫氰酸钾和硝酸钴各0.1g,混合后,加入二氯甲烷5ml,溶液呈蓝色。
4.5.3 检查4.5.3.1 平均分子量:取本品约12.5g,精密称定,置干燥的250ml具塞锥形瓶中,加入吡啶25ml,加温使溶解,放冷,精密加入邻苯二甲酸酐的吡啶溶液(取邻苯二甲酸酐14g,溶于无水吡啶100ml中,放置过夜,备用)25ml,摇匀,置沸水浴中,加热30-60分钟,取出冷却,精密加入氢氧化钠滴定液(0.5mol/L)50ml,以酚酞的吡啶溶液(1→100)为指示剂,用氢氧化钠滴定液(0.5mol/L)滴定至显红色,并将滴定的结果用空白试验校正。
供试量(g)与4000的乘积,除以消耗氢氧化钠滴定液(0.5mol/L)的容积(ml),即得供试品的平均分子量,平均分子量应为5400-7800。
《中国药典》2020版—聚乙二醇2000国家药用辅料标准

附件:聚乙二醇2000Juyi’erchun 2000Polyethylene Glycol 2000本品为环氧乙烷和水缩聚而成的混合物,分子式以H(OCH2CH2)n OH 表示,其中n 代表氧乙烯基的平均数。
【性状】本品为白色蜡状固体或颗粒状粉末;略有特臭。
本品在水、乙醇中易溶。
凝点本品的凝点(通则0613)为45~50℃。
黏度取本品25.0g,置100ml 量瓶中,加水溶解并稀释至刻度,摇匀,用毛细管内径为0.6mm 的平氏黏度计,依法测定(通则0633 第一法),在40℃时的运动黏度为3.5~4.5 mm2/s。
【鉴别】(1)取本品0.05g,加稀盐酸5ml 和氯化钡试液1ml,振摇,滤过;在滤液中加入10%磷钼酸溶液1ml,产生黄绿色沉淀。
(2)取本品0.1g,置试管中,加入硫氰酸钾和硝酸钴各0.1g,混合后,加入二氯甲烷5ml,溶液呈蓝色。
【检查】平均分子量取本品约6.0g,精密称定,置干燥的250ml 具塞锥形瓶中,精密加邻苯二甲酸酐的吡啶溶液(取邻苯二甲酸酐14g,溶于无水吡啶100ml 中,放置过夜,备用)25ml,摇匀,加少量无水吡啶于锥形瓶口边缘封口,置沸水浴中,加热30 分钟,取出冷却,精密加入氢氧化钠滴定液(0.5mol/L)50ml,以酚酞的吡啶溶液(1→100)为指示剂,用氢氧化钠滴定液(0.5mol/L)滴定至显红色,并将滴定的结果用空白实验校正。
供试量(g)与4000 的乘积,除以消耗氢氧化钠滴定液(0.5mol/L)的容积(ml),即得供试品的平均分子量,应为1800~2200。
酸度取本品1.0g,加水20ml 溶解后,依法测定(通则0631),pH 值应为4.0~7.0。
溶液的澄清度与颜色取本品5.0g,加水50ml 溶解后,依法检查(通则0901 与通则0902),溶液应澄清无色;如显浑浊,与2 号浊度标准液(通则0902 第一法)比较,不得更浓;如显色,与黄色2 号标准比色液(通则0901 第一法)比较,不得更浓。
分析测试分光光度法测定不同分子量聚乙二醇浓度

mination of PEG content etc. are investigated. The optimal conditions are as follows : amount of iodine and BaCl2 used 1. 0 mL and 1. 2 mL ; chromogenic reaction time 1200~1400s. This method of determination is
Determination of Polyethylene Glycol Content with
Various Molecular Weight by Ultraviolet Spectrophotometry Method
L IU Hai - xia , ZHANG Hao - qin , L IU Jin - dun , L UO Qing - tao (College of Chemical Engineering , Zhengzhou University , Zhengzhou 450002 , China)
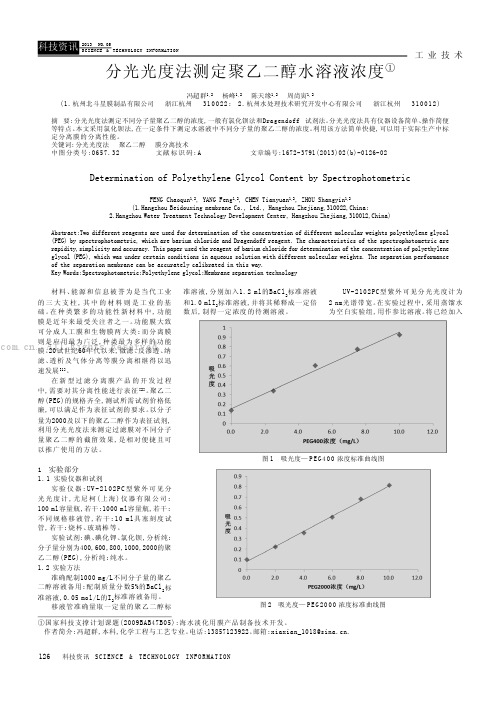
图 1 吸光度 - PEG浓度标准曲线
图 1 结果表明 ,用该方法对纳滤膜分离性能进 行表征 ,具有较高的精确度 。 3. 2 实验条件的优化 3. 2. 1 显色剂用量 3. 2. 1. 1 I2 用量的影响 (见图 2)
图 4 不同 PEG分子量的动力学曲线
3. 2. 3 扫描波长的选择
聚乙二醇试剂价格低 、易买到 ,以聚乙二醇作为 标准物质 ,用分光光度法测定纳滤膜的截留性能 ,操 作简单 、稳定性好 。在一定的浓度范围内 ,标准曲线 的线性关系较好 ,测定的准确度高 。在实际膜的截 留率分析中采用一般的分光光度计 ,便于推广应用 。 参考文献 :
聚乙二醇化蛋白质类药物的结构分析方法

聚乙二醇化蛋白质类药物的结构分析方法摘要近年来,聚乙二醇修饰技术已经成为改良蛋白药物最有效的技术之一,得到越来越广泛的应用。
鉴于聚乙二醇本身的特性与蛋白质结构的复杂性,如何使它更好的修饰蛋白并对修饰后产物进行分析鉴定是研究的重点与难点。
本文主要就PEG定点修饰的技术和PEG化蛋白的成分、结构分析方法及各种方法的优缺点作一介绍,并展望了未来的发展趋势。
Abstract Polyethylene Glycol(PEG) modification technology has become one of the most effective technologies in protein drugs ,getting more and more widely used in recent years. In view of the characteristics of polyethylene glycol itself and the multiple structure of proteins,it’s necessary and difficult to achieve better modification and analyse the Modified products. In this paper,we fixed on the PEG-modified-protein technology and components, structural analysis methods and the advantages and disadvantages of various methods to make a presentation and prospect the future trend of development.关键词:蛋白类药物,聚乙二醇化,修饰位点,结构分析方法Key words:Protein drugs, Peginterferon, modification sites, structure analysis methods.正文药物的聚乙二醇修饰即聚乙二醇化,是将活化的聚乙二醇通过化学方法偶联到蛋白、多肽、小分子有机药物和脂质体上。
分光光度法测定聚乙二醇水溶液浓度
126科技资讯 SC I EN C E & TE C HN O LO G Y I NF O R MA T IO N工 业 技 术材料、能源和信息被誉为是当代工业的三大支柱,其中的材料则是工业的基础。
在种类繁多的功能性新材料中,功能膜是近年来最受关注者之一。
功能膜大致可分成人工膜和生物膜两大类;而分离膜则是应用最为广泛,种类最为多样的功能膜。
20试世纪60年代以来,微滤、反渗透、纳滤、透析及气体分离等膜分离相继得以迅速发展[1]。
在新型过滤分离膜产品的开发过程中,需要对其分离性能进行表征[2]。
聚乙二醇(PEG)的规格齐全,测试所需试剂价格低廉,可以满足作为表征试剂的要求。
以分子量为2000及以下的聚乙二醇作为表征试剂,利用分光光度法来测定过滤膜对不同分子量聚乙二醇的截留效果,是相对便捷且可以推广使用的方法。
1 实验部分1.1实验仪器和试剂实验仪器:UV -2102PC 型紫外可见分光光度计,尤尼柯(上海)仪器有限公司;100ml容量瓶,若干;1000ml容量瓶,若干;不同规格移液管,若干;10ml具塞刻度试管,若干;烧杯、玻璃棒等。
实验试剂:碘、碘化钾、氯化钡,分析纯;分子量分别为400,600,800,1000,2000的聚乙二醇(PEG),分析纯;纯水。
1.2实验方法准确配制1000mg/L不同分子量的聚乙二醇溶液备用;配制质量分数5%的BaCl 2标准溶液,0.05mol/L的I 2标准溶液备用。
移液管准确量取一定量的聚乙二醇标①国家科技支撑计划课题(2009BAB47B05):海水淡化用膜产品制备技术开发。
作者简介:冯超群,本科,化学工程与工艺专业。
电话:138********。
邮箱:xiaxian_1018@.准溶液,分别加入1.2ml的BaCl 2标准溶液和1.0mlI 2标准溶液,并将其稀释成一定倍数后,制得一定浓度的待测溶液。
UV-2102PC型紫外可见分光光度计为2nm光谱带宽。
聚乙二醇快速澄清原子吸收分光光度法连续测定矿石中铜铅锌

聚乙二醇快速澄清原子吸收分光光度法连续测定矿石中铜铅锌王洪波;王勇【摘要】利用聚乙二醇的水溶性和高聚合性,建立了原子吸收分光光度计连续快速测定矿石中的Cu、Pb、Zn的方法.矿石样品用HCl-HNO3-HClO4完全溶解,在均匀的试液中,选择聚乙二醇用量3 mL,澄清时间仅2.5 h,试液快速澄清.方法精密度(RSD,n=5)小于5%,加标回收率为86.3%~106.0%.方法用于测定岩石国家标准物质中的Cu、Pb和Zn,结果与标准值相符.【期刊名称】《岩矿测试》【年(卷),期】2007(026)002【总页数】2页(P167-168)【关键词】聚乙二醇;原子吸收分光光度法;试液;铜;铅;锌;矿石【作者】王洪波;王勇【作者单位】核工业新疆理化分析测试中心,新疆,乌鲁木齐,830011;核工业新疆理化分析测试中心,新疆,乌鲁木齐,830011【正文语种】中文【中图分类】O657.31;O652.4地质样品中Cu、Pb、Zn的测定,常采用原子吸收分光光度法测定[1],样品采用HCl-HNO3-HClO4体系溶解完全后,定容至一定体积,制备成均匀的试液,静置5 h以上,待试液完全澄清后,再用原子吸收法连续测试[2-3]。
由于试液澄清时间过长,影响分析效率。
本文利用聚乙二醇具有水溶性和高聚合性的特点[4],尝试在已制备成均匀的尚未澄清的试液中,加入一定量的聚乙二醇。
实验表明,试液快速澄清,采用国家标样及加标回收验证,方法可行,提高了分析效率。
1 实验部分1.1 仪器及工作条件日立Z-5000型偏振塞曼原子吸收分光光度计(日本日立公司);铜、铅、锌空心阴极灯(日本日立公司)。
仪器工作条件见表1。
1.2 标准溶液及主要试剂Cu、Pb、Zn标准储备液:在0.32 mol/L HNO3介质中,用常规方法分别配制成Cu、Pb、Zn浓度均为1.000 g/L的标准储备液。
Cu、Pb、Zn混合标准工作液:分别移取10.00 mL Cu标准储备液、10.00 mLPb 标准储备液、2.00 mL Zn标准储备液于100 mL容量瓶中,用0.32 mol/L HNO3溶液稀释至刻度,混匀。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
分光光度法测定聚乙二醇水溶液浓度
摘要:分光光度法测定不同分子量聚乙二醇的浓度,一般有氯化钡法和Dragendoff 试剂法。
分光光度法具有仪器设备简单、操作简便等特点。
本文采用氯化钡法,在一定条件下测定水溶液中不同分子量的聚乙二醇的浓度。
利用该方法简单快捷,可以用于实际生产中标定分离膜的分离性能。
关键词:分光光度法聚乙二醇膜分离技术
Determination of Polyethylene Glycol Content by Spectrophotometric
Abstract: Two different reagents are used for determination of the concentration of different molecular weights polyethylene glycol (PEG) by spectrophotometric, which are barium chloride and Dragendoff reagent. The characteristics of the spectrophotometric are rapidity, simplicity and accuracy. This paper used the reagent of barium chloride for determination of the concentration of polyethylene glycol (PEG), which was under certain conditions in aqueous solution with different molecular weights. The separation performance of the separation membrane can be accurately calibrated in this way.
Key words: spectrophotometric; polyethylene glycol; membrane separation technology.
1 引言
材料、能源和信息被誉为是当代工业的三大支柱,其中的材料则是工业的基础。
在种类繁多的功能性新材料中,功能膜是近年来最受关注者之一。
功能膜大致可分成人工膜和生物膜两大类;而分离膜则是应用最为广泛,种类最为多样的功能膜。
20试世纪60年代以来,微滤、反渗透、纳滤、透析及气体分离等膜分离相继得以迅速发展[1]。
在新型过滤分离膜产品的开发过程中,需要对其分离性能进行表征[2]。
聚乙二醇(PEG)的规格齐全,测试所需试剂价格低廉,可以满足作为表征试剂的要求。
以分子量为2000及以下的聚乙二醇作为表征试剂,利用分光光度法来测定过滤膜对不同分子量聚乙二醇的截留效果,是相对便捷且可以推广使用的方法。
2 实验部分
2.1 实验仪器和试剂
实验仪器:UV-2102 PC型紫外可见分光光度计,尤尼柯(上海)仪器有限公司;100mL容量瓶,若干;1000mL容量瓶,若干;不同规格移液管,若干;10mL具塞刻度试管,若干;烧杯、玻璃棒等。
实验试剂:碘、碘化钾、氯化钡,分析纯;分子量分别为400,600,800,1000,2000的聚乙二醇(PEG),分析纯;纯水。
2.2 实验方法
准确配制1000mg/L不同分子量的聚乙二醇溶液备用;配制质量分数5%的BaCl2标准溶液,0.05mol/L的I2标准溶液备用。
移液管准确量取一定量的聚乙二醇标准溶液,分别加入 1.2mL 的BaCl2标准溶液和1.0mL I2标准溶液,并将其稀释成一定倍数后,制得一定浓度的待测溶液。
UV-2102 PC型紫外可见分光光度计为2nm光谱带宽。
在实验过程中,采用蒸馏水为空白实验组,用作参比溶液。
将已经加入显色剂的待测溶液进行紫外检测操作,适宜的吸光度范围为0.2—0.8。
3 实验结果与讨论
3.1 标准曲线的制作
以PEG400的标准曲线制作为例,利用移液管移取一定量1000mg/L的PEG400溶液,分别稀释于100mL容量瓶中,使其浓度分别为0,5,10,15,20mg/L的PEG400标准溶液。
准确移取不同浓度的聚乙二醇标准溶液各5.0mL,置于已洗净的10mL具塞刻度试管中;分别加入1.0mL 0.05mol/L的I2标准溶液,以及1.2mL 5%的BaCl2标准溶液;加入蒸馏水,稀释至刻度。
在610nm波长下,测定其吸光度与浓度之间的关系,绘制PEG400吸光度—浓度的标准曲线。
其余各分子量聚乙二醇操作方法雷同,部分所作标准曲线如图1, 图2
所示。
实验数据显示聚乙二醇吸光度—浓度有良好的线性关系,各分子量样品的线性相关系数R2均大于0.99。
结果表明,使用该方法对表征过滤膜的分离性能,具有较高的精确度,可以满足时下对于过滤膜截留性能的测定。
3.2 实验条件的选择
3.2.1 显色剂I2用量的影响
样品使用浓度为5.0mg/L的PEG1000标准溶液,显色剂BaCl2标准溶液的使用量为1.2mL,加入不同体积的I2标准溶液,在610nm 波长下测定其吸光度,结果如图3所示。
实验结果显示:在一定范围内,随着碘使用量的增加,吸光度数值也在增大;当碘使用量超出某一范围时,吸光度呈现下降趋势,且出现波动的情况。
参考文献[2],同时综合考虑吸光度的强度和稳定性,本实验选择I2标准溶液的使用量为1.0mL。
3.2.2 显色剂BaCl2用量的影响
样品使用浓度为5.0mg/L的PEG1000标准溶液,显色剂I2标准溶液的使用量为1.0mL,加入不同体积的BaCl2标准溶液,在610nm 波长下测定其吸光度,结果如图4所示。
实验结果显示:在较小范围内,随着BaCl2的使用量的增加,吸光度呈快速上升趋势;当BaCl2使用量达到某一数值时,吸光度降低并保持有一定的稳定性;当BaCl2较大时,吸光度呈现下降趋势。
参考文献[3],同时综合考虑吸光度的强度和稳定性,本实验选择BaCl2标准溶液的使用量为1.2mL。
3.2.3 显色时间的影响
样品使用浓度为5.0mg/L的PEG2000标准溶液,显色剂使用量为I2标准溶液1.0mL,BaCl2标准溶液1.2mL,在620nm波长下扫描,吸光度—时间曲线如图5所示。
实验结果显示:在10min之内,吸光度随着时间小幅上升,在10—30min时间段内稳定在峰值,当显色时间大于30min时,吸光度呈现下降趋势。
在实际操作中,可以根据所需精确度,选择相对适宜的显色时间。
在本组实验中,显色时间基本选择15min左右。
4 结语
上述实验表明,在浓度小于10mg/L浓度范围内,聚乙二醇(PEG)
标准曲线的线性关系较好,用于检测分析的准确度和精确度较高,可以满足对过滤膜分离性能的测定。
同时无论是聚乙二醇,还是该方法使用的所需试剂药品,均易于购买且价格低廉。
综上,以聚乙二醇作为标准物质,利用分光光度法来表征过滤膜的分离性能,操作简单、稳定性好,可以加以有效利用。
参考文献
[1] 王学松. 现代膜技术及其应用指南. 北京:化学工业出版社,2004.
[2] 刘海霞,张浩勤,等. 分光光度法测定不同分子量聚乙二醇浓度[J].河南化工,2004,5:36—37.
[3] 武少华,何宏,等. 氯化钡法及其在聚砜超滤膜性能测定中的应用[J].水处理技术,1995,21(4):193—197.
[4] 中国标准出版社第五编辑室. 膜技术标准汇编(第2版). 北京:中国标准出版社,2010.。
