人教选修4《原电池》教学设计
“原电池”教学设计

人教版高二年级化学选修4“原电池”教学设计刘勤勇学习任务3 寻找盐桥替代物评价任务3 进一步优化改进原电池,自主学习新知识,培养思维深刻性,发展诊断学生解决实际问题的能力和对化学价值的水平。
学生活动 设计意图3.练习巩固 学以致用学习任务4 完成练习,学以致用评价任务4 诊断并发展学生真实问题解决能力(孤立水平、系统水平) (2016浙江高考11题改编)金属(M )–空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。
该类电池放电的总反应方程式为:4M+nO 2 +2nH 2O=4M(OH)n 。
下列说法不正确的是____A .金属(M )电极是该电池的负极B .多孔电极上发生还原反应C .阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡D .在M –空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜4.获取信息,实践分析学习任务5 了解车用电池及工作原理,展望电池研究前景评价任务5 培养学生模型认知、科学态度与社会责任核心价值,发展科技转化为生产力的时候都会遇到问题,学生只有了解设计的前因后果,才能真正理解其中的化学原理。
学生在思考解决问题的时候体会化学是真实有用的。
小组合作,交流研讨分析寻找便捷有效的盐桥替代物,画出装置,进行分析化学学科价值的认识水平。
四、强化练习(2013江苏卷)Mg-H 2O 2电池可用于驱动无人驾驶的潜航器。
该电池以海水为电解质溶液,示意图如下。
该电池工作时,下列说法正确的是A .Mg 电极是该电池的正极B .H 2O 2在石墨电极上发生氧化反应C .石墨电极附近溶液的pH 增大D .溶液中Cl - 向正极移动八、板书设计原电池:化学能 电能低效,电流不稳 高效,电流稳定九、课后反思通过提供材料,探究实验,设计问题串、让学生实验探究、思考讨论,达到对有盐桥的原电池的工作原理的清晰的认识。
此时学生的思维活跃起来,最后再通过与单液原电池的实验现象的对比,让学生讨论两种装置的优缺点,这样也就让学生明白双液原电池的核心理念就是要让还原剂和氧化剂分开以提高能量转换效率。
高中化学 人教版选修4 第四章第一节 原电池 教学设计、教案、学案
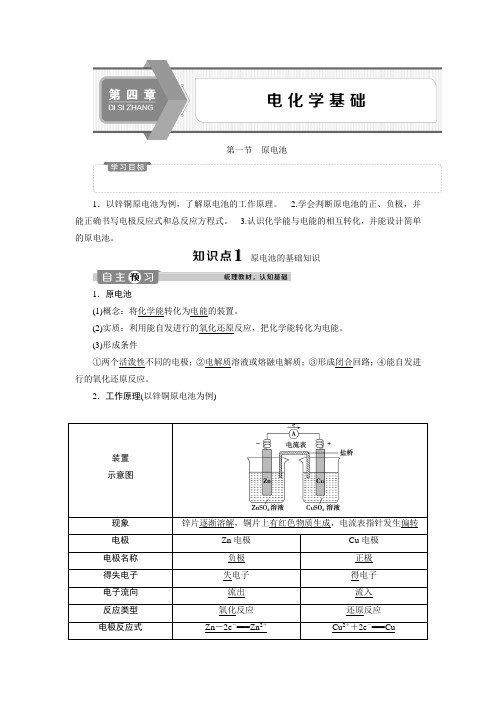
第一节原电池1.以锌铜原电池为例,了解原电池的工作原理。
2.学会判断原电池的正、负极,并能正确书写电极反应式和总反应方程式。
3.认识化学能与电能的相互转化,并能设计简单的原电池。
原电池的基础知识1.原电池(1)概念:将化学能转化为电能的装置。
(2)实质:利用能自发进行的氧化还原反应,把化学能转化为电能。
(3)形成条件①两个活泼性不同的电极;②电解质溶液或熔融电解质;③形成闭合回路;④能自发进行的氧化还原反应。
2.工作原理(以锌铜原电池为例)装置示意图现象锌片逐渐溶解,铜片上有红色物质生成,电流表指针发生偏转电极Zn电极Cu电极电极名称负极正极得失电子失电子得电子电子流向流出流入反应类型氧化反应还原反应电极反应式Zn-2e-===Zn2+Cu2++2e-===Cu总反应式Zn+Cu2+===Zn2++Cu3.盐桥及其作用(1)成分:含有琼胶的KCl饱和溶液。
(2)离子移动方向:Cl-移向负极区,K+移向正极区。
(3)作用①通过离子在盐桥中的定向移动,使两个隔离的电解质溶液连接起来,可使电流持续传导。
②将两个半电池完全隔开,使副反应减至最低程度,可以获得单纯的电极反应,有利于最大程度地将化学能转化为电能。
1.正误判断:正确的打“√”,错误的打“×”,并阐释错因或列举反例。
语句描述正误阐释错因或列举反例(1)在原电池构成的闭合回路中,电子从原电池的正极通过导线流向负极(2)原电池的正极一定是化学性质较不活泼的金属(3)原电池工作时,正极上发生氧化反应,负极上发生还原反应(4)只有自发进行的氧化还原反应才能设计成原电池(5)反应Cu+2Ag+===2Ag+Cu2+能以原电池的形式来实现(2)×不一定,如Mg、Al和NaOH溶液构成原电池时,Al为负极,Mg为正极;导电非金属也可做正极(3)×原电池工作时,正极上发生还原反应,负极上发生氧化反应(4)√(5)√2.锌片和铁片紧贴在一起,放置于稀硫酸溶液中,能否形成原电池?答案:能。
人教版选修四原电池 教案

第四章电化学基础
第一节原电池
[讲]我们已所学过的原电池,是为了便于说明原电池化学原理的一种最简单的装置。如果用它作电源,不但效率低,而且时间稍长,电流就不断减弱,因此不适合于实际应用。这是什么原因呢?主要是由于在铜极上很快就聚集了许多氢气泡,把铜极跟稀硫酸逐渐隔开,这样就增加了电池的内阻,使电流不能畅通。为了避免发生这种现象,我们来设计一种更为科学的原电池装置。
[小结]原电池作为一种化学电源,当它用导线连接上用电器形成闭合回路时就会有电流通过。
(1)在外电路:
①电流的流向是从电源的正极出发经用电器流向电源的负极。
②电子的流向是从电源的负极出发经用电器流向电源的正极。
(2)在内电路:
①电解质溶液中的阳离子向正极移动,因为:正极是电子流入的电极,正极聚集了大量的电子,而电子带负电,吸引阳离子向正极移动。
一、原电池工作原理
锌片(-):Zn-2e-=Zn2+氧化反应;
铜片(+):Cu2++2e-=Cu还原反应
总反应式:Cu2++Zn=Cu+Zn2+
[讲]从分析铜--锌原电池的组成可以看出,原电池是由两个半电池组成的。锌和锌盐溶液组成一个半电池,铜和铜盐溶液组成另一个半电池。中间通过盐桥连接起来。组成半电池的导体叫电极,失去电子的电极为负极,得到电子的电极为正极。不参加电极反应的电极叫惰性电极,如铜电极。
②电解质溶液中的阴离子向负极移动,因为:负极溶解失去电子变成阳离子,阳离子大量聚集在负极,吸引阴离子向负极移动。
教学回顾:
课题:第二节化学电源
教
学
目
的
知识
与
技能
1、一次电池与二次电池的区别
人教选修4原电池教学设计

人教选修4原电池教学设计【教学目标】1.了解电池的基本概念和工作原理;2.掌握电池的使用方法和注意事项;3.能够通过实验探究电池的特性和使用规则;4.培养学生观察、实验、分析和解决问题的能力。
【教学重点】1.电池的基本概念和工作原理;2.电池的使用方法和注意事项;3.通过实验探究电池的特性和使用规则。
【教学难点】1.电池的工作原理和化学反应过程;2.分析实验结果,总结电池的特性和使用规则。
【教学准备】实验器材:干电池、镍镉电池、锂电池、醋酸、铜片、纸巾等;实验设备:万用表、灯泡等;教学材料:电池的工作原理和使用方法的PPT,实验操作指导书等。
【教学过程】一、导入(10分钟)1.利用PPT介绍电池的基本概念和作用,引发学生对电池的兴趣。
2.提问:大家平时使用电池的经验有哪些?电池有哪些不同类型?请举个例子说明。
二、讲解(20分钟)1.电池的工作原理:通过化学反应产生电能。
结构上由正极、负极和电解质组成。
2.电池的化学反应:以干电池为例,将电池的正负极分别与铜片和纸巾接触,浸泡在醋酸中,实验观察放电现象。
3.电池的电压和电流:电压是电能转化为另一种形式的能力,电流是电荷流动的速度。
4.电池的注意事项:不要将电池短路,避免过度充放电,及时更换电池等。
三、实验操作(20分钟)1.实验一:比较不同类型电池的电流大小。
材料:干电池、镍镉电池、锂电池、万用表、灯泡。
方法:将不同类型的电池串联,连接到灯泡两端,测量灯泡亮度。
结果:干电池亮度较弱、镍镉电池亮度适中、锂电池亮度较强。
2.实验二:测量电池的电压。
材料:干电池、万用表。
方法:将万用表的正负极分别接触电池的正负极,测量电压。
结果:干电池电压约为1.5V,符合标称电压。
四、实验结果分析(15分钟)1.从实验一结果中,我们可以发现不同类型电池的电流大小不同,主要取决于电池的化学反应过程和结构设计。
2.从实验二结果中,我们可以验证电池的电压与标称电压基本相符,说明电池的设计和制造工艺成熟。
新人教版高中化学选修4原电池教案

新人教版高中化学选修4原电池教案高中化学4.1原电池教案(新人教版选修4)一、内容及解析1.内容:研究原电池的概念、原理、组成和应用。
2.解析:要求学生了解化学能和电能之间的相互转化原理。
二、目标及解析1.目标:①了解原电池的工作原理。
②掌握原电池正负极反应式和电池总反应式的书写。
2.解析:1)通过从电子转移的角度理解化学能向电能转化的本质。
2)通过练,让学生掌握原电池正负极反应式和电池总反应式的书写。
三、教学问题诊断分析1.重点:初步认识原电池的概念、原理、组成和应用。
难点:引导学生从电子转移的角度理解化学能向电能转化的本质,以及这种转化的综合利用价值。
2.通过对原电池实验的研究,引导学生从电子转移的角度理解化学能向电能转化的本质,以及这种转化的综合利用价值。
四、教学过程引入】电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源,又称电力。
例如,日常生活中使用的手提电脑、手机、相机、摄像机,这一切都依赖于电池的应用。
那么,电池是怎样把化学能转变为电能的呢?我们这节课来一起复一下有关原电池的相关内容。
板书】§4.1 原电池一、原电池实验探究讲:铜片、锌片、硫酸都是同学们很熟悉的物质。
利用这三种物质,我们再现了1799年意大利物理学家伏打留给我们的历史闪光点!实验探究】(铜锌原电池)实验步骤1.将锌片插入稀硫酸中。
2.将铜片插入稀硫酸中。
现象:Cu Zn3.将锌片和铜片上端连接在一起插入稀硫酸中。
问题探究】1.锌片和铜片分别插入稀硫酸中有什么现象发生?2.锌片和铜片用导线连接后插入稀硫酸中,现象又怎样?为什么?3.锌片的质量有无变化?溶液中c (H)如何变化?4.锌片和铜片上变化的反应式怎样书写?5.电子流动的方向如何?讲:我们发现检流计指针偏转,说明产生了电流。
这样的装置架起了化学能转化为电能的桥梁,这就是生活中提供电能的所有电池的开山鼻祖——原电池。
板书】(1)原电池概念:能够将化学能转化为电能的装置叫做原电池。
人教版选修四第四章电化学基础原电池教学设计

第四章第一节原电池一、教学设计思路新课标对本节教材的教学要求是“学生能从根本上了解化学能与电能之间发生转化的原因;能正确书写电极反应式和电池反应方程式。
”基于此,我认为:本节内容是在《必修2:化学能与电能》的基础上,通过对电池效率的探究,引出半电池、盐桥、内电路、外电路等概念,从本质上了解原电池的工作原理,是在必修2基础上的深化。
于是我以下面的思路进行教学设计。
通过影视片段导入,引导学生提取情节涉及到的利用化学物质“造电”信息,明确本节课的学习内容。
通过使学生置身情境,发现问题,通过实验探究继而解决问题。
1.情境线:影片主人公要想回到未来世界,必须与未来世界沟通,即利用通讯设备收到未来世界的讯号,可惜通讯设备没有电了。
本节课,同学们就是要为主人公设计出一个“电池”。
根据必修二的知识,设计“铜—锌—稀硫酸”原电池,发现电池输出电能不够大,引出探究一“原电池输出电能的能力”。
选用“铜—锌—硫酸铜”原电池,电流是大了,但也出现缺陷:电流越来越小,不能产生稳定的电流,从而进行探究二“如何改进实验,提供持续稳定的电流”,引出加盐桥的原电池的学习。
通过参与思考实践,为主人公设计出一个既可以给通讯设备提供相应的电流,又能够持续稳定地供电的电池。
2.实验线:根据影片所给信息,设计“铜—锌—稀硫酸”原电池。
复习原电池构成条件后,根据Zn + Cu2+ = Zn2+ + Cu,设计“铜—锌—硫酸铜”原电池。
通过观察比较电流计指针偏转的角度,完成探究一“原电池输出电能的能力”影响因素。
对实验现象“锌片上也有铜附着”进行再分析,提出问题“能否设法阻止溶液中的Cu2+在负极表面还原”,让学生讨论进行改进,并完成教材实验4—1探究二“原电池(加盐桥)”。
了解盐桥的作用,并感受设置盐桥不是一个普通的技术改进,而是对旧的思维模式的一个质的突破。
二、教案的条件也是影响因素。
强。
【提问】刚刚大家在做实验的时候,有没有注意到电流大小的变化?是不是一直指示着最大值?【现象再分析】为什么负极的锌片也有红色物质析出?【解释原因】由于锌片与硫酸铜溶液直接接触,会有铜在锌片表面析出,锌表面也构成了原电池,进一步加速铜在锌表面析出,致使向外输出的电流强度减弱。
人教选修4《原电池》教学设计

WORD整理版2013年邵阳市高中化学教师教学素养大赛教学设计评比《原电池》教学设计模块:人教版选修4《化学反应原理》课题:第四章第一节《原电池》授课人:李峰屹(绥宁县第二中学)时间: 2013年12月16日高中化学新课程(人教版)选修4第四章第一节《原电池》教学设计绥宁县第二中学李峰屹一、教材分析与学情分析1、教材分析:在人教版教材必修2中以铜锌单液电池模型为载体,简单介绍了原电池的工作原理和形成条件;在选修4《化学反应原理》的第四章第一节中以双液电池模型为载体,深化认识原电池原理和形成条件;随之,第二节《化学电源》则在此基础上介绍实用化学电池及其工作原理。
因此,本节课在教材内容上起着承上启下的作用。
2、学情分析:【认知基础】对原电池原理有初步认识;具有一定的实验探究能力。
【局限认识】氧化剂和还原剂只有接触才可能发生氧化还原反应。
【发展方向】通过实验活动对原电池原理形成完整认识,提高解决问题的能力。
从单液电池模型到双液电池模型,学生的知识和能力层次需要进行一次较大的跨越。
因此,本节课的关键是寻找学生的“最近发展区”,帮助学生主动思考,突破认识的局限性,完成对原电池原理及形成条件的认知跨越。
二、教学目标与教学策略:1、教学目标设计【知识与技能】深入理解原电池的工作原理;完整的认识原电池的形成条件;学会书写电极反应式和电池总反应方程式;能根据反应设计简单的原电池。
【过程与方法】通过桔子电池实验活动体验建构原电池模型的过程;通过Zn-CuSO4电池的设计活动,感悟科学探究的思路和方法;体会控制变量在科学探究中的应用。
【情感态度与价值观】通过介绍电池发展史,激发学习兴趣,感受原电池原理应用于化学电源的关键作用;通过双液电池模型的建构,渗透对立统一的辩证唯物主义思想。
【教学重点】原电池工作原理和形成条件【教学难点】氧化还原反应完全分开在两极发生(分池、分液)2、教学策略设计教师引导下的学生实验探究与模型建构相结合:3、教学用品:多媒体电脑及投影设备、灵敏电流计、导线、原电池容器两个、铜丝、铝线、铜片、锌片、盐桥、培养皿、硫酸铜溶液、硫酸锌溶液、氯化钠溶液、桔子、滤纸、吸管若干(仪器药品按4名学生一组准备)。
人教版选修四原电池教案完美版

§4-1原电池〈知识目标〉1、在必修2的基础上,进一步学习原电池的工作原理,探究简单原电池的不足和改进。
2、形成完备的原电池概念,理解构成原电池的条件,掌握电极反应式的书写。
〈过程及方法〉1、经历对化学能与电能转化的化学实验探究的过程,进一步理解探究的意义,学习科学探究的基本方法,提高科学探究的能力。
2、能对自已探究电池概念及形成条件的学习过程进行计划、反思、评价和调控,提高自主学习化学的能力。
〈情感与价值观〉1、发展学习化学的兴趣,乐于探究化学能转化成电能的奥秘,体验科学探究的艰辛和喜悦,感受化学世界和奇妙与和谐。
2、赞赏化学科学对个人生活和社会发展的贡献,关注能源问题,逐步形成正确的能源观。
〈教学重点及难点〉进一步理解原电池的工作原理,能够书写电极反应式和总反应式〈教学方法〉实验探究〈教学用具〉实验仪器、电脑〈教学过程〉〈引入〉电能已经成为人类最重要的能源之一,人们利用特定装置将自然界中的各种能量转化成电能,又发明出另外一些装置将电能转化为其它能量为人们所需要,而研究化学能与电能相互转换的装置、过程和效率的科学叫电化学。
〈板书〉第四章电化学基础在必修Ⅱ我们已经认识了两种化学能转化成电能的方法:一、火力发电,二、原电池。
在这里我们将进一步的研究和学习原电池。
〈板书〉§4-1 原电池一、原电池〈师〉上周五老师留的家庭作业,复习原电池的知识,并自己设计和组装一个原电池,大家完成没有。
下面就请各组派代表将你组的最优作品到前面来展示,看是否设计成功,电流是否强劲,评出今天的最牛电池。
这一环节的主题是——自创电池大PK投影:《自创电池大PK》〈学生活动〉展示电池〈师〉下面请最牛电池设计者讲讲自己的设计理念?〈投影〉1、构成条件两个电极电解质溶液闭合电路放热的氧化还原反应〈师〉这个能不能构成原电池,请写出他的电极反应式和总反应式,并在装置图上标出电子流动方向。
2、原电池的电极反应式和总反应式(-):锌片 Zn-2e-=Zn 2+(+):铜片 2H ++2e-=H 2↑总电极方程式:Zn+2H +=Zn 2++H 2↑〈师〉找一个同学说一下原电池是怎么产生电流的,即原电池的工作原理是什么?3、原电池的工作原理负极:失电子,发生氧化反应;电子流出, 正极:得电子,发生还原反应,电子流入。
原电池教案(优秀3篇)

原电池教案(优秀3篇)(经典版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的经典范文,如工作资料、求职资料、报告大全、方案大全、合同协议、条据文书、教学资料、教案设计、作文大全、其他范文等等,想了解不同范文格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!In addition, this shop provides you with various types of classic model essays, such as work materials, job search materials, report encyclopedia, scheme encyclopedia, contract agreements, documents, teaching materials, teaching plan design, composition encyclopedia, other model essays, etc. if you want to understand different model essay formats and writing methods, please pay attention!原电池教案(优秀3篇)在教学工作者开展教学活动前,就不得不需要编写教学设计,借助教学设计可以更好地组织教学活动。
人教版高中化学选修四第四章第一节《原电池》教学设计

第 1 页 共 2 页 发生 反应 原电池 离子 离子负极正极 电解质溶液(标出电子转移情况) 发生 反应第一节《原电池》教学设计一、解读课标1、掌握原电池的结构和工作原理,根据原电池的结构和工作原理会判断电池的正负极。
2、利用原电池的结构和工作原理设计原电池。
二、教材分析由于原电池在必修二第二章已经详细介绍过,因此,在本节课原电池的结构和工作原理以复习为主,由单液原电池向双液原电池过度,熟练掌握将一个氧化还原反应设计成原电池。
三、重点、难点1、掌握原电池的工作原理和结构。
2、根据工作原理会判断原电池的正负极。
3、掌握构成原电池的条件。
4、学会将一个氧化还原反应设计成原电池四、《导学案》自己填写,小组讨论,每组找代表展示。
对展示成员进行鼓励和表扬。
五、学习过程【导入新课】以生活中应用广泛的“暖宝宝”为例。
通过本节课学习,思考“暖宝宝”的工作原理。
【设计思路】以生活实际入手,引起学生注意,生活处处是化学,学以致用,激发学生的兴趣。
【观看视频】观看铜--锌原电池的实验视频。
【独立自学】回顾《氧化还原反应》和必修二《原电池》的内容并结合课本七十一至七十二页内容完成《导学案》上的【复习】部分。
【展评激学】学生展示成果,学生点评,教师补充。
【加强巩固】每组同学讨论完成《导学案》上的【练习】1,展示小组讨论结果。
【学生总结】如何判断电池的正负极?【总结升华】第 2 页 共 2 页 原电池 离子离子 负极 正极 电解质溶液 (标出电子转移情况) 发生 反应 (填“阴”或“阳” , 右同)【小组讨论】比较《导学案》上【练习】1中的图Ⅰ和图Ⅱ,完成《导学案》上的【思考】1、2、3、4部分【设计思路】通过旧知识的复习,向新知识过度。
由单液原电池引入双液原电池。
从而引出原电池的构成条件。
【学生总结】构成原电池的条件。
【学以致用】 讨论《导学案》上【思考】5.“暖宝宝”的工作原理:以还原铁粉为负极,石墨粉作为正极材料,氯化镁或氯化钙为吸水剂,氯化钠为电解质,空气中的氧气在石墨上得到电子,形成原电池。
原电池-人教版选修4化学反应原理教案

原电池-人教版选修4 化学反应原理教案1. 教学目标1.了解原电池的基本概念和组成结构。
2.掌握原电池的工作原理和电解质浓度对电动势的影响。
3.理解原电池和其他电化学电池的区别和联系。
4.能够运用原电池的相关知识解决实际问题。
2. 教学内容2.1 原电池的基本概念和组成结构2.1.1 基本概念原电池是利用自然界中某些金属或半金属在自身与其离子之间转移电子形成电势差的装置。
即金属或半金属电极与其离子之间的氧化还原反应会释放或吸收电子,从而形成电势差。
如锌原电池的电位为-0.76V,铜原电池为+0.34V,两者之差为1.10V。
2.1.2 组成结构原电池由电极和电解质两部分组成。
其中电极由可氧化金属或半金属制成。
电解质为可以导电的溶液或固体。
例如,锌原电池中,锌是负极,铜是正极,硫酸锌溶液是电解质。
2.2 原电池的工作原理和电解质浓度对电动势的影响2.2.1 工作原理原电池的工作原理是利用自然界中某些金属或半金属在自身与其离子之间转移电子形成电势差的装置。
通过对电极和电解质进行适当的选择和设计,可以使离子的沉淀和析出在电极上发生氧化还原反应,从而引起电流流动。
2.2.2 电解质浓度对电动势的影响电解质浓度是原电池电动势大小的一个重要参数。
随着浓度的增加,电池电动势也相应增大。
例如,对于锌原电池,如果溶液中的硫酸锌浓度变大,则锌离子在负极上的活动性也会增大,从而使电子的传递速率增加,电流变大,电动势也相应增大。
2.3 原电池和其他电化学电池的区别和联系原电池与其他电化学电池的区别主要在于其组成和工作原理。
原电池是利用自然界中某些金属或半金属在自身与其离子之间转移电子形成电势差的装置,而其他电化学电池则根据不同的需求进行设计和制造,在结构和性质上都有所区别。
但不管是何种电池,它们的核心都是氧化还原反应,即在电极和电解质中发生的氧化还原反应。
因此,从氧化还原反应的角度来看,原电池和其他电化学电池都有相同的基本原理和特点。
人教版选修四第四章《原电池》教案

第四章电化学基础第一节原电池【教学目标】知识与技能:1.复习原电池的构成,深入了解原电池的工作原理;2.能理解盐桥的作用;3.能够按要求设计简单的原电池,会书写简单的电极反应式。
过程与方法:1.经历探究如何避免普通原电池内耗的过程,学习科学探究的基本方法;2.经历尝试使带盐桥的原电池形成闭合回路的过程,提高思维的发散性。
情感态度与价值观:在探究学习的过程中,体验追根究底、锲而不舍的探究精神并体验成功的乐趣。
【教学重难点】盐桥的作用、探究能力的培养【教学方法】实验探究法─通过实验、分析、讨论、总结应用等过程,引导学生观察、思考、推理、探究。
【教学过程】【投影】第四章电化学基础【引入】图片引入【板书】第一节原电池【讲述】必修二已经学过原电池,现在又学原电池,区别在于现在是在原来的基础上进一步提高原电池的能量转化效率。
【探究实验一】把锌片和铜片与贺卡扬声器用导线连通,然后把锌片和铜片放入【归纳】复习原电池工作原理【思考】1、锌片上为什么有红色物质析出,贺卡扬声器为什么声音越来越弱?2、该原电池不使用时能否长期保存?为什么?【思考与交流】实验探究一是我们在必修2中学习过的原电池,如果用它做电源,不但效率低,而且时间稍长电流就很快减弱,又不能长期保存,因此不适合实际应用。
这是什么原因造成的呢?有没有什么改进措施?溶液直接接触)(提示:刚才的实验中锌与CuSO4【回答】把锌与硫酸铜溶液分开【提问】分开后,锌的烧杯里加什么物质?【投影】加金属对应的盐溶液【探究实验二】把锌片和铜片与贺卡扬声器用导线连通,然后把锌片放入硫酸锌溶液中,把铜片放入硫酸铜溶液中,贺卡扬声器会发出声音吗?为什么?【回答】不会发出声音,因为构不成闭合回路。
(提示:从微观的角度)那怎么解决这个问题呢?【回答】搭桥【探究实验三】【思考】什么物质能作为离子通道,让Zn2+、SO42-沿着它移动呢?(提示:能吸水的物质就能让溶液沿着它移动,就能让离子沿其运动)用提供的材料把两烧杯连通,观察现象:_______________________________ 【提问】通过实验,设想成立,但声音微弱,为什么?【回答】电流小,单位时间内通过的电量小。
选修四原电池教案

选修四原电池教案选修四原电池教案一、基本信息学科:化学年级:高中选修四教时:2课时教学目标:1. 理解原电池的定义和构造2. 掌握原电池的工作原理3. 了解原电池的应用和发展教学重点:原电池的工作原理教学难点:原电池的应用和发展二、教学准备教材:高中化学选修四教材教具:PPT、实物原电池三、教学步骤第一步,导入新课1. 向学生介绍本节课的教学目标,并激发其学习兴趣。
2. 提问:你们了解什么是原电池吗?它有什么应用?3. 让学生总结原电池的定义和应用。
第二步,讲解原电池的基本概念1. 通过PPT向学生介绍原电池的概念和起源。
2. 引导学生了解原电池的基本构造和工作原理。
第三步,实验展示1. 展示实物原电池,让学生观察和描述。
2. 教师进行实验演示,让学生亲手操作。
3. 导出实验结论,总结原电池的工作原理。
第四步,讲解原电池的应用和发展1. 向学生介绍原电池的应用领域和发展状况。
2. 引导学生思考原电池的优缺点,并与其他电池进行比较。
第五步,课堂讨论1. 组织学生进行小组讨论,探讨原电池的前景和应用。
2. 让学生展示讨论结果,并与全班分享。
第六步,总结与检验1. 整理本节课的学习内容,向学生进行知识点总结。
2. 设计一份小测试,检验学生的学习成果。
四、教学反思本节课通过导入新课、讲解概念、实验演示、讨论等多种教学方法,激发了学生的学习兴趣,提高了他们的参与度。
通过实物展示和实验演示,学生深刻理解了原电池的构造和工作原理。
通过讨论和总结,学生了解了原电池的应用和发展。
整个教学过程轻松愉快,达到了预期的教学目标。
人教版高中化学选修四41《原电池》第一课时教案

人教版高中化学选修四41《原电池》第一课时教案教案名称:人教版高中化学选修四《原电池》第一课时教案一、教学目标1. 让学生了解原电池的概念、组成和分类。
2. 使学生掌握原电池的工作原理及其能量转化过程。
3. 培养学生运用化学知识解决实际问题的能力。
二、教学内容1. 原电池的概念2. 原电池的组成和分类3. 原电池的工作原理4. 原电池的能量转化过程三、教学重点与难点1. 教学重点:原电池的概念、组成、分类和工作原理。
2. 教学难点:原电池的能量转化过程。
四、教学方法1. 采用问题驱动法,引导学生主动探究原电池的相关知识。
2. 利用多媒体课件,形象直观地展示原电池的工作原理和能量转化过程。
3. 结合实例分析,让学生体会化学知识在生活中的应用。
五、教学步骤1. 引入新课1.1 展示干电池、燃料电池等日常生活中的原电池实例,引导学生关注原电池的应用。
1.2 提问:什么是原电池?原电池是如何工作的?2. 讲解原电池的概念2.1 讲解原电池的定义:原电池是一种能够将化学能直接转换为电能的装置。
2.2 强调原电池的特点:自发的氧化还原反应、两极性、闭合回路。
3. 介绍原电池的组成和分类3.1 讲解原电池的组成:负极、正极、电解质、导线。
3.2 介绍原电池的分类:酸性电池、碱性电池、中性电池、燃料电池等。
4. 讲解原电池的工作原理4.1 展示原电池工作原理的示意图,讲解负极和正极的反应过程。
4.2 强调电子转移和离子迁移在原电池工作中的重要性。
5. 分析原电池的能量转化过程5.1 讲解化学能转化为电能的过程:氧化还原反应、电子转移、离子迁移。
5.2 举例说明原电池在实际应用中的能量转化过程。
6. 巩固知识,解决问题6.1 提问:原电池的工作原理和能量转化过程有哪些实际应用?6.2 让学生结合生活实例,分析原电池的工作原理和能量转化过程。
7. 课堂小结7.1 回顾本节课所学内容,总结原电池的概念、组成、分类和工作原理。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
人教选修4《原电池》
教学设计
-CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN
2013年邵阳市高中化学教师教学素养大赛教学设计评比《原电池》教学设计
模块:人教版选修4《化学反应原理》
课题:第四章第一节《原电池》
授课人:李峰屹(绥宁县第二中学)
时间: 2013年12月16日
高中化学新课程(人教版)选修4第四章第一节
《原电池》教学设计
绥宁县第二中学李峰屹
一、教材分析与学情分析
1、教材分析:在人教版教材必修2中以铜锌单液电池模型为载体,简单介绍了原电池的工作原理和形成条件;在选修4《化学反应原理》的第四章第一节中以双液电池模型为载体,深化认识原电池原理和形成条件;随之,第二节《化学电源》则在此基础上介绍实用化学电池及其工作原理。
因此,本节课在教材内容上起着承上启下的作用。
2、学情分析:
【认知基础】对原电池原理有初步认识;具有一定的实验探究能力。
【局限认识】氧化剂和还原剂只有接触才可能发生氧化还原反应。
【发展方向】通过实验活动对原电池原理形成完整认识,提高解决问题的能力。
从单液电池模型到双液电池模型,学生的知识和能力层次需要进行一次较大的跨越。
因此,本节课的关键是寻找学生的“最近发展区”,帮助学生主动思考,突破认识的局限性,完成对原电池原理及形成条件的认知跨越。
二、教学目标与教学策略:
1、教学目标设计
【知识与技能】深入理解原电池的工作原理;完整的认识原电池的形成条件;学会书写电极反应式和电池总反应方程式;能根据反应设计简单的原电池。
【过程与方法】通过桔子电池实验活动体验建构原电池模型的过程;通过Zn-CuSO4电池的设计活动,感悟科学探究的思路和方法;体会控制变量在科学探究中的应用。
【情感态度与价值观】通过介绍电池发展史,激发学习兴趣,感受原电池原理应用于化学电源的关键作用;通过双液电池模型的建构,渗透对立统一的辩证唯物主义思想。
【教学重点】原电池工作原理和形成条件
【教学难点】氧化还原反应完全分开在两极发生(分池、分液)
2、教学策略设计
教师引导下的学生实验探究与模型建构相结合:
3、教学用品:
多媒体电脑及投影设备、灵敏电流计、导线、原电池容器两个、铜丝、铝线、铜片、锌片、盐桥、培养皿、硫酸铜溶液、硫酸锌溶液、氯化钠溶液、桔子、滤纸、吸管若干(仪器药品按4名学生一组准备)。
三、教学过程设计
1、教学流程图
2、教学过程设计
教学环节教师活动学生活动设计意图
展示图片复习已知【引入】回忆小学课文冰心的
《小桔灯》,并展示现代版
“小桔灯”,激发学生回忆复
习。
【复习】铜锌原
电池装置中正负
极分别发生了什
么反应?电流如
何产生
【回顾复习】化学能转化
为电能的装置。
【复习】原电池工作原
理:
负极:氧化反应失电子
正极:还原反应得电子
电子从负极流向正极,
阴离子从正极流向负极,
形成闭合回路。
第一次理论
分析,激活
学生对原电
池原理及形
成条件的已
有认知。
为
后续产生认
知冲突奠定
基础。
桔子实验提炼模型【过渡】在必修中有一个家庭
实验——设计水果电池。
【提出实验内容】现在给你提
供了以下材料,请你设计桔子
电池,观察实验现象并提炼出
原电池模型。
可供选择的材料:灵敏电
流计、铜丝、铝线、导
线、培养皿、桔子滤纸、
吸管、NaCl溶液
【小组实验】
【方案展示,提炼模型】
通过桔子实
验的方案讨
论,使学生
从“单瓣”→
“两瓣”形象实
验演化成“单
池”→“双池”
的模型建
构;从“膜”上
升到“盐桥”的
认识。
第二次理论
分析提出双交流方案,汇总
教师引导,学生主动建构模型,集体讨论修改:
方案1:方案2:
序号方案、现象
方案1
铜丝和铝线同时插入一瓣桔子中
(有电流)
方案2
铜丝和铝线分别插入未分开的两瓣桔子中
(有电流)
方案3
铜丝和铝线分别插入分开的两瓣桔子中
(无电流)
【针对方案2提问】为何两
瓣未分开的桔子也能产生电
流?
【针对方案3提问】为何两
瓣分开的桔子不能产生电流
如何改进,产生电流
【教师演示两种解决方案】
“连隧道”(用吸满果汁的导管
【可能解释】因为两瓣中间
的膜可以让离子通过,离子
定向移动形成闭合回路。
【可能解释】未形成闭合回
路。
解决方法:将两瓣桔子
贴在一起。
还有可能会有将其浸入电解
质溶液中。
连通)、“搭桥”(用浸有NaCl 溶液的滤纸条连接)。
【提问】这两种解决方案为何能产生电流?请提炼模型。
【知识介绍】在化学实验中常用的盐桥是在U型管里装含有琼胶的饱和KCl溶液。
【可能解释】在“隧道”和“桥”
中离子能够定向移动,构成
闭合回路。
【提炼模型】
池-盐桥模
型,在模型
分析中再次
强调电流的
形成过程,
同时强调盐
桥的作用。
实验探究完善认识【连接】水果中含有电解质
溶液,因此可以设计水果电
池实现化学能转化电能的过
程。
如何将化学反应设计成
原电池装置呢?
【提出问题】现有反应Zn
+CuSO4=ZnSO4+Cu,如
何设计成原电池装置?
【组织学生交流,确定设计
思路】先将氧化还原反应拆
分,再根据反应确定电极材
料和电解质溶液。
【提出实验目的】按盐桥模
型,根据Zn+CuSO4=
ZnSO4+Cu反应设计成原电
池装置。
【指导学生实验】
联系已学知识,回忆根据化
学反应设计成原电池装置的
思路和方法。
思路1:先选材料,后定反
应。
Zn是负极,发生氧化反应;
Cu是正极,发生还原反应。
思路2:先拆反应,后选材
料。
Zn-2e-=Zn2+氧化反应负极
Cu2++2e-=Cu还原反应正极
可供使用的仪器和药品:灵
敏电流计、铜片、锌片、导
线、培养皿、ZnSO4溶液、
NaCl溶液、CuSO4溶液、浸
NaCl溶液的滤纸条(盐桥)。
注意:及时清洗电极。
【小组实验设计方案,并实
通过方法讨
论和交流,
后面学生实
验过程会有
的放矢,防
止漫无目的
的实验。
通过实验活
动,感悟科
学探究的思
路和方法,
四、教学反思
1、教学素材选取得当,有助于激发学习兴趣,突破教学难点
本节课借助妙趣横生的课堂引入和桔子实验,使学生在探究过程中自主建立了分池、盐桥等观点,从而突破了对原电池原理认知发展的教学难点。
2、教学中问题线索及学生活动设计得当
教学中问题线索设计及学生活动设计有利于使学生产生认知冲突,可以为学生提供真实的科学探究背景,模拟解决实际问题的过程,符合学生认知发展的规律。
从而使学生在已有基础上发现问题,并在不断解决新问题的过程中实现能力升华,达成教学目标。
3、教学设计应安排得更紧凑
本节课的实际教学中教师还安排了根据H2+O2==H2O这一反应来设计原电池的学生活动。
由于课堂容量大、时间紧,因此通过教学实践认为将该活动放在下一节《化学电源》中作为课堂引入和过渡的线索更为妥当。
