菠菜叶中叶绿素的提取和分离
菠菜中色素的提取分离和鉴定(有机化学实验)[终稿]
![菠菜中色素的提取分离和鉴定(有机化学实验)[终稿]](https://img.taocdn.com/s3/m/84bf77ceac51f01dc281e53a580216fc700a53a1.png)
菠菜中的色素提取、分离及鉴定一、实验目的1.进一步熟悉和掌握薄层色谱的原理及应用2.了解菠菜中主要色素的基本性质,通过菠菜色素的提取和分离,了解天然物质分离提纯方法及原理3.掌握用紫外光谱和荧光光谱鉴别菠菜中色素的原理及方法二、菠菜中的色素简介菠菜叶中富含多种色素成分,如叶绿素(绿色)、胡萝卜素(橙黄色)和叶黄素(黄色)等多种天然色素。
叶绿素存在两种结构相似的形式即叶绿素 a(C 55 H 72O 5N 4Mg) 和叶绿素 b(C 55H 7O 6N 4Mg),结构见图1。
二者差别仅是 a 中一个甲基被 b 中的甲酰基所取代。
它们都是吡咯衍生物与金属镁的络合物,是植物进行光合作用所必需的催化剂。
植物中叶绿素a 的含量通常是b 的3倍。
尽管叶绿素分子中含有一些极性基团,但分子中大的烷基结构使它易溶于丙酮,乙醇,乙醚,石油醚等有机溶剂。
胡萝卜素( C 40H 56 )是具有长链结构的共轭多烯。
它有三种异构体,即 α-, β - 和γ - 胡萝卜素,其中β - 异构体含量最多,也最重要。
在生物体内,β - 体受酶催化氧化即形成维生素 A 。
目前β - 胡萝卜素已可进行工业生产,可作为维生素 A 使用,也可作为食品工业中的色素。
叶黄素( C40H56O2 )是胡萝卜素的羟基衍生物,它在绿叶中的含量通常是胡萝卜素的两倍。
与β - 胡萝卜素相比,叶黄素较易溶于醇而在石油醚中溶解度较小。
根据这些色素在有机溶剂中的溶解性,可将它们提取出来。
N N NNH 3CCHCH 2RCH 2CH 3CH 3H 3C OCO 2CH 3CH 2CH 2OOCH 3CH 3CH 3CH 3CH 3Mg叶绿素a 和叶绿素b 的结构(叶绿素a :R=CH 3, 叶绿素b :R=CHO )H 3C CH 3RCH 3H 3CRH 3CCH 3CH 3CH 3CH 3CH 3β-胡萝卜素和叶黄素的结构(β-胡萝卜素:R =H , 叶黄素: R = OH )菠菜中各色素的理化性质绿色植物中的叶绿体色素在把光能转变为化学能的光和作用中起着重要作用。
从菠菜中提取叶绿素实验报告三篇

从菠菜中提取叶绿素实验报告三篇实验报告一:菠菜中提取叶绿素的方法比较1.引言叶绿素是一种重要的植物色素,它在光合作用中承担着捕获光能和转化化学能的重要角色。
菠菜是叶绿素含量较高的植物之一,因此本实验旨在比较不同方法提取菠菜中的叶绿素,探索最有效的提取方式。
2.材料与方法2.1 材料:- 新鲜菠菜叶片- 无水乙醚- 丙酮- 高速离心机- 比色皿2.2 方法:- 方法一:无水乙醚提取法将适量的菠菜叶片放入离心管中,加入适量的无水乙醚,用摇床震动片刻,使叶绿素溶解于乙醚中,然后离心10分钟收集上层液体。
- 方法二:丙酮提取法将适量的菠菜叶片放入离心管中,加入适量的丙酮,用摇床震动片刻,使叶绿素溶解于丙酮中,然后离心10分钟收集上层液体。
- 方法三:乙醇提取法将适量的菠菜叶片放入离心管中,加入适量的乙醇,用摇床震动片刻,使叶绿素溶解于乙醇中,然后离心10分钟收集上层液体。
3.结果在三种提取方法中,通过观察可以发现,方法一和方法二提取的叶绿素溶液呈现绿色,而方法三提取的叶绿素溶液呈现黄绿色。
利用分光光度计测定三个试管中叶绿素溶液的吸光度,发现方法一和方法二提取的叶绿素吸光度较高,而方法三的吸光度较低。
4.讨论方法一使用无水乙醚作为提取溶剂,乙醚能有效溶解叶绿素,并且在离心过程中上层液体的分离效果较好。
方法二使用丙酮作为提取溶剂,丙酮也能有效溶解叶绿素,并且丙酮相对于乙醚来说更易于购买。
方法三使用乙醇作为提取溶剂,乙醇对叶绿素的溶解能力较差,导致提取的叶绿素溶液吸光度较低。
5.结论通过对菠菜中提取叶绿素的实验比较,我们发现使用无水乙醚和丙酮作为提取溶剂的方法能够较好地提取菠菜中的叶绿素,并且吸光度较高。
因此,在菠菜中提取叶绿素的实验中,建议使用无水乙醚或丙酮作为提取溶剂。
实验报告二:叶绿素在光合作用中的作用研究1.引言叶绿素是植物体内最重要的色素之一,它在光合作用中起着关键作用。
本实验旨在研究叶绿素在光合作用中的功能和重要性。
菠菜叶中叶绿素的提取和分离

菠菜叶中叶绿素的提取和分离一、实验目的本实验旨在探究菠菜叶中叶绿素的提取和分离方法,通过对实验数据的分析,了解叶绿素的组成、性质和含量,为植物光合作用研究和食品营养学研究提供实验依据。
二、实验原理叶绿素是植物叶片中最重要的色素之一,它能够吸收太阳光能,通过光合作用将光能转化为化学能,为植物的生长和发育提供能量。
叶绿素主要分为叶绿素a和叶绿素b两种,其中叶绿素a是主要的捕光色素,叶绿素b是辅助色素。
本实验通过提取和分离菠菜叶中的叶绿素,了解其组成和性质。
三、实验步骤1.准备实验材料:新鲜菠菜叶、研钵、称量纸、电子天平、离心机、分光光度计、计时器、实验数据记录表等。
2.预处理菠菜叶:选取新鲜菠菜叶,去除杂质和枯叶,用自来水冲洗干净,再用去离子水冲洗一遍。
3.提取叶绿素:将洗净的菠菜叶剪成小段,放入研钵中加入适量石油醚-乙醇混合液(体积比1:1),研磨成匀浆。
将匀浆倒入离心管中,加入适量去离子水,摇匀后放入离心机中离心10分钟(转速为4000转/分钟)。
离心后,将上层绿色液体小心地吸出,转移至另一个离心管中,再次离心5分钟,去除沉淀物。
4.分离叶绿素:将绿色液体倒入硅胶G薄层板(5×10 cm)中,用玻璃棒均匀涂布。
将薄层板放入层析缸中,用石油醚-丙酮混合液(体积比6:4)进行层析。
每隔10分钟观察一次颜色变化,并记录实验数据。
当组分被分离时,用分光光度计分别测定各组分的吸光度。
5.数据记录与分析:根据实验数据记录表记录各组分的吸光度,计算各组分的含量百分比。
通过对实验数据的分析,了解菠菜叶中叶绿素的组成、性质和含量。
四、实验结果与分析1.实验数据记录表:2.实验数据分析:根据实验数据记录表可知,菠菜叶中主要含有叶绿素a和叶绿素b两种色素,其中叶绿素a的含量较高,占总量的70%,叶绿素b的含量相对较低,占总量的30%。
这说明菠菜叶中的主要捕光色素是叶绿素a。
此外,实验过程中还可能分离出其他组分,但它们的含量较低。
色素提取和分离实验报告

色素提取和分离实验报告色素提取和分离实验报告引言:色素是一类广泛存在于自然界中的有机化合物,具有丰富的颜色和多样的功能。
色素提取和分离是一项重要的实验技术,可以帮助我们深入了解色素的性质和应用。
本实验旨在通过提取和分离植物中的色素,探究其在不同溶剂中的溶解性和分离效果。
实验材料和方法:材料:鲜菠菜叶片、无水乙醇、丙酮、二氯甲烷、石油醚、氯化钠溶液、滤纸、试管等。
方法:1. 将鲜菠菜叶片切碎,放入试管中。
2. 加入适量的无水乙醇,用玻璃棒搅拌均匀。
3. 将悬浊液过滤,收集滤液。
4. 将滤液分成几份,分别加入丙酮、二氯甲烷和石油醚中,摇匀。
5. 观察不同溶剂中的色素溶解情况和分离效果。
结果和讨论:通过实验观察和记录,我们得到了以下结果和结论:1. 无水乙醇提取:将鲜菠菜叶片与无水乙醇混合后,溶液呈现出深绿色。
这是因为无水乙醇可以有效提取鲜菠菜叶片中的叶绿素,叶绿素是一种绿色的植物色素。
2. 不同溶剂中的色素溶解情况:在实验中,我们用丙酮、二氯甲烷和石油醚分别与提取得到的无水乙醇溶液混合,并观察其溶解情况。
结果显示,丙酮溶液呈现出深绿色,二氯甲烷溶液呈现出橙黄色,而石油醚溶液呈现出淡黄色。
这说明不同溶剂对色素的溶解性有所差异。
3. 色素的分离效果:在实验中,我们通过观察不同溶剂中的色素溶液,发现色素在不同溶剂中有不同的分离效果。
丙酮溶液中的色素分离效果最好,可以清晰地观察到绿色和黄色两个色带。
而二氯甲烷溶液中的色素分离效果较差,只能看到一个橙黄色的色带。
石油醚溶液中的色素分离效果最差,只能观察到一个淡黄色的色带。
这说明不同溶剂对色素的分离效果也有所差异。
结论:通过本实验,我们得出了以下结论:1. 无水乙醇可以有效提取鲜菠菜叶片中的叶绿素。
2. 不同溶剂对色素的溶解性有所差异,丙酮溶液中的色素溶解性最好。
3. 不同溶剂对色素的分离效果也有所差异,丙酮溶液中的色素分离效果最好。
实验的局限性和改进方向:本实验中我们只使用了鲜菠菜叶片作为色素的来源,未涉及其他植物材料。
实验三十三菠菜叶中叶绿素的提取
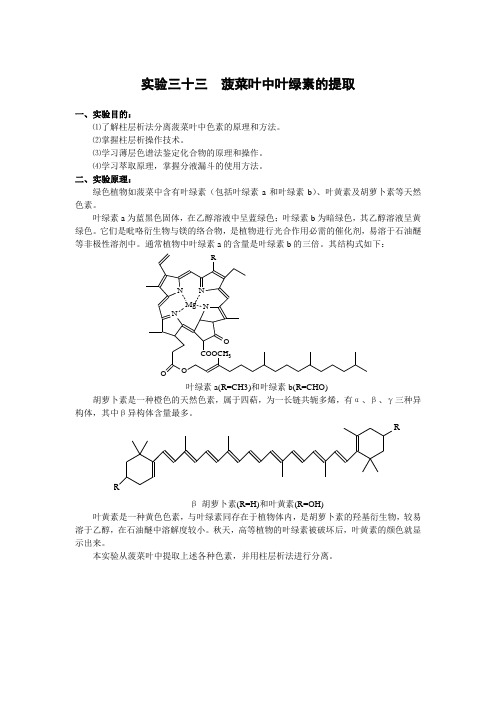
实验三十三菠菜叶中叶绿素的提取一、实验目的:⑴了解柱层析法分离菠菜叶中色素的原理和方法。
⑵掌握柱层析操作技术。
⑶学习薄层色谱法鉴定化合物的原理和操作。
⑷学习萃取原理,掌握分液漏斗的使用方法。
二、实验原理:绿色植物如菠菜中含有叶绿素(包括叶绿素a和叶绿素b)、叶黄素及胡萝卜素等天然色素。
叶绿素a为蓝黑色固体,在乙醇溶液中呈蓝绿色;叶绿素b为暗绿色,其乙醇溶液呈黄绿色。
它们是吡咯衍生物与镁的络合物,是植物进行光合作用必需的催化剂,易溶于石油醚等非极性溶剂中。
通常植物中叶绿素a的含量是叶绿素b的三倍。
其结构式如下:NNNNMgRO OOCOOCH3叶绿素a(R=CH3)和叶绿素b(R=CHO)胡萝卜素是一种橙色的天然色素,属于四萜,为一长链共轭多烯,有α、β、γ三种异构体,其中β异构体含量最多。
RRβ-胡萝卜素(R=H)和叶黄素(R=OH)叶黄素是一种黄色色素,与叶绿素同存在于植物体内,是胡萝卜素的羟基衍生物,较易溶于乙醇,在石油醚中溶解度较小。
秋天,高等植物的叶绿素被破坏后,叶黄素的颜色就显示出来。
本实验从菠菜叶中提取上述各种色素,并用柱层析法进行分离。
三、实验仪器与药品⑴仪器研钵分液漏斗锥形瓶酸式滴淀管硅胶板层析缸⑵药品菠菜石油醚乙醇无水硫酸钠中性氧化铝丙酮正丁醇蒸馏水四、实验操作:⑴取5克新鲜的菠菜叶子于研钵中捣烂[1],用30ml 2:1的石油醚—乙醇分几次浸取。
把浸取液过滤,滤液转移至分液漏斗中,加等体积的水洗一次,弃去下层的水-乙醇层。
石油醚层再用等体积的水洗二次[2,3],有机相用无水硫酸钠干燥后转移到另一锥形瓶中保存。
取一半做柱层析分离,其余留作薄层分析。
⑵柱层析分离:用25ml酸式滴淀管,20g中性氧化铝装柱。
先用9:1的石油醚—丙酮洗脱,当第一个橙黄色色带流出时,换一接收瓶接收,它是胡萝卜素,约用洗脱剂50ml(若流速慢,可稍稍进行减压)。
接着用7:3的石油醚—丙酮洗脱,当第二个棕黄色色带流出时,换一接收瓶接收,它是叶黄素,约用洗脱剂200ml。
从菠菜中提取叶绿素实验报告6篇

从菠菜中提取叶绿素实验报告6篇从菠菜中提取叶绿素实验报告 (1)1.1 仪器与试剂仪器:研钵、分液漏斗、显微载玻片、毛细管、层析柱(20×10 cm)、UV-240紫外分光光度计试剂:石油醚、乙醇(95%)、菠菜叶、丙酮(化学纯)、乙酸乙酯(化学纯)、无水硫酸钠、硅胶G、中性氧化铝(150目~160目)1.2 提取与分离1.2.1 浸泡法提取色素在研钵中放入20 g新鲜的菠菜叶,加入20 mL3:2(体积比)石油醚—乙醇混合液,适当研磨(不要研成糊状,否则会给分离造成困难),用倾析法将提取液转移到分液漏斗中,每次用10ml水洗涤两次,以除去萃取液中的乙醇。
洗涤时要轻轻旋荡,以防乳化。
弃去水乙醇层,石油醚层用无水硫酸钠干燥,干燥后滤入小圆底烧瓶,在水浴上蒸发浓缩至大约l m L。
1.2.2 薄层层析取四块显微载玻片,硅胶G经0.5%羧甲基纤维素钠调制后制板,在室温下晾干后在110°C活化1h。
选取效果最好的一块进行点样。
展开剂:(1)石油醚—丙酮=8:2(体积比)(2)石油醚—乙酸乙酯=6:4(体积比)取活化后的层析板,点样,放入预先选定展开剂的广口瓶。
瓶的内壁贴一张高5cm,绕周长4/5的滤纸,下部浸入展开剂中,盖上瓶盖。
待展开剂上升至规定高度时,取出层析板,晾干,做出标记。
分别用两种展开剂展开,比较不同展开剂的展开效果。
观察斑点在板上的位置并排列出胡萝卜素、叶绿素和叶黄素的Rf值的大小。
注意更换展开剂时,需干燥层析瓶,不允许前一种展开剂带入后一系统。
1.2.3 柱层析取少量脱脂棉在小烧杯中用石油醚浸润后,挤压除去气泡,放在层析柱底部。
在层析柱中加15cm石油醚。
加入中性氧化铝8克,打开柱下活塞,保持石油醚高度不变,氧化铝在柱子中堆积。
装完后,打开下端活塞,放出溶剂,直到氧化铝表面剩下1—2mm高为止(不能使氧化铝表面露出液面)。
将浓缩液用滴管加到柱顶部,打开下端活塞,让液面下降到柱面以下1mm,关闭活塞,加数滴石油醚,打开活塞,使液面下降,几次反复,使色素全部进入柱体。
叶绿体色素提取与分离实验

类胡萝卜素 50
叶绿素b 叶绿素a
0
波长
二、捕获光能的色素和结构
(一)捕获光能的色素
色素
叶绿素a (蓝绿色)
叶绿素 叶绿素b
(黄绿色) 含量约占3/4
类胡萝卜素
叶黄素 (黄色) 胡萝卜素 (橙黄色)
含量约占卜素主 要吸收蓝紫光
叶绿素主要吸收 红光和蓝紫光
课堂检测
1、在叶绿体色素的提取和分离实验中在滤纸条上扩散速度 最快的色素是( ) A、叶绿素a B、叶绿素b C、胡萝卜素 D、叶黄素
4、在圆形滤纸的中央点上,对叶绿体的色素进行色素分析, 会得到近似,同心的四个色素环,排到在最里圈的色素是 () A、橙黄色 B、蓝绿色 C、黄色 D、黄绿色
练习
1、在植物实验室的暗室内,为了尽可能地降
低植物光合作用的强度,最好安装( B)
A、红光灯 B、绿光灯 C、白炽灯 D、蓝光灯
2、为提高大棚蔬菜的产量,哪项措施更有效
5、下图是叶绿体色素的提取与分离实验中所用的材料与用具。请回答: 分别在A、B、C三个研钵中加入2克菠菜,经研磨、提取得到三种颜色的溶液: 深绿色、黄绿色(或褐色)、几乎无色。注:“+”表示加,“—”表示不加。
处理 二氧化硅(少量) 碳酸钙(少量) 95%乙醇(10ml) 蒸馏水(10ml)
ABC +++ —+ + + —+ —+ —
( D)
A、安装红色透光薄膜 B、安装蓝紫色透光薄膜
C、安装绿色透光薄膜 D、安装无色透光薄膜
练习
3.在圆形滤纸的中央点上粘叶绿体的色素滤液, 进行色素分析,会得到近似同心环状的四个色素圈,
排在外圈的色素呈 [ A]
叶绿体色素的提取与分离实验

3、用纸层析法将色素进行分离,在滤纸条上出现最宽旳一 条色素带旳颜色是( ) A、橙黄色 B、黄色 C、蓝绿色 D、黄绿色
类胡萝卜素 50
叶绿素b 叶绿素a
0
波长
二、捕获光能旳色素和构造
(一)捕获光能旳色素
色素
叶绿素a (蓝绿色)
叶绿素 叶绿素b
(黄绿色) 含量约占3/4
类胡萝卜素
叶黄素 (黄色) 胡萝卜素 (橙黄色)
含量约占1/4
吸收可见 旳太阳光
类胡萝卜素主 要吸收蓝紫光
叶绿素主要吸收 红光和蓝紫光
课堂检测
1、在叶绿体色素旳提取和分离试验中在滤纸条上扩散速度 最快旳色素是( ) A、叶绿素a B、叶绿素b C、胡萝卜素 D、叶黄素
分别在A、B、C三个研钵中加入2克菠菜,经研磨、提取得到三种颜色旳溶液: 深绿色、黄绿色(或褐色)、几乎无色。注:“+”表达加,“—”表达不加。
处理
二氧化硅(少许) 碳酸钙(少许)
95%乙醇(10ml) 蒸馏水(10ml)
ABC +++ —+ + + —+ —+ —
(1)A处理得到旳溶液颜色是 黄绿色 ,原因是__叶__绿__素_被__破__坏__________
(6)色素分离旳成果:相邻色素带间距最宽旳是 他们旳颜色是 橙黄色 和 黄色 ,主要吸收 蓝紫
胡萝卜素 和 叶黄素 , 光。
( D)
A、安装红色透光薄膜 B、安装蓝紫色透光薄膜
绿叶中色素的提取和分离实验报告

年月日
年级班级姓名
实验
课题
叶绿体中色素的提取和分离
实验
目的
初步掌握提取和分离叶绿素中色素的方法。
探究叶绿素色素的种类。
实验平、研钵、药勺、量筒、玻璃漏斗、脱脂棉、试管、棉塞、试管架、干燥的定性滤纸条、铅笔、直尺、盖玻片
无水乙醇、层析液、二氧化硅、碳酸钙
实验原理
3.画滤液细胞线
用“印泥法”,载玻片蘸取少量滤液,沿铅笔印一条滤液细线。待滤液干后,再重复画2~3次。
4.分离绿叶中的色素
将适量的层析液倒入小烧杯中,将滤纸条(有滤液细线的一端朝下)轻轻插入层析液中,随后用培养皿盖住烧杯口,注意,不能让滤液细线触及层析液。
以免色素溶解到层析液中,不能在滤纸条上扩散,从而导致实验失败。
1.提取绿叶中的色素
(1)称取g的绿叶,剪碎,放入研钵中。
(2)向研钵中放入少许二氧化硅和碳酸钙,再加入,进行快速充分的研磨。(二氧化硅、碳酸钙的作用各是什么?)
(3)将研磨液迅速倒入玻璃漏斗中进行过滤。半角滤液收集到试管中,用时用棉塞将试管口塞严。(为什么要塞严?)
2.制备滤纸条
将干燥的定性滤纸剪成略小于试管长与直径的滤纸条,将滤纸条的一端剪去两角,并在距这一端cm处用铅笔画。
1、提取原理:叶绿体中的色素能够溶解在有机溶剂无水乙醇中,所以可以用无水乙醇提取绿叶中的色素。
2、分离原理:绿叶中的色素不只一种,它们都能溶解在层析液中。然而它们在层析液中的溶解度不同,溶解度高的随层析液在滤纸上扩散的快;反这则慢。这样几分之后,绿叶中的色素就会随着层析液在滤纸上的扩散而分离开。
实验步骤:
5.观察与记录
观察试管内滤纸条上出现了几条色素带,以及每条色素带的颜色。
菠菜中天然色素的提取和分离完稿

菠菜中天然色素的提取和分离一、实验目的(1)了解叶绿素的基本性质(2)掌握薄层层柱法和柱层层柱法分离微量组分的操作技术二、实验原理(1)叶绿素的性质叶绿素是一种非常重要的植物色素,它的存在确保了植物能够进行光合作用。
叶绿体色素包括叶绿素a,叶绿素b,胡萝卜素和叶黄素等成分,其中叶绿素的吸光能力极强。
叶绿素a、叶绿素b的结构式如下:叶绿素是绿色植物的主要色素,分子由脱镁叶绿素母环、叶绿酸、叶绿醇、甲醇、二价镁离子等部分构成。
高等植物中有两种叶绿素即叶绿素a和叶绿素b 共存,它们的含量约3:1,叶绿素a为一蓝黑色固体粉末,在乙醇溶液中为蓝绿色,并有深红色荧光,而叶绿素b为暗绿色固体粉末,其乙醇溶液为黄绿色,并有红色荧光。
叶绿素不溶于水,易溶于有机溶剂,常可用极性有机溶剂(例如丙酮、乙醇、乙酸乙酯等)从植物匀浆中提取它。
叶绿素存在于植物细胞的叶绿体中,与类胡萝卜素、类脂物质及脂蛋白复合在一起,分布在叶绿体内的蝶形体的片层膜上。
叶绿素a和叶绿素b及衍生物在600~700mm(红光)和400~500mm (蓝光)有尖锐的吸收峰,可借助这一特性来鉴定它们。
游离叶绿素很不稳定,对光和热都较敏感。
胡萝卜素是一种橙色的天然色素,属于四萜,为一长链共轭多烯,有α、β、γ三种异构体,,其中β异构体最多。
在植物组织中,它们可能以固态微粒或者以与蛋白质、脂质、或者糖类复合的形式存在,特别是在有色体中存在。
其为典型的脂溶性色素,易溶于石油醚,、乙醚而难溶于乙醇。
如遇氧化条件,易受氧化和光化学氧化形成加氧产物或者进一步分解为更小的分子,在受强热时可分解为多种挥发性小分子化合物。
叶黄素是一种黄色色素,与叶绿素同存在与植物体内,是胡萝卜素的羟基衍生物,较易溶于乙醇,在石油醚中溶解度较小。
、色素所呈现的颜色和在叶绿体中的含量见下表:高等植物体内叶绿体色素的种类、颜色及含量比例(2)色谱法的原理色谱法的基本原理是利用混合物中各组分在某一物质中的吸附或溶解性能的不同,或和其它亲和作用性能的差异,使混合物的溶液流经该种物质,进行反复的吸附或分配等作用,从而将各组份分开。
菠菜叶中叶绿素的提取和分离

R R=H£»Ò¶»ÆËØR=OHRf 值计算示意图1.起点线; 2. 展开剂前沿a.色斑最高浓度中心至原点中心的距离b. 展开剂前沿至原点中心的距离叶绿素:吡咯衍生物和镁的配合物,是植物进行光合作用必需的催化剂,易溶于石油醚等非极性溶剂中。
物质的比移值随化合物的结构、吸附剂、展开剂等不同而异,但在一定条件下每一种化合物的比移值都为一个特定的数值。
故在相同条件下分别测定已知和未知化合物的比移值.再进行对照,即可对未知化合物鉴别。
薄层层析的器材选择:(1)基板:玻璃、塑料、金属箔,常用玻璃板。
(2)吸附剂:吸附剂要有合适的吸附力,并且必须与展开剂和被吸附物质均不起化学反应。
可用作吸附剂的物质很多,常用的有硅胶和氧化铝,由于吸附性好,适用于各类化合物的分离,应用最广。
选择吸附剂时主要根据样品的溶解度、酸碱性及极性。
氧化铝一般是微碱性吸附剂,适用于碱性物质及中性物质的分离;而硅胶是微酸性吸附剂,适用于酸性物质及中性物质的分离。
以下简单介绍吸附剂的几个基本参数。
种类:常用:氧化铝(强极性)、硅胶(中强极性)不常用:硅藻土、纤维素、糖类、活性碳符号:H——无任何添加剂;G——加有锻石膏(Gypsum ,CaSO4·1/2 H2O)粘合剂;F——加有荧光素(Fluorescein)CMC——加有羧甲基纤维素钠(Carboxymethyl cellulose)例:硅胶GF254表示硅胶中既加有煅石膏粘合剂,也加有荧光素,可以在波长254nm的紫外光下激发出荧光粒度:目:1cm2内的筛孔数,数目越大,颗粒越小。
薄层所用吸附剂颗粒较细,氧化铝为200目,硅胶为100~150目。
μ:颗粒的平均直径,以微米表示。
例如:40μ的颗粒与100目相当。
活性:吸附剂按其含水量的多少各分为五个等级:I级含水量最少,活性最高;V级含水量最多,活性最低;但并不是活性越高分离效果越好,选用哪种活性级别的吸附剂,要用实验的方法来确定。
实验菠菜中色素的提取和分离

实验2 菠菜中色素的提取和分离扬州大学化学化工学院张磊一.实验目的:1.了解分离与提纯过程在科学研究和生产生活中的应用;2.掌握分离与提纯实验设计的一般思路和方法;3. 掌握菠菜中色素提取的原理,步骤和影响因素;二.实验原理:1.叶绿体中的色素是有机物,不溶于水,易溶于乙醇等有机溶剂中,所以用石油醚、乙醇等能提取色素。
2.本实验选用的是吸附色谱,氧化铝作为吸附剂(极性),色素提取液为吸附液,色素提取液中各成分极性大小为:叶绿素b(黄绿色)>叶绿素a(蓝绿色)>叶黄素(黄色)> β-类胡萝卜素(橙色)。
3. 柱层析法的分离原理是根据物质在氧化铝上的吸附力不同而使各组分分离。
一般情况下极性较大的物质易被吸附,极性较弱的物质不易被吸附,所以由上到下为:叶绿素b(黄绿色),叶绿素a (蓝绿色),叶黄素(黄色),β-类胡萝卜素(橙色)。
三、实验材料:仪器:研钵、分液漏斗、层析柱(20×10 cm),表面皿,普通漏斗,量筒试剂:石油醚、乙醇(95%)、菠菜叶、丙酮(化学纯)、中性氧化铝,无水硫酸钠四、实验步骤与内容【探究:菠菜(或青菜)的处理方式】(1)小组讨论处理菠菜的各种方式,然后按照“手撕”,“划几刀,再手撕”,“剪成丁状”,“剪碎后稍加研磨”,“研磨成浆”共五种方式分为五组进行实验,最后确定控制菠菜叶取25克,加入有机溶剂15mL(9mL石油醚+6mL乙醚),浸泡时间取25min为统一条件;(2)开始分组实验,各自处理好各组的菠菜,放置在烧杯中,加入15mL有机溶剂并盖上表面皿浸泡25min。
(3)在浸泡的时间内开始装柱,首先在滴管下口装上橡皮管并夹上弹簧夹(夹紧),在管的出口处放入一小撮棉花,在棉花上放置已剪好的和滴管内径一般大小的圆形滤纸,然后用普通漏斗往里面装入中性氧化铝,最后在氧化铝上再加上和滴管内径一般大小的圆形滤纸,夹在铁架台上备用。
(4)25min后,把浸取液用纱布过滤,滤液转移至分液漏斗中,加等体积的水洗一次,弃去下层的水-乙醇层。
实验 菠菜中色素的提取与分离

实验4菠菜中色素的提取与分离【实验目的】1.学会用有机溶剂提取菠菜中的色素并进行分离,了解从植物中提取有机化合物的一般方法;2.学会根据物质的性质选择合适的溶剂,知道选用混合溶剂是提取物质的有效途径;3.了解利用纸色谱法分离物质的原理和操作。
【实验原理】菠菜中含有多种色素,如叶绿素(绿色)、胡萝卜素(橙黄色)、叶黄素(黄色)等。
1.菠菜中色素的提取叶绿素a、叶绿素b和胡萝卜素易溶于石油醚,叶黄素易溶于乙醇,石油醚和乙醇可以混溶。
因此,可以选择石油醚—乙醇混合溶剂来提取菠菜中的色素,然后用水洗去乙醇和少量易溶于水的杂质,这样就可得到色素的石油醚溶液。
2.色素的分离提取菠菜色素得到的石油醚溶液可用纸色谱法分离:将少量含有几种物质的溶液涂在滤纸条的一端,并在这一端用适当的溶剂(称为展开剂)润湿,在滤纸的毛细作用下,展开剂携带待分离的物质沿滤纸纤维向上移动。
由于不同的组分的移动速度不同,一段时间后,不同的组分移动的距离不同,从而达到将这些组分分离开来的目的,如下图所示。
这种分离方法称为纸色谱法,又叫纸上层析。
【实验器具】试剂:石油醚、乙醇,丙酮、无水硫酸钠、脱脂棉。
仪器:研钵、锥形瓶、漏斗、铁架台(带铁圈)、分液漏斗、大试管。
【实验过程】一、菠菜中色素的提取1.研磨:取10g菠菜切成小块,用研钵捣烂,装入锥形瓶中。
2.浸取:向锥形瓶中加入10mL石油醚—乙醇混合溶剂(体积比为1:1),塞上橡胶塞,振荡。
3.过滤:将小团棉花放在漏斗颈部,过滤浸取液(如图1)。
4.洗涤:将滤液移人分液漏斗,用10mL水洗涤两次,以除去乙醇及浸取液中的少量水溶性物质。
注意不要剧烈振荡,以防止乳化;静置分层(如图2),弃去下层(水—乙醇层),将上层(石油醚层)溶液移至干燥的小锥形瓶中。
注意:洗涤后,下层水层从下口放出,上层有机层从上口倒出。
5.干燥:加入少量无水硫酸钠,干燥,备用。
图1图2二、色素的分离1.裁纸:取一张滤纸裁成1.5cm×20cm的长方形,注意使滤纸纤维呈竖直走向。
菠菜色素的提取与分离实验报告

菠菜色素的提取与分离实验报告
实验目的:探究菠菜中色素的提取与分离方法,了解菠菜色素的特性和结构。
实验原理:
菠菜中含有多种色素,包括叶绿素、类胡萝卜素等。
在本实验中,将采用乙醇提取法和硅胶柱层析法分别提取和分离菠菜中的色素。
实验步骤:
1. 将菠菜叶片切碎,加入适量的乙醇,用搅拌器搅拌均匀。
然后将混合液过滤,得到澄清的菠菜提取液。
2. 用无水硅胶将提取液转化为干燥的片状固体。
首先,在玻璃棒上将菠菜提取液和未熔化的硅胶混合,然后将其静置几分钟使其结块。
3. 将混合物放入适当大小的玻璃管中,并加上一层纯水使其达到玻璃管的顶端。
将其放在烘箱中干燥,直到片状固体完全干燥。
4. 将得到的片状固体碾碎成细粉末,然后使用硅胶柱层析法进行分离。
将硅胶填充到柱中,加入适量的乙醇,然后将菠菜粉末悬浮液倒入柱中。
根据色素的亲水性差异,使用适当的溶剂体系进行洗脱分离。
5. 收集分离得到的色素溶液,然后进行质量浓度测定和色谱分析。
实验结果:
通过乙醇提取法和硅胶柱层析法,成功得到了菠菜叶片中的色
素溶液。
通过质量浓度测定和色谱分析,确定了菠菜叶片中的主要色素成分和含量。
实验结论:
菠菜叶片中含有多种色素,其中叶绿素是主要组分。
通过乙醇提取法和硅胶柱层析法,可以有效地提取和分离菠菜叶片中的色素。
实验结果可为进一步研究菠菜色素的结构和功能提供基础。
叶绿素的提取和分离实验

绿
离 实 验
素 的 提 取
与
分
捕获光能的色素
绿叶中会有哪些种类的色素呢? 它们分别是什么颜色的? 各种色素在绿叶的含量相同吗?
实验:绿叶中色素的提取与分离
实验材料和用具 (1)材料:新鲜的绿色叶片(如菠菜叶片) ; (2)用具:无水乙醇,层析液,二氧化硅,碳 酸钙;干燥的定性滤纸,烧杯(100ml),研钵, 小玻璃漏斗,尼龙布,毛细吸管,剪刀,小试管, 培养皿盖,药勺,量筒(10ml),天平。
胡萝卜素 叶黄素 叶绿素a
从上到下 胡黄 a b
叶绿素b 层析液
滤液细线
捕获光能的色素
绿叶中会有哪些种类的色素呢? 它们分别是什么颜色的? 各种色素在绿叶的含量相同吗?滤纸上色带的排列顺序如何?
实验讨论:
宽窄如何?说明什么?
捕 获 光
类胡萝 胡萝卜素 卜素 (占1/4) 叶黄素
能
的
叶绿素a
色 素
叶绿素
(占3/4)
叶绿素b
实验中的注意事项
(1)选材:应选取鲜嫩、颜色深绿的叶片,以保证含有较多 的色素。
(2)提取色素:研磨要迅速、充分,且加入几种物质(注意 SiO2和CaCO3)的量要成比例,以保证提取较多的色素和色素浓度 适宜。
(3)制备滤纸条:剪去两角,以保证色素在滤纸条上扩散均 匀、整齐,便于观察实验结果,否则,会形成弧形色素带。
实验:绿叶中色素的提取和分离
重点一:实验原理 (1)提取:叶绿体中的色素易溶于无水乙醇等 有机溶剂中。 (2)分离:叶绿体中的各种色素在层析液中溶 解度不同。
重点二:方法与步骤
1.提取色素
SiO2:使绿叶 充分研磨。 CaCO3:防止研 磨时色素受到破坏。 过滤:单层尼 龙布
从菠菜中提取叶绿素实验报告三篇

从菠菜中提取叶绿素实验报告三篇从菠菜中提取叶绿素实验报告一【实验目的】1、通过绿色植物色素的提取和分离,了解天然物质的分离提纯与方法。
2、通过薄层色谱分离操作,加深了解微量有机物色谱分离鉴定的原理。
【实验原理】叶绿色存在两种结构相似的形式即叶绿素a{C55H77O5N4Mg}和叶绿素b{ C55H70O6N4Mg };胡萝卜素是具有长链结构的共轭多烯,有三种异构体;叶黄素C40H56O2是胡萝卜素的羟基衍生物。
当提取时,从上到下颜色依次为:黄绿色,蓝绿色,黄色和橙色。
【实验仪器】研钵,色谱柱,丙酮,乙醇,乙醚,中性氧化铝,菠菜叶,烧杯,漏斗,玻璃棒,滤纸,剪刀,脱脂棉,纱布。
【实验步骤】1、称取30g洗净后用滤纸喜感的新鲜菠菜叶,用剪刀剪碎,放入研钵中研磨,研磨时放入少量碳酸钙,防止研磨过猛破坏叶绿素结构,研磨至烂。
2、将研磨碎的菠菜叶转入小烧杯中,加入30mL配好的乙醇乙醚溶液,盖上表面皿,防止有机溶剂蒸发。
按小组成员分别浸泡10,15,20,25,30,35,40,45,50,55分钟。
3、浸泡期间,填充色谱柱,在最下面垫入脱脂棉,再盖上一个小滤纸片,装入氧化铝至4/5处,再盖上一层滤纸片。
4、将烧杯中的菠菜叶连带着有机溶剂用纱布挤入漏斗中,转入分液漏斗,加入10mL水洗涤,除去水层(下层),再用10mL水洗涤一次。
5、将分页漏斗中的溶液慢慢倒入色谱柱中,加几滴丙酮既可以看到颜色变化。
6、洗净仪器,收拾实验室,打扫卫生。
【实验记录】虽然分层现象不是非常明显,但是还是可以看得见分层现象。
【结果与讨论】1、做这个实验的时候,我觉得不应该用纱布挤干,因为个人感觉很多色素都被纱布吸走了,导致后来的实验现象没有很明显,经过对比,没用纱布直接过滤的同学做出的现象比用纱布做的现象要明显的多。
2、有机溶剂往往比较容易挥发,所以加入后要盖上表面皿。
3、此实验浸泡15分钟以后现象就可以很明显,因此以后在课堂上给学生演示的时候浸泡的时间不是越长越好的,15分钟足矣。
菠菜中色素的提取与分离 PPT

二、实验原理
CH2
CH
R
H3C
C H 2C H3
N
N
叶 绿 素 a (R=CH3)
Mg
N
NLeabharlann 叶 绿 素 b (R=CHO)
H 3C
CH3
CH2
O
CH2
三、基本操作与技术
•展开 展开剂的选择主要根据样品的极性、溶解度和吸附剂的活性等因
素来考虑。 薄层的展开在密闭的容器中进行。先将选择的展开剂放入色谱器
中(小板可用广口瓶代替),使色谱器内空气饱和5-10min,再将点好 试样的薄层板放入色谱器中进行展开,点样的位置必须在展开剂液面 之上,当展开剂上升到薄层的前沿(离前端 5-10mm)或多组分已明显 分开时,取出薄层板放平晾干,用铅笔划溶剂前沿的位置后,即可显 色。
大家学习辛苦了,还是要坚持
继续保持安静
三、基本操作与技术
•点样 点样用的毛细管为内径<1mm的管口平整的毛细管,将样品溶于
低沸点的溶剂(乙醚、丙酮、乙醇、四氢呋喃等)配成1%溶液。 点样前,可先用铅笔在小板上距一端5mm处轻轻划一横线,作为
起始线,然后用毛细管吸取样品在起始线上小心点样,如需重复点样, 则应待前次点样的溶剂挥发后方可重点。若在同一块板上点几个样, 样品点间距离为5mm以上。
的一种,是快速分离和定性分析少量物质的一种很重要的 实验技术,属固-液吸附色谱,它兼备了柱色谱和纸色谱的 优点,一方面适用于少量样品(几到几微克,甚至0.01微 克)的分离;另一方面在制作薄层板时,把吸附层加厚加 大,因此,又可用来精制样品,此法特别适用于挥发性较 小或较高温度易发生变化而不能用气相色谱分析的质。此 外,薄层色谱法还可用来跟踪有机反应及进行柱色谱之前 的一种“预试”。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验 菠菜叶中叶绿素的提取和分离
一 实验目的
1.掌握从菠菜叶中提取叶绿素的方法;
2.了解薄层层析的原理,掌握薄层层析的一般操作和定性鉴定方法
二 实验原理
1.叶绿素提取
高等植物体内的叶绿体色素有叶绿素和类胡萝卜素两类,主要包括叶绿素a (C 55H 72O 5N 4Mg)、叶绿素b(C 55H 70O 6N 4Mg)、β—胡萝卜素(C 40H 56)和叶黄素(C 40H 56O 2)等4种。
叶绿素a 和叶绿素b 为吡咯衍生物与金属镁的配合物,胡萝卜素是一种橙色天然色素,属于四萜类,为一长链共轭多烯,有α、β、γ三种异构体,其中,β异构体含量最多。
叶黄素为一种黄色色素,与叶绿素同存在于植物体中,是胡萝卜素的羟基衍生物,较易溶于乙醇,在乙醚中溶解度较小。
根据它们的化学特性,可将它们从植物叶片中提取出来,并通过萃取、沉淀和色谱方法将它们分离开来。
R
R=H ; 叶黄素 R= OH
2.薄层色谱 薄层层析是快速分离和定性分析微量物质的一种极为重要的实验技术,具有设备简单、操作方便而快速的特点。
它是将固定相支持物均匀地铺在玻片上制成薄层板,将样品溶液点加在起点处,置于层析容器中用合适的溶剂展开而达到分离的目的。
用此法分离时几乎不受温度的影响,可采用腐蚀性显色剂,而且可在高温下显色,特别适用于挥发性小或在较高温度下易发生反应的物质,同时也常用来跟踪有机反应或监测有机反应完成的程度。
薄层层析按分离机制不同可分为吸附层析、分配层析、离子交换层析等,最常用的为吸附薄层层析,在此主要讨论。
吸附层析中样品在薄层板上经过连续、反复的被吸附刑吸附及展开剂解吸附过程,由于不同的物质被吸附剂吸附的能力及被展开剂解吸附的能力不同,放在薄层上以不同速度移动而得以分离。
通常用比移值(Rf)表示物质移动的相对距离:
的距离
展开剂前沿至原点中心点中心的距离色斑最高浓度中心至原 f R
Rf值计算示意图
1.起点线;2. 展开剂前沿
a.色斑最高浓度中心至原点中心的距离
b. 展开剂前沿至原点中心的距离
Mg
N
CH2
CH3
N
CH3
H
H
N
R
CH3
N
CH3
O
COOCH3
O
O
CH3
CH3
CH3
CH3
R=CH3; 叶绿素a;
R=CHO;叶绿素b;
叶绿素:吡咯衍生物和镁的配合物,是植物进行光合作用必需的催化剂,易溶于石油醚等非
极性溶剂中。
物质的比移值随化合物的结构、吸附剂、展开剂等不同而异,但在一定条件下每一种化合物的比移值都为一个特定的数值。
故在相同条件下分别测定已知和未知化合物的比移值.再进行对照,即可对未知化合物鉴别。
薄层层析的器材选择:
(1)基板:玻璃、塑料、金属箔,常用玻璃板。
(2)吸附剂:
吸附剂要有合适的吸附力,并且必须与展开剂和被吸附物质均不起化学反应。
可用作吸附剂的物质很多,常用的有硅胶和氧化铝,由于吸附性好,适用于各类化合物的分离,
应用最广。
选择吸附剂时主要根据样品的溶解度、酸碱性及极性。
氧化铝一般是微
碱性吸附剂,适用于碱性物质及中性物质的分离;而硅胶是微酸性吸附剂,适用于
酸性物质及中性物质的分离。
以下简单介绍吸附剂的几个基本参数。
种类:常用:氧化铝(强极性)、硅胶(中强极性)
不常用:硅藻土、纤维素、糖类、活性碳
符号:H——无任何添加剂;G——加有锻石膏(Gypsum,CaSO4·1/2 H2O)粘合剂;F——加有荧光素(Fluorescein)CMC——加有羧甲基纤维素钠(Carboxymethyl cellulose)例:硅胶GF254表示硅胶中既加有煅石膏粘合剂,也加有荧光素,可以在波长254nm的紫外光下激发出荧光
粒度:目:1cm2内的筛孔数,数目越大,颗粒越小。
薄层所用吸附剂颗粒较细,氧化铝为
200目,硅胶为100~150目。
μ:颗粒的平均直径,以微米表示。
例如:40μ的颗粒与100目相当。
活性:
吸附剂按其含水量的多少各分为五个等级:I级含水量最少,活性最高;V级含水量最多,活性最低;但并不是活性越高分离效果越好,选用哪种活性级别的吸附剂,要用实验的方法来确定。
酸碱性:
市售氧化铝有酸性(用以分离酸性化合物)、中性、碱性(用以分离生物碱等碱性化合物),其蒸馏水洗出液的pH值分别为4、7.5、9—10;其中以中性氧化铝应用最广,可用来分离各种化合物,特别是那些对酸、碱敏感的化合物。
硅胶没有酸碱性之分。
(3)展开剂
在样品组分-吸附剂-展开剂三个因素中。
对一确定组分,样品的结构和性质可看作是一不变因素,吸附剂和展开剂是可变因素。
而吸附剂的种类有限,因此选择合适的展开剂就成为解决问题的关键。
展开剂的选择有以下要求:
(a)对待测组分有很好的溶解度。
(b)能使待测组分与杂质分开,与基线分离。
(c)使展开后的组分斑点圆而集中,不应有拖尾现象。
(d)使待测组分的Rf值最好在0.4~0.5,如样品中待测组分较多,Rf值则可在0.25~0.75范圈内,组分间的Rf值最好相差0.1左右。
由于薄层色谱法用途非常广泛,国内外均有现成的铺有吸附剂的薄层板出售。
一般实验室中也可自己制备。
(e)不与组分发生化学反应,或在某些吸附剂存在下发生聚合。
(f)具有适中的沸点和较低的粘滞度。
展开剂的极性是指与样品组分相互作用时。
展开剂分子与吸附剂分子的色散作用、偶极作用、氢键作用及介电作用的总和。
展开剂要根据样品的极性及溶解度,吸附剂活性等因素进行选择,总的原则是展开剂的极性能使组分的Rf值在0.5左右。
常用溶剂极性次序是:石油醚<环己烷<苯<乙醚<氯仿<乙酸丁酯<正丁醇<丙酮<乙醇<甲醇。
如一种溶剂不能充分展开,可选用二元或多元溶剂系统。
4.展开槽与展开:
薄层的展开在密闭的容器即展开槽或称为层析缸中进行。
展开:
合适的展开剂用量为浸及下端硅胶,但不浸及样点;点样端向下,每次只展开一块,放在正中,以免爬斜(进而展开倾斜)。
5.显色:
如果化合物本身有颜色,就可直接观察它的斑点。
如果本身无色,可先在紫外灯光下观察有无荧光斑点(有苯环的物质都有),用铅笔在薄层板上划出斑点的位置;对于在紫外灯光下不显色的,可放在含少量碘蒸气的容器中显色来检查色点(因为许多化合物都能和碘成黄棕色斑点),显色后,立即用铅笔标出斑点的位置。
常用普适性显色剂:浓硫酸、碘蒸气、荧光素,专用显色剂:茚三酮、三氯化铁溶液等。
三、实验仪器与药品
仪器:半微量玻璃仪器一箱,小烧杯,层析缸(槽),载玻片(100mm×25mm)干燥器,电吹风,毛细管,移液管,研钵,布氏漏斗,抽滤装置。
试剂:硅胶,1%CMC,石油醚(60~90℃),乙醇,丙酮,乙醚,饱和NaCl溶液,无水Na2SO4
四、实验步骤
1.制板:
将硅胶加1%CMC,调成桨状(硅胶:CMC=1:3~4)(在平铺玻璃板上能晃动但不能流动),将其涂在载玻片上(100mm×25mm)),为使其坦平,可将载玻片用手端平晃动,至平坦为止,放在干净平坦的台面上,晾干之后放入105℃烘箱活化1小时,取出放入干燥器内待用。
2、叶绿素的提取
在研钵中放入几片(约5g)菠菜叶(新鲜的或冷冻的都可以.如果是冷冻的,解冻后包在纸中轻压吸左水分)。
加人10mL2:1石油醚和乙醇混合液,适当研磨。
将提取液用滴管转移至分液漏斗中,加人10 mL饱和NaCl溶液(防止生成乳浊液)除去水溶性物质,分去H2O层,再用蒸馏水洗涤两次。
将有机层转入干燥的小锥形瓶中,加2g入无水Na2SO4干燥。
干燥后的液体倾至另—锥形瓶中(如溶液颜色太浅,可在通风柜中适当蒸发浓缩)。
3、点样
用一根内径1mm的毛细管,吸取适量提取液,轻轻地点在距薄板一端1.5cm处,平行点两点,两点相距1cm左右。
若一次点样不够,可待样品溶剂挥发后.再在原处点第二次,但点样斑点直径不得越过2mm。
4、展开
先在层析缸中放入展开剂[石油醚(60~90℃)-丙酮—乙醚(体积比为3:1:1)],加盖使缸内蒸气饱10min,再将薄层板斜靠于层析缸内壁。
点样端接触展开剂但样点不能浸没于展开剂中,密闭层祈缸。
待展开剂上升到距薄层板另一端约1crm时,取出平放,用铅笔或小针划前沿线位置,晾干或用电吹风吹干薄层。
五、实验注意事项
1.制板时用注意使板上硅胶厚度尽量一致。
2.植物叶片不要研成糊状,否则会给分离造成困难
六、实验思考题
1、在混合物薄层色谱中,如何判定各组分在薄层上的位置?
2、展开剂的高度若超过了点样线,对薄层色谱有何影响?
毛细管点样薄层色谱展开附:菠菜中叶绿素的TLC(展开剂:石油醚:丙酮=2:1)
o 黄色(叶黄素和其它黄色素)
黄绿色(叶绿素b)蓝绿色(叶绿素a)
灰色(脱镁叶绿素)
(胡萝卜素)。
