分析化学期中试题
分析化学期中考试题答案

分析化学(一)期中考试题答案一、选择题 ( 共10题 20分 )1. D2. B3. A4. D5. A6. D7. B8. C9. D 10. C二、填空题 ( 共15题 30分 )1. 1.B;2.D;3.C;4.A2. 橙红至黄,黄至橙3. 取样、 试样分解、 干扰组分的掩蔽和分离、 测定、 计算结果。
4. 第二 , 35. 溶解、 熔融、 干灰化6. c /K a 1= 0.010/(1.2×10-3) < 500[]()()L mol 1092201001021410211021H 33233/.....----+⨯=⨯⨯⨯+⨯+⨯-= pH = 2.547. (1)[][][][][][]3342443NH PO 2HPO OH PO H H +++=+---+(2)[][][]-+=+OH HAc H8. 5;9. 100 ; 10. [][]622200100lg 922P H HP lg p pH 2a 1....K =+=+=- 11. 1,0.1;12. 1.8×10-4, 2.4×10-8 (10-3.75, 10-7.62) ;13. NH 4Cl-NH 3·H 2O ;14. -0.02 %,-1.5 %;15. [][][][][]--++++=++F OH CaF Ca 2H 2三、计算题 ( 共 3题 30分 )[]()[]()62.11,38.2,/102.410100.0cK 2 87.2/1035.110100.0cK 1.1375.31374.4==⨯=⨯===⨯=⨯==-----+pH pOH L m ol OH pH L m ol H b a )()(2.0.1000×24.25×500×80.04w (NH 4NO 3) = ───────────────── ×100% = 97.1%25×4.000×100097.1换算成干试样时, w '(NH 4NO 3) = ────── = 99.2%(1-2.20%)3. (20.01+20.04+20.04+20.05+20.06)平均值x = ──────────────── %5= 20.04%s x x i =-=∑()/.240019查表得置信度为95%的t 值为2.78所以 μ=±=±t s n (...)%2004%27800195= (20.04 ± 0.024)% ≈ (20.04 ± 0.02)%四、问答题 ( 共 4题 20分 )1. 进行对照试验,回收试验,空白试验,校准仪器和用适当的方法对分析结果校正。
分析化学期中测试卷

分析化学期中测试卷《分析化学》期中测试姓名:学号:一、单项选择题。
1.可用下列何种方法减小分析测试中的系统误差()。
A.进行仪器校正B.增加测定次数C.认真细致操作D.测定时保持环境湿度一致2.下列各数中,有效数字为四位的是()。
A.[H+]=0.070B.pH=11.57C.2000ppbD.Cu%=17.503.按被测组分含量来分,分析方法中常量组分分析指含量()A.<0.1%B.>0.1%C.<1%D.>1%4.欲配制pH=5.0的缓冲溶液,最好选择()A.一氯乙酸(p K a=2.86)B.氨水(p K b=4.74)C.六亚甲基四胺(p K b=8.85)D.甲酸(p K a=3.74)5.滴定分析的相对误差一般要求达到0.1%,使用常量滴定管滴定时,耗用标准溶液的体积应控制在()。
A. 10mL以下B. 10~15mLC. 20~30mLD. 40~50mL6.用邻苯二甲酸氢钾(KHP)为基准物标定0.1 mol/L NaOH溶液,每份基准物的称取量宜为[Mr(KHP)=204.2]()。
A. 0.2g左右B.0.2g~0.4gC. 0.4g~0.5gD. 0.5g~1.0g7.配制0.1 mol/LHCl溶液时使用的仪器是()。
A.电子天平和烧杯B.量筒和烧杯C.容量瓶和烧杯D.电子天平和容量瓶8.在滴定分析中,对其化学反应的主要要求是()。
A. 反应必须定量完成B. 反应必须有颜色变化C. 滴定剂与被测物必须是1:1反应D. 滴定剂必须是基准物9.已知H3PO4的pK a1,pK a2,pK a3分别为2.12、7.20、12.36,则PO43-的pK b为 ( )。
A. 11.88B. 6.80C. 1.64D. 2.1210.下列酸碱滴定中,由于滴定突跃不明显而不能用直接滴定法进行滴定分析的是:( )A.HCl滴定NaCN (HCN:pKa=9.21)B.HCl滴定苯酚钠 (苯酚:pKa=10.00)C.NaOH滴定吡啶盐 (吡啶:pKb=8.77)D.NaOH滴定甲胺盐 (甲胺:pKb=3.37)11.用0.1mol/L HCl滴定0.1mol/L NaOH时的pH突跃范围是9.7-4.3,用0.01mol/L HCl滴定0.01mol/L NaOH 的突跃范围是()A.9.7~4.3B.8.7~4.3C. 8.7~5.3D.10.7~3.312.已知H3PO4的K a1 = 7.6×10-3, K a2 = 6.3×10-8, K a3 = 4.4×10-13,若以NaOH溶液滴定H3PO4溶液,则第二化学计量点的pH约为( )A. 10.7B. 9.7C. 7.7D. 4.913.已知H3AsO4的p K a1= 2.2, p K a2= 6.9, p K a3= 11.5,则在pH=7.0时, 溶液中[H3AsO4]/[AsO43-]等于( )A. 100.4B. 10-0.4C. 10-5.2D. 10-4.814.某病人吞服10g NH4Cl 1小时后, 他血液的pH = 7.38。
分析化学期中考试试题

一、单项选择题。
(每题2分,共40分)1误差是衡量 .............................................................. ( )A. 精密度B.置信度C.准确度D.精确度2、........................................... 分析测定中论述偶然误差正确的是( )A. 大小误差出现的几率相等B.正误差出现几率大于负误差C.负误差出现几率大于正误差D.正负误差出现的几率相等3、计算x=11.25+1.3153+1.225+25.0678,答案x 应为....................... ( )A.38.66B.38.6581C.38.86D.38.674、有两组分析数据,要比较它们的精密度有无显著差异,则应用 ......... ( )A. t检验B. F检验C. Q检验D. u检验5、在置信度为95%时,测得Al 2O3的平均值的置信区间为35.21 ± 0.10,其意是( )A. 在所测定的数据中有95%的数据在此区间内B. 若再进行测定系列数据,将有95%落入此区间C. 总体平均值卩落入此区间的概率为95%D. 在此区间内包括总体平均值□的把握有95%6、二乙三胺五乙酸(H5L)的pKa1~pKa5分别为1.94, 2.87, 4.37, 8.69, 10.56。
其溶液中的Na2H3L组分浓渡最大的pH值是....................................... ( )A.3.62B.5.00C.9.62D. 2.877、浓度为cmol/L的H2SO4和HCOOH混合液的质子条件是 .................... ( )- 2 -A. [H +]=[OH ]+[HSO 4 ]+[SO 4 ]+[HCOO ]B. [H +]=[OH ] +[SO 4 ]+[HCOO ]—2 -C. [H+]=[OH ]+[HSO 4 ]+2[SO 4 ]+[HCOO ]+ - 2D. [H ]=[OH ]+[HSO 4 ]+2[SO 4 ]8、用NaOH 滴定H3PO4 (pKa1~ pKa3 分别为2.12, 7.20, 12.36)至第二计量点,pH 值为..................................................................... ( )A.10.70B.9.78C.8.74D.7.789、在pH=10.0 的氨性溶液中,已计算出Zn(NH3) =104.7, zn(oH) 卩2" , y(H) 卩0",则在此条件下,lgK MY为(已知IgK MY =16.5) ............................... ( )A.8.9B.11.8C.14.3D.11.310、铬黑T (EBT )与Ca2+的络合物的稳定常数K ca-EBT=105.4,已知EBT的逐级质子化常数K H1=1011.6,K H2= 106。
分析化学期中试卷原稿

下列有关准确度、精密度、系统误差、随机误差之间的关系的说法中,正确的是哪一种?A.准确度高,精密度一定高。
B.精密度高,不一定能保证准确度高。
C.系统误差小,准确度一般较高。
D.随机误差小,准确度一定高。
E.准确度高,系统误差与随机误差一定小。
下列有关准确度、精密度、系统误差、随机误差之间的关系的说法中,错误的是哪一种?A.准确度高,精密度一般较高。
B.精密度高,不一定准确度高。
C.系统误差小,准确度一般较高。
D.随机误差小,准确度一定高。
D减少随机误差的方法有A.增加平行测定次数B.进行对照试验C.进行空白试验D.进行方法校正A3、根据有效数字运算法则,(1.276×4.17)+ 1.7×10-4 -(0.0021764×0.012)=( B )。
A.5.321B.5.32C.5.3D.5.3211下列数据中两位有效数字的是A.0.32 B.98 C.K a1=1.05×10-4 D.pK a=8.00A溶液的[H+]为1.0×10-7mol/L,则该溶液的PH为A.7B.7.0C.7.00D.7.000C6、下列因素中,产生系统误差的是( B )。
A.称量时未关天平门B.砝码稍有侵蚀C.滴定管末端有气泡D滴定管最后一位读数估计不准.9、对于酸碱指示剂,全面而正确的说法是( B )。
A.指示剂为有色物质B.指示剂为弱酸弱碱,其酸式或碱式结构具有不同颜色C.指示剂为弱酸或弱碱D.指示剂在酸碱溶液中呈现不同颜色10、以下四种滴定反应,突跃范围最大的是( B )。
A. 0.1mol·L-1 NaOH滴定0.1mol/L HClB. 1.0mol·L-1 NaOH滴定1.0mol/L HClC. 0.1mol·L-1 NaOH滴定0.1mol/L HACD. 0.1mol·L-1 NaOH滴定0.1mol/L HCOOH6、已知标准溶液B与被测物质A之间的化学反应为:aA + bB = cC + dD,则滴定度T B/A与物质的量浓度C B之间的换算公式为:T B/A=()。
分析化学期中考试试题

一、单项选择题。
(每题2分,共40分)1、误差是衡量 ······································································································ ( )A.精密度B.置信度C.准确度D.精确度2、分析测定中论述偶然误差正确的是 ······························································ ( )A.大小误差出现的几率相等B.正误差出现几率大于负误差C.负误差出现几率大于正误差D.正负误差出现的几率相等3、计算x=11.25+1.3153+1.225+25.0678,答案x 应为········································ ( )A.38.66B.38.6581C.38.86D.38.674、有两组分析数据,要比较它们的精密度有无显著差异,则应用 ·················· ( )A. t 检验B. F 检验C. Q 检验D. u 检验5、在置信度为95%时,测得Al 2O 3的平均值的置信区间为35.21±0.10,其意是( )A.在所测定的数据中有95%的数据在此区间内B.若再进行测定系列数据,将有95%落入此区间C.总体平均值μ落入此区间的概率为95%D.在此区间内包括总体平均值μ的把握有95%6、二乙三胺五乙酸(H 5L )的pKa 1~pKa 5分别为1.94,2.87,4.37,8.69,10.56。
定量分析化学期中复习试题2(1)[1]
![定量分析化学期中复习试题2(1)[1]](https://img.taocdn.com/s3/m/d379c60ea4e9856a561252d380eb6294dd882221.png)
定量分析化学期中复习试题2(1)[1]定量分析化学期中复习试题2一、单项选择题:(共15题,每小题2分,共30分)1、下列操作正确的是()A、把碘标准溶液放在碱式滴定管中B、K MnO4标准溶液放在酸式滴定管中C、把Na2CO3标准溶液从酸式滴定管中放出D、K2Cr2O7标准溶液从碱式滴定管中放出2、下面数值中,有效数字为4位的是()A、ω(Ca)=25.30%B、pH=10.50C、pM=10.10D、c(H+)=0.0130mol·L-13、定量分析中精密度和准确度的关系是()A、准确度是保证精密度的前提B、分析中首先要求准确度其次才是精密度C、分析中只要求准确度不要求精密度D、只有消除了系统误差后,精密度高,准确度才好4、用0.1000mol·L-的NaOH标准溶液滴定0.1000 mol·L-的EDTA溶液,在滴定曲线上,可能有几个突跃范围(EDTA的Kθa 1=1.0×10-2,Kθa,2=2.1×10-3,Kθa,3=6.9×10-7,Kθa,4=5.5×10-11)()A、4个C、2个D、1个5、在滴定一未知弱酸接近终点时,为什幺要煮沸溶液()A、驱除氧气B、驱除氢气C、驱除CO2D、由于溶液加热时更易看到终点6、摩尔法测定Cl-时,用什幺作指示剂()A、Fe3+B、二苯胺磺酸钠C、二甲酚橙D、K2CrO47、用佛尔哈德法测定Br-含量,没有过滤分离,也没有加入硝基苯,其测定会()A、偏高B、偏低C、无影响D、不能确定8、偶然误差是由某些偶然的外因所引起的测量误差,所以:A、若认真细致的操作,这类误差是可以避免的操作B 、这类误差的统计分布是无规律的C 、这类误差在重复测定中或者一直偏正,或者偏负D 、这类误差在重复测定中有时偏正,有时偏负9、计算2012.1)45.958.13(176.0-?应保留几位有效数字: A 、1 B 、2 C 、3D 、410、1.0×10-1mol ·L -1NH 3Cl 水溶液的pH 值是(NH 3 K b =1.8×10-5):B 、6.37C 、5.13D 、8.8711、双指示剂法测定混合碱溶液时,甲基橙变色时所用的HCl 体积为V 1,酚酞变色所用HCl 体积为V 2,若V 2=V 1,则此溶液组成为:A 、Na 2CO 3B 、NaOH+Na 2CO 3C 、NaHCO 3+Na 2CO 3D 、NaOH+NaHCO 312、HCl 的标定可采用以下何种基准物质:A 、NaOHB 、Na 2OC 、硼砂D 、草酸钠13、用0.1000mol ·L -1NaOH 标准溶液滴定相同浓度的H 3PO 4溶液,在滴定曲线上可能出现几个突跃。
2022分析化学期中测验(含答案)

2022分析化学期中测验(含答案)一、选择题(单项选择题,每小题2分,共30分)1、分析天平上称取样品7.00某10-2g,其有效数字为:()A、3B、4C、5D、62、某溶液的pH=11.20,其有效数字为:()A、2B、3C、4D、53、用0.1000mol·L-1NaOH溶液滴定0.1000mol·/LHAC溶液时,指示剂应选:()A、甲基橙B、甲基红C、酚酞D、EDTA4、Na2CO3水溶液的质子条件为:()A、[H+]+[H2CO3-]=[OH-]+[CO32-];B、[H+]+[HCO3-]+2[H2CO3]=[OH-]C、[H+]+[HCO3-]+[H2CO3]=[OH-];D、[H+]+2[Na+]+[HCO3-]=[OH-]5、某酸碱指示剂的KHIn为1某10-4,理论上其pH变色范围应为:()A、5—6;B、6—7C、3—5D、2—46、酸碱滴定中选择指示剂的原则是:()A、Ka=KbB、指示剂的变色点pH与化学计量点pH完全符合C、指示剂变色范围处于或部分处于滴定突跃范围内D、指示剂应在pH=7.00时变色7、下列物质均为“分析纯”,何种可用直接法配制标准溶液:()A、固体NaOH;B、液体盐酸;C、固体K2Cr2O7;D、固体Na2S2O38、浓度相同的下列物质水溶液的pH最高的是:()A、NaCl;B、NaHCO3;C、NH4Cl;D、Na2CO33+9、在实验室用EDTA滴定Al,应该采用那种滴定方式比较合适:()A、直接滴定;B、返滴定法;C、置换滴定;D、间接滴定10、根据酸碱质子理论,下列物质中既是酸、又是碱的是:()A、HAcB、COC、HPOD、NH11、下列各组物质中,不能用来制备缓冲溶液的是:()A、HCl和NH3·H2O;B、NaOH和HAc;C、Na2H2PO4和Na2HPO4;;D、NaOH和Na2CO312、某酸碱滴定pH突跃为7.7~9.7,适宜用的指示剂是:()A、苯胺黄(pH变色范围为1.3~3.2)B、甲基橙;C、甲基红D、酚酞13、0.2000mol/LEDTA溶液的TFe2O3/EDTA是()(注:Fe2o3的相对分子质量为159.7)A、0.007985g/ml;B、0.07985g/ml;C、0.1597g/ml;D、0.01597g/ml14、影响EDTA配合物稳定性的因素之一是酸效应,酸效应是指:()A、酸能使EDTA配位能力降低的现象B、酸能使某些电解质溶解度增大或减小现象C、酸能使金属离子M配位能力降低的现象D、酸能抑制金属离子M水解的现象15、下列措施中,与改变吸光光度分析的灵敏度无关的(A)A、改变被测溶液的浓度B、改变被测溶液的温度C、改变入射光波长D、采用不同的显色剂16、某学生在用Na2C2O4标定KMnO4溶液浓度时,所得结果偏高,原因可能是(A)A、将Na2C2O4溶解加H2SO4后,加热至沸,稍冷即用KMnO4溶液滴定,B、在滴定的开始阶段,KMnO4溶液滴加过快,C、终点时溶液呈较深的红色;D、无法判断17、用K2Cr2O7滴定Fe2+时,常用H2SO4-H3PO4混合酸作介质,加入H3PO4的主要作用是(B)A、增大溶液酸度B、增大滴定的突跃范围C、保护Fe2+免受空气氧化D、可以形成缓冲体系18、摩尔吸光系数的单位为(A)A、L/mol·cmB、mol/L·cmC、g/mol·cmD、cm/mol·L119、已知TK2Cr2O7/Fe=0.003284g/ml,且MFe=55.85g/mol,则C(K2Cr2O7)=(A)mol/l6A、0.05880B、0.3528C、0.5880D、0.00588020、待测组分为MgO(相对分子量40.304),沉淀形式为MgNH4PO4·6H2O(相对分子量245.41),称量形式为Mg2P2O7(相对分子量222.55),换算因数F等于(A)(A)0.362(B)0.724(C)1.105(D)2.210二、填空题(每空1分,共20分):1、准确度是描述测定值与()相符合的程度,而()是描述平行测定值之间相一致的程度,两者间,()是保证()的先决条件。
大学分析化学期中试题

分析化学(一)期中考试试卷学号班级姓名分数一、选择题( 共10题20分)1. 2 分表示一组数据离散特性的最好标志是------------------------------------------( )(A)全距(B)偏差(C)平均偏差(D)标准差2. 2 分已知H3PO4的p K a1 = 2.12, p K a2 = 7.20, p K a3 = 12.36。
今有一磷酸盐溶液的pH = 4.66, 则其主要存在形式是-------------------------------------------------------------( )(A) HPO42-(B) H2PO4-(C) HPO42- + H2PO4(D) H2PO4-+ H3PO43. 2 分用0.10 mol/LNaOH溶液滴定0.10 mol/L HA(K a=5.0×10-5), 若终点的pH为9.0, 则终点误差为----------------------------------------------------------------------------( )(A) +0.02% (B) +0.01%(C) -0.02% (D) -0.01%4. 2 分磷以MgNH4PO4·6H2O形式沉淀,经过滤、洗涤后用适量HCl标准溶液溶解,而后以NaOH标准溶液返滴定,选甲基橙为指示剂,这时磷与HCl的物质的量比n(P):n(HCl)为---------------------------------------------------------------------------( )(A) 1:3 (B) 3:1 (C) 1:1 (D) 1:25. 2 分将PO43-以MgNH4PO4·6H2O形式沉淀,经过滤、洗涤后先用过量HCl标准溶液溶解, 而后以NaOH标准溶液返滴定,此时应选的指示剂是------------------( )(A) 甲基橙(B) 石蕊(C) 酚酞(D) 百里酚酞6. 2 分以下溶液稀释10倍时,pH改变最大的是--------------------------------------( )(A) 0.1mol/L NH4Ac (B) 0.1mol/L NaAc(C) 0.1mol/L HAc (D) 0.1mol/L HCl7. 2 分下面四种表述中,正确的是--------------------------------------------------------( )(1) 置信水平定得越高越好(2) 置信水平太高,对总体平均值的估计往往失去意义(3) 置信水平越高置信区间越宽(4) 置信水平越高置信区间越窄(A)1,2 (B)2,3 (C)3,4 (D)4,18. 2 分今有1L含0.1mol H3PO4和0.3mol Na2HPO4的溶液,其pH应当是--------( )(H3PO4的p K a1~p K a3分别为2.12、7.20、12.36)(A) 2.12 (B) (2.12+7.20)/2 (C) 7.20 (D) (7.20+12.36)/29. 2 分将13.5g六次甲基四胺加到4.0mL 12mol/L HCl中,稀释至100mL,其pH为( ) {p K b[(CH2)6N4] = 8.85, M r[(CH2)6N4] = 140.0}(A) 0.32 (B) 2.57 (C) 4.43 (D) 5.1510. 2 分c(NaCl) = 0.1mol/L的NaCl水溶液的质子平衡式是-------------------------( )(A) [Na+] = [Cl-] = 0.1mol/L (B) [Na+]+[Cl-] = 0.1 mol/L(C) [H+] = [OH-] (D) [H+]+[Na+] = [OH-]+[Cl-]二、填空题( 共15题30分)1. 2 分以下测定和标定各应采用的滴定方式分别是:(填A,B,C,D)(1) 用酸碱滴定法测定CaCO3试剂的纯度____(2) 以K2NaCo(NO2)6形式沉淀,再用KMnO4滴定以测定K+ ____(3) 用K2Cr2O7标定Na2S2O3____(4) 用H2C2O4标定KMnO4____(A)直接法(B)回滴法(C)置换法(D)间接法2. 2 分以甲基橙为指示剂,用NaOH滴定HCl时,终点颜色变化是___________________,用HCl滴定NaOH时,终点颜色变化是__________________________________。
分析化学期中考试试题(答案)
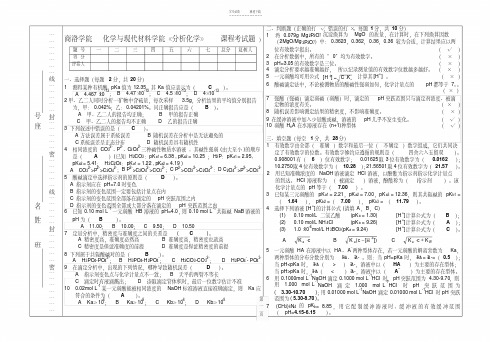
K 2Cr2O7 溶液的物质的量浓度;(2)K 2Cr2O7 对 Fe2+的滴定度(T
)和 K 2Cr2O7
K 2 Cr 2 O 7 / Fe
T 对 Fe2O3 的滴定度(
)(9 分)
K 2 Cr 2 O 7 / Fe 2 O3
解: (1) C m / M
V
2.4515 / 294.18 500.0 10 3
号…
座
密 …
…
…
…
…
线
…
…
…
…
名…
封
姓…
…
…
班…
…
密
…
…
…
…
…
…
…
4. 下列酸碱溶液浓度均为 0.10 mol·L-1,能否采用等浓度的滴定剂直接准确进行滴
定? (共 5 分)
(1)H3BO3 (2 分)
(3)(CH 2)6N4·HCl
( 3 分)
解:( 1) CSP?Ka=0.050 × 5.8 ×-101<010-8 ( 1 分)
=0.007986g m·L-1
(2 分)
或: T = T · K 2Cr2O7 / Fe2O3
K 2 Cr2 O7 / Fe
M Fe2 O3
=0.005586×
159.69
=0.007986g·
-1
mL
2M Fe
2 55.85
第 二 页
(1 分) (1 分 )
学习必备
欢迎下载
…
…
…
…
…
封
…
…
…
…
[H +] 计算公式为(
B ); A ); C )。
分析化学期中考试题(答案)

分析化学期中考试题(答案)分析化学期中考试题(答案)1. 选择题1) 在一次质量为2.5 g的样品中,有1.2 g的氧元素,其氧的质量分数为多少?解答:氧的质量分数 = (氧的质量) / (样品质量) × 100% = (1.2 g) / (2.5 g) × 100% = 48%2) 下列物质中,酸性最强的是:A. Na2SO4B. FeCl3C. H2SO3D. NH3解答:酸性由酸根离子的酸性强弱决定,硫酸根离子(SO4^2-)比氯离子(Cl^-)酸性更强,因此酸性最强的物质是A. Na2SO4。
3) 某元素M的原子量为48,恰好能与氧元素结合成化合物M2O3,求M的化合价。
解答:化合物M2O3表明元素M的化合价为3,因为氧的化合价为-2,而化合物的总电荷为零。
2. 简答题1) 什么是稀释法?解答:稀释法是在已知浓度的溶液中加入溶剂,使其溶液浓度降低的方法。
通过稀释法可以调节溶液的浓度,用以满足实验要求或分析测定的需要。
2) 请简述草酸定量分析法的原理。
解答:草酸定量分析法是基于草酸与高锰酸钾反应的滴定分析方法。
高锰酸钾溶液是一种强氧化剂,草酸是还原剂。
在酸性条件下,草酸与高锰酸钾反应生成无色的四氧化二锰和二氧化碳。
通过滴定的方法,可以确定高锰酸钾溶液中草酸的含量。
3. 计算题1) 某个研究人员称在一种果汁中发现了超过预定值的维生素C含量。
已知该果汁中维生素C的摩尔浓度为0.025 mol/L,某瓶果汁体积为500 mL,求该瓶果汁中维生素C的质量。
解答:维生素C的摩尔质量为176.12 g/mol。
由摩尔浓度可知,该瓶果汁中维生素C的摩尔数为0.025 mol/L × 0.5 L = 0.0125 mol。
维生素C的质量为0.0125 mol × 176.12 g/mol = 2.20 g。
2) 一份未知样品中含有硫酸铜 (CuSO4) 和甲状腺素 (TH)。
《分析化学》期中测试题

《分析化学》期中测试题总分100分单选题(只有一个最佳选项) 多选题(答案为两个或两个以上)姓名: [填空题] *_________________________________1.用移液管移取溶液后,调节液面高度到标线时,移液管应怎样操作( ) [单选题] *A.悬空在液面上B.置容器外C.管口浸在液面下D.管口紧贴容器内壁(正确答案)2.下列哪种滴定液不能装于酸式滴定管( ) [单选题] *A.盐酸滴定液B.高锰酸钾滴定液C.氢氧化钠滴定液(正确答案)D.硫代硫酸钠滴定液E.HAc滴定液3.可以配制准确配制浓度的量器为( ) [单选题] *A.滴定管B.移液管C.容量瓶(正确答案)D.锥形瓶E.吸量管4.下列有关偶然误差的叙述中不正确的是( ) [单选题] *A.偶然误差在分析中可消除(正确答案)B.偶然误差正负误差出现的机会相等C.偶然误差由一些不确定的偶然因素造成D.偶然误差不可消除,但可降低5.用25ml移液管移出的溶液体积应记录为 [单选题] *A. 25mlB.25. 0mlC.25.00ml(正确答案)D.25.000mlE.25.0000ml6.根据滴定突跃范围,用氢氧化钠滴定液滴定盐酸时,可选用下列哪种指示剂 [单选题] *A.甲基黄B.酚酞(正确答案)C.两者均可D.两者均不可7.用0.1mo/L的盐酸滴定0.1mol/L的氢氧化钠溶液,当滴定至化学计量点时,溶液的pH为 [单选题] *A.7.0(正确答案)B.4.3C.9.7D.138.下列叙述中结论错误的是 [单选题] *A. EDTA-2Na的酸效应使配合物的稳定性降低B金属离子的水解效应使配合物的稳定性降低C辅助配位效应使配合物的稳定性降低D.各种副反应均使配合物的稳定性降低(正确答案)9.使用铬黑T指示剂的酸度范围是 [单选题] *A. pH<6.3B. pH6.3~11.6(正确答案)C pH>Il.6D pH 6.3±110.用EDTA滴定金属离子,终点所呈现的颜色是 [单选题] *A.EDTA-金属离子配合物的颜色B.指示剂一金属离子配合物的颜色C.游离指示剂自身的颜色(正确答案)D.EDTA的混合色11.在EDTA-2Na的各种存在形式中,能直接与金属离子配合的是 [单选题] *A.Y⁴⁻(正确答案)B.HY³⁻C.H₄YD.H₆Y²⁺12.化学计量点时,指示剂不变色,使得无法判断滴定终点,是因为 [单选题] *A.指示剂封闭现象(正确答案)B.指示剂僵化想象C.发生沉淀反应D.发生氧化反应13.0.1mol/LNaOH滴定20.00ml 0.1mol/L HAc溶液滴定突跃范围在7.76-9.70 可选用什么指示剂? [单选题] *A.甲基红 pH变色范围4.4-6.2B.酚酞 pH8.0-9.8(正确答案)C.甲基橙pH3.1-4.4D.溴百里酚蓝pH6.0-7.614.间接碘法中若酸度过高,,将会发生什么? [单选题] *A.反应不定量易挥发B.I₂易挥发C.终点不明显D.I⁻被氧化,Na₂S₂O₃被分解(正确答案)15.高锰酸钾法测定H₂O₂含量时,调节酸度时应选用 [单选题] *A.HACB.HCLC.HNO₃D.H₂SO₄(正确答案)16.滴定法中,不用另外加指示剂的是 [单选题] *A.重铬酸钾法B.碘量法C.高锰酸钾法(正确答案)D.福尔哈德法17.对高锰酸钾滴定法,下列说法错误的是 [单选题] *A. 可在盐酸介质中进行滴定(正确答案)B.直接法可测定还原性物质C.标准滴定溶液用标定法制备D.在硫酸介质中进行滴定E.可使用自身指示剂18.莫尔法滴定条件应在 [单选题] *A强酸性B.强碱性C.中性或弱碱性(正确答案)D.中性19.碘量法常用的淀粉指示剂属于 [单选题] *A.自身指示剂B.专属指示剂(正确答案)C.氧化还原指示剂D.金属指示剂20.高锰酸钾法用的指示剂属于 [单选题] *A.自身指示剂(正确答案)B.特殊指示剂C.氧化还原指示剂D.金属指示剂21.在EDTA滴定中,要求金属指示剂与待测金属离子形成配合物的条件稳定常数K′(MIn)值应( )。
分析化学题1

中鉴分析化学期中试题(2)一:选择题1.A2.A3.B4.A5.B6.B7.B8.A9.B10.C11.C12.B13.A1、已知某溶液的氢离子浓度为0.0063,该溶液的pH值是:()A) 2.20;B) 2.201;C) 2.2007 ;D) 2.22、已知硼砂(Na2B4O7·10H2O)的摩尔质量为381.4 g/mol,用它来标定0.1 mol/LHCl溶液,宜称取硼砂为:( )A) 0.45g左右;B) 0.9 g左右;C) 2.25 g左右;D) 4.5g左右3、有关酸碱指示剂的描述,正确的是:()A) 能指示溶液的确切pH值;B) 能在pH值一定的变化范围内呈现不同颜色;C) 显酸色时溶液为酸性,显碱色时溶液为碱性;D) 都是有机弱酸4、如果NaOH标准溶液吸收了空气中的CO2,当用其测定米醋中的醋酸含量时,所得结果将:()A) 偏高;B) 偏低;C) 不受影响;D) 不确定5、用HCl标准溶液滴定一元弱碱时,一定能使滴定突跃增大的情况是:()A) K b不变,c弱碱减小;B) pK b减小,c弱碱增大;C) K b减小,c弱碱增大;D) K b增大,c弱碱减小6、配制NaOH标准溶液时,正确的操作方法是:()A) 在托盘天平上迅速称取一定质量的NaOH,溶解后用容量瓶定容;B) 在托盘天平上迅速称取一定质量的NaOH,溶解后稀释至一定体积,再标定;C) 在分析天平上准确称取一定质量的NaOH,溶解后用量瓶定容;D) 在分析天平上准确称取一定质量的NaOH,溶解后用量筒定容7、在水溶液中共轭酸碱对Ka与Kb的关系是:( )A) Ka•Kb=1;B) Ka•Kb=Kw;C) Ka/Kb=Kw;D) Kb/Ka=Kw8、以下溶液用纯水稀释10倍时pH改变最小的是:( )A) 1 mol/L NaAc-1 mol/L HAc溶液;B) 0.1 mol/L HCl溶液;C) 0.1 mol/L HAc溶液;D) 1 mol/L NH3·H2O溶液9、以甲基红指示剂,能用NaOH 标准溶液准确滴定的酸是()A) 甲酸(pKa=3.75);B) 硫酸(pKa2=1.99);C) 乙酸(pKa=4.75);D) 硼酸(pKa=9.24)10、下列酸碱溶液的浓度均为0.1000 mol/L,其中可按二元酸碱被分步滴定的是()A) 乙二胺(pK b1=4.07,pK b2=7.15);B) 邻苯二甲酸(pK a1=2.95,pK a2=5.41);C) 亚磷酸(pK a1=1.30,pK a2=6.60);D) 联胺(pK b1=5.52,pK b2=14.12)11、.试样用量为0.1 ~ 10 mg的分析称为--------- (C )(A) 常量分析 (B) 半微量分析 (C) 微量分析 (D) 痕量分析12、当pH = 5.00时,0.20 mol L-1二元弱酸(H2A)溶液中,H2A的平衡浓度(游离浓度)为-----( B)(设H2A的pKa1 = 5.00, pKa2 = 8.00)(A) 0.15 mol L-1 (B) 0.10 mol L-1 (C) 0.075 mol L-1 (D) 0.050 mol L-113、下列各组溶液中可用作标准缓冲溶液的是------------------------------------------( A )(A) 0.05 mol L-1 邻苯二甲酸氢钾(B) 甲酸--NaOH(C) 邻苯二甲酸氢钾-HCl(D) Na2B4O7-HCl二、填空题1.(NH4)2HPO4溶液的质子平衡方程为________________________________________________。
分析化学试题b卷参考答案

分析化学 期中试题 (B卷) 参考答案环境科学与工程学院(2007.4)姓名班级学号一、选择题(有且只有一个答案正确,将正确答案的序号写在题前的方括号内,每题2分,共60分)[ A ] 1.根据试样的用量,分析方法可以分成常量、半微量、微量和超微量分析,那么用于常量分析的固体取样量为:(A)>100mg;(B)10~100mg;(C)0.1~10mg;(D)<0.1mg.[ C ] 2.实验室常用的化学试剂按其纯度高低分级,一级试剂是优级纯试剂,其英文简写为:(A)AR;(B)CP;(C)GR;(D)BP.[ B ] 3.物质的量的单位是:(A)g;(B)mol;(C)mol/m3;(D)mol/L.[ C ] 4.下列有关系统误差的正确叙述是:(A)系统误差具有随机性;(B)系统误差在分析过程中不可避免;(C)系统误差具有单向性;(D)系统误差是由不确定的偶然因素造成的.[ D ] 5.下列有关偶然误差的论述,正确的是:(A)偶然误差可以用空白实验消除;(B)偶然误差中大小误差出现的几率是相等的;(C)偶然误差的大小可以衡量准确度的好坏;(D)样本标准偏差大小随测定次数而变化.[ D ] 6.实验室两位新分析人员对同一样品进行分析,得到两组分析结果。
考察两组结果的精密度是否存在显著性差异,应采用的检验方法是:(A)t 检验法;(B)Q检验法;(C)4d检验法;(D)F检验法.[ D ] 7.在分析实验室中,希望尽量减少铬酸洗液的使用,这样因为:(A)目前的玻璃仪器都很清洁;(B)铬酸洗液不稳定;(C)铬酸洗液腐蚀玻璃仪器;(D)铬酸洗液污染环境.[ B ] 8.常用于标定盐酸的基准物质是:(A)邻苯二甲酸氢钾;(B)硼砂;(C)二水合草酸;(D)分析纯石英砂. [ D ] 9.已知浓度的NaOH标准溶液放置时吸收了少量CO2,用它标定HCl时,不考虑终点误差,对标定出的HCl浓度影响是:(A)结果偏高;(B)结果偏低;(C)无影响;(D)决定于滴定时所用的指示剂.[ C ] 10.在滴定分析中,滴定剂的浓度与被测物质的浓度:(A)必须相等;(B)必须均在0.1mol/L;(C)最好大致相当;(D)需要相差10倍以上.[ C ] 11.HPO42-的共轭碱是:(A)H3PO4;(B)HPO42-;(C)PO43-;(D)H2PO4-.[ B ] 12.[H+]+[H3PO4]=[OH-]+[HPO42-]+2[PO43-]是下列哪个化合物在水中的质子条件:(A)H3PO4;(B)NaH2PO4;(C)Na2HPO4;(D)Na3PO4.[ A ] 13.用HCl标准溶液滴定某含有NaOH或NaHCO3或 Na2CO3或任意混合物的样品溶液,量取2份同量溶液,1份以甲基橙为指示剂,耗用HCl标准溶液V1 mL;另1份用酚酞指示剂,耗用HCl标准溶液V2 mL。
定量分析化学期中试卷

定量分析化学期中试卷一、填空题(1)EDTA与金属离子形成的络合物具有_____、______、_______和_______等特性。
(2)已知HCN的pKa=9.14,在pH=5.0时,氰化物的酸效应系数为___________。
(3)pH为7.20的磷酸盐溶液(H3PO4的p K a1 = 2.12, p K a2 = 7.20, p K a3 = 12.36), 磷酸盐存在的主要形式为__________和____________; 其浓度比为___________________。
(4)0.1mol/L NaCl溶液的电荷平衡式是_____________________________________。
(5)用甲醛法测定工业(NH4)2SO4{M r [(NH4)2SO4]=132}中氨的质量分数w(NH3), 把试样溶解后用250 mL容量瓶定容,移取25 mL,用0.2 mol/L NaOH标准溶液滴定, 则应称取试样约_________ g。
二、选择题(1)称取钢样2.000 g,充分燃烧后产生的SO2通入50.00 mol 0.01000 mol/L NaOH溶液中吸收,过量的NaOH 用0.01000 mol/L HCl溶液返滴定至酚酞终点,消耗30.00 mL,则钢样中硫的质量分数为( ) [Ar(S)=32.06, H2SO3的pKa1=1.89,pKa2=7.20](A) 0.16 (B) 0.32 (C) 0.08 (D) 0.64(2)以下物质必须采用间接法配制标准溶液的是 ( )(A) K2Cr2O7 (B) Na2S2O3 (C) Zn (D) H2C2O4·2H2O(3)使用碱式滴定管进行滴定的正确操作是 ( )A 用左手捏稍低于玻璃珠的近旁 B用左手捏稍高于玻璃珠的近旁C 用左手捏玻璃珠上面的橡皮管 D用右手捏稍低于玻璃珠的近旁(4)用基准邻苯二甲酸氢钾标定NaOH溶液时,下列情况对标定结果产生负误差的是A 标定完成后,最终读数时,发现滴定管挂水珠B 规定溶解邻苯二甲酸氢钾的蒸馏水为50ml,实际用量约为60mlC 读数时,终点颜色偏深D 锥形瓶中有少量去离子水,使邻苯二甲酸氢钾稀释(5) HPO42-的共轭碱是 ( )(A) H2PO4-(B) H3PO4(C) PO43- (D) OH-(6)用NaOH标准溶液滴定0.1mol/LHCl-0.1mol/L H3PO4混合液,在滴定曲线上出现几个突跃 ( )(A) 1 (B) 2 (C) 3 (D) 4(7)下列溶液用酸碱滴定法能准确滴定的是 ( )(A) 0.1 mol/L HF (p K a = 3.18)(B) 0.1 mol/L HCN (p K a = 9.21)(C) 0.1 mol/L NaAc [p K a(HAc) = 4.74](D) 0.1 mol/L NH4Cl [p K b(NH3) = 4.75](8)EDTA的酸效应曲线是指 ( )(A) a Y(H)-pH 曲线 (B) pM-pH 曲线(C) lg K'(MY)-pH 曲线 (D) lg a Y(H)-pH 曲线(9)用EDTA直接滴定有色金属离子,终点所呈现的颜色是 ( )(A) 指示剂-金属离子络合物的颜色(B) 游离指示剂的颜色(C) EDTA-金属离子络合物的颜色(D) 上述 B 与 C 的混合颜色(10)在络合滴定中, 用回滴法测定Al3+时, 若在pH=5~6时以某金属离子标准溶液回滴过量的EDTA, 金属离子标准溶液应选 ( )(A) Mg2+ (B) Zn2+ (C) Ag+ (D) Bi3+(11)今有A、B浓度相同的Zn2+-EDTA溶液两份:A为pH = 10.0的NaOH溶液;B为pH = 10.0的氨性缓冲溶液。
《分析化学》期中考试

《分析化学》期中考试1、徐寿:考质求数之学,乃格物之大端,而为化学之极致也”。
这句话中考质”、求数”分别表示()革选题]*A、定性分析、定量分析正确答案)B、定量分析、定性分析C、定性分析、结构分析D、定量分析、结构分析2、下列各项定义中不正确的是()革选题]*A、绝对误差是测定值和真值之差B、相对误差是绝对误差在真值中所占的百分率C、绝对偏差是指测定值与平均值之差D、准确度是反映数据的分散程度正确答案)3、定量分析中,精密度与准确度之间的关系是()单选题]*A、精密度高,准确度必然高B、准确度高,精密度也就高C、精密度是保证准确度的前提(正确答案)D、准确度是保证精密度的前提4、偶然误差具有()单选题]*A、可测性B、重复性C、不确定性(正确答案)D、可校正性5、下列哪种方法可以减小分析测试定中的偶然误差()革选题]*A、对照试验B、空白试验C、仪器校正D、增加平行试验的次数正确答案)6、在进行样品称量时,由于汽车经过天平室附近引起天平震动是属于()单选题]*A、系统误差B、偶然误差正确答案)C、过失误差D、操作误差7、可用下列何种方法减免分析测试中的系统误差()革选题]*A、进行仪器校正正确答案)B、增加测定次数C、认真细心操作D、测定时保证环境的湿度一致8、分析工作中实际能够测量到的数字称为()革选题]*A、精密数字B、准确数字C、可靠数字D、有效数字正确答案)9、下面数值中,有效数字为四位的是()单选题]*A、0. 060pH=11.50Pka = 1.380D、0.6正确答案)10、按有效数字运算规则,213.64+3.8+0.38 =)革选题]*A、217.82B、217C、217.正确答案)D、217.82011、在不加样品的情况下,用测定样品同样的方法、步骤,对空白样品进行定量分析,称之为()革选题]*A、对照试验B、空白试验正确答案)C、平行试验D、预试验12、滴定分析中,对化学反应的主要要求是()单选题]*A、滴定剂必须是基准物B、反应必须有颜色变化C、滴定剂与被测物必须是1:1的计量关系D、反应必须定量完全反应正确答案)13、直接法配制标准溶液必须使用()革选题]*A、基准试剂正确答案)B、化学纯试剂C、分析纯试剂D、优级纯试剂14、滴定管可估读到±).01mL,若要求滴定的相对误差小于0.1%,至少应耗用体积()mL [单选题]*A、10(正确答案)B、20C、30D、4015、欲配制10mL 0.1mol/L HCl溶液,应取浓盐酸12mol/L HCl()mL。
分析化学期中考试考试题答案

分析化学考试题(化工专业)一、填空题每填空1分,共32分)1.根据测量原理分类,分析方法有(化学分析)和(仪器分析)。
2.定量分析过程通常包括(取样);(试样的分解);(待测组分测定);(结果计算)。
3.用沉淀法测定纯NaCl中氯的质量分数,得到下列结果:0.5982,0.6000,0.6046,0.5986,0.6024。
则平均结果为(0.6009 );平均结果的绝对误差为(-5.7x10-3 );相对误差为(-0.94% );中位数为(0.6006 );平均偏差为(2.1x10-3 );相对平均偏差为(0.35% )。
4.按照有效数字的运算规则,下列计算式的结果各应包括几位有效数字:(1)213.64+4.402+0.3244 (五)位;(2)0.1000 x (25.00-1.52)x 246.47/(1.000x1000)(四)位;(3)pH=0.03求H+浓度(两)位。
5. 在分析过程中,下列情况各造成何种(系统、随机)误差。
(1)称量过程中天平零点略有变动(随机误差);(2)分析用试剂中含有微量待测组分(系统误差);6. 标定HCl溶液的浓度时,可用Na2CO3或硼砂(Na2B4O710H2O)为基准物质,若Na2CO3吸水,则测定结果(偏高):若硼砂结晶水部分失水,则测定结果(偏低);(以上两项填无影响、偏高、偏低)。
若两者均保存妥当,不存在上述问题,则选(硼砂)作为基准物质更好,原因为(HCL与两者均按1:2计量比进行反应,硼砂摩尔质量大,称量时相对误差小)。
7. 从质量保证和质量控制的角度出发,为了使分析数据能够准确地反映实际情况。
要求分析数据具有(代表性)、(准确性)、(精密性)、(可比性)和(完整性)。
这些反映了分析结果的(可靠性)。
8. 浓度为c(mol/L)H2C2O4溶液的电荷平衡方程:([H+]=[OH-]+[ HC2O4-]+2[C2O42-])9. 根据酸碱质子理论,OH-的共轭酸是(H2O ),HAc的共轭酸是(H2Ac+)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、单项选择题(每题1分,共60分)1.下列说法不正确的是()。
A.随机误差小,准确度一定高B.系统误差小,准确度一般较高C.精密度高,不一定保证准确度高D.准确度高,系统误差与随机误差一定小2.下列情况中,使分析结果产生负误差的是()。
A.以HCl标准溶液测定某碱样,因滴定管未洗净,滴定时内壁挂液珠B.测定H2C2O4·H2O的摩尔质量时,草酸失去部分结晶水C.用于标定标准溶液的基准物质在称量时吸潮了D.滴定速度过快,并在到终点时立即读取滴定管读数3.用邻苯二甲酸氢钾标定NaOH浓度时,会造成系统误差的是()。
A. NaOH溶液吸收了空气中的CO2B.每份邻苯二甲酸氢钾的质量不同C.用甲基橙作指示剂D.每份加入的指示剂量不同4.溶液中含有6.9×10﹣2mol/L OH﹣,其溶液的pH()。
A.12.8388B.12.839C.12.8D.12.845.实验室两位新分析人员,对同一样品进行分析,得到两组分析结果,考查两组结果的精密度是否存在显著性差异,应采用的检验方法是()。
A.F 检验法B. Q检验法C.G检验法D. t检验法6.以加热除去水分法测定2CaSO4·H2O(CaSO4:136.14;H2O:18.02)中结晶水的含量时,称取试样0.2000g,已知天平称量误差为±0.1mg,分析结果的有效数字位数为()。
A. 四位B. 三位C. 二位D. 一位7.下列有关置信度和置信区间的表述中正确的是()。
A. 置信度越高,测定的可信度越高B.置信度越高,置信区间越窄C.置信区间的大小与测定次数有关D.置信区间的中心位置取决于测量次数8.分析测定中,随机误差的特点是()。
A.大小误差出现的几率相等B.负误差出现的几率大于正误差C.正误差出现的几率大于负误差D.正负误差出现的几率相等9.某石灰石试样中CaCO3的质量分数平均值的置信区间为65.38%±0.1%(置信度95%),对此结果应理解为()。
A. 在此区间内,包括总体平均值μ的把握为95%B.有5%的分析结果落在65.28%到65.48%的范围之外C.每次测定值落在此区间的可能性95%D.若再进行测定,将有95%的数据落入此区间10.测定某硅酸盐试样中SiO2的质量分数(%),7次平行测定结果为20.03%、20.04%、20.02%、20.05%、20.06%,20.02%,20.07%标准偏差为()。
A. 2%B. 0.02%C.1.95%D. 0.019%11.测定某钛铁矿中TiO2的质量分数,测定结果符合正态分布N(0.5243,0.00062)。
则20次测定中,落在0.5231~0.5255区间的测定结果有()。
(u=1.0,P=68.3%;u=2.0,P=95.5%;u=3.0,P=99.7%;A.17次B. 18次C. 20次D. 19次12.从精密度好就可以判定分析结果可靠的前提是()。
A. 系统误差小B. 标准偏差小C.随机误差小D.平均偏差小13. 羟胺(NH2OH, p K b=8.04)与HCl 所组成的缓冲溶液pH缓冲范围是( )。
A. 8~10B. 5~7 C .7~9 D. 6~814.已知某一元弱酸HB 的p K a =4.00,用NaOH 标准溶液滴定此溶液时, 应选用的指示剂是( )。
A.甲基红B. 甲基橙C. 酚酞D. 石蕊15.已知浓度的NaOH 标准溶液,因保存不当吸收了CO 2,若用此NaOH 滴定 HAc 至化学计量点,则 HAc 测定结果会( )。
A.无影响 B. 不确定 C. 偏低 D. 偏高16.在0.1 mol/LH 3PO 4溶液中,[HPO 42-]的值约等于( )。
K K K K K K a3a2a2a1a3a2 D..C B.A.17.下列滴定中,只出现一个pH 突跃的是( )。
A.NaOH 滴定H 3PO 4 (p K a1=2.12,p K a2=7.20, p K a3=12.32)B. NaOH 滴定HCl + HAc ( p K a =4.74)C. NaOH 滴定H 2C 2O 4 (p K a1=1.23, p K a2=4.19)D. HCl 滴定Na 2CO 3 (H 2CO 3: p K a1=6.38 p K a2=10.25) 18.下列滴定中,不可以分步滴定的是( )。
A.NaOH 滴定H 3PO 4 (p K a1=2.12,p K a2=7.20, p K a3=12.32)B. HCl 滴定Na 3PO 4C. NaOH 滴定H 2C 2O 4 (p K a1=1.23, p K a2=4.19)D. HCl 滴定Na 2CO 3 (H 2CO 3: p K a1=6.38 p K a2=10.25)19.欲用等浓度的H 3PO 4和Na 2HPO 4溶液 配制pH=7.20的缓冲溶液,则两溶液的体积比应为( )。
A. 3:1B.1:1C.1:2D. 1:320.下列酸中,不能用强碱标准溶液直接滴定的是( )。
A. H 3BO 3(K a =5.8×10-10) B.HAc (K a =1.8×10-5) C.HCOOH (K a =1.8×10-4) D. HCl21.用NaOH 标准溶液滴定一元弱酸(HA)时,一定能使滴定突跃增大的情况是( )。
A . K a 不变,c HA 减小 B.K a 增大,c HA 减小C.p K a 减小,c HA 增大D.K a 减小,c HA 增大22.已知0.10mol/L 一元弱酸HA 溶液的pH=3.00,其等浓度共轭碱NaA 溶液的pH 是( )。
A.9.20 B. 10.00 C. 8.50 D. 9.00 23.浓度相同的下列溶液中,缓冲作用最大的是( )。
A. Na 2B 4O 7·10H 2OB. NaH 2PO 4C. Na 2HPO 4D. NaHCO 3 24.H 2C 2O 4溶液中,分布分数随pH 值增大而增大的型体是( )。
A. OH -B. C 2O 42-C. HC 2O 4-D. H 2C 2O 425.浓度为c mol/L 的HAc 溶液中加入c a mol/L 的HCl 和c b mol/LNaOH 后的质子守恒式正确的是( )。
A.[H +]+ c a = c b + [Ac -]+[OH -]B. [H +]=c b + c a + [Ac -]+[OH -]C. [H +]+ c b = c a + [Ac -]+[OH -]D. [H +]+ c a +c b =[Ac -] +[OH -]26.若用0.1000mol/L NaOH 滴定同浓度的某弱酸HB(p K a=2.70), 则化学计量点pH 为( )。
A 6.30 B. 6.15 C. 7.85 D. 7.70 27.第26题中,突跃范围为( )。
A. 5.70~9.70B. 4.70~9.70C. 6.70~9.70D. 4.30~9.70 28.第26题中,若终点时pH=9.5,则终点误差为( ) A.-0.06% B. +0.06% C. -0.1% D.+0.1%29.用0.1000 mol/LNaOH 滴定0.1000mol/LHCOOH,若将NaOH 和HCOOH 的浓度均增大10倍,则滴定突跃范围ΔpH ( )。
A.不变 B.增大2个pH 单位 C.增大1个pH 单位 D.减小1个pH 单位30.有一碱溶液,可能含有NaOH ,Na 2CO 3或NaHCO 3,也可能是其中两者的混合物,今用HCl 滴定,用酚酞作指示剂,消耗HCl 体积为V 1;若以甲基橙作指示剂,消耗 HCl 体积为V 2。
当V 2 > 2V 1 > 0 ;时,则试液组成为( )。
A. Na 2CO 3 B. NaOH+Na 2CO 3C. NaOH +NaHCO3D. Na2CO3+NaHCO331.在甲基橙(p K a=3.4)指示剂变为红色时pH=3.1,其酸式型体与碱式型体的浓度比[HIn]/[In-]约为()。
A.0.5B. 2C. 0.25D. 432. pH一定的缓冲溶液,其缓冲容量大小与下列因素有关的是()。
A. 缓冲组分的浓度比B. 外来酸碱的量C. 缓冲溶液的总浓度D.缓冲溶液的总浓度和缓冲组分浓度比33.酸碱滴定法选择指示剂可以不考虑的因素是()。
A.滴定突跃的范围B.指示剂的变色范围C.指示剂的颜色变化D.指示剂的相对分子质量的大小34.纯NaOH和NaHCO3固体按1:3的物质的量溶于水中,摇匀后再用双指示剂法测定,已知酚酞﹑甲基橙变色时,滴入HCl标准溶液的体积分别为V1、V2,则V1/V2为()。
A. 1:3B.1:2C.3:1D. 2:135.标定NaOH溶液时,下列基准物质中最合适的是()。
A. H2C2O4·2H2OB.邻苯二甲酸氢钾C. HCl标准溶液D. 硼砂36.络合滴定中下列说法正确的是()。
A.酸度越低,滴定突跃越大B.酸度越低,lg K´MY越大C.酸度越低,EDTA的酸效应越小D.酸度越低,EDTA的酸效应越大37.pH=12.0的水溶液中, EDTA存在的主要形式是( )。
A.H6Y2+B. H4YC. H2Y2-D. Y4-38.在络合滴定中,用返滴定法测定Al3+, 若在pH = 5~6时,以某金属离子标准溶液返滴过量的EDTA, 最合适的标准溶液是()。
A. Zn2+B. Mg 2+C. Ag+D. Bi3+39.若配制EDTA溶液的水中含Ca2+,以CaCO3为基准物质标定EDTA,并用此EDTA滴定试液中的Zn2+ ,二甲酚橙为指示剂,会使测定结果( )。
A.无影响B. 偏低C.偏高D.不确定40.在pH=10.0的氨性缓冲溶液中,用EDTA滴定等浓度的Zn2+,化学计量点时,下列关系正确的是()。
A. [Zn]=[Y']B. [Zn']=[Y]C. [Zn']=[Y']D.[Zn]=[Y]41.在络合滴定中能增大滴定突跃范围的是()。
A.同时增大c M和K'MYB. 同时减小c M和K'MYC.减小c M,.增大K'MYD. 增大c M,减小K'MY42.关于金属指示剂,下列说法正确的是()。
A.MIn越稳定越好B. 指示剂本身随pH改变而显不同颜色C. MIn与MY稳定性应接近相等D.指示剂僵化是由其变质引起的43.准确滴定金属离子可行性的条件是ΔpM=±0.2,E t≤0.1%,( )。
A.lg c M,sp K'MY≥8B. lg K'MY≥8C. l g c M,sp K'MY≥6D. lg K'MY≥644.EDTA测定水中Ca2+和Mg2+含量时,以EBT作指示剂,为消除水样中少量的Fe3+、Al3+对指示剂的封闭作用,应加入()。
