初中常见元素,原子团名称,化学式,化合价
初三化学化合价详细讲解

初三化学化合价详细讲解一、常见元素及原子团的化合价:钾K 钠Na 氢H 银Ag +1价,氟F 氯Cl 溴Br 碘I -1价钙Ca 镁Mg 钡Ba 锌Zn +2价,+1、+2铜Cu,+2、+3铁Fe铝Al+3 硅Si+4 氧O-2常见带电离子团:硫酸根SO42+,硝酸根NO3-,氢氧根OH-,氯酸根ClO3-,碳酸根CO32-铵根NH4+,高锰酸根MnO4- 锰酸根MnO42-,磷酸根PO43-注意:标原子团的化合价时,应标在原子团的上方,如:书写离子符号时,应在原子团右上角标明带电荷数,如硫酸根离子:SO42-一个亚铁离子Fe2+,一个铁离子Fe3+。
二、初中化学物质的检验(一)、气体的检验1、氧气:带火星的木条放入瓶中,若木条复燃,则是氧气.2、氢气:在玻璃尖嘴点燃气体,罩一干冷小烧杯,观察杯壁是否有水滴,往烧杯中倒入澄清的石灰水,若不变浑浊,则是氢气.3、二氧化碳:通入澄清的石灰水,若变浑浊则是二氧化碳.4、氨气:湿润的紫红色石蕊试纸,若试纸变蓝,则是氨气.5、水蒸气:通过无水硫酸铜,若白色固体变蓝,则含水蒸气.(二)、离子的检验.6、氢离子:滴加紫色石蕊试液/加入锌粒7、氢氧根离子:酚酞试液/硫酸铜溶液8、碳酸根离子:稀盐酸和澄清的石灰水9、氯离子:硝酸银溶液和稀硝酸,若产生白色沉淀,则是氯离子10、硫酸根离子:硝酸钡溶液和稀硝酸/先滴加稀盐酸再滴入氯化钡11、铵根离子:氢氧化钠溶液并加热,把湿润的红色石蕊试纸放在试管口12、铜离子:滴加氢氧化钠溶液,若产生蓝色沉淀则是铜离子13、铁离子:滴加氢氧化钠溶液,若产生红褐色沉淀则是铁离子(三)、相关例题14、如何检验NaOH是否变质:滴加稀盐酸,若产生气泡则变质15、检验生石灰中是否含有石灰石:滴加稀盐酸,若产生气泡则含有石灰石16、检验NaOH中是否含有NaCl:先滴加足量稀硝酸,再滴加AgNO3溶液,若产生白色沉淀,则含有NaCl。
初中常见元素_原子团名称_化学式_化合价_相对原子质量_一览表

元素名称原子序数元素符号相对原子化合价质量氢 1 H 1 +1氦2He 4锂3Li 7铍4Be 9硼5 B 11碳6 C 12+2+4氮7N 14-3、+2、+3、+4、+5氧8O 16-2氟9 F 19-1氖10Ne 20钠11Na 23+1镁12Mg 24+2铝13Al 27+3硅14Si 28+4磷15P 31-3、+3、+5硫16S 32-2、+4、+6氯17Cl 35.5-1、+1、+5、+7氩18Ar 40钾19K 39+1钙20Ca 40+2锰25 Mn 55 +2、+4、+6、+7 铁26 Fe 56 +2、+3铜29 Cu 63.5 +1、+2锌30 Zn 65银47 Ag 108钡56 Ba 137铂78 Pt 195金79 Au 197汞80 Hg 201碘53 I 127溴35 Br 80 -1氢氧根OH -1硝酸根NO3-1高锰酸根MnO4-1氯酸根ClO3-1硫酸根SO4-2碳酸根CO3-2铵根NH4+1初中化学常见的原子团(根)及其化合价根的名称根的符号常见化合价常见化合物举例铵根NH4+1 NH4Cl 硝酸根NO3-1 K NO3氢氧根OH -1 Na OH高锰酸根MnO4-1 K MnO4锰酸根MnO4-2 K2MnO4氯酸根ClO3-1 K ClO3醋酸根CH3COO -1 CH3COO H 碳酸根CO3-2 Na2CO3碳酸氢根HCO3-1 Na HCO3硫酸根SO4-2 Cu SO4硫酸氢根HSO4-1 Na HSO4SO3-2 Na2SO3亚硫酸根磷酸根PO4-3 H3PO4HPO4-2 (NH4)2HPO4磷酸氢根H2PO4-1 Ca(H2PO4)2磷酸二氢根二氧化碳的实验室制法。
1、药品:稀盐酸和大理石(或石灰石,主要成分是CaCO3)。
2、条件:常温。
3、原理:CaCO3+2HCl==CaCl2+H2O+CO2↑注意:(1)制取CO2不能用稀硫酸与大理石(或石灰石)反应,因为反应CaCO3+H2SO4==CaSO4+H2O+CO2↑,生成的CaSO4微溶于水,在溶液中析出后包裹在大理石(或石灰水)的外面,阻碍了反应的进一步发生。
常见元素及原子团的化合价

常见元素及原子团的化合价【实用版】目录1.引言2.常见元素的化合价1.1 一价元素:K、Na、Ag、H(NH4)1.2 二价元素:Ca、Mg、Ba、Cu1.3 三价元素:Al(显高价时)1.4 其他元素:S(显负价时)、原子团 O3.常见原子团的化合价3.1 负一价原子团:F、Cl、Br、I、OH、NO33.2 正一价原子团:NH43.3 负二价原子团:硫酸根离子、碳酸根离子、亚硫酸根离子、锰酸根离子3.4 正二价原子团:铜、汞3.5 正三价原子团:铝3.6 负一价离子:氯离子3.7 负三价离子:磷酸根离子4.化合价规律与口诀5.结论正文一、引言化学反应是物质之间相互作用的过程,其中元素和原子团之间的化合价起着至关重要的作用。
了解元素及原子团的化合价规律,有助于我们更好地掌握化学反应的规律,从而在实际应用中发挥更大的作用。
本文将详细介绍常见元素及原子团的化合价,以及相关的规律和口诀。
二、常见元素的化合价1.1 一价元素:K、Na、Ag、H(NH4)钾(K)、钠(Na)、银(Ag)和氢(H)在一般情况下显示 +1 价。
在氨根离子(NH4)中,氢原子团显示 +1 价。
1.2 二价元素:Ca、Mg、Ba、Cu钙(Ca)、镁(Mg)、钡(Ba)和铜(Cu)在一般情况下显示 +2 价。
1.3 三价元素:Al(显高价时)铝(Al)在显高价时,显示 +3 价。
1.4 其他元素:S(显负价时)、原子团 O硫(S)在显负价时,显示 -2 价。
原子团 O 一般显示 -2 价。
三、常见原子团的化合价3.1 负一价原子团:F、Cl、Br、I、OH、NO3氟(F)、氯(Cl)、溴(Br)、碘(I)、氢氧根(OH)和硝酸根(NO3)原子团通常显示 -1 价。
3.2 正一价原子团:NH4铵根(NH4)原子团显示 +1 价。
3.3 负二价原子团:硫酸根离子、碳酸根离子、亚硫酸根离子、锰酸根离子硫酸根离子(SO4^2-)、碳酸根离子(CO3^2-)、亚硫酸根离子(SO3^2-)和锰酸根离子(MnO4^-2)原子团通常显示 -2 价。
常见元素及原子团的化合价表

常见元素及原子团的化合价表CuSO4+2NaOH=Cu(OH)2↓+Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验Ca(OH)2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁Ca(HCO3)2Δ CaCO3↓+H2O+CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成HCl+AgNO3= AgCl↓+HNO3生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Ba(OH)2+ H2SO4=BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+ H2SO4=BaSO4↓+2HCl 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4=BaSO4↓+2HNO3生成白色沉淀、不溶解于稀硝酸检验SO42—的原理FeCl3+3NaOH=Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH=Al(OH)3↓+3NaCl 有白色沉淀生成MgCl2+2NaOH = Mg(OH)2↓+2NaClCuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O = Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2=CaSO3↓+ H2O 有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3=BaCO3↓+2NaOH 有白色沉淀生成Ca(OH)2+K2CO3=CaCO3↓ +2KOH 有白色沉淀生成AgNO3+NaCl = AgCl↓+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子初中常见物质俗称1、氯化钠(NaCl):食盐2、碳酸钠(Na2CO3) :纯碱,苏打,口碱3、氢氧化钠(NaOH):火碱,烧碱,苛性钠4、氧化钙(CaO):生石灰5、氢氧化钙(Ca(OH)2):熟石灰,消石灰 6 、二氧化碳固体(CO2):干冰7、氢氯酸(HCl):盐酸8、碱式碳酸铜(Cu2(OH)2CO3):铜绿9、硫酸铜晶体(CuSO4 .5H2O):蓝矾,胆矾10、甲烷(CH4):沼气11、乙醇(C2H5OH):酒精12、乙酸(CH3COOH):醋酸13、过氧化氢(H2O2):双氧水14、汞(Hg):水银15、碳酸氢钠(NaHCO3):小苏打中化学常见物质的颜色(一)、固体的颜色1、黑色固体(5种):木炭,氧化铜,二氧化锰,四氧化三铁,铁粉2、红色固体:铜——紫红色,氧化铁Fe2O3——红(棕)色3、蓝色晶体:硫酸铜晶体CuSO4·5H2O4、蓝色沉淀:氢氧化铜5、红褐色沉淀:氢氧化铁6、白色沉淀(6种):碳酸钙,碳酸钡,碳酸银;氢氧化镁;硫酸钡,氯化银。
初中常见元素的化合价记忆口诀(完整版)

Al3+
+3
氟
F-
-1
铜
Cu
+1 +2
氯
Cl-
-1
铁
Fe
+2 +3
溴
Br-
-1
氢氧根OH--1锰 NhomakorabeaMn
+2 +4 +6 +7
硝酸根
NO3-
-1
亚硫酸根
SO32-
-2
硫酸根
SO42-
-2
碳酸根
CO32-
-2
铵根
NH4+
+1
★★化合物中化合价有正价和负价、单质都为零价
(1)氧元素通常显-2价(2)氢元素通常显+1价
常见元素和原子团的化合价
元素和根的名称
元素和根
的符号
常见的
化合价
元素和根
的名称
元素和根
的符号
常见的
化合价
氢
H+
+1
碳
C
+2 +4
钠
Na+
+1
硅
Si
+4
钾
K+
+1
银
Ag+
+1
氮
N
-3 +2 +3 +4 +5
钙
Ca2+
+2
磷
P
-3 +3 +5
镁
Mg2+
+2
钡
Ba2+
+2
氧
O2-
(完整版)初中化学必背知识点
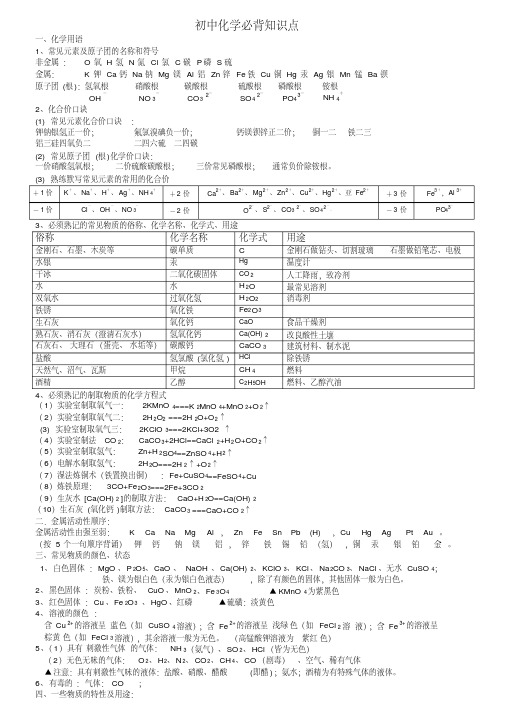
8 、固体物质的溶解度随温度变化的情况可分为三类:
(1) 大部分固体物质溶解度随温度的升高而增大; (2) 少数物
质溶解度受温度的影响很小,如 NaCl; (3) 极少数物质溶解度随温度的升高而减小,如
Ca(OH)2
9 、 CO 2 可以灭火的原因有三个:不能燃烧、不能支持燃烧、密度比空气大。 10 、当今世界上最重要的三大矿物燃料是:煤、石油、天然气。
棕黄 色(如 FeCl 3 溶液),其余溶液一般为无色。 (高锰酸钾溶液为 紫红 色)
5 、( 1 )具有 刺激性气体 的气体: NH 3(氨气)、 SO 2、 HCl (皆为无色)
( 2 )无色无味的气体: O 2、 H2、 N 2、 CO 2、 CH 4、 CO (剧毒) 、空气、稀有气体
▲ 注意:具有刺激性气味的液体:盐酸、硝酸、醋酸
盐酸( HCl ) : 用于除铁锈,是胃酸的主要成份,浓盐酸有挥发性(挥发出
HCl 气体)
石灰石( CaCO3): 建筑材料,制水泥、高温煅烧制 CaO;
生石灰 CaO: 易与水反应并放热,做食品干燥剂,可用来制取
Ca(OH)2。
熟石灰 Ca(OH)2 : 用于改良酸性土壤,配制波尔多液,与
Na 2 CO 3 反应制取 NaOH
(3) 实验室制取氧气三: 2KClO 3===2KCl+3O2 ↑ ( 4)实验室制法 CO 2: CaCO3+2HCl==CaCl 2+H2 O+CO 2↑ ( 5)实验室制取氢气: Zn+H 2SO4==ZnSO 4+H2↑ ( 6)电解水制取氢气: 2H 2O===2H 2↑+O 2↑ ( 7)湿法炼铜术(铁置换出铜) : Fe+CuSO4==FeSO4+Cu ( 8)炼铁原理: 3CO+Fe2O3===2Fe+3CO 2 ( 9)生灰水 [Ca(OH) 2 ]的制取方法: CaO+H 2O==Ca(OH) 2 ( 10)生石灰 (氧化钙 )制取方法: CaCO3 ===CaO+CO 2↑ 二.金属活动性顺序: 金属活动性由强至弱: K Ca Na Mg Al , Zn Fe Sn Pb (H) ,Cu Hg Ag
常见元素及原子团化合价

+2
碳酸根
CO32-
-2
锌
Zn
+2
硝酸根
NO3-
-1
铜
Cu
+1,+2
氢氧根
OH-
-1
铁
Fe
+2,+3,
铵根
NH4+
+1
铝
Al
+3
磷酸根
PO43-
-3
锰
Mn
+2,+4,+6,+7
氯酸根
CLO-
-1
氢
H
+1碳酸氢根HCO3- Nhomakorabea-1
氟
F
-1
亚硫酸根
SO32-
-2
氯
C1
-1,+1,+5,+7
锰酸根
MnO42-
元素名称
元素符号
常见的化合价
(口诀)
一价氢氯钠钾银,
二价氧钙钡镁锌,
三铝四硅五价磷,
二三铁,二四碳,
二四六硫都齐全,
铜汞二价最常见。
元素名称
元素符号
常见的化合价
钾
K
+1
硅
Si
+4
钠
Na
+1
碳
C
+2,+4
银
Ag
+1
氮
N
-3,+2,+4,+5
钙
Ca
+2
磷
P
-3,+3,+5
镁
Mg
+2
硫酸根
初中化学必须记住的元素符号和化合价

初中化学必须记住的元素符号和化合价
元素符号书写规则:第一个字母大写,第二字母小写。
(字母都是手写体)
一、1-20号元素:(记住汉字和对应符号)(五个一组进行记忆)
氢H 氦He 锂Li 铍Be 硼B 碳C 氮N 氧O 氟F 氖Ne 钠Na 镁Mg 铝Al 硅Si 磷P 硫S 氯Cl 氩Ar 钾
K 钙Ca
二、金属性活动顺序表:(利用前面的谐音按顺序记)
嫁给那美女(钾K、钙Ca、钠Na、镁Mg、铝Al )
锌铁锡铅轻(锌Zn、铁Fe、锡Sn、铅Pb、氢H )
铜共一百斤(铜Cu、汞Hg、银Ag、铂Pt、金Au
三、其记忆的元素符号:(手写体)
钡Ba 锰Mn 碘I 溴Br
四、常见元素、原子团的化合价:
常见元素化合价:
钾钠氢银+1价,钙镁钡锌+2价,
铝+3、硅+4,铁有+2和+3,
铜汞+2最常用,氧硫-2氯-1,
单质元素价为0,正负价和必为0。
常见原子团化合价
-1硝酸、氢氧根, -2硫酸、碳酸根,
-3常见磷酸根, +1价的是铵根。
常见原子团的写法:
NO3 硝酸根 OH 氢氧根
SO4 硫酸根 CO3 碳酸根PO4 磷酸根 NH4 铵根。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
35
Br
80
-1
氢氧根
OH
-1
硝酸根
NO3
-1
高锰酸根
MnO4
-1
氯酸根
ClO3
-1
硫酸根
SO4
-2
碳酸根
CO3
-2
铵根
NH4
+1
初中化学常见的原子团(根)及其化合价
根的名称
根的符号
常见化合价
常见化合物举例
铵根
NH4
+1
NH4Cl
硝酸根
NO3
-1
KNO3
氢氧根
OH
-1
NaOH
高锰酸根
MnO4
-1
KMnO4
32
-2、+4、+6
氯
17
Cl
35.5
-1、+1、+5、+7
氩
18
Ar
40
钾
19
K
39
+1
钙
20
Ca
40
+2
锰
25
Mn
55
+2、+4、+6、+7
铁
26
Fe
56
+2、+3
铜
29
Cu
63.5
+1、+2
锌
30
Zn
65
银
47
Ag
108
钡
56
Ba
137
铂
78
Pt
195
金
79
Au
197
汞
80
Hg
201
碘
53
I
127
磷酸二氢根
H2PO4
-1
Ca(H2PO4)2
(注:文档可能无法思考全面,请浏览后下载,供参考。可复制、编制,期待你的好评与关注)
锰酸根
MnO4
-2
K2MnO4
氯酸根
ClO3
-1
KClO3
醋酸根
CH3COO
-1
CH3COOH
碳酸根
CO3
-2
Na2CO3
碳酸氢根
HCO3
-1
NaHCO3
硫酸根
SO4
-2
CuSO4
硫酸氢根
HSO4
-1
NaHSO4
亚硫酸根
-2
Na2SO3
磷酸根
PO4
-3
H3PO4
磷酸氢根
HPO4
-2
(NH4)2HPO4
元素名称
原子序数
元素符号
相对原子质量
化合价
氢
1
H
1
+1
氦
2
He
4
锂
3
Li
7
铍
4
Be
9
硼
5
B
11
碳
6
C
12
+2+4
氮
7
N
14
-3、+2、+3、+4、+5
氧
8
O
16
-2
氟
9
F
19
-1
氖
10
Ne
20
钠
11
Na
23
+1
镁
12
Mg
24
+2
铝
13
Al
27
+3
硅
14
Si
28
+4
磷
15
P
31
-3、+3、+5
硫
16
S
