初中化学元素化合价
初三化学化合价详细讲解

初三化学化合价详细讲解一、常见元素及原子团的化合价:钾K 钠Na 氢H 银Ag +1价,氟F 氯Cl 溴Br 碘I -1价钙Ca 镁Mg 钡Ba 锌Zn +2价,+1、+2铜Cu,+2、+3铁Fe铝Al+3 硅Si+4 氧O-2常见带电离子团:硫酸根SO42+,硝酸根NO3-,氢氧根OH-,氯酸根ClO3-,碳酸根CO32-铵根NH4+,高锰酸根MnO4- 锰酸根MnO42-,磷酸根PO43-注意:标原子团的化合价时,应标在原子团的上方,如:书写离子符号时,应在原子团右上角标明带电荷数,如硫酸根离子:SO42-一个亚铁离子Fe2+,一个铁离子Fe3+。
二、初中化学物质的检验(一)、气体的检验1、氧气:带火星的木条放入瓶中,若木条复燃,则是氧气.2、氢气:在玻璃尖嘴点燃气体,罩一干冷小烧杯,观察杯壁是否有水滴,往烧杯中倒入澄清的石灰水,若不变浑浊,则是氢气.3、二氧化碳:通入澄清的石灰水,若变浑浊则是二氧化碳.4、氨气:湿润的紫红色石蕊试纸,若试纸变蓝,则是氨气.5、水蒸气:通过无水硫酸铜,若白色固体变蓝,则含水蒸气.(二)、离子的检验.6、氢离子:滴加紫色石蕊试液/加入锌粒7、氢氧根离子:酚酞试液/硫酸铜溶液8、碳酸根离子:稀盐酸和澄清的石灰水9、氯离子:硝酸银溶液和稀硝酸,若产生白色沉淀,则是氯离子10、硫酸根离子:硝酸钡溶液和稀硝酸/先滴加稀盐酸再滴入氯化钡11、铵根离子:氢氧化钠溶液并加热,把湿润的红色石蕊试纸放在试管口12、铜离子:滴加氢氧化钠溶液,若产生蓝色沉淀则是铜离子13、铁离子:滴加氢氧化钠溶液,若产生红褐色沉淀则是铁离子(三)、相关例题14、如何检验NaOH是否变质:滴加稀盐酸,若产生气泡则变质15、检验生石灰中是否含有石灰石:滴加稀盐酸,若产生气泡则含有石灰石16、检验NaOH中是否含有NaCl:先滴加足量稀硝酸,再滴加AgNO3溶液,若产生白色沉淀,则含有NaCl。
元素化合价口诀初中

元素化合价口诀初中好的,以下是为您生成的文章:初中化学里,元素化合价这玩意儿可是个重要的“小怪兽”,想要打败它,咱们得有秘密口诀!话说我当年教过一个叫小明的学生,这孩子聪明是聪明,就是对化合价老是搞混。
有一次化学课上,我刚讲到化合价,他那迷茫的小眼神就告诉我,他又迷糊啦!咱先来说说常见元素的化合价口诀:“钾钠氢银正一价,钙镁钡锌正二价,氟氯溴碘负一价,通常氧是负二价,铜汞一二铝正三,铁有正二和正三。
”就拿钾来说吧,在各种化合物里,钾元素常常就是正一价。
比如氯化钾(KCl),钾就是正一价,氯是负一价。
钠也是一样,氯化钠(NaCl)里钠就是正一价。
氢和银也不例外,像氯化氢(HCl)里氢就是正一价,而银在硝酸银(AgNO₃)中就是正一价。
钙、镁、钡、锌这些家伙,多数时候都是正二价。
比如氧化钙(CaO),这里面钙就是正二价,氧是负二价,正负化合价代数和为零,这样化学式才能平衡嘛。
氟、氯、溴、碘,它们通常是负一价。
像氢氟酸(HF)里氟就是负一价,盐酸(HCl)里氯是负一价。
氧呢,一般是负二价,像水(H₂O),双氧水(H₂O₂),氧都是负二价。
铜和汞有正一价和正二价的时候。
像氧化亚铜(Cu₂O)里铜就是正一价,氧化铜(CuO)里铜就是正二价。
铝通常是正三价,比如氧化铝(Al₂O₃)。
铁就有点调皮啦,有正二价和正三价。
像氯化亚铁(FeCl₂)里铁是正二价,氯化铁(FeCl₃)里铁就是正三价。
小明一开始总是记不住,我就给他举例子,让他多写多练。
后来有一次测验,他居然把化合价相关的题目都做对了,那高兴劲儿,就像发现了新大陆似的。
总之,化合价这东西,多记多练,结合具体的化合物去理解,慢慢就能掌握啦。
可别像刚开始的小明那样,被它给难住哟!相信大家都能把化合价这个“小怪兽”打得落花流水,在化学的世界里畅游无阻!。
化学常见元素化合价

化学常见元素化合价
化学中,元素的化合价是指一个元素在化合物中的电价。
对于常见元素,其化合价是可以预测的,因为它们都遵循着特定的规律。
以下是常见元素的化合价:
1. 氢 (H):+1
2. 氧 (O):-2
3. 氮 (N):-3
4. 碳 (C):-4
5. 硫 (S):-2, +4, +6
6. 氯 (Cl):-1, +1, +3, +5, +7
7. 硼 (B):+3
8. 钠 (Na):+1
9. 铝 (Al):+3
10. 锌 (Zn):+2
11. 铁 (Fe):+2, +3
12. 铜 (Cu):+1, +2
13. 氟 (F):-1
14. 硒 (Se):-2, +4, +6
15. 硅 (Si):+4
需要注意的是,元素的化合价可以有多个值。
比如,硫可以具有 -2、+4、+6 的化合价。
这是因为不同的化合物中,元素的价电
子数不同,因而化合价也会发生变化。
此外,还需要注意的是,在某些情况下,元素的化合价可能会发生变化。
比如,氧化铁中的铁的化合价为 +3,但是在酸性条件下,铁的化合价可以升高到 +6。
这些变化会受到化合物的环境和条件的影响。
总的来说,了解常见元素的化合价对于理解化学反应和化合物的性质非常重要。
初中常见化合价化学式化学方程式
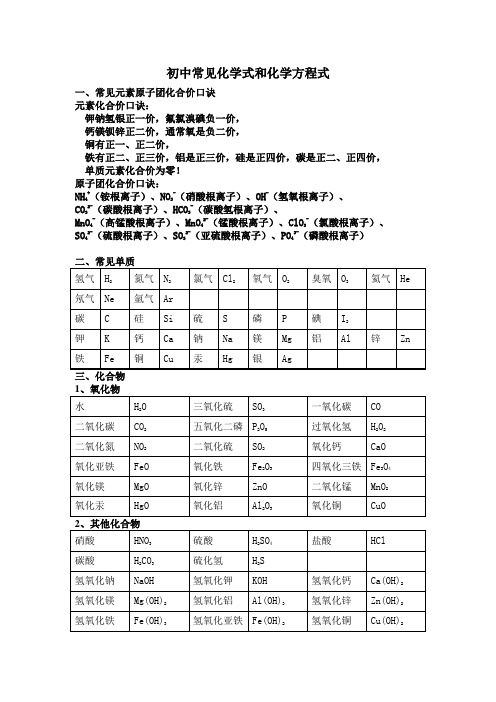
初中常见化学式和化学方程式一、常见元素原子团化合价口诀元素化合价口诀:钾钠氢银正一价,氟氯溴碘负一价,钙镁钡锌正二价,通常氧是负二价,铜有正一、正二价,铁有正二、正三价,铝是正三价,硅是正四价,碳是正二、正四价,单质元素化合价为零!原子团化合价口诀:NH4+(铵根离子)、NO3-(硝酸根离子)、OH-(氢氧根离子)、CO32-(碳酸根离子)、HCO3-(碳酸氢根离子)、MnO4-(高锰酸根离子)、MnO42-(锰酸根离子)、ClO3-(氯酸根离子)、SO42-(硫酸根离子)、SO32-(亚硫酸根离子)、PO43-(磷酸根离子)初中常见的化学方程式一、化合反应1、红磷在空气(或氧气)中燃烧:4P+5O2 2P2O52、氢气在空气中燃烧生成水:2H2+O22H2O3、硫磺在空气(或氧气)中燃烧:S+O2SO24、镁条在空气(或氧气)中燃烧:2Mg+O22MgO5、铁丝在氧气中燃烧:3Fe+2O2Fe3O46、木炭在空气(或氧气)中完全燃烧:C+O2 CO27、木炭不充分燃烧:2C+O22CO8、一氧化碳燃烧:2CO+O2 2CO29、二氧化碳和水反应生成碳酸:CO2+H2O ==H2CO310、二氧化碳通过灼热的炭层:CO2+C 2CO点燃点燃点燃点燃点燃点燃点燃高温点燃11、生石灰作为干燥剂:CaO +H2O == Ca(OH)2二、分解反应11、高锰酸钾制氧气:2KMnO4K2MnO4+MnO2+O2↑12、氯酸钾制氧气:2KClO32KCl+3O2↑13、双氧水制氧气:2H2O22H2O + O2↑14、电解水:2H2O 2H2↑+ O2↑15、碳酸分解:H2CO3H2O+CO2↑16、高温煅烧石灰石(工业制取二氧化碳):CaCO3 CaO +CO2↑三、置换反应17、铜和硝酸银溶液反应:Cu + 2AgNO3 == 2Ag +Cu(NO3)218、铁和硫酸铜溶液反应:Fe + CuSO4 == Cu + FeSO419、锌和硫酸反应制取氢气:Zn + H2SO4== ZnSO4+ H2↑20、铝和稀硫酸反应:2Al + 3H2SO4== Al2(SO4)3+ 3H2↑21、木炭还原氧化铁:3C+2Fe2O34Fe + 3CO2↑木炭还原氧化铜:C+2CuO 2Cu +CO2↑木炭还原四氧化三铁:2C+Fe3O43Fe +2CO2↑氢气还原氧化铜:H2+ CuO Cu + H2O四、复分解反应(一)酸 + 碱→盐 + 水22、氢氧化钠与盐酸反应:NaOH + HCl == NaCl + H2O23、氢氧化钠与硫酸反应:2NaOH + H2SO4== Na2SO4+ 2H2O24、氢氧化铝治疗胃酸过多:Al(OH)3 + 3HCl == AlCl3+ 3H2O25、氢氧化镁与硫酸反应:Mg(OH)2 + H2SO4== MgSO4+ 2H2O(二)酸 + 盐→新酸 + 新盐26、盐酸与硝酸银溶液反应:HCl+AgNO3== AgCl↓+HNO3△MnO2△MnO2通电高温高温高温高温高温27、氯化钡溶液与硫酸溶液反应:BaCl2 +H2SO4== BaSO4↓+ 2HCl28、碳酸钠与稀盐酸:Na2CO3+2HCl == 2NaCl+H2O+CO2↑碳酸氢钠与稀盐酸:NaHCO3+HCl == NaCl+H2O+CO2↑29、石灰石与稀盐酸反应(实验室)制取二氧化碳:CaCO3+2HCl =CaCl2+H2O+CO2↑(三)碱 + 盐→另一种碱 + 另一种盐30、硫酸铜溶液和氢氧化钠溶液反应:CuSO4+2NaOH = Na2SO4+Cu(OH)2↓31、氯化铁溶液和氢氧化钠溶液反应:FeCl3+3NaOH==Fe(OH)3↓+3NaCl(四)盐 + 盐→两种新盐32、硝酸银溶液与氯化钠溶液反应:AgNO3 + NaCl == AgCl↓+ NaNO333、氯化钡溶液与碳酸钠溶液反应:BaCl2+ Na2CO3= BaCO3↓+ 2NaCl(五)金属氧化物 + 酸→盐 + 水34、稀盐酸清洗铁锈:6HCl+Fe2O3== 2FeCl3+3H2O35、氧化铜与稀硫酸反应:CuO+H2SO4== CuSO4+H2O五、非金属氧化物 + 碱→盐 + 水36、二氧化碳通入澄清石灰水中:CO2+Ca(OH)2== CaCO3↓+H2O37、氢氧化钠在空气中变质:CO2+2NaOH=Na2CO3+H2O38、氢氧化钠溶液吸收二氧化硫:SO2+2NaOH==Na2SO3+H2O39、氢氧化钠溶液吸收三氧化硫:SO3 +2NaOH==Na2SO4+H2O六、其他反应类型40、一氧化碳还原氧化铜:CO + CuO Cu + CO241、一氧化碳还原氧化铁:3CO+ Fe2O32Fe + 3CO2↑42、一氧化碳还原四氧化三铁:4CO+ Fe3O43Fe + 4CO2↑43、酒精燃烧:C2H5OH + 3O22CO2+ 3H2O44、甲烷燃烧:CH4 + 2O2CO2+ 2H2O△点燃点燃高温高温。
初中化学化合价概念详细图文解析

初中化学化合价概念详细图文解析【导言】化学是一门研究物质变化性质及其应用的学科,而化合价则是化学中一个基本概念。
本文将详细解析初中化学中化合价的概念,并通过图文结合的方式进行解析,帮助读者更好地理解和掌握化合价的知识。
【概念解析】化合价,又称原子价、价值、电价等,是指元素在化合物中正负电荷的表现形式。
化合价的概念来源于化学反应中的化学键。
在化学式中,原子通过原子上的电子迁移或共用来构成化学键。
化合价的数值表示原子在化合物中所带的电荷数。
【基本规则】化合价的计算遵循以下基本规则:1. 单负离子的化合价等于离子的所带电荷数。
2. 单正离子的化合价等于离子所带电荷数的相反数。
3. 自由原子的化合价为0。
4. 非金属元素的化合价通常是正的,而金属元素的化合价通常是负的。
5. 氧元素通常化合价为-2,氢元素通常化合价为+1。
6. 非氧族元素的化合价通常不超过其周期数减去8。
7. 阳离子和阴离子的化合价绝对值之和相等。
【图文解析】图一:化合价的计算规则(插入一张图表,图表中包含了化合价的计算规则,可以通过示例原子和离子的化合价计算来帮助读者理解)图二:常见离子的化合价(插入一张图表,图中列出了常见元素的离子以及离子的化合价,例如Na+、Cl-、Mg2+等,以帮助读者记忆常见离子的化合价)图三:氧族元素的化合价(插入一张图表,图中给出了氧族元素的周期表,标注了氧族元素的化合价,例如O、S、Se、Te等,以帮助读者理解氧族元素的化合价规律)图片说明:1. 图一中的计算规则示例:以氢氧化钠(NaOH)为例,Na的化合价为+1,O的化合价为-2,根据化合价绝对值之和相等的规则,可推算出Na的化合价为+1。
2. 图二中的常见离子示例:Na+的化合价为+1,Cl-的化合价为-1,Mg2+的化合价为+2,通过图表可以直接查找常见离子的化合价。
3. 图三中的氧族元素示例:O的化合价为-2,S的化合价为-2或+6,Se的化合价为-2或+6,Te的化合价为-2或+6,通过图表可以了解氧族元素的化合价规律。
元素化合价口诀初中顺口溜

元素化合价口诀初中顺口溜
初中化学中,元素化合价的记忆可以通过以下顺口溜来帮助:
1.一价钾钠银氢正一价,钡锌钙镁正二价,一二铜,二三铁,亚铜
亚铁是低价,铝是正三氧负二,氯是负一最常见,硫有负二正四六,正二正三铁可变,二三铁,二四碳,单质零价永不变。
2.负一硝酸氢氧根,负二硫酸碳酸根,负三记住磷酸根,正一价的
是铵根。
3.氟氯溴碘负一价;正一氢银与钾钠。
氧的负二先记清;正二镁钙
钡和锌。
正三是铝正四硅;下面再把变价归。
全部金属是正价;
一二铜来二三铁。
锰正二四与六七;碳的二四要牢记。
非金属负主正不齐;氯的负一正一五七。
氮磷负三与正五;不同磷三氮二四。
硫有负二正四六;边记边用就会熟。
初中化学化合价口诀

初中化学化合价口诀[初中化学化合价口诀]初中化学口诀1、常见元素的化合价:一价钾钠氯氢银,二价钙钡镁锌,三铝四硅五价磷;二三铁,二四碳;二四六硫都齐全,铜汞二价最常见。
2、实验室制取氧气的步骤:“茶(查)、庄(装)、定、点、收、利(离)、息(熄)”“查”检查装置的气密性“装”盛装药品,连好装置“定”试管固定在铁架台“点”点燃酒精灯进行加热“收”收集气体“离”导管移离水面“熄”熄灭酒精灯,停止加热。
3、用CO还原氧化铜的实验步骤:“一通、二点、三灭、四停、五处理”“一通”先通氢气,“二点”后点燃酒精灯进行加热;“三灭”实验完毕后,先熄灭酒精灯,“四停”等到室温时再停止通氢气;“五处理”处理尾气,防止CO污染环境。
4、电解水的实验现象:“氧正氢负,氧一氢二”:正极放出氧气,负极放出氢气;氧气与氢气的体积比为1:2。
6、组成地壳的元素:养闺女(氧、硅、铝)7、原子最外层与离子及化合价形成的关系:“失阳正,得阴负,值不变”:原子最外层失电子后形成阳离子,元素的化合价为正价;原子最外层得电子后形成阴离子,元素的化合价为负价;得或失电子数=电荷数=化合价数值。
8.化学实验基本操作口诀:固体需匙或纸槽,一送二竖三弹弹;块固还是镊子好,一横二放三慢竖液体应盛细口瓶,手贴标签再倾倒;读数要与切面平,仰视偏低俯视高滴管滴加捏胶头,垂直悬空不玷污;不平不倒不乱放,用完清洗莫忘记托盘天平须放平,游码旋螺针对中;左放物来右放码,镊子夹大后夹小试纸测液先剪小,玻棒沾液测最好;试纸测气先湿润,粘在棒上向气靠酒灯加热用外焰,三分之二为界限;硫酸入水搅不停,慢慢注入防沸溅实验先查气密性,隔网加热杯和瓶;排水集气完毕后,先撤导管后移灯9、金属活动性顺序:金属活动性顺序由强至弱:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au (按顺序背诵)钾钙钠镁铝锌铁锡铅(氢)铜汞银铂金10、“十字交叉法”写化学式的口诀:“正价左负价右,十字交叉约简定个数,写右下验对错”11、过滤操作口诀:斗架烧杯玻璃棒,滤纸漏斗角一样;过滤之前要静置,三靠二低莫忘记。
初中化学元素化合价完整版

一、常见元素化合价
元素名称
元素符号
常见化合价
元素名称
元素符号
常见化合价
钾
K
+1
氢
H
+1
钠
Na
+1
氯
Cl
-1+5+7
银
Ag
+1
溴
Br
-1
钙
Ca
+2
碘
I
-1
镁
Mg
+2
氧
O
-2
硫
S
-2+4+6
钡
Ba
+2
碳
C
+2+4
锌
Zn
+2
硅
Si
+4
铜
Cu
+2-1
氮
N
-3+2+4+5
铝
Al
+3
磷
P
+5
铁
溶
不
Fe2+
不
溶
溶
溶
不
Fe3+
不
溶
溶
溶
—
Cu2+
不
溶
溶
溶
不
Ag+
—
溶
不
微
不
Fe
+2+3
二、常见原子团化合价原子团
名称原子团
名称
原子团
符号
原子团
化合价
原子团
名称原子团Fra bibliotek符号原子团
化合价
氢氧根
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
溶
溶
溶
不
Zn2+
不
溶
溶
溶
不
Fe2+
不
溶
溶
溶
不
Fe3+
不
溶
溶
溶
—
Cu2+
不
溶
溶
溶
不
Ag+
—
溶
不
微
不
MnO4
-2
高锰酸根
MnO4
-1
磷酸根
PO4
-3
磷酸氢根
HPO4
-2
磷酸二氢根
H2PO4
-1
溶解度表
OH-
NO3-
Cl-
SO42-
CO32-?
H+
溶,挥
溶,挥
溶
溶,挥
NH4+
溶,挥
溶
溶
溶
溶
K+
溶
溶
溶
溶
溶
Na+
溶
溶
溶
溶
溶
Ba2+
溶
溶
溶
不
不
Ca2+
微
溶
溶
微
不
Mg2+
不
溶
溶
溶
微
Al3+??
不
溶
溶
溶
—
Mn2+
Al
+3
磷
P
+5
铁
Fe
+2 +3
二、常见原子团化合价原子团
名称原子团
名称
原子团
符号
原子团
化合价
原子团
名称
原子团
符号
原子团
化合价
氢氧根
OH
-1
碳酸氢根
HCO3
-1
硫酸根
SO4
-2
磷酸根
PO4
-3
碳酸根
CO3
-2
亚硫酸根
SO3
-2
硝酸根
NO3
-1
铵根
NH4
+1
醋酸根
CH3COO
-1
氯酸根
ClO3
-1
锰酸根
初中化学元素化合价
一、常见元素化合价
元素名称
元素符号
常见化合价
元素名称
元素符号
常见化合价
钾
K
+1
氢
H
+1钠Na源自+1氯Cl
-1 +5 +7
银
Ag
+1
溴
Br
-1
钙
Ca
+2
碘
I
-1
镁
Mg
+2
氧
O
-2
硫
S
-2 +4 +6
钡
Ba
+2
碳
C
+2 +4
锌
Zn
+2
硅
Si
+4
铜
Cu
+2 -1
氮
N
-3 +2 +4 +5
铝
