超声多普勒胎儿心率仪产品技术要求深圳市莱佳医疗
超声多普勒胎儿心率仪产品技术要求huirenyangguang

超声多普勒胎儿心率仪适用范围:该产品供妊娠15周以上孕妇对胎儿心率在家进行自我测量。
1.1 产品型号:DPI100B。
1.2 产品型号划分说明1.3 组成:由主机和探头组成。
2.1 正常工作条件2.1.1 环境条件a)环境温度:10℃~30℃;b)相对湿度:≤80%;c)大气压力:700hPa~1060hPa。
2.1.2 电源条件:充电锂电池DC3.7V。
2.2 声工作频率:3.0MHz±15%。
2.3 综合灵敏度:在距探头200mm距离处,综合灵敏度应不小于90dB。
2.4 超声输出功率:不大于10mW。
2.5 空间峰值时间峰值声压:≤0.5MPa。
2.6 胎心率a)测量和显示范围:100次/min~180次/min。
b)测量误差:不大于±2次/min。
2.7 声输出参数公布要求:应符合GB9706.9-2008的规定。
2.8 超声换能器敏感元件的有效面积:50mm2±20%。
2.9 电源电压适应能力:电压下降至额定值3.7V的85%后,仪器应能正常工作。
2.10 连续工作时间:仪器在常温下,应能连续工作2h以上。
2.11 功能:a)具有胎心率及心率曲线显示功能;b)具有播放韵率音乐功能。
2.12 安全应符合GB 9706.1-2007《医用电气设各第1部分:安全通用要求》、GB 9706.9-2008的规定《医用电气设备第2-37部分:超声诊断和监护设备专用安全要求》。
产品电气安全特征及产品电气绝缘图见附录A。
2.13 环境试验环境试验要求应按GB/T 14710-2009《医用电器环境要求及试验方法》中气候环境试验Ⅱ组,机械环境试验Ⅱ组及表1的规定,表1见附录B。
2.14 外观和结构胎心仪的外观应整洁,色泽均匀,无伤痕、划痕、裂纹等缺陷。
控制和调节机构应安装正确、灵活、牢固、可靠,紧固部位应无松动。
超声多普勒胎儿心率仪产品技术要求kangbochuangxiang

超声多普勒胎儿心率仪适用范围:适用家庭和医疗单位从孕妇腹部检测胎儿心率信息1.1型号命名1.2产品组成DFMX超声多普勒胎儿心率仪是由医用超声多普勒胎儿心率仪主机、耳机、USB 充电线组成。
2.1 正常工作条件•温度:15℃~35℃;•相对湿度:30%~90%;•大气压力:70kPa~106 kPa;•电源电压:锂电池3.7V,USB供电 DC5V。
2.2 外观和结构要求2.2.1 外表应色泽均匀、表面整洁,无划痕、裂缝等缺陷。
2.2.2 面板上符号和标志应清晰易认、持久。
2.2.3 控制和调节机构应灵活、可靠,紧固部位无松动。
2.3 性能要求2.3.1 声工作频率声工作频率与标称额定声工作频率2.0MHz的偏差应不大于±15%。
2.3.2 胎心率的测量范围胎心率的测量范围不少于(65~210)次/min。
2.3.3 胎心率测量的误差胎心率测量的误差不大于±2次/min。
2.3.4综合灵敏度在距探头表面200mm距离处,综合灵敏度应不小于90dB。
2.3.5空间峰值时间峰值声压空间峰值时间峰值声压应不大于0.2MPa。
2.3.6 输出超声功率输出超声功率应不大于10mW。
2.3.7超声换能器敏感元件的有效面积超声换能器敏感元件的有效面积<2.0cm22.3.8 电源电压适应能力采用电池供电的仪器,在电压下降至额定值的85%时,仪器应能正常工作。
2.3.9 连续工作时间连续工作时间应在产品说明书中予以公布。
2.4 电气安全应符合GB 9706.1-2007、GB 9706.9-2008中的要求。
产品电气安全基本特征见附录A。
2.5 电磁兼容性要求应符合YY 0505-2012的要求。
2.6 环境试验要求应符合GB/T 14710-2009中气候环境试验II组和机械环境试验II组及附录B的要求。
超声多普勒胎儿监护仪技术参数要求

超声多普勒胎儿监护仪技术参数要求整机:1、隐藏式提手,方便移动;2、一体化探头架设计,支持挂墙放置探头、移动放置探头,方便医生出诊;3、机顶报警灯柱,人性化报警设置:三级声光报警,范围、声音大小可调,报警信息按病人生理报警和监护仪技术报警分类,并分区域以黄色字体显示报警信息,胎心率报警可调整报警延迟;4、回顾报警功能,可回顾最近的100条报警信息;5、模块化结构,方便升级;6、内置通讯接口,可与中央站组成网络系统;7、监护参数:胎心率,宫缩压力,胎动,胎儿活动曲线;8、12小时CTG存储、回放,打印,掉电数据存储;9、具有查找监护记录功能;10、双胎心率重合报警(SOV);11、良好的音腔设计,声音洪亮柔和;12、通过欧盟CE认证。
★13、通过SFDA和美国FDA注册。
显示:★14、5.6英寸高清晰液晶黑白屏,90度角度内任意翻转。
15、良好的人机对话界面,多种界面可选。
按键加飞梭操作,操作更简便;16、胎心率120-160bpm正常范围区域标识;17、可同步显示和打印胎儿活动图曲线;18、多种监护界面,显示胎儿监护曲线及数字;探头:19、全新探头外观设计,更符合人机工程学原理;★20、新式探头防水设计,方便医院开展水中分娩等项目;★21、无凸点宫缩压力探头设计,监护中孕妇更感舒适。
胎儿监护指标:★22、胎心:多晶片1MHz宽波束脉冲多普勒防水探头,自适应追踪,胎心信号捕捉稳定超声工作频率:1MHz 超声波束声强:<10 mW/cm2心率范围:30~240bpm 分辨率: 1bpm23、宫缩压力:0-100相对单位24、胎动:手动/自动胎动检测,显示并打印胎儿活动图;打印:★25、内置式152mm宽行打印,符合国际标准,连续准确记录胎心率、宫缩压曲线及胎儿活动曲线;26、打印机走纸速度1、2、3cm/min可调,支持最高速度15mm/s高速回放打印;27、支持缺纸缓存打印,选段打印和定时打印功能,定时时长范围:10-90min。
胎儿监护技术参数

胎儿监护技术参数一基本性能要求:1、工作方式:连续波超声多普勒。
★2、显示方式:高亮度真彩液晶(TFT)显示,显示屏≥7″可90度翻屏。
★3、探头工作频率:1MHz。
★4、探头晶片种类: 7晶片、9晶片、13晶片可选。
5、探头输出波束声强:<3mW/c㎡。
6、事件标记功能:≥9种。
7、数据存储:可连续保存24小时监护曲线和数据,并可以查找和回放。
8、打印机:点阵热敏打印机,分辨率不≥600*400,打印宽度≥112MM。
9、电源种类:高性能锂离子电池,,监护状态下连续工作不少于3小时。
10、电源管理功能:掉电保护功能,交直流两用。
11、仪器安全主动防护:掉电数据保护功能。
二详细参数:测量方法:超声多普勒测量范围:30~210BPM测量误差:不超过±1BPM胎心率曲线范围:30~210BPM胎心率数码显示范围:30~210BPM超声工作频率:1.0MHz±1%超声输出强度:1 mW/cm2宫缩压力测量测量方法:外测法测量范围:0~100PA宫缩压力曲线范围:0~100单位宫缩压力数码显示范围:0~100单位非线性误差:不超过±10%调零功能:有胎动记录:手控按钮标记,自动胎动识别功能显示屏:7'color TFT-LCD超声探头频率种类: 1MHZ超声探头宽波束种类: 7晶片,9晶片,12晶片可选★事件标记:9种可选记录方式:热敏点阵打印系统记录纸:112mm×100mm折叠热敏打印纸走纸速度:1、2、3cm/min三档可调胎心率声光报警:下限120BPM,上限160BPM报警触发时间<3s多种报警功能,能及时提供诊疗诊疗警示支持,包括:胎动过速、过缓报警,监护时间到提示,打印机缺纸报警等。
声音输出:2~3W喇叭输出音量可调电源:正常连续工作>3h组网功能:有可选配双胞胎及胎儿评分功能两煎煎药机参数及配置一、产品参数:1、煎药锅容量20L/个×3个2、包装能力5~8袋/min3、袋装容量50~250ml4、包装数量设定范围0~250袋循环5、总功率4450W6、额定电压220V7、外形尺寸:长1300mm×宽580mm×高1250mm二、功能要求:★1、产品必须是国家中医药管理局推荐机型,且具有二煎功能;★2、煎药包装一体设计,两次煎药一次包装,并设有储存药液的装置;★3、包装成袋容量50~250ml自由设定,分别设有定量包装和均分包装;4、产品能够自动计量上水,误差小于3%;5、采用优质进口流量传感器,管路具有减压装置、安全可靠;6、产品外壳全部采用优质不锈钢,经久耐用,易于清洗;★7、产品具有故障自检系统,故障时自动停机并用相应符号显示;双级水处理系统技术参数一、主要参数:1、产水水质:符合YY0572-2005及美国AAMI/ASAIO透析用水标准2、二级产水量:≥2000L/H(20℃水温)3、离子去除率:≥99%4、细菌、内毒素清除率≥99.5%5、系统回收率≥50-70%二、主要性能特点:★1、主要工艺:双级反渗透,一二级直接耦合,全流程无水储存。
彩色多普勒超声诊断仪技术参数及要求重点参数请用“”标注;参数无指向性

彩色多普勒超声诊断仪技术参数及要求(重点参数请用“*”标注;参数无指向性)一、功能要求需配置阴超探头;需弹性成像。
二、参数要求
1、高分辨率液晶显示器223英寸,操作面板具备液晶触摸屏215英寸。
2、探头接口25个,全激活、相互通用。
3、自动血流跟踪技术,一键实时自动优化CoIOr/Power及PW频谱图像、CoIor/Power框的位置和角度、PW取样门的位置、角度和大小等。
4、自动工作流,检查过程中可按照协议自动注释,自动标记体位图,自动切换图像模式等。
5、自动化盆底解决方案,可对肛提肌裂孔进行全自动描迹和自动测量。
6、心功能自动测量软件。
7、硬盘:21T硬盘,SSD固态硬盘2128G。
8、复合成像。
9、台式机、可录像、内存大。
科室负责人签字:
主管处室负责人签字:
日期:。
彩色心脏多普勒超声诊断仪主要技术要求和规格

彩色心脏多普勒超声诊断仪主要技术要求和规格一.设备名称及用途:高档心脏彩色多普勒超声诊断仪1台用于成人心脏,胎儿、新生儿及小儿心脏;血管(外周、脑血管);腹部、浅表等超声诊断和相关科研。
二.交货日期:合同签订后90天三.投标时要求提供原厂家的技术白皮书,评标以此为准四.具有“中华人民共和国医疗器械注册证”,提供有效期内医疗器械注册证或医疗器械备案表五.主要技术规格及系统概述:1.主机系统性能概括1.1显示器及操作系统*1.1.1医学专用彩色液晶监视器,≥21英寸,自由臂可调节360°*1.1.2主机具备彩色触摸屏,≥10.4英寸,合理功能分区,可滑屏操作,可同屏显示检查图像。
1.1.3功能分区控制面板,可升降、旋转、前后左右平移,电子锁定1.1.4中文操作平台*1.1.5通用成像探头接口≥4个,无针式接口,并可互通互用。
1.2主机系统1.2.1全数字化多波束形成器*1.2.2数字化通道数≥7,000,000*1.2.3动态范围≥320dB1.2.4系统主机CPU36核,1TB硬盘,4GB独立显存1.2.5全新精准波束形成技术和海量并行处理,依次接收原始声学数据,系统进行实时逐像素聚焦。
1.3二维灰阶成像(部件)单元*1.3.1纯净波单晶体探头技术,用于经胸心脏探头、腹部凸阵探头、经胸矩阵探头、经食道矩阵探头1.3.2具备自适应像素优化技术,可增强组织边界,抑制斑点噪声,可用于多种模式(2D、3D),多级可调(≥5级)1.3.3空间复合成像技术,同时作用于发射和接收,最大偏转角度≥9,可与宽景成像、造影联用,支持所有凸阵、微凸阵和线阵成像探头1.3.4凸阵、线阵探头具备扩展成像技术,可联合空间复合成像,扩展角度≥15度。
1.3.5一键优化TGC曲线,可实时优化二维增益、对比度、动态范围1.3.6单键持续增益补偿1.3.7LGC侧向增益补偿技术,可视可调1.3.8具备对比双幅显示,可自动识别收缩期及舒张期1.4频谱多普勒显示及分析系统1.4.1自适应多普勒技术1.4.2提供PW、CW、HRPW模式,高性能三同步成像1.4.3实时自动多普勒测量分析,可提供参数选择≥15个参数1.4.4一键自动优化多普勒频谱,自动调整基线及量程1.4.5频谱取样门自动追踪技术,实时追踪血管位置,调整取样门位置1.4.6智能多普勒优化技术,实时智能调整取样容积位置、角度校正和偏转角度1.5彩色血流成像(部件)单元1.5.1自适应超宽频带彩色多普勒成像技术1.5.2彩色能量图及方向能量图1.5.3单键调节血流成像参数1.5.4彩色对比及实时对比显像1.5.5智能多普勒优化技术,实时智能调整取样框位置和偏转角度1.6组织多普勒成像1.6.1高帧频彩色和脉冲波组织多普勒成像1.6.2二维、彩色M型、速度曲线同屏显示1.6.3专业TDI测量软件包*1.6.4可进行心肌应变及应变率定量分析1.6.5动态组织追踪取样1.7.负荷超声成像1.7.1具备二维及三维负荷超声1.7.2可提供负荷超声斑点追踪定量分析1.8超宽视野成像扫描技术(测量功能,线阵和凸阵探头具备),可与空间复合成像技术及像素优化技术结合使用。
超声多普勒胎儿心率仪产品注册技术审查指导原则

超声多普勒胎儿心率仪产品注册技术审查指导原那么本指导原那么旨在标准超声多普勒胎儿心率仪产品的技术审评工作,同时指导审评人员增进对该类产品原理、构造、主要性能、预期用途等方面的理解,把握技术审评工作的根本要求和尺度,以便对产品平安性、有效性作出系统评价。
本指导原那么也用于指导企业产品生产以及产品注册申报工作。
本指导原那么是对超声多普勒胎儿心率仪的一般技术要求,申请人/生产企业应依据具体产品的特性对注册申报材料的容进展充实和细化。
本指导原那么是对超声多普勒胎儿心率仪的技术审查人员和申请人/生产企业的指导性文件,但不包括注册审批所涉及的行政事项,亦不作为法规强制执行。
本指导原那么是在现行法规和标准体系以及当前认知水平下制订的,随着法规和标准的不断完善,以及科学技术的不断开展,本指导原那么相关容也将进展适时的调整和更新。
一、适用围本指导原那么适用于根据超声多普勒原理从孕妇腹部获取胎儿心脏运动信息的超声多普勒胎儿心率检测仪器。
根据?医疗器械分类目录?类代号为6823-2。
本指导原那么不适用于系附在孕妇腹部,采用多元扁平超声多普勒换能器的连续胎儿心率监护装置。
本指导原那么所涉及的超声多普勒胎儿心率仪只用于短时间检测。
如果本超声多普勒胎儿心率仪作为一个系统中的一局部,本指导原那么也适用于该局部。
本指导原那么所涉及的超声多普勒胎儿心率仪,其定义采用YY O448-2009?超声多普勒胎儿心率仪?所规定的围。
由于新技术的不断更新,实际技术可能与本指导原那么所介绍的容存在一定差异,类似的建议参考本指导原那么中适用的局部。
二、技术审查要点(一)产品名称的要求产品名称应以发布的国家标准、行业标准以及?医疗器械产品分类目录?中的产品名称为依据。
产品名称应以表达产品的工作原理、技术构造特征、功能属性为根本准那么。
如“超声多普勒胎儿心率仪〞、“超声多普勒胎心音仪〞等。
(二)产品的构造和组成产品一般至少由探头〔一般采用单元探头〕、超声波发射/接收电路、信号输出局部组成。
15超声多普勒胎儿监护仪产品注册技术审查指导原则

15超声多普勒胎儿监护仪产品注册技术审查指导原则超声多普勒胎儿监护仪是一种用于对孕妇和胎儿进行监护的医疗设备。
为了确保该产品的质量和安全性,需要在生产和销售前进行产品注册,并进行技术审查。
下面是15超声多普勒胎儿监护仪产品注册技术审查指导原则的详细说明。
1.技术评价:评估产品的设计和工艺,确保其满足国家和国际标准的要求。
包括电子部件、传感器、软件等方面的技术评估。
2.安全性评价:对产品的使用安全性进行评估,包括电气安全、辐射安全、机械安全等方面。
确保产品在使用过程中不会对孕妇和胎儿造成伤害。
3.效能评价:评估产品的监护功能和性能,包括胎心率检测的准确性、分析算法的可靠性等方面。
确保产品能够提供准确的监护结果。
4.软件验证和验证:对产品软件进行验证和验证,确保其功能和性能符合要求。
包括输入和输出数据的验证、算法的验证等方面。
5.标识和说明书评价:评估产品的标识和说明书,确保其清晰、准确、易懂。
包括产品名称、规格、使用方法、预防措施等方面的评估。
6.设备质量管理:评估产品的质量管理体系,确保产品在整个生产过程中都能够符合要求。
包括原材料采购、生产工艺、质量控制等方面的评估。
7.生物相容性评价:评估产品与人体组织之间的相容性,确保产品不会引起过敏反应或其他不良反应。
8.改装和维修评价:评估产品是否容易改装和维修,以及改装和维修是否会影响产品的性能和安全性。
9.临床试验:进行相关的临床试验,验证产品在实际使用中的安全性和有效性。
10.标准符合性评估:评估产品是否符合相关国家和国际的标准要求。
11.环境适应性评估:评估产品在不同环境条件下的适应性,确保产品能够在各种环境条件下正常工作。
12.风险管理评估:评估产品的风险管理措施,确保产品在使用过程中能够控制风险。
13.制造和检验程序评估:评估产品的制造和检验流程,确保产品在生产过程中符合要求,检验流程能够准确检测产品的性能。
14.设备操作和维护培训评估:评估产品供应商提供的设备操作和维护培训,确保用户能够正确操作和维护产品。
超声多普勒胎儿监护仪产品注册技术审查指导原则

编写说明
一、指导原则编写的目的 本指导原则用于指导和规范超声多普勒胎儿监护仪在注册申报过程中审评人员对注册材料的技术审评。 超声多普勒胎儿监护仪是借助超声能量作用对患者(孕妇)予以监测,其临床适用较为广泛。本指导原则旨 在让初次接触该类产品的注册审评人员对产品的原理、结构、主要性能、预期用途等各个方面有一个基本的了解, 同时让技术审评人员在产品注册技术审评时把握基本的尺度,以确保产品的安全、有效。 二、指导原则编写的依据 (一)《医疗器械监督管理条例》 (二)《医疗器械注册管理办法》(16号令) (三)《医疗器械临床试验规定》(5号令) (四)《医疗器械说明书、标签和包装标识管理规定》(10号令) (五)《医疗器械标准管理办法》(31号令) (六)关于印发《境内第一类医疗器械注册审批操作规范(试行)》和《境内第二类医疗器械注册审批操作 规
谢谢观看
超声多普勒胎儿监护仪产品注册技术 审查指导原则
医疗产品技术审查指导原则
01 适用范围
03 审查点
目录
02 审查要点 04 编写说明
《超声多普勒胎儿监护仪产品注册技术审查指导原则》,是医疗产品技术审查分类目录》中6823-3中“超声母婴监护设备”中的超声多普勒胎儿监护仪。如 果超声多普勒胎儿监护仪作为一个系统中的一部分,则本指导原则也适用于该部分。
审查要点
(一)产品名称的要求 产品名称应以发布的国家标准、行业标准以及《医疗器械产品分类目录》中的产品名称为依据。产品名称应 以体现产品的工作原理、技术结构特征、功能属性为基本准则。如“超声胎儿监护仪”,“超声母亲/胎儿综合监 护仪”等,不宜采用病症命名。 (二)产品的结构和组成 一般由主机、超声探头、宫缩压力传感器及与之相连接的仪器组成。一般的结构示意框图如下: 图1产品结构示意框图 对超声多普勒胎儿监护仪及其部件进行全面评价所需的基本信息应包含但不限于以下内容: 1.产品设计和说明 应包括对产品工作原理的概述,该部分内容应当包括: 1.1产品构成说明 1.1.1整机总体构造的详细描述,应包括所有组成部分,应给出有标记的图示(如图表、照片和图纸等), 清
国家药品监督管理局关于发布《超声多普勒胎儿心率仪》等5项医疗器械行业标准的通知

国家药品监督管理局关于发布《超声多普勒胎儿心率仪》等5项医疗器械行业标准的通知
文章属性
•【制定机关】国家药品监督管理局
•【公布日期】2003.02.09
•【文号】国药监械[2003]52号
•【施行日期】2003.09.01
•【效力等级】部门规范性文件
•【时效性】已被修改
•【主题分类】药政管理
正文
*注:本篇法规的YY 0451-2003《一次性使用输注泵》中部分内容已被《国家食品药品监督管理局关于印发YY0451-2003<一次性使用输注泵>等两项行业标准第1号修改单的通知》(发布日期:2006年4月19日实施日期:2006年4月19日)修改
国家药品监督管理局关于发布
《超声多普勒胎儿心率仪》等5项医疗器械行业标准的
通知
(国药监械[2003]52号)
各省、自治区、直辖市药品监督管理局,各医疗器械标准化技术归口单位:《超声多普勒胎儿心率仪》等5项医疗器械行业标准已审定通过,现予发布。
各项行业标准的编号、名称及实施日期如下:
1.YY 0448-2003 《超声多普勒胎儿心率仪》
2.YY 0449-2003 《超声多普勒胎儿监护仪》
3.YY 0450.1-2003 《一次性使用无菌血管内导管辅件第1部分:导引器
械》
4.YY 0450.2-2003 《一次性使用无菌血管内导管辅件第2部分:套针外周导管管塞》
5.YY 0451-2003 《一次性使用输注泵》
以上标准自2003年9月1日起实施。
国家药品监督管理局
二00三年二月九日。
超声多普勒胎儿心率监护仪产品技术要求

2. 性能指标2.1性能2.1.1胎儿心率测量范围及误差胎心率测量和显示范围:50~210bpm。
胎心率测量准确度:误差±2bpm或±2%(两者取大值)2.1.2超声工作频率超声工作频率fw为2.5MHz,与标称频率的误差不大于±15%。
2.1.3综合灵敏度距探头表面距离200mm的综合灵敏度 S(dB):≥ 90dB。
2.1.4空间峰值时间峰值声压空间峰值时间峰值声压P(MPa):< 1 MPa。
2.1.5超声换能器敏感元件的有效面积超声换能器敏感元件的有效面积:127mm2±10%。
2.1.6输出超声功率输出超声功率应小于20mW。
2.1.7连续工作时间电池充满电,仪器能正常连续工作3小时。
2.1.8胎心仪功能2.1.8.1支持实时胎心率显示屏幕应可显示实时胎心率值:50~210bpm。
2.1.8.2 支持胎心音量调节功能应支持胎心音量增加、音量减小功能。
仪器扬声器具有0、1、2、3、4、5共6档声音调节功能,2.2电气安全要求应符合GB 9706.1-2007《医用电气设备第1部分:安全通用要求》、GB 9706.9-2008《医用电气设备第2-37部分:超声诊断和监护设备安全专用要求》的要求。
2.3声输出公布的要求声输出参数应满足GB/T 16846-2008《医用超声诊断设备声输出公布要求》的规定测试,结果满足免予公布的要求。
2.4电磁兼容要求应符合YY0505-2012《医用电气设备第1-2部分:安全通用要求并列标准:电磁兼容要求和试验》的要求。
2.5电源电压适应能力采用电池供电,在电压下降至额定值的85%时,仪器应能正常工作。
2.6外观与结构2.6.1外观胎心仪的外壳应无机械损伤、锈蚀、毛刺、锋棱和明显凹凸;其塑料件应无起泡、开裂、变形及灌注物溢出现象。
2.6.2文字和标志胎心仪上的文字和标志应清晰、准确、牢固。
2.6.3控制和调节机构应灵活、可靠,紧固部位无松动。
超声多普勒胎儿心率仪

超声多普勒胎儿心率仪1 范围本标准规定了超声多普勒胎儿心率仪(也称“胎心音仪”、“胎儿听诊器”)的术语和定义、要求和试验方法。
本标准适用于根据超声多普勒原理从孕妇腹部获取胎儿心脏运动信息的超声多普勒胎儿心率仪(以下简称“仪器”)。
本标准不适用于系附在孕妇腹部,采用多元扁平超声多普勒换能器的连续胎儿心率监护装置。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB 9706.1 医用电气设备第1部分:安全通用要求GB 9706.9 医用电气设备第2-37部分:医用超声诊断和监护设备安全专用要求GB/T 14710 医用电器设备环境要求及试验方法YY/T 0749-2009 超声手持探头式多普勒胎儿心率检测仪性能要求及测量和报告方法3 术语和定义YY/T 0749-2009定义的以及下列术语和定义适用于本文件。
超声多普勒胎儿心率仪 ultrasonic Doppler fetal heartbeat detector根据超声多普勒原理,以数字显示和(或)声音输出的方式提供胎儿心率信息的仪器。
声工作频率 acoustic working frequency基于观察置于声场的水听器输出的声信号频率。
标称声工作频率 nominal acoustic working frequency由制造商标称的超声波工作频率。
综合灵敏度 overall sensitivity在噪声电平之上,仪器检出由已知平面波反射损失的模拟点状靶(宽度小于3个波长)产生的多普勒信号能力的量度,该靶与探头处于规定的距离,并在规定的速度下运动。
综合灵敏度由式(1)确定:S=A+B+C (1)式中:S ——综合灵敏度,单位为分贝,dB;A——在距探头规定距离处,靶的平面波反射损失,单位为分贝,dB;B——在声学路径上,包括声衰减片、声窗及水径的双程衰减量,单位为分贝,dB;C——仪器的信噪比,单位为分贝,dB。
超声多普勒胎儿监护仪产品技术要求含检测方法
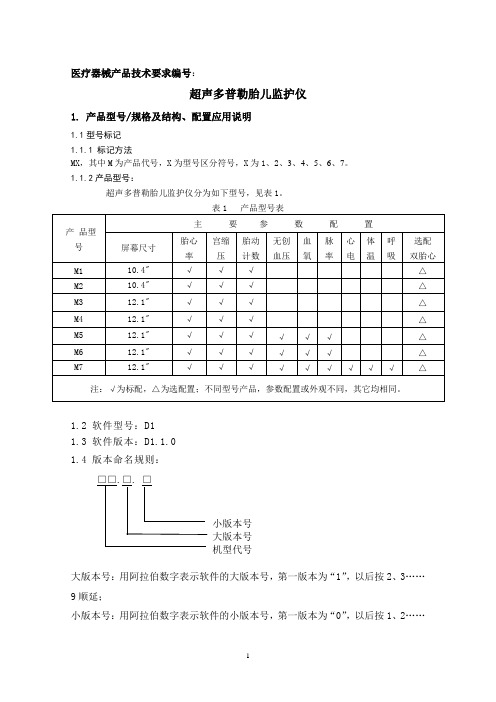
医疗器械产品技术要求编号:超声多普勒胎儿监护仪1. 产品型号/规格及结构、配置应用说明1.1型号标记1.1.1 标记方法MX ,其中M 为产品代号,X 为型号区分符号,X 为1、2、3、4、5、6、7。
1.1.2产品型号:超声多普勒胎儿监护仪分为如下型号,见表1。
1.2 软件型号:D1 1.3 软件版本:D1.1.0 1.4 版本命名规则:大版本号:用阿拉伯数字表示软件的大版本号,第一版本为“1”,以后按2、3……9顺延;小版本号:用阿拉伯数字表示软件的小版本号,第一版本为“0”,以后按1、2……小版本号 大版本号 机型代号9顺延,大版本号每升级一次,小版本号重新从第一版本开始编号;1.5 产品结构组成监护仪由主机、相应的功能附件:宫缩压探头、胎心率探头、胎动打标器、心电电缆、心电电极片、血氧探头、血压袖套、体温探头组成(外购部件包括:宫缩压探头、胎心率探头、胎动打标器、心电电缆、心电电极片,血氧探头、血压袖套、体温探头)。
1.6 基本参数1.6.1电源:a.c. 100-240V,50/60Hz。
1.6.2输入功率:<100VA;1.6.3 监测项目:心电、呼吸、体温、血氧饱和度、无创血压(收缩压、平均压和舒张压)、脉率、胎心率、宫缩压、胎动计数。
1.6.4 平均无故障工作时间:>5000h。
1.6.5 导联色标定义见表2。
1.6.6 心电电缆、心电电极片,血氧探头、血压袖套、体温探头的型号、规格及生产企业见表3。
表3 探头规格2.1心电参数2.1.1过载保护对任意的患者电极在任意导联选择的组合情况下,施加网电源频率的1V p-v差模电压10秒后,监护仪应符合本标准的要求。
2.1.2辅助输出不适用,无辅助输出接口。
2.1.3呼吸、导联脱落检测和有源噪声抑制对于任一患者电极连接,当所有其他的患者电极连到一个公共节点时,通过的直流电流不应超过0.1μA(即,任何用于输入给放大器来测量ECG电势的连接)。
超声多普勒胎儿监护仪产品技术要求深圳市和心重典医疗

1性能指标1.1安全要求安全要求应符合 GB 9706.1-2007、GB 9706.9-2008、YY 0709-2009 要求。
1.2电磁兼容性要求应符合 YY 0505-2012、GB 9706.9-2008 第 36 章的要求。
1.3性能参数1.3.1胎心率测量和显示范围胎心率测量和显示范围不窄于 30 次/min~240 次/min。
1.3.2胎心率测量误差胎心率测量的误差不大于±2 次/min。
1.3.3宫缩压力测量范围宫缩压力的测量范围应覆盖 0~100 单位,其非线性误差不大于±9%。
1.3.4超声工作频率超声工作频率 fw 与标称频率的偏差应不大于±10%。
1.4报警功能仪器应装有发光或发声的报警装置,在测量胎心率超过预置值时,应产生报警信号,并可消除报警。
从胎心率越限至开始报警的时间不大于 30s。
1.5贮存记录功能1.5.1内置实时记录器的仪器,其走纸速度的误差不超过±5%。
1.5.2内置实时记录器的基线漂移不大于全量程的 5%。
1.6电源电压适应能力1.6.1采用交流电源供电的仪器,在交流220V±22V的范围内,仪器应能正常工作。
1.6.2采用电池供电的仪器,在电压下降至额定值的 85%时,仪器应能正常工作。
1.7正常连续工作时间1.7.1采用交流电源供电的仪器,在正常交流电压情况下,仪器连续工作时间应达到 24h。
1.7.2采用电池供电的仪器,在充满电的条件下连续工作时间不少于 2h。
1.8外观与结构1.8.1外表应色泽均匀、表面整洁,无划痕、裂缝等缺陷。
—1 —1.8.2面板上文字和标志应清楚易认、持久。
1.8.3控制和调节机构应灵活、可靠,紧固部位无松动。
1.9监护仪功能要求具有评分功能。
1.10设备环境试验要求1.10.1气候环境试验应符合 GB/T 14710-2009 中Ⅱ组及表 2 的规定。
1.10.2机械环境试验应符合 GB/T 14710-2009 中Ⅱ组及表 2 的规定。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2.性能指标
2.1标称声工作频率:2.5MHz,声工作频率与标称声工作频率的偏差小于±5%。
2.2综合灵敏度:在距离探头表面 200mm 处综合灵敏度不小于 90dB。
2.3空间峰值时间峰值声压:<0.2MPa。
2.4输出超声功率:〈40mW。
2.5超声换能器敏感元件的有效面积:FD-100 系列为 1.57cm2±10%, FD-200、FD-800 系列为
3.07cm2±10%, FD-120 系列为 1.57cm2±10%, FD-210 系列为
1.57cm2±10%,FD-220 系列为
2.45cm2±10%。
2.6胎心率测量范围及误差
2.6.1胎心率测量范围:50~240 次/分。
2.6.2胎心率测量误差:±1%或±1次/分,取两者之间的大值。
2.7安全要求
2.7.1仪器的通用安全应符合 GB 9706.1-2007 的要求。
2.7.2仪器的专用安全应符合 GB 9706.9-2008 的要求。
仪器的声输出参数若不能达到 GB/T 16846-2008 免予公布的条件,则应在使用说明书中予以公布。
2.8电源电压适应能力
在电池电压下降至额定值的 85%时,仪器应能正常工作。
FD-220A 机型使用3.7V 锂电池,当电池电压下降至 3.3V 时,仪器应能正常工作。
FD-800 系列的机器,在交流220V±22V的范围内,适配器应能正常给机器充电。
2.9连续工作时间
当内部电池为满电量时,FD-100 系列连续工作时间应不小于 60 分钟,FD-200 系列连续工作时间应不小于120 分钟, FD-800 系列连续工作时间应不小于 6 小时。
FD-120 系列连续工作时间应不小于 60 分钟,FD-210 系列连续工作时间应不小于 120 分钟,FD-220 系列连续工作时间应不小于 120 分钟。
2.10外观和结构要求
2.10.1外表应色泽均匀,表面整洁,无明显划痕、裂缝等缺陷。
2.10.2仪器表面的丝印及标贴中的文字、图案应清楚易认、持久。
2.10.3按键、旋钮等操作应灵活、可靠,紧固部位无松动。
2.11功能要求
当探头处有信号输入时,仪器应能从喇叭或耳机中发出清晰洪亮的声音。
操作音量调节旋钮或音量按键,声音大小应能对应的增大或者减小。
FD-100、FD-120、FD-200、FD-220 系列产品可选配蓝牙通讯功能,最大通讯距离为空旷场地 10 米。
2.12环境试验要求
环境试验应符合GB/T 14710-2009 中气候环境试验II 组和机械环境试验III 组的规定,试验要求及检测项目按表 2 执行。
表2 环境试验要求及检测项目
电磁兼容应符合 YY0505-2012 的要求。
FD-120 系列、FD-210 系列、FD-220 系列应符合 GB9706.9-2008 第36 章的要求。
