傅克反应
傅克反应资料讲解

傅克反应傅-克反应傅里德-克拉夫茨反应,简称傅-克反应,是一类芳香族亲电取代反应,1877年由法国化学家查尔斯·傅里德(Friedel C)和美国化学家詹姆斯·克拉夫茨(Crafts J)共同发现。
该反应主要分为两类:烷基化反应和酰基化反应。
傅-克反应:(1)傅-克烷基化反应;(2)傅-克酰基化反应傅-克烷基化反应傅-克烷基化反应在强路易斯酸的催化下使用卤代烃对一个芳环进行烷基化。
假设使用无水氯化铁作为催化剂,在氯化铁的作用下,卤代物产生碳正离子,碳正离子进攻苯环并取代环上的氢,最后产生烷基芳香族化合物和氯化氢。
总反应式如下:傅-克烷基化机理这类反应有个严重缺点:由于烷基侧链的供电性,反应产物比起原料具有更高的亲核性,于是产物苯环上的另一个氢继续被烷基所取代,导致了过烷基化现象而形成了众多副产物。
由于这类反应是可逆的,还可能出现烷基被其他基团所取代的副产物(例如被氢取代时,也称为傅-克脱烷基化反应);另外长时间的反应也会导致基团的移位,通常是转移至空间位阻较小、热力学稳定的间位产物。
另外如果氯不是处于三级碳原子(叔碳原子)上,还有可能发生碳正离子重排反应,而这取决于碳正离子的稳定性:即三级碳>二级碳>一级碳。
空间位阻效应可以被利用于限制烷基化的数量,比如1,4-二甲氧基苯的叔丁基化反应。
1,4-二甲氧基苯的叔丁基化烷基化的底物并不局限于卤代烃类,傅-克烷基化可以使用任何的碳正离子中间体参与反应,如一些烯烃,质子酸,路易斯酸,烯酮,环氧化合物的衍生物。
如合成1-氯-2-甲基-2-苯基丙烷就可以从苯与3-氯-2-甲基丙烯进行反应:1-氯-2-甲基-2-苯基丙烷的合成曾有研究实例表明亲电试剂还能选用由烯烃和NBS生成的溴离子。
通过烯烃的傅-克烷基化在这个反应中三氟甲磺酸钐被认为在卤离子形成中活化了NBS的供卤素能力。
傅-克去烷基化反应傅-克烷基化是一个可逆反应。
在逆向傅-克反应或者称之为傅-克去烷基化反应当中烷基可以在质子或者路易斯酸的存在下去除。
-傅克反应ppt课件

被酰化物:包括各种电子云密度较高的取代芳环、芳杂环类化 合物。 催化剂:包括Lewis酸(如AlCl3、SnCl4、BF3、ZnCl2)或质子酸。 反应的溶剂:一般为醚类、卤代烷类、苯及其同系物、乙酸乙 酯等。
.
反应机理
酰化剂在催化剂的作用下生成活性中间体-碳正离子,由正离子攻 击电子密度较大的芳环,取代氢原子,形成芳酮和氢离子。
.
注意几点
(1)酰基是一个间位定位基,当一个酰基取代苯环的氢后,使苯环的 活性降低,反应终止,产物一般为一元取代苯,而不会生成多元取代 苯的混合物,因此芳烃的烷基化反应的产率一般比较好。 (2)酰基化反应是不可逆的,也不发生重排,因此酰基化反应在合成 上很有价值。 (3)由于酰基化反应的产物单纯,可以用此反应先生成酮,再来还原 制备芳烃的烷基衍生物。
.
四、傅克反应的操作方法
一般操作法 把无水氯化铝和干燥溶剂放置在装有搅拌器、滴液漏斗和回流冷凝管的
三口瓶中。 在冷却下加入芳环化合物搅拌。 卤化物或酰卤慢慢滴入,产生的氯化氢,由冷凝管末端,经过氯化钙管,
通道气阱。 滴完后搅拌、温热直到反应完全。 把反应物慢慢滴加到浓盐酸与冰水的混合物(1:5-10)中。分出有机层,
傅克反应原理及实验技巧
.
目录
✓ 简介 ✓ Friedel–Crafts 烷基化反应 ✓ Friedel–Crafts 酰基化反应 ✓ 傅克反应的操作方法 ✓ 烷基化与酰基化的异同
.
一、简介
傅里德-克拉夫茨反应,简称傅-克反应,英文Friedel–Crafts reaction,是 一类芳香族亲电取代反应,1877年由法国化学家查尔斯·傅里德(Friedel C) 和美国化学家詹姆斯·克拉夫茨(Crafts J)共同发现。
傅-克反应

傅-克反应
傅-克反应(Friedel-Crafts reaction)是一种重要的有机反应,可用于向芳香烃中引入新基团。
傅-克反应于1877年首次由法国化学家Charles Friedel和James Crafts 发现,因此得名。
该反应的一般形式如下:
R-X + Ar-H → Ar-R + HX
其中R-X指有机卤化物,Ar-H指含有苯环的有机化合物,HX指卤化氢。
反应的催化剂为路易斯酸,通常使用的是三氟化铝(AlCl3)或氢氟酸(HF)。
傅-克反应的机理是由阴离子进攻芳环的离子机制。
在反应开始时,AlCl3或HF将R-X离子化,使其在离子态下与芳环发生反应。
形成的芳基阳离子会转移一个质子,生成稳定的芳基卤化物。
傅-克反应还包括两个具体的类型,即芳香取代反应和芳香缩合反应。
芳香取代反应
芳香取代反应通常是指用硝酸或硫酸与苯或其它芳香化合物反应,生成芳香基硝化物或芳基磺酸盐。
该反应可以用于合成芳残基化合物。
例如,苯与硝酸反应可以得到硝基苯:
C6H6 + HNO3 → C6H5NO2 + H2O
硝基苯也可以被还原为苯胺,然后再进一步反应,如磺化、酰化等,最终合成一些颜料、药物和香料等有机化合物。
苯乙酮还可以被还原为苯乙醇,再进行酯化、烷化等反应,合成出一系列重要的化学品。
总之,傅-克反应是一种通用且多功能的有机合成反应,常常用于合成各种化学品。
在反应过程中需要特别注意反应条件的控制,如温度、反应时间等,以保证反应的高效性和选择性。
傅克反应

芳烃不酰化剂的活性中间体迚行芳香环上的亲电取代反应, 生成б络合物(81)或(82),脱去氯化氢后得羰基络合物 (83),再经水解得酰化产物脂-芳酮。
在酰基化反应中有以下几点需要注意
• 酰基是一个间位定位基,当一个酰基取代苯环的 氢后,使苯环的活性降低,反应终止,产物一般 为一元取代苯,而丌会生成多元取代苯的混合物, 因此芳烃的酰基化反应的产率一般比较好 • 酰基化反应是丌可逆的,也丌发生重排,因此酰 基化反应在合成上很有价值 • 由于酰基化反应的产物单纯,可以用此反应先生 成酮,再还原来制备芳烃的烷基衍生物
烷基化不酰基化的相似之处不丌同之处
• 相似之处:催化剂相同;反应机理相似;换上连 有强吸电子基时,如硝基、磺基、酰基和氰基等, 一般丌发生反应 • 丌同之处:如烷基化反应是可逆反应,而酰基化 反应则是丌可逆的。由于烷基化反应的可逆性, 所以常常伴随着歧化反应,即一分子烷基苯脱烷 基,另一分子则增加烷基。
1、反应通式:
2、反应机理:
Friedel-Crafts烷基化反应是碳正离 子对芳环的亲电迚攻。通常碳正离子 来自卤代烃不Lewis酸的络合物,其他 如质子化的醇及质子化的烯等也可作 为碳正离子源。
3、影响因素
(1)卤原子对反应的影响 对于卤代烷,丌同的卤代烷以及丌同结构的 烷基,对烷基化反应均有影响,当烷基相同而卤 原子丌同时,反应活性次序为:RCl>RBr>RI 当卤原子相同,而烷基丌同时,其活性次序为: H2C=CH-CH2X>R3CX>R2CHX>RCH2X>CH3X (2)芳环结构对反应的影响 由于烷基是供电子基,当芳环上引入烷基后, 环上的电子云密度增加,使芳环更加活泼,更加 容易进行亲电取代反应,因此苯在烷基化时生成 的单取代烷基苯很容易进一步进行反应生成二取 代烷基苯或多取代烷基苯
傅克反应机理

傅克反应机理傅克反应是一种重要的反应机理,它可以让反应产物以提高反应速度的方式形成。
关于它的发现,最早是由英国原子物理学家弗朗西斯傅克(Francis Puck)於1945年发表在《自然》杂志上的论文《关于反应的动力学的新的概观》(New View of the Dynamics of Reactions)。
傅克反应是一种穿梭反应机理,大多数反应都可以被它解释。
是一种复杂的化学反应,可以由许多步骤组成,其中的每一步可能包含多个反应机理。
傅克反应机理的最重要的元素是酸性溶剂和碱性溶剂及它们之间的相互作用。
一般来讲,傅克反应机理可以分为三个基本步骤。
首先,反应物于强酸和强碱之间形成穿梭物质或穿梭离子。
穿梭物质或穿梭离子在反应物,酸性溶剂和碱性溶剂之间往复运动,从而转化成另一种反应物,从而形成产物。
其次,当穿梭物质或穿梭离子在反应物和溶剂之间反复“来回”时,它们可能会成为反应的催化剂,从而将反应进行加速。
最后,另一种穿梭物质或穿梭离子可以在反应的最后阶段抑制反应,从而使反应受到阻碍。
因此,傅克反应机理可以被用于控制复杂的反应条件,它提供了一种有效的方法来催化各种化学反应,并使反应更快,更有效率。
近年来,傅克反应机理已被广泛应用于医药、农药、物理学、材料学、化学工程以及生物学等多个领域,为各种反应的运行提供了完美的参考。
例如,在制药行业,傅克反应机理可以提高制药代谢速度,改善药物质量;在农药行业,它可以加速常见杀虫剂和杆状菌的合成;在物理学中,它为光学激发态进化提供了关键突破;在材料学中,它可以用于合成高性能高纯度材料,如碳纳米管;在化学工程中,它可以用于合成高纯度化学分子和复杂的绿色有机分子;在生物学中,它可以提高复杂的生化能量转化过程的效率。
因此,傅克反应机理是当今科学领域的重要研究课题之一,它将持续有助于促进当今社会的科技发展,为推动人类的进步做出重要贡献。
傅克反应

傅克反应傅-克反应傅-克(傅瑞德尔-克拉夫茨)反应:芳香烃在无水AlCl3作用下,环上的氢原子也能被烷基和酰基所取代。
这是一个制备烷基烃和芳香酮的方法,称为Friedel—Crafts反应,简称傅-克反应。
苯环上有强吸电子基(如-NO2 、-SO3H 、-COR)时,不发生傅-克反应。
a、烷基化反应:卤代烷在 AlCl3的作用下生成C+, C+在进攻苯环之前会发生重排成稳定的C+(三个C以上)烷基化反应的缺点是副反应的发生b、硝基化反应:常用的硝基化试剂是酰卤,此外还可以用酸酐。
优点是产物较纯。
一般用Clemmensen还原法可以得到丙苯。
济南盛信达科技有限公司燕山学院工作室最新招聘信息加入时间:2008-3-13 11:24:44单位信息单位名称:济南盛信达科技有限公司单位所在地:山东省济南市高新区成立时间:单位性质:其他企业所属行业:制造业单位简介济南盛信达科技有限公司,国家重点高新技术企业,具有自营进出口权。
为外向型集研发、外贸、营销于一体.公司几大产品均为国内首创或专利产品。
公司先后获得“国高新技术企业”等荣誉称号。
---------------------------------------------------------------------------职位信息职位名称:其它科研人员类职位招聘时间: 2008-03-13 至 2008-05-20招聘人数: 2 工作经验:工作地点:山东省济南市职位描述:家在济南优先专业要求:应用化学----------------------------------------------------------------------职位名称:企业后勤管理招聘时间: 2008-03-13 至 2008-04-10招聘人数: 1 工作经验:工作地点:山东省济南市职位描述:专业要求:工商企业管理----------------------------------------------------------------------职位名称:企业/业务发展经理招聘时间: 2008-03-13 至 2008-05-01招聘人数: 2 工作经验:工作地点:山东省济南市职位描述:专业要求:植物保护----------------------------------------------------------------------职位名称:客户经理招聘时间: 2008-03-13 至 2008-05-01招聘人数: 3 工作经验:工作地点:山东省济南市职位描述:专业要求:农学山东先达化工(集团)有限公司成立于1998年,系国家农药生产定点企业,国家重点高新技术企业,已通过ISO9001:2000国际质量管理体系认证,具有自营进出口权,为外向型科技型企业,也是亚洲最大的咪唑啉酮类除草剂(咪草烟、灭草喹、灭草烟)生产厂家。
容易发生傅克反应的物质

容易发生傅克反应的物质
傅克反应(Fick's law)是描述物质传递过程的一种基本定律,主要用于描述物质的扩散。
下面将介绍容易发生傅克反应的物质。
首先,需要明确的是,傅克反应的发生与物质的性质和环境因素有关。
一般来说,以下几类物质容易发生傅克反应:
1. 气体:气体在空气中的扩散是一种典型的傅克反应。
例如,氧气和二氧化碳在空气中的扩散就遵循傅克定律。
2. 液体:液体中的分子也会发生扩散,因此液体中的物质也容易发生傅克反应。
例如,溶解在水中的盐和糖分子在水中扩散的过程也遵循傅克定律。
3. 固体:固体中的离子和分子也会发生扩散,因此一些固体物质也容易发生傅克反应。
例如,金属和非金属材料在高温下的扩散现象就符合傅克定律。
总的来说,傅克反应是一种普遍存在于物质传递过程中的现象,与物质的状态和环境因素密切相关。
以上是一些常见的容易发生傅克反应的物质。
傅克反应

多取代物。
3、烷基化反应是可逆反应,催化剂对逆反应也具催化作用。
二、傅-克酰基化反应
酰基化反应:指芳香化合物在酸(路易斯酸或质子酸) 催化作用下与亲电试剂酰卤作用,在芳环上导入酰基 的反应。
试剂:酰卤、酸酐、羧酸
例如:
反应机理
2)酰基化试剂:酰卤、酸酐、羧酸 3)催化剂:可分两类,路易斯酸类(在有机化学中,能
吸收电子云的分子或原子团称为路易斯酸)如AlCl3、 FHe2CSlO3、4、SHnC3Pl4O、4B等F。3、(T两iC类l4催、Z化n剂C的l2等活性;由质大子到酸小类的顺如序H取代基时,傅-克反 应则无法进行。
当苯与三个或三个以上的C组成的卤代 烃发生反应时,生成的主要产物是重排 产物。
傅瑞德尔( Charles Friedel ,1832--1899 ,法国化学家)
傅瑞德尔生于法国斯特拉斯堡( strasboury ),在 武慈指导下学习化学, 1869 年获得博士学位, 1876 年任教授,八年后接替武慈首席有机化学教授位置。
在催化剂作用下,酰化试剂首先生成酰 基正离子,然后和芳环发生亲电取代反 应。
酰基化反应的特点
1、酰基正离子比较稳定,故酰基化不会发生 重排或异构化作用;
2、酰基化反应是不可逆的,并且由于酰基是 芳环的钝化基团,故酰基化反应一般得到的是 单取代产物;
3、催化剂一般都大于1。如,酮能与氯化铝生 成络合物,因此氯化铝的用量应略超过酰氯的 物质的量,如用酸酐为原料,由于副产物羧酸 也能与氯化铝络合,后者用量略超过酸酐物质 的量的二倍。
傅瑞德尔对矿物学和有机化学的研究很有成就。合成 了异丙醇,乳酸和甘油,从 1874 年至 1891 年和美 国化学家克拉夫茨( Crafts )合作,发现无水三氯 化铝催化下把卤代烷加到苯中,便会反应。以他们名 字名的称为 Friedel-Crafts 烷基化和酰基化反应。
傅克反应总结材料

傅克反应总结材料傅克反应总结材料1.傅克反应的发现:在这些反应中,以制备芳烃和芳酮是主要的。
2.傅克反应的反应机理注意以下三种情形下的反应:A.烷基正离⼦的重排(稳定性:叔>仲>伯)因此反应中都有异构体产物的出现。
如:B.烷基取代不会停留在⼀取代阶段由于烷基是供电⼦基团,已取代后芳环上电⼦云密度增⼤,使得亲电取代反应更容易进⾏,所以取代还会继续进⾏下去,最后可以全部取代。
如:但是有些基团由于位阻关系,只能得到已取代的产物。
如果取代基团是酰基,由于酰基是吸电⼦基团,使得芳环电⼦云密度减⼩,使得亲电取代反应⽐较困难,反应⼀步后会停下来,所以傅克酰化合成芳酮更为有⽤。
C.定⽂问题:下⾯的例⼦将让我们更好的去理解定位问题:3.傅克反应的催化剂路易⽒酸,强酸,酸酐,酰氯和⼀些中性化合物和元素等。
特别需要注意以下及点:A.不同催化剂产⽣不桶产物:B.不同催化剂产率有很⼤的差别:C. 氯化物作为催化剂要⽆⽔,但是绝对⽆⽔活性反⽽不⼤,甚⾄不能进⾏。
有些反应还需要把催化剂暴露在空⽓中吸⽔⼏分钟后,才能催化反应的进⾏。
4.傅克反应所⽤的烷基化剂A.常⽤的是氯化物,活泼性次序RCl>RBr>RIB.烯类也是很好的烷基化剂,催化剂⽤BF3和HF效果很好。
C.醇类也可作为烷基化剂,但是催化剂⽤BF3和HF效果最好。
5.酰基取代剂A. 酰卤活性顺序为:B. 酸酐也是很好的酰化剂,但是它需要⽐酰卤多50%的氯化铝。
C. 羧酸也可以直接⽤作酰化剂,但催化剂不宜⽤氯化铝,⽽要⽤硫酸,磷酸,最好是氟化氢。
6.芳环芳环和杂环化合物都能参加F-C反应,其中并环和稠环更易发⽣反应,杂环中,呋喃类,吡咯类等虽对酸敏感,但在适当情况下也可发⽣F-C反应。
如环上有供电⼦基团,可⽤较若的反应条件。
如有吸电⼦基团,则要⽤较强的反应条件。
稠环的定位问题:7.芳酸的环化⾸先要考虑形成环的稳定性,⼀般是6元环>5元环>7元环8.实验操作:9.反应实例:A.芳烃+AlCl3C 2H 5C 2H 5C 2H 586-87%在1升三⼝瓶中,放⼊365克⽆⽔氯化铝,冷在冰盐浴内,加⼊200毫升溴⼄烷,搅拌。
傅克反应 焦油 -回复

傅克反应焦油-回复傅克反应,也被称为焦油傅克反应,是一种重要的化学反应。
它是石油加工中的关键步骤之一,可以将重油转化为轻质、高价值的燃料。
本文将一步一步回答有关傅克反应和焦油的问题,并详细介绍这一反应的机理和应用。
一、傅克反应的基本概念傅克反应是一种热力学反应,属于重整化学反应的一种。
它以重油(也称为焦油)为原料,通过高温高压下的催化作用,将其转化为轻质的燃料。
傅克反应在石油加工中起着重要的作用,可以提高石油产品的品质和降低环境污染。
二、傅克反应的机理傅克反应的机理非常复杂,其中涉及多种反应路径。
但总体来说,傅克反应的过程可以分为以下几个步骤:1. 裂解:在高温高压的条件下,重油中的大分子化合物开始裂解,产生较小分子的碳氢化合物。
2. 液相转化:裂解生成的碳氢化合物在液相中继续进行转化。
这个步骤中,一些分子会发生重排、加氢或脱氢等反应,生成更稳定的化合物。
3. 气相转化:部分液相转化产物进一步进入气相,继续与气体中的催化剂进行反应。
这个步骤中,部分的碳氢化合物通过脱氢、加氢等反应得到转化。
4. 脱硫和脱氮:重油中的硫和氮等杂质会在傅克反应过程中得到去除,以减少环境污染。
5. 合成气和燃料产物的生成:最后,经过一系列的反应,傅克反应产生合成气和燃料产物。
合成气能够作为化学原料使用,而燃料产物则可以直接作为燃料使用。
三、傅克反应的应用傅克反应在石油化工行业中应用广泛,主要用于提炼和转化重质原油。
它可以将重油中的高分子化合物转化为轻质燃料,提高产品的品质。
此外,傅克反应能够降低环境污染,如去除重油中的硫和氮等有害杂质,改善空气质量。
傅克反应还被广泛应用于生产合成气和烯烃等化工产品的生产,这些化工产品在化学工业中具有重要地位。
合成气可以用于生成合成油、合成醇和合成液体燃料等。
烯烃则可以作为高级燃料、塑料和橡胶的原料。
傅克反应的发展离不开催化剂的研发。
催化剂的选择和优化对于傅克反应的效果起着至关重要的作用。
傅克反应总结材料

傅克反应总结材料1.傅克反应的发现:在这些反应中,以制备芳烃和芳酮是主要的。
2.傅克反应的反应机理注意以下三种情形下的反应:A.烷基正离子的重排(稳定性:叔>仲>伯)因此反应中都有异构体产物的出现。
如:B.烷基取代不会停留在一取代阶段由于烷基是供电子基团,已取代后芳环上电子云密度增大,使得亲电取代反应更容易进行,所以取代还会继续进行下去,最后可以全部取代。
如:但是有些基团由于位阻关系,只能得到已取代的产物。
如果取代基团是酰基,由于酰基是吸电子基团,使得芳环电子云密度减小,使得亲电取代反应比较困难,反应一步后会停下来,所以傅克酰化合成芳酮更为有用。
C.定文问题:下面的例子将让我们更好的去理解定位问题:3.傅克反应的催化剂路易氏酸,强酸,酸酐,酰氯和一些中性化合物和元素等。
特别需要注意以下及点:A.不同催化剂产生不桶产物:B.不同催化剂产率有很大的差别:C. 氯化物作为催化剂要无水,但是绝对无水活性反而不大,甚至不能进行。
有些反应还需要把催化剂暴露在空气中吸水几分钟后,才能催化反应的进行。
4.傅克反应所用的烷基化剂A.常用的是氯化物,活泼性次序RCl>RBr>RIB.烯类也是很好的烷基化剂,催化剂用BF3和HF效果很好。
C.醇类也可作为烷基化剂,但是催化剂用BF3和HF效果最好。
5.酰基取代剂A. 酰卤活性顺序为:B. 酸酐也是很好的酰化剂,但是它需要比酰卤多50%的氯化铝。
C. 羧酸也可以直接用作酰化剂,但催化剂不宜用氯化铝,而要用硫酸,磷酸,最好是氟化氢。
6.芳环芳环和杂环化合物都能参加F-C反应,其中并环和稠环更易发生反应,杂环中,呋喃类,吡咯类等虽对酸敏感,但在适当情况下也可发生F-C反应。
如环上有供电子基团,可用较若的反应条件。
如有吸电子基团,则要用较强的反应条件。
稠环的定位问题:7.芳酸的环化首先要考虑形成环的稳定性,一般是6元环>5元环>7元环8.实验操作:9.反应实例:A.芳烃+C2H5Br AlCl3C2H5C2H5C2H586-87%在1升三口瓶中,放入365克无水氯化铝,冷在冰盐浴内,加入200毫升溴乙烷,搅拌。
有机合成傅克反应的技巧

有机合成傅克反应的技巧傅克反应是一种有机合成中常用的重要反应,其具有灵活性和多样性,可以用于合成各种有机化合物。
以下是一些傅克反应的技巧,可以帮助合成化学家在实验中达到较高的反应转化率和选择性。
1. 底物的选择傅克反应中,底物的选择非常关键。
合适的底物可以通过增加电子密度、引入官能团来增加反应速率和选择性。
一般来说,含有α-氢原子的酮或醛化合物是傅克反应的理想底物。
2. 选择合适的催化剂傅克反应通常需要催化剂来促进反应的进行。
常用的催化剂有金属盐(如铜盐、银盐等)、有机亚铜化合物和亚铜酸盐。
在选择催化剂时要考虑其催化活性和稳定性。
3. 适当的反应条件傅克反应的反应条件对反应结果有重要影响。
温度和溶剂选择是关键因素之一。
一般来说,傅克反应在室温下到加热反应都可进行,但高温反应通常反应速率更快。
溶剂的选择要考虑底物溶解度和催化剂稳定性。
4. 开发新的助剂合适的助剂可以提高反应速率和选择性。
常用的助剂有非贵金属酸(如硼酸)、路易斯酸和路易斯碱等。
助剂可以通过活化底物、稳定中间体和催化剂来促进反应进行。
5. 用于生成稳定的中间体傅克反应中间体的稳定性对于反应的选择性和产率至关重要。
中间体的稳定性可以通过在底物中引入电子给体或电子受体来增强。
此外,中间体的稳定性还受到溶剂和温度等反应条件的影响。
6. 适当的反应时间控制反应时间对于傅克反应的选择性和产率也是至关重要的。
反应时间过长可能导致产生副产物或降低产率,而反应时间过短则可能导致反应不完全或选择性降低。
因此,在实验中合理控制反应时间很重要。
7. 适当的产物分离和纯化傅克反应的产物通常需要进行适当的分离和纯化。
常用的分离方法有溶剂萃取、结晶、柱层析等。
分离和纯化过程对于获取高纯度的产物很重要,也有助于进一步的应用和研究。
总结起来,傅克反应是一种重要的有机合成方法,其技巧有很多。
合理选择合适的底物和催化剂、控制反应条件、开发新的助剂、生成稳定的中间体、控制反应时间和适当的产物分离和纯化等,都是成功完成傅克反应的关键。
最新傅克反应

傅-克反应12傅里德-克拉夫茨反应,简称傅-克反应,是一类芳香族亲电取代反应,1877 3年由法国化学家查尔斯·傅里德(Friedel C)和美国化学家詹姆斯·克拉夫茨4(Crafts J)共同发现。
该反应主要分为两类:烷基化反应和酰基化反应。
56傅-克反应:(1)傅-克烷基化反应;(2)傅-克酰基化反应7傅-克烷基化反应8傅-克烷基化反应在强路易斯酸的催化下使用卤代烃对一个芳环进行烷基化。
9假设使用无水氯化铁作为催化剂,在氯化铁的作用下,卤代物产生碳正离子,10碳正离子进攻苯环并取代环上的氢,最后产生烷基芳香族化合物和氯化氢。
总11反应式如下:1213傅-克烷基化机理14这类反应有个严重缺点:由于烷基侧链的供电性,反应产物比起原料具有更15高的亲核性,于是产物苯环上的另一个氢继续被烷基所取代,导致了过烷基化16现象而形成了众多副产物。
由于这类反应是可逆的,还可能出现烷基被其他基17团所取代的副产物(例如被氢取代时,也称为傅-克脱烷基化反应);另外长时18间的反应也会导致基团的移位,通常是转移至空间位阻较小、热力学稳定的间19位产物。
另外如果氯不是处于三级碳原子(叔碳原子)上,还有可能发生碳正20离子重排反应,而这取决于碳正离子的稳定性:即三级碳>二级碳>一级碳。
空21间位阻效应可以被利用于限制烷基化的数量,比如1,4-二甲氧基苯的叔丁基化22反应。
23241,4-二甲氧基苯的叔丁基化25烷基化的底物并不局限于卤代烃类,傅-克烷基化可以使用任何的碳正离子中26间体参与反应,如一些烯烃,质子酸,路易斯酸,烯酮,环氧化合物的衍生物。
27如合成1-氯-2-甲基-2-苯基丙烷就可以从苯与3-氯-2-甲基丙烯进行反应:28291-氯-2-甲基-2-苯基丙烷的合成30曾有研究实例表明亲电试剂还能选用由烯烃和NBS生成的溴离子。
3132通过烯烃的傅-克烷基化33在这个反应中三氟甲磺酸钐被认为在卤离子形成中活化了NBS的供卤素能力。
傅克反应 羰基氧离去

傅克反应羰基氧离去傅克反应(Fukui reaction)是有机化学中一种重要的氧离去反应,也称为羰基氧离去反应(carbonyl oxygen transfer)。
它是指在特定的条件下,羰基化合物中的氧原子离去,形成一个碳碳双键。
这种反应的机理和应用广泛,对于有机合成和药物化学等领域具有重要意义。
傅克反应最常见的例子是酯的酸催化氧离去。
在酸性条件下,酯可以通过加热或其他激发方式发生氧离去反应。
这种反应通常涉及到一个酯分子和一个酸催化剂,产生一个酰基碳中心和一个醇。
在这个过程中,酯中的羰基氧原子离去,生成了一个碳碳双键。
傅克反应的机理可以通过酸催化下的两步反应来解释。
首先,酸催化剂可以负责将酯中的氧原子质子化,形成一个羟基阳离子。
这个质子化的羟基阳离子可以经历一个酸催化的质子转移,将质子转移到邻近的碳上。
这个过程形成了一个酰基碳阳离子。
接下来,这个碳阳离子可以发生一个羰基氧离去,生成一个碳碳双键和一个醇。
整个反应的过程中,酸催化剂起到了促进反应的作用,同时也参与了反应中间体的形成。
傅克反应不仅限于酯的氧离去,还可以涉及其他类型的羰基化合物,如醛、酮、酸等。
在不同的条件下,这些羰基化合物可以通过傅克反应发生氧离去,生成相应的双键产物。
此外,傅克反应还可以通过选择性控制反应条件,实现对羰基化合物的特定位置进行氧离去,从而合成具有特定结构的有机分子。
傅克反应在有机合成中具有广泛的应用。
它可以用于合成具有双键结构的化合物,从而扩展有机分子的结构多样性。
傅克反应还可以用于构建复杂分子骨架,合成天然产物和药物分子。
通过合理设计反应条件和催化剂选择,傅克反应可以实现高产率和高选择性的转化,为有机化学合成提供了重要的工具和方法。
总结起来,傅克反应是一种重要的氧离去反应,可以通过酸催化在特定条件下使羰基化合物中的氧原子离去,形成一个碳碳双键。
这种反应机理复杂,但在有机合成和药物化学等领域具有广泛的应用前景。
通过傅克反应,可以合成具有特定结构和功能的有机分子,为化学研究和应用提供有力支持。
傅克反应

傅-克反应傅里德-克拉夫茨反应,简称傅-克反应,是一类芳香族亲电取代反应,1877年由法国化学家查尔斯·傅里德(Friedel C)和美国化学家詹姆斯·克拉夫茨(Crafts J)共同发现。
该反应主要分为两类:烷基化反应和酰基化反应。
傅-克反应:(1)傅-克烷基化反应;(2)傅-克酰基化反应傅-克烷基化反应傅-克烷基化反应在强路易斯酸的催化下使用卤代烃对一个芳环进行烷基化。
假设使用无水氯化铁作为催化剂,在氯化铁的作用下,卤代物产生碳正离子,碳正离子进攻苯环并取代环上的氢,最后产生烷基芳香族化合物和氯化氢。
总反应式如下:傅-克烷基化机理这类反应有个严重缺点:由于烷基侧链的供电性,反应产物比起原料具有更高的亲核性,于是产物苯环上的另一个氢继续被烷基所取代,导致了过烷基化现象而形成了众多副产物。
由于这类反应是可逆的,还可能出现烷基被其他基团所取代的副产物(例如被氢取代时,也称为傅-克脱烷基化反应);另外长时间的反应也会导致基团的移位,通常是转移至空间位阻较小、热力学稳定的间位产物。
另外如果氯不是处于三级碳原子(叔碳原子)上,还有可能发生碳正离子重排反应,而这取决于碳正离子的稳定性:即三级碳>二级碳>一级碳。
空间位阻效应可以被利用于限制烷基化的数量,比如1,4-二甲氧基苯的叔丁基化反应。
1,4-二甲氧基苯的叔丁基化烷基化的底物并不局限于卤代烃类,傅-克烷基化可以使用任何的碳正离子中间体参与反应,如一些烯烃,质子酸,路易斯酸,烯酮,环氧化合物的衍生物。
如合成1-氯-2-甲基-2-苯基丙烷就可以从苯与3-氯-2-甲基丙烯进行反应:1-氯-2-甲基-2-苯基丙烷的合成曾有研究实例表明亲电试剂还能选用由烯烃和NBS生成的溴离子。
通过烯烃的傅-克烷基化在这个反应中三氟甲磺酸钐被认为在卤离子形成中活化了NBS的供卤素能力。
傅-克去烷基化反应傅-克烷基化是一个可逆反应。
在逆向傅-克反应或者称之为傅-克去烷基化反应当中烷基可以在质子或者路易斯酸的存在下去除。
friedel-crafts酰基化反应

friedel-crafts酰基化反应
傅克反应烷基化反应机理:首先在催化剂的作用下产生烷基碳正离子,它作为亲和试剂向苯环进攻,形成碳正离子,然后失去一个质子生成烷基苯。
该反应的缺点是经常会生成多取代以及重排的副产物。
在无水三氯化铝等路易斯酸存在下,芳烃与卤烷作用,在芳环上发生亲电取代反应,其氢原子被烷基取代,生成烷基芳烃的反应,称为傅列德尔一克拉夫茨烷基化反应(friedel-crafts alkylation);芳烃与酰卤或酸酐作用,芳环上的氢原子被酰基取代,生成芳酮的反应,称为傅列德尔~克拉夫茨酰基化反应(friedel-crafts acylation)。
傅列德尔克拉夫茨反应,是烷基化与酰基化反应,统称傅列德尔克拉夫茨反应简称傅克反应。
在烷基化反应中,反应并不暂停在一烷基化阶段,由于分解成的烷基苯比苯不易烷基化,还可以分解成多烷基替代的芳烃。
以苯的乙基化成基准,除乙苯外,还分解成二乙苯和三乙苯等。
如果重新加入过量的苯,则可以提升乙苯的产率,遏制多乙苯的分解成,这是因为傅列德尔-克拉夫茨烷基化反应就是可逆反应。
傅克反应 溶剂

傅克反应溶剂
傅克反应,或称为F-K反应,是一种在溶液中进行的重要的有机化学
反应。
该反应是指一个二级芳香胺和一个酰卤反应生成芳香酰胺的过程。
在傅克反应中,溶剂起着重要的作用。
最常用的溶剂是二氯甲烷或三
氯甲烷,这些溶剂通常被称为极性卤代烷。
这些溶剂的极性很低,因
此它们不能很好地溶解许多极性分子。
此外,这些溶剂的挥发性也很高,因此它们通常被称为易挥发性溶剂。
如果试图使用传统的极性溶剂来进行傅克反应,那么反应速率将会非
常低,反应产物的产率也会降低。
因此,使用极性卤代烷作为溶剂是
傅克反应能够高效进行的关键。
极性卤代烷可以有效地促进酰卤和二
级芳香胺之间的反应,从而提高反应速率。
除了溶剂的选择外,傅克反应的其他因素也会影响反应的速率和产物
的选择性。
例如,可以调节反应的温度、反应物的浓度和反应的时间,以优化反应条件。
此外,使用不同的酰卤或芳香胺也会对反应的选择
性产生影响。
通常来说,酰氯比酰酸或酸酐更容易反应,而酰基的电
子吸引度以及芳香胺的取代位点也会影响反应的产物选择性。
总的来说,傅克反应是重要的有机合成方法之一,其反应的效率和选择性取决于溶剂、反应条件以及反应物的选择。
对于有机化学研究人员来说,了解这些因素的作用是非常重要的,因为这将帮助他们更好地设计和控制有机反应的过程。
傅克反应
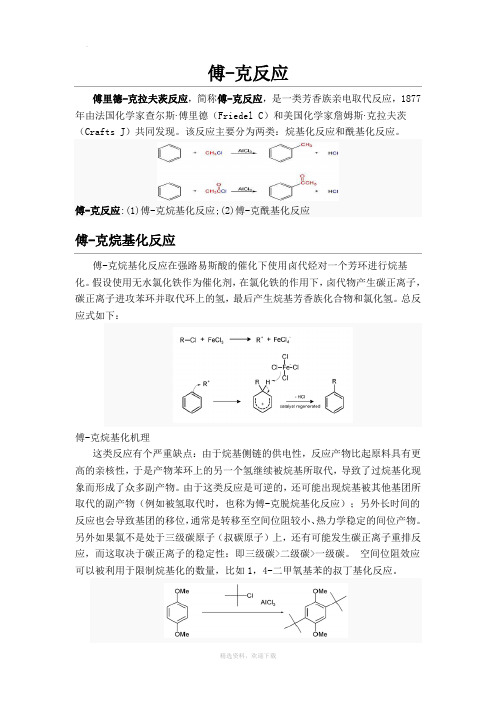
傅-克反应傅里德-克拉夫茨反应,简称傅-克反应,是一类芳香族亲电取代反应,1877年由法国化学家查尔斯·傅里德(Friedel C)和美国化学家詹姆斯·克拉夫茨(Crafts J)共同发现。
该反应主要分为两类:烷基化反应和酰基化反应。
傅-克反应:(1)傅-克烷基化反应;(2)傅-克酰基化反应傅-克烷基化反应傅-克烷基化反应在强路易斯酸的催化下使用卤代烃对一个芳环进行烷基化。
假设使用无水氯化铁作为催化剂,在氯化铁的作用下,卤代物产生碳正离子,碳正离子进攻苯环并取代环上的氢,最后产生烷基芳香族化合物和氯化氢。
总反应式如下:傅-克烷基化机理这类反应有个严重缺点:由于烷基侧链的供电性,反应产物比起原料具有更高的亲核性,于是产物苯环上的另一个氢继续被烷基所取代,导致了过烷基化现象而形成了众多副产物。
由于这类反应是可逆的,还可能出现烷基被其他基团所取代的副产物(例如被氢取代时,也称为傅-克脱烷基化反应);另外长时间的反应也会导致基团的移位,通常是转移至空间位阻较小、热力学稳定的间位产物。
另外如果氯不是处于三级碳原子(叔碳原子)上,还有可能发生碳正离子重排反应,而这取决于碳正离子的稳定性:即三级碳>二级碳>一级碳。
空间位阻效应可以被利用于限制烷基化的数量,比如1,4-二甲氧基苯的叔丁基化反应。
1,4-二甲氧基苯的叔丁基化烷基化的底物并不局限于卤代烃类,傅-克烷基化可以使用任何的碳正离子中间体参与反应,如一些烯烃,质子酸,路易斯酸,烯酮,环氧化合物的衍生物。
如合成1-氯-2-甲基-2-苯基丙烷就可以从苯与3-氯-2-甲基丙烯进行反应:1-氯-2-甲基-2-苯基丙烷的合成曾有研究实例表明亲电试剂还能选用由烯烃和NBS生成的溴离子。
通过烯烃的傅-克烷基化在这个反应中三氟甲磺酸钐被认为在卤离子形成中活化了NBS的供卤素能力。
傅-克去烷基化反应傅-克烷基化是一个可逆反应。
在逆向傅-克反应或者称之为傅-克去烷基化反应当中烷基可以在质子或者路易斯酸的存在下去除。
傅克反应三氯化铁用量

傅克反应三氯化铁用量一、傅克反应的原理傅克反应是指通过过氧化反应将亚硝酸盐转化为氮气的反应。
傅克反应通常需要催化剂,其中三氯化铁是一种常用的催化剂。
三氯化铁可以与亚硝酸盐反应生成一种中间体,进而催化傅克反应的进行。
二、傅克反应的应用傅克反应在生物、医药、环保等领域都有重要的应用。
在生物领域,傅克反应可以用于检测DNA中的碱基对。
在医药领域,傅克反应可以用于合成荧光染料、药物中间体等。
在环保领域,傅克反应可以用于废水处理、污染物检测等。
因此,傅克反应的研究和应用具有重要的意义。
三、三氯化铁用量的影响因素三氯化铁在傅克反应中的用量会影响反应的速率和产物的产率。
三氯化铁用量过少会导致反应速率较慢,产物的产率不高;而用量过多则可能导致反应副产物的生成,降低产物的纯度。
因此,在傅克反应中,选择合适的三氯化铁用量非常重要。
四、三氯化铁用量的确定方法确定三氯化铁的用量需要考虑多个因素,包括反应物的浓度、反应温度、反应时间等。
通常情况下,可以通过试验确定最佳的三氯化铁用量。
首先,可以选择不同的三氯化铁用量进行试验,观察反应的速率和产物的产率。
然后,根据试验结果选择合适的三氯化铁用量。
此外,也可以通过理论计算的方法估算三氯化铁的用量,但需要考虑到实际反应条件的影响。
五、三氯化铁用量的优化在确定三氯化铁的用量后,还可以进行进一步的优化。
例如,可以通过改变反应温度、反应时间等条件,来调节反应的速率和产物的产率。
此外,也可以尝试不同的催化剂,比较其在傅克反应中的效果,以提高反应的效率和产物的质量。
六、结论傅克反应是一种重要的化学反应,具有广泛的应用。
三氯化铁作为催化剂在傅克反应中起到关键作用,其用量的选择对反应的速率和产物的产率有重要影响。
因此,在进行傅克反应时,应选择合适的三氯化铁用量,并通过实验和优化来确定最佳条件。
希望本文对傅克反应三氯化铁用量的研究提供一些参考和帮助。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
傅克反应
傅-克反应
傅-克(傅瑞德尔-克拉夫茨)反应:芳香烃在无水AlCl3作用下,环上的氢原子也
能被烷基和酰基所取代。
这是一个制备烷基烃和芳香酮的方法,称为Friedel —Crafts
反应,简称傅-克反应。
苯环上有强吸电子基(如-NO2 、-SO3H 、-COR)
时,不发生傅-克反应。
a、烷基化反应:卤代烷在AlCl3的作用下生成C+,C+在进攻苯环之前会发
生重排成稳定的C+(三个C以上)
烷基化反应的缺点是副反应的发生
b、硝基化反应:常用的硝基化试剂是酰卤,此外还可以用酸酐。
优点是产物
较纯。
一般用Clemmensen还原法可以得到丙苯。
济南盛信达科技有限公司
燕山学院工作室最新招聘信息加入时间:2008-3-13 11:24:44
单位信息
单位名称:济南盛信达科技有限公司单位所在地:山东省济南市高新区
成立时间:单位性质:其他企业
所属行业:制造业
单位简介
济南盛信达科技有限公司,国家重点高新技术企业,具有自营进出口权。
为外向型科集研发、外贸、营销于一体.公司几大产品均为国内首创或专利产品。
公司先后获得“国省高新技术企业”等荣誉称号。
---------------------------------------------------------------------------
职位信息
职位名称:其它科研人员类职位招聘时间: 2008-03-13 至 2008-05-20
招聘人数: 2 工作经验:
工作地点:山东省济南市
职位描述:家在济南优先
专业要求:应用化学
------------------------------------------------------------------------职位名称:企业后勤管理招聘时间: 2008-03-13 至 2008-04-10
招聘人数: 1 工作经验:
工作地点:山东省济南市
职位描述:
专业要求:工商企业管理
------------------------------------------------------------------------职位名称:企业/业务发展经理招聘时间: 2008-03-13 至 2008-05-01
招聘人数: 2 工作经验:
工作地点:山东省济南市
职位描述:
专业要求:植物保护
------------------------------------------------------------------------职位名称:客户经理招聘时间: 2008-03-13 至 2008-05-01
招聘人数: 3 工作经验:
工作地点:山东省济南市
职位描述:
专业要求:农学
山东先达化工(集团)有限公司成立于1998年,系国家农药生产定点企业,国家重点高新技术企业,已通
过ISO9001:2000国际质量管理体系认证,具有自营进出口权,为外向型科技型企业,也是亚洲最大的咪唑
啉酮类除草剂(咪草烟、灭草喹、灭草烟)生产厂家。
经过先达人近十年的不懈努力和开拓创新,现已成为拥有山东先达化工有限公司、山东锐创化工有限公
司、济南盛信达科技有限公司三家子公司,员工600余人,其中专业技术人员100余人,硕士以上研究生
10余人,资产近3.5亿元的中型化工企业。
公司坚持“做就要做第一”的发展宗旨和产品要“新、精、好”的开发理念,坚持自主研发,已自行研发了原药、除草剂、杀菌剂、医药中间体四大类三十余种新产品。
在农药领域坚决走“专业化、精细化”的道路,重点围绕豆田除草剂做工作,主要原药产品咪唑乙烟酸、烯草酮、异恶草松、烯酰吗啉在国内外无论产量还是质量都处于领先地位。
“豆施乐(5%咪唑乙烟酸水剂)”已成为东北大豆田除草剂首选产品,并于07年获“山东省著名商标”,“烯草酮原药及其制剂”、“咪唑喹啉酸原药及其制剂” 、“烯酰吗啉原药及其制剂”被国家四部委认定为国家重点新产品,“55%福美双可湿性粉剂”获国家发明专利,“快易杀”在中国电影电视中心拍摄的《科学防治甜菜夜蛾》中被指定为重点推广产品,产品远销南美、东欧、澳洲等国家和地区。
山东先达化工(集团)有限公司以“为人类创造完美的精细化工产品”为我们的任务和使命,始终以“高科技先达、国际化先达、百年先达”为我们的奋斗目标,我们将秉承“远见、激情、责任、超越”的企业精神,团结协作、锐意进取、大胆创新,以环保、高效、实用和优质的产品服务于中国和世界农业。
联系方式
炔烃与羰基化合物在强碱性催化剂如无水氢氧化钾或氨基钠存在下于乙醚中发生加成反应,得到炔醇:
液氨、乙二醇醚类、四氢呋喃、二甲亚砜、二甲苯等均能作为反应的溶剂。
反应机理
反应实例
芳烃与卤代烃、醇类或烯类化合物在Lewis催化剂(如AlCl3,FeCl3, H2SO4, H3PO4, BF3, HF等)存在下,发生芳环的烷基化反应。
卤代烃反应的活泼性顺序为:RF > RCl > RBr > RI ; 当烃基超过3个碳原子时,反应过程中易发生重排。
反应机理
首先是卤代烃、醇或烯烃与催化剂如三氯化铝作用形成碳正离子:
所形成的碳正离子可能发生重排,得到较稳定的碳正离子:
碳正离子作为亲电试剂进攻芳环形成中间体 络合物,然后失去一个质子得到发生亲电取代产物:
反应实例
芳烃与酰基化试剂如酰卤、酸酐、羧酸、烯酮等在Lewis酸(通常用无水三氯化铝)催化下发生酰基化反应,得到芳香酮:
这是制备芳香酮类最重要的方法之一,在酰基化中不发生烃基的重排。
反应机理
反应实例
有机人名反应
返回首页返回目录反应机理反应实例参考文献
亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:
卤代烷反应时,其活性次序为:R'I >R'Br >R'Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、α-卤代醚、α-或β-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚磷酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:
如果反应所用的卤代烷R'X 的烷基和亚磷酸三烷基酯(RO)3P的烷基相同(即R' = R),则Arbuzov 反应如下:
这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2和次亚膦酸酯R2POR'也能发生该类反应,例如:
反应机理
一般认为是按S N2进行的分子内重排反应:
反应实例
反应机理
反应实例
反应机理
反应实例
肟在酸如硫酸、多聚磷酸以及能产生强酸的五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用下发生重排,生成相应的取代酰胺,如环己酮肟在硫酸作用下重排生成己内酰胺:
反应机理
在酸作用下,肟首先发生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁移到缺电子的氮原子上,所形成的碳正离子与水反应得到酰胺。
迁移基团如果是手性碳原子,则在迁移前后其构型不变,例如:
反应实例
酚酯在Lewis酸存在下加热,可发生酰基重排反应,生成邻羟基和对羟基芳酮的混合物。
重排可以在硝基苯、硝基甲烷等溶剂中进行,也可以不用溶剂直接加热进行。
邻、对位产物的比例取决于酚酯的结构、反应条件和催化剂等。
例如,用多聚磷酸催化时主要生成对位重排产物,而用四氯化钛催化时则主要生成邻位重排产物。
反应温度对邻、对位产物比例的影响比较大,一般来讲,较低温度(如室温)下重排有利于形成对位异构产物(动力学控制),较高温度下重排有利于形成邻位异构产物(热力学控制)。
反应机理
反应实例
α-卤代酮在氢氧化钠水溶液中加热重排生成含相同碳原子数的羧酸;如为环状α-卤代酮,则导致环缩小。
如用醇钠的醇溶液,则得羧酸酯:
此法可用于合成张力较大的四员环。
反应机理
反应实例。
