检测实验室工作流程图
检测工作流程图

检测工作流程图
检测委托、交接工作流程图
通知检测室
现场检测
安排车辆
(调度)
样品交接
(收样员)
无损检测工作流程图
符合
资料上交资料室
建材检测工作流程图
通知客服部
填写不合格通知
(检测员)
上报室主任
通知母户是
确认是否复检
结构室检测工作流程图(现场检测)
结构室检测工作流程图(力学检测)
环境检测工作流程图(材料检测)
委托单及样品交接
(主任助理与客服)
不合格N
环境检测工作流程图(现场检测)
联系委托方J
-
检测准备(检测员) a 准备检测设备
上报室主
任
委托单交接
(与客服部)
交接(检测员)
1 F
Y
资料上交资料室
环境检测工作流程图(现场采样检测)
接受业务委托(业务员)
资料上交资料室
制定检测计划(室主任与技术支持)
('文
员)
上报室主
任
Y
节能检测工作流程图
报告更改流程图
报告发放流程
资料上报
(各检测
室)
Y
F
报告盖章
(印章专员)
父费
不
交
费
告
发放报告
人
员
招
聘
、
培
训
、
入
职
流
程
图C3
行政人事部(仪器设备采购流程图)
行政人事部
(实验室借款流程图)
注:单线为第一次,双线为第二次。
实验室质量控制程序(含流程图)

文件制修订记录1.0目的规范实验室管理,确保在组织质量控制、质量改进工作中所进行的检验、测量、试验等工作的顺利进行,快速准确的完成各项质量检验、测量和试验工作。
2.0适用范围本规定适用于公司范围内所有用于检测、测量和试验活动所涉及到的实验室的全过程管理控制。
3.0术语及定义3.1实验室进行包括但不限于包括化学、冶金、尺寸、物理、电性能或可靠性试验在内的检验、测量、试验和校准的机构,包括人员、设施和环境。
4.0职责4.1过程质量管理部4.1.1负责实验室测量设备的检定/测量归口管理,对外部实验室能力及进货检验的性能试验进行监控;4.1.2负责整车检测线委外检测、整车路试、三坐标测试及日常管理。
4.2人力资源部负责组织对实验室人员的培训和资格确认。
4.3试制试验部4.3.1负责编制实验室管理制度、制定实验室操作及维护保养规程;4.3.2负责实验室的日常管理,遵守实验室的操作规程;4.3.3负责对生产制造过程和新产品研制开发过程中的零部件、发动机、白车身和整车等依据技术文件标准进行检验、测量和试验工作。
5.0工作程序5.1工作流程:见附件。
5.2试验范围5.2.1实验室有资格进行的特定试验、评价和校准。
本公司实验室试验项目:检测线整车检测试验、整车性能与排放性能试验、整车安全性能试验、发动机性能试验、传动系统性能试验、电驱系统性能试验、混合动力系统性能试验、电池性能试验、环境与材料性能试验。
实验室设备及试验项目一览表应建立相应的方法并经试验主管部门负责人批准后方可执行,并在试验记录中说明。
5.2.3用来进行上述活动的设备、方法和标准的清单详见《实验室设备及试验项目一览表》。
5.3实验室人员资格确认5.3.1实验室应由技术、测量、试验人员组成,技术人员对技术负全面责任,测量、试验人员按照各自的职责完成测量/试验任务,确保测量、试验工作的公正性和准确性。
5.3.2监控与测量装置的有关人员(包括计量检测、计量管理以及其使用操作人员),应当具备相应的能力和资格,以确保测量系统的准确性和完整性。
临床检验标准化实验室完整SOP程序文件

13、三级医院必须设置清洁区,污染区,操作有气溶胶可能的标本应配置生物安全柜及其它防护设置,如紫外线灯,排气扇等。
14、非科室工作人员不准进入实验室,外来人员参观需经科主任同意方可进入
(二)质量管理制度
1、各专业实验室根据省临检中心的有关规定,开展实验室内的质量控制,并制定有关措施。对室內质控应每日有记录,对失控情况有纠正方法,有预防性措施,对于目前尚无完整的室内质控体系的实验室,应积极创造条件,建立室内质量控制体系。
D10、铁染色标准操作规程
D11、酸性磷酸酶(ACP)染色标准操作规程
D12、红细胞渗透脆性试验标准操作规程
D13、自体溶血试验标准操作规程
D14、血清酸化溶血试验(Ham试验)标准操作规程
D15、热溶血试验(定性)标准操作规程
D16、蔗糖溶血试验(糖水试验)标准操作规程
D17、变性珠蛋白小体检查(Heinz小体染色)标准操作规程
3、对工作中可能发生的触电、失火、玻璃割伤、针头刺伤、烧伤、不慎中毒、传染性标本的污染,各实验室应有应急处理的方法,有关人员均应熟悉。
4、用电设备、电源线路、CO2气体、给排水系统的安全性符合使用要求,不能带电检修仪器。
5、使用强酸碱腐蚀品时,应在适当的环境下正确操作,防止腐蚀、灼伤、中毒、火灾和爆炸等事件发生。
8、易燃,易爆试剂应分开存放远离火源和电源。
9、供应商所送的试剂必须先经药库清点才能接受,检验科人员清点后必须在货单上签字,有出入者必须向科主任或试剂管理员、组长报告,再将货单交给试剂管理员,以便月底结帐。
10、科室试剂管理员:钟梁。
(五)实习生管理制度
1、科室按实习大纲安排实习时间表,如遇特殊情况科室统一安排。
实验室检测工作流程图
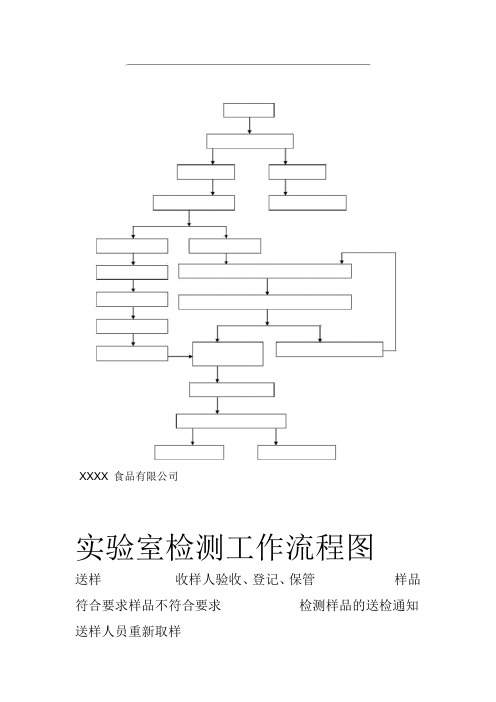
XXXX食品有限公司
实验室检测工作流程图
送样收样人验收、登记、保管样品符合要求样品不符合要求检测样品的送检通知送样人员重新取样
无检测能力的,外检检测能力的,自检
严格按标准规定的项目、方法进行检测,超差需重测协议/填写检测委托书样品邮寄数据处理、原始记录经检测人员自校后,送复核人复核
跟踪检测结果
复核无误后,结合外复核发现问题,提出复检处理意见
收取检测报告检报告编制检测报告
检测主管审核检测报告
授权签字人批准、签发检测报告
反馈送样人员/QA原始记录、报告存档。
HIV实验室检测及规范操作

快速检测试剂的优缺点
硒标记法和金标记法 与ELISA相比 ►优点 所需时间短 操作简便,不需特殊设备。 试剂贮存于室温。 ►缺点 特异性和敏感性与ELISA有差距。 费用较高。
HIV抗体检测程序及流程图
1、筛查试验 标本验收合格后,用筛查试剂进行检测,如 呈阴性反应,报告为HIV抗体阴性;对呈阳性 反应的标本须进行重复检测。 2、重复检测 用原有试剂和另外一种不同原理或不同厂家 的试剂重复检测,如两种试剂复测均呈阴性 反应,则报告HIV抗体阴性;如均呈阳性反应, 或一阴一阳,需送艾滋病确认实验室进行确 认。
HIV抗体确认检测流程
筛查试验阳性反应样品 免疫印迹法(WB,HIV-1/2混合型)
HIV抗体初筛检测
ELISA)
(阿克苏
结果判定 ⑴阴性对照(Negative Control,,NC)的参考标准 NC必须<0.250,去除≥0.250的各孔; 计算剩余NC的平均值(NCx) 0.6NCx<NC<1.4NCX,如果有一个以上超出此范围, 去除后重新计算NCx。 ⑵判定实验有效性: 至少有2个阴性对照OD值有效。 PC1-NCx≥0.400(PC1:HIV-1抗体阳性对照值) PC2-NCx≥0.400(PC2:HIV-2抗体阳性对照值)
HIV抗体初筛检测结果解释
造成检测结果不确定的原因
(1)处于窗口期,血清中还没有形成典型的HIV抗 体。 (2)艾滋病进展到终末期,人体免疫力缺陷,抗体 水平下降。 (3)与其他非病毒蛋白抗体有交叉反应.自身免疫 性疾病、恶性肿瘤、怀孕、输血或器官移殖 等,此时,身体产生的一些抗体与P24核 心蛋白抗体相似。 (4)以前接种过HIV疫苗。
HIV抗体检测(明胶颗粒凝集试验)
实验室质量控制程序(含流程图)

1/14文件制修订记录NO 制/修订日期1 2022-03-012 2022-10-16核准 实验室质量控制程序页数- 2022/10/16 新版全面升级版本 页次A0 C02022-10-16文件名称:文件编号:生效日期:生效版本: 制/修订内容新制订修订编号制订审核1.0 目的规范实验室管理, 确保在组织质量控制、 质量改进工作中所进行的检验、 测量、 试验等工作的顺利进行,快速准确的完成各项质量检验、测量和试验工作。
2.0 合用范围本规定合用于公司范围内所实用于检测、测量和试验活动所涉及到的实验室的 全过程管理控制。
3.0 术语及定义3.1 实验室进行包括但不限于包括化学、冶金、尺寸、物理、电性能或者可靠性试验在内的 检验、测量、试验和校准的机构,包括人员、设施和环境。
4.0 职责4.1 过程质量管理部4.1.1 负责实验室测量设备的检定/测量归口管理, 对外部实验室能力及进货检 验的性能试验进行监控;4.1.2 负责整车检测线委外检测、整车路试、三坐标测试及日常管理。
4.2 人力资源部负责组织对实验室人员的培训和资格确认。
4.3 试制试验部4.3.1 负责编制实验室管理制度、制定实验室操作及维护保养规程; 4.3.2 负责实验室的日常管理,遵守实验室的操作规程;4.3.3 负责对生产创造过程和新产品研制开辟过程中的零部件、发动机、白车 身和整车等依据技术文件标准进行检验、测量和试验工作。
5.0 工作程序5.1 工作流程:见附件。
5.2 试验范围C045.2.1 实验室有资格进行的特定试验、评价和校准。
本公司实验室试验项目: 检测线整车检测试验、整车性能与排放性能试验、整车安全性能试验、发动机 性能试验、传动系统性能试验、电驱系统性能试验、混合动力系统性能试验、 电池性能试验、环境与材料性能试验。
实验室 试验设备 试验项目等速行驶燃油消耗量试验、多工况燃油消耗量试验、 加速行驶油耗、 最高车速试验、 起步, 连续换挡加速 试验、 最低稳定车速、直接挡加速、 滑行试验、摹拟 爬坡试验、 常温下冷起动后排气污染物排放试验、 双怠速的 CO 、HC 和高怠速的λ值(过量空气系数)、曲 整车性能与排放轴箱污染物排放试验、蒸发污染物排放试验、、污染实验室控制装置耐久性试验、 低温下冷起动后排气中 CO 和 THC 排放试验、 OBD 系统试验、 0—100km/h 百公里加 速、 60—100km/h 超越加速、整车空调降温试验、整 车空调除雾试验、整车热平衡试验、整车温度场试验、汽车驱动轮输出功率试验、其他研发类试验汽车前/后端保护装置防护性能试验、汽车车顶抗压强度试验、汽车侧门静强度试验、汽车门锁/门铰链开闭耐久试验变速器传动效率试验、 变速器噪声测量、 变速器动态 密封试验、 变速器静态扭强度试验、 变速器疲劳寿命 试验、 换挡齿轮齿端冲击磨损试验、 变速器同步器性 能和寿命试验、变速器温升试验、变速器高速试验、测功机、数据采集系统、数控差速器可靠性试验、 变速器换挡性能试验、 定力矩牵系统、变速器安装支架等引试验、 定道路负载试验、 定力矩反拖试验、 寄生损 失试验、 全油门试验、 行驶道路负载试验、 发动机摩 擦力矩反拖试验、 静态跳动量试验、 剩余不平衡量试 验、临界转速试验、扭转间隙试验、静扭转刚性试验、 C04底盘测攻击、排放分析系统、 环境舱 (-10℃到+60℃)、称重 室等先后端防护摆锤碰撞试验台、 车顶静压试验机、车门侵入试 验机、四门两盖试验机传动系统测试实 验室整车安全实验室静扭转强度试验、 冲击强度试验、 扭转疲劳试验、 万向节磨损试验、滑动花键磨损试验电池组循环寿命试验、 电池组容量试验、 直流内阻试验、 电池组充电特性试验、 电池组放电特性试验、 电池组荷电保持能力试验、 电池组充放电效率试验、 电池组过充、 过放速率承受能力试验、 电池组温度特性试验、电池组单体电池电压测试机电及相应控制器的动/静态性能测试、机电机械特性测试、效率特性测试、再生制动测试、堵转测试、 温升测试、 驱动机电系统可靠性试验、 机电控制器测试、 直流机电测试、 三相异步电动机测试、 动态工况测试普通性起动试验、 发动机怠速试验、 功率试验、 负荷 特性试验、 万有特性试验、 柴油机调速特性试验、 机 械损失功率试验、 各缸工作均匀性试验、 机油消耗量试验、 活塞漏气量试验、 压气机性能试验、 涡轮性能试验、 200h 热循环试验、止推轴承评定试验、密封性评定试验、最高转速/最高温度试验、壳体包容性 评定试验、 燃油喷射系统 (电喷) 试验及 ECU 标定试 验、发动机摹拟装载整车道路行驶试验、 发动机排气污染物评价试验发动机外特性试验、 发动机部份符合特性试验、 万有 特性试验、 发动机排放特性试验、 发动机转矩输出特 性试验、机电外特性试验、机电部份符合特性试验、机电效率特性试验、 机电转矩输出特性试验、 机电再生制动特性试验、 电池组容量特性试验、 电池组效率特性试验、 电池状态 SOC 试验、 零部件(变速器、 离合器) 特性试验、 整车控制器性能试验、 整车控制策 略与控制算法验证与优化试验、混合动力各总成控制 器性能试验、 混合动力总成系统性能匹配试验、 整车测功机、油门执行单元、通用 测量设备、发动机进气流量计、 油耗仪、自动化主控系统等电池性能测试台、震动试验台、 冲击试验台、高低温试验台、 信号采集装置等测功机、高精度电流钳、功率分析设备、变频系统测功机、功率分析仪、电池组摹拟装置等混合动力系统性能测试实验室发动机系统性能 测试实验室电驱动性能测试实验室电池性能实验室的动力性试验、 整车的经济性试验、 整车的排放性试验对零部件及整车尺寸的测量安全碰撞仿真分析、 NVH 相关仿真分析、结构强度仿各种仿真分析软件真分析、流体 CFD 仿真分析汽车相关零部件及总成的耐高温冲击试验、试件的温度湿度振动三综合试验、 共振点检测试验、 振动性能试验、振动耐久试验、扫描振动耐久试验5.2.2 试验过程采用现行国家标准、行业标准、企业标准,当无尚述标准时, 应建立相应的方法并经试验主管部门负责人批准后方可执行,并在试验记录中 说明。
艾 梅 乙 检测服务流程图

附件1(产科门诊、病房上墙)预防艾滋病、梅毒和乙肝母婴传播服务流程图1. 预防艾滋病、梅毒和乙肝母婴传播服务流程)附件2-I(检验科上墙)孕产妇艾滋病抗体检测及服务流程图2. 孕妇艾滋病抗体检测及服务流程附件2-II(检验科上墙)产时艾滋病抗体检测及服务流程说明:# 再次确认结果阴性报告“阴性”,结果阳性报告“阳性”,结果仍为“不确定”继续随访,4周后再次进行确认试验;仍为不确定结果,报告“阴性”。
必要时可进行HIV核酸检测作为辅助诊断。
图3 产时艾滋病抗体检测及服务流程)(适用于孕期未接受HIV检测的产妇)附件3(检验科上墙)孕产妇梅毒检测及服务流程图4.孕产妇梅毒检测及服务流程艾滋病感染孕产妇及所生儿童抗艾滋病病毒用药方案预防艾滋病母婴传播抗病毒药物的应用可分为预防性抗病毒用药方案和治疗性抗病毒用药方案。
对于处于艾滋病临床I期或II 期,免疫功能相对较好,CD4+T淋巴细胞计数>350/mm3的艾滋病感染孕产妇,建议采用预防性抗病毒用药方案;对处于艾滋病临床Ⅲ期或Ⅳ期,CD4+T淋巴细胞计数≤350/mm3的艾滋病感染孕产妇,建议采用治疗性抗病毒用药方案。
一、预防性应用抗病毒药物(一)孕产妇预防性应用抗病毒药物。
1.孕期和分娩时。
从妊娠14周或14周后发现艾滋病感染后尽早开始服用齐多夫定(AZT)300mg +拉米夫定(3TC)150mg +洛匹那韦/利托那韦(克力芝)(LPV/r)400/100mg,每天2次;或者AZT300mg+3TC150mg,每天2次,依非韦伦(EFV)600mg,每天1次,直至分娩结束。
2.分娩后。
若选择人工喂养,产妇可在分娩结束后停止抗病毒药物的应用;若选择母乳喂养,产妇持续应用抗病毒药物至停止母乳喂养后1周。
(二)婴儿应用抗病毒药物。
婴儿可以选择应用以下两种抗病毒药物方案中的任一种。
1.奈韦拉平(NVP)方案:新生儿出生体重≥2500g,服用NVP 15mg(即混悬液1.5ml),每天1次;出生体重<2500g且≥2000g,服用NVP 10mg(即混悬液1.0ml),每天1次;出生体重<2000g,服用NVP 2mg/kg(即混悬液0.2ml/kg),每天1次;至出生后4~6周。
工地试验室质量管理体系实施流程图

1、内部文件:试验室制定的各类管理文件、各种记录表等
2、外部文件:法律法规、标准规范、图纸等(组织不能修改,为避免使用无效文件,应进行受控管理)
3、文件的层次:方针目标 质量手册 程序文件 指业指导书 记录表(空白)
4、管理文件种类:质量管理体系文件、经济管理文件
5、受控文件与非受控文件:受控文件是“非受控文件”的对称,凡是组织能够控制并修改存在多个版本的文件(仅一个版本有效)都是受控文件,也就是说凡是存在修改和换版的文件就是受控文件。受控文件主要是控制使用文件的唯一有效版本。受控文件可以复制阅读参考,但复制的文件不生效。一般来说这些文件是长期使用并始终处于修改和换版状态的文件,如:质量手册、程序文件、各种规章制度。 受控文件作废时,应从所有使用场合及时收回,以防止其误用。
标准物质核查:对标准物质应进行期间核查,主要是保存条件、有效期等。
填写的表格:年采购计划表、材料验收记录、供货商评价表、化学危险品入库登记表、危险品领用记录、标准物质一览表、标准物质领用登记表
五、管理制度(质量管理体系)、检测方法管理(法)
1、管理制度的管理
1.1制度建立与改进流程
1.2内审实施:出现重大质量问题、按计划(机构的体检),由中心试验室组织
2.2标准规范管理
2.3受控管理:受控管理确保不使用过期作废文件。工地试验室受控文件管理主要包括:登记(建清单)、加受控标记、过期文件标记与回收。受控文件一般包括:质量管理体系文件、标准规范等
填写的表格有:《受控文件清单》、《标准规范清单》、《数据库、软件光盘登记表》
2.4自动化试验、数据采集系统管理:验证程序数据采集、计算的准确性。
填写表格:《检测委托书》
2、样品管理表格:委托抽样单、样品登记表、样品留样登记表、样品处理登记表
检验科各种流程图

查验科工作流程图各实验组接收各种标本并查对当日检验标本贴条码编号,并离心处理标本调整各种仪器运转状态查验剖析室内质量控制紧急值、疑难结果剖析批准质控及检记录仪器有关参进行复查做好记录并通知临床医生或护士验结果,做好登记数室内质控结果查验、审查签发双署名报告查验后标本按要求办理标本、寄存各种穿刺液等穿刺标本按要求办理医生申请查验项目申请、填写查验申请输入电脑网络护士工作站填写患者标识、抽血、上花费血液大小便按有关要求采嘱病人按要取血液样本求留取标本查验科各实验组签收详细实验组进行查验各实验组查验后签发报告单送回各病房并签收病人持就诊卡医生填写查验申请单血液标本查验病人持就诊卡到收费处交费大小便其余查验项目病人凭查验单到门病人留取标本到相应实验组留取诊采血室采血(按项目要求),瞩病人取报告时间体液实验室或有关部门各实验组查验后并各实验组检测后签发报告单查对签发报告患者取报告患者取报告到医生处诊断查验科不合格标本办理流程病房标本接收检查查对患者信息及条形码,察看标本状态门诊标本采集核对条形码及患者信息,察看标本状态不合格标本不合格标本送实验室办理不合格标本记录后,通不合格标本登记退后知申请科室从头留取回从头留取从头留取后,各实验组检验后并查对签发报告病房查验单每天下午返回病房门诊查验单:血液每天下午13点 30分取体液其余按查验人员提示取查验科各岗位平时工作流程图生化室岗位平时工作流程图接收标本(门诊、病房)准备阶段:在收到标本后,按条码组合进行分类、编号,离心分别血清,并将血清吸入检测杯或直接将样品管按次序放入样品架上(盘)。
血清标本上机剖析:开机后先检查试剂,用省临检中心供给的质控物做病人标本和室内质控检测,质控在控(± 2SD)范围合格。
不然需要检查不合格项单个项目和小组合先安排,若有急诊项目则于急诊程序优先检测。
结果报告与审查查对:生化剖析仪每达成一个组合的测定即给出结果,其结果及时传递到 LIS 系统,经过在电脑屏幕上依据条码收费项目逐个审查后打印出查验报告。
各实验室工作流程图

实验室工作流程图目录
1、实验室工作流程图
2、临床和特殊诊断工作流程图
3、细菌学检验室工作流程图
4、血清学检验室工作流程图
5、生理生化试验室工作流程图
6、寄生虫检验工作流程图
7、病理组织学检验工作流程图
8、分子生物学诊断室工作流程图
9、细胞室工作流程图
10、病毒室工作流程图
11、出具诊断报告流程图
12、出具监测报告流程图
1 实验室工作流程图
2 临床和特殊诊断室工作流程图
5 生理生化试验室工作流程图
6 寄生虫学检验流程图
7 病理组织学检验流程图
8 分子生物学诊断室工作流程图
9 细胞室工作流程图
10 病毒室工作流程图。
检验科危急值报告制度程序及流程图

V
02
结果判断
|
03
危急值报告流程图展示
|--异常--| ||
VV
危急值报告流程图展示
危急值报告 正常结 果报告
VV
||
危急值报告流程图展示
• 临床医师处理 结束
危急值报告流程图展示
|
1
V
2
记录与归档
3
危急值报告流程图展示
01
02
03
04
|
V
```
结束
关键步骤解析
01 接收样本
02 样本检测
02
03
04
危急值
指检验结果高度异常,可能表 明患者处于生命危险状态,需
要立即采取行动的指标。
报告时限
从发现危急值到通知医生的时 间限制,通常要求在最短时间
内完成。
复核与确认
为确保报告的准确性,要求对 危急值结果进行复核和确认,
避免误报或漏报。
记录与追踪
对危急值的处理过程进行详细 记录,以便后续追踪和改进。
操作符号
表示具体的操作步骤或处理过程,通常使 用矩形表示。
流向符号
表示流程的方向或顺序,通常使用箭头表 示。
判断符号
表示流程中的决策点或分支点,通常使用 菱形表示。
危急值报告流程图展示
``` 开始
|
危急值报告流程图展示
V 接收样本
|
危急值报告流程图展示
V 样本检测 |
危急值报告流程图展示
01
THANKS
感谢观看
临床医生。
制定标准化流程
建立完善的危急值报告制度和 处理流程,明确各个环节的责 任人和时限要求,提高工作效 率和准确性。
质检部工作流程图

质检部工作流程图理要求,或发现异常情况,应及时向品质主管提报。
异常处理:品质主管应及时组织相关人员进行异常处理,分析原因并提出改善措施,确保产品质量;成品检验:生产完成后,检验员对成品进行检验,合格后放行;不合格品处理:不合格品应及时通知相关部门进行处理,如返工、报废等;入库:合格品放行后,仓库接收并安排入库,存档所有文件记录。
记录/参考生产计划单来料检验标准首检记录单生产巡检记录表品质异常提报单不合格品处理单成品检验记录单入库单存档文件记录品管部:进料工作流程图流程叙述:供应商送货:供应商将物料送到待检区,并提供产品质量报告单。
仓库按送货单暂收。
生产抽样并将样品送外协检验机构进行检验,准备验收。
外协检验报告核对:外协检验完成后,外协检验机构提供《检验报告单》,检验员核对外协检验报告是否与供应商提供之质量报告单结果一致。
判定与处理:检查《检验报告单》上的各指标是否符合要求,是否与供应商提供的质量报告单内容一至。
如果物料检验报告核对合格,仓库接到检验通行单,放行入库待生产。
如果不合格,质检主管审批,在送检通知单填写不合格,通知仓库退货处理,同时与采购部沟通该供应商提供该批次产品的问题。
挑选加工:来料不合格,经过物料评审,质检主管同意挑选使用,通知生产部门对物料进行挑选分类。
并最后由检验员检验确定,做好标识,区分存放。
可使用物料办理入库手续,待生产。
不合格物料办理退货手续。
入仓与存档:仓库接到检验通行单,安排入仓。
所有文件检验记录存档。
负责人:供应商/仓管员、送检员、检验员、品管主管、仓管员、采购员、质检主管、相关部门负责人。
记录/参考:送货单、《送检单》、《检验报告单》、《来料检验标准》、《供应商每批供应记录表》、《送检通知书》、《来料检验报告》、来料送检通知。
品管部:生产过程工作流程表流程叙述:原料、物料投产:根据生产计划原料、物料投入生产;检验员核对物料及来料品质状况。
首件检验:生产过程中,现场管理或技术人员对本车间或机台生产的产品进行自检,合格后现场QC通知检验员进行首件检验,如有需要应取样送实验室进行检测。
临床检验科操作SOP

一、检验科检测项目标准操作规程(见附录)A 、临检室A1、血常规检验标准操作规程A2、尿常规标准操作规程B 、生化室B1、糖尿病检测(诊断酶联试剂盒)标准操作规程二、检验室工作流程图大小便体液 血液标本三、检验科各项规章制度(一)生物安全制度1、医务人员1)每1—2年做体检一次,并接受乙肝疫苗接种。
2)每1—2年检查乙肝病毒抗原抗体水平,发现乙型肝炎者应进行隔离治疗。
3)检验人员进入实验室应穿好工作服,不允许在实验室进食和吸烟。
4)检验人员在工作前后和被污染后,应用肥皂和流水清洗,必要时由消毒液浸泡双手,每季度抽查检验人员的手,并做细菌培养一次。
2、环境消毒隔离1)实验室应分为清洁区和操作区,清洁区要注意保护不受污染。
操作有气溶胶可能的标本应配置生物安全柜及其它防护设置,如紫外线灯,排气扇等操作区的工作台及地面每日用消毒液擦拭一次,有污染时随时消毒,每周大扫除一次。
2)采血室每日操作前用清水擦拭操作台一次,采血结束用消毒液擦拭操作台、桌子和地面一次,紫外线每日照射消毒一次,每月空气细菌培养一次,紫外线强度定期测定。
并做记录。
3、各种检验标本的收集,送检必须用相应指定的容器留取,不得外溢污染。
4、静脉及末稍采血,应严格执行消毒隔离措施,静脉抽血做到一人一针一筒一巾一带一消毒,所用止血带及纸垫每日消毒,末稍采血一人一片一管,杜绝交叉污染。
5、一次性医用器具包括采血针,注射器、尿杯、血红蛋白微量吸血吸管,应严格做好领发登记,注射器先浸泡消毒后由供应室一对一调换,统一处理,其余一次性器具浸泡消毒后装入污物袋送焚烧炉焚烧。
6、检验人员在进行静脉抽血时应严格遵守无菌操作技术,操作前必须洗手必须戴好帽子与口罩,操作台和手被污染时应用肥皂和流水认真洗手,必要时用消毒液浸泡双手,酒精、碘酒瓶每周更换消毒两次。
7、凡是肝炎病人和透析病人的血液标本及疑有黄疸的血标本,都视为肝炎的污染标本,应贴上红色危险标记,放在规定区域内,引起警惕和防止扩大污染面。
