高中化学常用物质溶解性表及沉淀颜色(xin)
高中化学沉淀物质大全

高中化学沉淀物质大全1.氢氧化铜Cu(OH)2:氢氧化铜是一种蓝色沉淀,难溶于水,但能溶于氨水和稀硫酸。
2.氢氧化铁Fe(OH)3:氢氧化铁是一种红棕色沉淀,难溶于水,但能溶于酸。
3.氢氧化镁Mg(OH)2:氢氧化镁是一种白色沉淀,难溶于水,能溶于酸。
4.氢氧化铝Al(OH)3:氢氧化铝是一种白色沉淀,难溶于水,能溶于酸和碱。
5.氯化银AgCl:氯化银是一种白色沉淀,难溶于水,是高中化学中常见的沉淀物质之一。
6.硫酸钡BaSO4:硫酸钡是一种白色沉淀,难溶于水,不溶于酸。
7.碳酸钙CaCO3:碳酸钙是一种白色沉淀,难溶于水,但能溶于酸。
8.碳酸镁MgCO3:碳酸镁是一种白色沉淀,难溶于水,但能溶于酸。
9.碳酸铜CuCO3:碳酸铜是一种蓝色沉淀,难溶于水,但能溶于酸。
10.碳酸锌ZnCO3:碳酸锌是一种白色沉淀,难溶于水,但能溶于酸。
11.碳酸银Ag2CO3:碳酸银是一种白色沉淀,难溶于水,但能溶于酸。
12.氯化银AgCl:氯化银是一种白色沉淀,难溶于水,是高中化学中常见的沉淀物质之一。
13.溴化银AgBr:溴化银是一种淡黄色沉淀,难溶于水,是高中化学中常见的沉淀物质之一。
14.碘化银AgI:碘化银是一种黄色沉淀,难溶于水,是高中化学中常见的沉淀物质之一。
15.磷酸银Ag3PO4:磷酸银是一种淡黄色沉淀,难溶于水,是高中化学中常见的沉淀物质之一。
16.亚硫酸银Ag2SO3:亚硫酸银是一种白色沉淀,难溶于水,是高中化学中常见的沉淀物质之一。
17.硫酸铅PbSO4:硫酸铅是一种白色沉淀,难溶于水,不溶于酸。
18.硝酸铅Pb(NO3)2:硝酸铅是一种无色结晶,易溶于水。
19.氯化汞HgCl2:氯化汞是一种无色结晶,易溶于水。
20.碳酸锂Li2CO3:碳酸锂是一种白色结晶,易溶于水。
21.氢氧化锰Mn(OH)2:氢氧化锰是一种绿色沉淀,难溶于水,但能溶于酸。
22.硫酸镉CdSO4:硫酸镉是一种无色结晶,易溶于水。
2020年化学常见常见沉淀及溶解性口诀

作者:旧在几作品编号:2254487796631145587263GF24000022时间:2020.12.13常见沉淀白色:BaSo4∕BaCO3∕CaCO3∕AgCI∕Ag2CO3∕Mg(OH)2∕Fe(OH)2∕AI(OH)3∕CuCO3∕ZnCO3∕MnCO3∕ Zn(OH)2 Fe(OH)2蓝色:CU(OH)2浅黄色:AgBr红褐色:Fe(OH)3沉淀鉴别CU(OH)2蓝色沉淀Fe(OH)3红褐色沉淀AgBl■淡黄色沉淀AgI ,Ag3PO4黄色沉淀CUO黑色沉淀Cu20红色沉淀Fe2O3红棕色沉淀FeO黑色沉淀FeS2黄色沉淀PbS黑色沉淀FeC03灰色沉淀Ag2CO3黄色沉淀AgBr注黄色沉淀AgCl白色沉淀Cu2(OH)2CO3暗绿色沉淀BaC03白色沉淀(且有Co2生成)CaC03白色沉淀(且有CO2生成)BaS04白色沉淀不溶的破酸盐白色沉淀(且有Co2生成) 不溶的碱、金属氧化物白色沉淀(且有C02生成)Fe(OH)2为白色絮状沉淀(在空气中很快变成灰緑色,再变成Fe(OH)3红褐色沉淀)相关口诀钾钠钱盐硝酸盐均可溶盐酸盐银不溶硫酸盐倾不溶白色沉淀:CaC03. BaC03 . BaSO4. AgCL. Mg(OH)2蓝色沉淀:CU(OH)2红褐色沉淀:Fe (OH) 3不建议死记硬背,只需记住每个阴离子里哪个不溶即可,钾钠拔硝都溶溶解性口诀一钾钠银盐溶水快,①硫酸盐除去换银铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③氢氧根多溶一个领④口诀中未有皆下沉。
⑤注:①钾钠讓盐都溶于水;②硫酸盐中只有硫酸换、硫酸铅不溶(硫酸钙硫酸银微溶也是沉淀):③硝酸盐都溶于水:④碱性物质中除了钾离子钠离子彼离子锂离子还有领离子也可溶⑤口诀中没有涉及的盐类都不溶于水:溶解性口诀二钾、钠、钱盐、硝酸盐;氯化物除银、亚汞:硫酸盐除领和铅:碳酸、磷酸盐,只溶钾、钠、彼。
说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
高中化学沉淀颜色

高中常见沉淀的颜色黄色:AgI 、溴水(黄 --橙、 FeS 2、某些蛋白质加硝酸。
淡黄色:S 、 Na 2O 2、 TNT(三硝基甲苯、 AgBr棕黄色:FeCl 3溶液、碘水(深黄 --褐黑色:CuS 、 Ag 2S 、 Cu 2S 、 FeS 、 FeO 、 Fe 3O 4、 MnO 2、 CuO 、 Ag 2O 、 I 2(紫黑、 Si (灰黑、 C 、 Ag 、 KMnO 4(紫黑绿色:CuCl 2溶液、 Cu 2(OH 2CO3、FeSO 4• 7H 2O (浅绿、 F 2(浅黄绿、 Cl 2(黄绿、氯水(浅黄绿红色:CuO 、Cu 、Fe (SCN 2+、甲基橙在酸性环境中、紫色石蕊试液在酸性环境中、酚酞在碱性环境中、品红试液、红磷(暗红、 Br2(深红棕、 Br2在 CCl4溶液中(紫红、苯酚被空气氧化(粉红棕色:固体 FeCl 3、固体 CuCl 2 NO2(红棕、 Fe 2O 3(红棕紫色:KMnO 4溶液、 I 2在 CCl 4溶液中褐色:Fe (OH 3(红褐蓝色:CuSO 4/5H2O 、 Cu (OH 2、淀粉遇碘、紫色石蕊试液在碱性环境中, Cu 2+的稀溶液有色反应产生的沉淀有颜色红褐色絮状沉淀:Fe(OH3浅绿色沉淀:Fe(OH2蓝色絮状沉淀:Cu(OH2白色沉淀:CaCO 3, BaCO 3, AgCl, BaSO4,(其中 BaSO 4、 AgCl 是不溶于 HNO 3的白色沉淀 ,CaCO 3 BaCO 3是溶于 HNO 3的白色沉淀 ,Mg(OH2.淡黄色沉淀 (水溶液中 ----S微溶于水 ------------Ca(OH2,CaSO 4,生成的溶液或气体有颜色1、水溶液中含有 Fe 3+的为黄色 . 如 :Fe2(SO43、 FeCl 3、 Fe(NO3 3溶液2、水溶液中含有Cu 2+为蓝色, 如:CuCl2、Cu(NO3 2、CuSO 4溶液;但是, CuSO 4•5H2O 是蓝色 , 无水 CuSO 4是白色3、红棕色液体 :Br24、红棕色的气体:NO 2; SO 2, 无色有刺激性的气体; H 2S, 有臭鸡蛋气味的气体铁:铁粉是黑色的;一整块的固体铁是银白色的。
高中化学所有沉淀与微溶物总结

高中化学所有沉淀与微溶物总结一、硝酸盐全溶;二、硫酸盐除硫酸钡(白色)不溶;硫酸钙、硫酸银、硫酸铅(黑色)微溶;其他全溶;三、氢氧化物除钾、钠、钡溶,钙(氢氧化钙)微溶外,其余不溶;氢氧化铝(白色絮状)氢氧化铜(蓝色絮状)氢氧化铁(红褐色絮状)氢氧化亚铁(白色絮状,迅速变成灰绿色,最后变成红褐色)氢氧化镁(白色)氢氧化锌Zn(OH)2(白色絮状物)氢氧化银AgOH,沉淀立即分解2AgOH=2AgO(黑色)+H2o四、氯化物除氯化银不溶,其余全溶(卤素类似);除氟外的卤素(F,Cl,Br,I)和银的化合物:氯化银(白色)溴化银(浅黄色)碘化银(黄色)五、碳酸盐、亚硫酸盐、硅酸盐、硫化物除钾、钠、铵溶外,其余一般不溶;碳酸钙(白色)碳酸银(白色)碳酸铜(蓝色)亚硫酸钡、碳酸钡(都是白色)碳酸镁(白色),微溶六、酸式盐一般都溶,但磷酸盐特殊:磷酸二氢盐全溶,磷酸盐、磷酸一氢盐除钾、钠、铵外,其余一般不溶。
CaHPO4白色Ca3(PO4)2白色七、其他硫化银、氧化银(都是黑色)FeS(黑色沉淀)MnO2(黑色沉淀)S单质黄色沉淀CuS(黑色沉淀)三溴苯酚(白色沉淀)补:有色液体Fe2+——浅绿色Fe3+——黄色Cu2+——蓝色MnO4- 紫红色溴单质红棕(一般是溴的CCl4溶液)溴水橙色KSCN和Fe3+——血红苯酚和Fe3+紫色PS:这是我自己整理的,可能不全,重要的还是平时学习做题中积累记忆。
不过,可以看书后面的溶解度表,其实沉淀、微溶仅仅是溶解度大小的一个代称,易溶:大于10克/100克水.(100克水中溶解10克气体)可溶:大于1克/100克水,小于10克/100克水.微溶:大于0.1克/100克水,小于1克/100克水.难溶:大于0克/100克水,小于0.1克/100克水,一般称为沉淀。
高中溶解性表
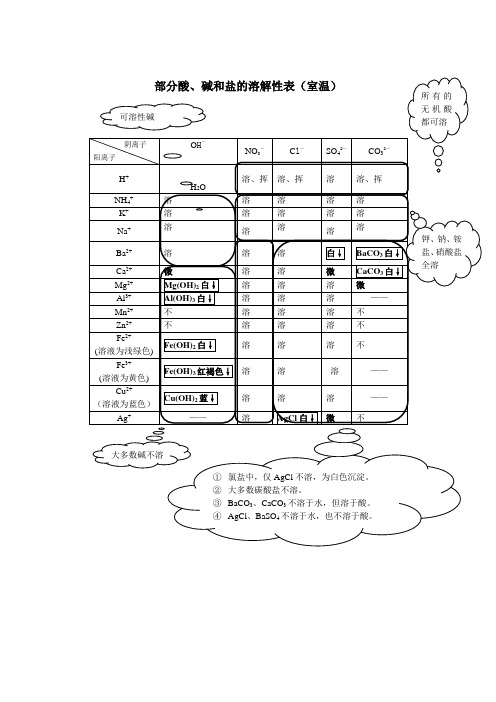
2+
大多数碱不溶 ① ② ③ ④ 氯盐中,仅 AgCl 不溶,为白色沉淀。 大多数碳酸盐不溶。 BaCO3、CaCO3 不溶于水,但溶于酸。 AgCl、BaSO4 不溶于水,也不溶于酸。
溶、挥 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶
白↓ 微 溶 溶 溶 溶 溶 溶 溶 微
BaCO3 白↓ CaCO3 白↓ 微 —— 不 不 不 —— —— 不
Ca2+ Mg Al Mn Zn
2+ 3+ 2+
钾、钠、铵 盐、 硝酸盐 全溶
2+
Fe (溶液为浅绿色) Fe3+ (溶液为黄色) Cu2+ (溶液为蓝色) Ag+
部分酸碱和盐的溶解性表室温可溶性碱阴离子阳离子oh所有的无机酸都可溶no3clso4溶溶溶溶白微溶溶溶溶溶溶溶不不不不2co3溶挥溶溶溶baco3白caco3白微钾钠铵盐硝酸盐全溶2hnh4knaba2ca2mg2al3mn2zn2溶溶溶溶微h2o溶挥溶挥溶溶溶溶溶溶溶溶溶溶溶溶溶溶溶溶溶溶溶溶溶溶mgoh2白aloh3白不不fe2feoh2白溶液为浅绿色fe3溶液为黄色feoh3红褐色溶溶溶cu2cuoh2蓝溶液为蓝色agagcl白微大多数碱不溶氯盐中仅agcl不溶为白色沉淀
部分酸、碱和盐的溶解性表(室温) 部分酸、碱和盐的溶解性表(室温)
可溶性碱
阴离子 阳离子
所有的 无机酸 都可溶 OH
-
NO3
-
Cl
-
SO4 溶 溶 溶 溶
2-
CO3 溶、挥 溶 溶 溶
2-
H+ NH4+ K
+ +
溶、挥 H 2O 溶 溶 溶 溶 微 Mg(OH)2 白↓ Al(OH)3 白↓ 不 不 Fe(OH)2 白↓ Fe(OH)3 红褐色↓ 红褐色↓ Cu(OH)2 蓝↓ —— 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶
化学常用物质溶解性表及沉淀颜色

化学溶解性表盐类溶解性表的规律可编成如下口诀记忆:钾、钠铵盐都可溶,硝盐遇水影无踪;硫(酸)盐不溶铅和钡,氯(化)物不溶银、亚汞。
氢气还原氧化铜实验,操作顺序可编成如下口诀记忆:氢气应早去晚归,酒精灯迟到早退,试管口下倾水滴。
氧化一还原反应的定义、性质、特征可编成如下口诀记忆:升失氧,降得还;若说剂,两相反。
盐类水解规律可编成如下口诀记忆:无“弱”不水解,谁“弱”谁水解;愈“弱”愈水解,又“弱”剧水解;谁“强”显谁性,双“弱”由K定。
盐类水解离子方程式的书写可编成如下口诀:左边水写分子式,中间符号写可逆,右边不写“↑”和“↓”。
溶解性口诀一钾钠铵盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
④注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅、硫酸钙不溶;③硝酸盐都溶于水;④口诀中没有涉及的盐类都不溶于水;溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶溶解性口诀四钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
溶解性口诀五钾钠铵盐硝酸盐完全溶解不困难氯化亚汞氯化银硫酸钡和硫酸铅生成沉淀记心间氢硫酸盐和碱类碳酸磷酸硝酸盐可溶只有钾钠铵钾钠铵盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
常见物质溶解性及颜色

常见物质的溶解性及颜色硝酸HNO3溶、挥无色氯化氢HCl 溶、挥无色硫酸H2SO4 溶无色碳酸H2CO3溶、挥无色一水合氨NH3.H2O 溶、挥无色硝酸铵NH4NO3溶无色氯化铵NH4Cl 溶无色硫酸铵(NH4)2SO4溶无色碳酸氨(NH4)2CO3溶无色氢氧化钾KOH 溶无色硝酸钾KNO3溶无色氯化钾KCL 溶无色硫酸钾K2SO4溶无色碳酸钾K2CO3溶无色氢氧化钠NaOH 溶无色硝酸钠NaNO3溶无色氯化钠NaCl 溶无色硫酸钠Na2SO4溶无色碳酸钠Na2CO3 溶无色氢氧化钡Ba(OH)2溶无色硝酸钡Ba(NO3)2溶无色硫酸钡BaSO4溶白色碳酸钡BaCO3不白色氢氧化钙Ca(OH)2微无色、白色硝酸钙Ca(NO3)2溶无色氯化钙CaCl2溶无色硫酸钙CaSO4微无色、白色碳酸钙CaCO3不白色氢氧化镁Mg(OH)2不白色硝酸镁Mg(NO3)2溶无色氯化镁MgCl2溶无色硫酸镁MgSO4溶无色碳酸镁MgCO3微无色、白色氢氧化铝Al(OH)3不白色硝酸铝Al(NO3)3溶无色氯化铝AlCl3溶无色硫酸铝Al2(SO4)3溶无色碳酸铝/氢氧化锰Mn(OH)2不白色硝酸锰Mn(NO3)2溶无色氯化锰MnCl2溶无色硫酸锰MnSO4溶无色碳酸锰MnCO3不白色氢氧化锌Zn(OH)2不白色硝酸锌Zn(NO3)2溶无色氯化锌ZnCl2溶无色硫酸锌ZnSO4溶无色碳酸锌ZnCO3不白色氢氧化亚铁Fe(OH)2不白色硝酸亚铁Fe(NO3)2溶浅绿色氯化亚铁FeCl2溶浅绿色硫酸亚铁FeSO4溶浅绿色碳酸亚铁FeCO3不白色氢氧化铁Fe(OH)3不红褐色硝酸铁Fe(NO3)3溶黄色氯化铁FeCl3溶黄色硫酸铁Fe2(SO4)3溶黄色碳酸铁/氢氧化铜Cu(OH)2不蓝色硝酸铜Cu(NO3)2溶蓝色氯化铜CuCl2溶蓝绿色硫酸铜CuSO4溶蓝色碳酸铜CuCO3不蓝色氢氧化银/硝酸银AgNO3溶无色氯化银AgCl 不白色硫酸银Ag2SO4微无色、白色碳酸银Ag2CO3不白色。
高中化学沉淀表

高中化学沉淀表是一份记录高中化学常见沉淀物质及其颜色的表格。
沉淀是指在化学反应过程中,由于生成的化合物在溶液中溶解度较小,会以固体形式从溶液中析出。
高中化学常见沉淀的颜色和生成物质:
1.红色沉淀:
铜(Cu):生成的沉淀通常是暗红色。
氧化亚铜(Cu2O):红色沉淀。
红磷(P):暗红色固体。
三氧化二铁(Fe2O3):红棕色固体,也称为铁锈。
氢氧化铁(Fe(OH)3):红褐色沉淀。
2.黄色沉淀:
磷酸铜(Cu3(PO4)2):黄色沉淀,但不常见。
硫磺(S):淡黄色固体。
过氧化钠(Na2O2):淡黄色固体。
溴化银(AgBr):浅黄色沉淀。
3.蓝色沉淀:
五水硫酸铜(CuSO4·5H2O),也称为胆矾或蓝矾:蓝色晶体。
氢氧化铜(Cu(OH)2):蓝色沉淀。
4.绿色沉淀:
七水硫酸亚铁(FeSO4·7H2O):绿色晶体。
碱式碳酸铜(Cu2(OH)2CO3):绿色沉淀。
5.白色沉淀:
碳酸钙(CaCO3)和硫酸钡(BaSO4)等。
其中,碳酸钙会伴有二氧化碳(CO2)生成。
6.红褐色沉淀:
氢氧化铁(Fe(OH)3)和氢氧化亚铁(Fe(OH)2)在空气中氧化后的颜色。
7.黑色沉淀:
氧化铜(CuO)、二氧化锰(MnO2)、硫化亚铁(FeS)和硫化铜(CuS)等。
注意:沉淀的颜色可能会受到溶液pH、浓度以及存在其他离子的影响,实际观察到的颜色可能有所不同。
高中化学常见的沉淀与离子的颜色

高中常见沉淀离子的颜色红色Fe(SCN)]2+( 血红色);Cu2O( 砖红色);Fe2O3( 红棕色);红磷(红棕色);液溴(深红棕色 );Fe(OH)3( 红褐色 );I2 的 CCl4 溶液 (紫红色 );MnO4-( 紫红色 );Cu( 紫红色 ); 在空气中久置的苯酚 (粉红色 ).2.橙色 :溴水 ;K2Cr2O7 溶液 .3.黄色 :AgI( 黄色 );AgBr( 浅黄色 );K2CrO4( 黄色 );Na2O2( 淡黄色 );S( 黄色);FeS2( 黄色 );久置浓 HNO3( 溶有 NO2); 工业浓盐酸 (含 Fe3+);Fe3+ 水溶液 (黄色);久置的 KI 溶液 (被氧化成 I2)4.绿色 :Cu2(OH)CO3;Fe2+ 的水溶液 ;FeSO4.7H2O;Cl2( 黄绿色 );F2( 淡黄绿色 );Cr2O35.蓝色 :Cu(OH)2;CuSO4.5H2O;Cu2+的水溶液 ;I2 与淀粉的混合物 .6.紫色 :KMnO4( 紫黑色 );I2(紫黑色 );石蕊 (pH=8--10);Fe3+ 与苯酚的混合物 .7.黑色 :FeO,Fe3O4,FeS,CuS,Cu2S,Ag2S,PbS,CuO,MnO2,C粉.8.白色 :Fe(OH)2,AgOH, 无水CuSO4,Na2O,Na2CO3,NaHCO3,AgCl,BaSO4,CaCO3,CaSO3,Mg(OH)2,Al(OH)3, 三溴苯酚 ,MgO,MgCO3, 绝大部分金属等 .一、单质绝大多数单质:银白色。
Cu 紫红 O2 无 Au 黄 S 黄 B 黄或黑 F2淡黄绿 C(石墨黑 Cl2 黄绿 C(金刚石)无 Br2 红棕 Si 灰黑I2 紫黑H2 无稀有气体无 P 白、黄、红棕。
二、氢化物 LiH 等金属氢化物:白NH3 等非金属氢化物:无三、氧化物大多数非金属氧化物:无主要例外: NO2 棕红 N2O5 和 P2O5 白N2O3 暗蓝 ClO2 黄大多数主族金属的氧化物:白主要例外: Na2O2 浅黄 PbO 黄 K2O 黄Pb3O4 红 K2O2 橙 Rb2O亮黄 Rb2O2 棕 Cs2O 橙红 Cs2O2 黄大多数过渡元素氧化物有颜色 MnO 绿 CuO 黑 MnO2 黑 Ag2O棕黑 FeO 黑 ZnO白Fe3O4 黑 Hg2O 黑 Fe2O3 红棕 HgO 红或黄 Cu2O 红 V2O5 橙四、氧化物的水化物大多数:白色或无色其中酸:无色为主碱:白色为主主要例外: CsOH 亮黄 Fe(OH)3 红褐 HNO2 溶液亮蓝 Cu(OH)2 蓝 Hg(OH)2 桔红五、盐大多数白色或无色主要例外: K2S 棕黄 CuFeS2 黄 KHS 黄 ZnS 白 Al2S3 黄 Ag2S 黑 MnS 浅红 CdS 黄 FeS 黑棕 SnS 棕 FeS2 黄 Sb2S3 黑或橙红 CoS 黑HgS 红 NiS 黑 PbS 黑 CuS 、Cu2S 黑 Bi2S3 黑 FeCl3 ·6H2O 棕黄 Na3P 红FeSO4·9H2O 蓝绿 NaBiO3 黄 Fe2 (SO4 )3·9H2O 棕黄 MnCl2 粉红 Fe3C 灰 MnSO4 淡红 FeCO3 灰 Ag2CO3 黄Fe(SCN )3 暗红 Ag3PO4 黄 CuCl2 棕黄 AgF 黄 CuCl2·7H2O 蓝绿 AgCl白CuSO4 白 AgBr 浅黄 CuSO4· 5H2O 蓝 AgI 黄 Cu2 ( OH)2CO3 暗绿盐溶液中离子特色: NO2- 浅黄 Cu2+ 或 [Cu( H2O) 4]2+ 蓝 MnO4- 紫红[CuCl4]2- 黄 MnO42- 绿 [Cu( NH3 )4]2+ 深蓝 Cr2O72- 橙红 Fe2+ 浅绿 CrO42-黄 Fe3+ 棕黄非金属互化物 PCl3 无 XeF2 、 XeF4 、XeF6 无 PCl5浅黄氯水黄绿 CCl4 无溴水黄—橙 CS2 无碘水黄褐 SiC 无或黑溴的有机溶液橙红—红棕SiF4无I2的有机溶液紫红六.其它甲基橙橙 CXHY(烃)、CXHYOZ无(有些固体白色)石蕊试液紫大多数卤代烃无(有些固体白色)石蕊试纸蓝或红果糖无石蕊遇酸变红葡萄糖白石蕊遇碱变蓝蔗糖无酚酞无麦芽糖白酚酞遇碱红淀粉白蛋白质遇浓 HNO3 变黄纤维素白 I2 遇淀粉变蓝 TNT 淡黄 Fe3+ 遇酚酞溶液紫焰色反应 Li 紫红 Ca 砖红 Na 黄 Sr 洋红 K 浅紫(通过蓝色钴玻璃) Ba 黄绿 Rb 紫Cu 绿稀有气体放电颜色 He 粉红 Ne 鲜红 Ar 紫。
溶解性口诀及常见物质颜色

钾钠铵硝都 易溶, 还有碳酸镁微溶, 碳酸磷酸盐, 硫酸钙 ( CaSO4 )
氯化物中银不溶, 溶碱有五位, 只溶钾钠铵。 硫酸银 ( Ag2SO4 )
硫酸钡不钙银微,
钾钠氨钙钡,
四微溶:氢氧化钙 ( Ca(OH)2 ) 碳酸镁 ( MgCO3 )
常见固体颜色
1、黑色固体:铁粉、木炭、Fe3O4、CuO、MnO2、FeO 2、绿色固体:Cu2(OH)2CO3 3、紫黑色固体:KMnO4、I2 4、红色固体:Cu、Fe2O3、HgO、Cu2O(氧化亚铜,砖红色) 5、蓝色固体:Cu(OH)2、CuSO4·5H2O(胆矾,五水硫酸铜) 6、淡黄色固体:S(硫磺) 7、银白色固体:铁丝(铁片…)、Mg、Al、Ag、Zn… 8、白色固体:MgO、CaCO3、P2O5、CuSO4(无水硫酸铜)、 NaCl、……
01
蓝色溶液:CuSO4溶液、 Cu(NO3)2溶液、CuCl2
溶液
04
无色溶液:大部ห้องสมุดไป่ตู้溶液
02
浅绿色溶液:FeSO4溶液 、FeCl2溶液
05
I2 遇淀粉→蓝色溶液
03
黄色溶液:Fe2(SO4)3溶 液、FeCl3溶液
06
常见液体颜色
高中化学沉淀表背诵口诀

高中化学沉淀表背诵口诀高中化学沉淀记忆口诀:口诀1:酸类大多都可溶,铵钾钠钡碱可溶。
钾钠铵盐全都溶,氯化物只银不溶。
硫酸铅钡不怕水,硝酸银见水影无踪。
口诀2:钾钠铵盐水中溶,硝酸盐入水无影踪。
氯化物中除去银亚汞,硫酸盐中除去钡铅都可溶。
若问碳酸磷酸其他盐,钾钠铵外都不溶。
常见沉淀:Cu(OH)2蓝色沉淀CuO黑色沉淀Cu2O红色沉淀Cu2(OH)2CO3暗绿色沉淀CaCO3白色沉淀(且有CO2生成)Fe(OH)3红褐色沉淀Fe(OH)2为白色絮状沉淀(在空气中很快变成灰绿色,再变成Fe(OH)3红褐色沉淀)Fe2O3红棕色沉淀FeO黑色沉淀、FeCO3灰色沉淀FeS2黄色沉淀AgBr淡黄色沉淀Ag2CO3黄色沉淀AgCl白色沉淀AgI ,Ag3PO4黄色沉淀PbS黑色沉淀BaCO3白色沉淀(且有CO2生成)BaSO4白色沉淀不溶的碳酸盐白色沉淀(且有CO2生成)不溶的碱、金属氧化物白色沉淀(且有CO2生成)常见的高中化学沉淀口诀:物质溶解性口诀钾钠铵盐硝酸盐,完全溶解不困难,氯化亚汞氯化银,硫酸钡和硫酸铅。
生成沉淀记心间,氢硫酸盐和碱类,碳酸磷酸硝酸盐,可溶只有钾钠铵。
常见的高中化学沉淀口诀:溶解性的口诀钾钠铵硝溶得全,没有不溶水的盐。
氯化物,要记住,只有银是不溶物。
硫酸盐,溶得多,只有钡在水中搁。
碳磷酸盐很简单,溶于水的钾钠铵。
常见的高中化学沉淀口诀:常见物质溶解钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
) 其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)常见的高中化学沉淀口诀:酸的溶解性酸的溶解性:除了硅酸都可溶.碱的溶解性:碱中溶的有五位,钾钠还有氨钙钡.(氢氧化钙微溶)盐的溶解性:钾钠铵硝醋可溶,盐酸(盐)不溶氯化银,硫酸(盐)不溶钡和铅,碳硅磷硫(化)亚硫酸(盐)他们只溶钾钠铵.后两句也可以这样说:其它弱酸盐,只溶钾钠铵微溶物常用的单记:氢氧化钙、硫酸钙、硫酸银、碳酸镁。
高中化学常用物质溶解性表及沉淀颜色(xin)

高中化学常用物质溶解性表及沉淀颜色(xin)高中化学常用物质溶解性表及沉淀颜色钾、钠铵盐都可溶,硝盐遇水影无踪;硫(酸)盐不溶铅和钡,氯(化)物不溶银、亚汞。
氢气应早去晚归,酒精灯迟到早退,试管口下倾水滴。
升失氧,降得还;若说剂,两相反。
无“弱”不水解,谁“弱”谁水解;愈“弱”愈水解,又“弱”剧水解;谁“强”显谁性,双“弱”由K定。
左边水写分子式,中间符号写可逆,右边不写“↑”和“↓”。
钾钠铵盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
④注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅、硫酸钙不溶;③硝酸盐都溶于水;④口诀中没有涉及的盐类都不溶于水;钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
钾钠铵盐硝酸盐完全溶解不困难氯化亚汞氯化银硫酸钡和硫酸铅生成沉淀记心间氢硫酸盐和碱类碳酸磷酸硝酸盐可溶只有钾钠铵钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
高中化学必背沉淀表

高中化学必背沉淀表八大沉淀是: AgCl , BaSO 4 ,CaCO 3, BaCO 3, Al (OH) 3 和 Mg (OH) 2 为白色沉淀,Cu (OH) 2 为蓝色絮状沉淀, Fe (OH) 3 为红褐色沉淀。
在化学变化中,一般来说有八大沉淀。
其中氯化银和硫酸钡不溶于酸,其它六大沉淀都溶于酸。
碳酸钙,碳酸钡,氯化银,氢氧化镁,氢氧化铝,硫酸钡为白色物理性质其中,AgCl , BaSO4,CaCO3, BaCO3, Al(OH)3 和 Mg(OH)2为白色沉淀,Cu(OH)2为蓝色絮状沉淀, Fe(OH)3为红褐色沉淀。
化学性质氯化银和硫酸钡不溶于酸,碳酸钙和碳酸钡溶于酸有气泡,氢氧化镁、氢氧化铝、氢氧化铁和氢氧化铜溶于酸无气泡。
沉淀通常存在于复分解反应中。
例如,氢氧化铜通常由硫酸铜和氢氧化钠反应生成.Fe(OH)3 氢氧化铁,红褐色沉淀。
化学方程式可溶性碱和铁盐溶液反应,例如氢氧化钠和硫酸铁反应生成氢氧化铁和硫酸钠:6NaOH+Fe2(SO4)3==2Fe(OH)3↓+3Na2SO44Fe(OH)2+O2+2H2O==4Fe(OH)32Fe(OH)3=△=Fe2O3+3H2O2.Cu(OH)2 氢氧化铜,蓝色沉淀。
化学方程式CuSO4+2NaOH==Na2SO4+Cu(OH)2↓CuCl2+2CaOH==Cu(OH)2↓+2CaClCuSO4+Ca(OH)2==Cu(OH)2↓+CaSO43.CaCO3碳酸钙,白色沉淀。
化学方程式Ca(OH)2+CO2==CaCO3↓+H2O4.BaCO3 碳酸钡,白色沉淀。
化学方程式Na2CO3+BaCl2==2NaCl+BaCO3↓5.&6.AgCl 氯化银,白色沉淀。
BaSO4 硫酸钡,白色沉淀。
这两种沉淀既不溶于水,也不溶于酸!化学方程式Ag2SO4+BaCl2==2AgCl↓+BaSO4↓7.Mg(OH)2氢氧化镁,白色沉淀。
化学方程式MgCl2+Ca(OH)2==CaCl2+Mg(OH)2↓8.Ag2CO3碳酸银,白色沉淀。
化学物质溶解度表及常见物质颜色
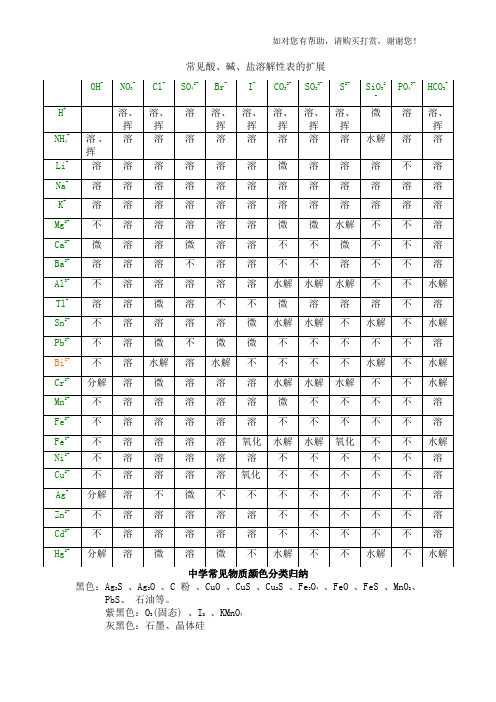
常见酸、碱、盐溶解性表的扩展黑色:Ag2S 、Ag2O 、C粉、CuO 、CuS 、Cu2S 、Fe3O4、FeO 、FeS 、MnO2、PbS、石油等。
紫黑色:O3(固态) 、I2、KMnO4灰黑色:石墨、晶体硅灰色:As 、Fe3C 、Se、Sn 银灰色:Ge白色:AgCl 、AgOH 、Al(OH)3、 Al2O3、BaCO3、BaSO4、CaCO3、CaSO3、无水CuSO4、Fe(OH)2、Fe(略带灰色) 、KClO3、 KCl 、K2SO4、MgO、Mg(OH)2、MgCO3、 NH4HCO3、 NH4NO3、(NH4)2SO4、Na2O、 NaOH、Na2CO3、NaHCO3、 P2O5、P 4(白磷)、 ZnSO4、C6H12O6(葡萄糖)、 (C6H10O5)n(淀粉)、 (C6H10O5)n(纤维素)、三溴苯酚等。
银白色:K、 Na、 Mg、 Al、 Sn 、Sb 、Bi 、Te 、Ti 、Hg 、Li 、Rb、Cs(略带金色)等。
青白色:Zn蓝白色:Pb红色:[FeSCN]2+(血红色) 、Cu2O(砖红色)红棕色:P(红磷)、NO2、Fe2O3紫红色:Cu 、MnO4-红褐色:Fe(OH)3、碘酒(褐色)深红棕色:Br2黄色:AgI 、P4(黄磷) 、Au 、Ag3PO4、FeS2、Al2S3、K2CrO4淡黄色:Na2O2、AgBr 、TNT 、S、PCl5、混有NO2的浓HNO3、混有Fe3+的浓HCl、溶有NO2的硝基苯灰黄色:Mg3N 2棕黄色:FeCl3、CuCl2橙色:溴水、K2Cr2O7溶液绿色:Cu(OH)2CO3、 Cr2O3浅绿色:Fe2+、FeSO4·7H2O黄绿色:Cl2浅黄绿色:氯水、F2蓝色:CuSO4·5H2O 、Cu(OH)2、Cu2+的稀溶液淡蓝色:O3(气体)深蓝色:O3(液态)常见与Cu有关的颜色:Cu紫红色; Cu2O红色; CuO黑色;CuF2白色; CuCl2黄棕色; CuBr2棕黑色;CuI白色; Cu(OH)2淡蓝色; Cu2S黑色;CuS黑色; CuSO4·5H2O蓝色;无水CuSO4白色;含Cu2+溶液:浓度很浓显黄绿色,浓度浓显绿色,浓度稀显蓝色。
化学——物质颜色状态及溶解性

常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、 NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3 、HgO、红磷▲硫:淡黄色▲ Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸) AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2 红褐色↓:Fe(OH)3白色↓:其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
酒精为有特殊气体的液体。
7、有毒的,气体:CO 液体:CH3OH 固体:NaNO2 CuSO4(可作杀菌剂 ,与熟石灰混合配成天蓝色的粘稠状物质——波尔多液)物质的溶解性1、盐的溶解性含有钾、钠、硝酸根、铵根的物质都溶于水含Cl的化合物只有AgCl不溶于水,其他都溶于水;含SO42-的化合物只有BaSO4 不溶于水,其他都溶于水。
含CO32-的物质只有K2CO3、Na2CO3、(NH4)2CO3溶于水,其他都不溶于水2、碱的溶解性溶于水的碱有:氢氧化钡、氢氧化钾、氢氧化钙、氢氧化钠和氨水,其他碱不溶于水。
难溶性碱中Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色沉淀,其他难溶性碱为白色。
(包括Fe(OH)2)注意:沉淀物中AgCl和BaSO4 不溶于稀硝酸,其他沉淀物能溶于酸。
如:Mg(OH)2 CaCO3 BaCO3 Ag2 CO3 等3、大部分酸及酸性氧化物能溶于水,(酸性氧化物+水→酸)大部分碱性氧化物不溶于水,能溶的有:氧化钡、氧化钾、氧化钙、氧化钠(碱性氧化物+水→碱)俗名(1)金刚石、石墨:C(2)水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3(7)氢硫酸:H2S(8)熟石灰、消石灰:Ca(OH)2(9)苛性钠、火碱、烧碱:NaOH(10)纯碱:Na2CO3 碳酸钠晶体、纯碱晶体:Na2CO3•10H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4•5H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH(CH3COO- 醋酸根离子)具有酸的通性(17)氨气:NH3 (碱性气体)(18)氨水、一水合氨:NH3•H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2 (工业用盐、有毒)。
高中化学沉淀表必背

高中化学沉淀表必背在高中化学的学习中,沉淀表是一个非常重要的知识点,它对于我们理解化学反应、判断物质的溶解性以及进行化学实验和解题都有着至关重要的作用。
下面,就让我们一起来详细了解一下高中化学中必背的沉淀表。
首先,我们来看看常见的阳离子与阴离子结合形成的沉淀。
一、银离子(Ag⁺)1、与氯离子(Cl⁻)结合形成氯化银(AgCl)沉淀,这是一种白色沉淀,且不溶于稀硝酸。
2、与溴离子(Br⁻)结合形成溴化银(AgBr)沉淀,为浅黄色沉淀,同样不溶于稀硝酸。
3、与碘离子(I⁻)结合形成碘化银(AgI)沉淀,是黄色沉淀,也不溶于稀硝酸。
二、钡离子(Ba²⁺)1、与硫酸根离子(SO₄²⁻)结合形成硫酸钡(BaSO₄)沉淀,白色,不溶于稀硝酸。
三、钙离子(Ca²⁺)1、与碳酸根离子(CO₃²⁻)结合形成碳酸钙(CaCO₃)沉淀,白色。
四、镁离子(Mg²⁺)1、与氢氧根离子(OH⁻)结合形成氢氧化镁(Mg(OH)₂)沉淀,白色。
五、铝离子(Al³⁺)1、与氢氧根离子(OH⁻)结合的情况较为复杂。
当氢氧根离子少量时,生成氢氧化铝(Al(OH)₃)沉淀,白色。
当氢氧根离子过量时,氢氧化铝沉淀会溶解,生成偏铝酸根离子(AlO₂⁻)。
六、铜离子(Cu²⁺)1、与氢氧根离子(OH⁻)结合形成氢氧化铜(Cu(OH)₂)沉淀,蓝色。
七、铁离子(Fe³⁺)1、与氢氧根离子(OH⁻)结合形成氢氧化铁(Fe(OH)₃)沉淀,红褐色。
八、亚铁离子(Fe²⁺)1、与氢氧根离子(OH⁻)结合形成氢氧化亚铁(Fe(OH)₂)沉淀,白色,但在空气中容易被氧化成氢氧化铁,颜色逐渐变为灰绿色最终变为红褐色。
接下来,我们了解一下这些沉淀的溶解性规律。
一般来说,硝酸盐、钠盐、钾盐、铵盐等都是可溶的。
而碳酸盐中,除了碳酸钠、碳酸钾、碳酸铵可溶,其余大多不溶。
硫酸盐中,硫酸钡不溶,硫酸钙和硫酸银微溶,其余大多可溶。
化合价及物质溶解性,颜色

熟记常见物质的颜色:
1、红色固体:Cu、Fe2O3 、P(红磷)
2、黑色固体:C、CuO、Fe3O4、MnO2 、铁粉、KMnO4 (紫黑色固体)
3、白色固体: CuSO4(无水硫酸铜)、Na2CO3、NaCl、CaCO3 、Mg(OH)2、 Al (OH)3 、BaSO
4、AgCl 、BaCO3 、生石灰、熟石灰等
4、蓝色固体:CuSO4·5H2O 蓝色絮状沉淀:Cu(OH)2 蓝色溶液: CuSO4、CuCl2、Cu(NO3)2等Cu2+溶液
5、黄色的溶液:FeCl3、Fe2(SO4)3、Fe(NO3)3等Fe3+溶液
6、红褐色沉淀:Fe(OH)3
7、浅绿色的溶液:FeSO4、FeCl2等Fe2+溶液
8、黄色的固体:S
化合价口诀(熟记)
钾钠银氢正一价,氟氯溴碘负一价;
钙镁钡锌正二价,通常氧是负二价;
二三铁,二四碳,三铝四硅五价磷;
一三五七正价氯,二四六硫锰四七;
铜汞二价最常见,单质化合价为零。
负一硝酸氢氧根,负二碳酸硫酸根;
还有负三磷酸根,只有正一是铵根。
可溶物与不溶物的记忆口诀
钾钠铵盐均可溶;硝盐入水影无踪
硫酸盐中钡不溶;氯化盐中银不溶;
碳酸盐中只溶钾、钠、铵;
碱只溶钾钠钙钡铵。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学常用物质溶解性表及沉淀颜色
钾、钠铵盐都可溶,
硝盐遇水影无踪;
硫(酸)盐不溶铅和钡,
氯(化)物不溶银、亚汞。
氢气应早去晚归,酒精灯迟到早退,试管口下倾水滴。
升失氧,降得还;若说剂,两相反。
无“弱”不水解,谁“弱”谁水解;愈“弱”愈水解,
又“弱”剧水解;谁“强”显谁性,双“弱”由K定。
左边水写分子式,中间符号写可逆,右边不写“↑”和“↓”。
钾钠铵盐溶水快,①
硫酸盐除去钡铅钙。
②
氯化物不溶氯化银,
硝酸盐溶液都透明。
③
口诀中未有皆下沉。
④
注:
①钾钠铵盐都溶于水;
②硫酸盐中只有硫酸钡、硫酸铅、硫酸钙不溶;
③硝酸盐都溶于水;
④口诀中没有涉及的盐类都不溶于水;
钾、钠、铵盐、硝酸盐;
氯化物除银、亚汞;
硫酸盐除钡和铅;
碳酸、磷酸盐,只溶钾、钠、铵。
说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
钾钠铵硝皆可溶、盐酸盐不溶银亚汞;
硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶
钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)
盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)
再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)
只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)
最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)
另有几种微溶物,可单独记住。
钾钠铵盐硝酸盐
完全溶解不困难
氯化亚汞氯化银
硫酸钡和硫酸铅
生成沉淀记心间
氢硫酸盐和碱类
碳酸磷酸硝酸盐
可溶只有钾钠铵
钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)
盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)
再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)
其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)
只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)
最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)
另有几种微溶物,可单独记住
高中化学常用物质溶解性表及沉淀颜色Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解溶液呈黄色铁器除锈
Al2O3+3H2SO4= Al2(SO4)3+3H2O 白色固体溶解
CuO+H2SO4=CuSO4+H2O 黑色固体溶解溶液呈蓝色
ZnO+H2SO4=ZnSO4+H2O 白色固体溶解
MgO+H2SO4=MgSO4+H2O 白色固体溶解
2NaOH+H2SO4=Na2SO4+2H2O
Cu(OH)2+H2SO4=CuSO4+2H2O 蓝色固体溶解
Ca(OH)2+H2SO4=CaSO4+2H2O
Mg(OH)2+H2SO4=MgSO4+2H2O 白色固体溶解
2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O 白色固体溶解
2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O 红褐色沉淀溶解溶液呈黄色
Ba(OH)2+ H2SO4=BaSO4+2H2O 生成白色沉淀不溶解于稀硝酸检验SO42的原理BaCl2+ H2SO4=BaSO4+2HCl 生成白色沉淀不溶解于稀硝酸检验SO42的原理Ba(NO3)2+H2SO4=BaSO4+2HNO3 生成白色沉淀不溶解于稀硝酸检验SO42的原
理
Na2O+2HNO3=2NaNO3+H2O 白色固体溶解
CuO+2HNO3=Cu(NO3)2+H2O 黑色固体溶解溶液呈蓝色
ZnO+2HNO3=Zn(NO3)2+ H2O 白色固体溶解
MgO+2HNO3=Mg(NO3)2+ H2O 白色固体溶解
CaO+2HNO3=Ca(NO3)2+ H2O 白色固体溶解
NaOH+HNO3=NaNO3+ H2O
Cu(OH)2+2HNO3=Cu(NO3)2+2H2O 蓝色固体溶解
Mg(OH)2+2HNO3=Mg(NO3)2+2H2O 白色固体溶解
Al(OH)3+3HNO3=Al(NO3)3+3H2O 白色固体溶解
Ca(OH)2+2HNO3=Ca(NO3)2+2H2O
Fe(OH)3+3HNO3=Fe(NO3)3+3H2O 红褐色沉淀溶解溶液呈黄色
3NaOH + H3PO4=3H2O + Na3PO4
3NH3+H3PO4=(NH4)3PO4
2NaOH+CO2=Na2CO3+ H2O 吸收COO2H2中的CO2
2NaOH+SO2=Na2SO3+ H2O 2NaOH+SO3=Na2SO4+ H2O 处理硫酸工厂的尾气
(SO2)
FeCl3+3NaOH=Fe(OH)3+3NaCl 溶液黄色褪去有红褐色沉淀生成。
