水的电离及影响因素-高考化学解答题大题练习
天津高考化学复习练习题 水的电离和溶液的pH

天津高考化学专项训练水的电离和溶液的pH 基础题1.下列说法正确的是( )A.水的电离方程式:H2O===H++OH-B.pH=7的溶液一定是中性溶液C.升高温度,水的电离程度增大D.将稀醋酸加水稀释时,c(H+)减小,c(OH-)也减小解析:A.水是弱电解质,电离方程式应该使用可逆号,电离的方程式应为H2O H++OH-,错误;B.若溶液的温度不是室温,则pH=7的溶液不一定是中性溶液,错误;C.水是弱电解质,电离吸收热量,所以升高温度,水的电离程度增大,正确;D.将稀醋酸加水稀释时,c(H+)减小,由于存在水的电离平衡,所以c(OH-)增大,错误。
答案:C2.已知常温下水的离子积常数K w=1.0×10-14,在100 ℃时水的离子积常数K′w=1.0×10-12。
将常温下的下列溶液加热至90 ℃(忽略溶液体积变化),溶液的pH不变的是( )A.硫酸钠溶液B.稀硫酸溶液C.氢氧化钠溶液 D.盐酸的浓溶液解析:由题目提供的不同温度下水的离子积常数K w和K′w可知,温度升高时水的离子积常数增大。
A选项错误,硫酸钠不会破坏水的电离,但升温时,水的电离程度增大,溶液的pH减小;B选项正确,决定溶液pH的因素是硫酸完全电离产生的c(H+),它不会随温度变化而变化;C选项错误,升温时,氢氧化钠溶液中c(OH-)不会变化,但由于水的离子积常数增大,所以c(H+)增大,溶液的pH减小;D选项错误,因为加热盐酸的浓溶液时,会有大量HCl气体逸出,c(H+)减小,溶液的pH增大。
答案:B3.25 ℃时,水的电离达到平衡:H2O H++OH-。
下列叙述错误的是( )A.向水中通入氨气,平衡逆向移动,c(OH-)增大B.向水中加入少量稀硫酸,c(H+)增大,K w不变C.将水加热平衡正向移动,K w变大D.升高温度,平衡正向移动,c(H+)增大,pH不变解析:向水中通入NH3,c(OH-)增大,平衡左移,A正确;向水中加入少量稀H2SO4,c(H +)增大,但温度不变,KK w变大,C正w不变,B正确;将水加热,水的电离平衡正向移动,确;升高温度,能促进水的电离,c(H+)增大,pH减小,D错误。
高一化学水的电离和溶液的酸碱性试题答案及解析

高一化学水的电离和溶液的酸碱性试题答案及解析1.将等物质的量浓度、等体积的硫酸与烧碱溶液混合后,滴入紫色石蕊试液,溶液呈( ) A.紫色B.红色C.蓝色D.无色【答案】B【解析】硫酸和氢氧化钠反应的方程式为:H2SO4+2NaOH=Na2SO4+2H2O. 等物质的量浓度、等体积的硫酸与烧碱溶即硫酸和氢氧化钠的物质的量相等。
由于反应是二者的物质的量的比是1:2,所以硫酸过量。
反应后溶液呈酸性。
滴入紫色石蕊试液溶液变为红色。
选项为:B。
【考点】考查酸碱混合后溶液的酸碱性的问题。
2.测定石灰石中钙元素的质量百分含量时,都是先把钙元素全部转化为草酸钙沉淀 (CaC2O4・H2O),然后将草酸钙沉淀 (CaC2O4・H2O),用硫酸溶解,用a mol/L的标准高锰酸钾溶液滴定生成的草酸,发生化学反应:H2C2O4+ MnO4- + H+→ Mn2+ + CO2 ↑+ H2O(未配平)。
(1)配平后离子方程式的系数依次为、、、、、。
(2)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、250mL容量瓶外,还需。
(3)上述实验中的KMnO4溶液需要酸化,不能使用盐酸酸化的原因是。
(4)开始取用样品的质量为m g,硫酸溶解后所得草酸溶液的体积为100mL,每次取25.00mL进行滴定,达到滴定终点时所耗KMnO4溶液体积为 b mL,所得草酸溶液的物质的量的浓度是;石灰石中钙元素的质量百分含量为。
(相对原子质量:Ca—40)【答案】(19分)(1)5、2、6、2、10、8 (4分)(2)胶头滴管量筒(4分)(3)KMnO4会把Cl-氧化而损耗(3分)(4)0.1ab mol/L; 40ab/m %或0.4ab/m×100%(8分)【解析】(1)根据方程式可知,在反应中碳元素的化合价从+3价升高到+4价,失去1个电子,则1mol草酸失去2mol电子。
重难点09 水的电离与溶液的酸碱性-2023年高考化学专练(解析版)

重难点09 水的电离与溶液的酸碱性1.水的电离(1) 水的电离是吸热反应,常温时水的离子积K w=10-14,100℃时,K w=10-12。
(2) 不能把10-7作为判断一切溶液酸、碱性的分界线,应比较c(H+)和c(OH-)的大小。
(3) 已知水的c(H+)或c(OH-),并不能确定溶液的酸碱性。
(4) 水的电离平衡与影响因素①酸、碱可以打破水的电离平衡,促使水的电离平衡逆向移动,造成c(H+)≠c(OH-),αw下降。
溶液的pH表示的c(H+)为溶质酸的,通过水的离子积(K w) 的公式计算出水电离的c(OH-)w,c(H+)w=c(OH-)w。
碱溶液的pH表示的c(H+)则为水电离出的c(H+)w,因为碱本身不含有H+。
增大。
只有②能水解的盐可以打破水的电离平衡,促使水的电离平衡正向移动,αw 一种弱离子水解,则c(H+)≠c(OH-);若双水解,则可能相等,也可能不相等。
水解呈酸性的盐溶液的pH与酸溶液相同,水解呈碱性的盐溶液的pH与碱溶液相同。
增大,K w增③温度可以影响水的电离平衡。
温度升高,水的电离平衡向右移动,αw 大,pH降低,但c(H+)=c(OH-)。
2.溶液的pH定义:pH=-lg{c(H+)},通常的使用范围0~14,pH变化1个单位,则c(H+)变化10倍。
(1) pH─c(H+)─酸性─碱性─c(OH-)的关系;(2) 两溶液的pH相差n个单位,则c(H+)和c(OH-)相差10n倍(3) 酸、碱溶液稀释时,pH与c(H+)或c(OH-)的关系;酸、碱溶液稀释后的pH计算:若把已知pH的酸或碱溶液稀释n倍,① 强酸、强碱溶液的pH=原pH±lg n(酸为“+”,碱为“-”)① 弱酸、弱碱溶液的pH=原pH±lg n(酸为“+”,碱为“-”)一般情况下,强酸溶液稀释10倍,溶液的pH增大1;而弱酸溶液稀释10倍后,其pH只增大0.5左右。
① 当用水稀释溶液并求溶液的pH时,如强酸溶液的c(H+)远远大于纯水的c(H+),水的氢离子浓度可以忽略不计。
考点44 水的电离——备战2021年高考化学一轮复习考点一遍过(教师版含解析)

考点44 水的电离一、水的电离1.水的电离平衡水是一种极弱的电解质,能发生微弱的电离。
2.水的离子积常数(1)概念:在一定温度下,c(H+)与c(OH−)的乘积是一个常数,称为水的离子积常数,简称水的离子积。
(2)表达式:水的离子积用K w表示。
实验测得,25 ℃时,1 L水中只有1.0×10−7 mol H2O电离。
所以该温度时的纯水中c(H+)=c(OH−)=1.0×10−7 mol·L−1,K w=c(H+)·c(OH−)=1.0×10−14,室温下K w一般也取这个值。
(3)影响因素:K w只与温度有关。
温度升高,K w增大。
注意事项(1)水的离子积不仅适用于纯水,也适用于稀的电解质水溶液。
(2)在室温时,任何物质的水溶液,K w=10−14。
K w与溶液的酸碱性无关,只与温度有关。
(3)K w的重要应用在于溶液中c(H+)和c(OH−)的换算。
(4)外界条件改变,水的电离平衡发生移动,但任何时候水电离出的c(H+)和c(OH−)总是相等的。
二、c(H+)与c(OH-)的反比关系图像(1)A、B线表示的温度A<B。
(2)a、b、c三点表示溶液的性质分别为中性、酸性、碱性。
提醒:(1)曲线上的任意点的K w都相同,即c(H+)·c(OH-)相同,温度相同;(2)实现曲线上点之间的转化需保持温度不变,改变酸碱性;实现曲线上点与曲线外点之间的转化一定改变温度。
三、水的电离平衡的影响因素和有关计算1.外界因素对水电离的影响改变条件电离平衡溶液中c(H+) 溶液中c(OH−)pH溶液的酸碱性K W升高温度右移增大增大减小中性增大加入酸、碱加入酸,如稀硫酸、醋酸左移增大减小减小酸性不变加入碱,如NaOH溶液、氨水左移减小增大增大碱性不变加入盐加入强碱弱酸盐,如Na2CO3溶液右移减小增大增大碱性不变加入强酸弱碱盐,如AlCl3溶液右移增大减小减小酸性不变加入强酸强碱盐,如NaCl溶液不移动不变不变不变中性不变加入活泼金属如Na 右移减小增大增大碱性不变2.水电离出的c(H+)或c(OH−)的计算(25 ℃时)(1)中性溶液c(OH−)=c(H+)=10−7 mol·L−1(2)酸溶液--(H )(H )(H )(OH )(OH )(H )c c c c c c ++++⎧=+⎪⎨⎪==⎩酸水水水酸溶液中,H +来源于酸的电离和水的电离,而OH −只来源于水的电离。
高考化学 备考校小题精练 水的电离及影响因素试题

冠夺市安全阳光实验学校专题36 水的电离及影响因素(满分42分时间20分钟)_____________________________________________1.常温下,水存在H2O H++OH--Q的平衡,下列叙述一定正确的是A.向水中滴入少量稀盐酸,平衡逆向移动,K w减小B.将水加热,K w增大,pH减小C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低D.向水中加入少量固体NH4Cl,c(H+)=10-7mol/L,K w不变【答案】B【解析】点睛:水的电离是吸热过程,水的离子积常数只与温度有关,温度升高,水的离子积变大。
酸和碱可以抑制水的电离,能水解的盐通常都能促进水的电离。
2.下列微粒中不能破坏水的电离平衡的是()A. H+ B. OH- C. S2- D. Na+【答案】D【解析】【详解】A.加入氢离子,水中氢离子浓度增大,抑制了水的电离,故A不选;B.加入氢氧根离子,水中氢氧根离子浓度增大,抑制了水的电离,故B不选;C.加入硫离子,硫离子结合水电离的氢离子,氢离子浓度减小,促进了水的电离,故C不选;D.加入钠离子,钠离子不水解,不影响水的电离平衡,故D选;故选D。
3.常温下,在由水电离产生的H+浓度为1×10-13mol·L-1的溶液中,一定能大量共存的离子组是①K+、Cl-、NO3-、S2-②K+、Fe2+、I-、SO42-③Na+、Cl-、NO3-、SO42-④Na+、Ca2+、Cl-、HCO3-⑤K+、Ba2+、Cl-、NO3-A.①③ B.③⑤ C.④⑤ D.②⑤【答案】B【解析】【分析】常温下,由水电离产生的H+浓度为1×10-13mol·L-1,小于1×10-7mol/L,说明水的电离受到抑制,所以,溶液可能为酸溶液或碱溶液,再根据离子反应发生的条件分析。
【详解】【点睛】离子反应发生的条件有(1)有难溶物质生成;(2)有挥发性物质生成;(3)有水等弱电解质生成;(4)有氧化还原反应发生;(5)有相互促进的水解反应发生;(6)有络离子产生等,只要符合上述条件之一,离子反应即可发生。
2022届高考化学一轮复习常考题型41水的电离及离子积常数含解析

水的电离及离子积常数一、单选题(共14题)1.在某温度时,测得纯水中的c (H +)=2.4×10-7mol·L -1,则c (OH -)为 A .2.4×10-7mol·L -1B .0.1×10-7mol·L -1C .771.0102.410--⨯⨯mol·L -1 D .无法确定2.最近《科学》杂志评出10大科技突破,其中“火星上找到水的影子”名列第一、下列关于水的说法中正确的是 A .水的电离过程需要通电B .加入电解质一定会破坏水的电离平衡C .pH=7的水一定呈中性D .升高温度,纯水的pH 值变小 3.下列说法正确的是A .常温下,pH=1的稀硫酸中c(OH -)=10-13mol/LB .常温下,pH=5的NH 4Cl 溶液、NH 4HSO 4溶液中,c(NH +4)后者大C .常温下,向水中加少量醋酸铵固体,pH 保持7不变,说明水的电离平衡没有移动D .常温下,将0.1mol/L 醋酸溶液稀释,3-3c(CH COOH)c(CH COO )的比值增大4.25°C 时,二元酸H 2A 的盐溶液中,下列说法正确的是 ①NaHA 溶液呈酸性,H 2A 肯定为弱酸: ②NaHA 溶液呈中性,H 2A 肯定为弱酸: ③NaHA 溶液呈碱性,H 2A 肯定为弱酸:④NaHA 溶液呈中性,该溶液中水的电离度α(H 2O)=1.8×10-7% A .只有①②B .只有②③C .只有③④D .②③④5.室温时,下列溶液中有关物质的量浓度关系不正确...的是 A .0.1mol·L -1Na 2CO 3溶液中水电离出来的c(OH -)大于0.1mol·L -1NaOH 溶液中水电离出来的c(OH -)B .CH 3COONa 溶液的pH=8,则c(Na +)-c(CH 3COO -)=9.9×10-7mol·L -1C .0.1mol·L -1NaHA 溶液的pH=4,则有c(HA -)>c(H +)>c(H 2A)>c(A 2-)D.纯水加热到100℃时,水的离子积变大、pH变小、呈中性6.常温下,下列说法不正确的是A.CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中:c(CH3COO-)-c(Na+)=9.9×10-7mol·L-1B.已知HA的电离常数K a=1×10-8,等物质的量浓度的HA和NaA溶液等体积混合后溶液呈酸性C.将a mol/L氨水与0.01 mol/L的盐酸等体积混合,溶液呈中性,则NH3·H2O的电离常数K b为-9 10a-0.01D.已知:K sp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+Fe3++3H2O的平衡常数K=2.79×1037.25℃时,水中存在电离平衡:2H2O⇌H3O++OH-∆H>0.下列叙述正确的是A.将水加热,K w增大,pH不变B.向水中加入少量NH4Cl固体,抑制水的电离C.向水中加入少量NaOH固体,促进水的电离D.向水中加入少量NaHSO4固体,抑制水的电离,c(H+)增大,K w不变8.现有浓度为1mol/L的五种溶液:①H2SO4;②HCl;③CH3COOH ;④NaOH ;⑤NH4Cl,由水电离出的c(H+)大小关系正确的是A.①=②>③>⑤>④B.⑤>③>②>④>①C.①>②>③>⑤>④D.⑤ >③>②=④>①9.下列有关说法正确的是A.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0B.将纯水加热至较高温度,水的离子积变大、pH变小、呈中性C.N2(g)+3H2(g)⇌2NH3(g) ΔH<0,其他条件不变时升高温度,反应速率v(H2)和H2的平衡转化率均增大D.水的离子积常数K w随着温度的升高而增大,说明水的电离是放热过程10.在某温度下,水的离子积常数为1×10-12,该温度下等体积的①pH=0的H2SO4溶液、②0.05 mol·L-1的Ba(OH)2溶液、③pH=10的Na2S溶液、④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比(①∶②∶③∶④)是A.1∶10∶1010∶107B.1∶5∶5×109∶5×106C .1∶20∶1010∶107D .1∶10∶102∶10711.常温下,0.1 mol·L -1的某一元酸(HA)溶液中-+c OH c H ()()=1×10﹣8,下列叙述错误的是 A .该一元酸溶液的pH =3B .该溶液中水电离出的c(H +)=1×10-11mol•L -1C .该溶液中水的离子积常数为1×1014(mol•L -1)2D .用 pH =13的NaOH 溶液 与 0.1 mol·L -1该一元酸(HA)溶液等体积混合,混合后溶液的pH =712.下列有关叙述正确的是A .常温下,等体积的10.2mol L -⋅的盐酸与10.2mol L -⋅的氢氧化钡溶液混合,所得溶液的pH=13(设混合后溶液总体积的变化忽略不计)B .室温下,pH 均为4的稀硫酸、()442NH SO 溶液中,水的电离程度相同C .25℃时,10.1mol L -⋅的HA 溶液中()()-8+c OH 110c H-=⨯,则该溶液中由水电离出的()+31c H =110mol L --⨯⋅D .在饱和AgCl 、AgBr 的混合溶液中加入少量3AgNO 溶液,()()--c Cl c Br 增大 13.室温下向10mL0.1mol·L -1NaOH 溶液中加入0.1mol·L -1的一元酸HA ,溶液pH 的变化曲线如图所示。
高考化学电离平衡练习题附答案

高考化学电离平衡练习题附答案1.下列电离方程式中,错误的是A.Al2SO43====2Al3++3B.HF H++F-C.HI H++I-D.CaOH2 Ca2++2OH-解析:弱电解质存在电离平衡,强电解质全部电离。
Al2SO43、HI、CaOH2为强电解质。
书写电离方程式用“====”,HF为弱电解质,书写电离方程式用“ ”。
故答案为C、D。
答案:CD2.把0.05 mol NaOH固体,分别加入下列100 mL溶液中,溶液的导电能力变化不大的是A.自来水B.0.5 mol•L-1 盐酸C.0.5 mol•L-1醋酸D.0.5 mol•L-1 NH4Cl溶液解析:离子浓度变化不大,导电能力变化就不大。
在水中、CH3COOH中加入NaOH固体,离子浓度都增大;向HCl中加入NaOH固体,自由移动离子数基本不变,则离子浓度变化不大;向NH4Cl中加入NaOH固体,离子浓度基本不变。
答案:BD3.能影响水的电离平衡,并使溶液中cH+ >cOH-的操作是A.向水中投入一小块金属钠B.将水加热煮沸C.向水中通入CO2D.向水中加入食盐晶体解析:A项中加入钠,Na与H2O反应生成NaOH,影响水的电离平衡,使cOH->cH+;B项中加热使电离平衡右移,cH+=cOH-;C项中通入CO2,CO2+H2O====H2CO3,使cH+>cOH-;而D项中cH+=cOH-,故选C。
答案:C4.水的电离过程为H2O H++OH-,在不同温度下其平衡常数为K25 ℃=1.0×10-14,K35 ℃=2.1×10-14。
则下列叙述正确的是A.cH+随着温度的升高而降低B.在35 ℃时,cH+>cOH-C.水的电离百分率α25 ℃>α35 ℃D.水的电离是吸热的解析:本题考查水的电离的实质及水的电离平衡的影响因素。
由题中条件可以看出,温度升高后,K值增大。
25 ℃时cH+=cOH-=1.0×10-7 mol•L-1。
高二化学水电离练习题

高二化学水电离练习题一、选择题1. 下列物质中,属于强电解质的是:A. 蔗糖B. 四氧化三铁C. 硫酸D. 乙醇2. 下列物质中,属于弱电解质的是:A. 氨B. 氯化钠C. 醋酸D. 硝酸3. 当氯化钠溶解在水中时,生成的离子是:A. Na+ 和 Cl-B. H+ 和 Cl-C. Na+ 和 OH-D. H+ 和 OH-4. 下列溶液中,属于酸性溶液的是:A. 血液B. 柠檬汁C. 碳酸钙溶液D. 碱性溶液5. 当酒精溶解在水中时,酒精分子会完全离解成离子。
A. 正确B. 错误二、填空题1. 在水中,酸性溶液的pH值小于__7__。
2. 电离度大于50%的溶液属于__强电解质__。
3. 若一溶液中氢离子浓度为10^-6M,这个溶液的pH值为__6__。
4. 一溶液中氢离子浓度为1M,这个溶液的pOH值为__0__。
5. 溶液的pH和pOH值的和始终等于__14__。
三、解答题1. 有一溶液,其pH值为3,请求出该溶液的氢离子浓度和pOH值。
提示:pH + pOH = 14解答:根据提示可知,pOH = 14 - pH = 14 - 3 = 11。
由pOH = -log[OH-]可得,10^(-pOH) = [OH-],即10^(-11) = [OH-] = 0.0000000001 M。
由pH和pOH的定义可得,[H+] = 10^(-pH) = 10^(-3) = 0.001 M。
所以,该溶液的氢离子浓度为0.001 M,pOH值为11。
2. 柠檬汁的pH值约为2.3,若将柠檬汁加入纯净水中,会发生什么变化?为什么?解答:当将柠檬汁加入纯净水中时,柠檬汁中的酸性物质(如柠檬酸)会与水中的水分子发生反应,释放出氢离子(H+),使溶液变得更加酸性。
因此,纯净水的pH值会降低。
这是因为酸性物质的存在增加了氢离子的浓度,使得pH值减小。
3. 某化学实验室中,有两个溶液,一个溶液pH值为5,另一个溶液pOH值为9,请问哪个溶液更酸性?并解释原因。
高中化学 每日一题 影响水的电离平衡的因素 新人教版选修4-新人教版高二选修4化学试题
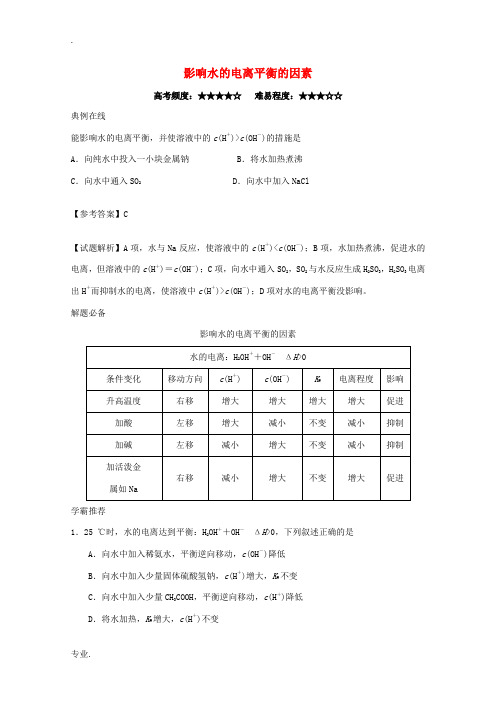
影响水的电离平衡的因素高考频度:★★★★☆难易程度:★★★☆☆典例在线能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的措施是A.向纯水中投入一小块金属钠 B.将水加热煮沸C.向水中通入SO2 D.向水中加入NaCl【参考答案】C【试题解析】A项,水与Na反应,使溶液中的c(H+)<c(OH-);B项,水加热煮沸,促进水的电离,但溶液中的c(H+)=c(OH-);C项,向水中通入SO2,SO2与水反应生成H2SO3,H2SO3电离出H+而抑制水的电离,使溶液中c(H+)>c(OH-);D项对水的电离平衡没影响。
解题必备影响水的电离平衡的因素学霸推荐1.25 ℃时,水的电离达到平衡:H2OH++OH-ΔH>0,下列叙述正确的是A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低B.向水中加入少量固体硫酸氢钠,c(H+)增大,K W不变C.向水中加入少量CH3COOH,平衡逆向移动,c(H+)降低D.将水加热,K W增大,c(H+)不变2.室温下,把1 mL 0.1 mol·L-1的H2SO4加水稀释成1 L溶液,在此溶液中由水电离产生的H+,其浓度接近于A.1×10-4mol·L-1 B.1×10-8mol·L-1C.1×10-11mol·L-1 D.1×10-10mol·L-13.已知水在25 ℃和100 ℃时,电离平衡曲线如图所示:(1)25 ℃时水的电离平衡曲线应为________(填“A”或“B”),请说明理由___________________________。
(2)将A点变为B点,采取的措施是______________________________________。
(3)C点c(H+)=________,D点c(OH-)=________。
答案1.【答案】B2.【答案】D【解析】温度不变时,水溶液中氢离子的浓度和氢氧根离子的浓度乘积是一个常数。
2023年高考化学总复习:水的电离平衡(附答案解析)

2023年高考化学总复习:水的电离平衡
基础过关练
题组一水的电离和水的离子积常数
1.关于水的离子积常数,下列说法不正确的是()
A.100℃水中,c(H+)·c(OH-)=1×10-14
B.纯水中,25℃时,c(H+)·c(OH-)=1×10-14
C.25℃时,任何以水为溶剂的稀溶液中c(H+)·c(OH-)=1×10-14
D.K
W
值随温度升高而增大
2.纯水在25℃和80℃时的H+浓度,前后两个量的大小关系为
()
A.大于
B.等于
C.小于
D.不能确定
3.下列说法正确的是()
A.水是极弱的电解质,它能微弱电离出H+,所以严格地说纯水呈微酸性
B.向水中加入稀氨水,水的电离平衡逆向移动,c(OH-)降低
C.25℃纯水中c
平(
OH-)×c平(H+)=K W,稀酸、稀碱溶液中K W=c平(OH-)×c平(H+)≠10-14
D.H
2
O H++OH-是吸热过程,所以温度升高,平衡向电离方向移动,K
W
随之增大
题组二外界条件对水的电离平衡的影响
4.向纯水中加入少量NaHSO
4
固体,在温度不变时,溶液中() A. (H+) (OH-)增大
第1页共13页。
2021年新高考化学专题练习--专题十八 水的电离和溶液的酸碱性

2021年新高考化学专题练习--专题十八水的电离和溶液的酸碱性高考帮·备考方向导航考点1 水的电离1.[2020浙江温州高考适应性考试]常温下,在体积均为20 mL、浓度均为0.1 mol·L-1的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)水的负对数[-lg c(H+)水]与滴加氢氧化钠溶液体积的关系如图所示。
下列说法不正确的是( )A.a、b、c三点溶液均显中性B.a点溶液中c(Na+)=c(X-)>c(H+)=c(OH-)C.b点溶液中的离子总浓度大于d点溶液D.常温下,K a(HX)≈10-5考点2 溶液的酸碱性与pH2.[2020浙江7月选考,17,2分]下列说法不正确的是( )A.2.0×10-7 mol·L-1的盐酸中c(H+)=2.0×10-7 mol·L-1B.将KCl溶液从常温加热至80 ℃,溶液的pH变小但仍保持中性C.常温下,NaCN溶液呈碱性,说明HCN是弱电解质D.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大考点3 酸碱中和滴定3.[2018浙江下半年选考,23,2分]常温下,分别取浓度不同、体积均为20.00 mL的3种HCl溶液,分别滴入浓度为1.000 mol·L-1、0.100 0 mol·L-1和0.010 00 mol·L-1的NaOH溶液,测得3个反应体系的pH随V(NaOH 溶液)变化的曲线如图,在V(NaOH溶液)=20.00 mL前后pH出现突跃。
下列说法不正确的是( )A.3种HCl溶液的c(HCl):最大的是最小的100倍B.曲线a、b、c对应的c(NaOH):a>b>cC.当V(NaOH溶液)=20.00 mL时,3个体系中均满足:c(Na+)=c(Cl-)D.当V(NaOH溶液)相同时,pH突跃最大的体系中的c(H+)最大4.[2019北京,26,12分]化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。
2021年高考化学专题练习:水的电离和溶液的酸碱性

2021年高考化学专题练习:水的电离和溶液的酸碱性一、选择题1、下列说法正确的是( )A.强酸的水溶液中不存在OH-B.pH=0的溶液是酸性最强的溶液C.在温度不变时,水溶液中c(H+)和c(OH-)不能同时增大D.某温度下,纯水中c(H+)=2×10-7 mol·L-1,其呈酸性2、下列关于水的电离叙述正确的是()A.无论在什么条件下,c(H+)增大,酸性都增强B.稀释氯化铵溶液,水的电离程度变大C.稀释氢氧化钠溶液,水的电离程度变小D.升高温度,K w变大,H+浓度增大3、常温时,纯水中由水电离的c(H+)=a,pH=1的盐酸中由水电离的c(H+)=b,0.2 mol/L的盐酸与0.1 mol/L的氢氧化钠溶液等体积混合后,由水电离的c(H+)=c,则a、b、c的关系正确的是()A.a>b=c B.a>c>b C.c>b>a D.b>c>a4、下列说法正确的是()A.向10 mL浓度为0.1 mol·L-1 CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中水的电离程度始终增大B.0.01 mol·L-1醋酸溶液中水的电离程度小于0.01 mol·L-1盐酸中水的电离程度C.将0.01 mol·L-1盐酸与pH=12的氨水等体积混合,所得溶液中由水电离出的c(OH-)<1×10-7 mol·L-1D.将0.01 mol·L-1醋酸溶液与等浓度的氨水等体积混合,所得溶液中由水电离出的c(OH-)>1×10-7mol·L-15、一定温度下,下列溶液的离子浓度关系式正确的是()。
A.pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol·L-1B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2)D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③6、在25 ℃时,某稀溶液中由水电离产生的c(H+)为1×10-13 mol·L-1,下列有关该溶液的叙述,正确的是()。
高中化学水的电离和溶液的酸碱性 例题解析四

煌敦市安放阳光实验学校水的电离和溶液的酸碱性例题解析【例1】(1)与纯水的电离相似,液氨中也存在着微弱的电离:2NH3NH4++NH2- 据此判断以下叙述中错误的是()A.液氨中含有NH3、NH4+、NH2-微粒B.一温度下液氨中C(NH4+)·C(NH2-)是一个常数C.液氨的电离达到平衡时C(NH3) = C(NH4+) = C(NH2-)D.只要不加入其他物质,液氨中C(NH4+) = C(NH2-)(2)完成下列反方程式①在液氨中投入一小块金属钠,放出气体____________________________。
②NaNH2溶于水的反____________________________。
③类似于“H++OH—=H2O”的反____________________________。
解析:此题要求掌握水自偶的实质(水分子电离产生的H+与H2O结合形成H3O+)以及水的电离平衡,并能迁移用于对于NH3电离的认识:NH3分子电离产生H+和NH2—,H+与NH3结合生成NH4+,液氨电离产生量的NH2—与NH4+,一温度下离子浓度乘积为一常数;NH4+类似于H+,NH2—类似于OH—。
具备上述知识后,就可顺利完成解题。
答案:(1)C(2)①2Na+2NH3=H2↑+2Na NH2②NaNH2+H2O=NaOH+NH3↑或NH2—+H2O=OH—+NH3↑③NH2—+NH4+ =2NH3↑或NH4Cl+NaNH2=2NH3↑+NaCl【例2】某温度下纯水中C(H+) = 2×10-7mol/L,则此时溶液中的C(OH-) = ___________。
若温度不变,滴入稀盐酸使C(H+) = 5×10-6 mol/L,则此时溶液中的C(OH-) = ___________。
解析:由水电离产生的H+与OH-量始终相,知纯水中C(H+) = C(OH-)。
根据纯水中C(H+) 与C(OH-)可求出此温度下水的Kw的值,由Kw的性质(只与温度有关,与离子浓度无关),若温度不变,稀盐酸中Kw仍为此值,利用此值可求出盐酸中的C(OH-)。
水的电离和溶液的pH---2023年高考化学一轮复习(新高考)
第47讲水的电离和溶液的pH复习目标 1.了解水的电离、离子积常数(K w)。
2.了解溶液pH的含义及其测定方法,能进行pH的简单计算。
考点一水的电离与水的离子积常数1.水的电离(1)水是极弱的电解质,水的电离方程式为H2O+H2O H3O++OH-或简写为H2O H++OH-。
(2)25 ℃时,纯水中c(H+)=c(OH-)=1×10-7_mol·L-1;任何水溶液中,由水电离出的c(H+)与c(OH-)都相等。
2.水的离子积常数3.填写外界条件对水的电离平衡的具体影响改变条件平衡移动方向K w水的电离程度c(OH-) c(H+) HCl 逆不变减小减小增大NaOH 逆不变减小增大减小Na2CO3正不变增大增大减小NH4Cl 正不变增大减小增大NaHSO4逆不变减小减小增大加热正增大增大增大增大1.水的电离平衡常数与水的离子积相等()2.25 ℃时CH 3COONa 溶液的K w 大于100 ℃时NaOH 溶液的K w ( ) 3.NaCl 溶液和CH 3COONH 4溶液均显中性,两溶液中水的电离程度相同( ) 4.温度一定时,在纯水中通入少量SO 2,水的电离平衡不移动,K w 不变( )5.室温下,0.1 mol·L -1的HCl 溶液与0.1 mol·L -1的NaOH 溶液中水的电离程度相等( ) 答案 1.× 2.× 3.× 4.× 5.√22H O H O (H )(OH )c c +-一或、的计算1.室温下,计算下列溶液中水电离出的2H O (H )c +。
(1)0.01 mol·L-1的盐酸中,2H O (H )c +=___________________________________。
(2)pH =4的亚硫酸溶液中,2H O (H )c +=___________________________________。
高二化学水的电离和溶液的酸碱性试题

高二化学水的电离和溶液的酸碱性试题1.在25 ℃的条件下,将体积都为10 mL,pH都等于3的醋酸和盐酸,加水稀释到a mL和b mL,测得稀释后溶液的pH均为5,则稀释时加入水的体积()A.a=b=10B.a=b>10C.a< b D.a>b【答案】D【解析】在溶液中,HCl电离是不可逆的,而CH3COOH的电离是可逆的,存在电离平衡,在加水稀释的过程中,HCl溶液里c(H+)的主要变化只有一个,即减小;CH3COOH溶液里c(H+)的主要变化有两个,即减小和增大。
若a=b,稀释后的CH3COOH溶液pH<5,若使CH3COOH溶液pH=5,就必须加水稀释,即a>b。
【考点】pH的计算2. 25℃时,水中存在电离平衡:。
下列叙述正确的是A.将水加热,增大,不变B.向水中加入少量NaHSO4固体,c(H+)增大,不变C.向水中加入少量固体,平衡逆向移动,降低D.向水中加入少量固体,平衡正向移动,增大【答案】B【解析】A.水是弱电解质,升高温度促进水的电离,所以将水加热,增大,pH减小,错误;B.向水中加入少量NaHSO4固体,c(H+)增大,由于温度不变,所以不变,正确;C.向水中加入少量固体,平衡逆向移动,但是平衡移动的趋势是微弱的,c(OH-)增大,错误;D.向水中加入少量NH4Cl固体,NH4+与水电离产生的OH-结合产生弱电解质,使水的电离平衡正向移动, c(OH-)减小,错误。
【考点】考查影响水的电离平衡的因素的知识。
3.已知某温度时CH3COOH的电离平衡常数为K。
该温度下向20 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。
下列说法中不正确的是A.a点时,CH3COOH的电离度是1%B.b点时,溶液中c(CH3COO-)>c(Na+)C.c点表示CH3COOH和NaOH恰好反应完全D.b、d点表示的溶液中均等于K【答案】C【解析】C点溶液的p H=7,而当CH3COOH和NaOH恰好反应完全时,溶质为CH3COO Na其p H>7,错误;【考点】弱电解质。
2021年高考化学专题练习:水的电离和水的离子积常数(2)

2021年高考化学专题练习:水的电离和水的离子积常数(2)1、下列说法正确的是( )A.水的电离方程式为H2O H++OH-B.升高温度,水的电离程度增大C.NaOH溶液中不存在H+D.HCl溶液中不存在OH-2、常温下,某溶液中由水电离出来的c(H+)=1.0×10-13mol·L-1,该溶液可能是( )①二氧化硫②氯化铵水溶液③硝酸钠水溶液④氢氧化钠水溶液A.②③ B.①② C.①④ D.③④3、下列操作会使H2O的电离平衡向正方向移动,且溶液呈酸性的是( ) A.将纯水加热到95 ℃时, 7pH<B.向水中加少量NaHSO4C.向水中加少量Na2CO3D.向水中加少量FeCl34、常温下,在pH=9的NaOH溶液和CH3COONa溶液中,设由水电离出的OH-浓度分别为M mol·L-1和N mol·L-1,则M和N的关系为( )A.M>NB.M=10-4NC.N=10-4MD.M=N5、已知NaHSO4在水中的电离方程式为NaHSO4=Na++H++24SO-。
某温度下,向c(H+)=1×10-6mol·L-1的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的c(H+)=1×10-2mol·L-1。
下列对该溶液的叙述不正确的是( )A.该温度高于25℃B.由水电离出来的H+的浓度为1×10-10mol·L-1C.加入NaHSO4晶体抑制了水的电离D.取该溶液加水稀释100倍,溶液中的c(OH-)减小6、已知常温下0.1mol/L的CH3COOH溶液中c(H+)=1.32×10-3mol/L,则常温下该CH3COOH溶液中的水的离子积常数KW的数值为( )A.1×10-14 B.1×10-13 C.1.32×10-14 D.1.32×10-157、25℃时,水的电离可达到平衡:H2O H++OH-ΔH>0。
高考化学真题(2010-2019)专题解析—水的电离和溶液的酸碱性

高考化学真题(2010-2019)专题解析—水的电离和溶液的酸碱性B .c (H +)=c (42H PO -)+2c (4HPO -)+3c (34P 题型一:水的电离平衡与溶液的酸碱性1.(2019·全国Ⅲ·11)设N A 为阿伏加德罗常数值。
关于常温下pH=2的H 3PO 4溶液,下列说法正确的是A .每升溶液中的H +数目为0.02N AO -)+c (OH −)C .加水稀释使电离度增大,溶液pH 减小D .加入NaH 2PO 4固体,溶液酸性增强【答案】B【解析】本题考查阿伏加德罗常数、电离平衡及其影响因素等,考查的核心素养是变化观念与平衡思想。
pH=2的H 3PO 4溶液中c (H +)=10-2mol·L -1,每升溶液中所含N(H+)=0.01N A ,A 错误;由电荷守恒知,该H 3PO 4溶液中存c (H +)=c (42H PO -)+2c (4HPO -)+3c (34PO -)+c (OH −),B 正确;加水稀释能促进H 3PO 4的电离,使其电离度增大,由于以增大溶液体积为主,导致溶液中c(H +)减小,溶液pH 增大,C 错误;向H 3PO 4溶液中加入NaH 2PO 4固体,溶液中c(H 2PO 4-)增大,促使平衡H 3PO 4H++H 2PO 4-逆向移动,抑制H 3PO 4电离,溶液酸性减弱,D 错误。
【命题动向】本题命题角度新颖,在同一道试题中综合考查微粒数目的计算、电离平衡及其影响因素和守恒思想,命题具有前瞻性和导向性。
2.(2019·北京·12)实验测得0.5mol·L -1CH 3COONa 溶液、0.5mol·L -1CuSO 4溶液以及H 2O 的pH随温度变化的曲线如图所示。
下列说法正确的是A.随温度升高,纯水中c(H +)>c(OH -)B.随温度升高,CH3COONa溶液的c(OH-)减小C.随温度升高,CuSO4溶液的pH变化是K W改变与水解平衡移动共同作用的结果D.随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO-、Cu2+水解平衡移动方向不同【答案】C【解析】题考查盐类水解等知识,考查的核心素养是变化观念与平衡思想。
高二化学水的电离和溶液的酸碱性试题答案及解析

高二化学水的电离和溶液的酸碱性试题答案及解析1.下列说法正确的是()A.水的电离方程式:H2O H++OH-B.升高温度,水的电离程度增大C.在NaOH溶液中没有H+,在HCl溶液中没有OH-D.纯水中c(H+)=10-7 mol·L-1【答案】B【解析】水是极弱的电解质,只有少部分电离,应用“”表示,故A错;水的电离是吸热的,所以升高温度,电离程度增大,B正确;在NaOH溶液中c(OH-)>c(H+),在HCl溶液中c(OH-)<c(H+),在酸碱溶液中都同时存在H+、OH-,所以C错;在常温下,纯水中c(H+)=10-7 mol·L-1。
【考点】水的电离溶液的酸碱性2.有一学生在实验室测某溶液的pH,实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测:(1)该学生的操作是(填“正确的”或“错误的”),其理由是。
(2)若用此方法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是,原因是。
(3)该学生以上述方式测定下列溶液的pH,无误差的是()A.NaOH B.CH3COONa C.NaCl D.NaHSO4【答案】(1)错误的润湿后,稀释了原溶液,使其浓度减小,导致测量误差(2)盐酸盐酸是强电解质,醋酸是弱电解质,在溶液中存在CH3COOH CH3COO-+H+,稀释时平衡右移,继续电离出H+,稀释时Δc(H+)较小,ΔpH较小,故误差较小(3)C【解析】用pH试纸测定溶液酸碱性时,不能用水润湿。
若润湿,会使待测液浓度下降,结果出现误差。
但是用pH试纸测定中性溶液时,对结果一般没影响。
【考点】pH的计算3.(10分)某化学实验小组从市场上买来一瓶某品牌食用白醋(主要是醋酸的水溶液),用实验室标准NaOH溶液对其进行滴定以测定它的准确浓度,完全反应时所得溶液pH大致为9 。
下表是4种常见指示剂的变色范围:(1)该实验应选用作指示剂。
(2)右图表示50 mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为 mL;反应达滴定终点时的现象为。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(满分60分时间30分钟)
姓名:_______________班级:_______________得分:_______________
1.现有常温下的六份溶液:①0.01mol•L﹣1CH3COOH溶液;②0. 01mol•L﹣1HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液;⑤0.01mol•L﹣1 CH3COOH溶液与pH=12的氨水等体积混合后所得溶液;⑥0.01mol•L﹣1 HCl溶液与pH=12的NaOH溶液等体积混合所得溶液.
(1)其中水的电离程度最大的是__________(填序号,下同),水的电离程度相同的是_____________________.
(2)若将②③混合后所得溶液的pH=7,则消耗溶液的体积:②_____③(填“>”“<”
或“=“).
(3)将六份溶液同等稀释10倍后,溶液的pH:①_____②,③_____④,⑤_____⑥(填“>”“<”或“=“).
(4)将①④混合,若有c(CH3COO﹣)>c(H+),则混合溶液可能呈___________(填序号).A.酸性 B.碱性 C.中性.
【答案】⑥②③④>>>> ABC
【解析】
(4)①④混合后,根据电荷守恒可知c(H+)+c(Na+)=c(OH-)+c(CH3COO-),若c(CH3COO -)>c(H+),则c(Na+)>c(OH-)。
但c(H+和c(OH-)的大小关系无法确定,所以该溶
液可能显酸性、碱性或中性。
2.Ⅰ.已知:H2A的A2-可表示S2-、SO42-、SO32-、SiO32-或CO32-。
(1)常温下,向20 mL 0.2 mol·L-1 H2A溶液中滴加0.2 mo l·L-1 NaOH溶液。
有关微粒物质的量变化如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。
请根据图示填
空:
①当V(NaOH)=20 mL时,溶液中离子浓度大小关系:________。
②等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水________
(填“大”、“小”或“相等”)。
(2)若H2A为硫酸:t ℃时,pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数K W=________。
【答案】c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)小 10-13
【解析】
试题分析:本题考查图像的分析,溶液中离子浓度的大小比较,外界条件对水的电离平衡的影响,K W的计算。
②等体积等浓度的NaOH溶液与H2A溶液混合后得到NaHA溶液,由图像知c(A2-)c(H2A),
HA-的电离程度(HA-的电离方程式HA-H++A2-)大于HA-的水解程度(HA-的水解方
程式HA-+H2O H2A+OH-),HA-电离的H+抑制水的电离,NaHA溶液中水的电离程度比
纯水小。
(2)pH=2的稀硫酸中c(H+)=110-2mol/L,pH=11的NaOH溶液中c(H+)=110-11mol/L,因为溶液呈中性,则硫酸溶液中H+物质的量与NaOH溶液中OH-物质的量相等,
110-2mol/LV=mol/LV,K W=110-13。
3.有下列物质的溶液①CH3COOH ②HCl ③H2SO4④NaHSO4
(1)若四种溶液的物质的量浓度相同,其c(H+)最大的是________(用序号表示,下同)。
(2)若四种溶液的c(H+)相同,其物质的量浓度最大的是________。
(3)将pH相同的上述四种溶液与Zn反应生成等量氢气,所需时间最短的是_________。
(4)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为________,经测定溶液中c(CH3COO-)为1.4×10-3mol·L-1,此温度下醋酸的电离常数K a=________,
(写出计算式,不必计算最终结果)。
温度升高,K a将______(填“变大”、“不变”
或“变小”)。
(5)在常温下将pH=11的NaOH溶液a L与pH=2的H2SO4溶液b L混合,若混合后溶液呈中性,则a:b=_________。
【答案】③①①0.1 mol/L(1.43×10-3)2/0.1变大10:1
【解析】
【详解】
(4)n(CH3COOH)==0.1mol,c(CH3COOH)==0.1mol/L;
c(CH3COO-)=c(H+)=1.4×10-3mol/L,
K===1.96×10-5;醋酸电离吸热,升温促
进电离,电离平衡常数增大,故答案为:0.1mol/L;1.96×10-5;变大;
(5)常温下,将pH=2的H2SO4溶液bL与pH=11的NaOH溶液aL混合,若所得混合液为中
性,说明氢离子和氢氧根离子物质的量相同,×a=10-2×b,得到a:b=10:1,故答案为:10:1。
4.现有①CH3COOH、②HCl两种溶液,用A、B、C选择填空:A.①>②;B.①<②;C.①=②。
(1)当它们pH相同时,其物质的量浓度_________。
(2)当它们的物质的量浓度相同时,其pH的关系是_________。
(3)中和等体积、等物质的量浓度的烧碱溶液,需同物质的量浓度的两种酸溶液的体积关系为_________。
(4)当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为_________。
(5)将pH相同的两种酸均稀释10倍后,pH关系为_________。
【答案】AACAB
【解析】
【分析】CH3COOH为弱电解质,在溶液中部分电离,HCl是强电解质,在溶液中完全电离,结合题干中的问题解答。
【详解】
产生氢气的体积:①>②,故选A;
(5)将pH相同的两种酸均稀释10倍后,盐酸中氢离子的物质的量基本不变,而醋酸在稀释过程中,电离程度增大,溶液中氢离子物质的量增大,溶液的pH小于盐酸溶液的,所以pH关系为为:②>①,故选B。
【点睛】
本题考查了酸碱反应中溶液性质及溶液pH计算,题目难度中等,题量稍大,注意醋酸为弱电解质溶液中部分电离、盐酸为一元强酸,明确电解质的电离特点、溶液pH计算依据以及有关反应特点是解答的关键。
