ASCO 2020直肠癌放疗进展全新辅助治疗
2020ASCO结直肠癌免疫治疗新进展(最新推荐)

瑞戈非尼抑制对巨噬细胞增殖重要的受体CSF-1R
• 巨噬细胞增殖和存活CS极F度-1信依号赖通于路CS及F-瑞1的戈作非用尼1对,其瑞的戈抑非制尼作能用抑制CSF-1受体2
体外试验证实,瑞戈非尼可有效抑制 VEGFR、TIE2、PDGFRs和FGFR等多个激酶靶点
• 生化检测发现,瑞戈非尼有效抑制VEGFR1-3, TIE2, FGFR1、PDGFR-β、KIT、RET和 RAF等激酶,IC50值 4~311nM
生化活性
VEGFR1 VEGFR2 VEGFR3 TIE2 PDGFR-β FGFR1 KIT RET RAF-1 BRAF BRAF V600
增加抗原特异性T细胞数量或 增强抗原呈递
治疗目标因免疫浸润情况而异:“热”vs“冷”肿瘤
“热肿瘤”(免疫炎症型) “冷肿瘤”(免疫排除型) “冷肿瘤”(免疫沙漠型)
大量T细胞浸润肿瘤
T细胞不能浸润肿瘤
没有T细胞激活/招募
肿瘤细胞 T细胞 树突状细胞 粒细胞 MDSC 巨噬细胞
破坏肿瘤 免疫循环
T细胞识别和 杀灭癌细胞 (步骤6和7)
大部分mCRC为非炎症性,无法接受免疫治疗
免疫炎症型
MSI-H (3-5% mCRC)
CD8+ T细胞浸润 但非功能性
免疫排除型
免疫沙漠型
MSS (>95% mCRC)
CD8+ T细胞累积 但未有效浸润
肿瘤和外周缺少 CD8+ T细胞
加速T细胞应答或 消除对T细胞应答的“刹车”
使T细胞与肿瘤细胞接触
瑞戈非尼 IC50 (nM) 平均值 ±SD 3±2 135 ± 10 ~90 31 ± 9 ~200 380 ± 60 272 43 ± 32 22 ± 10 ~10
2020年ASCO晚期结直肠癌CRC治疗进展(最新推荐)

CR率 3.9%
4040 • MSI-H患者一线采用Nivo+小剂量Ipi 的II期单臂研究,本次更新长期随访结果
NIVO + low-dose IPI continued to show robust, durable clinical benefit with a deepening of response, and was well tolerated with no new safety signals identified with longer follow-up. NIVO + low-dose IPI may represent a new 1L therapy option for pts with MSI-H/dMMR mCRC.
4001
Results before 2020
Updates in 2020: 两靶 vs 对照(OS)
Updates in 2020: 两靶 vs 对照(OS亚组分析)
MSI-H
Updates in 2020: 三靶 vs 对照(OS)
Updates in 2020: 三靶 vs 对照(OS亚组分析)
3-4级 治疗周期(中位) 中性粒细胞减少
贫血 血小板减少症
疲乏 腹泻 手足综合征 高血压 皮疹
TAS-102组(n=177) 2.99**
59(33.91%) 24(13.79%)***
5(2.92%)*** 29(16.67%)***
8(4.60%)*** 1(0.57%)*** 1(0.58%)***
6
1 MSI-H 28 MSS
标准治疗失败
呋喹替尼3mg +信 迪利单抗200mg q3w
中国临床肿瘤学会 (CSCO)结直肠癌诊疗指南2020版

≥1位一级或二级 亲属患大肠癌
Lynch HT, et al. 2013
遗传性结直肠癌指南总体框架
遗传性结直肠癌主要包括:
• Lynch综合症 • FAP (家族性腺瘤性息肉病)
典型的FAP
结直肠内息肉数均在100枚以上,癌变 年龄早,癌变风险几乎为100%
AFAP (轻症FAP)
结直肠癌 患者
息肉 (10-20枚)
关注家族史
(+) 强烈建议
本人定期结肠镜检查 三甲/省级专科医院就诊
体格检查
CHRPE* 颅骨骨瘤
*CHRPE: 眼底视网膜色素上皮细胞肥大
腹腔肿块
• FAP家系受影响者可出现有多种肠外疾病,我国人群的文献报道,肠外疾病以腹腔内硬纤维瘤和骨瘤 最容易被识别且相对较为常见。因此,怀疑FAP时,应特别注意是否有腹腔内硬块和骨瘤。
家组取得一致共识(支持意见
变,主要考虑的因素
≥80%)
是患者的明确获益性
II级 1B类证据:
2A类证据:
• 可及性差或者效价比
专家推荐 基于高水平证据,如严谨的 基于稍低水平证据,如一般质量
低
Meta分析或大型随机对照 的meta分析、小型随机对照研
临床研究结果,专家组取得 究(II期)、设计良好的大型回
虽然缺乏循证医学证 据,但是专家组具有 一致共识的
良好的大型回顾性研究、病 得共识,而且存在较大争议(支
例-对照研究,专家组取得 持意见<60%)
基本一致共识,但有小的争
议(支持意见60%~80%)
结直肠癌的MDT诊治原则
—— MDT基本概念
核心:以病人为中心,以专家组为依托
直肠癌新辅助放化疗

0 6 患者生活质量:评估患者在治疗后的生活质量和满意度
副作用和并发症
腹泻:放疗可能导致肠道功 能紊乱,引起腹泻
放射性肠炎:放疗可能导致 肠道炎症,引起腹痛、腹泻
等症状
放射性膀胱炎:放疗可能导 致膀胱炎症,引起尿频、尿
急等症状
皮肤反应:放疗可能导致皮 肤红肿、瘙痒等症状
骨髓抑制:化疗可能导致骨 髓抑制,引起白细胞、红细
放化疗联合治疗方案的优化:如同步放化疗、序贯放化 疗等,提高治疗效果和降低复发风险
个体化治疗方案的优化:根据患者的具体情况,制定个 性化的放化疗方案,提高治疗效果和降低副作用
联合治疗方案探索
1
放化疗与靶向治疗相结合:提高治疗 效果,降低副作用
2
放化疗与免疫治疗相结合:提高免疫结合:通过基因 编辑技术,提高放化疗的疗效
4
放化疗与其他治疗方法相结合:探索 新的治疗方案,提高治疗效果
提高患者生存质量
01
优化放化疗方案:根据患者个体差异,制定个性化的放化疗方案,提高治疗效果
02
加强患者心理辅导:通过心理干预,减轻患者心理压力,提高治疗依从性
03
提高患者生活质量:通过营养支持、疼痛管理等措施,改善患者生活质量
2
治疗方案设计
01
确定放化疗的适应 症和禁忌症
04
制定放化疗的副作 用预防和处理措施
02
制定放化疗的剂量 和疗程
05
制定放化疗的疗效 评估和随访计划
03
确定放化疗的联合 方案和顺序
放疗技术选择
01
放疗技术:三维适形放疗、调强放疗、立体定向放疗等
02
放疗剂量:根据肿瘤大小、位置、分期等因素确定放疗剂量
直肠癌新辅助放化疗

演讲人
目录
直肠癌新辅助放化疗概述
01
直肠癌新辅助放化疗的适应症
02
直肠癌新辅助放化疗的副作用及应对措施
03
直肠癌新辅助放化疗的预后及随访
04
1
直肠癌新辅助放化疗概述
治疗原理
新辅助放化疗:在直肠癌手术前进行的放化疗
01
目的:缩小肿瘤,降低手术难度,提高手术成功率
02
治疗方法:根据肿瘤分期和患者身体状况选择合适的放化疗方案
05
靶向治疗:使用药物或抗体攻击特定的癌细胞,如抗EGFR药物
06
免疫治疗:使用药物激活或增强免疫系统,以攻击癌细胞,如PD-1/PD-L1抑制剂
治疗效果
提高手术切除率
降低局部复发率
提高生存率
降低远处转移率
改善生活质量
降低术后并发症发生率
2
直肠癌新辅助放化疗的适应症
肿瘤分期
01
早期直肠癌:T1-T2期
04
参加康复治疗和锻炼,提高身体素质和免疫力
谢谢
01
定期进行身体检查,及时发现并处理副作用
02
保持良好的心理状态,避免焦虑、抑郁等负面情绪
03
及时与医生沟通,寻求专业建议和治疗方案
04
预防方法
保持良好的生活习惯,如健康饮食、规律作息、适量运动等
01
定期进行体检,及时发现并治疗疾病
02
避免接触致癌物质,如吸烟、饮酒等
03
保持良好的心理状态,避免过度紧张和焦虑
02
局部进展期直肠癌:T3-T4期
03
局部晚期直肠癌:N1-N2期
04
转移性直肠癌:M1期
肿瘤位置
中国临床肿瘤学会 (CSCO)结直肠癌诊疗指南2020版

无症状健康人群的筛查:高危人群 (III 级专家推荐)
高危 人群
非进展期腺瘤
2-3年复查 结肠镜
复发 未复发
继续 2-3年复查结肠镜
延长间隔至3-5年
结直肠癌的筛查及遗传学
• 无症状健康人群的结直肠癌筛查
见指南第2.1节
• 遗传性结直肠癌筛检和基因诊断原则
见指南第5节
1/3 的大肠癌具有遗传背景
Familial CRC:
≥1位一级或二级 亲属患大肠癌
Lynch HT, et al. 2013
遗传性结直肠癌指南总体框架
遗传性结直肠癌主要包括:
• Lynch综合症 • FAP (家族性腺瘤性息肉病)
典型的FAP
结直肠内息肉数均在100枚以上,癌变 年龄早,癌变风险几乎为100%
AFAP (轻症FAP)
虽然缺乏循证医学证 据,但是专家组具有 一致共识的
良好的大型回顾性研究、病 得共识,而且存在较大争议(支
例-对照研究,专家组取得 持意见<60%)
基本一致共识,但有小的争
议(支持意见60%~80%)
结直肠癌的MDT诊治原则
—— MDT基本概念
核心:以病人为中心,以专家组为依托
来自两个以上不同学科的一组相对固定的专家 在固定的时间、固定的地方聚在一起
• FAP患者会出现先天性视网膜色素上皮肥大(CHRPE),在典型的FAP中发生率可达80%。 • 1/3-1/4的FAP患者无家族遗传史,为该个体胚系新发肿瘤。家族史并不是诊断FAP的必要条件。
FAP筛检——II 级专家推荐
结直肠癌 患者
息肉 (≥20枚)
关注家族史
(+) 强烈建议
体格检查
ASCO2020直肠癌放疗进展全新辅助治疗

ASCO2020直肠癌放疗进展全新辅助治疗ASCO2020直肠癌放疗进展全新辅助治疗2020ASCO会议在美国芝加哥顺利召开,多项全新辅助治疗(TotalNeoadjuvantTherapy,TNT)模式的研究作为局部进展期直肠癌治疗的亮点在今年的会议中进⾏了报道,包括短程放疗加巩固化疗对⽐长程放化疗的RAPIDO研究(4006),诱导化疗对⽐巩固化疗观察器官保留率的OPRA研究(4008),以及三药化疗联合放化疗的PRODIGE23研究(4007)。
对于局部进展期直肠癌,传统的新辅助治疗模式是在新辅助放化疗之后进⾏全直肠系膜切除术(TME)和辅助化疗,这种治疗模式较辅助放化疗能显著降低局部复发率,但并没有带来⽣存的获益,远处转移是其主要失败模式,这可能和术后辅助化疗开始晚、完成率较低相关。
此外,对于低位局部进展期直肠癌的患者,不能保肛带来的功能损失,影响了患者的⽣活质量。
全新辅助治疗(TNT)模式把辅助化疗前移到术前,提⾼化疗顺应性,理论上能降低远处转移,改善远期⽣存,同时术前治疗模式的叠加,追求最⼤化的肿瘤退缩,可争取更⾼的完全缓解率,提⾼患者器官保留的可能性。
今年ASCO的多项研究,就对TNT的疗效进⾏了报道。
⼀、RAPIDO研究—短程放疗加巩固化疗对⽐长程放化疗该研究是⼀项欧洲多中⼼、III期RCT研究,⼊组的是MRI评估具有⾼危因素的局部进展期直肠癌,⾄少包括下列因素之⼀:cT4a/b,cN2,肠壁外⾎管侵犯(EMVI+),直肠系膜筋膜侵犯(MRF+)或侧⽅淋巴结增⼤。
研究共⼊组了920例患者,随机分配到两组,试验组是55Gy短程放疗后进⾏6周期CAPOX或9周期FOLFOX4化疗后⾏TME⼿术,对照组是长程放化疗,同期给予卡培他滨单药,6-10周后⼿术,术后⾏辅助化疗。
研究的主要终点为疾病相关的治疗失败率(DrTF)。
在报道的结果中,两组治疗耐受性均较好,⼿术及术后并发症之间没有显著差异,短程放疗加化疗组的3年DrTF和远处转移率降低了7%左右,DrTF为23.9%,明显低于对照组的30.4%(P=0.019),远处转移率也更低(20.0%vs26.8%,P=0.005),病理完全缓解率(pCR)在短程放疗加化疗组较对照组提⾼1倍(28.4%vs14.3%,P<0.001),两组的局部复发率(8.7%vs6.0%,P=0.09)、OS(89.1%vs88.8%,P=0.59)之间⽆显著差异。
直肠癌的新辅助治疗

新辅助治疗的临床研究
新辅助同步放化疗和辅助同步放化疗 德国直肠癌研究协作组开展了一项大型的前瞻性随机对照 临床试验(CAO/ARO/AIO-94 研究,比较新辅助同步放化疗与 辅助同步放化疗治疗Ⅱ / Ⅲ期直肠癌的疗效。共有799 例患者 被随机分为两组,分别接受新辅助同步化放疗,或辅助同步放 化疗,之后两组均接受氟尿嘧啶/ 甲酰四氢叶酸辅助化疗4 周期。 与辅助同步放化疗组相比,新辅助同步放化疗组的局部复发率 显著减少(6%对13%,P=0.006)、保肛率显著增加(39% 对19%,P=0.004),但两组的5 年无病生存率和5 年总生存率 相仿。并且新辅助同步放化疗组显著减少了治疗相关毒副作用 (27% 对49%,P=0.001),未增加吻合口瘘、术后出血和肠 梗阻的发生率,虽然伤口的延迟愈合高于术后同步放化临床研究
新辅助放疗与新辅助同步放化疗 法国2003 年发表了FFCD9203 研究的结果,该 研究比较了新辅助放疗和新辅助同步放化疗的结果, 724 例T3-4NX 可手术切除的直肠癌患者随机分为两 组,分别接受新辅助放疗或者新辅助同步放化疗, 化疗方案为氟尿嘧啶/ 甲酰四氢叶酸,手术在放疗或 同步放化疗结束后的3 ~ 10 周进行,结果接受新辅 助同步放化疗的患者取得了更高的病理完全缓解率 (11.4% 对3.6%,P < 0.0001)和更低的局部失败 率(8.1% 对16.5%,P=0.004), 但两组在保肛率、 5 年无病生存率和5 年总生存率上无显著性差异,而 新辅助同步放化疗组有更多的3/4 度不良反应 (14.9% 对2.9%,P < 0.0001)。
新辅助治疗的临床研究
该研究的结果显示尽管新辅助同步放化疗未能提高总生存率, 但其在保证与辅助同步放化疗相同生存率的前提下,进一步 降低了局部复发率和毒副作用,并且使更多的患者能够保留 肛门括约肌,提高了生活质量。因此,在欧洲和美国,越来 越多的医院倾向于新辅助同步放化疗。CAO/ARO/AIO-94 研究2012 年发表了中位随访11 年的结果[3],新辅助同步放 化疗和辅助同步放化疗组的10 年生存率分别为59.6% 和 59.9%(P=0.85) ;10 年累计局部复发率分别为7.1% 和 10.1%(P =0.048),10 年累计远地转移率分别为29.8% 和 29.6%(P =0.9)。EORTC22921 研究将可手术切除的临床诊 断T3-4 的患者分为新辅助放疗、新辅助同步放化疗、新辅 助放疗联合辅助化疗组和新辅助同步放化疗联合辅助化疗组, 结果同FFCD9203 研究相似,新辅助同步放化疗能够进一步 降低局部复发率,但是不能提高患者无病生存期(DFS)和 总生存期(OS)。
2020年结直肠癌治疗进展盘点(全文版)

2020年结直肠癌治疗进展盘点(全文版)2020年结直肠癌领域的治疗进展,分为围术期治疗篇和晚期疾病全身治疗篇。
前者主要包括直肠癌术前新辅助治疗、局晚结肠癌新辅助治疗、基于新型标志物的结肠癌辅助治疗决策和转移瘤不可切除的晚期结直肠癌无症状原发灶切除的争议与共识;后者主要包括MSI-H晚期结直肠癌一线免疫治疗进展、HER2扩增/BRAF突变型晚期结直肠癌的末线精准治疗进展和MSS型晚期结直肠癌免疫治疗进展。
第一部分围术期治疗篇1、直肠癌的术前新辅助治疗2020年是局部进展期直肠癌(locally advanced rectal cancer,LARC)研究丰收的一年,不论是ASCO还是ESMO年会均有重要研究报告出炉,关注了目前LARC术前治疗最重要的两个话题:如何提高疗效,如何注重器官功能保全。
在治疗策略里涉及到目前该领域最重要的理念-全程新辅助治疗(total neoadjuvant therapy,TNT),或非手术治疗观察等待(Watch & Wait,W&W)策略。
这些研究结果将给我们的临床实践带来怎样的影响呢?01. LARC新辅助治疗:TNT大放异彩2020年是TNT治疗模式大放异彩的元年,表1列举了2020年公布的最重要的TNT研究结果,总结来说,TNT获得了如下临床治疗优势:1) 显著增加全身治疗完成度2) 显著提高了肿瘤退缩3) 显著降低了肿瘤相关治疗转移复发事件4) 显著增加cCR比率及W&W概率LARC的治疗进入肿瘤学效果和功能并重的时代,传统“三明治”治疗(术前同步放化疗[CRT]-全直肠系膜切除术[TME]-术后化疗)模式的利弊凸显。
该模式可以显著降低局部复发率,但却没能改善远期生存,其中一个重要原因就是在CRT和TME之后,术后辅助化疗完成度很低(表1中的结果已经一目了然)。
另一方面,尽管CRT较单纯的术前RT提高了肿瘤缓解率,进而提高了保肛率,毕竟传统CRT模式带来的肿瘤完全缓解率一般不超过20%,这对于绝大多数极低位直肠癌的肛门功能保全显然是不够的。
直肠癌的放射治疗-2020ASTRO临床实践指南

直肠癌的放射治疗-2020ASTRO临床实践指南2020年10月,美国肿瘤放射治疗协会(ASTRO)正式推出直肠癌放射治疗临床实践指南。
1.该指南覆盖全新辅助治疗(TNT)、非手术治疗(NOM)、选择性放疗等热点问题;2.该指南制定专家共19名,通讯作者为M.D.Anderson 癌症中心的腹部放疗医生Prajnan Das 教授。
核心问题1:可手术切除直肠癌的新辅助治疗指证1.直肠癌,推荐盆腔MRI用于术前临床T和N分期-强烈推荐,中等质量证据;2.II-III期直肠癌,推荐新辅助放疗-强烈推荐,高质量证据;3.对于低复发风险II期直肠癌,经多学科讨论后,可以不做新辅助放疗-有条件推荐,中等质量证据;低复发风险定义:T3a/bN0肿瘤位于距离肛门>10cm,且MRI确定的环周切缘≥2mm,同时MRI下的无壁外血管受侵(EMVI);T3a/b=1-5mm肿瘤侵出肌层;4.对于T1-2N0 直肠癌,如果需要APR手术时,有条件推荐新辅助放疗,以提高保留括约肌的机会,以有可能转化为保留肛门的直肠癌低位前切除-有条件推荐,专家观点;5.如果需要放疗,推荐术前放疗而不是术后放疗-强烈推荐,高质量证据;6.核心问题2:新辅助治疗方案1.对于接受新辅助放化疗患者,推荐常规同步放化疗50-50.4Gy/25-28次-强烈推荐,高质量证据;2.3.对于接受新辅助短疗程放疗患者,推荐25Gy/5次,不同步化疗-强烈推荐,高质量证据;4.对于接受新辅助放化疗患者,仅5-FU或卡培他滨推荐放疗同步增敏化疗-强烈推荐,高质量证据;5.对于接受新辅助治疗,单纯应用化疗(FOLFOX或CAPOX)仅有条件推荐于临床试验-有条件推荐,低质量证据;6.对于接受新辅助治疗,无预示较高肿瘤复发风险因素,推荐放化疗或短疗程大分割放疗-强烈推荐,高质量证据;预示较高肿瘤复发风险因素包括:T3肿瘤距离肛门≤5cm或MRI下环周切缘<2mm;cT4肿瘤或cN2, MRI下壁外血管受侵(mrEMVI)7.对于接受新辅助治疗,无预示较高肿瘤复发风险因素,有条件推荐(1)长疗程同步放化疗前或后,给予多药联合化疗(FOLFOX或CAPOX);(2)短疗程大分割放疗后,给予多药联合化疗(FOLFOX或CAPOX)-有条件推荐,低质量证据;预示较高肿瘤复发风险因素包括:T3肿瘤距离肛门≤5cm或MRI下环周切缘<2mm;cT4肿瘤或cN2, MRI下壁外血管受侵(mrEMVI)。
2020ASCO肠癌辅助治疗新进展

TNT 模式
2
术前 CRT/SCRT
巩固/新辅助 化疗
TME手术
Abs4004: Ⅲ期结肠癌患者奥沙利铂和以氟嘧啶为基础的辅助治疗3
个月对比治疗6个月的OS和长期DFS:IDEA最终结果
Alberto F. Sobrero, IRCCS圣马蒂诺综合医院,热那亚,意大利
Abs4004—背景和目的
• III期CC的辅助化疗持续时间在毒性方面存在争议。 • 观察到来自6项试验的12,835例患者,比较III期CC患者3个月和6个
1. Andre T, JCO 2015; NS, non-inferiority,非劣效性; OS, overall surviva,总生存期l; HR, hazard ratio,风险比, DFS, disease-free survival,无病生存; FDRa, 调整错误发现率 ,m; months,月
– III期结肠癌辅助化疗
• #4004 IDEA
– 分子标志物在辅助化疗决策中的价值
• #4010 Model • #4012 TD • #4009 ctDNA
对临床实践有意义或 带来改变的研究
LARC术前治疗模式的优化:疗效与功能并重!
Less is More “减法”
More is Better “加法”
单纯肝切除术 41.5%
92.2%
• 化疗后3年DFS为52.1% (95% CI 43.2 - 60.2),单纯肝切除术后3年DFS为41.5%(33.2 49.6)(HR 0.63[0.45 - 0.89],单侧p = 0.002)。
• 化疗后3年OS为86.6%(79.2-91.4),单纯肝切除术后3年OS为92.2%(86.0 - 95.8) (HR1.35[0.84 - 2.19])。
直肠癌新辅助治疗后复发及远处转移的研究进展

疗结束 2 周后给予以 5-FU 为基础的化疗。TNT 在
标准的 nCRT 前给予 3~4 个月的全身化疗。
目前,直肠癌术前放疗可分为短程放疗(shortcourse radiotherapy,SCRT)和 长 程 放 化 疗(longcourse chemoradiation therapy,LCCRT)两 种 方 式 。
75.5%(95%CI:63.0%~88.0%);术后中位死亡时间
例患者发生远处转移,患者的 1 年 OS 为 86.7%;序
贯放化疗组中 6 例患者局部复发,9 例患者发生远
处转移,患者的 1 年 OS 为 70.0%。Tang 等 [18] 对患者
进 行 了 TNT,中 位 随 访 时 间 为 51 个 月(45~57 个
月),结果发现,12 例患者局部复发或发生远处转
局部复发一直是直肠癌患者高发病率和死亡率的
主要原因,手术是其主要治疗手段。随着术前评
估和手术技术水平的提高,选择性联合新辅助放
化疗(neoadjuvant chemoradiotherapy,nCRT)明显减
少了患者的盆腔局部复发率,使其从 25%降至 6%~
9% [3- 7] 。nCRT 联合全直肠系膜切除术(total mesorectal excision,TME)治疗直肠癌疗效显著,成为局
虽然 nCRT 已成为局部进展期直肠癌的“金标
准”,但放化疗的治疗方式并未统一 [16] 。陈永盛 [17]
对同步放化疗与序贯放化疗两种治疗方式的疗效
进行比较,结果显示,两种治疗方式的总有效率分
别 为 83.3% 和 60.0% ,差 异 有 统 计 学 意 义(P ﹤
中低位局部进展期直肠癌全程新辅助治疗的研究进展(全文)

中低位局部进展期直肠癌全程新辅助治疗的研究进展(全文)摘要新辅助放化疗增加了对进展期直肠癌的局部控制作用,但无法显著降低远处转移率和改善生存预后仍是该治疗策略的不足之处。
全程新辅助治疗主张将全身化疗放在根治性手术之前进行,具有改善治疗依从性、增加肿瘤的局部控制效果、提高器官保留率等优势。
目前全程新辅助治疗具体模式、化疗药物种类及剂量等缺乏共识,导致各研究结果之间差异较大。
此外,巩固化疗与诱导化疗、双药化疗与三药化疗、短程放疗联合巩固化疗与长程放化疗等治疗模式的选择亦存在较大争议。
为进一步降低结直肠肿瘤的远处转移率并改善患者的生存预后,学者提出全程新辅助治疗(total neoadjuvant therapy,TNT),将全身化疗放在根治性手术之前进行。
TNT可早期消除潜在微转移病灶,增加肿瘤的局部控制率,使更多的患者接受“等待-观察”策略,提高器官保留率,改善生活质量。
但TNT也延长了新辅助治疗结束到手术治疗之间的时间间隔,可能增加疾病进展的风险。
此外,双药或三药治疗、诱导化疗或巩固化疗、短程放疗联合化疗或长程放化疗等选择也是TNT研究的热点问题,需要进一步探索。
一、TNT提出的背景新辅助放化疗(neoadjuvant chemoradiotherapy,nCRT)联合全直肠系膜切除术和辅助化疗是NCCN推荐的局部进展期直肠癌标准治疗策略,其肿瘤学疗效已获得验证。
然而,标准治疗策略能否为直肠癌患者带来生存获益,尚存在较大争议。
文献报道,新辅助放疗联合根治性手术较单纯手术可改善直肠癌患者的5年总体生存率(58%比48%,P<0.05);但随后研究中又获得相反结论,尽管局部复发率降至10%以下,但nCRT组与非nCRT组的10年总体生存率(59.6%比59.9%)和远处转移率(29.8%比29.6%)相近,患者长期预后无改善。
另一方面,直肠癌患者对术后辅助化疗的依从性不佳。
EORTC 22921研究中,超过30%的适宜患者未接受辅助化疗,仅有50%接受辅助化疗的患者完成了规范的全部疗程。
2020年美国放射肿瘤学会ASTRO指南 直肠癌放射治疗更新要点(汇总表)
中等
4. 放疗剂量及放疗技术
对于T3-4和/或N+直肠癌患者,建议临床靶区体积(CTV)包括直肠,直肠系膜淋巴结,骶前区淋巴结,髂内淋巴结和闭孔淋巴结
强
高
对于肿瘤累及盆腔前器官(如前列腺,精囊腺,子宫,阴道,膀胱)的直肠癌患者,CTV有条件推荐包括直肠,直肠系膜淋巴结,骶前区淋巴结,髂内淋巴结、闭孔淋巴结和髂外区域淋巴结
a.患者将永久带结肠造口或TME手术后大便不完全失禁,并且;
b.拒绝TME手术,并且;
c.局部切除术后≤ypT1和R0切除,并且;
d.同意多学科团队密切随访。
有条件
中等
对于考虑非手术或局部切除的直肠癌患者,推荐常规分割同步放化疗,50-54Gy/25-30次
强
中等
对于考虑非手术或局部切除的直肠癌患者,有条件推荐常规分割同步放化疗之外的诱导或间歇期巩固化疗
2020年美国放射肿瘤学会ASTRO指南 直肠癌放射治疗更新要点(汇总表)
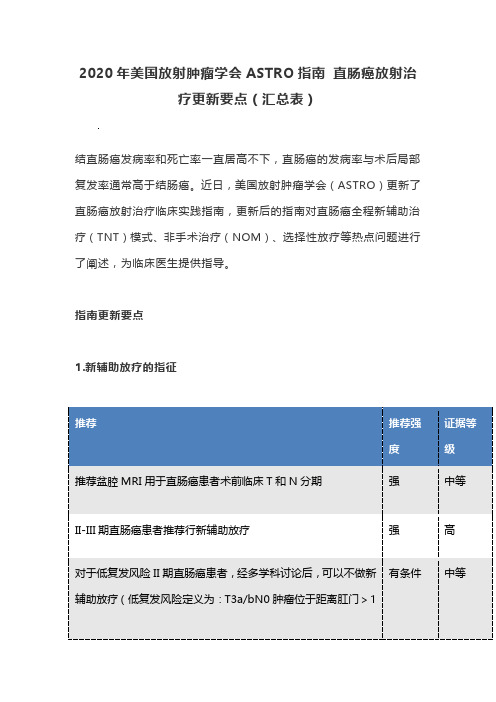
结直肠癌发病率和死亡率一直居高不下,直肠癌的发病率与术后局部复发率通常高于结肠癌。近日,美国放射肿瘤学会(ASTRO)更新了直肠癌放射治疗临床实践指南,更新后的指南对直肠癌全程新辅助治疗(TNT)模式、非手术治疗(NOM)、选择性放疗等热点问题进行了阐述,为临床医生提供指导。
有条件
低
对于肿瘤累及肛管的直肠癌患者,除直肠,直肠系膜淋巴结,骶前区淋巴结,髂内淋巴结和闭孔淋巴结外,CTV有条件推荐包括髂外区域淋巴结和腹股沟区域淋巴结
有条件
专家观点
对于接受放疗的直肠癌患者,有条件推荐使用IMRT / VMAT技术(IMRT/VMAT技术更适合需要包括髂外或腹股沟区域淋巴结时或当3DCRT可能会导致较高毒性反应时)
2024新辅助治疗后临床完全缓解或近临床完全缓解直肠癌病人临床治疗策略要点(全文)

2024新辅助治疗后临床完全缓解或近临床完全缓解直肠癌病人临床治疗策略要点(全文)摘要对于直肠癌新辅助放化疗后达到临床完全缓解和(或)近临床完全缓解的病人,其临床治疗策略一直存在争议,包括全直肠系膜切除(TME)手术、局部切除和等待观察策略。
TME手术带来了相关风险,而非手术治疗策略在实现了器官保留、改善病人生活质量的同时,有望实现与TME相当的肿瘤学安全性。
等待观察策略避免了不必要的手术创伤和严重并发症的风险,随着新辅助治疗完全缓解率的持续提高,等待观察策略在直肠癌综合治疗的地位也必将进一步提升。
优化新辅助治疗策略、准确识别获益群体、提升完全缓解评估的精确性,以及优化随访监测和补救治疗机制,是器官保留肿瘤学安全性的重要保障。
但须注意,如盲目选择等待观察,存在潜在局部复发和预后受损风险,故建议在具有丰富直肠癌综合治疗经验的临床中心开展,并加强医患沟通,提高随访依从性,保障治疗结局。
对于局部进展期(T3~4/N+M0)直肠癌(locally advanced rectal cancer,LARC),新辅助放化疗(neoadjuvant chemoradiotherapy,nCRT)后行全直肠系膜切除(total mesorectal excision,TME)手术是指南推荐的标准治疗模式。
但TME也带来了严重的问题,包括围手术期死亡风险(2%)、吻合口漏风险(11%)、并发症再次手术风险(5%)以及性功能和泌尿功能障碍风险,而且接受腹会阴联合切除术的病人将行永久性结肠造口[1]。
LARC的治疗理念随着等待观察(watch and wait)策略的提出,发生了巨大的改变[2]。
越来越多的研究显示,等待观察策略对于新辅助治疗后临床完全缓解(clinical complete response,cCR)的病人具有良好的安全性和有效性[3-7]。
接受等待观察和局部切除的病人不会出现明显创伤或肠道功能变化,保证了病人的良好生活质量。
2020CSCO结直肠癌指南

2020CSCO结直肠癌指南结直肠癌是一种常见的恶性肿瘤,严重威胁着人们的健康。
2020CSCO(中国临床肿瘤学会)结直肠癌指南的发布,为结直肠癌的诊断、治疗和管理提供了重要的指导和参考。
接下来,让我们一起深入了解一下这份指南的主要内容。
首先,在诊断方面,指南强调了多种检查方法的综合应用。
对于疑似结直肠癌的患者,医生通常会首先进行直肠指检,这是一种简单而有效的初步检查方法,可以发现低位直肠的病变。
结肠镜检查则是诊断结直肠癌的金标准,不仅能够直接观察肠道内的情况,还可以获取组织样本进行病理检查,以明确肿瘤的性质和类型。
此外,影像学检查如 CT、MRI 等也在诊断中发挥着重要作用,有助于评估肿瘤的大小、位置、侵犯范围以及是否有转移。
在治疗方面,指南根据肿瘤的分期和患者的具体情况制定了个体化的治疗方案。
对于早期结直肠癌,手术切除往往是首选的治疗方法,并且可以达到较好的治疗效果。
对于局部进展期的结直肠癌,通常需要在手术前进行新辅助治疗,如放化疗,以缩小肿瘤、降低分期,提高手术切除的成功率和根治性。
而对于晚期结直肠癌,治疗则更加复杂和多样化,包括化疗、靶向治疗、免疫治疗等。
化疗是晚期结直肠癌治疗的重要手段之一。
常用的化疗药物有氟尿嘧啶、奥沙利铂、伊立替康等。
这些药物可以单独使用,也可以联合使用,以提高治疗效果。
靶向治疗则是针对肿瘤细胞特定的靶点进行治疗,如针对血管内皮生长因子(VEGF)的贝伐珠单抗、针对表皮生长因子受体(EGFR)的西妥昔单抗等。
免疫治疗是近年来结直肠癌治疗领域的新突破,对于具有特定生物标志物(如微卫星不稳定高表达/MSIH 或错配修复缺陷/dMMR)的患者,免疫治疗可以带来显著的生存获益。
在治疗过程中,患者的身体状况和治疗反应需要密切监测。
定期进行血常规、肝肾功能、肿瘤标志物等检查,以及通过影像学检查评估肿瘤的变化情况,以便及时调整治疗方案。
同时,患者的营养支持和心理护理也不容忽视。
良好的营养状况可以提高患者对治疗的耐受性,而积极的心理状态有助于患者更好地应对疾病。
2020ASCO结直肠癌免疫治疗新进展护理课件

对于严重过敏反应,应立即停止免疫 治疗,给予抗过敏药物及对症治疗。
对于需要住院治疗的不良反应,应积 极配合医生的治疗建议,确保患者安 全。
对于危及生命的免疫相关不良反应, 应立即就医,采取紧急抢救措施。
06
结直肠癌免疫治疗的未来展
望
研究方向与重点
1 2
免疫治疗联合其他治疗方式
研究免疫治疗与其他治疗方式(如化疗、放疗) 的联合应用,以提高治疗效果和减少副作用。
02
免疫治疗具有特异性高、副作用 相对较小的优点,可提高患者的 生活质量和生存期。
结直肠癌免疫治疗的历史与发展
结直肠癌免疫治疗的研究始于20世纪80年代,经过多年的探 索和发展,已经取得了一定的成果。
目前,结直肠癌免疫治疗已经成为临床研究的热点领域,多 种新型免疫治疗药物和技术正在研发和试验阶段,有望为结 直肠癌患者带来更好的治疗选择。
临床应用前景
免疫治疗在结直肠癌中的广泛应用
随着研究的深入和技术的进步,免疫治疗在结直肠癌的临床应用前景广阔。未 来,免疫治疗有望成为结直肠癌治疗的重要手段之一。
联合治疗策略的探索
为了进一步提高疗效,研究者们正在探索免疫治疗与其他治疗手段如化疗、放 疗等的联合应用策略,以期为患者提供更加有效的治疗方案。
治疗后的护理
康复指导
心理支持
指导患者进行适当的锻炼和康复训练 ,促进身体功能的恢复。
关注患者的心理健康,提供必要的心 理支持和辅导,帮助他们更好地适应 生活。
随访观察
定期对患者进行随访,观察病情变化 ,及时发现和处理复发或转移的情况 。
04
结直肠癌免疫治疗患者的心
理护理
患者的心理状态评估
焦虑、抑郁情绪
和安慰。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ASCO 2020直肠癌放疗进展全新辅助治疗
2020ASCO会议在美国芝加哥顺利召开,多项全新辅助治疗(Total Neoadjuvant Therapy,TNT)模式的研究作为局部进展期直肠癌治疗的亮点在今年的会议中进行了报道,包括短程放疗加巩固化疗对比长程放化疗的RAPIDO研究(4006),诱导化疗对比巩固化疗观察器官保留率的OPRA研究(4008),以及三药化疗联合放化疗的PRODIGE 23研究(4007)。
对于局部进展期直肠癌,传统的新辅助治疗模式是在新辅助放化疗之后进行全直肠系膜切除术(TME)和辅助化疗,这种治疗模式较辅助放化疗能显著降低局部复发率,但并没有带来生存的获益,远处转移是其主要失败模式,这可能和术后辅助化疗开始晚、完成率较低相关。
此外,对于低位局部进展期直肠癌的患者,不能保肛带来的功能损失,影响了患者的生活质量。
全新辅助治疗(TNT)模式把辅助化疗前移到术前,提高化疗顺应性,理论上能降低远处转移,改善远期生存,同时术前治疗模式的叠加,追求最大化的肿瘤退缩,可争取更高的完全缓解率,提高患者器官保留的可能性。
今年ASCO的多项研究,就对TNT的疗效进行了报道。
一、RAPIDO研究—短程放疗加巩固化疗对比长程放化疗
该研究是一项欧洲多中心、III期RCT研究,入组的是MRI评估具有高危因素的局部进展期直肠癌,至少包括下列因素之一:cT4a/b,
cN2,肠壁外血管侵犯(EMVI+), 直肠系膜筋膜侵犯(MRF+)或侧方淋巴结增大。
研究共入组了920例患者,随机分配到两组,试验组是5*5Gy短程放疗后进行6周期CAPOX或9周期FOLFOX4化疗后行TME手术,对照组是长程放化疗,同期给予卡培他滨单药,6-10周后手术,术后行辅助化疗。
研究的主要终点为疾病相关的治疗失败率(DrTF)。
在报道的结果中,两组治疗耐受性均较好,手术及术后并发症之间没有显著差异,短程放疗加化疗组的3年DrTF和远处转移率降低了7%左右,DrTF为23.9%,明显低于对照组的30.4%(P=0.019),远处转移率也更低(20.0% vs 26.8%,P=0.005),病理完全缓解率(pCR)在短程放疗加化疗组较对照组提高1倍(28.4% vs 14.3%,P<0.001),两组的局部复发率(8.7% vs 6.0%,P=0.09)、OS(89.1% vs 88.8%,P=0.59)之间无显著差异。
因此,RAPIDO研究中短程放疗加间隔期化疗的TNT治疗模式对于高危的局部进展期直肠癌能显著降低远处转移、疾病相关治疗失败率,增加pCR率,可能成为治疗的新选择。
二、OPRA研究—诱导化疗对比巩固化疗观察器官保留率
MSKCC发起了一系列关于直肠癌放化疗后观察等待的临床研究,OPRA是一项II期的多中心RCT研究。
该研究一共入组了324例局部进展期直肠癌患者,均按TNT模式进行治疗,随机分为诱导化疗组
和巩固化疗组,诱导化疗组首先进行8周期FOLFOX或6周期CAPOX 化疗,再行长程放化疗,放疗同期给予卡培他滨单药;巩固化疗组在长程放化疗以后再进行8周期FOLFOX或6周期CAPOX化疗。
患者在新辅助治疗后如果未达到临床完全缓解(cCR)则进行TME手术,如果达到cCR则进入等待观察。
该研究的主要研究终点为3年DFS,次要终点包括器官保留率, 无转移生存率(DMFS)等。
诱导组和巩固组两组的毒性反应间无显著差异,DFS(77% vs 78%,P=0.63)及DMFS(82% vs 84%,P=0.83)亦无显著差异。
值得注意的是,器官保留率在巩固组明显升高,TME-free的生存率在巩固组为59%,优于诱导组的43%(P=0.007)。
从OPRA研究的数据可以看出,以长程放化疗为基础的TNT治疗模式可以让半数患者在治疗后达到cCR,诱导化疗和巩固化疗对患者远处转移的控制上无明显差异,但是对于想争取观察等待的患者而言,放化疗后再行巩固化疗能让患者有更多机会达到cCR。
三、PRODIGE 23研究—三药化疗诱导在新辅助治疗中的探索
该研究是法国发起的多中心III期RCT研究,对照组是长程放化疗(CRT),放疗同期予以卡培他滨单药,TME术后进行12周期mFOLFOX6化疗;试验组是TNT模式,首先行6周期mFOLFIRINOX
化疗后再进行长程放化疗,放疗同期给予卡培他滨单药,TME术后进行6周期mFOLFOX6化疗。
该研究的主要研究终点为DFS。
pCR率在TNT组为27.8%,明显高于CRT组的12.1%(P<0.001),cCR+near cCR的比例在TNT组也更高(47.6% vs 31.8%,P=0.003)。
TNT组的3年DFS和DMFS均优于CRT组,分别为75.7% vs 68.5%(P=0.034),78.8% vs 71.7%(P=0.017)。
TNT组三药化疗的应用虽然带来了更多的血液学毒性,但整体耐受情况可。
综上,今年的ASCO会议中,上述三项研究结果的公布证实了TNT 模式设计之初期望探讨的问题:将辅助化疗前移至新辅助阶段,降低远处转移的发生,提高DFS,增加cCR率和肛门保留的机会。
尽管OS数据尚有待进一步随访,TNT治疗模式已经开启了局部进展期直肠癌治疗的新篇章,应成为局部进展期直肠癌治疗模式的新选择之一。
