电偶腐蚀
电偶腐蚀 寿命

电偶腐蚀寿命
电偶腐蚀是一种常见的金属腐蚀现象,它会对金属材料的寿命造成一定的影响。
下面我将以人类的视角,通过叙述和描述,来展现电偶腐蚀对寿命的影响。
我们来了解一下电偶腐蚀的概念。
电偶腐蚀是指两种不同金属接触时,在电解质溶液中,由于两种金属的电位差异,产生了电流,从而引发了金属的腐蚀现象。
这种腐蚀现象会导致金属表面出现腐蚀坑,金属材料逐渐减薄,甚至出现破裂。
电偶腐蚀对金属材料的寿命有着显著的影响。
首先,电偶腐蚀会加速金属材料的腐蚀速度。
当两种不同金属接触时,由于电位差异,会引发电流的流动,从而加速金属的腐蚀过程。
这意味着金属材料的使用寿命会缩短,特别是在电解质溶液中,腐蚀速度更快。
电偶腐蚀还会导致金属材料的性能下降。
由于金属材料的腐蚀,金属表面会出现腐蚀坑,导致金属材料的表面粗糙度增加。
这会对金属材料的摩擦和磨损性能产生不利影响,使得金属材料的使用寿命进一步缩短。
电偶腐蚀还可能导致金属材料的力学性能下降。
金属材料在电解质溶液中发生腐蚀后,其强度和韧性会受到一定程度的损害。
这意味着金属材料在受力时更容易发生变形和断裂,从而影响了其使用寿命。
电偶腐蚀对金属材料的寿命造成了不可忽视的影响。
它加速了金属材料的腐蚀速度,降低了金属材料的性能,从而缩短了金属材料的使用寿命。
因此,在实际工程中,我们应该采取相应的措施,如选择合适的金属材料、涂层保护等,来减缓电偶腐蚀的发生,延长金属材料的使用寿命。
电偶腐蚀

电偶腐蚀电偶腐蚀也叫以异金属腐蚀或接触腐蚀,是指两种不同电化学性质的材料在与周围环境介质构成回路时,电位较正的金属腐蚀速率减缓,而电位较负的金属腐蚀加速的现象。
构成这种现象的原因是这两种材料间存在着电位差,形成了宏观腐蚀原电池。
电偶腐蚀作为一种普遍的腐蚀现象,可诱导甚至加速应力腐蚀、点蚀、缝隙腐蚀、氢脆等腐蚀过程的发生。
产生电偶腐蚀应同时具备下述三个基本条件:第一,具有不同腐蚀电位的材料,电偶腐蚀的驱动力是被腐蚀金属与电连接的高腐蚀电位金属或非金属之间产生的电位差;第二,存在离子导电支路,电解质必须连续地存在于接触金属之间,构成电偶腐蚀电池的离子导电支路;第三,存在电子导电支路,即被腐蚀金属与电位高的金属或非金属之间要么直接接触,要么通过其他电子导体实现电连接,构成腐蚀电池的电子导电支路。
浸泡试验浸泡试验是常用的电偶腐蚀试验方法之一。
将两种不同金属按实际的面积比例制成一定形状的试样,紧固在一起,构成一组点偶对试样。
将上述电偶对试样暴露于腐蚀介质中进行腐蚀实验,并将其试验结果与在相同介质条件下未经偶接的这两种金属的腐蚀试验结果相比较,以判断电偶效应。
根据试验的目的和要求,采用失重测量、电阻测量和表观检查等方法,对比上述两组试验结果。
大气中的电偶腐蚀试验在实验技术上要比溶液中的试验容易一些。
因为在大气条件下,作为电解质的水膜具有相当高的电阻,这就限制了电偶作用的距离,从而限制了相对面积作用,即使是最不相容的金属,电偶作用也仅限于对接触线附近的5~6mm处。
电位测量电位测量包括电偶对中各个金属本身的自然腐蚀电位测量、偶对金属的电位差测量和金属偶接后的电偶电对测量。
电位测量是研究电偶腐蚀的重要手段,测试简单易行。
不同金属在接近实际使用介质条件下所测得的稳定开路电位的高低,标志着它们在该特定环境下相对的热力学稳定性。
因此,可根据开路电位的测量结果,预测不同金属偶接后的电偶效应。
在某些情况下,按金属在特定介质中稳定电极电位排列的电偶序中两种金属之间间隔远近来大致表征电偶效应的相对大小。
电偶腐蚀的原理

电偶腐蚀的原理
电偶腐蚀是一种电化学腐蚀方式,它是利用两种不同金属之间的电化学反应来腐蚀其中一种金属的过程。
这种腐蚀方式广泛应用于工业生产中,特别是在金属加工和制造领域。
电偶腐蚀的原理是基于两种不同金属之间的电化学反应。
当两种不同金属接触时,它们之间会形成一个电池,其中一个金属成为阳极,另一个金属成为阴极。
在这个电池中,阳极会发生氧化反应,阴极会发生还原反应。
这些反应会导致阳极金属的电子流失,而阴极金属则会吸收这些电子。
在电偶腐蚀中,通常会选择一种金属作为基材,另一种金属作为腐蚀剂。
当这两种金属接触时,腐蚀剂会成为阳极,而基材则成为阴极。
这样,腐蚀剂就会发生氧化反应,而基材则会被还原。
这些反应会导致腐蚀剂金属的电子流失,而基材金属则会吸收这些电子。
这样,腐蚀剂金属就会逐渐被腐蚀掉,而基材金属则不会受到损害。
电偶腐蚀的应用非常广泛。
在金属加工和制造领域,电偶腐蚀可以用来去除金属表面的氧化层、清除金属表面的污垢、改善金属表面的光洁度等。
此外,电偶腐蚀还可以用来制备金属纳米颗粒、制备金属薄膜、制备金属合金等。
电偶腐蚀是一种非常重要的电化学腐蚀方式,它可以用来改善金属表面的性质、制备新型材料等。
在未来的发展中,电偶腐蚀技术将
会得到更广泛的应用和发展。
电偶腐蚀机理

电偶腐蚀机理电偶腐蚀机理概述电偶腐蚀是一种利用高速流动的电解液在金属表面上形成微小的气泡和局部高温来加速金属表面的氧化和溶解的一种化学反应。
这种反应常用于制造微细结构,如芯片、微机械等。
本文将对电偶腐蚀的机理进行详细介绍。
电偶腐蚀原理当两个不同金属或合金在电解液中接触时,会形成一个电池,其中一个金属成为阴极,另一个金属则成为阳极。
在正常情况下,只有阳极会发生氧化和溶解反应,而阴极则不会受到影响。
但是,在电解液中引入外加电源后,阴极和阳极之间就会产生一定的电位差。
如果这个电位差足够大,就会使得阴极也开始发生氧化和溶解反应。
这种现象被称为“异质结点腐蚀”。
异质结点腐蚀可以通过以下公式来表示:Anode + e- → Anode+(氧化)Cathode+ + e- → Cathode(还原)总反应:Anode + Cathode+ → Anode+ + Cathode其中,Anode表示阳极,Cathode表示阴极。
电偶腐蚀的机理在电偶腐蚀中,金属表面会形成一层氧化物或氢氧化物。
这些物质会随着电解液的流动而被冲走,从而暴露出新的金属表面。
这个过程会不断重复,直到金属表面被完全溶解或者形成所需的微细结构为止。
电偶腐蚀的速率取决于以下几个因素:1. 电解液中的离子浓度离子浓度越高,反应速率就越快。
这是因为高浓度的离子可以提供更多的反应物质,并加速反应速率。
2. 电解液中的温度温度越高,反应速率就越快。
这是因为高温可以使得离子更加活跃,并提高它们与金属表面发生反应的可能性。
3. 外加电压大小外加电压越大,反应速率也就越快。
这是因为外加电压可以提供更多的能量来促进反应。
4. 金属本身的化学性质不同金属的化学性质也会影响反应速率。
一般来说,易氧化的金属(如铝、镁等)会比难氧化的金属(如铜、铁等)更容易发生腐蚀反应。
电偶腐蚀的应用电偶腐蚀常用于制造微细结构,如芯片、微机械等。
这是因为电偶腐蚀可以在金属表面形成非常细小的孔洞或凸起,从而实现对微小器件的精确加工。
电偶腐蚀测试方法介绍

电偶腐蚀测试方法介绍电偶腐蚀的定义及其原理电偶腐蚀也叫以异金属腐蚀或接触腐蚀,是指两种不同电化学性质的材料在与周围环境介质构成回路时,电位较正的金属腐蚀速率减缓,而电位较负的金属腐蚀加速的现象。
构成这种现象的原因是这两种材料间存在着电位差,形成了宏观腐蚀原电池。
电偶腐蚀作为一种普遍的腐蚀现象,可诱导甚到口速应力腐蚀、点蚀、缝隙腐蚀、氢脆等腐蚀过程的发生。
产生电偶腐蚀应同时具备下述三个基本条件:第一,具有不同腐蚀电位的材料,电偶腐蚀的驱动力是被腐蚀金属与电连接的高腐蚀电位金属期E金属之间产生的电位差;第二,存在离子导电支路,电解质必须连续地存在于接触金属之间,构成电偶腐蚀电池的离子导电支路;第三,存在电子导电支路,即被腐蚀金属与电位高的金属或非金属之间要么直接接触,要么通过其他电子导体实现电连接,构成腐蚀电池的电子导电支路。
电偶腐蚀原理如下图所示:图1电偶腐蚀原理示意图电偶腐蚀测试的意义及应用领域电偶腐蚀存在于众多的工业装置和工程结构中,它是一种最普遍的局部腐蚀类型。
轮船、飞机、汽车等许多交通工具都存在着异种金属的相互接触,都会引起程度不同的电偶腐蚀。
电偶腐蚀甚至存在于电子和微电子装备中,它们在临界湿度以上及腐蚀性大气环境下工作时,许多铜导线、镀金、镀银件与焊锡相接触而产生严重的电偶腐蚀。
纽约著名的自由女神铜像内部的钢铁支架发生的严重腐蚀就是因为发生了电偶腐蚀,许多钢铁支架锈蚀得只剩下原来的一半,抑钉也已脱落;同时在潮湿空气、酸雨等作用下,铜皮外衣也被腐蚀得比原先薄了许多。
据报道,各军兵种的军事装备由于电偶腐蚀,破坏了它们的可靠性,导致电子装备的早期失效,直接影响乃至丧失它们的作战能力。
在某些情况下,两种不同的金属虽然没有直接接触,在意识不到的情况下也有引起电偶腐蚀的可能。
例如循环冷却系统中的铜零件,由于腐蚀下来的铜离子可通过扩散在碳钢设备表面上沉积,沉积下的疏松的铜粒子与碳钢之间便形成了微电偶腐蚀电池,结果引起了碳钢设备严重的局部腐蚀。
电偶腐蚀机理

电偶腐蚀机理介绍电偶腐蚀是一种常见的电化学腐蚀形式,主要发生在导电材料与电解质接触的区域。
它是由于化学反应中的电子转移而导致的物质的损失。
电偶腐蚀机理是研究电偶腐蚀过程中所涉及的电化学反应的原理和规律。
电偶腐蚀的基本概念电偶腐蚀是一种以金属与金属之间的接触为前提的腐蚀反应。
它涉及到两种不同的金属,一个作为阳极而被腐蚀,另一个是阴极,充当电子的供应者。
在电解质中,阳极上发生了氧化反应,同时在阴极上进行了还原反应。
电偶腐蚀的原理1.电子转移:在电偶腐蚀中,阴极金属释放出电子,氧化成阳离子,这些电子流经导电路径,沿金属表面流动到阳极金属。
在阳极金属上,阳离子接受电子并还原成金属原子或化合物。
2.电解质:电偶腐蚀发生在电解质中,电解质提供了导电路径和氧化反应所需的物质。
电解质中的离子在腐蚀反应中起着重要的催化作用。
3.极性:在电偶腐蚀中,阳极金属氧化,所以它具有正极性。
阴极金属还原,所以它具有负极性。
极性差异导致电子流从阴极向阳极。
电偶腐蚀的影响因素1.金属的电位差:金属的电位差是产生电偶腐蚀的根本原因之一。
金属的电位差决定了阳极和阴极之间的电势差,从而影响到腐蚀的发生程度和速率。
2.电解质浓度:电解质的浓度对腐蚀速率有着直接的影响。
当电解质浓度增加时,离子的活动性增强,导致腐蚀速率加快。
3.温度:温度对电偶腐蚀过程中的反应速率起着重要的影响。
通常情况下,随着温度的升高,反应速率也增加。
4.金属的面积比:阴极和阳极的面积比对腐蚀速率有着重要的影响。
当阴极面积相对较大时,阳极的损耗会更加显著。
5.电偶腐蚀电流:由于电子流的存在,电偶腐蚀过程中会有一定的电流流过。
电流的大小取决于阳极和阴极的电位差以及电解质的性质。
电偶腐蚀的防护方法1.绝缘:在电偶腐蚀中,通过在阴极和阳极之间增加一个绝缘层,可以防止电流的流动,从而减少电偶腐蚀的发生。
2.电解质的控制:控制电解质的浓度可以减少电偶腐蚀的速率。
通过定期更换电解质或调整其浓度,可以有效地控制腐蚀过程。
电偶腐蚀名词解释

电偶腐蚀名词解释电偶腐蚀啊,就像是金属世界里的一场“爱恨情仇”大戏。
你可以把不同的金属想象成性格迥异的小伙伴。
比如说吧,活泼的金属就像是热情过头的莽撞小子,而不那么活泼的金属就像安静内敛的小淑女。
当这两种金属凑到一块儿,就像莽撞小子对小淑女穷追不舍,可这一追啊,就出事儿了。
在有电解质存在的情况下,就像是给他们俩搭了一个“舞台”,这个舞台可不得了。
活泼金属那家伙就开始迫不及待地“献殷勤”,把自己的电子送出去,就像一个散财童子似的,毫不吝啬。
而不活泼的金属呢,就像是被强行塞了一堆礼物的小淑女,很无奈。
这一送一接的过程,就导致活泼金属开始被腐蚀,就像那个莽撞小子在这场追逐中逐渐“掉血”,变得伤痕累累。
这电偶腐蚀啊,有时候速度快得就像一阵龙卷风席卷而来。
你要是在金属结构里不小心安排了这样一对“冤家”,那简直就是在金属里埋下了一颗定时炸弹。
就好比你盖了一座房子,用铁和铜做支撑结构,这就相当于把两个爱吵架的家伙关在了一个小房间里。
电解质呢,可能就是从外面偷偷溜进来的调皮小鬼,一下子就把气氛给搅和起来了。
铁就开始疯狂地牺牲自己,那腐蚀的样子就像一个在沙漠里干渴得迅速枯萎的仙人掌。
在船舶上也是一样,要是船身的金属部件搭配不好,就像组建了一个混乱的小团队。
那些活泼金属就像队伍里那个老是被欺负却又默默承受的小可怜,在海水这个大电解质的作用下,很快就被腐蚀得千疮百孔,就像被无数只小虫子啃咬过的破布。
电偶腐蚀的危害可不小,就像一个隐藏在暗处的小恶魔,悄悄地破坏着各种金属制品。
不管是你漂亮的金属首饰,还是那些大型的金属设备,只要遇上这个恶魔,就可能变得惨不忍睹。
它就像一个搞破坏的小能手,所到之处,金属的完整性就像脆弱的肥皂泡一样被轻易击破。
不过呢,也不是拿它没办法。
就像处理两个爱吵架的小伙伴,把他们分开就好了。
通过合理的选材、涂层保护等方式,就能避免电偶腐蚀这个调皮鬼捣乱啦。
要是把金属结构看成一个大家庭,那我们就得像智慧的家长一样,协调好家庭成员之间的关系,不让电偶腐蚀这个捣蛋鬼有机可乘。
贾凡尼效应 电偶腐蚀

贾凡尼效应电偶腐蚀全文共四篇示例,供读者参考第一篇示例:贾凡尼效应,即电偶腐蚀,是一种电化学现象,常见于金属表面在一定环境条件下发生的腐蚀现象。
这一现象通常发生在由两种不同金属组成的电偶中,其中一种金属更为活泼,而另一种金属则更为惰性。
在这种情况下,更活泼的金属会向惰性金属释放电子,从而导致惰性金属表面出现腐蚀现象。
贾凡尼效应的发生机制可以用以下几个步骤来描述:首先是在电偶中,更活泼的金属会发生氧化反应,将电子释放到电解质中;接着是惰性金属接受释放的电子,发生还原反应,氧化物还原为金属;在电偶中形成电子流动的闭路,电子会一直流动直到两种金属之间的电位差消除。
在这个过程中,更活泼的金属会不断向更惰性的金属释放电子,导致惰性金属表面逐渐被腐蚀。
贾凡尼效应的实际应用非常广泛,特别是在船舶、汽车、航空航天等领域,在这些应用中,由于不同金属构成的部件必须连接在一起,而连接处又容易受到腐蚀的影响。
了解和控制贾凡尼效应对于提高部件的使用寿命和可靠性至关重要。
为了减少贾凡尼效应带来的腐蚀问题,可以采取一些措施来控制或减轻这种现象。
可以通过选择相似电位的金属或使用耐腐蚀性更好的金属来减少金属之间的电位差,从而降低贾凡尼效应的发生。
可以在金属表面涂覆保护层,例如喷涂防护漆或热浸镀锌等方法,来隔离金属与电解质的接触,减少金属表面的腐蚀。
定期检查和维护金属部件,及时发现并处理潜在的腐蚀问题也是防止贾凡尼效应的关键。
通过定期检测部件的表面状况,及时清除腐蚀物质以及修复受损的部件,可以有效延长金属部件的使用寿命,并确保设备的正常运行。
贾凡尼效应是一种常见的金属腐蚀现象,特别是在多金属环境下。
了解该现象的发生机制以及采取相应的控制措施对于减少金属腐蚀问题至关重要。
只有通过有效的预防和维护措施,才能确保金属部件的长期可靠运行,延长设备的使用寿命。
希望通过本文的介绍,读者可以更深入地了解贾凡尼效应的影响以及如何有效地避免和控制该现象。
电偶腐蚀
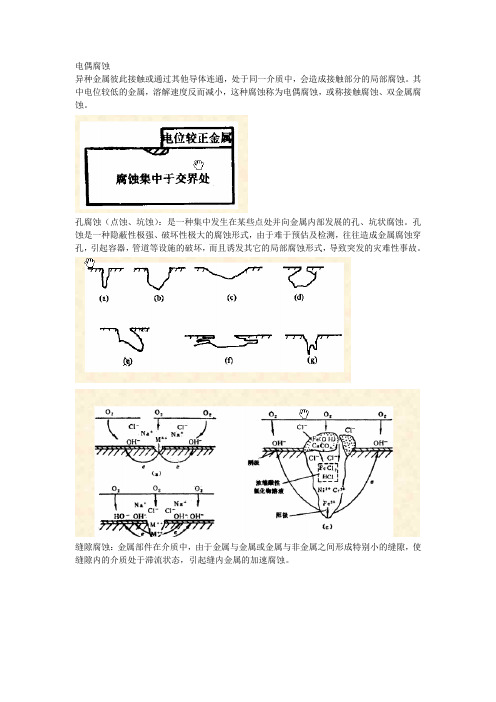
电偶腐蚀
异种金属彼此接触或通过其他导体连通,处于同一介质中,会造成接触部分的局部腐蚀。
其中电位较低的金属,溶解速度反而减小,这种腐蚀称为电偶腐蚀,或称接触腐蚀、双金属腐蚀。
孔腐蚀(点蚀、坑蚀):是一种集中发生在某些点处并向金属内部发展的孔、坑状腐蚀。
孔蚀是一种隐蔽性极强、破坏性极大的腐蚀形式,由于难于预估及检测,往往造成金属腐蚀穿孔,引起容器,管道等设施的破坏,而且诱发其它的局部腐蚀形式,导致突发的灾难性事故。
缝隙腐蚀:金属部件在介质中,由于金属与金属或金属与非金属之间形成特别小的缝隙,使缝隙内的介质处于滞流状态,引起缝内金属的加速腐蚀。
沿晶腐蚀:腐蚀沿着金属或者合金的晶粒边界或其它的邻近区域发展,晶粒本身腐蚀很轻微,这种腐蚀称为沿晶腐蚀,又叫做晶间腐蚀。
选择性腐蚀:合金在腐蚀过程中,腐蚀介质不是按合金的比例侵蚀,而是发生了其中某种成分的选择性溶解,使合金的机械强度下降,这种腐蚀形态称之为成分选择性腐蚀,或称为选择性腐蚀。
腐蚀疲劳:金属在腐蚀介质和交变力共同作用下引起的破坏为腐蚀疲劳。
磨损腐蚀:指在磨损和腐蚀的综合作用下材料发生的加速腐蚀破坏。
有三种表现形式:摩振腐蚀、湍流腐蚀和空泡腐蚀。
电偶腐蚀的原理

电偶腐蚀的原理电偶腐蚀是指在电化学腐蚀过程中,由于两种金属的电位差异而引起的一种金属腐蚀现象。
它是一种不可逆的电化学反应,经常发生在金属结构上,特别是在海洋和工业环境中。
电偶腐蚀在工程实践中经常引起金属结构的损坏,因此对其原理进行深入了解,可以有效预防和控制腐蚀的发生。
电偶腐蚀的原理可以通过电化学反应来解释。
当两种不同金属(或合金)以电导体的形式接触时,会形成一个电偶。
在这个电偶中,一种金属处于阳极位置,另一种金属处于阴极位置。
阳极金属会发生氧化反应,阴极金属则发生还原反应。
这些反应导致阳极金属的电子流向阴极金属,形成一个电流闭合回路。
电偶腐蚀的发生需要满足三个条件:第一,金属之间存在电位差。
这个电位差可以由金属的电化学特性和环境条件(如温度、湿度等)决定。
第二,金属之间存在电解质。
电解质可以是水、土壤、海水等,它们能导电并提供离子,促进电化学反应的进行。
第三,存在一个外部电源,提供电流以维持电偶中的反应。
电偶腐蚀的发生过程可以分为两个阶段:发生和传导。
在发生阶段,由于金属之间的电位差,阳极金属发生氧化反应,阴极金属发生还原反应。
在传导阶段,产生的电子从阳极金属流向阴极金属,形成一个电流闭合回路。
电偶腐蚀的速率取决于多种因素,包括金属的电化学特性、电解质的浓度和温度、电流密度等。
一般来说,金属的电位差越大,电偶腐蚀的速率越快。
此外,金属的电化学活性也会影响腐蚀速率,活性越高的金属腐蚀越快。
为了预防和控制电偶腐蚀,可以采取以下措施:首先,选择相似电位的金属进行接触,减小电位差,降低腐蚀速率。
其次,采用阴极保护技术,通过在金属表面施加电流,将金属表面变为阴极,减缓腐蚀反应的进行。
此外,合理设计金属结构,采用防腐涂层、隔离层等措施,可以有效降低电偶腐蚀的风险。
电偶腐蚀是由金属之间的电位差导致的一种金属腐蚀现象。
了解电偶腐蚀的原理对于预防和控制腐蚀非常重要。
通过选择相似电位的金属、采用阴极保护技术和合理设计金属结构等措施,可以有效减少电偶腐蚀的发生,延长金属结构的使用寿命。
电偶腐蚀

电偶腐蚀的影响因素4. 1 金属材料的起始电位差两金属在海水中的电位差是电偶腐蚀的必要条件和推动力,一般在工程设计中,异种金属接触电位差大于0. 25V 就不宜匹配使用,但这并不是绝对的,也有低电位差(45~60mV) 的异金属发生电偶腐蚀现象的实例,如海水中舰船钢(902 钢、921 钢)发生的电位电偶腐蚀。
图5 列出了滨海电厂海水循环水系统中常用材料的电偶序[2~4 ] 。
4. 2 海水流速对电偶腐蚀的影响通常,海水流速增加,金属材料的腐蚀电位向正方向移动,而在电偶腐蚀情况下,海水流速增加,会使偶对中阳极材料的腐蚀加剧,从静止海水增加到流速2m/ s 左右,电偶电流值会有数量级的增大,而滨海电厂海水循环水的流速一般都在2~4m/ s 之间,因此海水的流速会急剧增加循环水系统中存在电偶腐蚀区域的腐蚀速度。
表2 为低合金钢与几种金属材料在不同流速海水中电偶对的电偶电流值。
4. 3 其它方面的影响阴阳极面积比的影响:面积比增大可加快阳极腐蚀的速率,而减缓阴极腐蚀的速率。
当阴阳极面积比由1 ∶1 增大到 1 ∶5 时腐蚀速率会明显增大,可见面积效应对电偶腐蚀的影响很大,但面积比与腐蚀速率之间并没有简单的线形关系[5 ] 。
此外,极化作用、电偶对所处的介质条件对电偶腐蚀均有一定的影响要有效地防止电偶腐蚀的发生,首先要明确产生电偶腐蚀的必要因素:即发生电偶腐蚀必须存在腐蚀电解质,必须与电位较高的金属或非金属间有电接触。
因此,只要设法使其中一个条件不存在,就不会发生电偶腐蚀。
根据以上原则防止措施如下[2 ] :(1) 设计方面应注意的问题。
由不同金属组成构件时应尽可能选用电位相当的金属,应避免选用大阴极小阳极的结构件,实践表明,大阳极小阴极时,电位差控制在小于100mV ;小阳极大阴极时电位差应控制在10mV 以下且越小越好。
阳极部件要设计成易更换、易维修的结构和价廉的材料。
(2) 组装构件安装方面。
焊接时焊接材料的电位要比基体金属的电位高,一般为+ 5mV 以上。
电偶腐蚀发生条件

电偶腐蚀发生条件电偶腐蚀是一种常见的金属腐蚀现象,它发生的条件有很多方面。
本文将从电偶腐蚀的定义、原理、影响因素以及预防措施等方面进行探讨,以期对读者有所启发。
我们来了解一下电偶腐蚀的定义。
电偶腐蚀是指当两种不同金属或合金在电解质溶液中接触时,由于其电位差异而引起的一种腐蚀现象。
在这种情况下,其中一种金属(或合金)作为阳极,发生氧化反应,而另一种金属(或合金)则作为阴极,发生还原反应,从而导致金属的腐蚀。
电偶腐蚀的发生与多个因素密切相关。
首先是金属的电位差异。
当两种金属的电位差异较大时,电偶腐蚀的倾向性也会增加。
其次是电解质溶液的性质。
电解质溶液中的离子浓度、温度、pH值等因素都会对电偶腐蚀产生影响。
此外,还有金属的表面状态、氧气的存在以及外加电流等因素也会对电偶腐蚀的发生起到重要作用。
为了预防电偶腐蚀的发生,我们可以采取一些措施。
首先是选择相似电位的金属进行接触,以减小电位差异。
其次是在金属表面形成保护膜,如涂覆防腐涂料、进行阳极保护等。
此外,合理控制电解质溶液的性质,如控制离子浓度、维持适当的温度和pH值等,也是预防电偶腐蚀的有效手段。
总结起来,电偶腐蚀是一种由金属间电位差异引起的腐蚀现象。
它的发生与金属的电位差异、电解质溶液的性质以及其他因素密切相关。
为了预防电偶腐蚀的发生,我们可以选择相似电位的金属进行接触,形成保护膜,并合理控制电解质溶液的性质。
通过这些措施,我们可以有效地减少电偶腐蚀的发生,延长金属的使用寿命。
希望本文对读者对电偶腐蚀有所了解,并能在实际应用中采取相应的预防措施,以保护金属材料的完整性和使用寿命。
电偶腐蚀

目录:
1.电偶腐蚀的产生 2.电偶腐蚀的实验 3.电偶腐蚀的防护与控制
定义:金属自身在电解质溶液中发生 腐蚀溶解后,再接触或与自腐蚀电位 更高的金属电连接而使得腐蚀速率加 快的现象。(宏观,易于判别)
产生条件:
1.具有不同腐蚀电位的材料 2.存在离子导体支路 3.存在电子导体支路
形成机理:
根据混合电位理论,偶合的结果使得自腐蚀电位低的金
属腐蚀电流增大,产生阳极极化使之加速腐蚀,而自腐蚀电 位高的金属电流降低,作为阴极而被保护了起来。
Ec Ea Ig Pc Pa R Sc Sa
2015-4-20
影响因素:
1.材料自身特性(驱动力)
2.结构因素:阴阳极面积比值(影响氢过电位) 电偶对间距
谢 谢!
ห้องสมุดไป่ตู้
实验要求:
1.试样要求: a.长110mm,宽25mm,厚2~3mm的平板试样,Ra0.8 b.用汽油和酒精清洗后干燥器中放置七天 c.配对试样表面积需基本相等 d.试样间距5mm
2.腐蚀环境:电解液为化学氯化钠和蒸馏水,溶液体积400ml 电解液温度控制在30℃ 3.实验程序:试样在电解液中稳定30min测量各电极电位 连续测量和记录电偶电流20h,改过程中禁止搅动溶液 平行试验不少于三组
3.环境因素:介质组成,温度,pH值,应力 状态(可能引起电偶极性逆转)
实验方法:
1.浸泡试验:同时将电偶对试样和未经偶接的试样暴 露于同种腐蚀介质中进行腐蚀实验,采用失重测量、 表观检查等方法判断电偶效应。 2.电化学实验法:测量材料的自腐蚀电位和偶合后电 位,以及腐蚀过程中电流变化,极化过程来表征电偶 效应。
电偶序:金属或合金在某一确定电解质溶液中实测 而得的稳定电位相对大小排列而成的次序表。
电偶腐蚀电池电化学法

电偶腐蚀电池电化学法
电偶腐蚀,也称为双金属腐蚀或接触腐蚀,是一种电化学现象。
这种现象发生在不同金属在导电介质(如电解质溶液)中相互接触时。
由于不同金属具有不同的腐蚀电位,当它们接触时,会形成类似于电池的电偶系统。
在这个系统中,电位较正的金属充当阴极,而电位较负的金属则作为阳极。
以下是关于电偶腐蚀的一些详细信息:
- 阴阳极反应:在电偶腐蚀中,阴极发生的是还原反应,这会减缓其腐蚀过程。
相反,阳极发生的是氧化反应,导致该金属腐蚀加速。
因此,阳极金属在这种相互作用中被牺牲以保护阴极金属。
- 影响因素:电偶腐蚀的发生依赖于几个关键条件,包括不同腐蚀电位的金属材料、电子通道(即金属间形成的电连接),以及导电介质的存在。
- 防止措施:为了防止或减少电偶腐蚀,可以考虑使用防腐蚀涂层、选择电位接近的材料组合或者采用适当的设计来避免不同金属间的直接接触等方法。
总的来说,了解和研究电偶腐蚀对于工业应用和材料保护至关重要,可以帮助采取有效措施预防或减轻由电偶腐蚀引起的损害,从而延长设备的使用寿命并减少经济损失。
电偶腐蚀 寿命-概述说明以及解释

电偶腐蚀寿命-概述说明以及解释1.引言1.1 概述:电偶腐蚀是工业生产中常见的问题,指的是在两种不同金属或合金直接接触的环境中,由于电化学反应造成的一种腐蚀现象。
电偶腐蚀不仅会损坏设备和构件,还可能导致系统运行故障,甚至影响工业生产的正常进行。
因此,了解电偶腐蚀的定义、影响因素以及延长电偶腐蚀寿命的方法具有重要的意义。
本文将就电偶腐蚀的定义、影响因素和延长寿命的方法进行详细探讨,旨在帮助读者更好地了解电偶腐蚀问题,并提出有效的解决方案,以确保设备和构件的安全运行,延长其使用寿命。
在工业生产中,更好的了解和管理电偶腐蚀问题对提高设备可靠性,降低维修成本,提高设备寿命以及保证工艺安全稳定具有重要意义。
1.2 文章结构本文主要包括三个部分,分别为引言、正文和结论。
在引言部分中,将介绍电偶腐蚀和其寿命相关的基本概念,以及本文的研究目的。
在正文部分中,将分别讨论电偶腐蚀的定义、影响电偶腐蚀寿命的因素以及延长电偶腐蚀寿命的方法。
最后,在结论部分中,将对本文进行总结,强调电偶腐蚀寿命的重要性,并展望未来的研究方向。
整个文章结构清晰有序,希望读者能够通过本文更全面地了解电偶腐蚀及其寿命相关的知识。
1.3 目的:本文旨在探讨电偶腐蚀对系统寿命的影响,并分析影响电偶腐蚀寿命的因素,以及如何通过有效的方法来延长电偶腐蚀的寿命。
通过深入研究电偶腐蚀的定义和相关知识,我们可以更好地了解它对设备和系统的影响,为工程领域的从业者提供更多有益的建议和指导。
希望通过本文的介绍,读者能够加深对电偶腐蚀现象的认识,从而更好地应对和预防相关问题,保障系统的运行和使用寿命。
2.正文2.1 电偶腐蚀的定义电偶腐蚀是指由于金属材料的接触形成电化学电偶并处于不同的电位上,导致电流从一个金属到另一个金属的过程中,在电解质介质中发生的金属腐蚀现象。
在这种情况下,一个金属被作为阳极,另一个金属被作为阴极,阳极金属溶解,而阴极金属则得到保护。
电偶腐蚀的出现主要是由于金属之间的差电位和电解质介质的存在,导致了电流在金属之间流动,从而引起金属的氧化、溶解和腐蚀。
电偶腐蚀名词解释

电偶腐蚀名词解释
嘿,你知道啥是电偶腐蚀不?电偶腐蚀啊,就好比是一场悄悄进行
的“战斗”!比如说啊,有两种不同的金属,它们靠在一起,就好像两
个小伙伴。
但这可不是友好的相处哦!其中一个金属可能比较活泼,
就像个调皮捣蛋的家伙,而另一个相对不那么活泼,像是个安静的乖
孩子。
当它们在特定的环境中,比如潮湿的地方,那个调皮的金属就
会开始搞破坏啦!它会把自己的电子疯狂地往那个乖孩子金属身上送,自己慢慢就被腐蚀掉了,这可不就是自己作嘛!而那个乖孩子金属呢,虽然一开始没干啥坏事,但因为接收了这些电子,也会受到影响呢!
你说这冤不冤呀!
想象一下,这就像在一个班级里,有个调皮的同学总爱捉弄别人,
结果把自己也搭进去了,还连累了旁边无辜的同学。
电偶腐蚀不就是
这样嘛!再举个例子,像铁和铜放在一起,在有电解质的环境中,铁
就很容易变成牺牲品,被腐蚀得一塌糊涂,而铜可能还好好的呢。
电偶腐蚀可不是小事哦,它能在不知不觉中给金属制品带来大麻烦!比如那些长期在海水里的船只、埋在地下的管道等等,都可能因为电
偶腐蚀而受损。
这多让人头疼啊!所以啊,我们可得重视起来,想办
法去预防它。
我的观点就是,我们必须要充分了解电偶腐蚀的原理和特点,这样
才能更好地应对它呀!不能让它肆意妄为地破坏我们的金属宝贝们!
你说是不是呢?。
电偶腐蚀事件

电偶腐蚀事件
电偶腐蚀事件,是指在电化学反应中,由于电偶的存在,导致金属发生腐蚀现象。
这种现象在各种工业生产中经常出现,对设备的损害非常严重。
电偶腐蚀事件的原理是:当两种不同金属接触时,由于它们的电位不同,形成了一种电偶。
当液体中存在一些电解质时,电子和离子会在金属表面上发生反应,导致金属表面发生腐蚀。
由于电偶的存在,其中一种金属的腐蚀速度会比另一种金属快得多。
在工业生产中,电偶腐蚀事件经常出现在管道、储罐、换热器等设备中。
这些设备通常由不同种类的金属组成,而且在使用过程中经常接触到液体或气体。
如果不采取措施来防止电偶腐蚀事件的发生,设备的寿命会大大缩短,甚至会引起设备事故。
为了防止电偶腐蚀事件的发生,工业生产中通常采取以下措施:
1. 选择相似的金属材料组成设备,避免不同种类的金属接触。
2. 在金属表面涂覆保护层,例如喷涂或镀层等。
3. 在液体中加入缓蚀剂,减缓金属表面的腐蚀速度。
4. 定期对设备进行检查和维护,及时发现并处理可能存在的电偶腐蚀问题。
总之,电偶腐蚀事件是工业生产中常见的问题。
只有采取有效的措施来防止其发生,才能保证设备的正常运行和安全生产。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
不同材料的电偶腐蚀
海洋环境电势(V) 材料名称
+0.06到-0.05
生铁
-0.18
碳钢
-0.53
B30铜镍合金
-0.08到-0.12
B10铜镍合金
-0.19到-0.20
铝黄铜
-0.28到-0.36
錫黄铜
-1.5到-1.6
海洋环境电势(V) -0.60到-0.7ห้องสมุดไป่ตู้ -0.60到-0.72 -0.13到-0.22 -0.21到-0.28 -0.32 -0.24到-0.29
地址:钢厂 腐蚀方式:螺栓电偶腐蚀 材料:不同材质的不锈钢
地址:南海 腐蚀方式:电偶腐蚀 材料:碳钢和铝合金
地址:地埋管 腐蚀方式:电偶腐蚀 材料:不锈钢和铸钢管
地址:南海 腐蚀方式:电偶腐蚀 材料:铝合金和碳钢
电偶腐蚀的主要防止措施有: ①选择在工作环境下电极电位尽量接近(最好不超过50毫伏)的 金属作为相接触的电偶对; ②减小较正电极电位金属的面积,尽量使电极电位较负的金属表 面积增大; ③尽量使相接触的金属电绝缘,并使介质电阻增大; ④充分利用防护层,或设法外加保护电位。 选择防护方法时应考虑面积律的影响,以及腐蚀产物的影响等。
电偶腐蚀(galvanic corrosion )是由于腐蚀电位不同,造成同一 介质中异种金属接触处的局部腐蚀。
电偶腐蚀原理
由于腐蚀电位不同,造成同一介质中异种 金属接触处的局部腐蚀,就是电偶腐蚀,亦 称接触腐蚀或双金属腐蚀。该两种金属构成 宏电池,产生电偶电流,使电位较低的金属 (阳极)溶解速度增加,电位较高的金属 (阴极)溶解速度减小。所以,阴极是受到 阳极保护的。阴阳极面积比增大,介质电导 率减小,都使阳极腐蚀加重。发生电偶腐蚀 时,电极电位较负的金属通常会加速腐蚀,而电 极电位较正的金属的腐蚀则会减慢。
腐蚀微电池 合金中呈现不同电极电位的金属相、化合物、组分元素的贫化 或富集区,以及氧化膜等也都可能与金属间发生电偶现象,钝化与 浓差效应也会形成电偶型的腐蚀现象,这些微区中的电偶现象通常 称为腐蚀微电池,不称作电偶腐蚀。
材料名称 钛及钛合金 316不锈钢 304不锈钢 蒙乃尔合金 镍铝青铜 纯铜 镁合金
生物膜
形成过
程外部 因素
条件膜
可逆吸附 不可逆吸附 生物膜形成 部分生物膜脱落
