金属腐蚀与防护PPT课件
合集下载
金属的腐蚀与防护完整版PPT课件

数据分析与结果讨论
对实验数据进行处理和分析,提取金属内部或表面的缺陷信息,评 估金属的腐蚀程度和剩余寿命。
06 金属防护工程实践案例 分享
石油化工行业金属设备防护案例
案例一
某石化公司炼油厂塔器设备腐蚀防护。采用高分子复合涂层技术进 行防护,有效延长了设备使用寿命。
案例二
某油田输油管道腐蚀防护。采用阴极保护技术,结合涂层保护,降 低了管道的腐蚀速率。
阴极保护法
01
将被保护金属与外加直流电源的负极相连,使其成为阴极而防
止金属腐蚀的方法。
阳极保护法
02
将被保护金属与外加直流电源的正极相连,使其处于阳极电位
下成为钝态或致钝而防止金属腐蚀的方法。
牺牲阳极保护法
03
在被保护金属上连接电位更负的金属或合金作为阳极,使其在
腐蚀介质中优先溶解,从而保护被连接金属的方法。
金属的腐蚀与防护完 整版PPT课件
目录
CONTENTS
• 金属腐蚀概述 • 金属腐蚀类型及特点 • 金属防护方法及原理 • 不同环境下金属腐蚀与防护策略 • 金属腐蚀实验方法与检测技术 • 金属防护工程实践案例分享
01 金属腐蚀概述
腐蚀定义与分类
腐蚀定义
金属与周围环境发生化学或电化学 反应,导致金属性能劣化的现象。
案例三
某变电站高压开关柜金 属外壳腐蚀防护。采用 阴极保护技术,结合涂 层保护,降低了金属外 壳的腐蚀速率。
交通运输领域金属部件防护案例
案例一
某地铁列车车体腐蚀防护。采用 不锈钢车体材料,结合电化学保 护技术,提高了车体的耐蚀性。
案例二
某汽车制造厂车身钢板腐蚀防护。 采用镀锌钢板材料,结合涂层保 护技术,延长了车身的使用寿命。
对实验数据进行处理和分析,提取金属内部或表面的缺陷信息,评 估金属的腐蚀程度和剩余寿命。
06 金属防护工程实践案例 分享
石油化工行业金属设备防护案例
案例一
某石化公司炼油厂塔器设备腐蚀防护。采用高分子复合涂层技术进 行防护,有效延长了设备使用寿命。
案例二
某油田输油管道腐蚀防护。采用阴极保护技术,结合涂层保护,降 低了管道的腐蚀速率。
阴极保护法
01
将被保护金属与外加直流电源的负极相连,使其成为阴极而防
止金属腐蚀的方法。
阳极保护法
02
将被保护金属与外加直流电源的正极相连,使其处于阳极电位
下成为钝态或致钝而防止金属腐蚀的方法。
牺牲阳极保护法
03
在被保护金属上连接电位更负的金属或合金作为阳极,使其在
腐蚀介质中优先溶解,从而保护被连接金属的方法。
金属的腐蚀与防护完 整版PPT课件
目录
CONTENTS
• 金属腐蚀概述 • 金属腐蚀类型及特点 • 金属防护方法及原理 • 不同环境下金属腐蚀与防护策略 • 金属腐蚀实验方法与检测技术 • 金属防护工程实践案例分享
01 金属腐蚀概述
腐蚀定义与分类
腐蚀定义
金属与周围环境发生化学或电化学 反应,导致金属性能劣化的现象。
案例三
某变电站高压开关柜金 属外壳腐蚀防护。采用 阴极保护技术,结合涂 层保护,降低了金属外 壳的腐蚀速率。
交通运输领域金属部件防护案例
案例一
某地铁列车车体腐蚀防护。采用 不锈钢车体材料,结合电化学保 护技术,提高了车体的耐蚀性。
案例二
某汽车制造厂车身钢板腐蚀防护。 采用镀锌钢板材料,结合涂层保 护技术,延长了车身的使用寿命。
金属腐蚀与防护高温氧化课件.ppt

• C可以还原Fe的氧化物但不能还原Al的氧化物 • “选择性氧化” ——合金表面氧化物的组成
合金氧化膜主要由图下方合金元素的氧化物所组成
第12页,共100页。
第13页,共100页。
∆G0-T 图
1. 各直线:相变
熔化、沸腾、升华和晶型转变
在相变温度处,特别是沸点 处,直线发生明显的转折
——体系在相变时熵发生了变化
5.1.2 氧化物固相的稳定性
• ∆G0
判断金属氧化物的高温化学稳定性
根据氧化物的熔点、挥发性来估计其固相的高温稳定性 低熔点易挥发氧化物的产生往往是造成灾难性高温腐蚀的
重要原因之一
1. 氧化物的熔点
估计氧化物的高温稳定性
金属表面生成液态氧化物
失去氧化物保护性
如:硼、钨、钼、钒等的氧化物
合金氧化时更易产生液态氧化物
• 蒸气压随温度升高而增大,即氧化物固相的稳定性随温度升 高而下降
• 高温腐蚀中形成的挥发性物质
加速腐蚀过程
• 挥发性氧化物影响碳、硅、钼、钨和铬等的高温氧化动力学
第28页,共100页。
氧化物的挥发性
• 挥发性物质的热力学平衡图
• 例:Cr-O体系,1250K ,高温氧化 只生成Cr2O3一种致密氧化物 Cr(气)、CrO(气)、CrO2(气)和 CrO3(气)4种挥发物质 凝聚相-气相平衡有 2种类型
第30页,共100页。
氧化物的挥发性
• Cr-O体系的固有性质:
– pO2较低时,Cr(气)的蒸气压最大 – pO2较高时,CrO3(气)的蒸气压最大
• 影响铬及含铬合金的氧化
– 在Cr2O3膜与基体之间将产生很大的Cr(气)的蒸气压,使Cr2O3膜 与基体分离;
合金氧化膜主要由图下方合金元素的氧化物所组成
第12页,共100页。
第13页,共100页。
∆G0-T 图
1. 各直线:相变
熔化、沸腾、升华和晶型转变
在相变温度处,特别是沸点 处,直线发生明显的转折
——体系在相变时熵发生了变化
5.1.2 氧化物固相的稳定性
• ∆G0
判断金属氧化物的高温化学稳定性
根据氧化物的熔点、挥发性来估计其固相的高温稳定性 低熔点易挥发氧化物的产生往往是造成灾难性高温腐蚀的
重要原因之一
1. 氧化物的熔点
估计氧化物的高温稳定性
金属表面生成液态氧化物
失去氧化物保护性
如:硼、钨、钼、钒等的氧化物
合金氧化时更易产生液态氧化物
• 蒸气压随温度升高而增大,即氧化物固相的稳定性随温度升 高而下降
• 高温腐蚀中形成的挥发性物质
加速腐蚀过程
• 挥发性氧化物影响碳、硅、钼、钨和铬等的高温氧化动力学
第28页,共100页。
氧化物的挥发性
• 挥发性物质的热力学平衡图
• 例:Cr-O体系,1250K ,高温氧化 只生成Cr2O3一种致密氧化物 Cr(气)、CrO(气)、CrO2(气)和 CrO3(气)4种挥发物质 凝聚相-气相平衡有 2种类型
第30页,共100页。
氧化物的挥发性
• Cr-O体系的固有性质:
– pO2较低时,Cr(气)的蒸气压最大 – pO2较高时,CrO3(气)的蒸气压最大
• 影响铬及含铬合金的氧化
– 在Cr2O3膜与基体之间将产生很大的Cr(气)的蒸气压,使Cr2O3膜 与基体分离;
金属的腐蚀与防护_课件

实验1.铁的吸氧腐蚀(实验分析)
将金属置于不同条件下(例如电解池、原电池,或直接与氧化 剂接触......),你能否判断其腐蚀的快慢?
判断依据: 电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐 蚀>有防护措施的腐蚀 同一金属在不同物质中腐蚀的快慢: 强电解质>弱电解质>非电解质
练习 1.下列情况下,海水中铁腐蚀最快的是( B )
实验1.铁的吸氧腐蚀(步骤与现象) 把铁钉置于具支试管中,胶塞塞好,导管伸入水面下。
实验1.铁的吸氧腐蚀(步骤与现象) 随着反应的进行,导管处倒吸的水柱越来越高。
实验1.铁的吸氧腐蚀(实验分析)
为什么导管处会有倒吸的水柱? 铁钉发生电化学腐蚀,消耗了具支试管中的氧气,气压 减小,大气压将试管中的水压入导管中。
金属腐蚀的类型
化学腐蚀
条件
金属跟氧化性 物质直接接触
现象
无电流产生
电化学腐蚀 不纯金属或合金跟电解 质溶液及氧化剂接触
有微弱的电流产生
本质
金属被氧化的过程
较活泼的金属 被氧化的过程
相互关系
化学腐蚀与电化学腐蚀往往同时发生
实验1.铁的吸氧腐蚀(步骤与现象)
钢铁为什么在潮湿空气中容易生锈?除了潮湿空气还需要什 么条件?让我们一起来看一下这个实验~
蚀下去,最终整个铁制品都被腐蚀。
金属的电化学腐蚀一般既有析氢腐蚀又有吸氧腐蚀,以后者为主。
实验1.铁的吸氧腐蚀(实验分析)
了解了电化学腐蚀后,请你想想下面的问题: ①为什么说金属的电化学腐蚀比化学腐蚀危害程度更大? 金属制品往往有杂质,表面形成许多原电池,因此电化学腐 蚀现象就比较普遍;且电化学腐蚀(原电池反应)速度更快 。
金属的腐蚀在生活中非常普遍:
人教版高中化学选修1 3.2 金属的腐蚀和防护 课件(21张PPT) (共21张PPT)

【小试牛刀】
下图是铁钉在某溶液中被腐蚀的实验(开始时试管中液面和试管外 液面等高)。[来源:学科网ZXXK]
(1)甲、乙两图溶液中呈酸性的是___乙_____(填“甲”或“乙”)。 (2)甲图电极反应式是:正极___2_H__2_O__+_O__2_+__4_e_- _=__4__O_H__-___ 负极____F_e_-__2__e-_=__F_e_2_+___________
接触部分有 部份有较 有较多铁锈,
铁锈
多铁锈
下半部分有气 泡
结论
【科学探究】不同条件下铁钉的腐蚀
实验
一周后 铁钉生 锈程度
结论
煮沸冷
却蒸馏
蒸馏水
NaCl溶液
醋酸溶液
①
②水
③
④
⑤
铁钉表面 铁钉表面 铁钉与水面 铁钉上半
无锈蚀 无锈蚀 接触部分有 部份有较
铁锈
多铁锈
铁钉与空气、水同时接触才会发生锈蚀,与NaCl溶液、
【小组讨论】
2、结合原电池理论,分析实验⑤的腐蚀现象
正负极材料? 正负极反应物? 电解质溶液?
析氢腐蚀(水膜酸性较强)
钢铁的析氢腐蚀和吸氧腐蚀比较
析氢腐蚀
条 件
水膜呈_较__强__酸__性
吸氧腐蚀 水膜呈中__性__或__酸__性__很__弱__
电 负极Fe
极 正极C
反 应
总反应:
Fe-2e-=Fe2+
(3)乙图中发生反应的离子方程式是
____F_e_+__2_H__+_=__F_e_2_+_+_H__2↑______。
被口水冲垮的大桥
【小组讨论】
金属的腐蚀和防护PPT精品课件

含义
金属直接与具有腐蚀 性的化学物质接触发 生氧化还原反应而消
耗的过程
金属与电解质溶液 接触发生原电池反
应而消耗的过程
发生的 金属 条件 氧化剂
电子得失
金属或合金 非电解质为主(如O2、
Cl2、C2H5OH)
金属直接将电子转移 给有氧化性的物质
不纯金属或合金 电解质溶液中的溶
质 活泼间接转移给氧 化金属将电子性较
【基础题一】 (1)下列有关金属腐蚀的说法正确的 是( D ) A.金属腐蚀指不纯金属与接触到的电解质溶液进 行化学反应而损耗的过程 B.电化腐蚀指在外加电流的作用下不纯金属发生 化学反应而损耗的过程 C.钢铁腐蚀最普遍的是吸氧腐蚀,负极吸收氧气 最终转化为铁锈 D.金属的电化腐蚀和化学腐蚀本质相同,但电化 腐蚀伴有电流产生
1.(湖南祁东县鼎兴补习学校2010届高三化学第一次 月考)下列叙述不正确的是( A ) A.铁表面镀锌,铁作阳极 B.船底镶嵌锌块,锌作负极,以防船体被腐蚀 C.钢铁吸氧腐蚀的正极反应:
O2+2H2O+4e-===4OH- D.工业上电解饱和食盐水的阳极反应:
2Cl--2e-===Cl2↑
2.下列有关金属腐蚀与防护的说法正确的是(双 选)( AC ) A.纯银器表面在空气中因化学腐蚀渐渐变暗 B.当镀锡铁制品的镀层破损时,镀层仍能对铁制 品起保护作用 C.在海轮外壳连接锌块保护外壳不受腐蚀是采用 了牺牲阳极的阴极保护法 D.可将地下输油钢管与外加直流电源的正极相连 以保护它不受腐蚀
答案:(1)Mg+2H+===Mg2++H2↑
(2)2Al+Fe2O3
Al2O3+2Fe
(3)2H2O+O2+4e-===4OH-
(4)Al-3e-===Al3+ 铝表面易被氧化,生成一层致
高中化学新人教版化学选择性必修1金属的腐蚀与防护 课件(44张)

解析:酸性环境中,钢铁形成原电池发生析氢腐蚀,铁作负极,发生氧化反应,
电极反应式为 Fe-2e-===Fe2+,A 正确;钢铁表面水膜的酸性较弱或呈中性时, 发生吸氧腐蚀,正极为氧气得电子发生还原反应,电极反应式为 O2+4e-+ 2H2O===4OH-,B 正确;外加电流法是利用电解池原理让被保护的金属连接电源 的负极作为阴极,惰性电极作为辅助阳极,若被保护的金属作阳极将会发生氧化
关键能力培养
探究与创新能力
《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴 趣。“修旧如旧”是文物保护的主旨。
(1)查阅高中教材得知铜锈为 Cu2(OH)2CO3,俗称铜绿,可溶于酸。请写出铜绿 与盐酸反应的化学方程式。
提示:Cu2(OH)2CO3+4HCl===2CuCl2+3H2O+CO2↑。
反应而被腐蚀,C 错误;锅炉内壁镶嵌镁块,形成原电池,镁作负极被氧化,钢
铁作正极被保护,D 正确。
答案:C
2.如图是金属牺牲阳极法的实验装置,下列有关说法正确的是
()
A.该装置为电解池 B.本实验牺牲了金属 Fe 来保护金属 Zn C.若加入 K3[Fe(CN)6]溶液后,Fe 电极附近不会产生特征的蓝色沉淀 D.远洋货轮上镶嵌的金属 Zn 长时间没有什么变化,不需要更换
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有 Cu2(OH)2CO3 和 Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
Cu2(OH)2CO3 和 Cu2(OH)3Cl 分别属于无害锈和有害锈,请解释原因。 提示:结合图可知,Cu2(OH)2CO3 为致密结构,可以阻止潮湿空气进入内部 进一步腐蚀铜,属于无害锈。Cu2(OH)3Cl 为疏松结构,潮湿空气可以进入空隙内 将内部的铜进一步腐蚀,属于有害锈。
金属腐蚀与防护ppt课件
阳极 (Fe) :Fe(s)
Fe2+ (aq) + 2e-
阴极(杂质): 1/2 O2 + H2O + 2e-
2OH- (aq)
总反应: Fe(s) + 1/2O2 (g) + H2O
Fe(OH)2 (s)
2Fe(OH)2 (s) H2O+O2 Fe(OH)3 (s)
条 件: 弱酸性、中性或碱性介质
原理,将工件加工成型的一种技术。
电解液的要求:
有良好的导电性 不使阳极产生钝化 有利于阳极溶解
电流
—
直流电源 电压
+
阴极(模件) 阳极(工件)
泵
电解液
电解加工示意图
2. 金属的防腐
1、正确选材 2、覆盖保护层
要 求:
a. 膜层致密,完整无孔,不透介质; b. 与基体金属结合强度高,附着力强; c. 高硬度,耐磨; d. 均匀分布。
① 金属保护层
镀层 > 基体
例如: 铜上镀银、金,铁上镀锡,主要起 隔离和装饰作用。
镀层 < 基体
例如:铁上镀锌,主要起防腐作用。
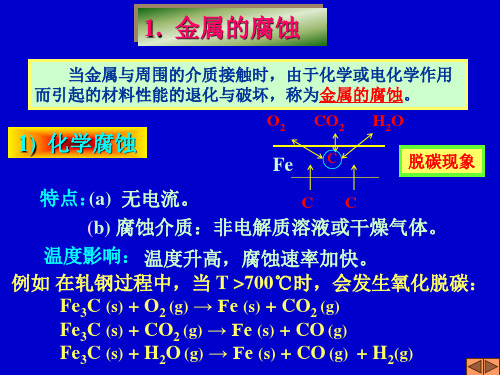
1. 金属的腐蚀
当金属与周围的介质接触时,由于化学或电化学作用 而引起的材料性能的退化与破坏,称为金属的腐蚀。
1) 化学腐蚀
O2 CO2
Fe C
H2O 脱碳现象
特点:(a) 无电流。
CC
(b) 腐蚀介质:非电解质溶液或干燥气体。
温度影响: 温度升高,腐蚀速率加快。
例如 在轧钢过程中,当 T >700℃时,会发生氧化脱碳:
难溶性碳酸钙覆盖于阴极表面,使电极的极化电势降低,阻滞 阴极反应继续进行,从而减缓金属的腐蚀速率。
金属的腐蚀与防护ppt课件

牺牲阳极保护法 外加电流的阴极保护法
21
总反应: Fe + 2H+ =Fe2+ + H2↑
★析氢腐蚀和吸氧腐蚀都属于电化学腐蚀
9
条件
化学腐蚀
金属与干燥气体或非电 解质液体直接接触
电化学腐蚀
不纯金属或合金与电解 质溶液接触
现象 无电流产生
有微弱电流产生
本质 金属被氧化
较活泼金属被氧化
影响 与接触物质的氧化性及 与电解质溶液的酸碱性
因素 温度有关
化学 · 选修4《化学反应原理》
1.3 金属的腐蚀与防护
1
钢 铁 生 锈
2
铜 器 生 锈
3
金属腐蚀 • 我国是世界上钢铁产量最多的国家,每年被腐蚀的铁占到我国钢铁
年产量的十分之一,因为金属腐蚀而造成的损失占到国内生产总值 的2%~4%;约合人民币3000亿元 。 • 根据各国调查结果,一般说来,金属腐蚀所造成的经济损失大致为 该国国民生产总值的4%左右。 • 另据统计,金属腐蚀的年损失远远超过水灾、火灾、风灾和地震(平 均值)损失的总和,在这里还不包括由于腐蚀导致的停工、减产和爆 炸等造成的间接损失。
4
一、金属的电化学腐蚀 1、 金属腐蚀 指金属或合金与周围环境中的物质发生化学反应而腐蚀损耗的现象。
➢金属腐蚀的本质 M – ne- → Mn+ (氧化反应)
化学腐蚀 ➢金属腐蚀的类型
电化学腐蚀
5
2、化学腐蚀 金属与其他物质直接接触反生氧化还原反应而引起的腐蚀
燃气灶的中心部位易生锈
食品罐头 放在南极80多年却很少生锈
及金属活性有关
联系 两者往往同时发生,电化学腐蚀更普遍
10
1、用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装 置及得到的图象如下,以下结论错误的是( C ) pH=2时,压强逐渐增
21
总反应: Fe + 2H+ =Fe2+ + H2↑
★析氢腐蚀和吸氧腐蚀都属于电化学腐蚀
9
条件
化学腐蚀
金属与干燥气体或非电 解质液体直接接触
电化学腐蚀
不纯金属或合金与电解 质溶液接触
现象 无电流产生
有微弱电流产生
本质 金属被氧化
较活泼金属被氧化
影响 与接触物质的氧化性及 与电解质溶液的酸碱性
因素 温度有关
化学 · 选修4《化学反应原理》
1.3 金属的腐蚀与防护
1
钢 铁 生 锈
2
铜 器 生 锈
3
金属腐蚀 • 我国是世界上钢铁产量最多的国家,每年被腐蚀的铁占到我国钢铁
年产量的十分之一,因为金属腐蚀而造成的损失占到国内生产总值 的2%~4%;约合人民币3000亿元 。 • 根据各国调查结果,一般说来,金属腐蚀所造成的经济损失大致为 该国国民生产总值的4%左右。 • 另据统计,金属腐蚀的年损失远远超过水灾、火灾、风灾和地震(平 均值)损失的总和,在这里还不包括由于腐蚀导致的停工、减产和爆 炸等造成的间接损失。
4
一、金属的电化学腐蚀 1、 金属腐蚀 指金属或合金与周围环境中的物质发生化学反应而腐蚀损耗的现象。
➢金属腐蚀的本质 M – ne- → Mn+ (氧化反应)
化学腐蚀 ➢金属腐蚀的类型
电化学腐蚀
5
2、化学腐蚀 金属与其他物质直接接触反生氧化还原反应而引起的腐蚀
燃气灶的中心部位易生锈
食品罐头 放在南极80多年却很少生锈
及金属活性有关
联系 两者往往同时发生,电化学腐蚀更普遍
10
1、用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装 置及得到的图象如下,以下结论错误的是( C ) pH=2时,压强逐渐增
金属的腐蚀与防护ppt课件

(2)在金属表面覆盖保护层 ①非金属保护层:如喷油漆、涂油脂。 ②金属保护层:如铁制品上镀铜、锌等。
铁制品镀锌,破损 后,仍能保护;
铁制品镀锡 ,破损 后,失去保护。
为什么?
(3)电化学防护法 ①牺牲阳极法
原理:原电池原理 要求:活泼性强的金属作负极,被保护金属作正极。
②外加电流法
原理:电解池原理 要求:被保护的金属与外接电源负极相连作阴极。
√C.可能产生Fe2O3·nH2O
D.腐蚀的总反应式一定是2Fe+O2+2H2O===2Fe(OH)2
12345
内容小结 04
课堂回顾
课后练习
1.金属腐蚀的电化学原理可用如图模拟。 (1)请写出有关电极反应式。 ①铁棒上电极反应式:_2_F_e_-__4_e_-_=__=_=_2_F_e_2_+_。 ②(2)碳该棒图上所电表极示反的应是式__吸:__氧_O-___2_(+填__2“_H_2析_O_氢_+_”_4_e或_-_=_“_=吸_=_4氧_O_H_”_)。腐蚀。 (3)若将O2撤走,并将NaCl溶液改为稀硫酸溶液,则此图可表示__析__氢__(填“析 氢”或“吸氧”)腐蚀原理;若用牺牲阳极的阴极保护法来保护铁棒不被腐蚀溶 解,则可将碳棒改为_锌__(_或__其__他__比__F_e_活__泼__的__金__属__)_棒。
2.科学态度与社会责任:认识金属腐蚀产生的危害和影响,培养防止金属腐蚀 的意识,熟知金属腐蚀常用的防护方法。
内容索引
NEIRONGSUOYIN
一、金属的腐蚀 二、金属的防护方法 三、练习 四、总结
金属的腐蚀 01
1.金属的腐蚀
(1)概念:金属发生 氧化还原反应 而引起损耗的现象。 实质:金属原子 失去电子 变为阳离子发生氧化反应
铁制品镀锌,破损 后,仍能保护;
铁制品镀锡 ,破损 后,失去保护。
为什么?
(3)电化学防护法 ①牺牲阳极法
原理:原电池原理 要求:活泼性强的金属作负极,被保护金属作正极。
②外加电流法
原理:电解池原理 要求:被保护的金属与外接电源负极相连作阴极。
√C.可能产生Fe2O3·nH2O
D.腐蚀的总反应式一定是2Fe+O2+2H2O===2Fe(OH)2
12345
内容小结 04
课堂回顾
课后练习
1.金属腐蚀的电化学原理可用如图模拟。 (1)请写出有关电极反应式。 ①铁棒上电极反应式:_2_F_e_-__4_e_-_=__=_=_2_F_e_2_+_。 ②(2)碳该棒图上所电表极示反的应是式__吸:__氧_O-___2_(+填__2“_H_2析_O_氢_+_”_4_e或_-_=_“_=吸_=_4氧_O_H_”_)。腐蚀。 (3)若将O2撤走,并将NaCl溶液改为稀硫酸溶液,则此图可表示__析__氢__(填“析 氢”或“吸氧”)腐蚀原理;若用牺牲阳极的阴极保护法来保护铁棒不被腐蚀溶 解,则可将碳棒改为_锌__(_或__其__他__比__F_e_活__泼__的__金__属__)_棒。
2.科学态度与社会责任:认识金属腐蚀产生的危害和影响,培养防止金属腐蚀 的意识,熟知金属腐蚀常用的防护方法。
内容索引
NEIRONGSUOYIN
一、金属的腐蚀 二、金属的防护方法 三、练习 四、总结
金属的腐蚀 01
1.金属的腐蚀
(1)概念:金属发生 氧化还原反应 而引起损耗的现象。 实质:金属原子 失去电子 变为阳离子发生氧化反应
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
9
吸氧腐蚀
析氢腐蚀
发生 钢铁表面吸附的水膜中溶有O2 钢铁表面吸附的水
条件
并呈极弱酸性或中性,反应中 O2得电子被还原为OHˉ
膜呈现较强酸性。 反应时有H2析出。
负 极
电极 正 反应 极
2Fe→2Fe2++4e-
O2+2H2O+4e-→4OHˉ
Fe→Fe2++2e2H++2e-→H2↑
总 2Fe+2H2O+O2= 2 Fe(OH)2
22
金属腐蚀快慢的比较
电解原理引起的腐蚀>原电池原理引 起的腐蚀>化学腐蚀>应用原电池原 理有保护的腐蚀>应用电解池原理有 保护的腐蚀
23
随堂演练
1.下列叙述中正确的是( ) ①锌跟稀硫酸制取氢气,加入少量硫酸铜溶
液能加快反应速率 ②镀层破坏后,白铁(镀锌的铁)比马口铁 (镀锡的铁)更易腐蚀 ③钢铁表面常易锈蚀生成 Fe2O3·xH2O
26
写在最后
经常不断地学习,你就什么都知道。你知道得越多,你就越有力量 Study Constantly, And You Will Know Everything. The More
You Know, The More Powerful You Will Be
27
谢谢你的到来
学习并没有结束,希望大家继续努力
反 应
4Fe(OH)2+2H2O+O2=4Fe(OH)3
Fe+2H+=Fe2++ H2 ↑
联系 通常两种腐蚀同时存在,后者(吸氧腐蚀)更普遍
10
金属的化学腐蚀与电化学腐蚀
金属腐蚀 的实质
种类
金属原子失去电子被氧化而消耗的过程:
M→Mn+ +ne-
化学腐蚀
电化学腐蚀
金属和其它物质直接接 不纯金属或合金发生原电池
(2) 电化学腐蚀
不纯的金属(或合金)跟电解质溶液接触时, 会发生原电池反应,比较活泼的金属失去电子而 被氧化。
5
(二)金属电化学腐蚀的原理
6
① 吸氧腐蚀(水膜呈碱性、中性或酸性很弱)
钢铁的吸氧腐蚀示意图
7
②析氢腐蚀 (水膜呈酸性)
钢铁的析氢腐蚀示意图
8
例1:埋在地下的输油铸铁管道,在下列各种情况
下,被腐蚀速度最慢的是
()
A. 在含铁元素较多的酸性土壤中
B. 在潮湿疏松透气的土壤中
C. 在干燥致密不透气的土壤中
D. 在含碳粒较多、潮湿透气的土壤中
例2:家用炒菜锅用水清洗放置后,出现红棕色的锈 斑。在此变化过程中不可能发生的化学反应是
A. 4Fe(OH)2+2H2O+O2 = 4Fe(OH)3 B. 2Fe+2H2O+O2 = 2Fe(OH)2 C. 正极反应:2H2O+O2+4eˉ→4OHˉ D. 负极反应:Fe→Fe3++3eˉ
Learning Is Not Over. I Hope You Will Continue To Work Hard
演讲人:XXXXXX 时 间:XX年XX月XX日
28
2. 在金属表面覆盖一层保护层
12
使 用 不 锈 钢
13
使用马口铁:在铁皮镀上千分之一 厘米的锡,可隔绝空气与水
14
在 金 属 表 面 烤 漆
15
交流·研讨
不同金属镀层对金属的保护作用一 样吗?
如果分别在铁制品表面镀上锌保护层 和锡保护层,请根据三种金属的原子失 电子能力的大小分析:当镀层局部破损 时,锌镀层和锡镀层还能对铁制品起保 护作用吗?
外加电源在金属表面形成保护膜
20
例3:为了避免青铜器生成铜绿,以下方法 正确的是 A. 将青铜器放在银质托盘上 B. 将青铜器保存在干燥的环境中 C. 将青铜器保存在潮湿的空气中 D. 在青铜器的表面覆盖一层防渗的高分子膜
21
课堂练习
例:下列各情况,在其中Fe片腐蚀由快到慢的顺序是
(5) (2) (1) (3) (4)
1
2
§1.3 化学能转化为电能——电池
三 、金属的腐蚀与防护
3
(一) 金属的腐蚀
1. 定义: 金属(或合金)跟周围接触到的气体
(或液体)反应而腐蚀损耗的过程。
化学腐蚀
2. 分类:
电化学腐蚀
3. 实质: 金属原子 失e氧化反应
金属阳离子
下一页
4
(1) 化学腐蚀
金属与接触到的干燥气体(如O2、Cl2、 SO2等)或非电解质液体(如石油)等直接发 生化学反应而引起的腐蚀。
原理 触发生氧化还原反应而 反应,使较活泼的金属失电
引起的腐蚀
子被氧化而引起的腐蚀
金
属 的
直接发生氧化还原反应 发生原电池反应
腐 蚀
区别
腐蚀过程无电流产生
有电流产生
金属被腐蚀
较活泼金属被腐蚀
联系
往往同时发生,但电化学腐蚀更普 遍,速率更快。
11
(三)金属的防护措施
1.改变金属的内部结构,使金属性质改 变,成为合金。
16
3. 电化学保护法
牺 牲 阳 极 保 护 法
17
牺牲阳极的阴极保护法示意图
18
2. 外加电流法
辅助阳Байду номын сангаас (不溶性)
外加电流的阴极保护法示意图
19
小结
金属防护的几种重要方法
①在金属表面覆盖保护层。 ②改变金属内部的组织结构,制成合金。 ③电化学保护法,即将金属作为原电池的
正极或电解池的阴极而受到保护。
A.都正确 B.①③ C.① D.②③
24
2.以下现象与电化学腐蚀无关的是( ) A. 黄铜(铜锌合金)制作的铜锣不易产
生铜绿 B. 生铁比软铁芯(几乎是纯铁)容易生锈 C. 铁制器件附有铜制配件,在接触处易
生铁锈 D. 银制奖牌久置后表面变暗
25
CLASS IS OVER! THANK YOU!
