关于有机化学第十章醛和酮课件
有机化学第二版第十章醛和酮

第十章 醛酮含有羰基的化合物:O H O CH3CCH3 O C CH3醛和酮:CH 3C羧酸 羧酸:CH3CO OHCOOH COOH COOHOH CH3CHCOOHO羧酸衍生物:CH3COCl (CH3CO) ( )2OCOOC 2H 5NHOβ-二羰基化合物:CH3CCH2COOC 2H5CH2COOC2H5 COOC2H5210 醛和酮教学大纲(醛和酮)醛和酮的结构与物理性质 醛和酮的结构与物理性质; 醛和酮的化学性质:1.与氢氰酸加成; 2.与亚硫酸氢钠加成; 3.与醇亲核加成; 4.与氨的衍生物反应; 5.与Grignard试剂加成; 试剂加成 6.醇醛缩合反应; 7 卤化和卤仿反应; 7. 卤化和卤仿反应 还 原 反 应 —— 催 化 加 氢 、 金 属 氢 化 物 还 原 、 Clemmenson 还 原 、 WolffKishner黄鸣龙还原、Cannizzaro反应;氧化反应)。
羰基 carbonylOR C H R O C R'醛(aldehyde)O R C O R C R' Ar H Ar O C O C R H酮(Ketone K t )Oβ αC H(R)CC脂肪族醛、酮芳香族醛、酮α,β-不饱和醛、酮4命名:O CH3CCH2CH2CHOO O CH3CCHCCH3 CH2CH=CH24-氧代戊醛3-烯丙基-2,4-戊二酮OO CHO环己酮CHO2'-氧代环己基甲醛CHO OH O CHO苯甲醛2-羟基苯甲醛 (水杨醛)呋喃甲醛 (糠醛)5z醛和酮的结构2spCσOδ C+δO键角接近 120 °1 C=O双键是由一个σ键和一个π键组成的。
2 羰基碳原子为 sp2杂化轨道与氧原子的 p 轨道和其它两个原子 形成三个 形成 个σ键 键,一个 个 p轨 轨道与氧原子的 与氧 子 p轨 轨道侧面交盖成 侧面交 成π键 键, 氧原子上另有两对孤对电子处于氧的s轨道和p轨道中。
李艳梅有机化学9醛和酮精品PPT课件

9 醛和酮
(Aldehydes and Ketones)
No Image
下页 返回 退出
基本内容和重点要求
No Image
n 醛、酮的分类、结构和命名 n 羰基上的亲核加成反应及机理 n 羟醛缩合反应 n 与氨衍生物的加成-消除反应,氧化还原反应 n 卤仿反应和康尼扎罗反应
重点要求掌握羰基上的亲核加成反应及机 理,羟醛缩合反应、康尼扎罗反应及在有机合 成中的应用,氨衍生物反应、卤仿反应及应用
反应机理
No Image
R
C (CH3)H
O OH O + ∶S
O
R
C (CH3)H
沸点:虽不能形成分子间氢键,但分子极性 较大,沸点比相对分子质量相当的醇低,但 高于相对分子质量相当的烷烃和醚
水溶性:醛、酮的羰基氧能和水分子形成氢 键,所以低级醛、酮可溶于水。
溶解性:醛、酮都能溶于有机溶剂。
No Image
上页 下页 返回 退出
9.3 醛、酮的化学性质
No Image
9.3.1 羰基的亲核加成反应 9.3.2 与氨及氨衍生物的反应 9.3.3 -氢的反应 9.3.4 氧化反应 9.3.5 还原反应 9.3.6 康尼扎罗反应 9.3.7 柏琴反应
1-苯基-1-丙酮
No Image
上页 下页 返回 退出
No mage
羰基的碳原 子参与成环 时,其命名 与脂肪族酮 相似,只是 在名称前加 一个“环” 字。
O
C H33-甲ຫໍສະໝຸດ 环己酮No Image上页 下页 返回 退出
9.2 醛、酮的物理性质
No Image
性状:甲醛为气体,C12以下的醛、酮为无 色液体,高级醛、酮为固体。
有机化学--醛和酮

羰基等吸电子基团活化-氢的能力有以下次序: CHO COPh COR CN COX CO2R CO2H
问题:薄荷酮、孟烷酮和异孟烷酮是三个具有光学活性的天然化合物:
O
O
O
(-)-薄荷酮
孟烷酮
异孟烷酮
试对以下现象提出合理的解释:
(1)在乙醇钠的乙醇溶液中放置一段时间,光学纯的 薄荷酮([]D = -32o)会变成消旋的薄荷酮([]D = 0)。
(2)用90%的硫酸处理,孟烷酮转变为孟烷酮和异孟 烷酮的混合物。
2、-卤化反应
O
X2
R CH3
O R CH2X
(X = Cl, Br或I)
酸催化过程:
O
H+
C R CH3
O+H
-H-
C
R CH2
H
+
OH
XX
OH X-
C
C
R CH2
R CH2 X
O
C
+ HX
R CH2 X
O
Br2 AcOH, H2O, 70oC
醛和酮
➢ 醛酮的命名,结构、物理性质 ➢ 醛酮的制备 ➢ 醛酮的反应
O C RH
醛
O C R R'
酮
O C R OH
羧酸
O C R OR'
酯
O C R NH2
酰胺
羰基 Carbonyl group 醛 Aldehydes 酮 Ketones
O C RX
酰卤
亲核加成 氢化还原
R (H)R'
C O
4-氧代戊醛
O
(R)-Carvone (R)-香芹酮
薄荷味
有机化学-第十章

10.2 醛酮的化学性质
如果利用NaHSO3与羰基化合物加成的可逆性,将 NaCN 与 α-羟基磺酸钠作用,使生成的 HCN 与分解出的羰基化合 物加成生成α-羟基腈,这样也可避免 HCN 的直接使用。 例如:
10.2 醛酮的化学性质
醛、酮与碳负离子的加成
Grignard 试剂,炔钠,Wittig试剂等,都含有碳负离子, 它们与羰基化合物的反应活性很高,有机合成上有广泛的 应用。
10.2 醛酮的化学性质
一、与氨、伯胺的反应
脂肪族醛、酮与氨、伯胺的反应可生成亚胺,也称为席夫 碱(Schiff base):
10.2 醛酮的化学性质
脂肪族醛、酮生成的亚胺中含的C=N双键在反应条件下不 是很稳定的,它易于发生进一步的聚合反应。芳香族的醛、 酮与伯胺反应生成的亚胺则比较稳定。
10.1 醛酮的结构及分类
在醛、酮分子中,羰基碳原子是以sp2 杂化状态与其它三 个原子构成键的,羰基碳原子的P轨道与氧原子上的P轨道 以相互平行的方式侧面重叠形成π键,即羰基是一个平面 构型的; 与羰基碳原子直接相连的其它三个原子处于同一平面内, 相互间的键角约为120度,而π键是垂直于这个平面的。
> > >
>
>
>
>
10.2 醛酮的化学性质
一、与水的加成
甲醛、乙醛、丙酮等小分子羰基化合物在水中的溶解性非 常好,这不仅是它们与水分子之间可以形成氢键,还在于 它们可以与水分子发生加成反应,生成了水合物; 这种水合物只有在水溶液中在一定浓度范围、一定的温度 下才是比较稳定的,游离的羰基水合物(同碳二元醇)是 极不稳定的,它将迅速脱水成为羰基化合物。
有机化学课件第十章醛酮1

2.5 与NaHSO3 加成
O HO S O
O C + NaHSO3
反应可逆
O
HO S O NaHSO3的亲核性
ONa C SO3H
H+(酸处理)
OH C SO3Na
白色结晶物
醛(芳香醛、脂肪醛) 脂肪族甲基酮,八个碳以下的环酮
应用:醛或甲基酮的 分析、纯化
3、醛酮羰基上的亲核加成反应(2)
❖ 分析:分子型亲核试剂的特点及与醛酮的加成
•特点分析
H Nu
水、醇、胺
•预测:直接与羰基加成
H OH H OR H NHR H NR2
✓有活泼 H ✓亲核性不强
羰基亲电 性较弱
亲核能 力不强
O C
NuH
可逆
O C NuH
较易离去
•结论:
分子型亲核 试剂难直接 与羰基加成
3、醛酮羰基上的亲核加成反应(2)
•预测: H+存在下与羰基加
成
H+
O
Jones 试剂
Oppenauer 氧化
二、醛酮的制备
❖氧化烯烃
例:
有合成意 义的反应
二、醛酮的制备
3、芳香酮的合成
芳香酮
三、醛、酮的化学性质
性质分析
羰基氧有弱碱性 可与酸结合
R1
R2
C
α碳有吸电子基
H
α氢有弱酸性
碳与氧相连
O
氢易被氧化
C H(R)
羰基碳有亲电性 可与亲核试剂结合
α氢与碱的反应
OR
OR
半缩醛(酮) 一般不稳定
例1:生成缩醛(酮)
CHO
2 CH3OH HCl
缩醛(酮) 碱性和中性中稳定
大学化学(有机物医学)第十章醛和酮.pptx(授课讲义)

H
C H
σ键
O
H
116.6°
sp2
C O
H H
C
δ
+
O
δ
-
H
平面分子
121.7°
甲醛的结构
三、醛和酮的物理性质
1. 沸点
正戊烷 乙醚 丁醛 丁酮 Mw 72 72 34.6 72 76 72 80 丁醇 丙酸 74 118 74 141
bp/℃ 36
羧酸 醇 醛、酮 烷烃、醚
氢键
极性
2. 溶解性
甲醛、乙醛、丙酮易溶于水 6个碳以上醛、酮不溶于水
3. 气味
用作香精、化妆品、食品 等,如 O
茉莉酮
福尔马林(40%的甲醛水溶液)
四、醛和酮的化学性质
醛、酮分子中含有活泼的羰基,可以 发生多种化学反应。
氧化反应 还原反应
亲核加成
OdC C +
d
R (H)
H
α-C及α-H的反应
(一)亲核加成反应
—C=O 与烯键 —C=C— 在结构上有相似之处,能发生 一系列加成反应。但烯烃的加成属于亲电加成;羰基的加 成属于亲核加成。亲核加成是醛酮最为特征的反应。
OH
HCN
R C R'(H) CN -氰醇(-羟基腈)
NaCN + H2SO4
毒性、危险性问题
反应物要求:醛、脂肪族甲基酮和8个碳以下的环酮
1
下列各化合物可否与HCN加成?
A. CH3(CH 2) 2CH O
B.
O
C. C6H 5CH O
O
D. CH3
C CH2C6H5
E. C6H 5COCH 3
实验 醛、酮与2,4-二硝基苯肼的反应
有机化学第10章 醛和酮

Witting反应是在醛酮基碳所在处形成碳碳双键的一个重要方法,产物中 没有双键位置不同的异构体。反应条件温和,产率也较好,但产物双键 的构型较难控制。 Witting也因该工作而与Brown H C共享了1979年的诺 贝尔化学奖。 另一种类型的磷叶立德试剂是霍纳(Horner L)提出的:用亚磷酸 酯为原料来代替三苯基膦与溴代乙酸酯得到的试剂磷酸酯,后者在强碱 作用下形成Horner试剂。
另一种类型的磷叶立德试剂是霍纳(Horner L)提出的:用亚磷酸 酯为原料来代替三苯基膦与溴代乙酸酯得到的试剂磷酸酯,后者在强碱 作用下形成Horner试剂。
补充: 醛、酮与炔化钠的加成
R-CC-Na+ NaNH2 (-NH3) R-CCH +
C=O
NH3(液) 或乙醚
C C ONa CR H O 2
• 醛和脂肪族甲基酮(或七元环以下的环酮)与之反应,生成
• -羟基磺酸钠
白色
过量
在酸碱下可逆反应,分离提纯
-羟基磺酸钠与等摩尔的NaCN作用,则磺酸基可被氰基取代, 生成 -羟基腈,避免用有毒的氰化氢,产率也比较高。
3、与醇的加成
*1 反应情况介绍 ① 与醛反应 CH3CH=O + CH3CH2OH
(hydrazine)
C 6H 5 H C O + H2NNH O2 N NO2
(hydrazone)
C 6H 5 H C NNH O 2N NO2 + H 2O
2,4–二硝基苯肼
O O + H2NNHCNH2
2,4–二硝基苯腙
O NNHCNH2 + H2O
氨基脲
(semicarbazine)
缩氨基脲 (半卡巴腙)
有机化学第十章醛酮PPT课件

在醇氧化制备醛的过程中,应控制反应条件,如温度、浓度、催化剂 等,以避免过度氧化或其它副反应的发生。
通过醇的氧化制备酮
总结词
醇氧化是制备酮的一种常用方法,常用的氧化剂有高锰酸 钾、硝酸、铬酸等。
详细描述
醇氧化制备酮的反应机理是醇分子中的羟基被氧化成羰基, 同时生成氢离子,常用的氧化剂可以将醇氧化成相应的酮, 同时生成水或其它相应的产物。
醛酮还可以用于合成生物活性分子,如激素、维生素等,对生命过程具有重要影响。
05 醛酮的制备方法
通过醇的氧化制备醛
总结词
醇氧化是制备醛的一种常用方法,常用的氧化剂有高锰酸钾、硝酸、 铬酸等。
详细描述
醇氧化制备醛的反应机理是醇分子中的羟基被氧化成羰基,常用的 氧化剂可以将醇氧化成相应的醛,同时生成水或其它相应的产物。
亲核加成反应
与氢氰酸加成
酮在氢氰酸的作用下,可以发生亲核加成反应, 生成相应的羟基腈。
与水加成
酮在水的作用下,可以发生亲核加成反应,生成 相应的醇。
与醇加成
酮在醇的作用下,可以发生亲核加成反应,生成 相应的酯。
亲电加成反应
与溴加成
01
酮在溴的作用下,可以发生亲电加成反应,生成相应的溴代酮。
与硫酸加成
02 醛的化学性质
还原反应
还原成醇
还原成醇和烃的混合物
在催化剂存在下,醛基可被还原成醇, 如用氢化铝锂(LiAlH4)作为还原剂。
在某些条件下,醛基可被还原成醇和 烃的混合物,如用氢气作为还原剂。
还原成烃
在酸性条件下,醛基可被还原成烃, 如用硫酸铜和亚硫酸氢钠作为还原剂。
氧化反应
氧化成酸
在强氧化剂存在下,醛基可被氧化成羧基,如用高锰酸钾 (KMnO4)作为氧化剂。
醛和酮—醛和酮(药学有机化学课件)

+ COCH3
Br2
COCH2Br + HBr
卤仿反应
卤仿反应:如果醛、酮α-碳上有三个氢,三个氢被卤素原子
取代,使得碳碳键极性增大,发生碳碳键的断裂,生成三卤
甲烷和羧酸盐的反应。
O
O
CH3C-R(H)+ 3X2
NaOH
OH CX3-C-R(H)
O
CHX3 + R(H)-C-O
O
O
CH3 C CH3 I2 + NaOH CI3 C CH3 NaOH CH3COONa + CHI3
有机化学/ 醛和酮
醛的特征反应
醛基上氢原子由于受羰基 的影响变得比较活泼,因此醛 具有不同于酮的特殊的反应。 醛能被弱氧化剂——托伦试剂、 斐林试剂氧化为羧酸。
一、托伦反应
托伦(Tollens)试剂是AgNO3与氨水生成的一种无色的 银氨配合物溶液,其中Ag+ 起着氧化剂作用,当它与醛共热时, 醛被氧化为羧酸,而它则被还原为金属银,附着在试管内壁上, 形成光亮的银镜,因此该反应也称为银镜反应。
或浓H2SO4
H
或浓H2SO4 H
半缩醛
缩醛
➢ 半缩醛不稳定,很难分离。 ➢ 缩醛具有双醚的结构,对碱、氧化剂、还原剂稳定,可
以分离出来。
➢ 缩醛在稀酸中易水解转变为原来的醛,合成中可利用此 反应来保护醛基。
一、加成反应
与醇加成 分子内也能形成半缩醛、缩醛。
CH O
干 HCl
OH
H OH O
环状半缩醛(稳定) 在糖类化合物中多见
O
C5 H3C4 H2C3 C2 HC1 H3
CH3 2-甲基-3-戊酮
C H3
有机化学陆涛第七版醛和酮课件

立体化学
在亲核加成反应中,反应的立体 化学特征也值得关注,例如加成 试剂从哪个方向进攻羰基碳原子 ,以及生成的产物是顺式还是反
式。
氧化反应
醛的氧化
醛容易被氧化剂氧化,生成羧酸。常见的氧化剂包括氧气、酸性高锰酸钾、硝酸 银等。
酮的氧化
酮在某些条件下也能被氧化,生成酯。例如,在酸性条件下,酮与过氧化氢反应 可生成酯。
溶解度
水溶性
低级醛在水中的溶解度较大,而高级醛的溶解度较小。酮的溶解度一般较小。
溶剂的影响
在非极性溶剂中,醛和酮的溶解度较大,而在极性溶剂中则较小。
折光率
折光率
随着相对分子质量的增加,醛和酮的 折光率逐渐升高。
影响因素
相对分子质量、极性、取代基等都会 影响醛和酮的折光率。
密度
密度
随着相对分子质量的增加,醛和酮的密度逐渐增大。
影响因素
相对分子质量、极性、取代基等都会影响醛和酮的密度。
03 醛和酮的化学性质
亲核加成反应
醛的亲核加成反应
醛的羰基碳原子具有部分正电荷 ,容易与亲核试剂发生加成反应 ,生成醇和羧酸。常见的亲核试
剂包括醇、氨、硫醇等。
酮的亲核加成反应
酮的羰基碳原子具有较高的电子 云密度,也能与亲核试剂发生加
成反应,生成新的酮或酯。
详细描述
在银镜反应中,醛基与银氨溶液发生氧化还原反应,生 成光亮的银镜。这个反应可以用于鉴别含有醛基的化合 物,如甲醛、乙醛等。
土伦试剂鉴别酮
总结词
土伦试剂是一种用来鉴别酮类化合物的化学试剂,通 过观察是否生成红色沉淀来判定是否为酮。
详细描述
土伦试剂是亚铜离子的络合物,与酮类化合物发生反 应,生成红色的亚铜盐沉淀。这个反应可以用于鉴别 含有酮基的化合物,如丙酮、丁酮等。
有机化学(下)课件10.4醛和酮的保护和去保护
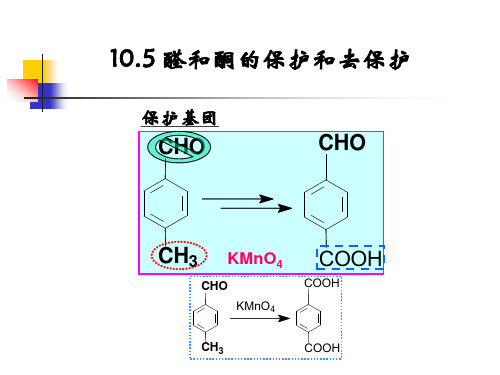
+ O2
V2O5
O
O
9,10-蒽醌
本节重点及作业
1、α,β-不饱和醛酮的1,4加成
2 、醛和酮的制法
作业:10-10; 10-11; 10-12; 10-14 10-15
CH2=dC+
O + HA
d-
CH2=C-OH A
O 烯醇式重排 CH3-C-A
O 以上反应相当于在HA中引入了 CH3C,-
所以乙烯酮是一个很好的乙酰化剂。
乙烯酮与格氏试剂反应还可以得到甲基酮
R CH2=C=O + RMgX 干醚 CH2=C-OMgX H2O/H+
R 烯醇式重排 CH3-C=O (甲基酮)
2CH3OH
CHO dry HCl
HOH2C
K2Cr2O7 H+
OOC
OCH3 CH
OCH3
H2O
H+
OCH3 CH
OCH3
HOOC
CHO
10.6 不饱和醛、酮
不饱和醛、酮一般指分子中含有碳碳双键的醛和酮
乙烯酮
α,β-不饱和醛 α,β-不饱和酮
10.6.1 乙烯 酮
乙烯酮(ketene) 是低沸点 的无色有毒气体, 能溶于乙醚等有机溶剂。
制反应条件,可以使氧化停留在生成芳醛或芳酮的阶段。如: 可以用二氧化锰及硫酸作催化剂。
CH3 MnO2
65 % H2SO4
CHO
由于醛比烃更容易氧化,故氧化剂不能过量,分批加入且迅速搅拌
也可以用氧化铬和乙酐或五氧化二钒作为氧化剂:
CH3 + O2
V2O5
CHO + H2O
CH3
-H,易被氧化
醛酮—醛酮还原(有机化学课件)

·提出问题·
δO-
CC
δ+
H
H(R)
如
OH
CHO
水杨醛
醛酮处于氧化还原的中间价态,它们既可以被氧化 也可以被还原。
?
还原剂
OH CH2OH
水杨醇
O
还原剂
C
O
还原剂
C
OH
C
醇
H
H
C
烃
H
目录
CONTENT
01
醛、酮还原成醇
02
醛、酮还原成烃
01
醛、酮还原成醇
醛、酮还原成醇
1. 催化还原
醛、酮在催化剂Ni、Pd、Pt等金属存在条件下,可被H2还原成相应的一级醇或者二级醇。
R H C=O + H2
R/ R C=O + H2
Ni △
R-CH2-OH
Pb
R/ CH-OH
△
R
对碳氧双键(C=O)进行加成
一级醇 二级醇
醛、酮还原成醇
ቤተ መጻሕፍቲ ባይዱ
1. 催化还原
特点:无选择性, C=O、C=C、-CN、-NO2等都可被还原
C=C
C≡C
√
√
×
×
×
×
×
×
b:稳定,不与水反应,操作处理容易;通常使用甲醇、乙醇作溶剂。
02
醛、酮还原成烃
醛、酮还原成烃
还原成烃
克里门森还原法 吉日聂尔—沃尔夫—黄鸣龙还原法
醛、酮还原成烃
1. 克里门森(Clemmensen)还原法
醛、酮在锌汞齐和浓盐酸作用下,可被还原为烃,羰基变为亚甲基。
O= C-CH2CH2CH3
醛酮—醛酮与醇反应(有机化学课件)

R H C=O + HOR/
干HCl
R OH
C
H
OR/
R/OH,H+
R
OR/
C
H
OR/
+ H2O
半缩醛 (不稳定)
缩醛
醛、酮与醇反应的原理 1.醛与醇反应
维 尼 纶 醚类化合物具有较好的化学稳定性
醛、酮与醇反应的原理
2. 酮与醇反应
与醛相比,酮与醇反应生成半缩酮、缩酮困难,即便在酸性催化下,也很难和 一元醇反应,但可以和某些二元醇反应顺利制得环状缩酮。
醛、酮与醇反应
·提出问题·
导入动画
维尼纶 面料
·提出问题·
吸水性强
具有较强 的化学稳 定性
与其主要成分 聚乙醇缩醛结 构密切相关
?
缩醛酮是如何反应生成的?它又有何应用呢?
目录
CONTENT
01
醛、酮与醇反应 的原理
02
醛、酮与醇反应 的用途
01
醛、酮与醇反应 的原理
醛、酮与醇反应的原理 1.醛与醇反应
H
作用:保护羰基
醛、酮与醇反应的用途 2. 在有机合成反应中的应用
任务:如何由4-戊烯醛合成戊醛?
转化
稀酸
保护醛基
双键还原
练习
下列哪一个化合物是缩醛?( )
O
O
O
O
A
B
缩醛(酮)
小结
100% 80% 60% 40% 20%
100% 80% 60% 40% 20%
思考
甘油醛是最简单的醛糖,是糖类代谢的中 间产物,无色具有甜味。它可以由丙烯醛 氧化生成,那氧化过程如何实现呢?请大 家设计出合理的合成方案。
3.3 醛、酮 课件(共27张PPT) 人教版(2019)选择性必修三

O H-C-H
O H-C-O-H
O H-C-O-CH3
甲醛简介
甲醛又称蚁醛,是无色、有刺激性气味的气体,有毒,易溶于 水。 甲醛用途非常广泛,是重要的有机合成原料;35%-40%的甲 醛水溶液叫福尔马林,具有杀菌、防腐性能。 在烃的含氧衍生物中,甲醛是唯一常温呈气态的物质。 甲醛毒性较高, 是主要的室内污染物,已被确定为致癌和致 畸形物质,是公认的变态反应源,也是潜在的强致突变物之一。
化学性质 氧化反应
HO
HO
2H-C-C-H
+ O2
催化剂
△
2H-C-C-O-H
H
H
乙醇
乙醛 乙酸 氧化(脱氢)
氧化(加氧)
还原(加氢)
化学性质 氧化反应
2ml 10% NaOH
2% CuSO4 4~6滴振荡
0.5 ml 乙醛
加热 煮沸
实验现象 蓝色絮状沉淀
砖红色沉淀
反应原理 Cu2++2OH-= Cu(OH)2↓ CH3CHO + 2Cu(OH)2 +NaOH △ CH3COONa + Cu2O↓+ 2H2O
有弱氧化性 Ag+表现氧化性
➢ CH3CHO + 2Ag(NH3)2OH △ CH3COONH4 +3NH3+ 2Ag↓+ H2O
乙酸与NH3·H2O 反应得到
无↑,因NH3 极易溶于水
1mol-CHO~2 molAg(NH3)2OH~ 2 mol Ag
【思考】1 mol甲醛最多可以还原得到多少 Ag? 甲酸能发生银镜反应吗? 甲酸甲酯能发生银镜反应吗?
【思考】将甲醛、乙醛混合发生上述反应,产物有多少种? 需断裂醛基的π键和α-C上的碳氢键,但甲醛无α-C。
有机化学课件(罗美明)
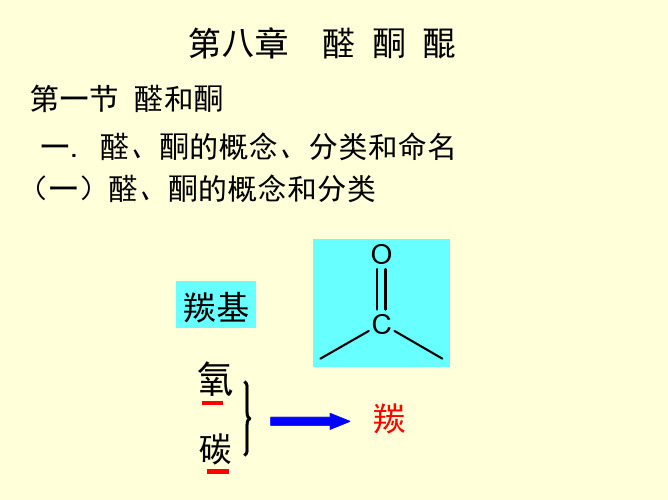
C O
CH2
H + NiS
R'
CH2 + H CH2CH2
4. 与氮亲核试剂的加成 醛、酮与氨衍生物反应
OC O + H2N Y
-H2O
OH H
+
[ Y
C NH2 Y ]
C N Y
C
N
C O
+
H2N Y
C N Y
H2N R (伯胺)
H2N-OH (羟胺) H2N-NH2 (肼)
C O +
H2N-NH
H H 2O
+
C H 2 = C H C H (O C 2 H 5 ) 2
C H 2= C H C H O
+ 2C H 3 C H 2 O H
O + H2O O
H+
O + HOCH2CH2OH
O
OCH2CH3
H+ H2O
?
OHC
• 应用:保护羰基
CHO
+ CH3CH2OH
CH2=CH-CHO
?
CH2 OH
OH C COOH
O CH3CH2CCH3 HCN
OH CH3CH2C CN CH3
浓 H2SO4
CH3CH=CCOOH CH3
O CH3 C CH3 + NaCN
H2SO4 10o-20oC
OH CH3 C CN CH3
CH3OH H2SO4
CH2=CCOOCH3 CH3
(2)与格氏试剂的加成反应
烃基中含有吸电子基团时反应活性增大。 Cl3CCHO > Cl2CHCHO > ClCH2CHO > CH3CHO
有机化学-醛和酮

O R CH2 C CH CHO
HR
O
H2O
R CH2 C CH CHO
HR
OH
R CH2
C
α
CH CHO
+ OH-
HR (-羟基醛)
Problem: 完成下列反应式:
稀碱
H3C CH2 CH2 CHO 4~5oC
OH O H3C CH2 CH2 CH CH C H
H2C CH2CH3
干燥HCl
R C H+ R’- OH
R C H + H2O
OR'
OR' 缩醛
例:
O
HCl
C H + 2 CH3CH2OH
CH OCH2CH3 OCH2CH3
苯甲醛缩 二乙醇
◆ 酮不易生成缩酮,但环状缩酮较易生成。
R
C=O + CH2OH 干燥HCl
R
O C
CH2
R
CH2OH
R O CH2
应用: 缩醛和缩酮对碱、氧化剂稳定,常用 于有机合成中保护醛(酮)基。缩醛(酮) 在酸性条件下水解回原来的醛(酮)和醇。
沉淀。
通常
R
为橙黄色
C NNH
NO2
的沉淀
R' NO2
(二) - 碳和 -氢的反应
-H,有弱酸性
HO
R-CH2-CH-C-H βα
p- 共轭,使碳 负离子稳定
R-CH2-CHO
NaOH
O R CH- C H
碳负离子
1. 醇醛缩合
在稀碱溶液中, 含α-H的醛的α-碳可以与另一 醛的羰基碳加成形成新的碳碳键,生成β-羟基醛 类化合物,该反应称为醇醛缩合。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
O A r CH
芳香醛
2. 一些制备醛酮的新方法
通过酰氯的还原制备醛
O R C Cl
H2 / Pd, 硫-喹啉(或硫-脲) Rosenmund 反应
LiAlH(OBu-t)3
S O C l2
O R C OH
醚 LiAlH4 + 3 t-BuOH
O RCH
➢反应活性比较
还原能力: 羰基的亲电性:
R1
C O + CO2 R2
芳香酮和醛的合成
•Friedel-Crafts 反应
O
O
O
R C Cl or R C O C R
Ar H
AlCl3 O R C OH
HF or PPA
O Ar C R
芳香酮
•Gattermann-Koch 反应
A r H
C O /H C l( 干 燥 )
A lC l3 , C u C l,
R ''
1o醇 2o醇 3o醇
2.2 醛酮与炔化物的加成
O M CCR (H )
C
H 2 O
M = N a ,K ,M g X 等
O H CCCR (H )
a-炔基醇
•进一步应用
H OH C CC CR
炔基醇
H2 Lindlar催化剂
Na / NH3
H2O/ Hg++ H C
R=H
OH
C
R
CC
H
H
OH R C C CH
R'
H2O Hg++
O R C CH2R
OH O R C C CH3
R'
氧化法
• 氧化醇
RCH2OH
OH R CH R'
R 可为不 饱和基团
CrO3 Pyridine
Sarrett 试剂
RCH O
CrO3 Pyridine
Sarrett 试剂
CrO3 / H2SO4
Jones 试剂
LiAlH4 > LiAlH2(OR)2> LiAlH(OBu-t)3
O R CX >
O RC H
O [ H ]
O [ H ]
R C X
R C H
R C H 2O H
LiAlH4 LiAlH(OBu-t)3
很快 较快
快
选择性差
慢
选择性好
通过酰氯合成酮(酰基上的亲核取代)
O R '2 C u L i
关于有机化学第十 章醛和酮
一. 醛酮的类型和命名
羰基 carbonyl
醛和酮
O R CH
O R C R'
醛、酮的分类
O R CH
O R CR '
醛(aldehyde)
O A r C H
O A r C R
酮(Ketone)
O b aC C C H (R )
脂肪族醛、酮
芳香族醛、酮
a, b-不饱和醛、酮
O
亲核加成
O
C
C
可逆
Nu
Nu
Nu
NaCN, NaHSO3
H2O
OH C Nu
2.1 醛酮与 RMgX 或 RLi 的加成
O
MgX
C
R
OMgX
OH
H2O
C
C
R
R
CH2O
RMgX
R 'C H O
O C R' R''
RMgX RMgX
H2O H2O H2O
R CH2 OH
OH R' CH R
OH R' C R
RCC l
O
R '2 C u L i
RCR '
N o R e a c tio n
o r R '2 C d
o r R '2 C d
•比较:
O R 'M g X
RCC l
O R 'M g X RCR '
O H RCR '
R '
R2CuLi和R2Cd活性 较低,但选择性好
三.醛、酮的性质 (I)
羰基氧有弱碱性 可与酸结合
(E)-chalcone
二. 醛、酮的制备 1. 几种已知的方法
炔烃的水解
HC CH
RX
R CC H
末端炔
H 2O H g++
O RC C H 3
甲基酮
RCCH
H2O Hg++
O R C CH3
MC CH (M = Na, MgX 等)
(1) O R C R'
(2) H2O
RC CR
H2O Hg++
cis-烯基醇
OH
C
H
CC
trans-烯基醇
H
R
OH O
H+
C C CH3
O
C
CC
CH3
a-羟基酮
a, b-不饱和酮
2.3 醛酮与LiAlH4 或 NaBH4 还原反应
R'CHO
LiAlH4 or NaBH4
O R' C R
性质分析
a碳有吸电子基 a氢有弱酸性
R1 O
碳与氧相连 氢易被氧化
R2
a
CC
H(R)
羰基碳有亲电性
H
可与亲核试剂结合
• a氢与碱
R1 O
的反应
R2
a
C
H(R)
H B
R1 C
R2
O C
H(R)
烯醇负离子
1. 羰基氧的碱性(与H+或Lewis酸的作用)
H + O
C
碳上正电荷少 亲电性较弱
O H C
强 较强
分子型 NuH
H 2N R , HN R 2 HOR H 2O
不强
醛酮与负离子型亲核试剂加成的两种形式
• 不可逆型(强亲核试剂的加成)
O
亲核加成
C
不可逆
Nu
O C Nu
H2O
OH C Nu
Nu
RMgBr, RLi, RC CMgBr, RC CNa, LiAlH4,NaBH4
• 可逆型(一般亲核试剂的加成)
dione
C H O
苯甲醛 benzaldehyde
C H O O H
O C H O
水杨醛 2-羟基苯甲醛 2-hydroxybenzaldehyde
呋喃甲醛 furan-2-carbaldehyde
O
C H 3 乙酰苯 苯乙酮 acetophenone
O
P h
P h
查尔酮(chalcone) 1, 3-二苯基丙烯酮
O Al[OC(CH3)3]3 / CH3CCH3
Oppenauer 氧化
O R C R'
• 氧化烯烃
R1
C R2
R3 C
H
(1) O3 (2) Zn/ H2O
KMnO4
例
R1 [O]
R2
R1
C R2
CH2
KMnO4
R1
R3
CO + OC
R2
H
R1 CO
R2
R3 + OC
OH
R1
O
O
R2
有合成价值
碳上正电荷增加 亲电性加强
O H C
•例:
O RCH
2R'OH
2R'OH H+
NoReaction R'OH 为弱亲核试剂
OH RCH
OR' RCH
OR'
缩醛
2. 醛酮羰基上的亲核加成反应(1)
一些常见的与羰基加成的亲核试剂
亲核试剂
相应试剂
亲核能力
负离子型
Nu
R RC C H CN HO 3S
R M gB r, R Li R C CMgBr , R C CNa L iA lH 4, N aB H 4 NaCN N aH SO 3
醛酮的命名
C H O H 3 C
O
O
巴豆醛 反-2-丁烯醛
甲基乙基甲酮 丁酮
1-环己基-2-丁酮
(E)-but-2-enal
butanone 1-cyclohexylbutan-2-one
O CHO
3-氧代(正)戊醛 3-oxopentanal
O
O
5, 5-二甲基-1, 3-环己二酮 5,5-dimethylcyclohexane-1,3-
