《单质碳的化学性质》PPT课件
合集下载
《碳单质的化学性质》课件

结构
碳原子有四个电子,可以形成多种化学键,包括单键、双键和三键,从而形成不同的化合物。
碳单质的化学反应
1
氧化反应
碳单质可以与氧气发生燃烧反应,生成二氧化碳。也可与氧化剂反应,产生其他 氧化物。
2
还原反应
碳单质可在高温下发生热分解反应,生成碳化物。也可以还原、氮气和卤素等元素发生反应,生成相应的化合物。
2 防护措施
使用时应佩戴防护眼镜和口罩,保持通风良好的工作环境,妥善存放和处理。
结束语
通过本课件,我们详细了解了碳单质的化学性质。它在各个领域都有重要的 应用,未来的研究方向主要集中在碳材料的合成和应用。
《碳单质的化学性质》 PPT课件
本PPT介绍碳单质的化学性质。包括碳单质的基本介绍、化学反应、实际应用、 安全使用方法等。适用于高中或大学化学专业相关课程的教学。
碳单质的基本介绍
定义
碳单质是由碳原子构成的纯净物质,是化学元素周期表中第六位的元素。
物理性质
碳单质有两种主要的晶体形式:金刚石和石墨。金刚石坚硬,石墨具有良好的导电性。
碳单质的实际应用
电子行业
钢铁冶炼
医疗行业
碳单质广泛用于电子行业,如制 造半导体器件、电池和显示屏等。
碳单质是冶金过程中不可缺少的 材料,用于还原矿石、炼制钢铁。
碳单质在医疗行业中用于制备生 物材料和医疗设备,如人工关节 和植入物。
碳单质的安全使用方法
1 危害
碳单质可引起呼吸道疾病和烟尘病,遇火可引发爆炸。
碳原子有四个电子,可以形成多种化学键,包括单键、双键和三键,从而形成不同的化合物。
碳单质的化学反应
1
氧化反应
碳单质可以与氧气发生燃烧反应,生成二氧化碳。也可与氧化剂反应,产生其他 氧化物。
2
还原反应
碳单质可在高温下发生热分解反应,生成碳化物。也可以还原、氮气和卤素等元素发生反应,生成相应的化合物。
2 防护措施
使用时应佩戴防护眼镜和口罩,保持通风良好的工作环境,妥善存放和处理。
结束语
通过本课件,我们详细了解了碳单质的化学性质。它在各个领域都有重要的 应用,未来的研究方向主要集中在碳材料的合成和应用。
《碳单质的化学性质》 PPT课件
本PPT介绍碳单质的化学性质。包括碳单质的基本介绍、化学反应、实际应用、 安全使用方法等。适用于高中或大学化学专业相关课程的教学。
碳单质的基本介绍
定义
碳单质是由碳原子构成的纯净物质,是化学元素周期表中第六位的元素。
物理性质
碳单质有两种主要的晶体形式:金刚石和石墨。金刚石坚硬,石墨具有良好的导电性。
碳单质的实际应用
电子行业
钢铁冶炼
医疗行业
碳单质广泛用于电子行业,如制 造半导体器件、电池和显示屏等。
碳单质是冶金过程中不可缺少的 材料,用于还原矿石、炼制钢铁。
碳单质在医疗行业中用于制备生 物材料和医疗设备,如人工关节 和植入物。
碳单质的安全使用方法
1 危害
碳单质可引起呼吸道疾病和烟尘病,遇火可引发爆炸。
单质碳的化学性质PPT

9.如图6-1-10,“卖炭翁,伐薪烧炭南山中。 满面尘灰烟火色,两鬓苍苍十指黑。卖炭 得钱何所营?身上衣裳口中食”。“炭” 木炭 指的是 (具体物质名称),碳在真空环境 中高温条件下可以将氧化镁中的镁还原出 来,并产生二氧化碳,请写出发生反
应的化学方程式:
,反应前后碳元素的化合价
由0价变为+4价
2.航天飞机表面覆盖石墨瓦可起到隔热和保 护作用,这主要是利用石墨 ( ) A A.熔点高、化学性质稳定 B.硬度小,有润滑作用 C.密度小 D.导电性
3.用木材做木桩时,常把埋入地下的部分表 面烧焦,目的是 ) D ( A.烘干木材 B.使木材变得更结实 C.烧死虫子 D.形成化学性质稳定的木炭层
试管内的氧气反应而部分消耗,故稍过量的炭
粉有利于反应的进行
A.36∶3
。 B.40∶3
C.48∶3
例2 用木炭还原氧化铜的实验如图6-1-7所 示。
集中火焰,提高温度 (1)酒精灯加灯罩的目的是
。 开始排出的是试管内的空气 (2)刚开始预热,试管②中立即产生气泡, 但石灰水不变浑浊,原因是 。 CO2+Ca(OH) CaCO3↓+H2O 2 (3)继续加热,观察到石灰水逐渐变浑浊, C+2CuO 2Cu+CO2↑ 黑色粉末中出现红色物质。请你写出带点部 分的化学方程式:
用止水夹夹住橡胶管,防止空气进入试管,将还 原的铜再次氧化。 (2)高温下,碳还能与CO2反应生成CO,反应 的化学
方程式为
。
• 4.还原反应 • 含氧化合物里的氧被夺去的反应,叫做 还原反应。 • 在2CuO+C 2Cu+CO2↑反应里,氧 化铜失去氧而变成了铜单质,氧化铜发生 还原反应。木炭是使氧化铜还原为铜的物 质,它具有还原性,是还原剂。木炭跟氧 化铜里的氧起反应生成了二氧化碳,又发 生了氧化反应。氧化铜在反应中提供氧, 具有氧化性,是氧化剂。
《单质碳的化学性质》PPT课件
还原氧化铁 3 C+ 2 Fe2O3 还原氧化锌 C+ 2 ZnO
高温
4 Fe+ 3 CO2
高温
2 Zn+CO2
点燃
碳还原二氧化碳
C+CO2
2 CO
小
结
碳在常温时很稳定,在加热或高温 条件下具有可燃性和还原性。
练习1:
下列碳单质的用途中,利用了碳的化学性质 的是( D )。 ①做电极 ②做滤毒剂 ③制作固体润滑剂 ④做燃料 ⑤制作装饰品⑥冶炼金属 ⑦制作染料⑧用金刚石切割玻璃 A.①②③④ B.⑤⑥⑦ C.①③⑤⑦ D.④⑥
字画 书法
2、可燃性:
氧气充足
C+O2
点燃
CO2 (放出热量)
2CO (放出热量)
氧: 1、黑色粉末变成红色;
2、产生使石灰水变浑浊 的气体。
氧化反应 还原性 还原反应
化学方程式:
高温
C+2CuO
2Cu+CO2↑
第二节
单质碳的化学性质
冶炼金属
碳可以还原其它金属氧化物
谢谢大家!
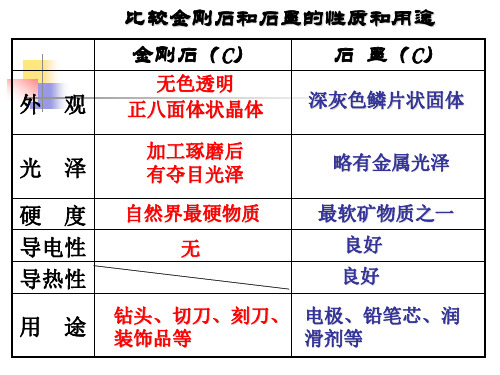
比较金刚石和石墨的性质和用途
金刚石(C)
外 光 观 泽
无色透明 正八面体状晶体 加工琢磨后 有夺目光泽 自然界最硬物质
无
石 墨(C)
深灰色鳞片状固体 略有金属光泽
硬 度 导电性 导热性 用 途
最软矿物质之一
良好 良好
钻头、切刀、刻刀、 电极、铅笔芯、润 装饰品等 滑剂等
第二节
1、稳定性:
单质碳的化学性质
练习2:
木炭还原氧化铜的实验中: (1)酒精灯加网罩的目的 集中火焰,提高温度 ___________________ (2)刚开始预热,导管口立 即产生气泡,但石灰水不变 最初排除的气体是装置内的空气 浑浊,原因是_____________________ (3)继续加热,观察到石灰水逐渐变浑浊,黑色粉 高温 末中出现红色物质。 C+2CuO 2Cu+CO2↑ 请你写出①中反应的化学方程式:____________ (4)停止加热时,应先将导管从试管②中撤出, 并用弹簧夹夹紧橡皮管,待试管①冷却后再把试 管里的粉末倒出。这样操作的原因是 ___________________________________ 防止发生倒吸.防止铜温度很高,未密封导致铜被被氧化.
高温
4 Fe+ 3 CO2
高温
2 Zn+CO2
点燃
碳还原二氧化碳
C+CO2
2 CO
小
结
碳在常温时很稳定,在加热或高温 条件下具有可燃性和还原性。
练习1:
下列碳单质的用途中,利用了碳的化学性质 的是( D )。 ①做电极 ②做滤毒剂 ③制作固体润滑剂 ④做燃料 ⑤制作装饰品⑥冶炼金属 ⑦制作染料⑧用金刚石切割玻璃 A.①②③④ B.⑤⑥⑦ C.①③⑤⑦ D.④⑥
字画 书法
2、可燃性:
氧气充足
C+O2
点燃
CO2 (放出热量)
2CO (放出热量)
氧: 1、黑色粉末变成红色;
2、产生使石灰水变浑浊 的气体。
氧化反应 还原性 还原反应
化学方程式:
高温
C+2CuO
2Cu+CO2↑
第二节
单质碳的化学性质
冶炼金属
碳可以还原其它金属氧化物
谢谢大家!
比较金刚石和石墨的性质和用途
金刚石(C)
外 光 观 泽
无色透明 正八面体状晶体 加工琢磨后 有夺目光泽 自然界最硬物质
无
石 墨(C)
深灰色鳞片状固体 略有金属光泽
硬 度 导电性 导热性 用 途
最软矿物质之一
良好 良好
钻头、切刀、刻刀、 电极、铅笔芯、润 装饰品等 滑剂等
第二节
1、稳定性:
单质碳的化学性质
练习2:
木炭还原氧化铜的实验中: (1)酒精灯加网罩的目的 集中火焰,提高温度 ___________________ (2)刚开始预热,导管口立 即产生气泡,但石灰水不变 最初排除的气体是装置内的空气 浑浊,原因是_____________________ (3)继续加热,观察到石灰水逐渐变浑浊,黑色粉 高温 末中出现红色物质。 C+2CuO 2Cu+CO2↑ 请你写出①中反应的化学方程式:____________ (4)停止加热时,应先将导管从试管②中撤出, 并用弹簧夹夹紧橡皮管,待试管①冷却后再把试 管里的粉末倒出。这样操作的原因是 ___________________________________ 防止发生倒吸.防止铜温度很高,未密封导致铜被被氧化.
单质碳的化学性质ppt

高温
碳的化学性质
三、碳具有还原性。跟某些氧化物的反应
失去氧,被还原,有氧化性,发生还原反应
得到氧,被氧化,有还原性,发生氧化反应 还原反应:失去氧的反应。 氧化反应:得到氧的反应。 还原剂:能夺取含氧化合物里氧元素的物质。 氧化剂:能给其它物质提供氧元素的物质。
还原剂和氧化剂都是指反应物。
写出碳跟氧化铁
2Fe2O3+3C
高温
4Fe+3CO2
课堂小结
1、常温下具有稳定性。(可用于书写重要文档、绘画) 单 质 碳 的 化 学 性 质 (1)完全燃烧: 2、具有可燃性 (作燃料) (2)不完全燃烧
C+O2
2C+O2
高温
点燃 点燃
CO2
2CO
3、具有还原性 (冶炼金属)
(C+金属氧化物=====金属单质+CO2
碳的化学性质
碳 C 12.01
猜谜语
它家孪生三兄弟,相貌悬殊 同根生。老大硬朗又阔气, 腰缠万贯无人比,老二黝黑 又柔软,缺乏阳刚男儿气, 老三长得象足球,超导方面 是能手。
我国现存最早的古代书法真迹 晋代陆机书法作品《平复帖》,距今1700多年。
碳的化学性质
一、碳在常温下具有稳定性。
元素的化学性质由什么决定?
用木炭还原氧化铜的实验如下图。 (1)酒精灯加灯罩的目的 集中火焰,升高温度 ; (2)刚开始预热,试管②中立即产生气泡,但石灰水不变 浑浊,原因是 刚开始出来的是装置中的空气 ; (3)继续加热,黑色粉末中出现红色物质。请你写出 出现红色物质的化学方程式: 。 (4)停止加热时,应先将导管从试管②中撤出,并用 弹簧夹夹紧橡皮管,待试管①冷却后再把试管里的粉末 倒出。这样操作的原因是 防止生成的铜被氧化成氧化铜 。
第二课时 碳单质的化学性质14PPT

说法中错误的是( B )
A、炭雕工艺品须特别注意防火 B、炭雕是轻质透明且不易变质的固体 C、碳的性质比较稳定,炭雕艺术品可以长期保存 D、炭雕能吸附室内微量有害气体,有利健康 【方法点拨】炭雕的主要成分是木炭,利用碳的物理性质和化学性质进行分析。 【解析】A、木炭具有可燃性,离火太近,会使其达到着火点而燃烧,故A正确。B、由碳元素 形成的单质中,金刚石是无色透明的,木炭是黑色的,故B错误。C、在常温下,碳的化学性质稳 定,木炭是由碳元素组成的,性质也较稳定,故C正确。D、木炭具有吸附性,可以吸附色素和异 味,故D正确。
强化练习
3、由下面实验现象可知,黑色粉末可能是( D )
A、Fe3O4和C B、Fe和CuO C、MnO2和CuO D、CuO和C 【方法点拨】本题属于推断题,应根据反应物和生成物的颜色和相互之间的反应来分析。 【解析】A、在高温条件下,碳与四氧化三铁反应生成铁和二氧化碳,不会出现红色粉末,故A错误; B、铁和氧化铜中不含碳元素,不会生成二氧化碳,故B错误;C、二氧化锰和氧化铜中不含碳元素,不会 生成二氧化碳,故C错误;D、氧化铜和碳在高温条件下反应,能生成铜和二氧化碳,铜是红色粉末,二 氧化碳能使澄清的石灰水变浑浊,故D正确。
强化练习
2、如图是碳和氧化铜反应的实验装置,相关说法错误的是( D )
A、灯罩的作用是:集中火焰提高温度 B、理论上a中减少的质量等于b中增加的质量 C、a中黑色粉末变成光亮红色说明碳具有还原性 D、反应结束后立即把a中的粉末倒出观察生成物的颜色
【方法点拨】碳具有还原性,能与氧化铜反应生成铜和二氧化碳,结合实验注意事项,分析判断。 【解析】A、实验中灯罩的作用是集中火焰提高温度,故A正确;B、碳与氧化铜在高温下反应生 成铜和二氧化碳,生成的二氧化碳被石灰水吸收,根据质量守恒定律,理论上a中减少的质量等于b中 增加的质量,故B正确;C、a中黑色粉末变成光亮红色,说明有铜生成,说明碳具有还原性,故C正确; D、反应结束后不能立即把a中的粉末倒出观察生成物的颜色,以防生成的铜再次被氧化,应等到试管 冷却至室温后,故D错误。
A、炭雕工艺品须特别注意防火 B、炭雕是轻质透明且不易变质的固体 C、碳的性质比较稳定,炭雕艺术品可以长期保存 D、炭雕能吸附室内微量有害气体,有利健康 【方法点拨】炭雕的主要成分是木炭,利用碳的物理性质和化学性质进行分析。 【解析】A、木炭具有可燃性,离火太近,会使其达到着火点而燃烧,故A正确。B、由碳元素 形成的单质中,金刚石是无色透明的,木炭是黑色的,故B错误。C、在常温下,碳的化学性质稳 定,木炭是由碳元素组成的,性质也较稳定,故C正确。D、木炭具有吸附性,可以吸附色素和异 味,故D正确。
强化练习
3、由下面实验现象可知,黑色粉末可能是( D )
A、Fe3O4和C B、Fe和CuO C、MnO2和CuO D、CuO和C 【方法点拨】本题属于推断题,应根据反应物和生成物的颜色和相互之间的反应来分析。 【解析】A、在高温条件下,碳与四氧化三铁反应生成铁和二氧化碳,不会出现红色粉末,故A错误; B、铁和氧化铜中不含碳元素,不会生成二氧化碳,故B错误;C、二氧化锰和氧化铜中不含碳元素,不会 生成二氧化碳,故C错误;D、氧化铜和碳在高温条件下反应,能生成铜和二氧化碳,铜是红色粉末,二 氧化碳能使澄清的石灰水变浑浊,故D正确。
强化练习
2、如图是碳和氧化铜反应的实验装置,相关说法错误的是( D )
A、灯罩的作用是:集中火焰提高温度 B、理论上a中减少的质量等于b中增加的质量 C、a中黑色粉末变成光亮红色说明碳具有还原性 D、反应结束后立即把a中的粉末倒出观察生成物的颜色
【方法点拨】碳具有还原性,能与氧化铜反应生成铜和二氧化碳,结合实验注意事项,分析判断。 【解析】A、实验中灯罩的作用是集中火焰提高温度,故A正确;B、碳与氧化铜在高温下反应生 成铜和二氧化碳,生成的二氧化碳被石灰水吸收,根据质量守恒定律,理论上a中减少的质量等于b中 增加的质量,故B正确;C、a中黑色粉末变成光亮红色,说明有铜生成,说明碳具有还原性,故C正确; D、反应结束后不能立即把a中的粉末倒出观察生成物的颜色,以防生成的铜再次被氧化,应等到试管 冷却至室温后,故D错误。
第六单元课题1碳单质的多样性第二课时碳单质的化学性质课件(共18张PPT内嵌视频).ppt

金属的冶炼
高温
3C + 2Fe2O3
4Fe + 3CO2↑
练习
1.(微型实验)某化学兴趣小组利用如图装置进行木炭还原氧化铜的实验(夹持装
置略)。下列有关说法错误的是( B )
A.实验前要将木炭粉末和氧化铜粉末混合均匀 B.点燃酒精灯,澄清石灰水会立即变浑浊 C.实验过程中可观察到管内黑色固体逐渐变红 D.该装置的优点之一是停止加热后可有效防止石灰水倒吸
第六单元 碳和碳的氧化物
课题1 碳单质的多样性 第2课时 碳单质的化学性质
学习目标
1. 通过碳的可燃性的学习,知道单质碳的化学性 质,认识到化学变化需要一定条件,条件不同反应就 不同。
2. 通过碳的还原性实验,了解还原反应,发展学 生问题意识和探究能力;
3. 初步形成“结构决定性质”“性质决定用途” 的思想观念。弃物少。
归纳小结
单质碳的化学性质
条件
化学性质
用途
常温下
碳的化学性质不活泼
点燃 高温
碳具有可燃性
碳具有还原性
性质
决定 体现
用途
制碳素墨水 作燃料 冶炼金属
课堂练习 1.易错辨析。判断下列说法是否正确,对的打“√”,错的打“×”。 (1)金刚石、石墨、C60在氧气中充分燃烧都生成二氧化碳。(√ ) (2)可用观察颜色的方法鉴别木炭粉末和氧化铜粉末。( × ) (3)木炭还原氧化铜过程中,碳元素的化合价发生了改变。( √ )
_二__氧__化___碳____,反应的化学方程式为
澄清石灰水_变__浑__浊__
高温
_C__+__2__C_u__O__=__=_=__=__2_C__u_+__C_O__2_↑__。
6C_单质碳的化学性质_课件

高温
还原反应:含氧化合物里的氧 被夺去的反应。
二、碳的还原性
1.碳还原金属氧化物
3 C+ 2 Fe2O3 = 4 Fe+ 3 CO2 C+ 2 ZnO = 2 Zn+CO2
应用:焦炭可用于冶金工业(还原铁的氧化物)
高温
高温
2.炽热的碳还原非金属氧化物 (如CO2, H2O)
C + CO2
C + H2O
比较稳定 这种元素的化学性质_____,故不易起变 化的缘故。
小
结
碳在常温时很稳定,在点燃或高温 条件下具有可燃性和还原性。
试一试
在一个通风良好的煤炉中,最不易发生
的反应是
A、C+O2 =
点燃 点燃
( C )
CO2 2 CO B、C+CO2 = 2CO D、2CO+O2 =2 CO2
点燃 高温
C、2C+O2 =
用墨书写的字画虽年深日久但仍不褪色,
碳 这是由于墨的主要成分是___,而在常温下
• • • • • • • • • • • • • • 1.装置包括有那些仪器? 酒精灯,大试管,铁架台,单孔橡皮塞导管,小试管 2.木炭和氧化铜分别是什么颜色和状态? 黑色固体 3.为什么要给酒精灯加金属网罩? 提供高温 4.为什么要将导管通人澄清石灰水? 检验产物有二氧化碳生成 5.安装过程中应该注意那些问题? 管口略微向下倾斜,伸入试管的导管短等 6.实验结束时,应该注意什么问题? 先移走石灰水,后灭酒精灯,是为了止液体倒吸; 7、用弹簧夹夹紧导管防是防止空气进入试管是O2 与Cu反应又变成CuO
高温
高温
2CO
H2 + CO
碳的化学性质说课稿(23张PPT)

活动三
氧化铜失去氧,发生了还原反应
教材分析 学情分析 教法分析
高温
教学过程
C+2CuO
还原性
2Cu+CO2↑ 板书设计
教学反思
碳得到氧 , 发生了氧化反应
设计意图:
1、通过分析、讲解,突破难点。
导 活活 入 动动 新 探探 课 究究
课当 堂堂 小练 结习
活动三
设计意图:通过动画,从微观的角度让学生
3、重点和难点
重点
碳单质的化学 性质
教材分析
难点
碳与某些氧化物的 反应
学情分析 教法分析 教学过程 板书设计 教学反思
学习兴趣浓厚
推理能力不足
实际应用 能力较差
学生特点
实验分析 能力欠缺
教材分析
学情分析
教法分析 教学过程 板书设计 教学反思
对物质的化学性 质有一定的认识
渴望获得化学知识
类比推理法
2C+O2 点燃 2CO(O2不足)
教学反思
作燃料导 活
入动 新探
度 下
②还原性
高温
2CuO +C
2Cu + CO2
课
冶炼 课课
金属
堂堂 小小
结结
究
当 堂 练 习
教材分析
1、具有保存价值的档案等都使用碳素墨水书写, 学情分析
这是因为墨汁中的碳 (
)
教法分析
A.常温下化学性质稳定 B.常温下被氧化成稳定性的物质
入 新 课
动点。 堂 堂
2、通过类比得出:量变引起质变。
小练
结习
活动二
设计意图:结合新闻实例,提高安全常识。
教材分析
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第二节 单质碳的化学性质
第二节 北宋黄庭坚用墨(用炭黑等制成)写的字
第二节
单质碳的化学性质
用途
一、常温下的稳定性: 常温下的稳定性:
试一试
“钻石恒久远,一颗永流传”(钻石的主要 钻石恒久远,一颗永流传” 成分是C)这句广告词说明碳在常温下 成分是 ) 比较稳定 化学性质_____。 化学性质_____。
C还原CuO实验 还原CuO实验
现象: 现象: 1、黑色粉末变成红色; 、黑色粉末变成红色 2、产生使石灰水变浑浊的气体。 、产生使石灰水变浑浊的气体。 化学方程式: 化学方程式:
高温
C+2CuO= 2Cu+CO2↑
第二节
2、还原性: 还原性:
单质碳的化学性质
C还原氧化铜的现象
第二节
单质碳的化学性质
碳可以还原其它金属氧化物, 碳可以还原其它金属氧化物,写出下列反应 方程式: 方程式:
3 C+ 2 Fe2O3 = 4 Fe+ 3 CO2
高温
高温
C+ 2 ZnO = 2 Zn+CO2
小 结
碳在常温时很稳定,在加热或高温 在常温时很稳定, 条件下具有可燃性和还原性。
课后作业
练习册
谢谢大家!
第二节
单质碳的化学性质
一、常温下的稳定性: 常温下的稳定性: 二、高温下的活动性: 高温下的活动性
点燃
用途: 用途:
放出热量) 放出热量 1、可燃性: C+O2 = CO2 (放出热量 可燃性:
哈!
真香啊
哦嗬! 哦嗬
栽了
单质C的可燃性 单质 的可燃性
1、与充足的O2的反应: 与充足的O 的反应:
点燃
C+O2 = CO2
点燃
(放出热量 放出热量) 放出热量
2、与不充足的O2的反应: 与不充足的O 的反应:
2C+O2 = 2CO
(放出热量 放出热量) 放出热量
讨论: 讨论 怎样证明纯净的金刚石和石墨 都是由碳元素组成的? 都是由碳元素组成的?
答:高温下将纯净的金刚石和石墨燃烧, 高温下将纯净的金刚石和石墨燃烧, 纯净的金刚石和石墨燃烧 得到的唯一产物都是CO 证明纯净的金 得到的唯一产物都是CO2。证明纯净的金 刚石和石墨都是由碳元素组成的。 刚石和石墨都是由碳元素组成的。
第二节 北宋黄庭坚用墨(用炭黑等制成)写的字
第二节
单质碳的化学性质
用途
一、常温下的稳定性: 常温下的稳定性:
试一试
“钻石恒久远,一颗永流传”(钻石的主要 钻石恒久远,一颗永流传” 成分是C)这句广告词说明碳在常温下 成分是 ) 比较稳定 化学性质_____。 化学性质_____。
C还原CuO实验 还原CuO实验
现象: 现象: 1、黑色粉末变成红色; 、黑色粉末变成红色 2、产生使石灰水变浑浊的气体。 、产生使石灰水变浑浊的气体。 化学方程式: 化学方程式:
高温
C+2CuO= 2Cu+CO2↑
第二节
2、还原性: 还原性:
单质碳的化学性质
C还原氧化铜的现象
第二节
单质碳的化学性质
碳可以还原其它金属氧化物, 碳可以还原其它金属氧化物,写出下列反应 方程式: 方程式:
3 C+ 2 Fe2O3 = 4 Fe+ 3 CO2
高温
高温
C+ 2 ZnO = 2 Zn+CO2
小 结
碳在常温时很稳定,在加热或高温 在常温时很稳定, 条件下具有可燃性和还原性。
课后作业
练习册
谢谢大家!
第二节
单质碳的化学性质
一、常温下的稳定性: 常温下的稳定性: 二、高温下的活动性: 高温下的活动性
点燃
用途: 用途:
放出热量) 放出热量 1、可燃性: C+O2 = CO2 (放出热量 可燃性:
哈!
真香啊
哦嗬! 哦嗬
栽了
单质C的可燃性 单质 的可燃性
1、与充足的O2的反应: 与充足的O 的反应:
点燃
C+O2 = CO2
点燃
(放出热量 放出热量) 放出热量
2、与不充足的O2的反应: 与不充足的O 的反应:
2C+O2 = 2CO
(放出热量 放出热量) 放出热量
讨论: 讨论 怎样证明纯净的金刚石和石墨 都是由碳元素组成的? 都是由碳元素组成的?
答:高温下将纯净的金刚石和石墨燃烧, 高温下将纯净的金刚石和石墨燃烧, 纯净的金刚石和石墨燃烧 得到的唯一产物都是CO 证明纯净的金 得到的唯一产物都是CO2。证明纯净的金 刚石和石墨都是由碳元素组成的。 刚石和石墨都是由碳元素组成的。
