红细胞洗涤液(pH7.2)
高致病性禽流感红细胞凝集(HA)与凝集抑制(HI)

高致病性禽流感红细胞凝集(HA)与凝集抑制(HI)试验1.原理:禽流感病毒具有凝集鸡的红细胞的能力,称为病毒的血凝,利用这种特性设计的试验称血球凝集(HA)试验,以此来推测被检材料中有无病毒存在,是非特异性的,但病毒的凝集红细胞的能力可被相应的特异性抗体所抑制,即血球凝集抑制(Hl)试验,具有特异性。
通过HA-HI试验,可用已知血清来鉴定未知病毒,也可用已知病毒来检查被检血清中的相应抗体和滴定抗体的含量。
2.用途:用于禽流感病毒的血凝素亚型鉴定和抗体检测。
3.试剂:禽流感病毒标准抗原、禽流感标准阴、阳性血清、阿氏液、1%的鸡红细胞、pH7.2的磷酸盐缓冲液。
4.设备耗材:普通天平、分析天平、普通离心机、微量振荡器、微量移液器、高压灭菌器、微量移液器、V形血凝反应板、吸头等。
5.操作步骤6.1血凝试验:5.L1取96孔V形微量反应板,用微量移液器在1孔〜12孔每孔加25μLPBS;5.L2吸取25μL病毒悬液加入第1孔中,吹打3〜5次充分混匀;5.L3从第1孔中吸取25uL混匀后的病毒液到第2孔,混匀后吸取251IL加入到第3孔,依次进行倍比稀释至第11孔,最后从第11孔吸取25UL弃之,设定第12孔位PBS对照;每孔再加入25μLPBSo5.1.4每孔加入25μLl%的鸡红细胞悬液(用前将鸡红细胞悬液充分混匀);振荡混匀反应混合液,室温(20-25。
C)静置40min后观察结果。
5.L5结果判定:在PBS对照出现正确结果的情况下,将反应板倾斜,观察红细胞是否完全凝集,以完全凝集的病毒最大稀释倍数为该抗原的血凝滴度。
完全凝集的病毒的最高稀释倍数为1个血凝单位(HAU)。
5.2血凝抑制试验:1.1.11配制4单位抗原:根据血凝试验结果配制4单位抗原,以能引起100%血凝的病毒最高稀释倍数代表1个血凝单位,4血凝单位抗原即为最高稀释倍数除以4。
加入抗原的血凝滴度为1:256,则4HAU抗原的稀释倍数为1:64,即ImI抗原加入到63mlPBS中即为4HAU 抗原;1.1.2取96孔V形微量反应板,用移液器在第1〜11孔各加入25ULPBS,第12孔加入50ULPBS;1.1.3第1孔加入25UL新城疫标准阳性血清,充分混匀后移出25μL至第2孔,依次倍比稀释至第10孔,第10孔弃去25μL,第11孔做阴性对照,第12孔为PBS对照。
红细胞裂解液的配制

红细胞裂解液的配制我在一个公司的网站上看到的红细胞裂解液的说明书上说操作要点是:1.在37度预热;2.充分混匀细胞我就是这样做的,效果还可以。
不过我只做流式细胞仪的检测,活性没测。
我的裂解液是0.16M NH4Cl,0.13mM EDTA,12mM NaHCO3我用的方法:全血:裂解液=1:3,如2ml的全血加上6ml的红细胞裂解液,充分混匀后,室温静置5mim,1000rpm离心6~10min。
红细胞裂解得非常充分。
0.15 M NH4CL, 0.01 M NaHCO3 and 1 mM EDTA (Sigma)Ammonium chloride (NH4Cl) 8.29 g 0.155 MPotassium bicarbonate (KHCO3) 1 g 10mMEDTA 0.37 g 1mMH2O 1l.Filter with 0.45µm filteraliquot in 100 ml aliquotsfilter the solution to be used with 0.2µm filter.我们用的是Tris-NH4Cl,具体配方如下:NH4Cl:4.15克加双蒸水500ml,取450ml;Tris:1.0297克加双蒸水50ml,再加上上面的450ml,共计500ml,高压灭菌,用时加10-20ml,静置5min,效果蛮好.9月29日我用的配方氯化铵3.735g,tris 1.3g,加在500ml水中,ph约7.2。
将全血约5ml加入配好的加入30ml裂解液的50ml试管中5分钟或15分钟,发现5分钟组细胞要多些,15分钟组细胞要少些,而且红细胞仍然有。
常用溶液的配制

常用试剂的配制1.无Ca2+、Mg2+Hanks液NaCl 4.5g KCl 0.2gNaHCO30.175gNa2HPO4·12H2O 0.076gKH2PO40.03g葡萄糖 0.5g0.4%酚红 2.5ml将上述成分依次溶解或加入到双蒸水中, 最后补加双蒸水至500ml, 以5.6%NaHCO3调整 pH 值至7.4,4℃冰箱保存备用。
2.甲基红试剂(1)成份甲基红 0.1g 蒸馏水 200ml95%乙醇 300ml(2)用途:测定甲基红反应。
3.Hanks液(原液)原液甲: NaCl 160gKCl 8gMgSO4·7H2O 2gMgCl2·6H2O 2g上述试剂加入800ml双蒸水。
溶解。
CaCl22.8g溶于100ml双蒸水上述二液混合,加双蒸水至1000ml,再加2ml氯仿防腐,4℃保存。
原液乙: Na2NPO4·12H2O 3.04gKH2PO41.2g葡萄糖 20g加入800ml双蒸水,溶解。
0.4%酚红溶液100ml上述二液混合,加双蒸水至1000ml,再加2ml氯仿防腐,4℃保存。
使用时甲,乙原液按下列比例配成Hanks 液使用液:原液甲1份、原液乙1份、双蒸水18份滤过,8磅20min灭菌,放4℃冰箱保存,使用前用NaHCO3调整PH值。
4.0.4%酚红溶液称取0.4g酚红置研钵中研碎,逐渐加入0.lmol/LNaOH并不断研磨,直到所有的颗粒几乎完全解,加入0.lmol/LNaOHl0ml,然后倒入容量瓶中,并加蒸馏水至l00ml,棕色瓶保存备用。
5.pH7.2 Tris-NH4CI溶液(红细胞崩解液)Tris (三羟甲基氨基甲烷) 1.03gNH4Cl(氯化氨) 3.735g加双蒸水至500ml,用浓HCl调pH=7.2,10磅15min灭菌后放4℃保存。
6.0.05moI/L pH8.6 巴比妥缓冲液巴比妥 1.84g加蒸馏水 200ml 加热溶解巴比妥纳 10.3g叠氮纳 0.2g加蒸馏水溶解 , 并补加到 1000ml 。
标准操作规程(SOP)——蔗糖密度梯度离心纯化流感病毒

标准操作规程(SOP)——一、目的流感病毒的浓缩和纯化方式可以分为物理和化学的方法。
如:超速离心法,酸沉淀法,红细胞吸附-释放法,蒸馏水透析法及聚乙二醇浓缩法等。
其中超速离心法最为常用并且纯度较高。
本SOP明确流感病毒蔗糖密度梯度离心纯化的标准操作方法,保证了实验结果的职能却可靠。
二、范围适用于中国国家流感中心的所有技术人员进行蔗糖密度梯度离心纯化流感病毒。
三、程序(一)生物安全要求H5、H7亚型高致病性禽流感病毒及H2N2亚型流感病毒的操作需要在BSL-3级实验室中进行。
其余流感病毒的操作需要在BSL-2级实验室中进行。
操作人员的生物安全防护要求详见流感中心“生物安全个人防护SOP”(二)材料1.病毒液2.PBS(100mmol/L pH7.2)液3.30%和60%蔗糖溶液4.耗材(注射器,离心管,吸管,实验滤纸)(三)实验步骤1.将待纯化的流感病毒种子株接种鸡胚或者MDCK细胞,收获病毒尿囊液。
具体接种方法参见“流感病毒的鸡胚分离方法SOP”和“MDCK细胞分离流感病毒SOP”。
2.将流感病毒收获的鸡胚尿囊液使用实验滤纸粗滤,以去除蛋壳或者其它沉淀物。
MDCK细胞培养的病毒收获液可以省略此步骤。
3.收集过滤液,使用SIGMA3K18 高速离心及2000rpm离心20min,去沉渣。
4.将上清使用OptimaTM L-80XP 超速离心机30000rpm的转速离心1h,去上清。
加入100mmol/L pH7.2的PBS液数滴浸泡沉淀,置4℃冰箱过夜。
5.制备蔗糖梯度管,用10mL吸管加5mL的60%的蔗糖溶液于管底,在其上小心加入10mL的30%的蔗糖溶液。
在其上缓慢加入20mL病毒悬液。
6.使用OptimaTM L-80XP 超速离心机20000rpm的转速离心1.5h,取出离心管。
使用注射器小心吸取位于30%和60%之间的靠近管底的病毒条带。
7.于所收获的液体加入5倍体积的PBS液,混匀后30000rpm的转速离心1h,去上清。
ACK红细胞裂解液(ACK Lysis Buffer)

ACK红细胞裂解液(ACK Lysis Buffer)产品简介:去除红细胞的方法有多种,Leagene生产的ACK红细胞裂解液(Red Blood Cell Lysis Buffer),也称为ACK Lysis Buffer,是一种从人、鼠或其他哺乳动物等体内的组织样品或血液中裂解并去除无核红细胞的溶液,其主要有效成分为氯化铵,ACK Lysis Buffer经过优化配方,在裂解无核红细胞的同时几乎不损伤淋巴细胞(lymphocyte)或其它有细胞核的细胞。
Leagene ACK Lysis Buffer对于裂解、去除有细胞核红细胞,例如鸟或禽类的红细胞,效果不佳,裂解类似细胞时,不建议采用。
本裂解液经过滤除菌,经过ACK Lysis Buffer 处理过的血液或组织细胞样品可以用于后续的细胞培养、细胞融合以及核酸或蛋白的提取及各种常规的分析和检测。
产品组成:主要成分:主要由NH4Cl组成,pH7.2。
自备材料:1、胰蛋白酶,亦可采购Leagene的胰蛋白酶-EDTA溶液(0.25%:0.02%)(CC0130)2、离心机3、PBS、HBSS、生理盐水或无血清培养液操作步骤(仅供参考):(一)组织细胞样本的常规操作1、制备细胞悬液: 新鲜组织经过胰蛋白酶或胶原酶等消化处理,通过适当方法制备成细胞悬液,离心弃上清。
2、裂解: 加入3~5倍细胞沉淀体积的ACK Lysis Buffer,轻柔吹打混匀,裂解1~2min。
本操作步骤在4℃条件下操作更佳,亦可在室温下操作。
3、离心: 4℃,400~500g离心5min,弃红色上清。
如无低温离心机本步骤亦可在室温下操作。
4、如果发现红细胞裂解不完全,可以重复上述步骤2和步骤3各一次。
5、洗涤:根据具体实验要求加入适量PBS、HBSS、生理盐水或无血清培养液,轻柔混匀重悬沉淀。
4℃,400~500g离心2~3min,弃上清,离心步骤亦可在室温下操作。
所加入的PBS、HBSS、生理盐水或无血清培养液的量一般应大于细胞沉淀体积的5倍以上。
洗涤红细胞

特点
一般手工洗涤红细胞可以除去红细胞中80%~90%的白细胞和9%以上的血浆蛋白。使用机器洗涤后的红细胞中, 白细胞减至5×10/L以下,几乎不含有任何血浆蛋白。该制品不仅可降低白细胞引起的 FNHTR反应,也可以减少或 避免血浆蛋白所致的变态反应,适用于自身免疫性溶血性贫血和阵发性睡眠性血红蛋白尿症需输血的患者及对血 浆蛋白、白细胞和血小板产生抗体的患者。无论哪种方法洗涤后的红细胞均应在24h内输注,因为在洗涤过程中破 坏了原血袋的密闭系统,有操作污染的可能。
适应症
(1)对血浆蛋白有变态反应的贫血患者。 (2)自身免疫性溶血性贫血患者。 (3)阵发性睡眠性血红蛋白尿症患者。 (4)高钾血症及肝肾功能障碍需要输血者。
注意事项
需输注洗涤红细胞悬液的病人在输前应作相应的配血试验本品制备时采取无菌技术可将血液成分转移到另一 袋。血样应作相应的交叉鉴定,并且每袋均须鉴定相符。
洗涤红细胞
外科常用的成份输血制品
01 制备方法
03 适应症 05 不良反应
目录
02 特点 04 注意事项
洗涤红细胞(Washed red blood cells,WRBC)是外科常用的成份输血制品。是健康血液除去全部血浆和 90%白细胞及血小板。临床用于因多次输血而产生白细胞抗体的贫血病人,以及器官移植后病人,减少排斥反应。
不良反应
1.循环负荷过度; 2.溶血性输血反应; 3.HLA抗原和红细胞抗原同种免疫: 4.当4℃保存后少于4天(96h)时,可能传染梅毒; 5.病毒传染(肝炎、艾滋病等),尽管有严格的供血者选择和血液; 6.筛选过程,病毒传染仍可能发生; 7.原虫感染(如疟疾)可发生于个别病例中; 8.细菌感染引起败血症; 9.输血后紫癜。
制备方法
实验六 新城疫实验室诊断

10
第1页共1页
11 12 稀释度 1∶2 1∶22 1∶23 1∶24 1∶25 1∶26 1∶27 1∶28 1∶29 1∶210 1∶211 1∶212 生理盐水
本文格式为 Word 版,下载可任意编辑,页眉双击删除即可。
25 25 25 25 25 25 25 25 25 25 25 25 鸡胚液 25 25 25
第1页共1页
本文格式为 Word 版,下载可任意编辑,页眉双击删除即可。
来说,出现临诊症状的鸡所占的比例及发病鸡的严峻程度可能有很大差异。 后继续卵乳化 24/ml,开始照蛋每日两次,连续 5 日,弃去 24h 内死胚,
典型 ND 的特征性病变是全身呈出血性败血改变:腺胃乳头出血或溃疡; 收集 24~ 120h 死胚和剩余活胚置 4℃保持,鸡胚液〔尿素液和羊水〕 置
本文格式为 Word 版,下载可任意编辑,页眉双击删除即可。
实验六 新城疫实验室诊断
的血液与 1/4 体积的抗凝剂混合,用 PH7.2、0.01mol/LPBS 液洗涤 3 次, 每次均以 3000rpm 离心 10min,洗涤后用 PBS 配成体积分数为 1%红细胞
试验六 新城疫的试验室诊断 〔一〕试验目的 1.把握鸡新城疫的临诊诊断要点。 2.把握鸡胚接种、病毒分别方法并用 H、HI 试验鉴定其病毒 〔二〕试验原理 有些病毒,如禽流感病毒、新城疫病毒、Eds76 等,能凝集某种动物 的红血球,故可以来推想材料中有无该病毒的存在。如有能凝集血球的病 毒,其凝集性可为相应的抗体所抑制,这种抑制还有特异性,故病毒的血 球凝集抑制试验,可用已知病毒来检查被检血清中的相应抗体,也可用已 知血清来鉴定未知病毒。 〔三〕试验预备 抗凝剂的制备:5%枸椽酸钠+0.9%生理盐水,分装、纱布扎口、灭菌 消毒 15 磅/20min。 1%红细胞悬液制备:采集无禽流感和新城疫等抗体的健康成年公鸡
影响血凝抑制实验的因素

影响血凝抑制实验的因素目前,县级实验室做的最多的要数血凝试验和血凝抑制试验。
经过反复操作,不断摸索,逐渐找出一些影响血凝抑制试验的因素。
现列举出来,以便日后引以为戒。
1 红细胞悬液浓度:来源于不同个体鸡的红细胞,对抗原的敏感性不尽相同。
因此实验时最好用3-4只未免疫鸡。
配制红细胞时,红细胞浓度低,HI滴度就会下降;红细胞浓度高,HI滴度就会上升。
有实验表明,红细胞浓度增加一倍,HI滴度就会上升20.7-0.9,因此,红细胞浓度以1%为宜。
2 抗原的稀释倍数:配制抗原时,浓度必须准确。
当抗原浓度高时,HI抗体效价就下降;当抗原浓度抵时,HI抗体效价就上升。
3 实验用的稀释液(PBS):稀释液的pH值对实验有影响。
稀释液的pH值5.8以下,红细胞容易产生自凝现象;pH值在7.8以上凝集图形易消失,也会造成实验误差。
而pH值为7.0时,红细胞沉降最充分,图形最清晰,HI效价也最高,因此实验时用ph7.0-7.2的稀释液。
4 实验时的温度:实验时的温度,从4-37℃,随着温度上升,HA与HI滴度提高,但在37℃时,凝集的红细胞易洗脱;4℃以下红细胞易产生自凝,故操作常用18-22℃。
(以上所阐述的是实验室操作过程中存在的几点因素,在实际工作中,也存在着其他诸多原因,如采样的时间、采样的数量、以及由疫苗产生的影响等第。
)血凝抑制试验:一些动物红细胞(如鸡、豚鼠等)以及人“O”型血红细胞上有流感病毒受体,遇流感病毒可产生红细胞凝集现象,简称血凝。
若将特异性抗体与流感病毒(血凝素)预先作用后再加入红细胞则不产生凝集,称为血凝抑制现象。
用定量血凝素与不同稀释度血清抗体作用后,能完全抑制血凝的最高稀释度,即为血凝抑制抗体效价。
血凝抑制试验主要材料:1 大孔塑料板,1mL吸管或1mL移液器。
2 双份血清收集及处理:急性期血清于发病3d内采取,恢复期血清于发病后2~4周采取。
取0.1mL已分离的血清加入0.9(或0.4)mL霍乱滤液(RDE)(即1∶10或1∶5稀释)摇匀,于37℃水浴中过夜,以去除血清中的非特异性抑制素,次日置56℃水浴50min以灭活多余的RDE。
红细胞裂解液配方

红细胞裂解液配方
1.裂解液:的确是ACK裂解液作用更柔和些
配方:
NH4CL 8.29g
KHCO3 1.00g
Na2EDTA 37.2mg
溶于1000mL蒸馏水,pH 7.2-7.4,效果一直很好。
注意:
(1)裂解液如果放在冰箱里,一定要预热,37度即可。
裂解期间试管也可水浴,但如果是夏天室温比较高则不必;
(2)裂解5min后立刻离心(从所有管都混匀后计时间);
(3)PBS离心洗涤2次;
(4)裂解液pH值很重要,最好一次不要配多,时间长效果不好,我一般一次配100mL,避光保存。
2.离心速度:800-1000rpm,5min
3.研磨轻柔很重要
4.培养淋巴细胞的最佳培养液是RPMI 1640,因为是原代细胞,要用10%胎牛血清。
还有非常重要的一点,要想让细胞增殖得好,必须加二巯基乙醇(beta-2ME)
5.细胞密度1-2X10^6/mL。
人红细胞生成素EPO说明书
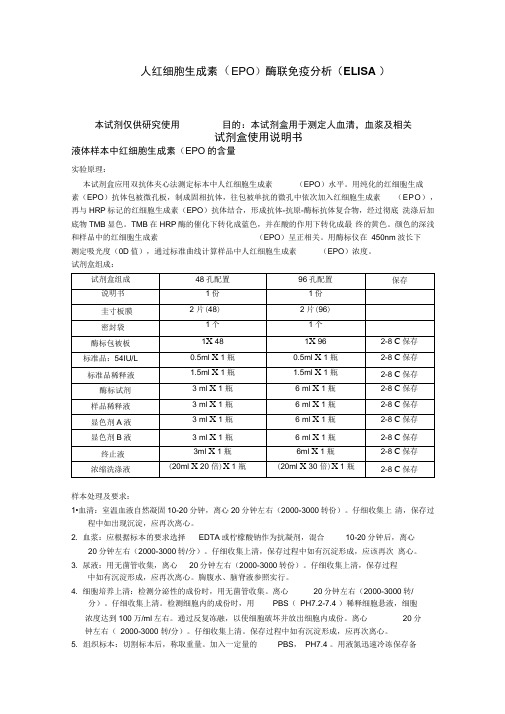
人红细胞生成素(EPO)酶联免疫分析(ELISA )本试剂仅供研究使用目的:本试剂盒用于测定人血清,血浆及相关试剂盒使用说明书液体样本中红细胞生成素(EPO的含量实验原理:本试剂盒应用双抗体夹心法测定标本中人红细胞生成素(EPO)水平。
用纯化的红细胞生成素(EPO)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入红细胞生成素(EPO),再与HRP标记的红细胞生成素(EPO)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的红细胞生成素(EPO)呈正相关。
用酶标仪在450nm波长下测定吸光度(0D值),通过标准曲线计算样品中人红细胞生成素(EPO)浓度。
试剂盒组成:样本处理及要求:1•血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转份)。
仔细收集上清,保存过程中如出现沉淀,应再次离心。
2. 血浆:应根据标本的要求选择EDTA或柠檬酸钠作为抗凝剂,混合10-20分钟后,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如有沉淀形成,应该再次离心。
3. 尿液:用无菌管收集,离心20分钟左右(2000-3000转份)。
仔细收集上清,保存过程中如有沉淀形成,应再次离心。
胸腹水、脑脊液参照实行。
4. 细胞培养上清:检测分泌性的成份时,用无菌管收集。
离心20分钟左右(2000-3000转/分)。
仔细收集上清。
检测细胞内的成份时,用PBS(PH7.2-7.4 )稀释细胞悬液,细胞浓度达到100万/ml左右。
通过反复冻融,以使细胞破坏并放出细胞内成份。
离心20分钟左右(2000-3000 转/分)。
仔细收集上清。
保存过程中如有沉淀形成,应再次离心。
5. 组织标本:切割标本后,称取重量。
加入一定量的PBS,PH7.4 。
用液氮迅速冷冻保存备用。
标本融化后仍然保持2-8C的温度。
酶联免疫吸附测定法

酶联免疫吸附测定法(ELISA)1.定义 (3)2.原理 (3)2.1抗原抗体反应 (3)2.2免疫测定在临床检验中的应用 (5)3.ELISA的类型 (5)3.1双抗体夹心法测抗原: (6)3.2双抗原夹心法测抗体 (6)3.3间接法测抗体 (6)3.4竞争法测抗体 (7)3.5竞争性测抗原 (7)3.6捕获包被法测抗体 (7)3.7ABS-ELISA法 (8)4.ELISA试剂的组成 (9)4.1固相载体: (9)4.2包被的方式 (9)4.3包被用抗原:天然抗原、重组抗原、合成多肽抗原。
(10)4.4包被的条件: (10)4.5洗涤液: (10)4.7酶的催化性; (11)4.8结合物的制备 (11)4.9结合物的保存 (12)4.10酶的底物 (12)4.11酶反应终止液 (12)4.12参考标准品 (13)4.13加样: (13)4.14保温 (13)4.15保温方式: (13)4.16室温温育的反应 (13)4.17洗涤 (14)4.18显色 (14)4.19比色 (14)4.20酶标比色仪 (15)4.21结果判定 (15)4.22定量测定 (16)4.23ELISA的操作要点 (16)1.定义酶联免疫吸附测定法(Enzyme Linked ImmunoSorbent Assay),简称ELISA,采用抗原与抗体的特异反应将待测物与酶连接,然后通过酶与底物产生颜色反应,对受检物质进行定性或定量分析的一种检测方法。
2.原理采用抗原与抗体的特异反应将待测物与酶连接,然后通过酶与底物产生颜色反应,可对受检物质的定性或定量分析。
2.1抗原抗体反应2.1.1可逆性抗原与抗体结合形成抗原抗体复合物的过程是一种动态平衡,其反应式为:Ag+Ab→Ag·Ab抗体的亲和力(affinity),可以用平衡常数K表示:K=[Ag·Ab]/[Ag][Ab],Ag·Ab的解离程度与K值有关。
全血及成分血质量要求

全血及成分血质量要求1 范围本标准规定了临床输注用全血和成分血的质量标准。
本标准适用于国内临床输注用的全血和成分血。
2 引用标准下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。
本标准出版时,所示版本均为有效。
所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。
GB 14232~1993 一次性使用塑料血袋GB 18467~2001 献血者健康检查要求YY 0168~1994 血液冷藏箱3 定义本标准采用GB 14232中的定义及下列定义。
3.1 保养液以抗凝剂、葡萄糖等为主要成分的用于防止血液凝固、维持血液内各种组分活性和生理功能的一类药剂。
3.2 血液制剂将一定量正常人的血液或血液成分与一定量的保养液混合在一起形成的均一制品。
3.3 添加液对某一种血液制剂进行再加工时,针对某一种血液成分而加入的能保持和(或)营养该血液成分生物活性,维持其生理功能的一类保养液。
3.4 全血将一定量的血液采集到含一定量保养液的采血袋内所制成的血液制剂。
3.5 成分血在一定条件下用物理方法分离出全血内的一种或几种血液成分而制成的血液制剂。
3.6 红细胞成分血以全血内红细胞为主要组成的一类成分血。
3.7 浓缩红细胞将采集到多联袋内的全血中大部分血浆在全封闭的条件下分离出后剩余的部分所制成的红细胞成分血。
3.8 悬浮红细胞将采集到多联袋内的全血中大部分血浆在全封闭的条件下分离出后并向剩余物加入红细胞添加液制成的红细胞成分血。
3.9 浓缩少白细胞红细胞将采集到多联袋内的全血中的大部分白细胞、血小板及血浆在全封闭的条件下去除后制成的红细胞成分血。
3.10 悬浮少白细胞红细胞将采集到多联袋内的全血中的大部分白细胞、血小板及血浆在全封闭的条件下去除后向剩余物加入红细胞添加液所制成的红细胞成分血。
3.11 洗涤红细胞采用物理方式在无菌条件下将保存期内全血、浓缩红细胞、悬浮红细胞血液制剂用大量静脉注射用0.9%的生理盐水洗涤,去除绝大部分非红细胞部分,并将红细胞悬浮在0.9%的生理盐水中制成的红细胞成分血。
RH血型鉴定

--
16
• 五、ABO血型的遗传
• A和B为显性基因,O为隐性基因
举例:
A
AO
B BO
AB
AO
BO
OO
--
17
任务一(第三节)ABO血型鉴定
• 一、标本的采集 • 柠檬酸钠抗凝剂 • 二、红细胞悬液的配制 • 1、洗涤: • 2、配制2%~5%的红细胞悬液 5%红细胞悬液=比容红细胞1滴+生理盐水1ml 2%红细胞悬液=比容红细胞1滴+生理盐水2ml
--
18
• 三、标准血清要求 • 1、特异性 • 2、效价 • 3、亲和力 • 4、不含冷凝集素 • 5、不含补体,无任何污染 • 四、标准红细胞悬液的制备
--
19
• 五、ABO血型鉴定方法
• 正定型: 用已知抗A、抗B和抗A+B分型血清来测定
红细胞上有无相应的A、B抗原
• 反定型:
用已知A抗原和B抗原红细胞来测定 血清中有无相应的抗A、抗B抗体。
的母亲孕育了Rh
胎儿后,胎儿红细胞可通过
胎盘屏障进入母体的血循环中,刺激母体产
生
,该抗体
进入胎儿体内
而发生新生儿溶血病。由于第一胎产生的抗体效价较
低,一般对胎儿无明显影响。但第二胎时抗体效价增
高,易引起新生儿溶血病。
--
12
复习思考题
• 4、木瓜酶可破坏红细胞表面带负电荷
的
,降低红细胞表面负电荷,使红
无察觉 输血)
大 小
4-25℃
对血型物质的作用 能否通过胎盘
易被血型物质中和
中和 不能
与红C反应的介质
盐水介质 白等
--
免疫抗体( Ig)G
有抗原刺激(妊娠、
洗涤红细胞的特点

洗涤红细胞(WRC)
这是一种目前认为比较安全的红细胞制剂。
1.洗涤红细胞的特点:
洗涤红细胞是在少白细胞红细胞的基础上用无菌生理盐水反复洗涤三遍以上
制备而成。
经过洗涤的红细胞去除了80%以上的白细胞和98%的血浆蛋白,也去除了大量的细胞碎屑、代谢产物、抗凝剂、乳酸盐、钾、氨和微聚物,同时也损失了大约20%以上的红细胞。
2.适应证:
(1)该成分适用于各类需要输注红细胞的病人;
(2)更适合于对血浆蛋白有严重过敏反应的病人;
(3)自身免疫性溶血性贫血;
(4)阵发性血红蛋白尿;
(5)高血钾症及肝肾功能障碍者以及新生儿换血等。
3.注意事项:
(1)开放制备的洗涤红细胞应在制备后24小时内输注。
(2)由于该成分内已基本不含抗A抗B抗体,输注前可只做主侧配血。
(3)输注剂量要比浓缩红细胞增加30%左右。
(五)冰冻解冻去甘油红细胞(FTRC)
红细胞加入甘油保护剂后在-80或-196 OC低温条件下保存,最长保存期可达10年。
使用前将贮存的红细胞放在37 OC水浴中解冻,然后洗净甘油,再用生理盐水悬浮24小时内输注。
该成分主要用于稀有血型血液的贮存也可用于自体血液的长期贮存。
该成分内也基本不含抗A抗B抗体,输注前可只做主侧配血。
在输注剂量上也应考虑到红细胞损失部分。
标准操作规程(SOP)——1%马红细胞悬液制备

一、目的该文件用以详细说明1%马红细胞悬液的制备过程和相关技术要求,用以确保马红细胞的采集、保存规范有效;确保马红细胞悬液的配制、保存质量良好,从而确保应用到该悬液的后续实验(流感病毒红细胞凝集及红细胞凝集抑制试验)的结果可靠准确。
二、范围适用于中国国家流感中心所有技术人员进行1%马红细胞悬液的制备。
三、程序(一)生物安全要求BSL-1实验室,详见生物安全个人防护SOP 。
(二)材料1.PBS pH 7.2~7.4 (Sigma P3813)将1包PBS 粉剂溶于1000mL 去离子水中,121 20min ℃高压灭菌,置室温保存。
2.0.85% NaCl0.85g NaCl 用蒸馏水配至100mL ,溶解,分装,121 20min ℃高压灭菌,置室温保存。
3.Alsever 氏液葡萄糖 2.08g柠檬酸钠 0.80g柠檬酸 0.055gNaCl 0.42g加蒸馏水至 100mL121 20min ℃高压灭菌,置4℃备用。
标准操作规程(SOP )——液制备4.注射器(60mL)5.医用酒精棉签6.2%~5%碘酒棉签7.无菌棉签8.15 mL离心管9.标签(三)实验步骤1.马红细胞采集和保存(1)操作者在实验前穿工作衣,戴手套、口罩。
(2)采血时由助手面对马站立拉住缰绳,将其颈部绕过结实柱子,使其颈部暴露于采血者。
采血者在其颈部下1/3处探明静脉,碘酒或酒精消毒,于60mL注射器中先吸入约20mLAlsever’s液,左手压在静脉沟下部使静脉怒张,右手持针头猛力刺入皮肤,此时血液流入注射器,采血至50mL。
可隔天采血,每天可采50~100mL血液。
(3)采血部位以干棉球压迫数分钟止血。
(4)迅速将血液注入灭菌容器中,在采集后的红细胞液中补加Alsever’s液至采血量的4倍(如:第二步采血至50mL后,则应补加100mLAlsever’s液)。
在采血容器上贴标签(标签内容包括:红细胞名称,采集时间,制备人)。
清洗液产品标准

目录前言 (Ⅳ)1 范围 (3)2引用标准.................................................... (3)3 命名 (4)4 要求 (4)5 试验方法 (5)6 检验规则 (6)7标志、标签和使用说明书 (6)8包装、运输、贮存 (7)前言血细胞分析仪用清洗液,按照国家《中华人民共和国医药行业标准》有关规定,根据临床检验体外诊断试剂技术基本要求,特制定本标准。
本标准由XXXX科技有限责任公司提出并起草。
本标准由XXX医疗器械行业标准化技术委员会归口。
本标准主要起草人:血细胞分析仪用清洗液1范围:本标准规定了血细胞分析仪用清洗液的命名、要求、试验方法、检验规则、标志、标签、使用说明书、包装、运输和贮存。
本标准适用于血细胞分析仪随机专用清洗液(以下简称清洗液)。
该产品为血细胞分析仪随机专用配套试剂,用于医疗机构使用血细胞分析仪进行血细胞分析。
2 引用标准:下列标准所包含的条文,通过在本标准中引用而构成本标准的条文。
本标准出版时,所示版本均为有效。
所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。
GB191-2000 包装储运图示标志GB/T6678-1986 化工产品采样总则GB/T9724-1988 化学试剂PH值测定通则GB/T13306-1991 标牌中华人民共和国药典2005年版二部附录VII DYY/T 0456.1-2003 中华人民共和国医药行业标准(清洗液部分)3.清洗液的命名:XXX清洗液产品型号4 要求:4.1外观:清洗液应无色、透明,不得有沉淀,颗粒或絮状物。
4.2 外部标志:清洗液产品外部标志应符合7.1的要求。
4.3净含量:清洗液净含量应符合表1的规定:表1 净含量要求4.4 pH值的要求:清洗液在(25℃±1℃)的PH值应在6.0-10.0 范围之内。
4.5清洗液的空白计数:表2 清洗液的空白计数要求4.6 洗净率:清洗液的洗净率不小于90%4.7批间差:PH值的批间差应符合:△PH<0.54.8 稳定性:清洗液有效期为一年,取到期后三个月的留样检测,4.1、4.4-4.6 ,结果应符合各项规定的要求。
促红细胞生成素生产工艺设计流程

促红细胞生成素生产工艺设计流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor.I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!促红细胞生成素生产工艺设计流程详解促红细胞生成素(Erythropoietin,简称EPO)是一种重要的生物制品,主要用于治疗肾性贫血和其他相关疾病。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
北京雷根生物技术有限公司
红细胞洗涤液(pH7.2)
简介:
在生物科研领域,经常需要去除红细胞。
去除红细胞的方法有ACK Lysis Buffer 、Tris-氯化铵红细胞裂解液、Gey's Lysis Buffer 等,在裂解红细胞之前,可以采用PBS 清洗红细胞,亦可用专门的红细胞洗涤液,以便充分清洗细胞。
本试剂为无菌溶液,主要由磷酸盐、氯化钠、氯化钾等组成。
组成:
操作步骤(仅供参考):
1、取新鲜抗凝血,离心,去除血浆。
2、 加入红细胞洗涤液(pH7.2),清洗2~3次。
注意事项:
1、后续试验如果是用于细胞培养,操作过程中应注意无菌操作,尽量在超净工作台内操作。
2、离心步骤尽量在4℃离心机上操作。
3、离心洗涤后,通常极微量的红细胞不会影响后续的检测。
4、为了您的安全和健康,请穿实验服并戴一次性手套操作。
有效期: 12个月有效。
相关:
编号 名称 CS0004 Storage 红细胞洗涤液(pH7.2) 100ml 4℃ 使用说明书 1份 编号 名称
CC0130 胰蛋白酶-EDTA 溶液(0.25%:0.02%)
CS0006 Tris-氯化铵红细胞裂解液
DA0020 Hoechst33342/PI 细胞凋亡染色试剂盒
DG0005 糖原PAS 染色液
NR0003 Lezol(总RNA 提取试剂)
TC0713 葡萄糖检测试剂盒(GOD-POD 比色法)。
