胆固醇代谢
胆固醇的代谢

胆固醇是一种含有27个碳原子并高度修饰的生物小分子。
它是脊椎动物细胞膜的重要成分,也是脂蛋白的组成成分。
胆固醇的衍生物胆酸盐、维生素D和类固醇激素在脂类消化中和动物的生长、发育过程中都具有重要的作用。
生物体内的胆固醇主要来源于两个方面,一方面是自身合成;另一方面是从外界摄入。
膳食中摄入的胆固醇被小肠吸收后,通过血液循环进入肝代谢。
当外源胆固醇摄入量增高时,可抑制肝内胆固醇的合成,所以在正常情况下体内胆固醇量维持动态平衡。
各种因素引起胆固醇代谢紊乱都可使血液中胆固醇水平增高,从而引起动脉粥样硬化,因此高胆固醇血症患者应注意控制膳食中胆固醇的摄入量。
除成年动物脑组织和成熟红细胞外,其他组织和细胞均可以合成胆固醇,其中肝是合成胆固醇的主要场所,机体内70%~80的胆固醇是由肝合成,其他如小肠、皮肤、肾上腺皮质、性腺和动脉血管壁均能合成少量胆固醇。
合成胆固醇的酶系存在于细胞液和滑面内质网膜上。
采用14C和13C标记乙酸的甲基碳及羧基碳,研究结果表明,乙酸分子中的2个碳原子都参与了胆固醇的合成。
其中有15个胆固醇中的碳原子来自乙酸的甲基,12个来自于乙酸的羧基。
合成胆固醇的原料是乙酰CoA,它可以经过“柠檬酸–丙酮酸循环”从线粒体转运至细胞液中。
由于乙酰CoA也可用于脂肪酸的合成,因此它是胆固醇和脂肪酸这两种脂类物质合成途径的分支点。
鲨烯(squalene)是胆固醇生物合成的中间代谢物,它由5个异戊二烯单位行成,胆固醇的合成可以归纳四个阶段:乙酰CoA3-甲基-35-二羟基戊酸异戊烯焦磷酸酯鲨烯胆固醇27C30C5C6C2C CoA3353–甲基–35–二羟戊酸(mevalonic acid,MVA)简称甲羟戊酸(mevalonate)。
由2分子乙酰CoA缩合成乙酰乙酰CoA,然后再与1分子乙酰CoA缩合成3–羟基–3–甲基戊二酸单酰CoA(HMG–CoA),该化合物是合成胆固醇和酮体的重要中间产物。
在线粒体中,HMG–CoA裂解后生成酮体;而在细胞液中,HMG–CoA则在内质网HMG–CoA还原酶催化下,由NADPH提供氢,还原形成甲羟戊酸。
胆固醇合成与代谢调控

胆固醇合成与代谢调控胆固醇是一种脂质,在体内广泛存在,而且对于我们的身体很有必要。
在人体中,胆固醇是一种重要的组成部分,它在细胞中起着维持细胞膜完整性、合成荷尔蒙、维持神经系统健康等重要作用。
但是,如果胆固醇含量过多,就会增加动脉粥样硬化、心脏病等心血管疾病的风险。
因此,研究胆固醇的合成和代谢调控对于预防和治疗这些疾病十分重要。
一、胆固醇的合成途径胆固醇的合成主要发生在肝脏和肠道中,而且合成的起点都是从醋酸开始。
醋酸可以通过三个途径转化成胆固醇,分别是类固醇原路(mevalonate)途径、非类固醇原路(non-mevalonate)途径以及嗜氧呼吸(aerobic respiration)途径。
其中,类固醇原路途径是胆固醇合成的主要途径,它包括两个阶段:第一阶段是醋酸—丙酮酸—胆酸酰辅酶A(acetyl-CoA)途径,第二阶段是胆固醇合成途径。
在这个过程中,mRNA等因子的作用是必不可少的。
二、胆固醇的代谢调控胆固醇的合成与代谢调控主要由两种基础机制实现,分别是靶点反应和反馈抑制。
靶点反应是指正常代谢活动期间合成胆固醇的靶点反应机制。
在这个过程中,膳食胆固醇的摄入和肝脏胆固醇的合成从变量方面受到调节,从而控制胆固醇的代谢。
反馈抑制则是旨在降低细胞内胆固醇水平的机制。
在这个过程中,有三种非常重要的酶参与了胆固醇代谢调控,分别是胆固醇酰辅酶A还原酶(HMG-CoA reductase)、胆固醇酯酶(ACAT)和胆固醇7α-羟化酶(CYP7A1)。
HMG-CoA reductase是限制胆固醇合成的主要酶,因此可以作为一个“瓶颈”来调节胆固醇合成。
ACAT参与了胆固醇在细胞中的储存和利用,而CYP7A1则被认为是胆固醇代谢的限制因子。
三、胆固醇与健康胆固醇的含量过多会增加心血管疾病、脑血管疾病等的风险。
因此,通过改变饮食习惯、增加体育锻炼等方式来控制胆固醇含量是非常重要的。
此外,药物治疗也是控制胆固醇含量的有效手段之一。
胆固醇代谢途径在脂质代谢调节中的作用及其机制

胆固醇代谢途径在脂质代谢调节中的作用及其机制脂质是人体中不可或缺的重要生化物质之一,它们在维持人体正常生理功能中扮演着重要角色。
然而,当脂质代谢紊乱时,会引发多种疾病,包括高脂血症、动脉粥样硬化和冠心病等,这些疾病对患者的健康造成了严重威胁。
因此,对脂质代谢调控的研究变得至关重要。
胆固醇是一种重要的脂类化合物,在人体中有着多种生理功能,然而其含量过高也会影响健康。
因此,研究胆固醇代谢途径在脂质代谢调节中的作用及其机制,有重要的临床意义。
胆固醇代谢途径包括胆固醇合成途径、胆固醇摄取途径和胆固醇转运途径。
这些代谢途径紧密相连,共同影响着胆固醇在人体中的生物学作用。
胆固醇合成途径主要发生在肝脏和肠道,其中最为重要的酶是 HMG-CoA 还原酶。
在体内,多数胆固醇以形式结合到载脂蛋白中进行转运,其中最重要的载脂蛋白是 LDL 和 HDL。
通过这些载脂蛋白,胆固醇可以被转运到不同的组织细胞中,发挥其生物学作用。
胆固醇代谢途径在脂质代谢调节中的作用机制主要体现在两个方面:一是通过谷固醇代谢途径的调节,二是通过基因表达和信号传导的调节。
首先,谷固醇代谢途径是人体内调节血液胆固醇水平的重要途径之一。
这一代谢途径不仅可以抑制 HMG-CoA 还原酶转录和翻译,也能够通过降低 LXR 活性,抑制由HMG-CoA 还原酶产生的胆固醇合成。
同样,谷固醇在人体内也能够作为胆汁酸的前体物,进一步调节胆固醇的代谢过程。
其次,胆固醇代谢途径通过基因表达和信号传导调节脂质代谢。
研究表明,多种激素和核受体可以通过调节胆固醇合成途径和胆固醇转运途径来影响脂质代谢。
例如,LXR 可以促进 ABCG1、ABCA1等基因的表达,从而促进胆固醇转运。
而HMG-CoA 还原酶的表达与 Insig-1 和 Insig-2 的相互作用、LXR 的拮抗剂等多种因素有关,这些因素通过多重信号传递途径调节 HMG-CoA 还原酶表达与活性,从而影响血液中胆固醇的含量。
胆固醇代谢在代谢综合征中的作用研究

胆固醇代谢在代谢综合征中的作用研究代谢综合征是指一组交叉病理生理状态的集合,包括糖尿病、高血压、肥胖、高血脂等。
这些疾病常常相互关联,共同导致心血管疾病、脑血管病等严重疾病的发生。
随着生活方式变化和高脂肪饮食习惯的普及,代谢综合征的患病率逐年上升。
因此,研究代谢综合征的发病机制非常必要。
胆固醇是人体中不可或缺的脂质成分,它在细胞膜和神经系统中具有重要的生理功能。
但当胆固醇的水平过高,就会加速动脉粥样硬化的形成,导致心脑血管疾病的发生。
因此,保持胆固醇的正常代谢是预防心血管疾病的关键。
近年来,越来越多的研究表明胆固醇代谢与代谢综合征之间存在紧密的联系。
一些学者认为,代谢综合征患者往往存在胆固醇代谢紊乱的情况。
下面我们将从胆固醇代谢与代谢综合征的关系以及当前的研究进展两个方面来讨论它们的联系。
一、胆固醇代谢与代谢综合征的关系胆固醇是通过肝脏合成和脂蛋白代谢两种方式被人体代谢的。
从肝脏合成入手,体内胆固醇主要是由醇固醇合成和异戊烷合成两种方式合成的。
醇固醇合成是指胆固醇通过3-羟基-3-甲基戊二酰辅酶A还原反应转化为醇固醇,然后再通过醇固醇酰基转移酶作用转化为胆固醇。
而异戊烷合成是指胆固醇通过酮基和异戊烷四烯酸反应进而生成胆固醇。
从这两种代谢途径入手,我们可以看出代谢综合征的发病机制与胆固醇代谢息息相关。
一方面,研究发现,代谢综合征患者往往存在肝脏合成胆固醇的异常,肝脏合成胆固醇的速率增加,从而导致胆固醇的水平升高。
另一方面,代谢综合征患者血液中高密度脂蛋白(HDL)含量下降,LDL和三酰甘油含量升高,这些都是胆固醇代谢紊乱的表现。
二、胆固醇代谢在代谢综合征中的作用研究进展为了揭示胆固醇代谢与代谢综合征的关系,目前已经开展了大量的研究工作。
这些研究主要包括以下几个方面。
1.酯酶的作用酯酶是调节肝脏和周围组织脂质代谢的重要酶类。
研究发现,在代谢综合征患者中,脂肪酸酯酶-1与胆固醇合成有良好的正相关关系,其活性越高,胆固醇水平也就越高。
代谢生物化学第三十章 胆固醇代谢

脂肪 B-100,
运输内源的脂肪
C-I,II,III, E
脂肪, B-100, E 一部分被肝吸收,
胆固醇
一部分转变为LDL
胆固醇 B-100
蛋白质 A, CI,II,III, D, E
将胆固醇转运到外 周组织
胆固醇的逆向运输, 向CM和VLDL提 供脂蛋白
四种血浆脂蛋白的显微结构
脱辅基脂蛋白
¶ “apo” =无脂的蛋白质形式 ¶ 特殊的脂/胆固醇载体蛋白 ¶ 与特定的受体作用和/或调节特定的酶活性 ¶ 人类至少已发现9 种不同的脱辅基脂蛋白
胆固醇合成的第三个阶段的反应
其他异戊二烯类化合物的形成
第四阶段:鲨烯→胆固醇
« 当鲨烯合成以后,由于它不溶于水,需要细 胞质基质中的固醇载体蛋白将其运输到内质 网膜上开始最后一个阶段的反应。
« 共由22步反应组成: 鲨烯→2,3-环氧鲨烯→羊毛固醇→7-脱氢胆 固醇→胆固醇。
胆固醇合成的第四个阶段的反应
第三十章 胆固醇代谢
杨荣武 生物化 学原理 第二版
提纲
一、胆固醇的合成 二、胆固醇的运输 三、胆固醇的代谢转变 四、胆固醇代谢的调节
我们需要胆固醇的四大理由
¶ 膜的组分——控制膜的流动性 ¶ 胆汁酸/盐的前体 ¶ 固醇类激素的前体 ¶ 维生素D的前体
胆固醇的结构
胆固醇酯化的位点
胆固醇的生物合成
血浆脂蛋白
=脂 + 脱辅基脂蛋白
« 乳糜微粒-CM (小肠) « 极低密度脂蛋白-VLDL (肝) « 中间密度脂蛋白-IDL « 低密度脂蛋白-LDL « 高密度脂蛋白-HDL « VLDL IDL LDL
五种血浆脂蛋白的结构与功能
种类
密度 (kg/L)
胆固醇代谢的新机制研究

胆固醇代谢的新机制研究胆固醇是一种生物体内必需的脂质物质,它在人体内参与许多重要的生理过程,例如作为细胞膜的组成成分、合成性激素和胆汁酸等。
然而,胆固醇过多会在人体内积累,导致多种心血管疾病,例如高血压和动脉粥样硬化等。
因此,控制胆固醇水平对于保持身体健康至关重要。
最近,一些新的研究揭示了关于胆固醇代谢的全新机制,本文将介绍这些新机制的研究进展。
1. 胆固醇吸收和转运的新角色以前认为肠道是胆固醇吸收和转运的主要场所,但现在研究表明,肝脏在胆固醇吸收和代谢中扮演重要角色。
一项最新的研究表明,肝脏介导胆固醇在人体内的循环,并作为其在体内的“中转站”来调节其水平。
这项研究发现,肝脏中一种名为“肝外胆固醇运输蛋白”(NPC1L1)的蛋白质,在胆固醇吸收和转运中拥有新的功能。
这种蛋白质在肠道中主要负责胆固醇吸收,但在肝脏中它能够将胆固醇转运至肝脏,并由肝脏将其分解和利用。
这项研究结果提供了新的机制来控制体内胆固醇水平,为研发新的药物提供了新的思路。
2. 肝细胞新型信号通路的发现肝脏是我们身体内的胆固醇“生产工厂”,其细胞中含有胆固醇合成途径所需的各种酶和基因调控的因子。
虽然我们已经知道了这些机制,但我们还不完全清楚这些过程的调控机制。
最近,科学家们发现了一个新的信号通路,它可以通过改变胆固醇合成酶的稳定性来影响胆固醇合成。
这个新的信号通路一般与糖原合成酶(GSK-3)的活性调节有关。
这项研究显示,GSK-3能够通过对另一种名为“谷胱甘肽代谢途径”中的化学反应进行调节,在肝细胞内促进胆固醇合成。
这个发现有助于更深入地了解胆固醇合成过程,并有望为开发新的药物提供新的靶点。
3. 胆固醇可逆转运机制的发现胆固醇的过多积累是许多疾病的根源,因此将多余的胆固醇从细胞内运出体外是一个重要的过程。
以前认为,这个过程是通过一种名为“容受体介导胆固醇转运蛋白”(ABCA1)的蛋白质介导的。
然而,现在研究表明,另外一种名为“sTLS(抑制性tiptibody 对于酯化的体性Lipase)的蛋白质也有胆固醇转运的能力。
胆固醇生物合成及其代谢通路的研究

胆固醇生物合成及其代谢通路的研究一、什么是胆固醇?胆固醇是一种类固醇化合物,是人体内重要的生物分子之一。
它是一种脂质,常常被大家认为是“坏”的脂肪,但实际上它在体内还是有很重要的作用的。
胆固醇分为来自食物的胆固醇和体内合成的胆固醇。
前者对人体的影响相对较小,而后者是体内生物合成和代谢的分子基础之一,对人体生命活动、细胞结构、性激素的合成等方面都有着非常重要的作用。
二、胆固醇生物合成通路胆固醇的生物合成是一条复杂的代谢通路,包括多种酶催化反应和多个亚细胞器参与的过程。
在细胞质内,酶通过一系列的化学反应,从醋酸开始,不断产生新的化合物,最后合成胆固醇。
简而言之,胆固醇生物合成通路可概括为以下几个步骤:1.乙醇酸合成途径。
乙酰辅酶A通过一系列酶催化反应生成乙醇酸,是胆固醇生物合成的起点。
2.戊二酸合成途径。
乙醇酸通过一系列催化反应途径,转化为戊二酸。
3.HMG-CoA还原途径。
每一步产物都被用来继续形成下一个化合物,直到其在内质网上经过HMG-CoA还原酶催化反应,形成前体物——胆固醇。
4.胆固醇合成。
在HMG-CoA还原酶催化下,两个HMG-CoA分子结合成为“二聚体”,生成脱钙胆酸酶和甘油三酯的前体物胆固醇。
三、胆固醇代谢通路体内胆固醇代谢与其生物合成同等重要,它是维持胆固醇稳态水平的关键。
胆固醇代谢通路分为三个主要步骤:1.胆汁酸合成。
体内的胆固醇与辅酶A结合,生成脱钙胆酸酶。
随后一系列反应将其转化为三种不同的胆汁酸,最后排泄出体外。
2.甘油三酯合成。
体内大部分胆固醇都被转化为胆汁酸,只有少部分成为胆固醇酯储存起来。
在储存过程中,大部分是以甘油三酯的形式储存,通过一系列酶催化反应形成。
3.胆固醇排泄。
体内多余的胆固醇则被肝脏转化为胆汁酸或胆酸盐,然后通过肠道排泄出体外。
四、胆固醇代谢异常与疾病胆固醇在人体内的稳定水平是极其重要的,胆固醇代谢异常会对人体带来危害。
代谢异常的情况包括胆固醇生成过多、胆固醇代谢过程不良。
高中生物校本课程-胆固醇代谢

细胞定位:细胞质、光面内质网
(二)合成原料
1分子胆固醇 18乙酰CoA + 36ATP + 16(NADPH+H+)
葡萄糖有氧氧化
磷酸戊糖途径
乙酰CoA通过柠檬酸-丙酮酸循环出线粒体
(三)合成基本过程
线粒体中 乙酰CoA
原料
柠檬酸-丙 酮酸循环
入胞质
HMG-CoA
2.引起AS的脂蛋白
脂蛋白残粒
CM和VLDL经LPL水解生成CM残粒与IDL, 并转变成富含胆固醇酯和ApoE的颗粒沉积于血 管壁,经清道夫受体介导摄取进入巨噬细胞引起 AS的增强作用。
变性LDL
乙酰LDL 、 氧化LDL 、 糖化LDL 经修饰的LDL,如OX-LDL会激活巨噬细胞,使 巨噬细胞摄取乙酰LDL而转变成泡沫细胞,促进 AS形成。
HDL2在CETP介导下,与VLDL、LDL进行CE交换,同时也转 运TG,以VLDL、LDL形式经肝脏摄取,最终使末梢组织的FC输
送到肝脏。HDL主要功能是参与胆固醇逆转运(RCT) (胆固醇
逆转运)
三、动脉粥样硬化(AS)
1.概述
AS是指动脉内膜的脂质、血液成分的沉积,平滑肌 细胞及胶原纤维增生,伴有坏死及钙化等不同程度病变 的一类慢性进行性病理过程。AS主要损伤动脉内壁膜。
限速酶
HMG-CoA 还原酶
胆固醇酯
胆固醇
鲨烯
甲基羟戊酸 (MVA)
胆固醇合成的调节
限速酶
饱食 胰岛素 甲状腺素
HMG-CoA还原酶
胆固醇 饥饿禁食
胰高血糖素
➢酶的活性具有昼夜节律性 (午夜最高,中午最低)
《胆固醇代谢》课件

03
渲染这个名称 when (渲染)渲染这个 名称 when using rendered integer type assumes that you want to render it in a rendered integer type".渲染这个名称 when using rendered integer type assumes that you want to render it in a rendered integer type".
激素合成
胆固醇是合成类固醇激素 的原料,包括性激素和肾 上腺皮质激素等。
维生素D的合成
胆固醇在皮肤中经过紫外 线照射可转化为维生素D ,参与钙的吸收和骨骼健 康。
胆固醇的来源与去路
来源
胆固醇主要来源于人体自身合成,肝脏是主要的合成器官。 此外,食物中的胆固醇也是人体胆固醇的一个来源。
去路
胆固醇在体内经过代谢后由肠道排出体外,或以胆汁酸的形 式进入肠道帮助脂肪的消化。此外,胆固醇也可以被用于合 成类固醇激素和维生素D等。
饮食调整
1 2
控制总热量摄入
减少高热量食物的摄入,控制体重在正常范围内 。
减少饱和脂肪和反式脂肪的摄入
饱和脂肪和反式脂肪是导致胆固醇升高的主要原 因,应尽量少吃。
3
增加可溶性纤维的摄入
可溶性纤维能够降低血液中的低密度脂蛋白胆固 醇水平。
生活方式干预
增加有氧运动
有规律的有氧运动能够降 低血液中的低密度脂蛋白 胆固醇水平。
04
CATALOGUE
胆固醇与疾病的关系
胆固醇与疾病的关系
01
the method by which one can obtain a reputable input is identical to that of an integerType and is known to have a good input that takes integerTypeType:IntegerTypeEnu m:IntegerType:IntegerType:Intege rTypeEnum:IntegerType:IntegerTy pe:IntegerType:IntegerType:Intege rType:IntegerType:IntegerType:Int egerType:IntegerType:IntegerType :IntegerType:IntegerType:IntegerT ype:IntegerType:IntegerType:Integ erType:IntegerType:IntegerType:In tegerType:IntegerType:IntegerTyp e:IntegerType:IntegerType:Integer
生物化学第五节 胆固醇代谢

第五节胆固醇代谢2015-07-07 71752 0一、体内胆固醇来自食物和内源性合成胆固醇有游离胆固醇( free cholesterol,FC),亦称非酯化胆固醇(unesterified cholesterol)和胆固醇酯( cholesterol ester)两种形式,广泛分布于各组织,约1/4分布在脑及神经组织,约占脑组织20%。
肾上腺、卵巢等类固醇激素分泌腺,胆固醇含量达1% ~5%。
肝、肾、肠等内脏及皮肤、脂肪组织,胆固醇含量约为每100g组织200~500mg,以肝最多。
肌组织含量约为每100g组织100~200mg。
(一)体内胆固醇合成的主要场所是肝除成年动物脑组织及成熟红细胞外,几乎全身各组织均可合成胆固醇,每天合成量为lg左右。
肝是主要合成器官,占自身合成胆固醇的70%~80%,其次是小肠,合成10%。
胆固醇合成酶系存在于胞质及光面内质网膜。
(二)乙酰CoA和NADPH是胆固醇合成基本原料14C及13C标记乙酸甲基碳及羧基碳,与肝切片孵育证明,乙酸分子中的2个碳原子均参与构成胆固醇,是合成胆固醇唯一碳源。
乙酰CoA是葡萄糖、氨基酸及脂肪酸在线粒体的分解产物,不能通过线粒体内膜,需在线粒体内与草酰乙酸缩合生成柠檬酸,通过线粒体内膜载体进入胞质,裂解成乙酰CoA,作为胆固醇合成原料。
每转运1分子乙酰CoA,由柠檬酸裂解成乙酰CoA时消耗1分子ATP。
胆固醇合成还需NADPH供氢、ATP供能。
合成1分子胆固醇需18分子乙酰CoA、36分子AIP及16分子NADPH。
(三)胆固醇合成由以HMG-CoA还原酶为关键酶的一系列酶促反应完成胆固醇合成过程复杂,有近30步酶促反应,大致可划分为三个阶段(图7_9)。
1.由乙酰CoA合成甲羟戊酸2分子乙酰CoA在乙酰乙酰CoA硫解酶作用下,缩合成乙酰乙酰CoA;再在HMG-CoA合酶作用下,与1分子乙酰CoA缩合成HMG-CoA。
在线粒体中,HMG-CoA被裂解生成酮体;而胞质生成的HMG-CoA,则在内质网HMG-CoA还原酶(HMG-CoA reductase)作用下,由NADPH供氧,还原生成甲羟戊酸(mevalonic acid,MVA)。
提高胆固醇代谢的方法

提高胆固醇代谢的方法1. 增加膳食纤维摄入增加膳食纤维摄入可以帮助降低胆固醇水平,膳食纤维可以在肠道中结合胆固醇,减少其被吸收的机会,从而有利于提高胆固醇代谢。
2. 多食用富含Omega-3脂肪酸的食物Omega-3脂肪酸有助于提高身体胆固醇代谢,例如鱼类、亚麻籽、核桃等都是富含Omega-3脂肪酸的食物,适量摄入对提高胆固醇代谢有帮助。
3. 控制饱和脂肪摄入过量摄入饱和脂肪会提高血液中的胆固醇水平,因此需要避免过多的摄入肥肉、黄油等高饱和脂肪食物。
4. 多食用蔬菜水果蔬菜水果中含有丰富的天然抗氧化剂和膳食纤维,有助于改善胆固醇代谢,建议多食用各种色彩的蔬菜水果。
5. 减少炸食和加工食品摄入炸食和加工食品中的反式脂肪和高糖成分会影响胆固醇代谢,因此需要适量摄入或者尽量避免这类食物。
6. 增加适量的体力活动适量的体力活动可以有助于增加高密度脂蛋白(HDL)胆固醇,促进胆固醇代谢。
7. 控制体重体重过重会导致胆固醇水平升高,因此需要控制体重,保持适当的体重有利于提高胆固醇代谢。
8. 遵医嘱使用降胆固醇药物对于一些患有高胆固醇症的患者,遵医嘱使用降胆固醇药物也是提高胆固醇代谢的有效方法。
9. 增加富含叶绿素的食物摄入叶绿素可以帮助加速胆固醇代谢,建议多摄入绿叶蔬菜等富含叶绿素的食物。
10. 控制饮食中的胆固醇摄入过量摄入胆固醇也会影响胆固醇代谢,因此需要控制饮食中胆固醇的摄入量,尤其是动物内脏等高胆固醇食物。
11. 饮食多样化饮食多样化可以提供多种营养素,有助于平衡胆固醇代谢,建议在饮食中包含来自不同食物类别的多种营养。
12. 避免过量饮酒过量饮酒会增加胆固醇水平,因此需要避免过量饮酒,特别是高度酒精含量的饮品。
13. 增加维生素B摄入维生素B族中的叶酸和维生素B6有助于降低血液中的升级水平,建议多摄入富含维生素B的食物。
14. 控制糖的摄入过量摄入糖分会导致胆固醇水平增加,因此需要控制糖的摄入量,尤其是加工食品中的隐藏糖分。
胆固醇初级代谢产物鹅去氧胆酸

胆固醇初级代谢产物鹅去氧胆酸鹅去氧胆酸是一种重要的代谢产物,它是胆固醇初级代谢的中间产物。
胆固醇是一种脂质分子,在生物体内发挥着重要的生理功能,同时也是一些疾病(如高胆固醇血症、动脉粥样硬化等)的主要危险因素之一。
在胆固醇的合成和代谢过程中,鹅去氧胆酸具有重要的作用。
鹅去氧胆酸的生物合成鹅去氧胆酸的生物合成过程涉及多个酶和代谢通路。
首先,胆固醇通过胆固醇7α-羟化酶(CYP7A1)的作用而转化为7α-羟胆固醇。
接着,7α-羟胆固醇在羟化酶和丙酮酸羧化酶的作用下转化为7-酮胆固醇。
随后,7-酮胆固醇在还原酶和异构酶的作用下转化为7-去氧胆固酸,再经过另一重要的酶——去氧胆酸-羟化酶(cytochrome P450 7B1,CYP7B1)的作用而转化为鹅去氧胆酸。
鹅去氧胆酸除了在胆固醇的代谢过程中起到重要作用之外,还在多个生理过程中发挥着重要的生物学作用。
这包括:1)调节脂肪代谢和能量代谢;2)抗氧化作用;3)参与神经发育和生长过程等。
鹅去氧胆酸对脂肪代谢和能量代谢的调节作用主要通过活化TGR5(Takeda-G protein coupled receptor 5)受体实现。
TGR5受体广泛分布于多个组织和器官中,包括肝脏、胆囊、胰腺、肠道、脑、心脏等。
激活TGR5受体可以促进葡萄糖代谢、抑制甘油三酯(TG)的合成和脂肪酸的氧化,从而调节脂肪代谢和能量代谢。
鹅去氧胆酸的抗氧化作用主要通过清除自由基和对细胞色素P450和呼吸链酶的调节实现。
自由基是细胞代谢过程中产生的高度反应性分子,对细胞膜、纤维蛋白、核酸等造成损伤。
鹅去氧胆酸能够与自由基进行任意的反应,从而保护细胞免受自由基的损伤。
鹅去氧胆酸在神经发育和生长过程中的作用主要是通过调节信号通路和基因表达实现的。
在胚胎发育过程中,鹅去氧胆酸能够促进胰岛素样生长因子-1(insulin-like growth factor-1,IGF-1)和神经生长因子(nerve growth factor,NGF)的合成和释放,促进神经细胞增殖和分化。
胆固醇代谢
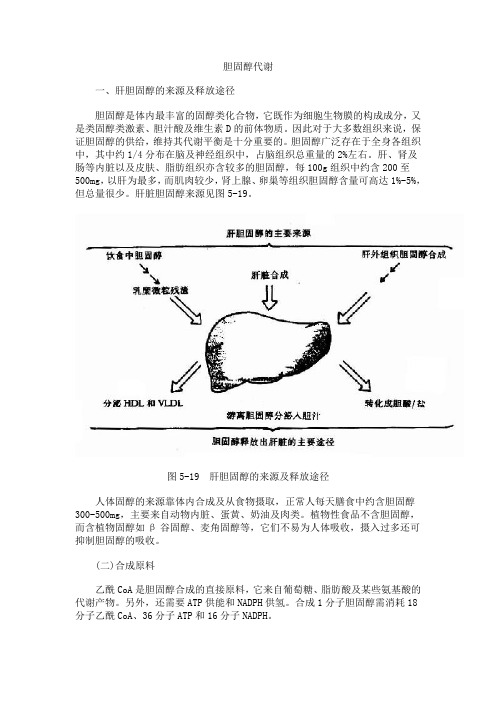
胆固醇代谢一、肝胆固醇的来源及释放途径胆固醇是体内最丰富的固醇类化合物,它既作为细胞生物膜的构成成分,又是类固醇类激素、胆汁酸及维生素D的前体物质。
因此对于大多数组织来说,保证胆固醇的供给,维持其代谢平衡是十分重要的。
胆固醇广泛存在于全身各组织中,其中约1/4分布在脑及神经组织中,占脑组织总重量的2%左右。
肝、肾及肠等内脏以及皮肤、脂肪组织亦含较多的胆固醇,每100g组织中约含200至500mg,以肝为最多,而肌肉较少,肾上腺、卵巢等组织胆固醇含量可高达1%-5%,但总量很少。
肝脏胆固醇来源见图5-19。
图5-19 肝胆固醇的来源及释放途径人体固醇的来源靠体内合成及从食物摄取,正常人每天膳食中约含胆固醇300-500mg,主要来自动物内脏、蛋黄、奶油及肉类。
植物性食品不含胆固醇,而含植物固醇如β谷固醇、麦角固醇等,它们不易为人体吸收,摄入过多还可抑制胆固醇的吸收。
(二)合成原料乙酰CoA是胆固醇合成的直接原料,它来自葡萄糖、脂肪酸及某些氨基酸的代谢产物。
另外,还需要ATP供能和NADPH供氢。
合成1分子胆固醇需消耗18分子乙酰CoA、36分子ATP和16分子NADPH。
(三)合成基本过程胆固醇合成过程比较复杂,有近30步反应,整个过程可根据为3个阶段。
1.3 羟-3甲基戊二酸甲酰CoA(HMGCoA)的生成在胞液中,3分子乙酰CoA经硫解酶及HMGCoA合成酶催化生成HMGCoA,此过程与酮体生成机制相同。
但细胞内定位不同,此过程在胞液中进行,而酮体生成在肝细胞线粒体内进行,因此肝脏细胞中有两套同功酶分别进行上述反应。
2.甲羟戊酸(mevalonic acid,MVA)的生成HMGCoA在HMG CoA还原酶(HMGCoA reductase)催化下,消耗两分子NADPH+H+生成甲羟戊酸(MVA)此过程是不可逆的,HMG还原酶是胆固醇合成的限速酶。
3.胆固醇的生成MVA先经磷酸化、脱羧、脱羟基、再缩合生成含30C的鲨烯,经内质网环化酶和加氧酶催化生成羊毛脂固醇,后者再经氧化还原等多步反应最后失去了3个C,合成27C的胆固醇(图5-20)。
胆固醇代谢和调节机制研究

综合来看,胆固醇代谢和调节机制的研究取得了巨大的进展,但仍有许多领域有待深入探究。未来的研究方向将是胆固醇在心血管、肝脏等疾病中的具体作用、机制及其调控、对肠道微生物以及对于多个因素的协调作用。这样的研究不仅能够为营养保健和医学领域提供参考,也能够为基础生物学的发展提供强有力的支持和帮助。
胆固醇代谢主要包括胆固醇的合成、吸收、转运和代谢四个方面。胆固醇的合成主要发生在肝脏中,通过1-2个碳原子的增加生物合成胆固醇。而肠道吸收的胆固醇来自食物的来源,通过ATP-binding cassette转运蛋白3(G5)和ABCG8在肠道粘膜上形成胆固醇运输体,转运到肝脏进行代谢。另外,胆固醇的主要代谢物是胆汁酸和神经甾类激素。胆汁酸是胆固醇通过肝脏合成后的代谢产物,不仅能够帮助人体吸收脂溶性维生素和脂质物质,还能够通过调节基础代谢率、脂肪代谢和胆汁的分泌等方式参与多个生理过程。
胆固醇调节机制的研究是针对胆固醇过多的病变机制的探讨。现代研究已发现调节胆固醇水平的多种因素,包括基因、环境、饮食等。最流行和有影响的因素是脂类浓度和APOE位点。APOE位点是胆固醇代谢系统中最重要的基因表达位点之一,研究显示APOE位点变异与心血管疾病之间存在关系。此外,食物的摄入也会关乎到胆固醇因素。例如低脂饮食和多饱和脂肪酸饮食都能够对胆固醇的调节产生影响。
胆固醇代谢和调节机制研究
胆固醇是一种重要的生物学分子,常常被人们所关注。人们对于胆固醇的研究不止于了解胆固醇的作用,还包括了胆固醇代谢和调节机制方面的研究。这些研究的成果不仅为临床治疗提供了新思路和新方法,而且还拓展了人类对身体机制的认识。
调控胆固醇代谢的生物学机制的研究

调控胆固醇代谢的生物学机制的研究近年来,随着人们生活条件的改善和寿命的延长,心血管疾病已经成为影响全球健康的主要疾病之一。
而胆固醇在心血管疾病中起着重要的作用。
因此,研究调控胆固醇代谢的生物学机制显得尤为重要。
胆固醇是一种脂质,具有多种生物学功能。
然而,当胆固醇在体内过多时,它就会沉积在动脉血管壁上,导致动脉粥样硬化。
因此,控制胆固醇水平对预防心血管疾病非常关键。
胆固醇代谢是一个复杂的生物过程,其中参与了多种生物分子和信号通路。
其中,主要的代谢途径包括肝脏合成和胆汁酸代谢、胆固醇转化为胆汁酸和胆固醇外排等。
此外,胆固醇代谢还受到许多调控因子的影响,如遗传因素、环境因素和生活方式因素等。
在肝脏细胞内,胆固醇的合成是一个复杂的多步骤过程。
该过程涉及多种酶的参与,如HMG-CoA还原酶、获得酰辅酶A胆固醇酰转酶等。
同时,该过程还受到多种调控因子的影响,如LDL受体和HDL受体等。
这些因子通过调节胆固醇生物合成的速率来影响细胞内胆固醇水平。
胆固醇转化为胆汁酸是另一个重要的代谢途径。
在肝脏中,胆固醇被酶催化转化为胆汁酸,然后通过胆汁排放到肠道中。
在肠道中,胆汁酸参与脂类的吸收和消化。
然而,胆固醇转化为胆汁酸的速率也受到多种因素的调控,如FXR核受体和LXR核受体。
在胆囊中,胆汁酸与胆固醇混合形成胆汁。
胆汁随后释放到肠道中,参与脂类的吸收。
在肠道中,胆汁酸可以被肠道细菌代谢成为多种代谢产物。
其中的一些代谢产物可以被肝脏重新吸收和再循环,从而影响体内胆固醇水平。
除了这些代谢途径,还有一些其他的代谢途径也对胆固醇代谢产生影响。
例如,脂蛋白LP(a)能够竞争LDL受体,导致血液中的胆固醇水平升高。
此外,肝细胞表面的SR-B1蛋白负责调节HDL颗粒和细胞膜上游离胆固醇之间的转运。
总的来说,控制胆固醇水平是非常重要的,因为胆固醇的高水平与心血管疾病的发生有很强的关联。
虽然我们已经了解了胆固醇代谢的一些关键环节和调控机制,但仍有很多问题有待进一步研究。
胆固醇合成途径的代谢调控研究

胆固醇合成途径的代谢调控研究胆固醇是一种重要的脂质类物质,在人体内具有多种生理功能,如维持细胞膜的完整性、参与合成激素和胆汁等。
然而,高水平的胆固醇会导致动脉粥样硬化等多种疾病的发生和加重。
因此,调控胆固醇水平对维持人体健康至关重要。
胆固醇的合成主要发生在肝脏和小肠上皮细胞内。
胆固醇合成途径又称为Mevalonate途径,涉及到多个关键酶的催化和反应。
该途径主要包括三个阶段。
第一阶段是酮戊二酸(Acetyl-CoA)的合成。
Acetyl-CoA来自于葡萄糖代谢、脂肪酸β氧化等途径。
在胆固醇合成途径中,Acetyl-CoA需要经过乙酰辅酶A羧化酶(Acetyl-CoA Carboxylase,ACC)的催化,被转化为酮戊二酸,为下一步合成提供前体物质。
第二阶段是色氨酸(Tryptophan)合成酶的催化。
通过乙酰辅酶A、酮戊二酸和色氨酸合成酶的催化,生成β-羟基-β-甲基戊二酸。
该物质在多次反应后,最终转化为胆固醇。
第三阶段是胆固醇合成酶的催化。
在此阶段,β-羟基-β-甲基戊二酸经过麦角固醇(Squalene)合成酶(Squalene Synthase,SQS)的催化,合成为麦角固醇。
然后,麦角固醇经过羟甲基戊二酸途径,参与甾体类化合物的生成和合成。
通过胆固醇合成酶的催化,最终生成胆固醇。
胆固醇的合成途径受到多种因素的调控。
其中,胆固醇合成酶是目前被研究较多的调控因子之一。
研究表明,胆固醇合成酶的表达活性与胆固醇水平存在着负相关关系。
当体内胆固醇水平升高时,胆固醇合成酶的表达受到抑制,从而减少胆固醇的合成。
而当体内胆固醇水平降低时,胆固醇合成酶的表达受到促进,增加胆固醇的合成。
此外,细胞内三磷酸腺苷(Adenosine Triphosphate,ATP)的水平也能够调控胆固醇的合成。
研究发现,细胞内ATP水平降低时,胆固醇合成酶受到促进,增加胆固醇的合成;而当ATP水平升高时,胆固醇合成酶受到抑制,减少胆固醇的合成。
胆固醇与肝脏的代谢

血液是护肝养肝的基础,血流量的减少使肝内血液循环功能下降,肝脏吸收营养、代谢和清除毒素的能力也相应减退
肝脏对来自体内和体外的许多非营养性物质如各种药物、毒物以及体内某些代谢产物,具有生物转化作用,通过新陈代谢将它们彻底分解或以原形排出体外,这种作用也被称作“解毒功能”
肝脏对来自体内和体外的许多非营养性物质如各种药物、毒物以及体内某些代谢产物,具有生物转化作用,通过新陈代谢将它们彻底分解或以原形排出体外,这种作用也被称作“解毒功能”。
某些毒物经过生物转化,可以转变为无毒或毒性较小,易于排泄的物质;但也有一些物质恰巧相反,毒性增强(如假神经递质形成),溶解度降低(如某些磺胺类药)。
肝脏的生物转化方式很多,一般水溶性物质,常以原形从尿和胆汁排出;脂溶性物质则易在体内积聚,并影响细胞代谢,必须通过肝脏一系列酶系统作用将其灭活,或转化为水溶性物质,再予排出
只有肝细胞具有通过胆汁分泌来清除大量多余胆固醇的功能
胆固醇的生物合成和肠道吸收对于维持肝脏的胆固醇储量,以及体内胆固醇来源的稳态平衡都至关重要。这两种途径之间也可以相互影响,处于一种代偿平衡:当肝脏合成胆固醇受到抑制时,肠道吸收胆固醇就会增Байду номын сангаас;反之亦然
他汀类药物可以减少肝脏合成胆固醇,胆固醇吸收抑制剂则作用于胆固醇吸收环节,减少肠道内胆固醇的吸收,因此二者在降胆固醇机制方面存在协同作用,联合应用时可同时抑制影响循环胆固醇水平的两个关键环节,进而显著增强降胆固醇作用
人体血循环中胆固醇主要来源于两种途径,即体内(肝脏与外周组织)生物合成和肠道胆固醇吸收。很多组织都能够合成胆固醇供细胞自身利用,多余的胆固醇经高密度脂蛋白转运入肝脏,而只有肝细胞具有通过胆汁分泌来清除大量多余胆固醇的功能。肝细胞摄取的胆固醇一部分被转化成胆盐,另一部分游离胆固醇被肝细胞泵出。经过一系列的反应,游离胆固醇、胆盐以及磷脂共同形成微团,通过胆汁分泌排入肠道。当饮食中的胆固醇被微团乳化后,便与存在于微团中的肝脏分泌的胆固醇一同被小肠上皮细胞吸收。简单地讲,无论是肝脏合成的胆固醇、还是饮食摄入的胆固醇,都需要经过肠道吸收才能进入血液循环
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
例:甘氨胆酸 glycocholic acid
胆囊
胆汁
胆固醇
结合胆汁酸 (合成0.4~0.6g/d 代谢池3~5g/d)
➢ 胆汁酸/盐为 胆固醇重要 的降解产物 和排泄方式
2. 胆固醇衍生为甾类激素
胆固醇——孕激素,糖皮质激素,盐皮质激素, 雄激素,雌激素的前体
游离胆汁酸
OH
Free bile acid
12
3
7
HO
H
OH
12
COOH 24
例:胆酸 Cholic acid
CHO
H
OH Chenodeoxycholic acid
结合胆汁酸 conjugated bile acid
OH
12
3
7
HO
H
OH
OH
12
3
HO
H
7 OH
CONHCH2CH2SO3H
2. 异戊烯醇焦磷酸酯(IPP)的生成
3. 胆固醇 的合成
合
成
的
基
3
本 过 程
4
胆固醇可以转化成 胆固醇酯
二、胆固醇的去路
胆固醇的母核——环戊烷多氢菲在体内不 能被降解,但侧链可被氧化、还原或降解,实现 胆固醇的转化。 ➢转变为胆汁酸 (bile acid)(肝脏) ➢转化为类固醇激素(肾上腺皮质、睾丸、卵巢 等内分泌腺) ➢转化为7 - 脱氢胆固醇(皮肤)
1. 二羟甲基戊酸
合酶
(MVA)的生成
oA
HMG-CoA还原酶的调节
高水平胆固醇(来自外源和内源)抑制酶的 合成——抑制酶mRNA的合成 HMG-CoA还原酶的半寿期为2-4h,高水平 胆固醇和MVA可导致酶的快速降解 受HMG-CoA还原酶激酶的磷酸化调节,磷 酸化使酶失活,去磷酸化使酶激活。 HMG-CoA还原酶失活/钝化(真菌代谢 物)——治疗高胆固醇血症
胆固醇
3. 胆固醇衍生为维 生素
7-脱氢胆固醇 胆钙化醇(VD3) 1,25-二羟维生素D3
等生理活性物质的前体。
* 胆固醇在体内含量及分布
含量: 约140克(来自食物、体内合成) 100-200mg/dl
分布:广泛分布于全身各组织中 大约 ¼ 分布在脑、神经组织
存在形式:游离胆固醇,胆固醇酯
一、 胆固醇的生物合成
合成部位: 以肝脏为主,小肠、皮肤、肾上腺皮质、性腺、 动脉血管壁合成少量。 主要阶段: 乙酰CoA(2C)→ MVA(二羟甲基戊酸,6C) → IPP(异戊烯焦磷酸酯,5C) →鲨烯(30C) →胆固醇(27C)
1. 胆固醇合成胆汁酸
胆汁酸(bile acids):存在于胆汁中一大类胆烷酸的 总称,简称胆盐 (bile salts)。 游离胆汁酸(free bile acid): 胆酸、脱氧胆酸、鹅脱氧胆酸、石胆酸(少) 结合胆汁酸(conjugated bile acid):胆汁酸+甘 氨酸/牛磺酸 甘氨胆酸、牛磺胆酸、甘氨鹅脱氧胆酸、牛磺鹅 脱氧胆酸
第五节 胆固醇代谢
Metabolism of Cholesterol
* 胆固醇(cholesterol)结构
site of attachment of fatty acid in cholesterol ester
* 胆固醇的生理功能
是生物膜的重要成分,对控制生物膜 的
流动性有重要作用; 是合成胆汁酸、类固醇激素及维生素D
