分子对接方法
分子对接的计算方法

分子对接的计算方法分子对接是研究分子之间相互作用的重要方法之一,也是药物设计和发现的重要手段。
本文将介绍分子对接的计算方法,包括分子对接的基本原理、常用的对接算法以及对接评价指标等内容。
一、分子对接的基本原理分子对接是指研究两个分子在特定条件下结合的过程。
在一个分子中,不同原子之间的结合方式是由不同的化学键决定的。
因此,在分子对接中,我们需要考虑来自两个分子之间的多种相互作用,如氢键、电荷相互作用和范德华力等。
分子对接的过程可以分为四步:1)预处理流程;2)构建计算模型;3)执行对接过程;4)结果分析。
在预处理流程中,需要进行双分子的构形搜索,即为每个分子寻找能量最低的构象以用于后面的分子对接计算。
在构建计算模型中,需要将每个分子的三维结构转化为能够进行计算的结构,并将两个分子同时输入计算机。
在执行对接过程中,需要调用分子对接算法,以计算两个分子之间的相互作用,找到最佳的配对方式。
最后,在结果分析中,需要评估分子对接的结果以确定这些分子是否适合结合,以及确定最佳的结合方式。
二、常用的对接算法为了找到最佳的配对方式,许多不同的分子对接算法已被开发出来。
这些算法中的一些常见的方法包括以下内容:1. 基于蒙特卡罗的对接方法基于蒙特卡罗(MC)的对接方法是一种在二维空间中进行随机游走的方法,通过模拟蒙特卡罗过程来寻找最佳的配对方式。
这种方法的优点在于其适合于使用分子动力学模拟技术进行计算,在计算中可以考虑原子或者分子之间的动态变化,更加真实地反映实验情况。
2. 基于分子力学的对接方法基于分子力学的对接方法是一种基于分子动力学模拟的方法。
该方法使用分子动力学技术来计算化学作用过程中的原子或分子的位置和速度变化。
由于该方法考虑了分子内部的相互作用和外部的环境条件对分子结合曲线和内部能量的影响,因此它比其他对接方法更加准确。
3. 基于评分函数的对接方法基于评分函数的对接方法是一种对接评估技术,它借助实验中已经被众所周知的分子结合模型来评估分子结合的力度。
分子对接的原理方法及应用

分子对接的原理方法及应用分子对接是一种计算机辅助药物设计的方法,旨在研究分子之间的相互作用,并预测化合物与靶点的结合能力。
本文将介绍分子对接的原理、方法和应用。
一、原理分子对接依赖于分子间的相互作用力,主要包括静电相互作用、疏水效应、范德华力、氢键等。
靶点通常是蛋白质,在药物设计中通常是疾病相关的蛋白质。
药物分子通过与靶点之间的相互作用,改变蛋白质的构象,从而调控其生物活性。
二、方法1.受体基因构建与表达:受体基因通过克隆技术构建并表达到适当的宿主细胞中,通常是大肠杆菌等。
2.配体库构建:配体库包括已知药物、天然产物等化合物。
配体库可通过多种方法构建,包括化学合成、天然产物提取等。
3.分子对接算法:常用的分子对接算法包括基于力场的对接、基于构象的对接和基于机器学习方法的对接。
其中,基于力场的对接方法基于分子力学力场和基本的物理原理进行模拟;基于构象的对接方法通过配体与受体结合的最佳构象;基于机器学习方法则通过对已知的配体-受体结合数据进行学习,同时预测新的配体-受体结合能力。
4.结果评估和优化:对于预测的配体-受体结合结果,可以通过计算结合自由能、氢键数目等来评估其可靠性。
同时,还可以通过化学修饰和结构优化等方法对候选物进行进一步优化。
三、应用1.药物研发:分子对接是药物设计的重要工具,通过预测化合物与靶点的结合能力,可以筛选出潜在的药物候选物。
其可以大幅度减少实验筛选的成本和时间。
2.靶标识别:分子对接可用于预测已知药物的作用靶点,为药物的多靶点设计提供参考。
3.蛋白质结构预测:利用分子对接方法,可以预测蛋白质的结构,尤其是在蛋白质晶体结构难以获取时,对药物设计和基因工程有重要意义。
4.农药和杀虫剂设计:分子对接可用于预测农药和杀虫剂与害虫体内受体结合的效果,从而设计出更高效的农药和杀虫剂。
5.仿生催化剂设计:分子对接可用于预测催化反应过程中底物与催化剂之间的相互作用,从而设计出更高效的仿生催化剂。
分子对接方法的应用与发展

分子对接方法的应用与发展分子对接方法是一种重要的生物物理学研究手段,用于研究分子之间的相互作用和识别机制。
该方法的应用范围广泛,涉及到药物发现、食品安全、环境监测等多个领域。
本文将介绍分子对接方法的发展历程、优点和不足,以及在各个领域中的应用场景,以期为相关领域的研究者提供参考和启示。
分子对接方法的发展可以追溯到20世纪90年代初,当时科学家们开始研究分子之间的相互作用和识别机制。
随着计算机技术的不断发展,分子对接方法逐渐成为生物物理学研究的重要工具。
目前,国内外研究者已经开发出了多种分子对接软件和算法,如AutoDock、Dock、FTDock等。
分子对接方法的优点在于其能够较为准确地预测分子之间的相互作用模式和结合亲和力。
同时,该方法还可以用于研究复杂生物体系中的多分子相互作用,从而为药物发现、食品安全、环境监测等领域提供理论支持和实践指导。
然而,分子对接方法也存在一定的不足之处,如对于某些类型的分子对接的精度和可靠性还有待进一步提高。
分子对接方法在药物发现领域中有着广泛的应用。
该方法可以通过预测药物与靶点分子之间的相互作用模式和结合亲和力,为新药研发提供重要的理论支持和实践指导。
例如,研究者可以利用分子对接方法预测候选药物与蛋白质靶点之间的相互作用,从而为药物设计和优化提供依据。
分子对接方法也可以应用于食品安全领域。
例如,可以利用该方法研究食品中添加剂与靶点分子之间的相互作用,从而为食品添加剂的合理使用和监管提供理论支持和实践指导。
在环境监测领域,分子对接方法可以用于研究污染物与生物体内部的靶点分子之间的相互作用,从而为环境污染的预防和治理提供理论依据和实践指导。
例如,可以利用该方法研究重金属离子与生物体中特定蛋白质的相互作用,进而探讨重金属污染的毒理效应和治理策略。
分子对接方法的基本原理是将两个或多个分子通过计算机模拟进行对接,以寻找它们之间最佳的相互作用模式和结合构象。
该方法主要分为自由空间中的对接和约束条件下的对接两种类型。
分子对接全

蛋白质二级结构的主要形式
• -螺旋 ( -helix ) • -折叠 ( -pleated sheet ) • -转角 ( -turn ) • 无规卷曲 ( random coil )
-螺旋
-折叠
-转角和无规卷曲
-转角
无规卷曲是用来阐述没有确定规律性的那部 分肽链结构。
❖ 定量指标,需要结合分子动力学进一步评价
AutoGrid 格点中相关能量的计算
AutoDock 构象搜索及评价
❖ 免费软件/
AutoDock分子对接的流程:
1.围绕受体活性位点的氨基酸残基形成一个盒 子(box),并划分成格点; 2.用配体不同类型的原子作为探针(probe)进 行扫描,计算格点能量; 3.对配体在box范围内进行构象搜索; 4.根据配体的不同构象、方向、位置及能量进 行评分,最后对结果进行排序。
蛋白质分子中各亚基的空间排布及亚基接 触部位的布局和相互作用,称为蛋白质的四级 结构。
亚基之间的结合力主要是疏水作用,其次 是氢键和 结 构
从一级结构到四级结构
血红蛋白
二、酶及其抑制剂
酶是由活细胞产生的对其特异的底物 起高效催化作用的蛋白质。
酶的分子组成
❖ 单纯酶(simple enzyme):仅由氨基酸残基构成 ❖ 结合酶(conjugated enzyme)
苏氨酸 threonine Thr T 5.60
3. 酸性氨基酸 4. 碱性氨基酸
天冬氨酸 aspartic acid Asp D 2.97 谷氨酸 glutamic acid Glu E 3.22
赖氨酸
lysine
Lys K 9.74
精氨酸 arginine Arg R 10.76
分子对接的原理,方法及应用
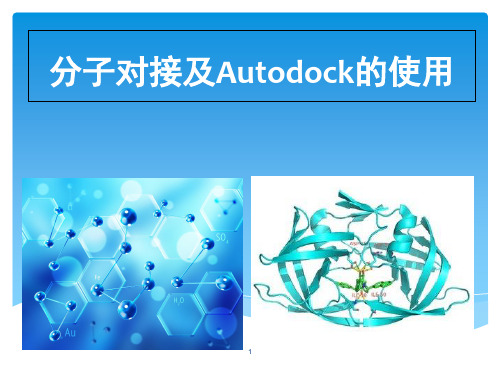
三个氢键受体的作用表面
Pose clustering 算法中的作用点
17
(二)柔性对接的方法 (1)构象的系综方法
Flexibase用来储存小分子库中每个分子的一系列 不同构象,用距离几何和能量最小化的方法产生构象, 每个分子根据rmsd的差异选择25个系列构象。每个 构象采用FLOG刚性对接的方法进行对接。
性键的二面角,寻找小分子化合物与靶标大分子作 用的最佳构象,计算其相互作用及结合能 在库中所有分子均完成了对接计算之后,即可从中 找出与靶标分子结合的最佳分子
9
10
4 分子对接的分类
1、刚性对接:对接过程中,研究体系的构象不发生变化。 适合考察比较大的体系,如蛋白质和蛋白质间以及蛋白质 与核酸间的对接。
14
受体的活性位点
配体
有效匹配的距离图集
受体-配体的示意图,字母代表特征部分如氢键等, 相应的有效匹配的图集如右,三个环性顶点组织的三角形 为这个图集的一个最大团(clique)
15
(2)基于几何哈希技术“geometric hashing”的方 法
第一部分中,几何哈希表从被对接的一个配体或一 系列配体中构建 。哈希矩阵含有配体名字和能调整 配体在空间方向的参考框架。
9.涂瑶生,孙冬梅,陈玉兴,等.中药新药筛选新技术及实践.世界科
学技术一中医药现代化,2014,16(8):1696—1702.
10.白晓光,许乐幸,李神亮,等.基于靶蛋白结构的CDK2小分子抑制
剂研究进展.中国新药杂志,2011,20(17):1667—1672. .................
——涉及到底物分子和受体分子间结合能力的预测, 牵涉到结合自由能的计算。
23
5 代表性对接软件
蛋白质-适配体相互作用预测的方法

蛋白质-适配体相互作用预测的方法引言蛋白质-适配体相互作用是生物学中重要的一部分,它们在细胞信号传导、药物靶点发现、蛋白质结构和功能研究等方面都扮演着重要的角色。
准确地预测蛋白质-适配体相互作用对于理解细胞功能和药物研发具有重要意义。
本文将介绍一些常用的蛋白质-适配体相互作用预测的方法,包括分子对接、结构基于方法和机器学习方法等,并对它们的优缺点进行讨论。
1. 分子对接方法分子对接是一种常用的蛋白质-适配体相互作用预测方法,它通过计算化合物或配体与蛋白质的结合能量,从而预测它们的结合方式和亲和性。
分子对接方法主要分为基于结构的对接和基于能量的对接两种类型。
基于结构的对接方法利用分子模拟技术,通过计算蛋白质和配体的结合方式和结合能量来预测它们的相互作用。
这种方法通常需要事先知道蛋白质和配体的晶体结构,然后通过计算它们的相互作用能量来推断它们的结合方式。
虽然基于结构的对接方法可以提供较为准确的结合方式和结合能量,但是它通常需要耗费大量的计算资源,且对蛋白质和配体的结构要求较高。
2. 结构基于方法除了分子对接方法外,还有一些结构基于方法也可以用于预测蛋白质-适配体相互作用,包括构效关系、药效团、分子动力学模拟等。
构效关系分析是一种常用的结构基于方法,它通过比较一系列类似分子的结构和活性,从而揭示它们之间的结构-活性关系。
这种方法可以帮助我们理解蛋白质-适配体相互作用的机制,进而设计出具有更高亲和性的配体。
构效关系分析通常需要大量的实验数据来支撑结论,而且往往无法提供准确的结合方式和结合能量信息。
药效团是分子对接中常用的结构基于方法,它通过识别分子中的关键功能团团,从而预测其与蛋白质的结合方式和亲和性。
药效团方法可以帮助我们快速地筛选出具有潜在活性的配体,并且在一定程度上可以降低计算复杂度。
药效团方法通常只能提供有限的结合信息,且在预测具有较强构效关系的配体时表现不佳。
分子动力学模拟是一种基于分子动力学原理的结构基于方法,它通过模拟蛋白质和配体在原子水平上的运动过程,从而预测它们的结合方式和亲和性。
分子动力学 分子对接的联系与区别

分子动力学分子对接的联系与区别下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!分子动力学与分子对接的联系与区别分子动力学和分子对接是生物化学领域两个重要的研究方向,它们分别从不同的角度探索分子之间的相互作用和生物过程。
分子对接简明教程

分子对接(Molecular Docking)理论所谓分子对接就是两个或多个分子之间通过几何匹配和能量匹配相互识别找到最佳匹配模式的过程。
分子对接对酶学研究和药物设计中有重要的应用意义。
分子对接计算是在受体活性位点区域通过空间结构互补和能量最小化原则来搜寻配体与受体是否能产生相互作用以及它们之间的最佳结合模式。
分子对接的思想起源于Fisher E的”钥匙和锁模型”,主要强调的是空间形状的匹配。
但配体和受体的识别要比这个模型更加复杂。
首先,配体和受体在对接过程中会由于相互适应而产生构象的变化。
其次,分子对接还要求能量匹配,对接过程中结合自由能的变化决定了两个分子是否能够结合以及结合的强度。
1958年D.E.Koshland提出分子识别过程中的诱导契合概念,受体分子活性中心的结构原本并非与底物完全吻合,但其是柔软和可塑的。
当配体与受体相遇时,可诱导受体构象发生相应的变化,从而便于他们的结合进而引起相应的反应。
分子对接方法根据不同的简化程度分为三类:刚性对接、半柔性对接和柔性对接。
刚性对接指在对接过程中,受体和配体的构象不发生变化,适合研究比较大的体系如蛋白-蛋白之间以及蛋白-核酸之间,计算简单,主要考虑对象之间的契合程度。
半柔性对接常用于小分子和大分子的对接,在对接过程中,小分子的构象可以在一定范围内变化,但大分子是刚性的。
这样既可以在一定程度上考察柔性的影响,又能保持较高的计算效率。
在药物设计和虚拟筛选过程中一般采用半柔性的分子对接方法。
柔性对接方法一般用于精确研究分子之间的识别情况,由于允许对接体系的构象变化,可以提高对接准确性但耗时较长。
分子对接的目的是找到底物分子和受体分子最佳结合位置及其结合强度,最终可以获得配体和受体的结合构象,但这样的构象可以有很多,一般认为自由能最小的构象存在的概率最高。
搜寻最佳构象就要用到构象搜索方法,常用的有系统搜索法和非系统搜索法。
系统搜索法通过改变每个扭转角评估所有可能的结合构象,进而选取能量最低的。
分子对接方法在药物设计中的应用指南

分子对接方法在药物设计中的应用指南导语:药物设计是一项旨在发现和优化新药物的领域,它涉及到大量的实验和计算技术。
其中,分子对接是药物设计中的一种重要方法,通过预测药物分子与靶点分子之间的结合方式和亲和性,为药物的发现和优化提供指导。
本文将重点探讨分子对接方法在药物设计中的应用,并为读者提供一份简明的应用指南。
一、分子对接方法简介分子对接是一种计算生物学方法,主要用于预测小分子药物与靶点分子之间的结合模式和亲和力。
分子对接方法的基本原理是利用计算机将药物分子与靶点分子的结构信息输入到对接软件中,通过模拟分子间的相互作用力,得出药物分子与靶点分子的最优结合方式。
二、分子对接方法在药物设计中的应用1. 靶点鉴定:分子对接方法可以通过筛选和评估大量候选靶点,从中选择适合药物设计的最佳靶点。
通过对几种靶点进行对接计算,可以评估它们与药物分子的亲和力和结合模式,从而选择合适的靶点进行下一步的药物设计和优化。
2. 药物发现:结合分子对接方法和药物数据库,可以快速筛选候选化合物并进行评估。
借助分子对接技术,研究人员可以预测候选化合物与目标蛋白的结合模式,并计算它们的亲和力。
这能够大大加快药物发现的速度,并帮助研究人员更好地理解候选化合物与目标蛋白之间的相互作用。
3. 药物优化:分子对接方法可以在药物优化的过程中提供有价值的信息。
在已有候选化合物的基础上,通过对目标蛋白进行分子对接计算,可以预测改变候选化合物结构或取向后对结合模式和亲和力的影响。
这有助于指导化合物的结构修改和合成优化,以提高药物的亲和力和选择性。
三、分子对接方法的使用指南1. 数据准备:在使用分子对接方法之前,需要对候选化合物和目标蛋白进行结构准备。
这包括裁剪水分子、添加氢原子,并进行相应的氧化还原修饰等。
2. 对接计算:选择合适的对接软件进行计算。
常用的分子对接软件有Autodock、Glide等。
在进行对接计算时,需要设置适当的参数,如搜索范围、计算方案等。
分子对接的原理方法及应用

分子对接的原理方法及应用分子对接是一种计算药物设计方法,用于预测和评估分子(通常是药物)与蛋白质的相互作用。
通过了解分子之间的相互作用和结合模式,可以提供药物设计的指导,从而提高药物发现和优化的效率。
本文将详细介绍分子对接的原理、方法和应用。
一、分子对接的原理分子对接的原理是基于分子之间的相互作用力,主要涉及键的形成与破裂、范德华力、静电相互作用和氢键等。
1. 键的形成与破裂:分子对接中的关键问题是理解药物与蛋白质之间的键的形成与破裂过程。
药物分子通过与蛋白质上的活性位点相互作用,形成稳定的配位键。
而非特异性的键则可以通过“握手”模型来解释。
2. 范德华力:范德华力是分子之间最常见的相互作用力之一。
药物分子与蛋白质之间的范德华力通过识别和匹配亲和力较高的非极性残基来发挥作用。
范德华力的大小与分子间的距离、体积和极性有关。
3. 静电相互作用:药物分子与蛋白质之间的静电相互作用是通过负电荷和正电荷之间的吸引力来实现的。
静电相互作用通常发生在含有电荷的氨基酸残基(如赖氨酸、组氨酸等)和带电的药物分子之间。
4. 氢键:氢键是分子对接中最重要的相互作用力之一。
氢键经常发生在药物分子和蛋白质上的氧、氮、硫等原子之间。
氢键的长度、角度和方向决定了分子之间的相对位置和结合方式。
二、分子对接的方法1. 穷尽搜索方法:穷尽搜索方法是最早的分子对接方法之一,它通过将药物分子的构象空间进行穷尽搜索,以找到与蛋白质最佳匹配的位点。
这种方法计算复杂度较高,通常通过启发式算法来减少搜索空间。
2. 蒙特卡洛方法:蒙特卡洛方法采用统计物理学的思想,通过产生一系列的随机构象来模拟药物分子与蛋白质的相互作用。
根据相互作用的能量,可以预测分子之间的最佳配位方式。
3. 分子动力学模拟:分子动力学模拟是一种基于牛顿力学的计算方法,通过对分子的运动进行迭代计算,可以模拟分子的结构、构象和动力学性质。
分子动力学模拟可以用于模拟药物分子与蛋白质之间的相互作用过程。
分子对接步骤

分子对接是一种计算化学方法,其主要目的是预测两个小分子之间的相互作用,以预测它们的复合物结构。
通常,分子对接软件会将一个小分子(配体)和一个大分子(受体)的结构文件输入,然后预测这两个分子之间最可能的相互作用模式。
以下是一般的分子对接步骤:
1. 建立配体和受体的结构文件:包括配体和受体的3D结构,分子的原子类型、键的类型和键长等信息。
2. 准备受体:该步骤包括选定受体的活性位点、提取受体的网格和电荷信息等。
3. 调用/设置分子对接软件:调用适当的分子对接软件,并根据需要设置参数。
4. 进行分子对接:将预处理的配体和受体输入分子对接软件中,并进行分子对接计算,得到分子间的相互作用模型。
5. 分析结果:评估每个配体-受体复合体的得分,根据得分选择最优的复合物结构。
6. 结果可视化:可视化得到的配体-受体复合物结构,以便对复合物的结构和相互作用进行更深入的研究。
这些步骤中的细节和软件取决于具体的分子对接问题和所使用的软件。
分子对接简要介绍
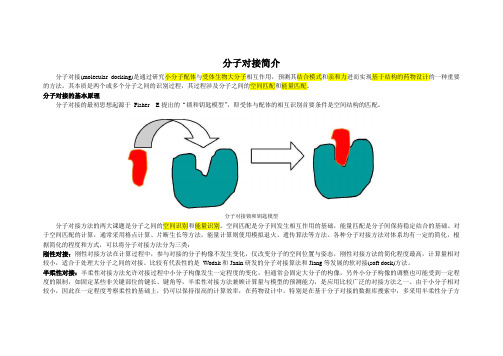
分子对接简介分子对接(molecular docking)是通过研究小分子配体与受体生物大分子相互作用,预测其结合模式和亲和力进而实现基于结构的药物设计的一种重要的方法。
其本质是两个或多个分子之间的识别过程,其过程涉及分子之间的空间匹配和能量匹配。
分子对接的基本原理分子对接的最初思想起源于Fisher E提出的“锁和钥匙模型”,即受体与配体的相互识别首要条件是空间结构的匹配。
分子对接锁和钥匙模型分子对接方法的两大课题是分子之间的空间识别和能量识别。
空间匹配是分子间发生相互作用的基础,能量匹配是分子间保持稳定结合的基础。
对于空间匹配的计算,通常采用格点计算、片断生长等方法,能量计算则使用模拟退火、遗传算法等方法。
各种分子对接方法对体系均有一定的简化,根据简化的程度和方式,可以将分子对接方法分为三类:刚性对接:刚性对接方法在计算过程中,参与对接的分子构像不发生变化,仅改变分子的空间位置与姿态,刚性对接方法的简化程度最高,计算量相对较小,适合于处理大分子之间的对接。
比较有代表性的是Wodak和Janin研发的分子对接算法和Jiang等发展的软对接(soft dock)方法。
半柔性对接:半柔性对接方法允许对接过程中小分子构像发生一定程度的变化,但通常会固定大分子的构像,另外小分子构像的调整也可能受到一定程度的限制,如固定某些非关键部位的键长、键角等,半柔性对接方法兼顾计算量与模型的预测能力,是应用比较广泛的对接方法之一。
由于小分子相对较小,因此在一定程度考察柔性的基础上,仍可以保持很高的计算效率,在药物设计中,特别是在基于分子对接的数据库搜索中,多采用半柔性分子方法。
其代表性软件是DOCK和AutoDock。
柔性对接:柔性对接方法在对接过程中允许研究体系的构像发生自由变化,由于变量随着体系的原子数呈几何级数增长,因此柔性对接方法的计算量非常大,消耗计算机时很多,适合精确考察分子间识别情况。
其中比较有代表性的方法有Accelrys 公司发展的基于分子力学和分子动力学的分子对接方法及Affinity 软件。
药物作用靶点选择的分子对接技术

药物作用靶点选择的分子对接技术药物作用靶点选择是药物研发的关键环节之一,对于减少药物研发的时间和成本、增加研发成功率具有重要意义。
分子对接技术是一种常用的药物作用靶点选择方法,通过计算机模拟分子之间的相互作用,得到药物与靶点之间的结合模式和亲和力。
本文将介绍分子对接技术的原理、常用方法和应用。
一、分子对接技术的原理分子对接技术基于分子间作用力的原理,主要包括力场计算、算法和评分函数等三个方面。
1.力场计算:分子在空间中的相互作用力可以通过力场计算来获得。
力场是一个数学模型,可以描述分子内部键长、键角、扭曲度等参数对分子的能量和构象的影响。
分子力场一般采用力场库分子力场、晶体分子力场等。
2.算法:分子对接算法用于预测和药物分子与靶点之间的最适合的结合模式。
常用的算法有蒙特卡洛模拟、遗传算法、模拟退火算法等。
3.评分函数:评分函数用于评估药物分子与靶点结合的亲和力。
评分函数一般通过考虑蛋白质、药物和水分子间的相互作用来计算。
合理选择评分函数能够准确预测和筛选出具有潜在活性的分子。
二、常用的分子对接方法目前常用的分子对接方法主要包括基于构象的对接和基于药物化合物的对接两种方法。
1.基于构象的对接:基于构象的对接方法通过药物分子和靶点的所有可能构象,找到最适合的结合构象。
这种方法适用于有已知结构的靶点。
2.基于药物化合物的对接:基于药物化合物的对接方法通过药物化合物库中的化合物,找到与靶点最适合的结合化合物。
这种方法适用于没有已知结构的靶点。
三、分子对接技术的应用分子对接技术在药物研发中具有广泛应用,主要包括以下几个方面:1.新药靶点发现:通过对模拟分子与靶点之间的结合模式和亲和力的预测,可以筛选出具有潜在活性的化合物,并作为潜在的药物候选靶点。
2.药物优化设计:通过对模拟分子与靶点结合的相互作用进行分析,可以指导药物分子结构的优化设计,提高药物的亲和力和药效。
3.靶点的机理研究:分子对接技术可以通过模拟药物与靶点的相互作用,揭示药物与靶点之间的结合机制和作用方式,为靶点的机理研究提供理论依据。
分子对接研究方法

分子对接研究方法分子对接呀,就像是给分子们安排一场超有趣的“相亲大会”呢。
分子对接主要是为了研究小分子和大分子之间的相互作用。
咱先说说小分子吧,它就像一个小小的精灵,而大分子呢,就像是一个有着很多小房间(活性位点)的大房子。
在这个研究方法里,首先得把小分子和大分子的结构搞清楚。
这就好比你要给两个人相亲,你得先知道他俩长啥样呀。
对于分子来说,就是通过各种技术手段,像X - 射线晶体衍射之类的,把它们的三维结构给确定出来。
然后呢,就开始找它们能结合的地方啦。
小分子就开始在大分子这个大房子里到处溜达,看哪个小房间最适合自己。
这个过程在技术上就是通过计算来评估小分子和大分子活性位点的匹配程度。
比如说,形状互补就很重要,如果小分子的形状刚好能严丝合缝地塞进大分子的活性位点那个小房间,那就有戏啦。
还有电荷的相互作用也不能忽视哦。
就像两个人相处,性格合不合很关键,分子之间电荷要是相互吸引,那结合起来就更容易啦。
再说说打分函数这个有趣的东西。
这就像是给小分子和大分子的“相亲”结果打分呢。
如果它们结合得很完美,得分就高;要是结合得很勉强,得分就低。
这个分数能帮助科学家们判断这个结合是不是真的靠谱。
分子对接在药物研发里可是超级有用的。
比如说,要研发一种新的药物来对抗疾病,就可以把可能有效的小分子和疾病相关的大分子(比如酶或者受体)进行对接研究。
如果对接结果显示它们能很好地结合,那这个小分子就很有可能成为一种有效的药物呢。
不过呢,分子对接也不是十全十美的。
有时候计算出来的结果和实际情况会有点小偏差。
但不管怎么说,它还是给科学家们在探索分子世界的相互作用方面提供了一个超级酷的工具,就像给他们开了一个特殊的“透视眼”,能看到分子之间那些微妙又神奇的关系。
分子对接的方法

分子对接的方法嘿,朋友们!今天咱来聊聊分子对接这个神奇的玩意儿!你说分子对接像不像一场奇妙的相亲会呀!一个个分子就像是等待缘分的单身男女,它们在特定的环境里相互试探、相互匹配。
就好比咱找对象,得看性格合不合、兴趣搭不搭,分子对接也是要找到最合适的那个“另一半”。
想象一下,在一个微观的世界里,各种分子在那里晃悠。
有的分子特别挑剔,不是它的“菜”根本不搭理;而有的分子就比较随和,和很多分子都能试着接触接触。
研究人员呢,就像是牵红线的月老,努力创造条件让它们更好地相遇、结合。
做分子对接可不容易哦!这可不是随便把两个分子往一块儿一放就行的事儿。
得考虑好多因素呢!比如说分子的形状、电荷分布、亲疏水性等等。
这就好像找对象要看外貌、性格、家庭背景啥的,一个都不能马虎。
要是不仔细研究,那可就像乱点鸳鸯谱,根本成不了事儿。
而且哦,这个过程还需要各种高科技手段来帮忙。
什么计算机模拟啦、专业软件啦,就像是给这场相亲会配备了最先进的相亲设备,能更精准地分析每个分子的特点和需求。
有时候,研究人员为了找到最合适的对接方式,那真是绞尽脑汁啊!就跟咱为了追到心仪的对象一样,得想尽各种办法去打动对方。
他们要不断尝试、调整参数,就像咱不断改变自己的策略去追求幸福。
分子对接的应用那可太广泛啦!在药物研发中,它能帮助找到最有效的药物分子和靶点的结合方式,就像是给病人找到最对症的良药,这多重要啊!在材料科学里,它也能发挥大作用,让材料的性能变得更出色。
咱再回过头来想想,这分子对接是不是特别神奇、特别有趣?它让我们能更深入地了解分子之间的关系,为科学研究和实际应用打开了一扇扇大门。
所以说啊,分子对接可真是个了不起的领域!它就像一把神奇的钥匙,能解开好多科学难题的锁。
让我们一起为分子对接点赞,为那些在这个领域努力钻研的科学家们加油!希望他们能通过分子对接取得更多惊人的成果,让我们的生活变得更加美好!。
分子对接指南

分子对接指南分子对接是指两个或多个分子(通常是蛋白质和核酸)之间通过某些相互作用力(如氢键、静电相互作用、范德华力等)结合形成复合物的过程。
在药物设计、生物物理学、生物化学等领域中,分子对接是一种重要的研究方法。
下面是分子对接的一些基本步骤:1. 准备分子模型:确定参与对接的分子,并构建其三维模型。
2. 选择对接算法:常用的对接算法包括刚性对接和柔性对接。
3. 生成构象:为目标分子生成大量的可能构象。
4. 计算相互作用能:计算目标分子与受体分子之间的相互作用能,以评估其结合能力。
5. 筛选最佳构象:根据相互作用能等因素筛选出最佳的对接构象。
6. 分析结果:对最佳构象进行分析,以了解其结合模式和作用机制。
在进行分子对接时,需要注意以下几点:1. 选择合适的对接算法和参数:根据具体情况选择合适的对接算法和参数,以获得准确的对接结果。
2. 考虑分子的柔性:分子通常具有一定的柔性,因此在对接时需要考虑分子的柔性。
3. 处理大分子体系:对于较大的分子体系,需要使用合适的算法和硬件设备来加速计算。
4. 分析对接结果的可靠性:对接结果需要经过仔细的分析和验证,以确保其可靠性。
分子对接是一项复杂的任务,需要综合运用多种技术和方法。
分子对接的结果可以用于多种用途,以下是一些常见的应用:1. 药物设计:分子对接可以帮助研究人员发现新的药物靶点,并设计出能够与靶点结合的候选药物分子。
2. 生物分子相互作用研究:分子对接可以用来研究生物分子之间的相互作用,例如蛋白质-蛋白质相互作用、蛋白质-DNA 相互作用等。
3. 药物筛选:通过分子对接,可以筛选出能够与特定靶点结合的化合物,从而为药物研发提供候选化合物。
4. 蛋白质结构预测:分子对接可以用来预测蛋白质的三维结构,特别是在没有晶体结构的情况下。
5. 分子机制研究:分子对接可以帮助研究人员了解分子之间的相互作用机制,从而深入理解生物过程和疾病发生的机制。
总之,分子对接是一种重要的计算方法,在药物设计、生物分子相互作用研究、药物筛选、蛋白质结构预测和分子机制研究等领域都有广泛的应用。
分子对接 配位

分子对接配位分子对接配位是一种在药物设计和化学反应研究中常用的方法。
在这种方法中,通过计算机模拟和实验验证,确定两种分子之间的相互作用以及它们如何结合在一起。
这种方法可以帮助科学家设计更有效的药物分子或者理解分子之间的相互作用机制。
在分子对接配位中,通常会涉及到蛋白质和小分子之间的相互作用。
蛋白质是生物体内重要的分子,具有各种生物学功能,包括催化化学反应、传递信号和结构支持等。
而小分子则是化学药物或其他生物活性分子,通过与蛋白质结合来实现治疗或其他作用。
分子对接配位的过程通常包括以下几个步骤:1. 数据准备:首先,需要准备好蛋白质和小分子的结构数据。
蛋白质结构可以通过X射线晶体学或核磁共振等方法确定,而小分子的结构则可以通过分子模拟或实验手段得到。
2. 对接计算:接下来,通过计算机模拟的方法,对蛋白质和小分子之间的相互作用进行预测。
这一步通常使用分子对接软件,根据蛋白质的结构和小分子的结构,预测它们之间的结合方式和亲和力。
3. 结果分析:分子对接计算会生成多个可能的结合构象,科学家需要对这些结果进行分析,找到最有可能的结合方式。
这可能涉及到分子间的氢键、疏水作用、范德华力等相互作用。
4. 实验验证:最后,通过实验验证分子对接计算的结果。
这可以包括分子间的结合亲和力实验、生物活性实验等,来验证分子对接的有效性。
分子对接配位在药物设计中扮演着重要的角色。
通过分子对接配位,科学家可以预测药物分子和靶标蛋白质之间的结合方式,优化药物的生物活性和药效,减少研发的时间和成本。
同时,分子对接配位也可以帮助科学家理解分子之间的相互作用机制,促进生物医药领域的研究和发展。
分子对接的原理方法和应用

分子对接的原理方法和应用1. 分子对接的概述分子对接是一种计算化学方法,旨在研究分子之间的相互作用和结合模式。
通过分子对接,可以预测小分子药物与靶点蛋白之间的相互作用,从而为药物设计和发现提供重要参考。
2. 分子对接的原理方法2.1 空间和矢量评分分子对接的基本原理是利用计算方法预测小分子药物与靶点蛋白的结合模式。
其中,空间评分方法主要通过计算小分子药物与蛋白的空间相互作用来评估结合模式的好坏;而矢量评分方法则通过计算小分子药物和靶点蛋白之间的相互作用能、矩阵元素等分子特征进行评估。
2.2 搜索算法为了找到最佳的分子对接结合模式,分子对接需要使用搜索算法进行寻优。
常见的搜索算法包括蒙特卡洛模拟、分子力学模拟、遗传算法等。
这些算法可以从不同的角度对结合模式进行搜索和优化,提高预测结果的准确性。
2.3 能量评估和结构优化分子对接中,通常需要进行能量评估和结构优化。
能量评估是通过计算小分子药物与靶点蛋白之间的相互作用能来评价结合模式的好坏;结构优化则是对分子对接得到的结合模式进行进一步调整,以提高预测的准确性。
3. 分子对接的应用3.1 药物发现与设计分子对接在药物发现与设计中发挥着重要作用。
通过分子对接,可以预测小分子药物与靶点蛋白的结合模式,从而为药物的设计和发现提供重要参考。
分子对接还可以用于筛选化合物库,快速筛选出具有潜在活性的化合物,加快药物研发的速度。
3.2 蛋白质工程与改造分子对接可以用于蛋白质工程与改造。
通过对已知蛋白质与小分子药物的分子对接模拟,可以预测蛋白质的结构与功能变化。
这对于理解蛋白质功能、改造蛋白质以及设计新型蛋白质具有重要意义。
3.3 食品和农药设计分子对接在食品和农药设计中也有广泛的应用。
通过分子对接,可以预测食品添加剂与食物成分之间的相互作用,为食品添加剂的选择和使用提供理论依据。
同时,分子对接还可以用于农药的设计与优化,提高农作物的抗病能力和产量。
4. 总结分子对接作为一种计算化学方法,在药物发现、蛋白质工程、食品和农药设计等领域都有重要应用。
分子对接方法的应用与发展

分子对接方法的应用与发展一、本文概述随着计算生物学和药物设计领域的迅速发展,分子对接作为一种重要的技术手段,已经成为药物研发、生物大分子相互作用研究等领域的重要工具。
分子对接方法的核心在于通过计算预测生物大分子(如蛋白质、核酸等)与小分子(如药物、配体等)之间的相互作用模式和结合亲和力,从而帮助研究者深入理解生物大分子的功能机制,指导药物设计和优化。
本文旨在全面综述分子对接方法的应用与发展,首先简要介绍分子对接的基本原理和常用方法,然后重点分析分子对接在药物设计、蛋白质功能研究、疾病机理探索等领域的应用案例,最后展望分子对接方法的未来发展趋势和挑战。
通过本文的阐述,希望能够为相关领域的研究者提供有益的参考和启示,推动分子对接技术的进一步发展和应用。
二、分子对接方法的基本原理分子对接(Molecular Docking)是一种基于计算机模拟的技术,其基本原理是通过模拟生物大分子(如蛋白质、DNA等)与小分子(如药物、配体等)之间的相互作用,预测和优化它们之间的结合模式和亲和力。
分子对接方法基于分子间相互作用的物理和化学原理,如氢键、离子键、疏水作用、范德华力等,利用计算机算法和力场模型,对分子间的相互作用进行模拟和计算。
分子对接方法的基本步骤包括:构建目标生物大分子和小分子的三维结构模型,这通常通过射线晶体学、核磁共振(NMR)等实验方法或同源建模、量子化学计算等方法获得。
对构建好的分子模型进行预处理,如能量最小化、电荷分配等,以确保分子处于能量最低的稳定状态。
然后,利用搜索算法在三维空间中寻找小分子与大分子的最佳结合位置,即对接过程。
在这个过程中,需要考虑分子间的相互作用能、空间位阻等因素,以评估对接构象的稳定性。
通过对接评分函数对得到的对接构象进行排序,选取得分最高的构象作为预测的结合模式。
分子对接方法的应用范围广泛,包括药物设计、蛋白质功能研究、生物传感器开发等领域。
随着计算机技术和算法的不断发展,分子对接方法的准确性和效率不断提高,为药物研发和生命科学研究提供了有力支持。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
8
3 分子对接的一般过程
找出空穴,定出表面 调整受体位点或药物的构象 计算对接时受体-药物相互作用能量 进行分子动力学模拟 复合物的全局最优结合构象
9
10
11
12
13
14
4 分子对接的分类
刚性对接:研究体系的构象不发生变化。 半柔性对接:研究体系尤其是配体的构象 允许在一定范围内变化。 柔性对接:研究体系的构象是可以自由变 化的。
15
3分子对接的基本方法
(一) 刚性的分子对接方法 这种方法是最初的分子对接的方法,在对接中,小 分子和蛋白质两种都保持刚性。
(1)基于最大团搜索的方法 (Clique-Search Based Approaches)
对接两个刚性分子可以理解为分子在空间的匹配 问题,这种匹配可以是一种形状上的互补或相互作用。 如氢键受体与氢键给体的互补。搜索在三维空间中有 效的条件下的最大匹配
21
(二)柔性对接的方法 (1)构象的系综方法
Flexibase用来储存小分子库中每个分子的一系列 不同构象,用距离几何和能量最小化的方法产生构象, 每个分子根据rmsd的差异选择25个系列构象。每个 构象采用FLOG刚性对接的方法进行对接。
22
(2)片段的方法
片断的方法是处理小分子柔性的最通用的方法,配 体分割成一些小的片断,这些片断可以认为是刚性构象 或一个小的构象系综。一般,有两种方法来处理: 第一种方法是把一个片段放入受体的作用位点,然后加 上余下的片段,这种方法称为连续构建 “incremental construction”. 第二种方法把所有或一部分片段独立地放入受体的作用 位点,再重新连接至到构成一个完整的配体分子,这种 策略称为“放置&加” “place & join”
计算机辅助药物设计的方法学
基于配体的药物设计方法 基于受体的药物设计方法 基于结构的药物设计
1
基于受体的药物设计方法
通过受体的特征以及受体和药物分子之间 的相互作用方式来进行药物设计的方法。 “有的放矢” 主要方法
分子对接法 从头设计
2
分子对接
1.概念 2.原理 3.一般过程 4.分类 5.代表性软件 6.DOCK软件 7.AUTODOCK软件
20
(3)基于pose clustering的方法 这种方法与几何哈希的方法相类似,也是一种 基于模式识别的方法。 在LUDI模型中,如图所示,对每一个作用基团,定 义作用中心和作用表面。受体的作用表面近似地用离 散的点表示,和对应的配体的中心目标点相匹配。
三个氢键受体的作用表面
Pose clustering 算法中的作用点
Oh boy! What a perfect match
7
3分子对接的基本原理
药物与受体的结合强度取决于结合的自由能变化 G结合 = H结合 - TS结合 = -RT ln Ki
大部分的分子对接法忽略了全部的熵效应,而在焓 效应也只考虑配体与受体的相互作用能,即:
Einteraction= Evdw + Eelectrostatic + Eh-bond
16
受体的活性位点
配体
有效匹配的距离图集
受体-配体的示意图,字母代表特征部分如氢键等, 相应的有效匹配的图集如右,三个环性顶点组织的三角形 为这个图集的一个最大团(clique)
17
Dock对接程序中刚性对接的算法就是基于这种思想
Dock利用球集来表示受体活性位点和配体的形状
18
一系列的球集填充在受体活性位点的表面,这些球 集代表能被配体占据的体积。配体可以用球集表示或者用 自己的原子表示,在Dock程序中,四个有效匹配的对应点 被考虑,先考虑配体中第一个球集与活性位点的球集的匹 配,第二个点则满足∆d ≤ ε,其中∆d为第二个匹配点中配 体和受体的球心与第一个点球心的距离,第三个点又必需 满足与前两个球心的距离限制,以上过程一直进行到找不 到更多匹配点为止。
19
(2)基于几何哈希技术“geometric hashing”的方 法 第一部分中,几何哈希表从被对接的一个配体或一 系列配体中构建 。哈希矩阵含有配体名字和能调整 配体在空间方向的参考框架。 第二部分即识别阶段,蛋白质的特征用来识别哈希 矩阵,每一次匹配表示蛋白质的特征与哈希矩阵中 已定义好方位的配体相匹配,具有大量匹配信息的 哈希矩阵代表着具有几个吻合特征的配体和方位
5
分子对接的最初思想起源于Fisher E提出的 “锁和钥匙模型”。即受体与配体的相互识别首 要条件是空间结构的匹配
配体
受体
复合物
受体-配体的锁和钥匙模型
6
这类方法首先要建立大量 化合物(例如几十至上百万个 化合物)的三维结构数据库, 然后将库中的分子逐一与靶标 分子进行“对接” (docking),通过不断优化 小分子化合物的位置(取向) 以及分子内部柔性键的二面角 (构象),寻找小分子化合物 与靶标大分子作用的最佳构象, 计算其相互作用及结合能。在 库中所有分子均完成了对接计 算之后,即可从中找出与靶标 分子结合的最佳分子(前50名 或前药物分子之间通过空间匹配和能量 匹配而相互识别形成分子复合物,并预测复 合物结构的操作过程。 整体上考虑配体与受体的结合效果,较好 地避免局部作用较好、整体结合欠佳的情况 。
4
2 分子对接的原理
理论基础: “锁和钥匙模型” “诱导契合模型” 重要原则: 互补性:决定识别过程的选择性 预组织性:决定识别过程的结合能力
23
第一个连续构建的算法是Kuntz发展的Dock程序, 首先,一个单独的锚碎片通过手工选择对接进受体的活 性结合位点,并且考虑了氢键的作用。其次这个锚的优 势位置主要包含有有大量匹配氢键对,高打分值,和低 相似性。接着,一种回溯的算法(backtracking algorithm)用来搜索整个配体在结合位点的非重叠放置 空间,在当前位置加上一个碎片后,优化的方法用来减 少立体的张力和改善氢键的几何构型。最后的位置通过 过滤,优化和基于力场的方法来打分评价。FlexX也是一 个基于连续构建算法的对接程序
