紫杉醇及多西紫杉醇的合成共20页
紫杉醇合成

紫杉醇合成
紫杉醇(Paclitaxel)是一种重要的抗肿瘤药物,常用于治疗乳腺癌、卵巢癌、非小细胞肺癌等多种恶性肿瘤。
以下是紫杉醇的合成过程:
1. 合成起始物:利用紫杉醇最主要的合成起始物为天然产物
10-脱乙酰二羟甲杉醇(10-DAB III)。
10-DAB III是一种通过纯天然合成提取的二萜化合物。
通过对其进行一系列的化学改性和化学反应来合成紫杉醇。
2. 发挥骨架的活性:通过对10-DAB III进行结构改造反应,
例如保护羰基氧化脱除反应(ozonolysis reaction)、酸催化等,将羟基保护基替换为更活性的取代基,形成活性骨架。
3. 反应活化:将活性骨架进行结构改造反应,如羟基取代、酸催化等反应,引入一些临时保护基,以保护紫杉醇分子的不同官能团。
4. 防护基处理:对于引入的临时保护基进行去保护反应(deprotection reaction),以恢复紫杉醇分子原有的官能团。
5. 结构改建:通过一系列化学反应,如环化反应、氧化反应、取代反应等,构建紫杉醇分子的特定官能团。
6. 叶酸酯法合成:最近研究还发现可以利用叶酸酯法,直接将叶酸与10-脱乙酰二羟甲杉醇反应,生成紫杉醇。
这种新的合
成方法简单、高效,并且不需要经过复杂的结构改造反应。
需要注意的是,紫杉醇的合成过程非常复杂,需要多步的化学反应和精确的反应控制,对于合成技术的要求很高。
因此,紫杉醇的生产往往需要专门的合成工艺和设备,在工业生产中产量较低,造成紫杉醇的价格较高。
紫杉醇的合成

紫杉醇的合成紫杉醇的合成一、紫杉醇简介紫杉醇(Paclitaxel),又称为紫杉碱(Taxol),是一种有效的抗癌药物,具有强烈的抗肿瘤活性,可以抑制肿瘤细胞的生长和分裂,是一种非常重要的化学治疗药物。
紫杉醇是一种非细胞膜透性的树脂,有很高的稳定性,广泛用于抗癌治疗、抗病毒以及抗菌药物等多种用途。
二、紫杉醇的合成原理紫杉醇是由多酚类烷酸衍生物(Taxus Baccata)中的紫杉醇类物质合成而来的,它是一种非细胞膜透性的树脂,可以通过稳定和耐受被吸收,具有很高的稳定性。
紫杉醇的合成一般是采用环化、氧化、酯化等多步反应进行,将各种原料进行反应后,用过滤、萃取、分离等技术对反应物进行精炼,最后得到紫杉醇最终产品。
三、紫杉醇的合成过程1. 紫杉酸法合成紫杉酸(taxa-olide)是紫杉醇的中间体,先将紫杉酸利用有机合成的方法合成出来,然后经氧化、酯化反应,可以得到紫杉醇,即Taxol。
2. 根木素法合成根木素(Taxusin)是紫杉醇的起始原料,将根木素经过环化、氧化、酯化等反应可以得到紫杉醇中间体紫杉酸,然后经氧化、酯化反应可以制备出紫杉醇,也可以节省原料成本。
3. 甲酰胺法合成甲酰胺(Acetamide)是紫杉醇的中间体,将甲酰胺经过环化、氧化、酯化等反应,可以得到紫杉醇,即Taxol。
四、紫杉醇的应用1. 抗癌治疗紫杉醇是一种强效的抗癌药物,可用于治疗乳腺癌、胃癌、肝癌、食管癌、肺癌等多种恶性肿瘤,其作用机制大概有几个方面,一是抑制癌细胞凋亡,使癌细胞不易死亡;二是抑制细胞分裂、增殖,使癌细胞不易生长繁殖。
2. 抗病毒紫杉醇也可以用于抗病毒,它可以抑制病毒的复制,阻断病毒蛋白的合成,从而达到抑制病毒的作用,对抗病毒性疾病有一定的效果。
3. 抗菌药物紫杉醇也可以用于抗菌药物,它可以抑制细菌的生长,并具有抗菌作用,在药物治疗中也具有重要的应用。
紫杉醇的合成

苏州大学研究生考试答卷封面考试科目: 有机合成考试得分院别: 材料与化学化工学部专业: 分析化学学生姓名: 饶海英学号: 20114209033授课教师:考试日期: 2012 年 1 月8 日天然抗癌药物紫杉醇的合成进展摘要:本文对多烯紫杉醇的合成的各种合成方法进行了综述。
关键词:多烯紫杉醇合成抗癌多烯紫杉醇(daxotere) 商品名为多西她赛(Docetaxel) , 化学名为[ 2aR-( 2aα, 4β, 4aβ, 6β,9α, ( aR3, βS3) , 11α, 12α, 12aα, 12bα) ] -β- [ [ (1, 1 2二甲基乙氧基)羰基]氨基] -α-羟基苯丙酸[ 12b-乙酰氧-12 -苯甲酰氧-2a, 3, 4, 4a, 5, 6, 9,10, 11, 12, 12a, 12b -十二氢-4, 6, 11-三羟基-4a, 8,13, 13 -四甲基-5-氧代-7, 11-亚甲基-1H-环癸五烯并-[ 3, 4 ]苯并[ 1, 2-b ]氧杂丁环-9-基]酯,就是法国罗纳普朗克·乐安公司开发的半合成紫杉醇的衍生物,它对晚期乳腺癌、非小细胞肺癌、卵巢癌、前列腺癌、胰腺癌、肝癌、头颈部癌、胃癌等均有效。
其作用机制就是通过与肿瘤细胞微管蛋白结合, 加强微管蛋白的聚合、抑制微管解聚,最终形成稳定的非功能性微管束, 从而抑制肿瘤细胞的有丝分裂与增殖[1-3] 。
商业化生产的紫杉醇类抗癌药物大多采用半合成方法,这就是现阶段最具经济性与可操作性的合成方法。
多烯紫杉醇的半合成方法就是利用从红豆杉属植物的针叶中提取的10-去乙酰基巴卡亭Ⅲ (10-DAB ) ,通过选择性保护部分羟基, 然后在10-DAB C13位的羟基上连接合成的手性侧链, 再去掉保护基团得到。
其中以多烯紫杉醇C13位侧链的合成以及该侧链与选择性保护的母核10-DAB进行酯化反应最为重要[4-5] 。
紫杉醇的构效关系已经被众多学者所研究与总结。
紫杉醇的全合成
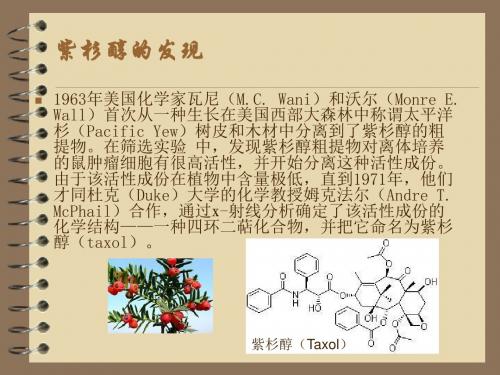
Mukaiyama的合成路线
Mukaiyama的合成路线
Danishefsky的合成路线
Wender的合成路线
J. Am. Chem. Soc. 1997, 119, 2755-2756 J. Am. Chem. Soc. 1997, 119, 2757-2758
Wender的合成路线
Wender的合成路线
Wender的合成路线
Wender的合成路线
紫杉醇(Taxol)
紫杉醇抗癌作用与生产现状
紫杉醇对卵巢癌、乳腺癌的治疗获得成功,治愈率达33%,有效 率为75%。对肺癌、大肠癌、黑色素瘤、头颈部癌、淋巴瘤、脑 瘤也都有一定疗效。是继阿霉素、顺铂以后,十五年来被认为是 对多种癌症疗效好、副作用小的新型抗癌药物。 紫杉醇主要是从红豆杉的根、皮、茎、叶中来提取。它的自然资 源数量有限,且其中有效成分的含量非常低。治疗一个病人需要6 棵百年树龄的红豆杉。 现在紫杉醇以及它的抗癌同源衍生物可以通过其前体进行化学半 合成制得。这些前体包括10-脱酰基巴卡丁 III、巴卡丁 III,10-脱 酰基紫杉醇,10-脱酰基三尖杉宁碱,7-戊醛基-10-脱酰基紫杉醇 等。 世界上年产紫杉醇仅250kg左右,市场供求失衡,价格十分昂贵, 每千克高达20多万美元
Kuwajima的合成路线
J. Am. Chem. Soc. 1998, 120, 12980
Kuwajima的合成路线
Mukaiyama的合成路线
Chem. Eu. J., 1999, 5, 121
Mukaiyama的合成路线
Mukaiyama的合成路线
Mukaiyama的合成路线
Mukaiyama的合成路线
书上紫杉醇合成方法

紫杉醇的化学合成途径1994年,美国佛罗里达州立大学R. Holton教授的研究组采用线性途径,实现了紫杉醇的全合成。
但是.紫杉醇的全合成步骤太多,总收率极低,因此没有进行大规模工业生产的意义。
1991年,Gibson等申请了用组织细胞培养方法生产紫杉醇及英类似物的美国专利。
中国华中理工大学王君健教授领导的研究组于1993年获得了细胞培养的紫杉醇,含量达0. 07% , 超过了同期国际上报道的0.032%的水平半合成的紫杉醇类似物紫杉醇的构效关系已经被众多学者所研究和总结。
具有游离疑基的C13位侧链,C2和C4 位的酯基,C4、C5位四元含氧环及紫杉烷的刚性环结构对抗癌活性都起着很重要的作用。
1989年佛罗里达州立大学的Robert A. Holton发现了一种半合成的方法,即由PhHadiraxel (l axol)Docetaxel Iv-L)caccrylb4ccatin III欧洲紫杉仃axus Baccata, European Yew)的树叶中提取的10-脱乙酰基浆果赤霉素111(10-Deacety I baccat i n 111)作为起始原料通过4步反应得到紫杉醇.欧洲紫杉树叶中的10-脱乙酰基浆果赤尊素III的含■可以达到0.1%o这一方法利用可再生的树叶,从而避免了砍伐紫杉得到树皮来提取的方法•在一定程度上解决了紫杉醇来源地匮乏。
1. n-BuLi, Et 2O, -78^C, 10 min2. benzoyl chloride, -78^C. 1h 95%Holton 的半合成路线(改进版)如下,10-脱乙酰基浆果赤霉素 I 11 (10-DeacetyIbaccat in 111)用三乙基氯硅烷先保护位阻相对较小的7-位的 二级醇,再把1 (Hi 的二级醇乙酰化得到仁1和环内酰胺2反应后在稀盐酸中 —步脱除TES(triethyIsi lyl)和EE(ethoxyethyI)的保护基直接得到紫杉醇。
紫杉醇有机全合成.

• 1994年,中国医学科学院药 物研究所有关专家会同中国 科学院的专家,在一次保护 野生红豆杉资源专题会议上 向林业部建议我国亦应颁布 保护这种野生资源的法令。 1995年野生红豆杉被列为国 家一级保护植物,相当于 “植物中的大熊猫”,严禁 砍伐。
紫杉醇来源的最新设想
• 目前生产紫杉醇的原料主要是红豆杉树皮, 而红豆杉是世界濒危的珍稀保护物种,所以 要在地球上得到紫杉醇非常难。由于太空环 境如微重力、高真空等条件与地面环境有天 壤之别,可以将紫杉醇菌带到宇宙飞船中, 实验证明,在太空特殊环境的“洗礼”中, 紫杉醇产生菌不但能够存活,而且它的繁殖 速度可以比地面高出许多倍,这就有望彻底 解决紫杉醇来源稀有的难题。
二、Nicolaou全合成路线(1994)
美国加利福尼亚大学圣迭戈分校Kyfiacos Costa Nicolaou教授领导的研究小组1994年1O月报了一 条紫杉醇全合成的路线-1 "J。Nicolaou法采非常简 明的会聚式合成战略,先分别得到含六元的A环化 合物和c环化合物,然后通过反应将A环与C环连接 起来并形成在其中间的含有8元环的B环,这样就 得到了含有ABC环的化合物,最后完成D环的构建 并连接上侧链。
将天然产物蒎烯(pinene)的氧化物verhenon(化合物 27)为起始原料,化合物27含有A环结构且可提供紫杉 醇母核骨架中20个碳中的1O个碳原子。经过若干步反 应将27转化为化合物31,再将化合物31转化为化合物 32,完成了AB环的构建。然后通过在C.3位上设计的 反应以及氧化反应得到化合物34、35,进一步通过醇 醛缩合得到化合物36、37,这样就完成了c环的构建。 再通过C.5位溴代、c4和C-20臭氧化完成了含氧D环 的构建(化合物38),最后得到了Baccatin III(2), 再完成C.10乙酰化及与侧链的加成反应等,最终完 成了紫杉醇的全合成(图7)
紫杉醇半合成路线

紫杉醇半合成路线
紫杉醇半合成路线通常包括以下步骤:
1.选择性脱去13-乙酰基-9-二氢巴卡丁Ⅲ的C-13乙酰基,得到化合物IM1。
2.用保护基保护化合物IM1的C-7羟基,得到化合物IM2。
3.将化合物IM2分别与化合物S1、S2进行缩合反应,
得到化合物IM3和IM5。
4.用氧化剂将化合物IM3、IM5的C-9羟基氧化,分别
得到化合物IM4和IM6。
5.脱去化合物IM4的C-7保护基团和R3保护基,得到
紫杉醇。
6.脱去化合物IM6的C-7保护基、R3保护基和乙酰基,得到多西紫杉醇。
以上步骤完成后,就可以得到紫杉醇。
紫杉醇是一种具有抗癌活性的天然产物,广泛用于治疗乳腺癌、肺癌、卵巢癌等多种癌症。
半合成紫杉醇的方法具有产品得率高、成本低、容易实现等优点,为解决紫杉醇的自然来源有限的问题提供了有效途径。
请注意,紫杉醇及其合成方法属于专业领域,以上内容仅供参考。
如需更多信息,建议咨询药学专家或查阅相关文献资料。
紫杉醇的人工合成方法

紫杉醇的人工合成方法:1 植物组织培养植物组织培养利用植物细胞全能性,可利用红豆杉植株嫩茎、针叶、树皮、形成层、假种皮、胚等作为外植体进行培养,从而形成大量的提取原料。
目前国内外有很多报道,取得了显著成果。
2 微生物生产Stierle等从短叶红豆杉韧皮部分离到一种寄生真菌(Taxomyces andreanae)可以在特定的培养基中产生紫杉醇及其相关经合物,但由于目前产量极低,还未能在生产中得到应用。
通过改变培养条件和应用重组DNA技术,可望提高紫杉醇的产量。
由于根是除树皮外紫杉醇含量较高的器官,人们利用发根农杆菌(Agrobacterium rhizogenes)侵染红豆杉植物外植体诱导生根,通过此培养系统进行紫杉醇生产的尝试,因为这一培养系统无需外援激素、发根生产迅速、遗传性状稳定而受到重视。
积极寻找能合成紫杉醇或其类似的微生物,从微生物的合成途径中定位关键酶和克隆相关基因,将比对植物的研究有更大的意义。
3 使用生物工程法来合成利用生物工程的方法大规模生产紫杉醇是使用生物工程手段,培育、筛选出可大量产生紫杉醇的菌株,通过对它们不断地扩充培养,实现在培养基里“无限制地”生产紫杉醇,而无须再去砍伐自然界已所剩无几的红豆杉树。
实例目前已从一棵百年红豆杉的树皮中分离、筛选出一株紫杉醇产生量十分可观的菌种,命名为HQD33,然后利用化学、物理等多种方法多次诱变、优化其基因结构,再利用生物工程的手段进行处理,最终培育构建出在每升培养液中可产出448.52微克紫杉醇的高产菌株。
4 人工半合成为了保护紫杉树珍贵的资源,避免大量采集紫杉树树皮造成资源破坏,应将目标瞄向了利用可再生资源进行紫杉醇的生产。
百时美施贵宝公司在充分保证泰素产品质量的前提下,1994年,他们成功地利用紫杉树的细枝、叶等可再生材料,提取初级原料,再人工半合成生产紫杉醇。
其半合成生产方法获得了美国FDA 的批准。
从此,太平洋紫杉树不再被破坏性采集,泰素的持续生产供应也得到了保障。
紫杉醇全合成

紫杉醇全合成紫杉醇是一种用于治疗肿瘤的药物,其原料来自于太平洋紫杉树。
但是由于太平洋紫杉树生长缓慢,净化成本高,所以大规模生产紫杉醇是一项巨大的难题。
为此,科学家们开始探索紫杉醇的全合成方法,即通过化学合成方式生产紫杉醇。
紫杉醇的全合成分为5个步骤:第一步:合成环氧局部结构在这个步骤中,将苯乙烯和氢氧化钠加入二氯甲烷中,制备出一个含有羟基的物质。
接着,通过邻二甲基苯基酚的合成,将羟基改为酚环,得到紫杉醇所必需的环氧局部结构。
第二步:引入侧链在这个步骤中,需要利用脂肪酸的结构来构建紫杉醇的侧链。
将乙烯基叔丁基基乙烯酸叔丁酯与一系列的化学品反应,可以制备出紫杉醇侧链的前体,即乙撑二酸酐。
第三步:连接环氧和侧链在这个步骤中,需要将侧链与环氧局部结构连接起来。
将环氧与乙撑二酸酐进行反应,得到含有侧链和环氧的物质。
第四步:制备紫杉醇的骨架在这个步骤中,需要将紫杉醇骨架的各个部分连接起来。
将含有侧链和环氧的物质与一系列的化学品反应,最终得到紫杉醇骨架,这个骨架就是紫杉醇的主要结构。
第五步:去保护基在这个步骤中,需要将合成过程中保护羟基的化学品去掉,使得紫杉醇的羟基暴露出来。
通过一系列化学反应,去掉羟基保护基,得到最终成品——紫杉醇。
总的来说,紫杉醇的全合成方法需要借助高级有机合成技术,包括羟基的保护和去保护、各种侧链的引入等。
虽然整个合成过程比较复杂,并且需要很多的前体物质,但相比于从太平洋紫杉树中提取的成本,这种化学合成方法仍然具有很大的优势,可以为大规模生产紫杉醇提供技术支持。
紫杉醇的半合成路线图解

药物合成路线图解 文章编号:100128255(2000)042193203紫杉醇的半合成路线图解Graph ica l Se m isyn thetic Routes of Taxol沈 钢, 尤启冬3(中国药科大学药化教研室,江苏南京210009)SH EN Gang , YOU Q i 2Dong3(D ep t .of M ed icinal Che m istry ,Ch ina P har m aceu tical U niversity ,N anj ing 210009) 中图分类号:O 629.6+1;R 979.1+9 文献标识码:B 收稿日期:1998206205;修回日期:1999209223作者简介:沈 钢(1975),男,硕士研究生。
专业方向:抗肿瘤药物研究。
T el :025233059963445E 2m ail :g -shen @sohu .com 紫杉醇(1,p aclitax el ,商品名:T axo l )是从红豆杉科红豆杉属植物——太平洋浆果紫杉(T ax us brev if olic )中分离得到的一个具有独特结构的二萜类成分,是目前癌症化疗中最具潜力的药物之一[1],美国FDA 于1992年批准上市,用于治疗卵巢上皮癌,也可用于转移性乳腺癌、小细胞肺癌及头颈部癌的治疗。
由于浆果紫杉树资源很少且1含量不高,远不能满足实际需要,从紫杉树获取也会导致该珍稀树种死亡。
因此,半合成1显得尤为重要。
1的半合成方法文献报道很多,一般都以其前体102脱乙酰浆果赤霉素 (16)为原料,延长边链而成。
16可由来源丰富的欧洲浆果紫杉(T ax usbacca ta )的针叶和树皮中分离而得[2]。
本文对1的半合成作一简要评述和图解,归纳如下:(1)手性原料2和3酰化得4,经加成,环化,水解得8,再与重要中间体17脱水缩合得9,再经盐酸水解得目标物1[3]。
(2)16经硅醚化,乙酰化制得17,再与18在相应碱性条件下缩合生成19,盐酸水解得1[2]。
紫杉醇的全合成路线

紫杉醇的全合成路线2008 九月 12by infinteDanishefsky Taxol total synthesis From Wikipedia, the free encyclopediaThe Danishefsky Taxol total synthesis in organic chemistry is an important third Taxol synthesis published by the group of Samuel Danishefsky in 1996[1]two years after the first two efforts described in the Holton Taxol total synthesis and the Nicolaou Taxol total synthesis. Combined they provide a good insight in the application of organic chemistry in total synthesis.Danishefsky's route to Taxol has many similarities with that of Nicolaou. Both are examples of convergent synthesis with a coupling of the A and the C ring from two precursors. The main characteristic of the Danishefsky variant is the completion of the oxetane D ring onto the cyclohexanol C ring prior to the construction of the 8-membered B ring. The most prominent starting material is the Wieland-Miescher ketone. This compound is commercially available as a single enantiomer and the single chiral group present in this molecule is able to drive the entire sequence of organic reactions to a single optically active Taxol endproduct. The final step, the tail addition is identical to that of Nicolaou and is based on Ojima chemistry.[2]In terms of raw material shopping, this taxol molecule consists of the aforementioned Wieland-Miescher ketone, 2-methyl-3-pentanone, lithium aluminium hydride, osmium tetroxide, phenyllithium, pyridiniumchlorochromate, the Corey-Chaykovsky reagent and acryloyl chloride. Key chemical transformations are the Johnson-Corey-Chaykovsky reaction and the Heck reaction.Contents∙ 1 Synthesis D ring∙ 2 Synthesis C ring∙ 3 Synthesis A ring∙ 4 Synthesis B ring∙ 5 Tail addition∙ 6 See also∙7 References[edit] Synthesis D ring第一张图显示D环的合成由Wieland-Miescher 酮开始。
天然抗癌药物紫杉醇的全合成

天然抗癌药物紫杉醇的全合成
李力更;吴明;史清文
【期刊名称】《天然产物研究与开发》
【年(卷),期】2008(20)6
【摘要】紫杉醇为著名的抗肿瘤天然产物,来源有限,化学合成是制备紫杉醇的可能途径之一.本文综述了目前已公开报道的6条全合成紫杉醇的路线.
【总页数】5页(P1104-1107,1113)
【作者】李力更;吴明;史清文
【作者单位】河北医科大学药学院天然药物化学教研室,石家庄,050017;河北医科大学药学院天然药物化学教研室,石家庄,050017;河北医科大学药学院天然药物化学教研室,石家庄,050017
【正文语种】中文
【中图分类】R914;R284.3;Q946.91
【相关文献】
1.应用现代发酵技术生产植物源珍稀药物的产业化前景——以天然抗癌药物紫杉醇为例 [J], 周佳;程新;李昆太
2.紫杉醇:具有里程碑意义的天然抗癌药物 [J], 刘先芳;梁敬钰;孙建博
3.天然抗癌药物紫杉醇制剂的探究 [J], 张姝梅
4.抗癌药物紫杉醇的全合成--Holton合成紫杉醇路线的剖析 [J], 陈巧鸿;王锋鹏
5.天然抗癌药物紫杉醇的研究进展 [J], 吴秀兰;贾艳;朱波;周杰
因版权原因,仅展示原文概要,查看原文内容请购买。
紫杉醇生物体内合成过程

紫杉醇生物体内合成过程
紫杉醇是一种天然产物,最初是从紫杉树(Taxus brevifolia)中提取的。
紫杉醇的生物体内合成过程涉及植物细胞中的多个生物
化学途径和酶的作用。
以下是紫杉醇在植物体内合成的一般过程:
1. 起始物质,紫杉醇的生物合成起始物质是丙酮和葡萄糖。
这
些起始物质通过植物体内的代谢途径被转化为更复杂的中间体。
2. 萘乙酰辅酶A的合成,在生物体内,丙酮和葡萄糖首先被转
化为萘乙酰辅酶A,这是紫杉醇合成途径的第一步。
3. 萘前体的合成,萘乙酰辅酶A接下来被转化为一系列的中间体,最终形成萘类化合物。
4. 萘类化合物的重排和环化,这些萘类化合物经过一系列酶催
化的反应,发生重排和环化反应,形成紫杉醇的前体物质。
5. 紫杉醇的合成,紫杉醇的前体物质最终被转化为紫杉醇,这
是通过多个酶催化的复杂反应完成的。
需要指出的是,紫杉醇的生物合成过程是一个复杂的生物化学过程,涉及多个酶的作用和多个中间产物的转化。
这个过程在植物细胞内进行,受到细胞内环境和调控因素的影响。
此外,紫杉醇的生物合成过程也是植物生物技术研究的热点之一,对其生物合成途径的研究有助于开发紫杉醇的生物合成技术,以满足医药和工业上对紫杉醇的需求。
多西紫杉醇与紫杉醇辅料

吐温80是一个亲水性的表面活性剂,具有很强的破裂细胞膜的作用而引起刺激性,溶血性和组胺释放(致敏性)。
吐温80作为一个聚合物本身纯度波动极在,高纯度的吐温80是无色透明的,而大多数吐温产品则是微黄到棕色,含有大量杂质或降解产品。
吐温80中亲脂成份包括不饱和脂肪酸,这些不饱和脂肪酸十分容易氧化降解而产生更多的有毒成份,由此而产生的毒副反应将会超过产品本身带来的益处。
医学界证实,吐温80用于注射剂,会引起过敏反应,包括休克,呼吸困难,低血压,血管性水肿,风疹等过敏样反应症状。
这些不良反应在人的临床实验可以十分严重,有死亡报道。
因此,使用吐温80是有严格限制条件的,它是一种有潜在不安全性的辅料,使用不当会对人的健康造成很大影响。
急性超敏反应是 CrEL引起的最广泛且严重的不良反应。
其表现主要有全身性过敏.皮肤、消化道及呼吸道超敏反应。
此反应出现的概率超过 4O%。
注射用 CrEL引起的过敏反应现已证实属于由补体激活所引起的急性超敏反应 (CARPA)。
CARPA与由特异性免疫球蛋白(IgE)介导的 I型过敏反应的症状相似。
但又具有一些独有的特点。
CARPA不需要预致敏.初次接触抗原即可发生酶促级联反应。
当再次接触抗原时,症状变轻。
即使不进行任何治疗其症状也可随时间自发慢慢缓解直至消失。
CrEL介导的 CARPA的发生是无法预知的,但它主要发生于前三次输液治疗中,症状通常在 10min内迅速出现。
目前,临床上应对措施主要分为两方面:第一.输液前药物预防。
对于紫杉醇注射剂,常用的药物组合是地塞米松、苯海拉明及组胺 H 受体拮抗剂(西米替丁、法莫替丁、雷尼替丁等)。
通过输液前服用这种皮质激素与组胺拮抗剂的药物组合,能够有效地降低临床上 CARPA发生的几率至 10%以下。
第二,输液监控及标准化救护。
在输液开始后,一套标准化的监控及救护措施对于病人具有十分重要的意义。
对于每位病人,应配备专门的护理人员。
详细记录整个救护处置过程,密切注意病人的身体状况。
抗癌药物紫杉醇的制备、抗癌机理和应用前景

抗癌药物紫杉醇的制备、抗癌机理和应用前景摘要紫杉醇具有显著的抗癌活性和独特的作用机理,现主要用于治疗晚期乳腺癌和卵巢癌等。
紫杉醇分子结构复杂,具有特殊的三环[6+8+6]碳架和桥头双键以及众多的含氧取代基,其全合成引起国内外许多有机化学家的兴趣。
本文简述紫杉醇的制备、抗癌机理和不良反应。
关键词紫杉醇制备抗癌机理不良反应紫杉醇(Taxol)是从短叶红豆杉树皮中分离得到的一种四环二萜化合物。
1992年12月29日美国FDA正式批准紫杉醇作为治疗晚期卵巢癌的新抗癌药物。
由于该药疗效确切、副作用小,在美国上市后销售情况一直很好,并保持着20%以上的年销售增长率。
2000年该药的销售额已超过10亿美元。
紫杉醇被当今世界上公认为广谱、活性最强的抗癌药物,尤其是对子宫癌、卵巢癌、乳腺癌具有特殊的疗效,它的问世被誉为20世纪90年代国际上抗癌药三大成就之一[1]。
美国FDA已原则上同意其他国家及厂家生产紫杉醇制剂并可以作为通用名药上市,这就打破了美国施贵宝公司对该药的垄断生产。
这一决定意味着紫杉醇制剂价格将大幅下降,从而有利于广大肿瘤患者服用。
然而由于这种天然化合物资源极其有限,严重的限制了其研究和应用的进度。
同时尖锐的供需矛盾也在医学、化学和植物组织培养领域的科学家中引起了一场非同寻常的广泛研究,以增加这种化合物的来源和寻找高效、低毒、来源丰富的紫杉醇类似物。
经过40多年努力,已经取得了可喜的进展。
1紫杉醇的制备1.1天然红豆杉植物提取[2,3]紫杉醇的直接来源是从天然植物红豆杉树皮、树叶中提取。
但并不是所有品种的红豆杉树均含有紫杉醇,而且不同种类的红豆杉紫杉醇含量的多少差别非常明显。
红豆杉属植物共11种,我国有4种及1种变种,它们分别是云南红豆杉、西藏红豆杉(又名喜马拉雅红豆杉)、中国红豆杉、东北红豆杉、南方红豆杉(又名美丽红豆杉)。
紫杉醇在不同植物来源以及植物体不同部位的含量与提取分离有着直接关系。
Vidensek对东北红豆杉幼苗以及成树的不同部位中的紫杉醇含量作了分析,结果表明,成树紫杉醇的含量高低依次为:树皮>树叶>树根>树干>种子>心材。
紫杉醇或多西紫杉醇的多肽偶合物[发明专利]
![紫杉醇或多西紫杉醇的多肽偶合物[发明专利]](https://img.taocdn.com/s3/m/b2e3f4975acfa1c7ab00cc93.png)
专利名称:紫杉醇或多西紫杉醇的多肽偶合物专利类型:发明专利
发明人:王朴,傅雪琦
申请号:CN201310045580.1
申请日:20081010
公开号:CN103254279A
公开日:
20130821
专利内容由知识产权出版社提供
摘要:本发明公开了系列紫杉醇或多西紫杉醇的多肽偶合物,所述紫杉醇或多西紫杉醇在2’位羟基通过不同连接序列与多肽的氨基相连。
本发明还公开了所述偶合物的制备方法及在制备药物方面的应用。
本发明的偶合物具备优异抗癌活性与癌细胞选择性,以及具有良好水溶性。
申请人:江苏天一时制药有限公司
地址:225300 江苏省泰州市中国医药城
国籍:CN
代理机构:深圳鼎合诚知识产权代理有限公司
代理人:罗瑶
更多信息请下载全文后查看。
