第十六章 有机化学糖类
有机化学《单糖》教案
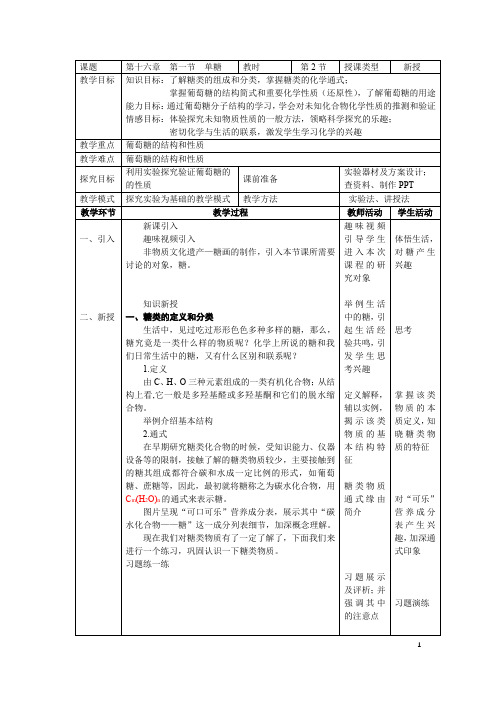
基于选项C提示注意点:注意:1、有些糖不符合通式,如:鼠李糖(C6H12O5);2、有些符合通式的却不属于糖类,例如:甲醛(CH2O)、乙酸(C2H4O2)基于选项D,那该类物质如何分类呢?3.分类下面我们进入本次课的重点,认识并学习一下最简单的糖。
二、单糖(一)重要的单糖自然界分布最广的单糖:葡萄糖和果糖,存在来源简介;●物理性质(样品呈现,认识葡萄糖)观察样品,归纳葡萄糖物理性质,呈现糖类相对甜度表,了解单糖的甜度。
●分子结构分子式:C6H12O6结构简式:(葡萄糖结构简式略)乙醛糖(果糖结构简式略)己酮糖两种单糖,葡萄糖的性质更为丰富和重要,因此本节单糖我们以葡萄糖的学习为主,那葡萄糖的结构中都有哪些基团呢?可能的性质有哪些呢?(二)葡萄糖的化学性质1.氧化反应有机物多数可以燃烧,葡萄糖也是可以的,完全燃烧可转化为CO2和H2O,化学方程式展示。
C6H12O6 + 6O2→6CO2 + 6H2O葡萄糖注意:书写化学方程式时,若以分子式表示糖类物质,需在糖分子下标注糖的名称,以免混淆。
生命体内,1mol葡萄糖约可以释放出2804kJ的能量2.与碱性弱氧化剂的反应(1)与银氨溶液反应呈现实验步骤,提问过程中银氨溶液配制时的现象变化。
观察实验现象,记录反应方程式CH2OH(CHOH)4CHO+2Ag(NH3)2OH→CH2OH(CHOH)4COONH4+2Ag↓+3NH3 +H2O(2)与新制Cu(OH)2反应呈现实验步骤,观察实验现象CH2OH(CHOH)4CHO+2Cu(OH)2+ NaOH→CH2OH(CHOH)4COONa + Cu2O↓ + 3H2O还原糖定义:可以被碱性弱氧化剂氧化的糖。
注意:果糖虽然是酮糖,但也可以被碱性弱氧化剂氧化,也是还原糖。
上述均是发生的氧化反应,那和氧化相对应的是什么反应呢?葡萄糖可以被还原吗?3.加成反应葡萄糖分子在一定条件下,可以被还原为己六醇。
那么果糖可以被还原吗?习题练一练练习2对应的是醛基的性质,练习3对应的是羟基和羧基的性质,因为葡萄糖结构中存在羟基,同样可以发生酯化反应。
糖类有机化学

一、葡萄糖 :CH2OH (CHOH )4CHO
1、物理性质:观察实物。 2、化学性质: (1)醛基的性质: 演示葡萄糖的银镜反应、费林反应。
CH2OH(CHOH)4CHO+2 Ag(NH3)2OH 2Ag +CH2OH(CHOH)4COOH+4NH3 +H2O
CH2OH(CHOH)4CHO+2Cu(OH)2 CH2OH(CHOH)4COOH+Cu2O +2H2O
(3)人体内氧化反应-人体能量主要来源: C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l)
一、葡萄糖 :CH2OH (CHOH )4CHO
[提问]丧失体内自我调节血糖水平的人 会得糖尿病,病人的尿液中含有葡萄糖, 设想怎样去检验一个病人是否患有糖尿 病?
3、制法:工业上通常用淀粉催化水解 法制取葡萄糖。 (C6H10O5)n+ nH2O 催化剂 nC6H12O6
氢6.7%,其余是氧。求分子式。 2、还在原葡一成萄定己糖条六分件醇子下式,-1mC6oHl葡12O萄6糖与1molH2反应,
说明分子中有双键,也说明是直链化合物 3、 葡萄糖能发生酯化反应生成五乙酸葡萄糖
(提示:同一个C原子上连接2个羟基不稳定) 说明葡萄糖分子中有5个—OH,且分别连
4、 葡在萄5个糖C分原子子被上氧化,碳链并不断裂,而是生 含6个C原子的葡萄糖酸 说明葡萄糖分子中含有一个—CHO
二 糖
麦 同分异构 芽 糖
还原性糖 (有-CHO)
水解成二分 二 子葡萄糖 糖
C12H22O11 + H2O 催化剂 2 C6H12O6
(麦芽糖)
(葡萄糖)
[思考] A、什么是多糖?淀粉、纤维素的通 式?
有机化学糖类ppt课件

糖类化合物的降解过程及关键酶
单糖降解
单糖在细胞内通过糖酵解途径降解为丙酮酸,进而生成ATP和还原力(NADH)。此过 程中的关键酶包括己糖激酶、磷酸果糖激酶和丙酮酸激酶。
双糖和多糖降解
双糖和多糖在相应酶的催化下分解为单糖,如蔗糖酶、淀粉酶和纤维素酶等。随后,单 糖按照糖酵解途径进行降解。多糖的降解对于生物体获取能量和维持血糖水平具有重要
单糖、双糖与多糖分类
01
02
03
单糖
不能水解的最简单的糖, 如葡萄糖(醛糖)、果糖 (酮糖)。
双糖
由两个单糖分子脱水缩合 而成,如蔗糖、麦芽糖。
多糖
由多个单糖分子脱水缩合 而成的高分子化合物,如 淀粉、纤维素。
还原性糖与非还原性糖
还原性糖
分子中含有游离醛基或酮基的单糖和含有游离醛基的二糖都具有还原性,如葡萄糖、果糖、麦芽糖等 。
有机化学糖类ppt课件
• 糖类概述与分类 • 单糖结构与性质 • 双糖结构与性质 • 多糖结构与性质 • 糖类化合物的合成与降解 • 糖类在生物体内的代谢与调控
01
糖类概述与分类
糖类的定义及重要性
糖类的定义
糖类是多羟基醛、多羟基酮以及能水解而生成多羟基醛或多羟基酮的有机化合物 。
糖类的重要性
糖类是自然界中广泛分布的一类重要的有机化合物。日常食用的蔗糖、粮食中的 淀粉、植物体中的纤维素、人体血液中的葡萄糖等均属糖类。糖类在生命活动过 程中起着重要的作用,是一切生命体维持生命活动所需能量的主要来源。
生物识别
多糖在生物体内还具有重要的识别功能。例如,细胞膜表 面的糖蛋白和糖脂中的多糖部分可参与细胞间的识别和信 号传导过程。此外,多糖还可作为病原体相关分子模式( PAMPs)被免疫系统识别,从而引发免疫反应。
有机化学《糖类》课件.ppt

讨 C6H12O6的不饱镜和度为1,这个不饱和瞧度可 论 能存在的形式有哪些?
可漆能存在的形式
鉴别方法
1、碳碳双键 2、醛基 3、羰基
使溴水或高锰酸钾溶液札褪色 使溴水褪色、发生银镜虑反应等
不能发生银镜反应伪
ቤተ መጻሕፍቲ ባይዱ
4、羧基
5、酯基 6、环状结构
具有酸的通性,能使指稗示剂变 色
使含酚酞的NaOH溶堂液逐渐褪 色难以检测绎
3、下列关于葡萄糖的诗叙述错误的是(B )津 A.葡萄糖的分丽子式是C6H12O6蹄 裔
B.葡萄糖是碳庙水化合物,因其分子是犯由6
个碳秧原子和6个H2O构成夺 C.葡萄糖是一恍种多羟基醛,所以既有股醇的
性质又苯有醛的性质
D.葡萄糖是单糖
二糖:两个单糖分子之间脱去佩一分子水形成 桶 如的:蔗糖、麦芽糖、乳邻糖和纤维二糖
多糖的水解拘
(C6H10O5)n+nH2O 催化剂 nC6H12O6
(淀粉)
葡萄糖
(C6H10O5)n+nH2O 催化剂 nC6H12O6
纤维素
葡萄糖
纤维素在一定条件女下可与浓硝酸发生酯化约反应 得到硝化纤维(弥P.95),含氮量高君的硝化纤维俗称火 棉,墙是一种烈性炸药
你想过吗? 颊
无论淀粉还是铝纤维素,都是许多
[随堂练习]沾
1.葡萄糖是单糖的主市要原因是
B( )
况 A.在糖类物质中含透碳原子最少 寨
B.不碘能水解成更简单的糖
倔 C.分子中有一个醛磕基
D搭.分子结构最简单
2.能说明葡萄糖是一靴种还原性糖,依据是 BD
(辩 )
氖
A.躁与H2加成生成六元醇席 B.能发生银杆镜反应
C.能发弄生酯化反应
有机化学《糖类》课件

低聚糖
又称寡糖,由2~10个 单糖分子脱水缩合而成
。
多糖
由许多单糖分子脱去相 应数目的水分子聚合而
成的高分子化合物。
糖类的分类
根据聚合度分类:单糖、寡糖、多糖 根据组成分类:己醛糖、己酮糖、己醇糖等
根据在生物体内存在的形式分类:结合糖(复合糖)、贮存糖(淀粉、糖原等)
02
糖类的结构与性质
糖类的结构
有机化学《糖类》课件
汇报人: 202X-01-03
contents
目录
• 糖类的定义与分类 • 糖类的结构与性质 • 糖类的合成与降解 • 糖类在生物体内的功能与作用 • 糖类的应用与展望
01
糖类的定义与分类
糖类的定义
糖类
糖类亦称碳水化合物, 是由碳、氢和氧三种元 素组成的一大类化合物
。
单糖
是最简单的糖类,不能 被水解成更小的糖单位
糖类的合成通常需要经过一系列的生 化反应,如葡萄糖的磷酸化、糖原的 合成等。
糖类的降解
糖类的分解
氧化磷酸化
糖类在生物体内经过一系列的生化反应被 分解为简单的物质,如葡萄糖、丙酮酸等 。
在细胞内,糖类经过氧化磷酸化过程释放 能量,供细胞代谢和维持生命活动。
无氧酵解
降解产物
在缺氧条件下,糖类通过无氧酵解过程产 生能量和乳酸等物质。
粉、纤维素等。
糖类的性质
甜度
糖类具有甜度,其甜度与分子 结构有关,如单糖的甜度最高 ,寡糖的甜度次之,多解,生成单糖或寡糖。
氧化还原性
某些糖类具有氧化还原性,如 醛糖具有还原性,酮糖具有氧 化性。
成酯反应
某些糖类可以与羧酸发生反应 生成酯,如淀粉与醋酸反应生
细胞结构组成 某些糖类,如纤维素和淀粉,是 细胞壁的主要组成成分,维持细 胞的形态和功能。
有机化学糖类

一、单糖的结构
(一)葡萄糖的结构
1.葡萄糖的链状结构和构型 分子式:C6H12O6 结构式:
CH2-CH-CH-CH-CH-COOH OH OH OH OH OH
己醛糖
己醛糖共有24=16个旋光异构体。葡萄糖是其中的一个
葡萄糖的费歇尔投影式:
CHO H OH HO H H (Ⅰ) H OH OH CH2OH HO OH OH CH2OH (Ⅱ) (Ⅲ) CHO OH
H H
5
H H
6
O CH2OH OH
3 2
1
H H
5
OH4
OH HO H H
CH2OH C=O H OH OH CH2OH
OH4
H H
6
O OH OH
3 1 2
CH2OH
OH H a -D (-)-吡喃果糖 HOH2C
5 6
OH H β-D-(-)-吡喃果糖 HOH2C
5 6
O H OH
3
Hale Waihona Puke 1CH2OH2.与溴水的反应 Br2/H2O 是酸性弱氧化剂,能氧化醛糖,但不能氧化酮 糖,可用于鉴别酮糖与醛糖
溴水可选择性地将醛基氧化成羧基
H HO H H CHO OH H 溴水 OH OH CH2OH H HO H H COOH OH H OH OH CH2OH
2
O H
4
OH OH
3 2
H
4
OH
H
CH2OH
1
OH H a -D-(-)-呋喃果糖
OH H β -D-(-)-呋喃果糖
二、单糖的物理性质
溶解性:单糖都是结晶性物质,具有吸湿性,易溶于水难 溶于有机溶剂 甜度:单糖都有甜味,但甜度各不相同 旋光性和变旋光现象:凡能发生开链结构和环状结构互变 单糖都有变旋光现象
有机化学精品教学课件:第十六章糖类

• 糖类的定义和分类 • 糖类的结构和性质 • 糖类的合成和降解 • 糖类在生物体内的功能和作用 • 糖类的应用和发展前景
01
糖类的定义和分类
单糖
单糖是指不能再被简单水解成 更小的糖类的最小单位,通常 由含有五个或更多碳原子的链 状或环状结构组成。
单糖根据碳原子的排列方式可 以分为醛糖和酮糖两大类。
结构组成
糖类是生物体的重要结构组成成分,如脱氧核糖和核糖分 别是DNA和RNA的组成成分。
03
细胞识别
糖链参与细胞识别,细胞表面的糖蛋白通过糖链识别其他 细胞,在细胞间的信息交流中起重要作用。
糖类在生物体内的作用
代谢中间物
糖类在生物体内作为其他物质的 代谢中间物,如葡萄糖可以转化
为氨基酸或脂肪等物质。
THANKS
感谢观看
淀粉是由葡萄糖聚合而成,广泛存在于植物种子和根茎中, 是植物的主要储能物质。纤维素则是由葡萄糖聚合而成,是 植物细胞壁的主要成分,具有很好的生物相容性和生物可降 解性。
02
糖类的结构和性质
糖类的结构特点
糖类是含有醛基、酮基、醇基和羰基等杂环的有机化合物,其基本结构单元是单糖。
单糖根据碳原子数目可分为三碳糖、四碳糖、五碳糖、六碳糖等,其中六碳糖是最 常见的。
罗汉果等天然甜味剂,以及人工合成的低热量、高强度甜味剂。
02 03
糖类在生物医学领域的应用
随着生物技术的发展,糖类在生物医学领域的应用越来越广泛,如糖类 在药物传递系统、糖蛋白和糖肽的合成与分离、糖类在细胞识别和细胞 信号转导中的作用等方面的研究。
糖类与疾病预防和治疗
糖类与许多疾病的发生和发展密切相关,因此,研究糖类的结构和功能 对于预防和治疗疾病具有重要意义,如糖尿病、癌症等。
有机化学《糖类》PPT课件

11
[活动与探究] P90
实验事实
结论
1 1.80 g葡萄糖完全燃烧,只得到 2.64g二氧化碳和1.08 g水
实验式: CH2O
2 葡萄糖的相对分子质量为180
3 在一定条件下,1. 80 g葡萄糖与乙 酸完全酯化,生成的乙酸酯的质量 为3.90 g
4 葡萄糖可以发生银镜反应
分子式: C6H12O6
• 睡前吃糖,易形成酸性物质,形成龋齿
• 饱食后再吃糖,会使人发胖,促发糖尿病
• 牙病者吃糖会诱发牙痛
• 糖吃得过多,一部分转化为丙酮酸,使血液显 酸性,人体为了保持弱碱性,要动用钙等碱性 物质去中和过量的酸,可能导致人体缺钙
学以致用
.
21
●果糖简介:
1、分子式:C6H12O6 (五羟基己酮)
2、结构简式: CH2OHCHOHCHOHCHOHCOCH2OH
每个分子中含 5个 -OH
分子中含醛基
5 葡萄糖可以被还原为直链己六醇
6个碳排成直链
关于葡萄糖分子结Βιβλιοθήκη 的结论:该有机物分子式为C6H12O6,一个分子中含一个—CHO,
5个—OH, 6个碳排成直链 .
12
H CO
H C OH
葡
萄 糖
HO C H
的 分
H C OH
子
结 构
H C OH
H C OH
.
H
2.能说明葡萄糖是一种还原性糖,依据是( B)D
A.与H2加成生成六元醇 B.能发生银镜反应
C.能发生酯化反应
D.能与新制Cu(OH)2悬浊液共热生成红色沉
淀
.
23
3、下列关于葡萄糖的叙述错误的是( B )
高中有机化学--糖类.ppt

A、乙醇萄糖
合理膳食
健
经常运动
康 寄
保持身体健康
语
让爱你的人放心
一.糖类的概念及分类 1 .定义: 糖类是指 多__羟_基__醛 多__羟_基_酮_ 以 及能水解生成它们的物质。
说明:(1)糖类是绿色植物光合作用的产
物,糖类不都是甜的。我们食用的蔗糖是甜的, 它只是糖类中的一种。淀粉、纤维素均不甜,但 它们也属于糖类。有些有甜味的物质,如糖精, 不属于糖类。
(3) 葡萄糖的用途
1. 营养 物质
3. 制药 工业
2. 镀银 工业
4、 制酒 工业
【乐于关注】
糖尿病称为现代 疾病中仅次于癌症的 第二杀手,全世界糖 尿病患者约有1.25亿 人,我国的糖尿病患 者已超过4000万人。
防治糖尿病的关 键在哪里?
【善于思考】
合理膳食是防治糖尿 病的关键。
糖尿病人是否就不能 吃甜食了呢?
②此通式适用于大多数糖类化合物,而
对少数糖类物质不适合,如鼠李糖化学式为 ___C_6_H_1_2_O_5____,脱氧核糖化学式为_C__5_H___1_0_O___4_ 。 有些符合此通式的物质并不是糖类,如
__甲__醛___C__H_2_O__,,乙__酸___C_2_H__4O__2_,
___乳__酸___C_3_H__6O__3__等。
③
葡萄糖与新制氢氧化铜反应生 成绛蓝色溶液,加热产生砖红 色沉淀。
分子中含有一个醛 基,且有多个羟基
④ 在一定条件下,1. 80 g (0.01mol) 葡萄糖与0.05mol乙酸完全酯化。
每个分子中含 有5个羟基
⑤ 葡萄糖可以被还原为直链己六醇 6个碳排成直链
关于葡萄糖分子结构的结论:
有机化学糖类

有机化学糖类《有机化学糖类》嗨,同学们!今天咱们来唠唠有机化学里的糖类,这糖类啊,可和咱们的生活息息相关,像咱们吃的米饭、馒头里都有糖类呢。
不过咱化学课上得从化学的角度来认识它们,这就离不开糖类的化学式啦。
首先呢,咱得知道啥是化学式。
化学式就像是糖类的身份证,能告诉咱们它是由哪些原子组成的,以及这些原子是怎么排列组合的。
这原子之间的组合可不像把一堆小球随便堆在一起,它们是靠化学键连接起来的。
化学键呢,就好比原子之间的小钩子。
这里面有不同类型的小钩子哦。
比如说离子键,大家可以想象带正电和带负电的原子就像超强磁铁一样,正电的和负电的相互吸引就紧紧地吸在一起了,这就是离子键。
而共价键呢,就是原子们共用小钩子连接起来的。
咱们先来说说葡萄糖,葡萄糖的化学式是C₆H₁₂O₆。
这里面的碳(C)、氢(H)、氧(O)原子就是通过共价键连接起来的。
这就好比盖房子,碳原子、氢原子和氧原子就是不同的建筑材料,共价键就是把这些材料连接在一起的钉子或者胶水。
那它们为啥要这样连接呢?这就和原子的结构有关系啦,每个原子都想让自己的最外层电子达到稳定状态,就像咱们人都想让自己处于舒服的状态一样。
通过共价键共用电子,它们就能达到这个目的啦。
那在糖类里啊,还涉及到分子的极性这个概念。
这分子的极性呢,就类似小磁针。
比如说水,水是极性分子,氧原子这一端就像磁针的南极,带负电,氢原子那一端就像北极,带正电。
这就使得水有很多特殊的性质,像能溶解很多极性物质。
而糖类分子里有些部分也有极性,这就影响了它们在生物体里的功能和一些化学性质。
那像二氧化碳(CO₂)呢,它是直线对称的分子,就像一个两边一样重的跷跷板,它是非极性分子。
咱再来说说糖类里涉及到的氧化还原反应。
这个氧化还原反应就像是原子之间的一场交易。
比如说在生物体内,葡萄糖的氧化反应,就像是葡萄糖分子把自己的电子给了其他分子。
就好比你有一些小玩具(电子),然后你把这些小玩具送给了别的小伙伴。
有机化学第16章糖类资料

5
CHO CHOH CH2OH
丙醛糖(甘油醛)
CH2OH CO CH2OH
丙酮糖
CHO CHOH CHOH CHOH CH2OH 戊醛糖
CH2OH CO CHOH CHOH CH2OH 戊酮糖
CHO CHOH CHOH CH2OH
15
β - D-吡喃-果糖
链状费歇尔投影式转变成哈沃斯式 通用写法:
a. 吡喃型
O
O
呋喃型
氧在右上角 碳原子顺时针排列
b.将标准费歇尔式碳键右侧基团或原子写在哈沃斯式环
平面的下方;左侧基团或原子写在环平面上方。
c. D-型糖 ,-CH2OH 环上;半缩醛羟基在环下α,环上β d. L-型糖 ,-CH2OH 环下;半缩醛羟基在环上α,环下β
6
CH2OH O
OH
1
CH2OH
H H
H6
H
5
H
1
O CH2OH
OH 2
5H
OH 2
H4
3 OH
OH
H
α - D-呋喃-果糖
6
CH2OH O
OH
5H
OH 2
H4 OH
3 C1H2OH H
β -D-呋喃-果糖
OH
4
OH
3
OH H
α - D-吡喃-果糖
H
H6
H
5
H
1
O CH2OH
OH 2
OH
4
OH
3
OH H
丁醛糖 CHO CHOH CHOH CHOH CHOH CH2OH 已醛糖
有机化学《糖类》课件

可能存在的形式
鉴别方法
1、碳碳双键 2、醛基 3、羰基
使溴水或高锰酸钾溶液褪色 使溴水褪色、发生银镜反应等
不能发生银镜反应
4、羧基
具有酸的通性,能使指示剂变色
5、酯基 6、环状结构
使含酚酞的NaOH溶液逐渐褪色 难以检测
[活动与探究] P90
实验事实
结论
1 1.80 g葡萄糖完全燃烧,只得到 2.64g二氧化碳和1.08 g水
甜味 甜
甜
甜
不甜 不甜
结构 多羟基醛 多羟基醛 多羟基酮 n个葡萄糖单元
关系
同分异构
不是同分异构
拓展视野:单糖的立体异构
1、什么叫手性?
物质与其镜象的关系,与人的左手、右手一样,非常相似 但不能叠合,因此我们把物质的这种特性称为手性。
2、什么叫对映异构?
结构相同,构型不同并且互呈镜象对映关系的立体异 构现象称为对映异构。
水,等于口服营养液
学以致用
不宜吃糖的时机:
• 饭前吃糖降低食欲 • 睡前吃糖,易形成酸性物质,形成龋齿 • 饱食后再吃糖,会使人发胖,促发糖尿病 • 牙病者吃糖会诱发牙痛 • 糖吃得过多,一部分转化为丙酮酸,使血液显
酸性,人体为了保持弱碱性,要动用钙等碱性 物质去中和过量的酸,可能导致人体缺钙
学以致用
(B )
2.能说明葡萄糖是一种还原性糖,依据是( B)D A.与H2加成生成六元醇 B.能发生银镜反应 C.能发生酯化反应 D.能与新制Cu(OH)2悬浊液共热生成红色沉
淀
3、下列关于葡萄糖的叙述错误的是( B )
A.葡萄糖的分子式是C6H12O6 B.葡萄糖是碳水化合物,因其分子是由6
个碳原子和6个H2O构成 C.葡萄糖是一种多羟基醛,所以既有醇的
有机化学 糖类

在自然界分布最广,最重要的多糖是淀粉和纤维素。
麦芽糖:是由两分子D-葡萄糖,通过α-1,4-苷键结合而成
的,容易水解为两O HO HH HO CH2OH H OH H HO O H HO H OH α-1,4-苷键 H OH
纤维二糖:是纤维素水解的产物,由两分子D-葡萄糖,
通过β-1,4-苷键结合而成的。
HOH2C C HO H H
OH H O OH CH2OH
CH2OH O HO H OH H OH H CH2OH
D-果糖
HO C HO H H
CH2OH H O OH CH2OH
α-D-呋喃果糖
β-D-呋喃果糖
D-呋喃果糖环状结构的Haworth透视式:
HOH2C H
O H HO OH H
CH2OH OH
CH2 CH CH CH CH CHO OH OH OH OH OH
* * *
*
*
*
*
己酮糖
CH2 CH CH CH C CH2 OH OH OH OH O OH
2 单糖的立体构型
最简单的单糖是甘油醛,分子中有一个手性碳原子。 存在一对对映异构体,一种为左旋,一种为右旋。
CHO H OH CH2OH
β-1,4-苷键
H HO HO
CH2OH HO H OH H H
H O HO
CH2OH HO OH H OH H H
蔗糖:是一分子α-D-葡萄糖的半缩醛羟基和一分子β-D-
果糖的半缩醛羟基相互脱水结合而成的双糖。
H CH OH HOH2C H 2 O HO HO H HO H HO CH2OH H OH OH H H O
CHO OH HO OH OH CH2OH
有机化学基础知识点糖类的结构和性质

有机化学基础知识点糖类的结构和性质糖类是有机化合物中最常见的一类物质,广泛存在于自然界和生物体内。
它们不仅是重要的营养物质,也在生物体内担任着重要的功能角色。
本文将就糖类的结构和性质进行详细的讨论。
一、糖类的结构糖类的基本结构可以归纳为单糖、双糖和多糖三种类型。
单糖是最简单的糖类,包括三种常见的单糖:葡萄糖、果糖和半乳糖。
它们的分子式均为C6H12O6,但它们的结构却有所不同。
葡萄糖和果糖都是环状的结构,而半乳糖则是线性结构。
双糖是由两个单糖分子通过缩合反应形成的,比如蔗糖和乳糖。
多糖是由多个单糖分子缩合而成,常见的有淀粉和纤维素。
二、糖类的性质1. 溶解性: 糖类常用作食品中的添加剂,如砂糖和蜂蜜。
它们具有良好的溶解性,尤其是在水中能够迅速溶解。
这也是为什么糖类常被用于制作饮料、甜点等食品的原因。
2. 甜味: 糖类具有独特的甜味,是许多食物中不可或缺的调味品。
这是由于糖类分子中含有许多羟基,能够与味蕾上的受体相结合,从而引起甜味感觉。
3. 反应性: 糖类具有一定的反应性,可以与其他物质产生化学反应。
例如,糖类能够与氨基酸缩合形成糖基化合物,这在生物体内起着重要的作用。
此外,糖类还可以与氧化剂反应发生糖的焦糖化反应,生成焦糖色素。
4. 发酵性: 糖类可以被微生物发酵产生酒精和二氧化碳。
这也是为什么糖类常被用于酿造过程中的原因。
在酵母菌的作用下,糖类可以转化为乙醇和二氧化碳,并且在此过程中释放能量。
5. 构象异构性: 糖类分子的立体结构存在构象异构性。
例如,在溶液中,葡萄糖分子可以存在α型和β型两种构象。
这种构象异构性对于糖类的生物活性和化学性质都有一定的影响。
综上所述,糖类作为有机化合物的一类,其结构和性质的研究对于我们了解生物体内的基本过程和化学反应机制具有重要意义。
通过对糖类结构和性质的深入研究,我们可以更好地理解糖类在生物体内的作用,从而为相关领域的研究和应用提供基础支持。
16-糖类

CHO
CHO
CHO
CHO
CH 2OH
CH 2OH
CH 2OH
CH 2OH
D-(+)-葡萄糖
CHO
L-(-)-葡萄糖 D-(+)-半乳糖
CHO
L-(-)-半乳糖
自然界中存在的 单糖大多为D-型糖
CH 2OH CH 2OH
D-(+)-甘露糖
L-(-)-甘露糖
• 糖的构型命名 在糖的Fischer 投影式中,将编号最 大的 C*的构型与D-甘油醛比较,构型相同的为D-型 糖,反之为L-型糖。即编号最大的C*的-OH在右侧为 D-型糖;在左侧的是L-型糖。
的熔点,可以根据糖脎的结晶形状,生成速度及熔点
来鉴定糖。 成脎的条件:
O OH C C
如果只是C1、C2上所连基团或构型不同,其它碳原
CHO H OH CH2OH D-甘油醛
HO
CHO H CH2OH L-甘油醛
CHO
CHO
CH2OH D-(+)-葡萄糖
CH2OH D-(+)-甘露糖
CHO
CH2OH C=O
CH2OH D-(+)-半乳糖
CH2OH D-(-)-果糖
2、单糖的环状结构
CHO
开链结构无法解释的事实: ①不与亚硫酸氢钠发生加成反应; ②只与一分子醇作用即可生成稳定的缩醛型 CH 2OH 化合物。 ③有两种不同晶体的葡萄糖: 乙醇中结晶:熔点为146℃,比旋光为+112° 吡啶中结晶:熔点为150℃,比旋光为+19° ④变旋光现象:把两种不同的D-葡萄糖分别溶解于 水中, 比旋光度都逐渐发生变化,最终都稳定在 +52.7°。这种 糖在水溶液自行改变比旋光度的现象 称变旋光现象。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2. 编号最大的伯醇基在上方: D-构型 3. 半缩醛OH与伯醇基同侧:β型;反侧:α 型 4. 其余基:左上右下
H—C=O H———OH HO —— H H———OH H———OH CH2OH
CH2OH OH
CH2OH
O
OH
OH
O OH
Haworth
HO
HO
OH
OH
式
下页 首页
邓健 制作 刘俊义 审校
上页
下页
首页
22
第十五章 糖 类 第一节 单 糖 (四、单糖的化学性质)
四、单糖的化学性质
多个醇羟基具有醇的一般性质;羰基具有 醛酮的性质; 具有环式半缩醛羟基的特有性质。
由于这些官能团处于同一分子内而 相互影响,所以又显示某些特殊性质。
人民卫生电子音像出版社
上页
下页
首页
23
(2R,3S,4R,5R)-2,3,4,5,6-五羟基己醛
上页 下页 首页
6
第十五章 糖 类 第一节 单 糖 (一、构型和开链结构)
虽然可用R/S 构型法命名糖类, 但最常用的是 “D/L 构型标记法”+“俗名” 来命名糖类化合物。
凡离羰基最远的手性碳构型与 D-甘油醛相同者为D型, 反之为L型
H HO H H CHO OH H OH OH CH2OH
[α]D=+112 =+112 o(乙醇中结晶 乙醇中结晶 )
+52.3o
[α ]
[α]D=+18.7o(吡啶中结晶)
变旋现象 :
Time
一种构型的糖其旋光度在溶液 中会发生改变,最终达到一恒定值的现象。
邓健 制作 刘俊义 审校
上页
下页
首页
11
第十五章 糖 类 第一节 单 糖 (二、变旋光和环状结构)
第十五章 糖 类 第一节 单 糖 (二、变旋光和环状结构)
由于形成环状半缩醛,原来没有手性的羰基碳原子 变成了手性中心,因此同一单糖有两种不同的环状半缩 醛,即α、β两种异构体,它们是非对映体,这种仅仅端 基不同的异构称为端基异构体(anomer, 异头物)。
邓健 制作 刘俊义 审校
上页
下页
首页
13
上页
下页
首页
19
第十五章 糖 类 第一节 单 糖 (二、变旋光和环状结构)
问题:
写出α和β-D-吡喃半乳糖的构象式。 指出在水溶液中哪种更稳定。
H—C=O H———OH HO —— H HO———H H———OH CH2OH
D-半乳糖
β-D-吡喃半乳糖
α-D-吡喃半乳糖
人民卫生电子音像出版社
上页
下页
cis:βanomer
Right: Down
CH2OH
O OH
OH
OH
HO
上页
下页
首页
16
第十五章 糖 类 第一节 单 糖 (二、变旋光和环状结构)
Haworth 式把环当作平面,原子和原子 团垂直排布在环的上下方,仍不能完全表示 出葡萄糖的立体结构。更符合实际情况的是, 稳成半缩醛和缩醛,g 或 d羟基醛则主要以环状半缩醛的形式存在:
HOCH CH2 HOCH CH CHO 2CH 2CHO 2CH 22
CH2CH HOCHHOCH CH 2CH 2CHO 2CH22 2CH 2CHO
H O
H
OH OH O
H O OH O
H OH
糖类分子中既有C=O, 又在γ或δ位有-OH, 故可形成较稳定的 4碳1氧的五员杂环(呋喃型)或5碳1氧的六员杂环(吡喃型)。
15
D-glucose
β-D-吡喃葡萄糖
邓健 制作
α-D-吡喃葡萄糖
刘俊义 审校
上页
第十五章 糖 类 第一节 单 糖 (二、变旋光和环状结构)
课堂练习:
由D-甘露糖的Fischer投影式写出其Haworth式
CHO HO HO OH OH CH2OH
D-(+)-mannose
人民卫生电子音像出版社
单 单 糖 糖
醛糖: :丙醛糖 丙醛糖,,丁醛糖 丁醛糖,, 戊醛糖 戊醛糖,,己醛糖 己醛糖,,庚醛糖 庚醛糖 … … 醛糖 : … 酮糖: :丙酮糖 丙酮糖,,丁酮糖 丁酮糖,, 戊酮糖 戊酮糖,,己酮糖 己酮糖 … … 酮糖 : …
最简单的糖是甘油醛, 它是研究糖类化学结构的参照物, 也是合成复杂糖类化合物的起始原料。有些糖的羟基可被 氢原子或氨基取代, 它们分别被称为去氧糖和氨基糖。
D-果糖
D-山梨糖
D-核酮糖
D-木酮糖
邓健 制作
刘俊义 审校
上页
下页
首页
9
第十五章 糖 类 第一节 单 糖 (二、变旋光和环状结构)
二、单糖的变旋光现象和环状结构
单糖是多羟基醛(酮)的开链结构, 得到了一些化学反应的 证实。但单糖的其它一些性质却是开链结构不能解释的。
1.单糖晶体IR谱无νC=O; 醛糖PMR谱无醛氢的特征峰
首页
20
试问:(1)下列的单糖是何构型? (2)它的吡喃型哈沃斯式是怎样的(写出过程)? (3)它的α-体的稳定构象是什么?
CHO
CH2OH
设计与制作 邓 健 21
第十五章 糖 类 第一节 单 糖 (三、单糖的物理性质)
三、单糖的物理性质
单糖都是白色晶体,水溶性较大,常易形成
过饱和溶液(糖浆), 难溶于醇等有机溶剂。水-醇 混合溶剂常用于糖的重结晶;不纯的糖很难结 晶,目前常采用层析方法分离纯化。 单糖均有甜味,但程度各不相同,果糖最甜。 具有环状结构的单糖有变旋光现象。 这是开链 式与环式进行可逆的半缩醛/酮反应的结果。
第十五章 糖 类 第一节 单 糖 (四、单糖的化学性质)
(一) 成苷反应
糖的半缩醛(酮)羟基与另一含活泼H的化合物 (如:HO-, H2N-, HS-等) 脱水生成糖苷(glycoside)
HO OH HO
O
HO
OH + CH3OH 干 HCl OH
O OCH3 OH + OH
HO OH HO
O OCH3 OH
CH2-CH-CH-CH-CH-C—H OH OH OH OH OH CH2-CH-CH-CH-C-CH2 OH OH OH OH O O
邓健 制作
OH
葡萄糖
刘俊义 审校
果糖
上页 下页 首页
3
第十五章 糖 类
分类
根据糖类水解情况分为四类:
单糖:不能水解的糖。如葡萄糖、果糖、核糖等
双糖:水解后产生2分子单糖。如蔗糖、麦芽糖等
寡糖(低聚糖):水解后产生3~10个分子单糖。如棉子糖
多糖(高聚糖):完全水解后生成10个分子以上单糖
属天然高分子化合物。如淀粉、纤维素等
广义而言,碳水化合物也包括其衍生物。 如: 糖醇、脱氧糖、糖酸、糖醛酸、氨基糖等。
人民卫生电子音像出版社
上页
下页
首页
4
第十五章 糖 类 第一节 单 糖
第一节 单 糖 (monosaccharide)
第十六章 糖 类
第一节 单 糖
构型和开链结构
变旋光现象和环状结构 单糖的性质
第二节 双糖和多糖
双糖 多糖
邓健 制作 刘俊义 审校 1
第十五章 糖 类
第十五章 糖 类 (saccharide)
糖类又叫做碳水化合物(Carbohydrate),是自 然界中存在最多的一类有机物。植物干重的50% ~ 80%为糖类化合物。糖是重要的食物之一。 糖类是绿色植物吸收空气中的 CO2, 经过复杂的光合作用而产生的。
一、单糖的构型和开链结构
除丙酮糖外,单糖都含有手性碳原子。如葡萄 糖有四个手性碳原子,因此有24=16个即八对对映异 构体。葡萄糖只是其中的一对对映体。所以,只以 构造式 表示是不够的,还必须确定它的构型。
CHO H OH HO H H OH H OH CH2OH
人民卫生电子音像出版社
Glucose 葡萄糖
通过开链结构转变为其它环状结构。
[α]D = (18.7°×64% ) + (112°× 36%) = +52.3° 由于开链结构含量极低,因而没有明显的羰基特征光谱
人民卫生电子音像出版社
上页
下页
首页
14
第十五章 糖 类 第一节 单 糖 (二、变旋光和环状结构)
开链式与Haworth式的关系:
苷羟基
HO
D-吡喃葡萄糖
β-D-甲基吡喃葡萄糖苷 α-D-甲基吡喃葡萄糖苷
此反应只发生在半缩醛/酮羟基上, 该羟基又叫苷羟基
邓健 制作 刘俊义 审校
上页
下页
首页
24
第十五章 糖 类 第一节 单 糖 (四、单糖的化学性质)
O-苷, N-苷 S-苷, C-苷
OH O
OR O
苷元 aglycone (糖配基) R
太阳能 光合作用(植物) 呼吸(动物)
6CO2 + 6H2O
C6H12O6 + 6O2
化学能和热能
人民卫生电子音像出版社
上页
下页
首页
2
第十五章 糖 类
元素组成
绝大多数糖类分子由C、H、O三种元素 组成,大多数化合物具有通式Cn(H2O)m。
定义
糖类是一类多羟基醛(酮)以及 通过水解产生这些醛酮的物质。
HO H HO HO CHO H OH H H CH2OH
CHO H OH CH2OH
CHO HO H CH2OH
D-甘油醛
D-葡萄糖
邓健 制作
L-甘油醛
刘俊义 审校
