泰索帝(多西他赛注射液)
泰索帝版说明书

核准日期:2006年11月修改日期:2008年1月2009年3月多西他赛注射液说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:多西他赛注射液商品名称:泰索帝® TAXOTERE®英文名称:DOCETAXEL INJECTION汉语拼音:DUO XI TA SAI ZHUSHEYE【成份】化学名称: (2R,3S)-N-羧基-3-苯基异丝氨酸,N-叔丁基酯,13-酯链上5β-20-环氧-1,2α, 4,7β,10β, 13α-六羟紫杉醇-11-烯-9-酮4-乙酸2-苯甲酸酯三水合物泰索帝®:20mg –每支:20mg注射液为将相当于20mg 多西他赛(无水)的多西他赛三羟化合物,溶解于吐温80中而制成。
泰索帝®:80mg –每支:80mg注射液为将相当于80mg 多西他赛(无水)的多西他赛三羟化合物,溶解于吐温80中而制成。
每毫升泰索帝®注射液含有40 mg无水多西他赛。
泰索帝®溶剂-浓度为13% w/w 的注射用乙醇(以95%计)水溶液。
化学结构式:•3H2O分子式:C43H53NO14•3H2O分子量:本注射剂的全部辅料为:浓溶液:吐温80和氮气;溶剂:95%乙醇和注射用水。
【性状】黄至棕黄色的粘稠液体,配有溶剂。
几乎不溶于水,高脂溶性。
【适应症】多西他赛的适应症如下:乳腺癌1. 适用于局部晚期或转移性乳腺癌的治疗。
2. 泰索帝(多西他赛)联合曲妥珠单抗,用于HER2基因过度表达的转移性乳腺癌患者的治疗,此类患者先期未接受过转移性癌症的化疗。
3. 泰索帝(多西他赛)联合阿霉素及环磷酰胺用于淋巴结阳性的乳腺癌患者的术后辅助化疗。
非小细胞肺癌适用于局部晚期或转移性非小细胞肺癌的治疗,即使是在以顺铂为主的化疗失败后。
【规格】(1):20mg;(2):80mg【用法用量】多西他赛只能用于静脉滴注。
推荐剂量:一般性多西他赛的推荐剂量为每三周75mg/m2滴注一小时。
多西他赛注射液说明书

多西他赛注射液说明书[整理]多西他赛注射液说明书多西他赛注射液说明书查看详细说明书【批准文号】国药准字H20041128【中文名称】多西他赛注射液【产品英文名称】Docetaxel for Injection【生产企业】齐鲁制药有限公司【功效主治】1.适用于局部晚期或转移性乳腺癌的治疗。
2.适用于局部晚期或转移性非小细胞肺癌的治疗,即使以顺铂为主的化疗失败后。
【化学成分】本品主要成份为多西份赛化学名称名{2Ar-[2aα,4β,4aβ,6β,9α(αR*,Βs*),11α,12α,12aα,12bα]}-β-{[(1,1-二甲基乙氧基)羰基]氨基}-α-羟基苯丙酸[12b-乙酰氧苯甲酰氧-2a,3,4,4a,5,6,9,10,11,12,12a,12b-十二氢-4,6,11-三羟基-4a,8,13,13-四甲基-5-氧代-7,11-亚甲基-1H-环癸五烯并[3,4]苯并[1,2-b]氧杂丁环-9-基]酯。
分子式:C43H53NO14分子量:807.88【药理作用】药理作用:多西他赛为紫杉类药物,通过促进微管双聚体装配成微管,同时通过防止去多聚化过程而使微管稳定,阻滞细胞于G2和M期,从而抑制癌细胞的有丝分裂和增殖。
多西他赛的药理作用比紫杉醇强,在细胞内浓度比紫杉醇高3倍,并在细胞内滞留时间长,其对微管亲和力是紫杉醇的2倍;作为微管稳定剂和装配促进剂,活性比紫杉醇大2倍;作为微管解聚抑制剂,活性比紫杉醇大2倍。
在体外抗瘤活性试验中,已证实多西他赛的抗瘤活性是紫杉醇的1.3~12倍。
临床研究表明,对于蒽环类耐药乳腺癌,多西他赛较紫杉醇有更高的有效率。
多西他赛是目前为止蒽环类耐药乳腺癌的二线治疗中最有效的药物;在非小细胞肺癌单药治疗和联合化疗中,多西他赛是最有效的药物之一。
遗传毒性:在CHO-K1细胞染色体畸变试验和小鼠骨髓微核试验中,多西他赛表现出致断裂作用,但在Ames试验和CHO/HGPRT基因突变试验中未见致突变作用。
多西他赛

多西他赛别名:多西紫杉、多西紫杉醇、泰索帝、艾素、多帕菲、多帕菲、多烯紫杉醇、紫杉特尔、Taxotere;[适应症]:用于治疗晚期乳腺癌、非小细胞肺癌。
也有报道用于治疗头颈部癌、小细胞肺癌、胃癌、卵巢癌等肿瘤。
;[药理作用]:本品为细胞周期特异性抗肿瘤药,可特异性作用于M期细胞。
本品可促进小管聚合成为稳定的微管,并抑制其解聚,以显著减少小管的数量,也可通过破坏微管的网状结构,抑制细胞有丝分裂,从而达到抗肿瘤的目的。
[注意事项]:1.肝功能不全者、严重衰弱者、严重水潴留者、严重感觉神经疾病患者慎用。
2.本品用于儿童的安全性尚未确定。
3.尚不清楚本品能否分泌人乳汁,哺乳期妇女的用药安全性尚未确定,用药前应停止哺乳。
4.配制本品时,粉针剂应先以指定溶剂溶解,再以生理盐水或5%葡萄糖注射液稀释后使用(配制后浓度不超过0.74mg/ml)。
工作台表面应覆盖可丢弃的塑料薄膜,操作者应穿戴防护衣服及手套。
若皮肤接触了药液,应立即用肥皂和水彻底清洗;如眼睛或黏膜接触了药液,立即用水彻底清洗。
配制好的药液应立即使用。
5.在使用本品的最初几分钟内,可能发生过敏反应,应具备相应的急救设施。
为预防液体潴留和过敏反应,推荐在用药前1天开始口服地塞米松(每天16mg,连用4~5天)。
6.如用药后仅发生面部潮红或局部皮肤反应,则不需要停止治疗。
如发生严重过敏反应(血压下降超过2.67kPa、支气管痉挛或全身皮疹/红斑),则需立即停止给药,并给予对症治疗。
已发生过严重不良反应者,不能再次使用本品。
7.使用本品治疗时如出现严重的周围神经病变、严重的或累积性皮肤反应,或严重的中性粒细胞减少(低于0.5×109/L,并持续7天或7天以上),建议下1个疗程减量给药。
8.当血胆红素高于正常值上限、氨基转移酶高于正常上限1.5倍、ALP高于正常上限2.5倍时,应停用本品治疗。
9.药物过量时,可能表现为中性粒细胞减少、皮肤反应和感觉异常。
多西他赛注射液市场调查

多西他赛注射液市场调查一、多西他赛注射剂产品简介1、上市情况简介多西他赛(docetaxel,docetaxol)又名多西紫杉醇,属于微管解聚抑制剂,是从欧洲浆果紫衫的针叶中提取的无活性化合物。
该产品由 Rhone-Poulenc Rorer公司开发的一个半合成紫杉醇衍生物,商品名Taxtotere,由Rhone-Poulenc Rorer公司于1995年4月在墨西哥首次上市,现已在英、美、法、意、德、日等主要国家上市,1998年获欧盟和美国FDA批准进入欧洲及美国市场。
Taxtotere于2010年在中国上市,由赛诺菲-安万特公司生产。
中国医学科学院药物研究所与恒瑞公司合作开发成功后,多西他赛原料药及粉针剂作为四类新药于2002年9月30日获准生产,商品为“艾素”,2003年齐鲁制药厂的原料药及注射剂获得生产注册证,商品名为“多帕菲”。
2、作用机理本品为细胞周期特异性抗肿瘤药,可特异性作用于M期细胞。
本品可促进小管聚合成为稳定的微管,并抑制其解聚,以显著减少小管的数量,也可通过破坏微管的网状结构,抑制细胞有丝分裂,从而达到抗肿瘤的目的。
3、适应症主要治疗晚期乳腺癌、卵巢癌、非小细胞肺癌,对头颈部癌、小细胞肺癌;对胃癌、胰腺癌、黑色素瘤等也有一定疗效。
4、专利:多西紫杉醇未在中国申请专利,1998年11月9日国家药管局受理了法国罗纳普朗克乐安公司的多西紫杉醇及泰素帝注射液的行政保护申请,申请号:A-FR98100614,现已审查结束,经药管局审核查实,泰素帝在该药品行政保护申请日(1998年10月6日)前已经在我国进口销售,据此,不符合《药品行政保护条例》第五条第三项的规定;根据《药品行政保护条例》第十一条,作出审查决定,对多西紫杉醇及泰素帝注射液不给予行政保护。
二、多西他赛注射剂市场情况1、抗肿瘤药市场概况1)2006-2011年抗肿瘤药市场规模与增长率在中国医院用药市场,近几年抗肿瘤药物的销售规模一直稳步增长,2013年达到了800亿元,同比增长了13.68%。
多西他赛药物说明书

3天激素预处理:在多西他赛用药前一天开始使用地塞米松8mg (口服),每日二次,连用三天
多西他赛—单周方案:
在多西他赛用药前12小时给予首剂地塞米松8mg,然后每隔12小时 给予一次,共3次
多西他赛的预处理要求及方法较紫杉醇简单
VS紫杉醇:血液学不良反应比 较
紫杉醇:
1. 剂量和疗程依赖性;剂量越大,毒性越大,注射时间越长,毒性越大 2. 24小时的毒性比3小时大 3. 中性粒细胞计数平均最低点第11天,第15-21天可恢复
一定要均匀、澄清、透明
多帕菲是国产质量最优的多 西他赛
总杂质含量在国产多西他赛中含量最低
多帕菲小结
• 1. 与紫杉醇相比更优,无交叉耐药; • 2. 广泛用于非小细胞肺癌、前列腺癌、乳腺癌的治疗,
NCCN指南明确推荐; • 3. 其他癌种NCCN指南中也具有广泛推荐; • 4. 质量最优、杂质含量最低的多西他赛。
推荐新辅助和辅助方案: 顺铂75mg/m2 d1;多西他赛75mg/m2 d1;21天为1周期,共4周期
化疗原则-一线治疗
已证实顺铂或卡铂和以下药物联用均疗效较好:紫杉醇,多西他赛,吉西 他滨,依托泊苷,长春新碱,培美曲塞及紫杉醇衍生物 新药物/不含铂类的联药方案如有研究显示有效且耐受性好也可选择。 (如吉西他滨/多西他赛,吉西他滨/长春新碱)
响也较大,如在室温中放置时间不足,药品温度较低时, 药液不易溶解,会造成后续药品溶解使用过程中主要成分 多西他赛析出产生浑浊。正立药液使药物集中在底部,方 便下一步操作。
2、溶剂应贴壁缓慢注入药液,采用手工或振荡器溶解。 建议采用一支溶剂对应一支药液进行溶解,手工缓慢反复
倒置混合或用“涡旋式振荡器”混匀(建议中速3分钟以 上),减少振摇,避免产生大量气泡。振摇也可能造成主 成分多西他赛析出而溶解不完全。
多西他赛-医肿讲课资料

➢多西他赛单药方案能显著提高转移性乳腺癌的肿瘤进 展时间、总有效率和总体生存。
Nabholts JM, et al, J Clin Oncol 1999,17(5):1413 S.E. Jones et al, J Clin Oncol, 2005, 23:5542-5551
治疗蒽环类药物化疗失败的复
严重不良反应发生率较低
多西他赛治疗乳腺癌 推广方案
多西他赛辅助治疗 早期乳腺癌
辅助治疗腋窝淋巴结阳性且无远
处转移的早期乳腺癌-TAC方案
药物 DOC ADM
CTX
剂量及途径
时间及疗程
75mg/m2 IV(1h) d1 q3w×6
50mg/m2 IV
d1 q3w×6
500mg/m2 IV
d1 q3w×6
2003年欧盟批准多西他赛用于NSCLC一 线治疗
单药治疗铂类药物化疗失败的局
部进行性或转移性NSCLC
药物 DOC
剂量及途径 75mg/m2 IV(1h)
时间及疗程 d1 q3w×6
➢一项前瞻性随机对照研究(TAX317)证明多西他赛75mg/m2, q3w给药与最佳支持治疗(BSC)相比能明显延长生存期。
d1
q3w×6
weekly,until
disease progression
➢此方案与单用多西他赛方案相比,ORR为61%:34% (P=0.0002);中位TTP为11.7月:6.1月(P=0.0001);中 位OS为31.2月:22.7月(P<0.05)。Ⅲ~Ⅳ度中性粒细胞 减少发生率(%)为32%:22%。
2000年欧盟批准多西他赛用于初治失败 的晚期NSCLC的治疗
2001年Lancet和ASCO公布:多西他赛 联合吉西他滨治疗晚期NSCLC,安全性 和患者耐受性优于含顺铂的化疗方案
多西他赛不良反应及分析

多西他赛不良反应及分析[摘要]目的:探讨多西他赛所致不良反应的特点,总结其所致不良反应的临床表现,为临床合理用药,预防不良反应提供参考。
方法:对1994-2008年国内报道的多西他赛所致不良反应进行分析。
结果:多西他赛的主要不良反应有过敏反应、骨髓抑制、神经毒性、消化系统反应、液体潴留和血管性水肿等。
结论:多西他赛最严重的不良反应是过敏性休克、肠黏膜缺血性炎症、重度致死性水肿,使用时应严加防范。
[关键词]多西他赛;不良反应[中图分类号]R954[文献标识码]B[文章编号]1673-7210(2009)02(c)-090-02多西他赛,又名多烯紫杉醇,是一种新型植物碱类抗肿瘤药物,是一种半合成抗肿瘤药,其前体从欧洲紫杉的针叶中提取。
多西他赛属紫杉烷类药物,它能通过实质上“冻结”细胞内在骨架而抑制肿瘤细胞分化。
细胞骨架由微管组成。
而微管在细胞周期中会适时发生装配和分拆现象。
多西他赛可以促使微管装配并阻止微管分拆,由此抑制肿瘤细胞分化,最终导致肿瘤细胞死亡。
多西他赛注射液是由法国罗纳普朗克・安乐公司于1986年研发成功的一种抗癌新药,1995年4月在墨西哥首先上市,随后在英、美、法、意、德、日等国家上市。
我国自2002年起,先后批准江苏恒瑞医药有限公司、齐鲁制药有限公司等6家生产该品。
2003年,法国罗纳普朗克・安乐公司向我国出口了多西他赛注射液,商品名“泰索帝”。
多西他赛目前主要用于乳腺癌、卵巢癌、非小细胞肺癌、前列腺癌等多种实体肿瘤,并具有非常好的疗效。
与紫杉醇相比,多烯紫杉醇在抗肿瘤方面有独特的优势,多烯紫杉醇的亲和性为紫杉醇的2倍,在体外抗癌活性试验中,多烯紫杉醇活性可达紫杉醇的10倍,除此之外,多烯紫杉醇还具有较好的生物利用度、更高的细胞内浓度、更好的水溶性及优异的抗癌广谱性,多烯紫杉醇与某些抗肿瘤药物联合使用时,还具有协同抗肿瘤作用。
多烯紫杉醇是继紫杉醇后又一种新型抗微管药物,与紫杉醇相比多烯紫杉醇从细胞内外流较少且低剂量诱导细胞凋亡效应显著。
多西他赛微乳注射液_新型抗癌药

化酶(Cl50=3.5mM)和抑制磷酸二酯酶环—磷腺苷(AMPc)(Cl50=5.4mM)而产生抗血小板聚集作用。
作为抑制磷酸二酯酶环—磷腺苷的结果,三氟柳使血小板内环-磷腺苷的水平显著增高。
由于对血管环氧化酶不产生作用,因而保留前列环素的生物合成,从而保留由它产生的对血小板聚集的生理抑制。
项目进度:已完成临床前研究工作,三个月内可以申报临床。
三氟柳(Trifiusal),1981年由西班牙Uriach公司开发上市,后在欧洲其他国家,南美,中东,东南亚等20多个国家注册上市。
三氟柳在临床上广泛应用于预防中风和心肌梗塞,是一种疗效确切,安全可靠的药物。
该药是西班牙Uriach公司最成功的产品,居该公司销售第一位。
国外剂型以片剂、胶囊为主。
该药1999年列入英国药典。
该品种在中国尚未上市,有三家申报,属化药3.1类新药。
在中国没有专利及行政保护问题。
1)生产工艺简单,无环境污染问题。
2)三氟柳预防和治疗血栓栓塞的临床效果与阿司匹林相似:与阿司匹林相比,三氟柳能降低局部缺血病人发生出血并发症的危险。
3)本品制成肠溶胶囊,可改善本品对胃刺激性。
血栓病是由于血栓引起的血管腔狭窄与闭塞,使主要脏器发生缺血和梗塞而引发机能障碍的各种疾病。
按照来自BusinessCommuncations公司的最新报告显示,近年来包括血栓类疾病在内的血液疾病治疗市场正在快速增长。
2003年,全球血液疾病治疗市场己达254亿美元,并且以每年6.7%的速度增长,2008年有望超过350亿美元。
抗血栓治疗市场也将从2003年的92亿美元增长到2008年的123亿美元。
目前国内使用抗血栓药物总金额在14亿一15亿人民币之间,年增长率在15%-20%左右,治疗血栓性疾病的三大类药物抗血小板类药物、抗凝血药物和溶血栓药处于三分天下的态势。
目前临床上使用的抗血小板类药物有阿司匹林、双嘧达莫(潘生丁),及近年上市的奥扎格雷和硫酸氯吡格雷等。
除阿司匹林外均只是用于治疗。
多西他赛注射液说明介绍模板--多帕菲之欧阳家百创编

多西他赛注射液说明书欧阳家百(2021.03.07)【药品名称】通用名称:多西他赛注射液商品名称:多帕菲英文名称:Docetaxel Injection汉语拼音:Duoxitasai Zhusheye【成份】本品主要成份为多西他赛,其化学名称为:{2aR-[2aα,4β,4aβ,6β,9α(αR*,βS*),11α,12α,12aα,12bα]}-β-{[(1,1-二甲基乙氧基)羰基]氨基}-α-羟基苯丙酸[12b-乙酰氧-12-苯甲酰氧-2a,3,4,4a,5,6,9,10,11,12,12a,12b-十二氢-4,6,11-三羟基-4a,8,13,13-四甲基-5-氧代-7,11-亚甲基-1H-环癸五烯并[3,4]苯并[1,2-b]氧杂丁环-9-基]酯。
化学结构式:分子式:C43H53NO14分子量:807.88Cas No:114977-28-5分子量:807.88辅料名称:柠檬酸,吐温-80,乙醇【性状】本品为黄色至棕黄色澄明油状液体。
【适应症】1.适用于局部晚期或转移性乳腺癌的治疗。
2.适用于局部晚期或转移性非小细胞肺癌的治疗,即使是在以顺铂为主的化疗失败后。
【规格】20mg【用法用量】多西他赛只能用于静脉滴注。
所有病人在接受多西他赛治疗前均必须口服糖皮质激素类药物,如地塞米松,在多西他赛滴注一天前服用,每天16mg,持续至少3天,以预防过敏反应和体液潴留。
多西他赛的推荐剂量为70-75mg/m2,静脉滴注一小时,每三周一次。
多西他赛注射液及溶剂使用说明:1.制备多西他赛预注射液1)若从冰箱中取出所需数目的多西他赛,需在室温下放置5分钟。
2)用一装有针头的刻度注射器将与多西他赛注射液对应的溶剂吸出。
3)将装药液的瓶子倾斜,将注射器中全部溶剂注入对应的多西他赛注射液瓶中。
4)拔出针管及针头,手工反复倒置混合至少45秒,不能摇动。
5)将混合后的药瓶室温放置5分钟,然后检查溶液是否均匀澄明(由于处方中含吐温-80,放置5分钟后通常还会有泡沫)。
多西他赛注射液的制备及质量控制

多西他赛注射液的制备及质量控制朱雷;沈琦【摘要】目的制备一种稳定的多西他赛注射液,并对其进行相应质量控制和稳定性考察.方法通过对多西他赛注射液的处方工艺的系统研究,制备一种稳定的多西他赛注射液.参照注射用多西他赛的国家试行标准和安万特的多西他赛注射液(泰索帝)的内控标准,制定相应标准并对其质量进行控制和稳定性考察.结果以酒石酸为pH调节剂,当溶液的pH为3.5左右时,注射液稳定性最好.通过12个月的稳定性考察,注射液的各项指标均符合要求.结论制备工艺比较简单,制成的多西他赛注射液稳定性好,质量符合标准要求.【期刊名称】《西北药学杂志》【年(卷),期】2010(025)002【总页数】3页(P121-123)【关键词】多西他赛注射液;制备;质量控制【作者】朱雷;沈琦【作者单位】上海交通大学药学院,上海,200030;上海迪赛诺医药发展有限公司,上海,201203;上海交通大学药学院,上海,200030【正文语种】中文【中图分类】R94多西他赛自1995年在墨西哥、南非被批准用于治疗乳腺癌及非小细胞肺癌(NSCLC)以来,已在世界范围内51个国家获准使用,且在其中24个国家中,它是唯一被批准用于治疗晚期NSCLC的药物。
2004年本品先后获得美国FDA批准用于激素难治性前列腺癌和淋巴结阳性的早期乳腺癌的治疗。
加之已批准的一线和二线治疗转移性NSCLC的适应证,以及在胃癌和头颈部肿瘤治疗上的巨大潜力,并已或正在成为这些癌种治疗的最常用或标准疗法之一,使得多西他赛成为治疗实体肿瘤应用最广泛的细胞毒药物,也是肿瘤治疗药物的里程碑。
现临床使用较多的是20 mg∶0.5 mL的制剂[1],临床使用时将多西他赛注射用浓溶液和多西他赛注射用溶剂(13%的乙醇水溶液)先混匀,然后再用9 g·L-1氯化钠输液或50 g·L-1葡萄糖输液稀释至给药浓度。
这不仅给医务工作者带来操作上的麻烦(多西他赛注射用浓溶液和多西他赛注射用溶剂不是特别容易混匀),而且更重要的是多步稀释增加了药物被污染的概率。
2024年多西他赛注射液市场需求分析

多西他赛注射液市场需求分析引言多西他赛注射液是一种常用于癌症治疗的药物,具有抗肿瘤的作用。
本文将对多西他赛注射液市场的需求进行分析,包括市场规模、需求动态、竞争格局等方面。
市场规模根据市场数据统计,多西他赛注射液市场在过去几年呈现出稳步增长的趋势。
截至目前,多西他赛注射液市场的规模已经达到XX亿美元。
预计在未来几年,市场规模还将持续扩大。
需求动态多西他赛注射液的需求主要来自于癌症患者,尤其是乳腺癌、肺癌等常见恶性肿瘤患者。
随着人口老龄化的加剧和癌症发病率的增加,多西他赛注射液的需求量在不断增长。
此外,随着医疗技术的不断进步,多西他赛注射液的应用范围也在不断扩大。
除了作为单药使用外,多西他赛注射液还常与其他抗癌药物联合使用,以提高疗效。
这进一步推动了多西他赛注射液的需求增长。
竞争格局目前,多西他赛注射液市场存在着激烈的竞争。
主要的竞争对手包括国内外药企,如赛诺菲、辉瑞等。
这些企业通过不断研发新产品、降低价格、提供优质服务等方式争夺市场份额。
在竞争格局方面,多西他赛注射液市场呈现出以下几个特点: - 品牌竞争激烈:不同的药企通过品牌宣传和市场推广来争夺消费者的注意力和认可度。
一些知名品牌在市场上占据着较大份额。
- 技术创新驱动:药企不断进行研发创新,推出更为安全、有效的多西他赛注射液产品。
技术创新成为企业在市场中立于不败之地的关键。
- 价格竞争激烈:多西他赛注射液的价格也成为药企争夺市场份额的重要竞争手段。
一些企业通过降低价格来吸引更多消费者。
市场前景多西他赛注射液市场在未来几年将保持稳步增长的趋势。
随着医疗技术的进步和人们对健康的重视,多西他赛注射液的需求将继续增加。
同时,随着市场竞争的加剧,药企需要注重产品质量和服务质量的提升,加强研发创新,提供个性化的解决方案,以满足不同消费者的需求。
结论多西他赛注射液市场需求的持续增长为药企带来了机遇和挑战。
通过了解市场规模和需求动态,把握竞争格局和市场前景,药企可以更好地制定市场营销策略,提高市场竞争力,实现可持续发展。
多西他赛注射液市场分析

多西他赛注射液的市场分析报告一、多西他赛产品简介多西他赛(Docetaxel/Taxotere)又名多西紫杉醇,是由法国原Rhone-Poulenc Rorer、即现在的Sanofi-Aventis公司开发的一个半合成抗肿瘤药,1995年4月在墨西哥首次上市,1996年经美国FDA批准,多西他赛用于肺癌、乳腺癌和结肠癌等的治疗。
2004年5月FDA批准了泰素帝与泼尼松联合给药,治疗晚期转移性前列腺癌。
目前已在包括中国和欧、美、日等国在内的世界近百多个国家或地区获准销售。
2009年中华药学会样本城市数据库显示,多西他赛已成为国内最畅销的抗肿瘤药。
二、多西他赛和紫杉醇的区别紫杉醇是从天然植物红豆杉中提取出的具有天然生物活性的化合物,多西他赛则是由紫杉醇再经人工合成所得到的紫杉醇衍生物。
与紫杉醇相比,多西他赛在抗肿瘤方面有独特的优势:1、它的亲和性为紫杉醇的2倍,在细胞内的浓度比紫杉醇高3倍,并在细胞内滞留时间更长。
2、在体外抗癌活性试验中,多西他赛活性可达紫杉醇的10倍。
3、多西他赛还具有较好的生物利用度、更好的水溶性及优异的抗癌广谱性,与某些抗肿瘤药物联合使用时,还具有协同抗肿瘤作用。
4、多西他赛对某些表达P-糖蛋白的耐药细胞株,甚至是对紫杉醇耐药者均有效。
毒性反应方面两者的特点有所不同,紫杉醇的过敏反应多,外周神经毒性大,多西他赛过敏反应少,神经毒性小;而血液学毒性(尤其是中性粒细胞减少)多西他赛较紫杉醇严重。
三、市场概况及市场前景分析1、疾病发展概况癌症是仅次于心血管疾病的第二大死因。
从1996年以来全球每年新确诊的肿瘤患者均在1030万以上。
世界卫生组织2001年报道,世界癌症发病率和死亡率比1990年上升了22%,今后20年还将上升大约50%。
中国卫生部的统计资料表明:目前中国每年新生肿瘤患者总数约212.7万人左右,其中,每年有106万左右的恶性肿瘤新生患者;同时,全国约有268.5万左右的肿瘤现有患者,其中,恶性肿瘤现有患者约148.5万左右。
抗肿瘤药——多西他赛

抗肿瘤药——多西他赛
汤致强
【期刊名称】《中国药学杂志》
【年(卷),期】1999(34)2
【摘要】多西他赛(Docetaxel、泰索帝)是一种新型抗肿瘤药物,它属于紫杉类化合物,为白色或近似白色粉状物,相对分子量8079。
结构式如下:1药效学本品的作用机制是加强微管蛋白聚合作用和抑制微管解聚作用,导致形成稳定的非功能性微管束,因而破坏肿瘤细胞的...
【总页数】1页(P134-134)
【关键词】抗癌药;多西他赛;药效学;药物相互作用
【作者】汤致强
【作者单位】中国医学科学院协和医科大学肿瘤医院
【正文语种】中文
【中图分类】R979.1
【相关文献】
1.抗肿瘤药物多西他赛研究进展 [J], 赵颖;王芮
2.肿瘤治疗与抗肿瘤药的进展与合理用药——抗肿瘤药临床应用专家圆桌会议纪要[J], 程迎秋;孙燕
3.抗肿瘤药多西他赛的临床地位及其市场趋势 [J], 马培奇
4.抗肿瘤药——Novacea公司的三种抗肿瘤药物 [J], 张振华(摘)
5.抗肿瘤药:11056 多西他赛成为日本乳腺癌研究中有益的补充药 [J], 施桂兰(摘)
因版权原因,仅展示原文概要,查看原文内容请购买。
多西他赛简介及抗肿瘤

多西他赛简介1.简介多西他赛(Docetaxol)是由欧洲浆果紫杉的针叶中提取的化合物半合成的紫杉醇衍生物,由法国的Rhone-Poulenc Rorer公司开发并上市。
其作用机理与紫杉醇类似,通过促进微管双聚体装配成微管,同时防止去多聚化过程而使微管稳定,阻滞细胞于G2和M期,抑制细胞进一步分裂,从而抑制癌细胞的有丝分裂和增殖。
多西他赛的药理作用比紫杉醇强,在细胞内浓度比紫杉醇高3倍,并在细胞内滞留时间长。
其对微管亲和力是紫杉醇的2倍;作为微管稳定剂和装配促进剂,活性比紫杉醇大2倍;作为微管解聚抑制剂,活性比紫杉醇大2倍。
在体外抗瘤活性试验中,已证实多西他赛的抗瘤活性是紫杉醇的1.3~12倍。
多烯紫杉醇抗瘤谱广、抗肿瘤作用强,对难治性的乳腺癌、非小细胞肺癌等的疗效均较突出,临床应用潜力深厚。
然而多西他赛难溶于水,且脂溶性也不大,严重影响了其临床应用。
目前上市品种仅为多西他赛注射液,是用吐温-80及乙醇作溶剂配制而成,易引起较多不良反应,如刺激、溶血、过敏反应、神经毒性、心血管毒性等等。
且使用前要使用抗过敏药物,给患者带来了极大的不便和痛苦。
本项目旨在解决多西他赛水溶性及稳定性问题,进而避免因使用吐温-80而引起的溶血、过敏等不良反应问题。
本项目的意义在于为临床提供一种安全有效的多西他赛静脉给药新制剂,同时对脂质体的制备工艺进行创新,在提高载药量的同时解决其稳定性问题,也为其它同性质药物制剂的制备提供借鉴作用。
2.研究现状及创新性中国专利CN1931157A公开一种可以注射或口服的多西他赛脂质体及其固体制剂。
其以磷脂、胆固醇为基本膜材,加入适当的附加剂,采用多种方法制备了各种类型的脂质体,制得的脂质体粒径小,包封率高,稳定性好且毒副作用低,基本达到了临床注射要求。
但制备的脂质体浓度较低,生产时需容积较大的容器,成本高,不适合大剂量给药。
中国专利CN1846692A和CN101057831A公开一种多西他赛长循环脂质体及其制备方法。
泰索帝(多西他赛注射液)

【药品名称】多西他赛注射液【英文或拉丁名】Docetaxel Injection 【汉语拼音】Duoxitasai Zhusheye 【主要成分】多西他赛【化学名】[2aR-(2aα,4β,4aβ,6β,9α,(αR*,βS*),11α,12α,12aα,12bα)]-b-[[(1,1-二甲基乙氧基)羰基]氨基]-α-羰基苯丙酸[12b-乙酰氧-12-苯甲酰氧-2a,3,4,4a,5,6,9,10,11,12,12a,12b-十二氢-4,6,11-三羟基-4a,8,13,13-四甲基-5-氧代-7,11-亚甲基-1H-环癸五烯并[3,4]苯并[1,2-b]氧杂丁环-9-基]酯【结构式及分子式、分子量】分子式:C43H53NO14分子量:807.89【性状】本品为淡黄色的澄明粘稠液体,配有稀释剂[13%(w/w)注射用乙醇水溶液]。
【药理毒理】药理作用多西他赛为紫杉醇类抗肿瘤药,通过干扰细胞有丝分裂和分裂间期细胞功能所必需的微管网络而起抗肿瘤作用。
多西他赛可与游离的微管蛋白结合,促进微管蛋白装配成稳定的微管,同时抑制其解聚,导致丧失了正常功能的微管束的产生和微管的固定,从而抑制细胞的有丝分裂。
多西他赛与微管的结合不改变原丝的数目,这一点与目前临床应用的大多数纺锤体毒性药物不同。
毒理研究遗传毒性:在CHO-K1细胞染色体畸变试验和小鼠骨髓微核试验中,多西他赛表现出致断裂作用,但在Ames试验和CHO/HGPRT基因突变试验中未见致突变作用。
生殖毒性:在大鼠静脉注射多西他赛0.3mg/kg(按体表面积折算,约为临床推荐剂量的1/50),未见对生育力的损伤,但可引起睾丸重量减轻。
该结果与大鼠和犬10个周期(每21天给药1次,连续6个月)的重复给药试验结果有相关性;大鼠和犬静脉注射剂量分别为5mg/kg和0.375mg/kg时(按体表面积折算,分别约相当于临床推荐剂量的1/3和1/15),可见睾丸萎缩和变性,大鼠在低剂量时增加给药次数也表现出相似的作用。
化疗药说明
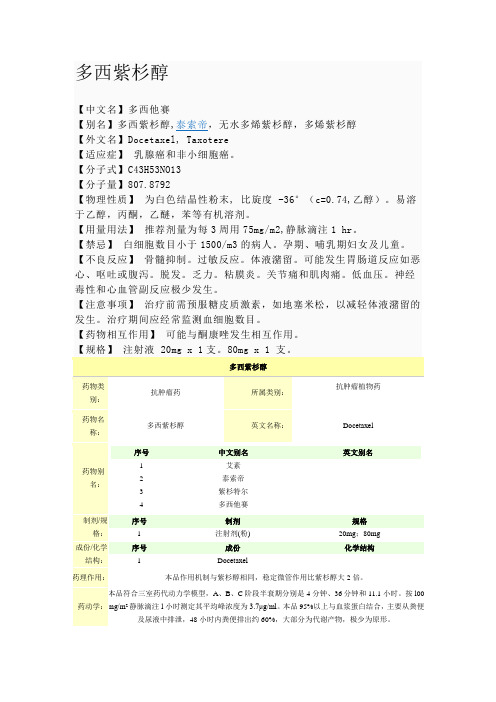
人体表面积怎么计算(化疗用)
由于人种、年龄、性别等的差异,体表面积的估算公式有很多,均为经验公式。
目前国内临床针对国人广泛采用的是1937年许文生发表在《中国生理学杂志》
上的Stevenson公式,即:体表面积(m2)=0.0061×身高(cm)+0.0128×体重(kg)-0.1529. 历经70多年,国人身体状况出现了一些变化,因此有研究人员
对此作出了修正。
以纸模法测量100 名成人(男女各50 名) 体表面积, 并测
量其身高、体重, 比较以
Stevenson 公式计算之人体表面积与实测体表面积的差异。
结果表明, Stevenson 公式已不适用于
计算当代中国人体表面积, 据男女各50 例所得到的男女体表面积计算公式分别为: S男= 010057
×身高+ 010121 ×体重+ 010882 , S女= 010073 ×身高+ 010127 ×体重- 012106 , 若不区别男和
女, 为中国人适用的通式为S = 010061 ×身高+ 010124 ×体重- 010099 。
尽管如此,这些经验公式仍然是可靠的,对肿瘤临床的用药的计算提供了基本的数据,然后医生会根据病人的个体差异,进行调整。
没有不负责任的公式,只有不懂得变通的医生。
个体化、人性化的治疗方案是患者的福祉。
要精确测量特定人体的体表面积可以有办法:1、比如纸膜法,但临床应用比较繁琐;2、设想--用光学仪器扫描后三维重建+表面展平软件分析,没有查阅相关文献,目前有Freesurfer软件用作大脑皮层面积展平分析的。
一般用成人简单的方法身高+体重—60/100。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
泰索帝(多西他赛注射液)
【药品名称】
商品名称:泰索帝
通用名称:多西他赛注射液
英文名称:Docetaxel Injection
【成份】
本品主要成份为多西他赛。
【适应症】
1、多西他赛适用于先期化疗失败的晚期或转移性乳腺癌的治疗。
除非属于临床禁忌,先期治疗应包括蒽环类抗癌药
【用法用量】
多西他赛只能用于静脉滴注。
所有病人在接受多西他赛治疗期前均必须口服糖皮质激素类,如地塞米松,在多西他赛滴注一天前服用。
每天16mg,持续至少3天,以预防过敏反应和体液潴留。
临用前将多西他赛所对应的溶剂全部吸入对应的溶液中,轻轻摇混合均匀,将混合后的药瓶室温放置5分钟,然后检查溶液是否均匀澄明,根据计算病人的所用药量,用注射器吸入混合液,注入5%葡萄糖注射液或0.9%氯化钠注射液的注射瓶或注射袋中,轻轻摇动,混合均匀,最终浓度不超过0.9mg/ml。
多西人赛的推荐剂量为75mg/m2 滴注一小时,每三周一次
【不良反应】
1.骨髓抑制:中性粒细胞减少是最常见的副反应而且通常较严重(低于500个/mm3)。
可逆转且不蓄积。
2、过敏反应:部分病例可发生严重过敏反应,其特征为低血压与支气管痉挛,需要中
断治疗。
停止滴注并立即治疗后病人可恢复正常。
部分病例也可发生轻度过敏反应。
如脸红,伴有或不伴有搔痒的的红斑,胸闷,背痛,呼吸困难,药物热或寒战。
3、皮肤反应常表现为红斑,主要见于手、足,也可发生在臂部,脸部及胸部的局部皮疹,有时伴有搔痒。
皮疹通常可能在滴注多西他赛后一周内发生,但可在下次滴注前恢复。
严重症状如皮疹后出现脱皮则极少发生。
可能会发生指(趾)甲病变。
以色素沉着或变淡为特点,有时发生疼痛和指甲脱落。
4.体液潴留包括水肿,也有报道极少病例发生胸腔积液,腹水,心包积液,毛细血管通透性增加以及体重增加。
经过4周期治疗或累积剂量400mg/m2后,下肢发生液体潴留,并可能发展至全身水肿,同时体重增加3公斤或3公斤以上。
在停止多西他赛治疗后,液体潴留逐渐消失。
为了减少液体潴留,应给病人预防性使用皮质类固醇。
5.可能发生恶心、呕吐或腹泻等胃肠道反应。
6.临床试验中曾有神经毒性的报道。
7.心血管副反应如低血压、窦性心动过速、心悸、肺水肿及高血压等有可能发生。
8.其它副反应包括:脱发、无力、黏膜炎、关节痛和肌肉痛,低血压和注射部位反应。
9.肝功能正常者在治疗期间也有出现氨基转移酶升高、胆红素升高者,其与多西他赛的关系尚不明确。
【禁忌】
以下患者禁用:
1.对多西他赛或吐温-80有严重过敏史的病人。
2.白细胞数目小于1500个/mm3的病人。
3.肝功能有严重损害的病人。
【注意事项】
1、多西他赛必须在有癌症化疗药物应用经验的医生指导下使用。
由于可能发生较严重的过敏反应,应具备相应的急救设施,注射期间建议密切监测主要功能指标。
2.在肝功能异常患者、使用本品高剂量治疗患者和既往接受铂类药物治疗的非小细胞肺癌患者,使用多西他赛剂量达100mg/m2时,与治疗相关的死亡的发生率会增加。
3.所有病人在接受多西他赛治疗前需预服药物以减轻体液潴留的发生,预服药物只包括糖皮质激素类,如地塞米松,在多西他赛注射头一天开始服用,每日16mg,服用4~5天。
4.中性粒细胞减少是最常见的副反应。
多西他赛治疗期间应经常对白细胞数目进行监测。
当病人中性粒细胞数目恢复至>1500个/mm3以上时才能接受多西他赛的治疗,多西他赛治疗期间如果发生严重的中性粒细胞减少(
【药物相互作用】
体外研究表明CYP3A4抑制剂可能干扰本品的代谢,因此当与此类药物(如酮康唑、红霉素、环孢素等)同时应用时应格外小心。
【药理作用】
本品的作用机制是加强微管蛋白聚合作用和抑制微管解聚作用,导致形成稳定的非功能性微管束,因而破坏肿瘤细胞的有丝分裂。
本品在细胞内浓度比紫杉醇高3倍,并在细胞内滞留时间长,这是本品在体外试验中比紫杉醇抗肿瘤活性大的重要原因。
在体内试验中,对小鼠的结肠癌、乳腺癌、肺癌、卵巢肿瘤移植物等有效。
对顺铂、足叶乙苷、5Fu、或紫杉醇耐药的细胞株,本品不产生交叉耐药
【贮藏】
遮光、密闭,在2-8℃贮存。
【批准文号】
H20090646。
