MW03耐热大肠菌群检测滤膜法原始记录表
微生物检测原始记录文本

XXXX检测有限公司
菌落总数与大肠菌群检验原始记录
共页第页主检:
菌落总数和大肠菌群检测原始记录
共页第页
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
水质微生物检验原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
乳酸菌与大肠菌群检测记录
共页第页主检:
XXXX检测有限公司
致病菌检验原始记录
共页第页
XXXX 检测有限公司 主检:
年 月 日 校核:
主检: 年 月 日 校核: 年 月 日
XXXX 检测有限公司
霉菌和酵母菌检验原始记录
菌落计数:
商业无菌检验原始记录
共页第页
XXXX检测有限公司
主检日期校核日期。
大肠菌群原始记录2003
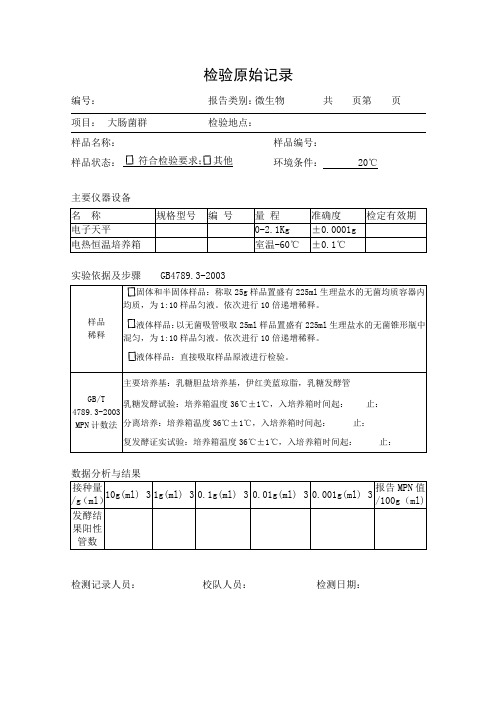
检验原始记录
编号:
报告类别: 微生物 共 页第 页 项目: 大肠菌群 检验地点:
样品名称: 样品编号: 样品状态:
符合检验要求; 其他 环境条件: 20℃
主要仪器设备
名 称
规格型号 编 号 量 程 准确度 检定有效期 电子天平
0-2.1Kg ±0.0001g 电热恒温培养箱
室温-60℃ ±0.1℃
实验依据及步骤 GB4789.3-2003 样品
稀释 固体和半固体样品:称取25g 样品置盛有225ml 生理盐水的无菌均质容器内均质,为1:10样品匀液。
依次进行10倍递增稀释。
液体样品:以无菌吸管吸取25ml 样品置盛有225ml 生理盐水的无菌锥形瓶中混匀,为1:10样品匀液。
依次进行10倍递增稀释。
液体样品:直接吸取样品原液进行检验。
GB/T 4789.3-2003
MPN 计数法 主要培养基:乳糖胆盐培养基,伊红美蓝琼脂,乳糖发酵管
乳糖发酵试验:培养箱温度36℃±1℃,入培养箱时间起: 止: 分离培养:培养箱温度36℃±1℃,入培养箱时间起: 止:
复发酵证实试验:培养箱温度36℃±1℃,入培养箱时间起: 止:
数据分析与结果
接种量/g (ml ) 10g(ml)×3 1g(ml)×3 0.1g(ml)×3 0.01g(ml)×3 0.001g(ml)×3 报告MPN 值/100g (ml) 发酵结
果阳性管数
检测记录人员:
校队人员: 检测日期:。
微生物检测原始记录

菌落总数与大肠菌群检验原始记录
主检:年月日校核:年月日
菌落总数和大肠菌群检测原始记录
主检:年月日校核:年月日
水质微生物检验原始记录
主检:年月日校核:年月日
乳酸菌与大肠菌群检测记录
主检:年月日校核:年月日
致病菌检验原始记录
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
菌落计数:
培养温度:28±1℃培养时间:年月日时--- 年月日时
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:。
大肠菌群检测原始记录

发酵试验
阳性管数
报出值 MPN/ml
LST肉汤管初 BGLG肉汤管复
发酵试验
发酵试验
阳性管数
报出值 MPN/ml
LST肉汤管初 BGLG肉汤管复
发酵试验
发酵试验
阳性管数
报出值 MPN/ml
审核:
年月
日
编号: 样品名称:
检验依据:GB/T4789.3-2016 培养开始时间: 年 月 培养结束时间: 年 月
稀பைடு நூலகம்度
1
稀释度
项目 管号
1 2 3 1 2 3 1 2 3
项目 管号
2
稀释度
3
稀释度
4
稀释度
1 2 3 1 2 3 1 2 3
项目 管号
1 2 3 1 2 3 1 2 3
项目 管号
1 2 3 1 2 3 1 2 3
项目 管号
1
2
3
5
1
2
3
1
2
3
检验员:
大肠菌群检测原始记录
批次:
日时
日时
LST肉汤管初 BGLG肉汤管复
发酵试验
发酵试验
恒温时间: h 恒温温度:36℃±1℃
阳性管数
报出值 MPN/ml
LST肉汤管初 BGLG肉汤管复
发酵试验
发酵试验
阳性管数
报出值 MPN/ml
LST肉汤管初 BGLG肉汤管复
发酵试验
大肠菌群检验原始记录

初发酵(月桂基硫酸盐胰蛋白胨肉汤,)支)
产气管数(支)
复发酵(煌绿乳糖胆盐
肉汤,
37℃,,48h)
产气管数(支)
10-1
10-2
10-3
检验结果
(MPN/100g)
检验人:复核人:
大肠菌群检验检验原始记录
样品名称
明胶
样品编号
样品状态
生产日期
检验依据
GB4789.3-2010
检验日期
大肠菌群检验过程:
1、称取样品25g样品放入盛有225ml灭菌的生理盐水中,制成1:10的样品匀液,用1ml无菌吸管吸取1:10的样品匀液1ml,沿管壁缓缓注入盛有9ml生理盐水的无菌试管中,制成1:100的样品均液,用1ml无菌吸管吸取1:100的样品匀液1ml,沿管壁缓缓注入盛有9ml生理盐水的无菌试管中,制成1:1000的样品均液。
2、初发酵试验:大肠菌群每个样品,选择3个适宜的连续稀释度的样品匀液,每个稀释度接种3管月桂基硫酸盐胰蛋白胨(LST)肉汤(大肠菌群测定:如果超过1ml,则用双料LST肉汤),36℃±1℃培养24h±2h,观察倒管内产气情况。如未产气,培养至48h±2h,如产气着进行复发酵试验。
三、复发酵试验:(大肠菌群的测定)用接种环从产气的LST肉汤管中分别取培养物1环,移种于煌绿糖胆盐肉汤(BGLB)管中,36℃±1℃培养48h±2h,,观察产气情况。
菌落总数、大肠菌群检验原始记录
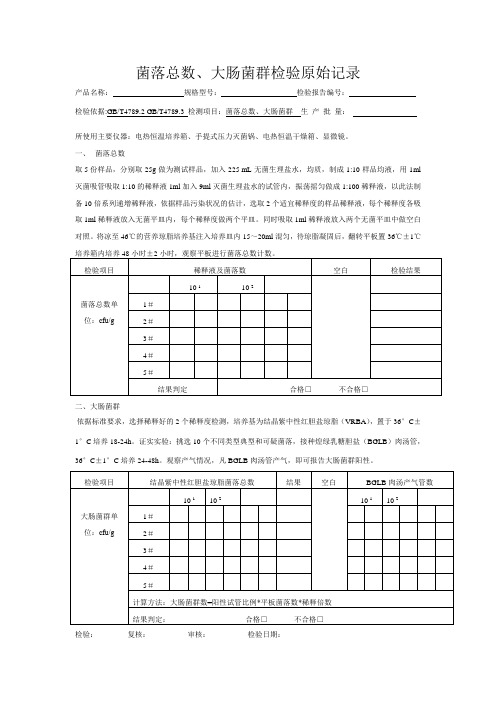
菌落总数、大肠菌群检验原始记录
产品名称:规格型号:检验报告编号:
检验依据:GB/T4789.2 GB/T4789.3 检测项目:菌落总数、大肠菌群生产批量:
所使用主要仪器:电热恒温培养箱、手提式压力灭菌锅、电热恒温干燥箱、显微镜。
一、菌落总数
取 5 份样品,分别取25g做为测试样品,加入225 mL无菌生理盐水,均质,制成1:10样品均液,用1ml 灭菌吸管吸取1:10的稀释液1ml加入9ml灭菌生理盐水的试管内,振荡摇匀做成1:100稀释液,以此法制备10倍系列递增稀释液,依据样品污染状况的估计,选取2个适宜稀释度的样品稀释液,每个稀释度各吸取1ml稀释液放入无菌平皿内,每个稀释度做两个平皿。
同时吸取1ml稀释液放入两个无菌平皿中做空白对照。
将凉至46℃的营养琼脂培养基注入培养皿内15~20ml混匀,待琼脂凝固后,翻转平板置36℃±1℃
二、大肠菌群
依据标准要求,选择稀释好的2个稀释度检测,培养基为结晶紫中性红胆盐琼脂(VRBA),置于36°C±1°C培养18-24h。
证实实验:挑选10个不同类型典型和可疑菌落,接种煌绿乳糖胆盐(BGLB)肉汤管,36°C±1°C培养24-48h。
观察产气情况,凡BGLB肉汤管产气,即可报告大肠菌群阳性。
检验:复核:审核:检验日期:。
大肠菌群检验原始记录表

从VRBA平板上挑取10个不同类型的典型和可疑菌落,分别移种于BGLB肉汤管内,36℃±1℃培养24-48h,观察产气情况
。凡是BGLB肉汤管产气,即可报告为大肠菌群阳性。
操作依据
GB4789.3-2010
稀释倍数
a-10倍
b-100倍
c灭菌生理盐水对照
/6.1
VRBA平板
操作依据 GB4789.3-2010
检验日期:
2016 年 月 日
采样依据 GB4789.12010/4.1、 4.2.1二级 采样方案 (n、c、m值 5、0、0)
10的均匀稀释液,编号a 灭菌生理盐水,编号c做
、b2、c1。向上述5个平 ,依次置于36℃±1℃培
养24-48h,观察产气情况
操作依据 B4789.3-2010
/6.1 操作依据 B4789.3-2010
/8.2 操作依据 B4789.3-2010
/8.3
实试验及观察结果 依据
B4789.3-2010 /8.4
肠菌群数的计算 据GB4789.3-2010
/8.5 数据修约依据 789.来自-2010/7.2报告依据 B4789.3-2010
/8.5
培养基)
年月日
。用灭菌吸管取1mla,加入9ml灭菌生理盐水中,混合均匀做成1:100的均匀稀释液,编号b。取1ml灭菌生理盐水,编号c做
为空白对照。
从a、b、c液中,分别前后2次,各吸取1ml移液到2个灭菌平皿中,平皿编号分别为a1、a2、b1、b2、c1。向上述5个平
皿中分别注入凉至46℃的VRBA15ml,混匀待VRBA凝固后,再加3mlVRBA覆盖平板表层,翻转平板后,依次置于36℃±1℃培 养箱中,培养20h。
微生物检验原始记录(大肠菌群)

编号:
报告类别:
微生物
共页
项目:
大肠菌群coliforms
检验地点:
样品名称:
样品编号:
样品状态:
符合检验要求; 其他
环境条件:
实验依据及步骤
GB4789.3-2016
样品稀释
固体和半固体样品:称取25g样品置盛有225ml生理盐水或磷酸盐缓冲液的无菌均质容器内均质,或放入盛有225ml稀释液的无菌均质袋中拍击式均质器拍打,制成为1:10样品匀液。依次进行10倍递增稀释。
M:微生物指标的最高安全限量值
2.例:n=5,c=2,m=1cfu/g,M=10cfu/g,即从一批产品中采集5个样品,
若5个样品的检测结果均小于或等于m值(≤1cfu/g),则这种情况是允许的;
若≤2个样品的结果(X)位于m值和M值之间(1cfu/g≤X≤10cfu/g),则这种情况也是允许的;
若有3个及以上样品的检验结果位于m和M之间,则这种情况是不允许的;
MPN检索表
(CFU/ml)
n=5 c=2 m=1
1
2
3
4
5
1
2
3
4
5
1
2
3
4
5
1
2
3
4
5
1
2
3
4
5
数据分析与结果
一、菌落计数
根据证实为大肠菌群的阳性管数,查MPN检索表,报告大肠菌群的最可能数。
二、缓冲液
1.磷酸盐缓冲液
磷酸二氢钾 34.0g 蒸馏水500ml (稀释液需要1000ml)
贮存液:将34.0g磷酸二氢钾溶于500ml蒸馏水中,用大约175ml的1mol/l氢氧化钠溶液调节ph至7.2,用蒸馏水稀释至1000ml后贮存冰箱。
大肠菌群计数(法一)原始记录

大肠菌群计数(法一)原始记录
第页共页
样品编号:环境温湿度:℃ %RH
检验依据:GB 4789.3-2016 检测地点:微生物室
检验日期:检毕日期:
培养开始时间:培养终止时间:
仪器设备:培养箱ZYXYJC/S- □天平ZYXYJC/S-
□pH计ZYXYJC/S-
检测过程:以无菌操作取样品□g或□mL,用□生理盐水或□磷酸盐缓冲液制成10倍梯度稀释液。
选择3个适宜连续稀释度的样品匀液(液体样品可包括原液),
每个稀释度接种3管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管接种1mL(如接种
量超过1mL,则用双料LST肉汤),36℃培养h进行初发酵试验,未产气
者为大肠菌群阴性,产气者进行复发酵试验。
用接种环从产气试管中取培养物1
环,移种于BGLB内,36℃培养h,根据复发酵产气试管数查MPN表,
上报结果。
微生物检测原始记录

菌落总数与大肠菌群检验原始记录
主检:年月日校核:年月日
菌落总数和大肠菌群检测原始记录
主检:年月日校核:年月日
水质微生物检验原始记录
主检:年月日校核:年月日
乳酸菌与大肠菌群检测记录
主检:年月日校核:年月日
致病菌检验原始记录
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
菌落计数:
培养温度:28±1℃培养时间:年月日时--- 年月日时
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:。
化妆品耐热大肠菌群检测原始记录
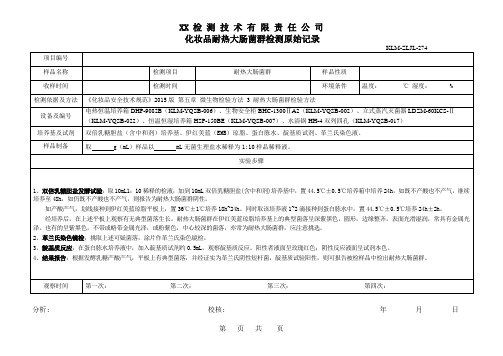
3、靛基质反应:在蛋白胨水培养液中,加入靛基质试剂约0.5mL,观察靛基质反应。阳性者液面呈玫瑰红色;阴性反应液面呈试剂本色。
4、结果报告:根据发酵乳糖产酸产气,平板上有典型菌落,并经证实为革兰氏阴性短杆菌,靛基质试验阳性,则可报告被检样品二次:第三次:第四次:
样 品 编 号
双倍乳糖胆盐发酵试验结果
革兰氏染色镜检
靛基质反应
检测结果
注:G+表示该菌为革兰氏阳性者,G-表示该菌为革兰氏阴性,+ 表示阳性,- 表示阴性。
备注:
项目编号
样品名称
检测项目
耐热大肠菌群
样品性质
收样时间
检测时间
环境条件
温度: ℃ 湿度: %
检测依据及方法
《化妆品安全技术规范》2015版 第五章 微生物检验方法 3 耐热大肠菌群检验方法
设备及编号
电热恒温培养箱DHP-9082B(KLM-YQSB-006)、生物安全柜BHC-1300ⅡA2(KLM-YQSB-002)、立式蒸汽灭菌器LDZM-60KCS-Ⅱ(KLM-YQSB-022)、恒温恒湿培养箱HSP-150BE(KLM-YQSB-007)、水浴锅HH-4双列四孔(KLM-YQSB-017)
培养基及试剂
双倍乳糖胆盐(含中和剂)培养基、伊红美蓝(EMB)琼脂、蛋白胨水、靛基质试剂、革兰氏染色液、
样品制备
取g(mL)样品以mL无菌生理盐水稀释为1:10样品稀释液。
实验步骤
1、双倍乳糖胆盐发酵试验:取10mL1:10稀释的检液,加到10mL双倍乳糖胆盐(含中和剂)培养基中,置44.5℃±0.5℃培养箱中培养24h,如既不产酸也不产气,继续培养至48h,如仍既不产酸也不产气,则报告为耐热大肠菌群阴性。
总大肠菌群检验原始记录
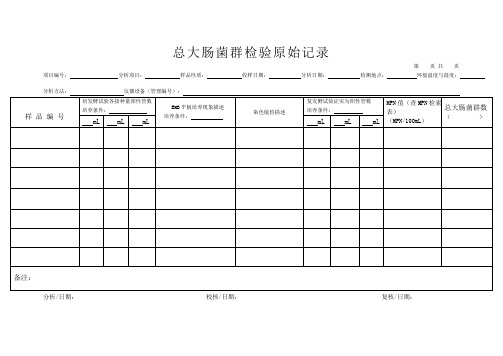
MPN值(查MPN检索表)
(MPN/100mL)
总大肠菌群数( )
mL
mL
mL
mL
mL
mL
备注:
分析/日期: 校核/日期: 复核/日期:
总大肠菌群数( )
mL
mL
mL
mL
mL
mL
备注:
分析/日期: 校核/日期: 复核/日期:
总大肠菌群检验原始记录(续表)
第 页 共 页
项目编号:分析项目:样品性质:收样日期:分析日期:
样 品 编 号
初发酵试验各接种量阳性管数
培养条件:
EMB平板培养现象描述
培养条件:
染色镜检描述
复发酵试验证实为阳性管数
总大肠菌群检验原始记录
第 页 共 页
项目编号:分析项目:样品性质:收样日期:分析日期:检测地点:环境温度与湿度:
分析方法:仪器设备(管理编号):
样 品 编 号
初发酵试验各接种量阳性管数
培养条件:
EMB平板培养现象描述
培养条件:
染色镜检描述
复发酵试验证实为阳性管数
培养条件:
MPN值(查MPN检索表)
(MPN/100mL)ቤተ መጻሕፍቲ ባይዱ
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
备注
①管网水
②管网水
③管网水
④管网水
⑤管网水
⑥管网水
⑦管网水
⑧管网水
江北水厂出厂水
江北水厂滤后水
江北水厂滤前水
河南岸水厂出厂水
桥东水厂出厂水
检验人:审核人:
惠州市水质检测综合有限公司
耐热大肠菌群滤膜法检测原始记录
HSZ/MW03 201310
检测方法平板法环境条件温度℃湿度%RH采样日期
年月日
培养温度、时间
温度℃时间h
检测日期
年月日
报告日期
年月日
培养基名称
培养基编号
培养基配制日期
有效期至
检测结果
样品编号
样品体积(mL)
耐热大肠菌群特征菌落数(个)
接种EC培养基培养
