人教版高中化学必修二第二节元素周期律课件1
化学:1.1《元素周期表》PPT课件(新人教版-必修2)

1869年2月 门捷列夫(俄)的第一张周期表
1871年
门捷列夫(俄)的第二张周期表
一、元素周期表编排原则:
1、把电子层数相同的元素按原 子序数递增的顺序由左到右排 成一个横行。 2、把不同横行中最外层电子数 相同的元素按电子层数递增的顺 序由上到下排成纵行。
二、元素周期表的结构: 1、周期:
难易程度。置换出氢越容易,则金属性越强。
2、根据金属元素最高价氧化物对应水化物碱性 强弱。碱性越强,则原金属元素的金属性越强。
已知NaOH为强碱、Mg(OH)2为中 强碱、 Al(OH)3为两性氢氧化物, 则Na、Mg、Al的金属性强弱顺序 如何?
金属性
Na〉Mg〉Al
元素金属性强弱判断依据:
1、根据金属单质与水或者与酸反应置换出氢的
牢记短周期元素:
熟记主族元素和0族元素:
Li 3锂 Na 11钠 K 19钾 Rb 37铷 Cs 55铯
它们的性质具有哪些相似 点?又有什么样的不同呢?
碱金属元素单质:
Rb
三、元素的性质与原子结构
1、碱金属元素
(1)碱金属的原子结构
【自主学习】 教材第5页“科学探究”,填写第5页表 格
思考与交流
碱金属元素的用途:
1.锂电池是一种高能电池。 锂有机化学中重要的催化剂。 锂制造氢弹不可缺少的材料。 锂是优质的高能燃料(已经 用于宇宙飞船、人造卫星和 超声速飞机)。 2.钾的化合物最大用途是做钾肥。 硝酸钾还用于做火药。 3.铷铯主要用于制备光电管、 真空管。铯原子钟是目前最准确的 计时仪器。
根据实验讨论钠与钾的性质有 什么相似性和不同性。你认为元素 的性质与他们的原子结构有关系吗? 其余碱金属的性质又如何?
钠与钾都能与氧气、水发生 反应,但反应的剧烈程度不同
元素周期律(原子半径、电离能、电负性)课件高二化学人教版(2019)选择性必修2

(金属性越强,单质还原性越强,对应阳离子氧化性越弱)
3.主族元素原子半径的周期性变化 左大下大
同主族
原 子
能层
半
占主导
径 增
大
同周期:左大 同主族:下大
原子半径增大
影响因素及结果: 1.电子的能层越多, 电子之间的排斥作用 越大,将使原子的半 径增大。 2.核电荷数越大,核 对电子的吸引作用也 就越大,将使原子的 半径减小。
注意:这两种作用是
同时存在,相互竞争
的关系。
同周期 核电荷数 占主导
知识拓展 常见简单微粒半径比较的方法和规律: 不同 原子 同周期 左大 r(Na)>r(Mg)>r(Al)>r(Si)>r(P)>r(S)>r(Cl)
同主族 下大 Cs>Rb>K>Na>Li>H
元 素
离子
电子层不同
层多径大
①r(K+)>r(Mg2+) ②r(Cl-)>r(Na+)
4.电负性的应用:
2)判断化学键的类型
通常
电负性相差很大(相差>1.7)
离子键
电负性相差不大(相差<1.7) 通常 共价键
电负性递变规律:
电负性 0.9
3.0
电负性差 2.1
离子化合物
特例:NaH、 CaS 为离子化合物;
思考: 电负性的差: 化学键类型:
AlCl3(BeCl3)
1.5 共价
电负性 2.1 3.0 电负性差 0.9
第一电离能(kJ·mol-1)
全充满,较稳定
半充满,较稳定
2s22p3 2s2
纵列序数 族序数
价电子排布式 最外层电子数
人教版高中化学必修二课件:1.1《元素周期表》(共37张PPT)

2KI+Br2 = I2+2KBr 静置后,液体分层, 氧化性: Br2 > I2
上层 无色 ,
下层 紫色 。
结论
氧化性:Cl2 > Br2 > I2 还原性:I - > Br - > Cl 小结: 氧化性:F2> Cl2> Br2>I2 还原性:F-> Cl- > Br- > I-
氧化性:F2> Cl2> Br2>I2。 Cl2可从溴、碘的盐 溶液中置换出相应的卤素单质,F2与氯、溴、 碘的盐溶液可以置换出相应的卤素单质吗?
H2+F2 = 2HF H2+Cl2 = 2HCl 暗处剧烈反应并爆炸;HF很稳定 光照或点燃反应;HCl较稳定
H2+Br2 = 2HBr
H2+I2
加热500℃ ,HBr不稳定
2HI 需不断加热,HI同时分解
■都能跟氢气反应,体现相似性 反应通式:H2 + X2 = 2HX (X= F、Cl、Br、I) ■单质氧化性减弱,体现递变性
① 除9、10、18纵行(列序)外,族序数=列序个位数。(记忆方法) ②18个纵行,只16个族;0族和第VIII族不属主族,也不属副族。
一、碱金属元素结构和化学性质的相似性和递变性
Li Na K Rb Cs
1.相似性:
最外层上都只 有一个电子 2.递变性: 核电荷数↑ 电子层数↑ 原子半径↑ 失电子能力↑ 化学性 质相似
3.请在下面的线框中用色笔画出周期表的轮廓。并标出族序数,写
出七个主族元素(可参考课本)和 0族元素的元素符号。
周期 ⅠA ⅡA ⅢB ⅣB ⅤB ⅥB VIIB
IB IIB ⅢA ⅣA ⅤA Ⅵ AⅦA 0 种类
人教版高中化学必修二《元素周期律》课件

2.化合价指的是一定数目的一种元素的原子与一定 数目的其他元素的原子化合的性质,元素化合价的数值与 原子的电子层结构,特别是最外层电子数有关。例如,稀 有气体原子核外电子排布已达稳定结构,既不易得到电子 也不易失去电子,所以稀有气体元素的常见化合价为0。 镁原子最外层只有2个电子,容易失去这两个电子而达到 稳定结构,因此镁元素在化合物中通常显+2价;氯原子 最外层有7个电子,只需得到1个电子便可达到稳定结构, 因此氯元素在化合物中可显-1价。
原子的核外电子排布,特别是最外层电子数决定着元 素的主要化学性质。从初中所学知识我们知道,金属元素 的原子最外层电子数一般少于4个,在化学反应中比较容 易失去电子,达到相对稳定结构;而非金属元素的最外层 一般多于4个电子,在化学反应中易得到电子而达到8个电 子的相对稳定结构。原子得到或失去电子后的阴、阳离子 也可用结构示意图来表示。
层,弧形上的数字表示该层的电子数。
二、元素性质与原子核外电子排布的关系 1.最外层电子数排满8个(He为2个)形成稳定结构, 不易得失电子,化学性质稳定。
最外层电子较少的(<4)易失去电子,达到稳定结构, 表现出金属性;最外层电子较多的(>4)易得电子或形成共 用电子对,从而形成稳定结构,表现出非金属性。通常, 我们把最外层8个电子(只有K层时为2个电子)的结构,称 为相对稳定结构,一般不与其他物质发生化学反应。当元 素原子的最外层电子数小于8(K层小于2)时,是不稳定结 构。在化学反应中,具有不稳定结构的原子,总是“想方 设法”通过各种方式使自己的结构趋向于稳定结构。
3.画出下列微粒的结构示意图 C________ O________ Al3+________ Si________ Cl-________ Ar________ K________ Ca________
高中化学必修二第一章第二节第一课时元素周期律

须 加 热
光照或 点燃爆 炸化合
Mg(OH)2 Al(OH)3 H4SiO4 H3PO4 H2SO4 HClO4
强碱
中强碱 两性氢 弱酸 氧化物
中强 酸
强酸
最强 酸
稀 有 气 体 元 素
金属性逐渐减弱,非金属性逐渐增强
随着原子序数的递增 元素原子的核外电子排布呈现周期性变化 元素原子半径呈现周期性变化 元素化合价呈现周期性变化 元素的化学性质呈现周期性变化
(2)最外层电子数不超过8个电子(K 为最外层时不超过2个) ; (3)次外层电子数不超过18个电子; 倒数第三层电子数不超过32个电子; (4)核外电子总是尽先排布在能量较 低的电子层,然后由里向外,依次排布 在能量逐步升高的电子层(能量最低原 理)。
练习:
1、判断下列示意图是否正确?为什么? A、 B、 +12 2 10
氟里昂的发现与元素周期表
米奇利还分析了其它的一些规律, 最终,一种全新的致冷剂CCl2F2终 于应运而生了。 80年代,科学家们发现氟里昂会破 坏大气的臭氧层,危害人类的健康 的气候,逐步将被淘汰。人们又将 在元素周期表的指导下去寻找新一 代的致冷剂。
例1.下列递变情况不正确的是: C
A. Na、Mg、Al最外层电子数依 次增多,其单质的还原性依次减弱 B. P、S、Cl最高正价依次升高, 对应气态氢化物稳定性增强 C. C、N、O原子半径依次增大 D. Na、K、Rb氧化物的水化物碱 性依次增强
2Al + 6HCl = 2AlCl3 + 3H2
Mg + 2HCl = MgCl2 + H2 2Al + 6HCl = 2AlCl3 + 3H2
元素周期律PPT课件37 人教课标版

例如:比较K+、Mg 2+、Na+的离子半径大小
r(K+)>r(Na+)>r(Mg 2+)
变式训练3 下列微粒半径大小比较正确的是
( B)
A.Na+<Mg2+<Al3+<O2- B.S2->Cl->Na+>Al3+ C.Na< Na+ D.Cs<Rb<K<Na
强酸 (比H2SO4强)
(2)Si、P、S、Cl非金属性强弱的比较。
Cl、S、P、Si
HClO4>H2SO4>H3PO4>H2SiO3
Cl>S>P>Si
总结:同周期元素性质的递变规律(自左至右)。
元素的金属性_____减,非弱金属性_____。 增 强
元素周期表中的递变规律
同周期(从左至右) 同主族(从上至下)
2.不同电子层的表示及能量关系
(1)原子是由___原__子__核___和__核__外__电__子____构成的
各电 子层 (由 内到 外)
序号(n) 1 2 3 4 5 6 7
符号 __K__ __L_ _M__ _N__ O P Q
与原子核 的距离
___由__近__到__远__
能量
_____由__低__到__高___
5.核外电子排布的表示方法
Cl + 1 7 2 8 7
核电荷数
最外层电子数
核外电子数 电子层
X是什么元素?
Br
1、画出Li、K的原子结构示意图。 2、画出K+、 Cl-的离子结构示意图。
微粒符号 H2O NH4+
质子数 10 11
电子数 10 10
人教版高中化学必修2原子的核外电子排布课件

P
+15
2 85
2021/2/4
19
第二关:画图
画出下列微粒的结构示意图。
19K 35Br 53I S2- K+
2021/2/4
20
第三关:元素推断
最外层电子数是电子层数2倍的短周期元素是:
He、C、S
内层电子数是最外层电子数2倍的元素是:
Li、P
某短周期元素的核电荷数是电子层数的5倍,其
具体示例
Mg2+ Cl-
2021/2/4
17
过关斩将
第一关 下列粒子的结构示意图正确的是( ⑦)
①Li
②Na
③Na+
④Cl
⑤Cl-
⑥K
⑦Ca2+
2021/2/4
⑧Xe
18
第三关:元素推断
最外层电子数是电子层数2倍的元素是:
He、C、S、Kr
内层电子数是最外层电子数2倍的元素是:
Li、P
某元素的核电荷数是电子层数的5倍,其质子数是最外 层电子数的3倍,该元素的原子结构示意图为
自主学习任务一
请画出元素周期表中1-18号元素原子的结 构示意图
2021/2/4
11
H
He
Li
Be
B
C
N
O
F
Ne
Na
Mg
Al
Si
P
S
Cl
Ar
2021/2/4
12
自主学习任务二
观察稀有气体原子的核外电子的排布,你 发现了什么?
2021/2/4
13
自主学习任务二 稀有气体元素原子电子层排布
核电 元素 元素
英国物理学家 汤姆生 J.J.Thomson,1856~1940
山西省运城中学高中化学人教版必修2备课资料第一章第二节 元素周期律(课件+教案+学案,9份)元素周期
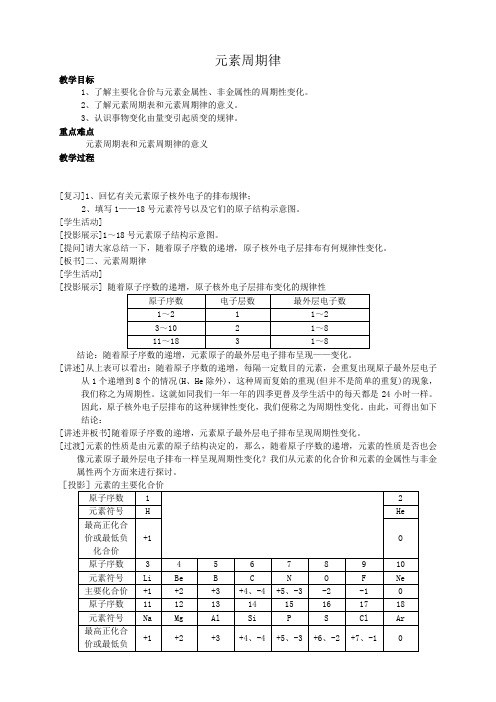
元素周期律教学目标1、了解主要化合价与元素金属性、非金属性的周期性变化。
2、了解元素周期表和元素周期律的意义。
3、认识事物变化由量变引起质变的规律。
重点难点元素周期表和元素周期律的意义 教学过程[复习]1、回忆有关元素原子核外电子的排布规律;2、填写1——18号元素符号以及它们的原子结构示意图。
[学生活动][投影展示]1~18号元素原子结构示意图。
[提问]请大家总结一下,随着原子序数的递增,原子核外电子层排布有何规律性变化。
[板书]二、元素周期律 [学生活动][投影展示] 随着原子序数的递增,原子核外电子层排布变化的规律性[讲述]从上表可以看出:随着原子序数的递增,每隔一定数目的元素,会重复出现原子最外层电子从1个递增到8个的情况(H 、He 除外),这种周而复始的重现(但并不是简单的重复)的现象,我们称之为周期性。
这就如同我们一年一年的四季更替及学生活中的每天都是24小时一样。
因此,原子核外电子层排布的这种规律性变化,我们便称之为周期性变化。
由此,可得出如下[讲述并板书][过渡]元素的性质是由元素的原子结构决定的,那么,随着原子序数的递增,元素的性质是否也会像元素原子最外层电子排布一样呈现周期性变化?我们从元素的化合价和元素的金属性与非金学反应,因此,把它们的化合价看作0。
[学生]原子序数为1~2时,化合价从+1下降到0;原子序数为3~9时,随着原子序数的递增,最高正价从+1到+5,最低负价从-4到-1;原子序数为11~17时,随着原子序数的递增,最高正价从+1到+7,最低负价从-4到-1。
稀有气体元素的化合价均为0。
[教师]很好!那么,能不能由此说明:随着原子序数的递增,元素的化合价也呈周期性变化呢?[过渡]下面我们通过第三周期元素的一些化学性质来探讨元素的金属性与非金属性有何变化。
[提问]假如我们要用实验来验证这个结论,又应从哪些方面着手呢?[学生回答,教教师板书]1.单质跟水(或酸)2.最高价氧化物的水化物——1.2.[教师]一般,对于金属元素我们主要研究其金属性,对于非金属元素我们主要研究其非金属性。
新教材人教版高中化学选择性必修2课件-元素周期律

738 kJ·mol-1
(2)第一电离能介于 B、N 之间的第二周期元素有___3_____种。依 据第二周期元素第一电离能的变化规律,参照图中 B、F 元素的位置, 用小黑点标出 C、N、O 三种元素的相对位置。
(3)如图是周期表中短周期的一部分,A 的单质是空气中含量最多 的物质,其中第一电离能最小的元素是___D_____(填“A”“B”“C” 或“D”)。
解析:从电子排布式可以看出①是 S,②是 P,③是 N,④是 F,第 一电离能:F>N>P>S;原子半径:P>S>N>F;电负性:F>N>S>P;最高 正化合价:S>N=P,F 无正价。
答案:A技能素养 提升点一 微粒半径大 Nhomakorabea规律应用
[例 1] 下列关于粒子半径大小的关系判断不正确的是( ) ①r(Li+)<r(Na+)<r(K+)<r(Rb+)<r(Cs+) ②r(F)<r(Cl)<r(Br)<r(I) ③r(Na+)<r(Mg2+)<r(Al3+)<r(F-)<r(O2-) ④r(Fe2+)<r(Fe3+)<r(Fe)
二、电离能
1.概念 气__态__电__中__性__基__态_原子失去一个电子转化为气态基态正离子所需要 的最__低__能__量_叫做第一电离能。 2.元素第一电离能的意义 衡量元素的原子失去一个电子的难易程度。第一电离能数值 ___越__小___,原子越容易失去一个电子。 3.元素第一电离能的变化规律 (1) 同 周 期 元 素 随 着 原 子 序 数 的 递 增 , 元 素 的 第 一 电 离 能 呈 现 逐__渐__增__大__的趋势。 (2)同族元素从上到下第一电离能逐渐__变__小____。
____M__g_、__A_l_位__于__同__一__周__期__,__M__g_最__外__层__电__子__排__布__式__为__3_s_2,__而___A_l_最。外层
高中新教材人教版化学课件+选择性必修2+第一章第2节+第1课时 原子结构与元素周期表

自主预习·新知导学
原子结构与元素周期表 1.元素周期律、元素周期系和元素周期表 (1)元素周期律的含义:元素的性质随元素原子的核电荷数递增发生周期性 递变。 (2)元素周期系:元素的这一按其原子核电荷数递增排列的序列称为元素周 期系。 (3)元素周期系与元素周期表的关系: ①元素周期表是呈现元素周期系的表格。 ②元素周期系只有一个,元素周期表多种多样。
金属 金属
合作探究·释疑解惑
探究任务1 价层电子排布与元素周期表中周期与族的划分
【问题引领】
请你阅读分析下列元素周期表并回答问题:
1.元素周期表中周期的划分与构造原理有何联系?每个周期各排了多少种 元素? 提示:除第一周期外,其余各周期总是从ns能级开始,以np能级结束,而从ns 能级开始以np能级结束递增的核电荷数就等于每个周期里的元素数。因 为第一周期元素只有一个1s能级,其结尾元素的电子排布式为1s2,跟其他周 期的结尾元素的电子排布式不同。7个周期,每个周期包括的元素数目分 别为:第一周期2种;第二周期8种;第三周期8种;第四周期18种;第五周期18 种;第六周期32种;第七周期32种。 2.元素周期表共有18个纵列,其中族的划分依据是什么?主族元素的主族序 数与价层电子数有什么关系? 提示:族的划分依据是原子的价层电子排布。主族元素的主族序数等于价 层电子数。
3.副族元素的副族序数是否只与最外层电子排布有关系? 提示:副族元素的副族序数除了与最外层电子排布有关系之外,还与次外层 电子排布有关。 4.为什么在元素周期表中金属元素主要集中在左下方区域,而非金属元素 主要集中在右上角区域? 提示:这是由元素原子的价电子层结构和元素周期表中元素性质的递变规 律决定的。在元素周期表中,同周期主族元素从左到右非金属性逐渐增强, 金属性逐渐减弱;同主族元素从上到下非金属性逐渐减弱,金属性逐渐增强, 结果使元素周期表左下方区域内的元素主要表现出金属性,右上角三角区 域内的元素主要表现出非金属性。
人教版高中化学必修二课件第一章第二节第1课时原子核外电子的排布

解析:K层即是第一层,只有1个电子的是氢原子,A项 正确;原子M层上有电子,说明L层已排满8个电子,此时M 层上电子数为L层的4倍,为32个,与最多有2n2即18个相矛 盾,B项错误;M层、L层上的电子数均为K层上的4倍,即 为“2、8、8”电子排布,则S2-、Cl-、K+、Ca2+均满足, C项正确;氢原子的核电荷数与最外层电子数相等,D项正 确。
名师点睛:判断10电子微粒的方法:
10电子微粒是高考的热点,因此高一就要夯实基础,但 死记硬背不利于知识的灵活应用。以下是快速确定10电子微 粒的有效方法。
(1)
(2)H+电子数为零,故与其他粒子结合,原粒子的电子 数不增也不减。则:
变式应用 2.下列微粒中,核外电子数相同的是( )
解析:F-中含10个e-,Na+中含10个e-,Ne中含10个e -,K+中含18个e-,⑤为Mg2+,含10个e-。故①②③⑤中 电子数相同。
(7)电子层数和最外层电子数相等的原子是H、Be、Al。 (8)电子层数是最外层电子数2倍的原子是Li、Ca。 (9)最外层电子数是电子层数2倍的原子是He、C、S。 (10)最外层电子数是电子层数3倍的原子是O。
变式应用
1.已知A、B、C三种元素的原子中,质子数为A<B< C,且都小于18,A元素的原子最外层电子数是次外层电子 数的2倍;B元素的原子核外M层电子数是L层电子数的一半; C元素的原子次外层电子数比最外层电子数多1个。试推断:
3.下列各原子结构示意图中所表示的核外电子排布正确的 是( ) C
一、原子核外电子排布规律 (2011年山东临沂模拟)下列说法中肯定错误的是( ) A.某原子K层上只有一个电子 B.某原子M层上电子数为L层上电子数的4倍 C.某离子M层上和L层上的电子数均为K层的4倍 D.某原子的核电荷数与最外层电子数相等
【优课】高中化学必修二:1.1.2元素周期表 课件(共39张PPT) - 最新

二、卤族元素
+9 2 7 +17 2 8 7 +35 2 8 18 7 +53 2 818 18 7
F
Cl
Br
I
原子结构 决定 性质
相同点: 最外层都有7个电子 易得1个电子
不同点: 核电荷数递增 电子层数递增 原子半径依次增大
得电子能力逐渐减弱 氧化性逐渐减弱
结构上的相同 决定性质上的相似
(最外层均为7个电子) (回忆氯气的性质)
0.534 180.5 1347
Na
银白色,柔软
0.97 97.81 882.9
K
银白色,柔软
0.86 63.65 774
Rb
银白色,柔软
1.532 38.89 688
Cs 略带金属光泽,柔软 1.879 28.40 678.4
碱金属在物理性质上的相似性和规律性
Li Na K Rb Cs
颜色
均为银白色(Cs略带金色)
球、在水面上四处游动
滴入酚酞溶液呈红色,有微 滴入酚酞溶液呈红色
弱爆炸
元素
现象
产物
结论
Li
会反应,比Na缓慢
Na
剧烈反应,有“浮、熔、 游、响、红”现象
对 应 的
从Li到Cs,随 电子层数的递 增,还原性
K
更剧烈,气体会燃烧, 轻微爆炸
碱 (金属性)逐 和 渐增强。 氢
Rb
遇水燃烧,甚至爆炸
气
Cs
相似性
Li Na K Rb Cs
最外层电子数为1,易失电 子,金属性、还原性强
递
核电荷数逐渐 增多 。
变
电子层数逐渐 增加 ,原子半径逐
规
人教版化学必修二全册精品课件(全)ppt课件

名师解惑
一、元素周期表(长式)的结构
1.第七周期属于长周期,因目前尚未排满也称不完全 周期,若排满应包括32种元素。
2.0族元素原子最外层电子数为8(He元素为2),因化学 性质不活泼,把它们的化合价定为0,叫做0族,在元素周期 表的第18纵行。
子序数为x+1的元素不可能处在( )
A.ⅢA族
B.ⅠA族
C.镧系元素
D.ⅢB族
解析 原子序数为x的元素位于ⅡA族,而与之相邻原子
序数为x+1的元素可能位于ⅢA族或ⅢB族,其中镧系属于
ⅢB族。
答案 B
跟踪练习2 同一主族的两种元素的原子序数之差不可能
是( )
A.16 B.26 C.36
D.46
答案 D
3.Ⅷ族包括周期表中第8、9、10三个纵行,其余15个 纵行,每个纵行为一族,因此周期表18个纵行共16个族。
4.周期表中族的排列方式 1~7纵行:ⅠA→ⅡA→ⅢB→…→ⅦB 8、9、10纵行:Ⅷ 11~18纵行:ⅠB→ⅡB→ⅢA→…→ⅦA→0 5.过渡元素包括所有的副族元素和Ⅷ族元素,且都是 金属元素。
2.元素周期表的结构 (1)周期 元素周期表有7个横行,叫做周期。 每一周期中元素的电子层数相同,从左到右原子序数递增。 其中,第一、二、三周期称为短周期,其他周期均为长周期。 (2)族 元素周期表有18个纵行,称为族。 主族:元素的族序数后标A 副族:元素的族序数后标B Ⅷ族:第8、9、10纵行 0族:稀有气体元素 思考题 某同学总结ⅡA族元素原子的最外层电子数都为 2 , 由 此 得 出 原 子 最 外 层 电 子 数 为 2 的 元 素 就 一 定 是 ⅡA ห้องสมุดไป่ตู้ 元 素。你认为正确吗?
元素周期律 课件 -高二化学人教版(2019)选择性必修2

电负性越大的原子, 其原子在形成化学键时吸引电子的能力越强
2.标准:
选定氟的电负性为4.0和锂的电负性为1.0作为相对标准,得 出各元素的电负性。
3.电负性的递变规律: 上大
右上大
右大
1、一般来说,同周期元素从左到右, 元素的电负性逐渐变大;表明其吸引
电子的能力逐渐增强(半径变小) 。
2020年全国卷ⅢT5 NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的 H呈负电性(Hδ-),电负性大小顺序是__________。
N>H>B
总结
在下列空格中,填上适当的元素符号。
(1) 在第3周期中,第一电离能最小的元素是( Na ) , 第一电离能最大的元素是( Ar );
渐小
渐大
主族元素原子半径的周期性变化
微粒半径大小的判断方法
1.一般情况下,电子层数越多,微粒半径越大; 2.微粒电子层数相同,则核电荷数越大,半径越小; 3.微粒核电荷数相同,则核外电子越多,半径越大。
判断下列微粒大小:
(1)r(O) r(F) r(Na) r(Al)
(2)r(O2-) r(F-) r(Na+) r(Al3+)
要的最低能量叫做第一电离能。 用符号 I1 表示
概念表述中的“气态” 、“基 态” 、“电中性” 、“失去一个 电子” 等都是保证“最低能量” 的条件。
M(g)===M+(g)+e- I1(第一电离能)
意义: 电离能可以衡量元素的原子失去一个电子的 难易程度。
第一电离能数值越小,表示在气态时该原子失去电子越 容易,即元素的金___属__性越强; 第一电离能数值越大,表明在气态时该原子失去电子越 难 ,即元素的_金___属____性越弱。
人教版-高一化学-必修二原子核外电子的排布

第一章 物质结构 元素周期律
第二节 元素周期律
第1课时 原子核外电子排布 元素周期律
第一章 物质结构 元素周期律
高中化学·必修二
学 习 目 标
1.初步了解原子核外电子排布的规律, 熟练画出1~ 20 号元素的原子结构 示意图。 2. 利用资料数据和实验探究,探讨出 第三周期元素及其化合物的性质变 化规律,从而导出元素周律。
第一章 金属性依次增强
原 子 半 径 依 次 减 小
得 电 子 能 力 依 次 增 强
非 金 属 性 依 次 增 强
物质结构 元素周期律
高中化学 ·必修二 非金属性逐渐增强 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
1 2
3 4 5 6 7
Cs
F 金 属 性 逐 渐 增 强 B Al Si Ge As Sb Te Po
第一章 物质结构 元素周期律
认真分析教材13页“表1-2”,试找出每个电子层 排布电子数的规律。
第一章 物质结构 元素周期律
高中化学·必修二
电子层排布电子数的规律
1.核外电子总是尽先排布在能量最低的电子层, 然后由里向外从能量低的电子层逐步向能量高 的电子层排布。
2.各电子层最多容纳的电子数是2n2(n表示电子层)。
3.最外层电子数不超过8个(K层是最外层时,最多 不超过2个),次外层电子数目不超过18个,倒 数第三层不超过32个。 注意: 以上规律是相互联系的,不能孤立地机械地套用。
Si
单质与氢气 反应条件
最高价氧化物 对应的水化物 高温
P
能反应,困难
S
加热反应
Cl
光照或 点燃反应
硅酸 H2SiO3
磷酸 H3PO4
人教版高中化学必修二元素周期律

(3)最低负价 = – 〔8 – 最外层电子数〕
3、注意
= – 〔8 – 主族序数〕
〔1〕金属无负价,氟无正价,氧无最高正价 〔2〕稀有气体元素化学性质不活泼,通常情况下难
以与其他元素化合,规定其化合价为0 〔3〕价电子:决定元素化合价的电子〔外层电子〕
〔四〕元素金属性、非金属性的周期性变化
1.判断元素金属性、非金属性强弱的方法
C. C、N、O原子半径依次增大 D. Na、K、Rb氧化物的水化物碱性依次增强
2、同一横行X、Y、Z三种元素,最高价氧化物对 应的水化物的酸性是 HXO4 > H2YO4 > H3ZO4,
↘
↗
↘
↗
↗
↘
↗
↘
↗
↘
↘
↗
↗
↘
↘
↗
由易到难
由难到易
〔五〕元素周期律 1.元素性质的周期性变化
随着原子序数的递增:
〔1〕元素原子的核外电子排布呈现周期性变化
〔2〕元素原子半径呈现周期性变化
〔3〕元素主要化合价呈现周期性变化
2. 元素周期律
〔元4素〕的元性素质的随金着属元性素、原非子金序属数性的呈递现增周而期呈性现变周化期性的 变化——元素周期律
......
(一〕元素原子核外电子排布的周期性变化
同周期:从左至右,电子层数一样,最外层电子数依次增加 同主族:从上至下,最外层电子数一样,电子层数依次增加
1
12
2
2
18
8
3
18
8
周期性
〔二〕元素原子半径的周期性变化
元素原子半径数据
主族元素原子半径的递变规律
主族 周期
A. 同周期主族元素: B. 从左到右原子半径依次减小 C. (除稀有气体〕 B. 同主族元素:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
SiH4 高温下少量反应
很不稳定
15P
PH3
磷蒸气,困难
不稳定
16S
H2S
加热反应
较不稳定
17Cl
HCl
光照或点燃
稳定
非金属性:Si < P < S < Cl
探究实验四
取一支试管,加 入2ml,1mo1/L、 MgCl2溶液,再逐 滴加入3mo1/L、 NaOH溶液,把 生成的溶液分成 两份,分别加入 3mo1/L、NaOH 溶液、稀盐酸观 察
现象
反应 方程
式
结论
Mg(OH)2的性质
加入NaOH
加入稀盐酸
沉淀不溶解
沉淀溶解
无
Mg(OH)2+2HCl=
MgCl2+2H2O
反应 方程
沉淀,把Al(OH)3沉 式
淀分别盛放于2支
试管中,然后,向 结 论
2支试管中分别加
入1mo1/L稀盐酸和
6mo1/LNaOH溶液,
观察现象。
Al(OH)3的性质
加入NaOH
加入稀盐酸
沉淀溶解
沉淀溶解
Al(OH)3+NaOH= Al(OH)3+3HCl=
NaAlO2+2H2O
AlCl3+3H2O
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
探究实验二
取一小段镁带用
砂纸去掉表面的
氧化膜,放入小
现象:镁与冷水反应缓慢,产生少量 气泡,滴入酚酞试剂后不变色。
加热后镁与沸水反应较剧烈,产生较
试管中,加入2-3 多气泡,溶液变为红色。
ml水,并滴入2滴
酚酞溶液。观察
现象。过一会儿, 用酒精灯给试管
ห้องสมุดไป่ตู้
性质 与水 与酸
钠(Na) 镁(Mg) 铝(Al)
与冷水水、反剧烈应:冷热N水水a、、>M缓快g慢速
不反应
与酸剧烈反应:Mg快>速Al
金属性:Na>Mg>Al
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
铝(Al) 不反应
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
探究实验三
取一小段镁带和 一小片铝,用砂 纸除去它们表面 的氧化膜,把镁 带和铝片分别放 入两支试管,再 各加入2-3ml稀 盐酸观察现象。
Mg(OH)2不 能溶于氢氧化钠
Mg(OH)2能溶 于盐酸
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
探究实验五
取一支试管,加入
1mo1/L AlCl3溶液, 加入3mo1/LNaOH 现象
溶液至少产生大量 的Al(OH)3白色絮状
现象:镁与铝均能与盐酸反应产 生气泡。但镁反应更剧烈。
反应式:Mg + 2HCl = MgCl2 + H2 2Al + 6HCl = 2AlCl3+ 3H2
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
钠(Na)、镁(Mg)、铝(Al)金属性比较
结论:金属性:Na>Mg>Al
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
硅(Si)、磷(P)、硫(S)、氯(Cl)非金属性的比较
从氢化物看
元素
氢化物 化学式
单质与氢气 的化合条件
氢化物的稳 定性
14Si
液,然后取 黄豆大的一
反应式:2Na + 2H2O == 2NaOH + H2
块钠放入其
中观察现象。
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
钠(Na)、镁(Mg)、铝(Al)金属性比较
性质
钠(Na) 镁(Mg) 铝(Al)
与水反应 冷水、剧烈
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
Al(OH)3既能溶于,也能溶于稀盐酸
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
NaOH 、Mg(OH)2、Al(OH)3的碱性比较
性质
NaOH
Mg(OH)2 Al(OH)3
氢氧化 物碱性
强碱
中强碱 两性氢氧 化物
1~2
二
3~10
三
11~18
化合价的变化
+1
+1→ +5 - → 最高正价:__________
4 -1
最低负价:__________
+1→ +7 - → 最高正价:___4_______-1
最低负价:__________
新课引入:
1-18号元素(除稀有气体元素外) 元素的金属性和非金属性随着原子 序数的递增,呈现出怎样的规律?
反应式:Mg
+
2H2O
△
=
Mg(OH)2
+
H2
加热至沸腾,并
移开酒精灯,再
观察现象。
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
人教版高中化学必修二第一章第二节 元素周 期律 课件(共25张PPT)
钠(Na)、镁(Mg)、铝(Al)金属性比较
性质
钠(Na) 镁(Mg)
与水反应 与冷水水、反剧烈应:冷热N水a水>、、M缓迅g慢速
二、教学重点难点: 重点:元素的金属性和非金属性随原子序数的递 增而呈现周期性变化的规律.
难点:元素的金属性和非金属性随原子序数的递 增而呈现周期性变化的规律.
三、教学过程
探究实验一 现 象:钠与冷水剧烈反应,金
在烧杯中加 100mL的蒸 馏水并滴入 几滴酚酞试
属钠迅速融为光亮的小 球,并且快速游动,溶 液的颜色立即变为红色。
一、教学目标:
1、知识与技能: (1)掌握元素的金属性和非金属性随原子序数的增递而呈现周 期性变化的规律。 (2)通过实验操作,培养学生实验技能和动手操作能力
2、过程与方法: (1)通过学生的自主探究学习归纳总结元素周期律。 (2)自主探究,通过实验探究,培养学生探究能力。 3、情感、态度与价值观:培养学生辨证唯物主义观点,量变到质 变规律。
知识回
1顾、:1-18号元素(除稀有气体元素外)
元素的原子半径,随着原子序数的递 增,呈现出怎样的规律?
周期 元素原子半径的周期性变化
1 2 3
4 5 6 7
知识回顾:
2、1-18号元素(除稀有气体元素外) 元素的化合价(最低和最高)随着原
子序数的递增,呈现出怎样的规律?
周期序数
一
原 子序数
