化合价组成化学元素表
常见元素及原子团的化合价表

常见元素及原子团的化合价表CuSO4+2NaOH=Cu(OH)2↓+Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验Ca(OH)2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁Ca(HCO3)2Δ CaCO3↓+H2O+CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成HCl+AgNO3= AgCl↓+HNO3生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Ba(OH)2+ H2SO4=BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+ H2SO4=BaSO4↓+2HCl 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4=BaSO4↓+2HNO3生成白色沉淀、不溶解于稀硝酸检验SO42—的原理FeCl3+3NaOH=Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH=Al(OH)3↓+3NaCl 有白色沉淀生成MgCl2+2NaOH = Mg(OH)2↓+2NaClCuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O = Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2=CaSO3↓+ H2O 有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3=BaCO3↓+2NaOH 有白色沉淀生成Ca(OH)2+K2CO3=CaCO3↓ +2KOH 有白色沉淀生成AgNO3+NaCl = AgCl↓+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子初中常见物质俗称1、氯化钠(NaCl):食盐2、碳酸钠(Na2CO3) :纯碱,苏打,口碱3、氢氧化钠(NaOH):火碱,烧碱,苛性钠4、氧化钙(CaO):生石灰5、氢氧化钙(Ca(OH)2):熟石灰,消石灰 6 、二氧化碳固体(CO2):干冰7、氢氯酸(HCl):盐酸8、碱式碳酸铜(Cu2(OH)2CO3):铜绿9、硫酸铜晶体(CuSO4 .5H2O):蓝矾,胆矾10、甲烷(CH4):沼气11、乙醇(C2H5OH):酒精12、乙酸(CH3COOH):醋酸13、过氧化氢(H2O2):双氧水14、汞(Hg):水银15、碳酸氢钠(NaHCO3):小苏打中化学常见物质的颜色(一)、固体的颜色1、黑色固体(5种):木炭,氧化铜,二氧化锰,四氧化三铁,铁粉2、红色固体:铜——紫红色,氧化铁Fe2O3——红(棕)色3、蓝色晶体:硫酸铜晶体CuSO4·5H2O4、蓝色沉淀:氢氧化铜5、红褐色沉淀:氢氧化铁6、白色沉淀(6种):碳酸钙,碳酸钡,碳酸银;氢氧化镁;硫酸钡,氯化银。
元素化合价口诀表

元素化合价口诀表化学中的元素化合价是指元素在化合物中所具有的价态。
熟练掌握元素化合价对于理解和预测化学反应非常重要。
下面将通过元素化合价口诀表来介绍元素化合价的规律和口诀。
一、主族元素化合价口诀1. 第一族:氢加一,盐中出现。
氢原子的化合价始终为+1,当氢与其他元素结合形成化合物时,其化合价为+1。
2. 第二族:碱土金,加二最真。
碱土金属元素的化合价始终为+2。
3. 第三族:硼铝金,加三不停。
硼、铝等元素的化合价始终为+3。
4. 第四族:碳硅锡,加四不离。
碳、硅、锡等元素的化合价始终为+4。
5. 第五族:氮磷,加五不忘。
氮、磷等元素的化合价始终为+5。
6. 第六族:氧硫硒,加六不退。
氧、硫、硒等元素的化合价始终为-2。
7. 第七族:氟氯溴,加一不少。
氟、氯、溴等元素的化合价始终为-1。
8. 第八族:氦尼,化合价为零。
氦和尼尔森(Ne)是稀有气体,它们的化合价始终为0。
二、过渡元素化合价口诀过渡元素的化合价不像主族元素那样固定,它们的化合价可以根据不同情况发生变化。
过渡元素的化合价需要根据具体的化合物和反应来确定,没有固定的口诀。
三、总结通过以上的元素化合价口诀表,我们可以得到一些规律性的结论。
主族元素的化合价相对固定,可以根据元素所在的族来确定。
而过渡元素的化合价则需要根据具体情况来确定,没有固定的规律可循。
掌握元素化合价对于理解和预测化学反应非常重要。
通过口诀表的记忆,我们可以更快速地确定元素的化合价,从而更好地理解和解决化学问题。
同时,掌握元素化合价也有助于我们理解化学反应的机理和原理,为进一步学习和研究提供了基础。
元素化合价是化学中的重要概念,通过掌握元素化合价口诀表,我们可以更好地理解和应用化学知识。
希望大家通过学习和记忆口诀表,能够在化学学习中取得更好的成绩,为未来的科学研究和实践打下坚实的基础。
初中化学元素_化合价_化学式_方程式整理

一、常见元素化合价元素名称元素符号常见化合价元素名称元素符号常见化合价钾氢钠氯Cl银溴Br -1钙Ca +2 碘I -1镁Mg +2 氧O -2硫S -2 +4 +6 钡Ba +2碳 C +2 +4 锌Zn +2硅Si +4 铜Cu +2 -1氮N -3 +2 +4 +5 铝Al +3磷P +5 铁Fe +2 +3二、常见原子团化合价原子团名称原子团名称原子团符号原子团化合价原子团名称原子团符号原子团化合价氢氧根OH -1 碳酸氢根HCO3-1 硫酸根SO4-2 磷酸根PO4-3 碳酸根CO3-2 亚硫酸根SO3-2 硝酸根NO3-1 铵根NH4+1 醋酸根CH3COO -1 氯酸根ClO3-1 锰酸根MnO4-2 高锰酸根MnO4-1 磷酸根PO4-3 磷酸氢根HPO4-2 磷酸二氢根H2PO4-1三、元素周期表四、化学式1、非金属单质:氢气H2金刚石/石墨C 氮气N2氧气O2磷P 硫S 氯气Cl22、金属单质:钠Na 镁Mg 铝Al 钾K 钙Ca 铁Fe 锌Zn 铜Cu 钡Ba 钨W 汞Hg3、非金属氧化物:水H2O 一氧化碳CO 二氧化碳CO2 五氧化二磷P2O5二氧化氮NO2二氧化硅SiO2二氧化硫SO2三氧化硫SO3一氧化氮NO4、金属氧化物:氧化镁MgO 氧化铜CuO 氧化钡BaO 氧化亚铜Cu2O 氧化钠Na2O 氧化亚铁FeO 三氧化二铁(铁红)Fe2O3四氧化三铁Fe3O4三氧化二铝Al2O3二氧化锰MnO25、常见的酸:硫酸H2SO4盐酸HCl 硝酸HNO3磷酸H3PO4硫化氢H2S 溴化氢HBr 碳酸H2CO3醋酸CH3COOH6、常见的碱:氢氧化钠NaOH 氢氧化钙Ca(OH)2氢氧化钡Ba(OH)2氢氧化镁Mg(OH)2氢氧化铜Cu(OH) 2氢氧化钾KOH 氢氧化铝Al(OH) 3氢氧化铁Fe(OH) 3氢氧化亚铁Fe(OH) 27、常见的盐—氯化物/盐酸盐:氯化钾KCl 氯化钠(食盐)NaCl 氯化镁MgCl2氯化钙CaCl2氯化铜CuCl2氯化锌ZnCl2氯化钡BaCl2氯化铝AlCl3氯化亚铁FeCl2氯化铁FeCl3氯化银AgCl8、常见的盐—硫酸盐:硫酸铜CuSO4硫酸钡BaSO4硫酸钙CaSO4硫酸钾K2SO4硫酸镁MgSO4硫酸亚铁FeSO4硫酸铁Fe2 (SO4) 3硫酸铝Al2 (SO4) 3硫酸氢钠NaHSO4硫酸氢钾KHSO4亚硫酸钠NaSO39、常见的盐—硝酸盐:硝酸钠NaNO3硝酸钾KNO3硝酸银AgNO3硝酸镁MgNO3硝酸铜Cu(NO3)2硝酸钙Ca(NO3) 2亚硝酸钠NaNO310、常见的盐—碳酸盐/碳酸氢盐:碳酸钠Na2CO3碳酸氢钠NaHCO3碳酸钙CaCO3碳酸镁MgCO3碳酸钾K2CO3碳酸氢钾KHCO311、常见的盐—酸式盐/碱式盐:碳酸氢钠NaHCO3碳酸氢钾KHCO3碳酸氢铵NH4HCO3磷酸二氢钾KH2PO4 / 碱式碳酸铜Cu2 (OH) 2CO312、常见有机物:甲烷CH4乙炔C2H2甲醇CH3OH 乙醇C2H5OH 乙酸CH3COOH13、常见结晶水合物:石膏CaSO4•2H2O 明矾KAl(SO4)2•12H2O 绿矾FeSO4•7H2O 蓝矾CuSO4•5H2O 碳酸钠晶体Na2CO3•10H2O14、常见化肥:尿素CO(NH2)2硝酸铵NH4NO3硫酸铵(NH4)2SO4碳酸氢铵NH4HCO3磷酸二氢钾KH2PO415、常见沉淀及其颜色:碳酸钙CaCO3(白色)氯化银AgCl(白色)碳酸钡BaCO3(白色)硫酸钡BaSO4(白色)氢氧化亚铁Fe(OH) 2(白色)氢氧化铁Fe(OH) 3(红褐色)氢氧化铜Cu(OH)2(天蓝色)氢氧化铝Al(OH) 3(白色)二氧化锰MnO2(黑色)氢氧化银AgOH (白色)碳酸银Ag2CO3(淡黄色)(黄色)氢氧化镁Mg(OH) 2(白色))碱式碳酸铜Cu(OH) CO3(暗绿色)216、常见俗名与化学式:硫酸盐类:1.皓矾:ZnSO4·7H2O2.钡餐,重晶石:BaSO43.绿矾,皂矾,青矾:FeSO4·7H2O4.芒硝,朴硝,皮硝:Na2SO4·10H2O5.明矾:KAl(SO4) 2·12H2O6.生石膏:CaSO4·2H2O 熟石膏:2CaSO4·H2O7.胆矾、蓝矾:CuSO4·5H2O矿石类:5.磁铁矿石:Fe3O46.赤铁矿石:Fe2O322.大理石(方解石、石灰石):CaCO323.孔雀石:CuCO3、Cu(OH)2气体类:1.高炉煤气:CO、CO2等混合气体2.水煤气:CO、H23.天然气(沼气):CH44.液化石油气:C3H8,C4H10为主2.有机类:1.福尔马林(蚁醛):HCHO2.蚁酸:HCOOH3.尿素:(NH4CNO)或CO(NH2)2 5.木精(工业酒精):CH3OH 13.葡萄糖:C6H12O614.蔗糖:C12H22O11其他类:2.石灰乳、消石灰、熟石灰:Ca(OH) 23.熟石膏:2CaSO4·H2O 5.铜绿:Cu2 (OH) 2CO3 6.纯碱(碱面):Na2CO39.小苏打:NaHCO310.苏打:Na2CO311.大苏打(海波):Na2S2O3 19.波尔多液:CuSO4、Ca(OH) 221. 纯碱、苏打、口碱:Na2CO322. 双氧水:H2O223.生石灰:CaO 24. 火碱、烧碱、苛性钠:NaOH17、常见固体、液体颜色:固体的颜色1、红色固体:铜,氧化铁2、绿色固体:碱式碳酸铜3、蓝色固体:氢氧化铜,硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫磺6、无色固体:冰,干冰,金刚石7、银白色固体:银,铁,镁,铝,汞等金属8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭)9、红褐色固体:氢氧化铁10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁液体的颜色1、无色液体:水,双氧水2、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液3、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液4、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液5、紫红色溶液:高锰酸钾溶液6、紫色溶液:石蕊溶液气体的颜色1、红棕色气体:二氧化氮2、黄绿色气体:氯气3、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体。
化学元素价表

化学元素价表家长可以教孩子一些化合价的顺口溜来帮助记忆。
家长每天有空时教孩子背一小段。
化合价顺口溜:一价钾纳氯氢银二价氧钙钡镁锌三铝四硅五价磷谈变价也不难二三铁二四碳硫有负二正四六铜汞二价最常见氢氧根负一价铵根正一价硝酸根负一价硫酸根负二价碳酸根负二价一氯氢钾钠银,二氧钡钙镁和锌。
(开头全是负价,其余是正价)一二铜汞,二三铁。
(中文有“亚”是低价)三价铝,要记清。
单质永远是零价。
其余都是多数价,恳请麻烦方程算。
一价钾钠氯氢银,二价钙镁氧钡锌,三铝四硅五价磷。
二四六硫二四碳,二三四五就是氮。
铁为二三铜一二,单质零价要牢记。
钾钠氢银正一价,钙镁钡锌正二价。
氟氯溴碘负一价,铜正一正二铝正三,铁有正二和正三。
一价钠钾银氢(哪家迎亲)二价镁钙锌钡(没盖新被)三铝四硅记在心一二铜,二三铁,二四碳二四六硫要记全(负价)氯一硫二最常见一价铵根钾钠银氢二价铜镁钙钡锌铁正二(正)三铝正三氯(负)一价氧负二金正非负单质零(金属正非金属负)还有四根要记清负一氢氧(根)硝酸根负二碳酸(根)硫酸根正一钾钠氢铵银正二钙镁钡铜锌负一氟氯负二氧三铝四铁五氮磷一价氢钾钠银与氟氯还有氢氧硝酸和铵根二价钙镁钡锌与氧硫还有硫酸和碳酸铜汞一二铁二三负一硝酸氢氧根负二硫酸碳酸根负三记住磷酸根正一价的是铵根钾钠银氢正一价,氟氯溴碘负一价;钙镁钡锌正二价,通常氧是负二价;硫三有一负二价,二三铁,二四碳,三铝四硅五价磷;一三五七正价氯,二四六硫锰四七;铜汞二价最常见,一价不能忽视它;单质化合价为零。
一价钾钠银氢二价钙镁钡锌三价铝,四价硅一二铜,二三铁钾钠氢银一价氢二价氧钙镁钡铜锌三铝四硅五氮磷谈变价,也不难二三铁,二四碳,二四六硫都齐全一五七氯要记清一价钾钠银氯氢二价氧钙钡镁锌铝价正三氧负二以上价态要记真铜一二来铁二三碳硅二四要记全硫显负二正四六负三正五氮和磷氯价通常显负一还有正价一五七锰显正价二四六最高价数也是七单质化合价是0一价氢氟钾钠银二价氧钙钡镁锌三铝四硅三五磷一二铜汞四七锰二三铁二四碳二四六硫三五氮一五七氯常常见单质为零永不变钾钠氢银正一价钙镁钡锌正二价铝三硅四氧负二氟氯溴碘常负一一价钾钠氢银氯二价氧钙钡镁锌三铝四硅五价磷二三铁二四碳二四六硫都齐全铜汞二价最常见原子团要记清正一价是铵根负一价氢氧根硝酸根负二价硫酸根碳酸跟还有负三价磷酸根化合价,要记准,一价钾钠氯氢银,二价氧钙钡镁锌,三铝四硅五氮磷。
化学元素符号及相对原子质量及化合价

化学元素符号及相对原子质量及化合价以下是一些常见元素的符号、相对原子质量和化合价的列表:
1.氢(H):相对原子质量1,化合价为+1
氢是宇宙中最常见的元素之一,通常以单质状态存在。
2.氧(O):相对原子质量16,化合价为-2
氧是一个非金属元素,是地球上最常见的元素之一,它在大多数化合物中以氧负离子(O2-)的形式存在。
3.碳(C):相对原子质量12,化合价为+4或-4
碳是有机化合物的基础元素,可以形成四种单键,也可以接受或捐赠电子以形成离子。
4.氮(N):相对原子质量14,化合价为+3或-3
氮是空气中最常见的元素之一,通常以三键形式出现,也可以接受或捐赠电子形成离子。
5.氯(Cl):相对原子质量35.5,化合价为-1
氯是一种强氧化剂,往往与其他元素形成负离子。
6.钠(Na):相对原子质量23,化合价为+1
钠是一种常见的金属元素,以阳离子的形式存在于许多化合物中。
7.铁(Fe):相对原子质量56,化合价为+2或+3
铁是一种过渡金属元素,可以以不同的化合价形式存在。
8.氟(F):相对原子质量19,化合价为-1
氟是一种强氧化剂,通常以氟离子(F-)的形式存在。
9.硫(S):相对原子质量32,化合价为+2或-2
硫是一种非金属元素,可以形成二键或六键。
10.铜(Cu):相对原子质量63.5,化合价为+1或+2
铜是一种金属元素,在自然界中以阳离子的形式存在。
这只是一些元素的例子,实际上,化学元素周期表中有118个元素,每个元素都有自己的符号、相对原子质量和化合价。
这些信息对于理解化学反应、化合物的形成以及元素的特性非常重要。
元素的化合价

元素的化合价化合价是指元素在化合物中所能显示的化学反应能力,其数值表示元素在化合物中与其他元素的组成部分结合的程度。
化合价是化学元素进行反应和形成化合物的重要属性之一。
了解元素的化合价有助于我们理解元素之间的化学反应和化合物的组成。
一、化合价的概念化合价是元素在化合物中表现出来的一种化学性质。
它表示元素参与化合物中的元素与元素之间的键的键强度和形成伴随的对电子结构的改变。
化合价可正可负,是正离子和负离子的理论基础。
二、常见1. 氢的化合价是+1,其氢化物中的氢原子失去一个电子成为正离子H+;2. 氧的化合价是-2,常见的含氧化合物有水(H2O)、氧化锌(ZnO)等;3. 碳的化合价是+4,其常见的化合物有甲烷(CH4)、乙烯(C2H4)等;4. 氮的化合价是-3,如氨(NH3);5. 氯的化合价是-1,如氯化钠(NaCl)。
三、元素的化合价和周期表元素的化合价和其在周期表中的位置有关。
在周期表的第一至第二十一族元素中,元素的化合价主要与其所属的族别有关。
例如,位于第一族的元素化合价通常为+1,位于第二族的元素化合价通常为+2,位于第十六族和第十七族的元素化合价分别为-2和-1。
然而,周期表中也存在一些特例。
例如,氨气中的氮元素的化合价为-3,而不是像氮素所在的第五族元素一样化合价为-5。
这是因为氮原子在三键形成后达到稳定的电子配置,而不需要五个电子形成共价键。
四、影响化合价的因素元素的化合价受到多种因素的影响。
以下是一些常见的影响因素:1. 原子的电子亲和能力:原子的电子亲和能力越强,其化合价可能越高;2. 元素的电子配置:元素的化合价与其电子配置有关。
趋于稳定的电子配置可能导致较低的化合价;3. 元素的氧化态:元素的氧化态越高,其化合价可能越高。
五、化合价的应用1. 化学反应的预测:了解元素的化合价有助于预测元素之间的化学反应。
例如,知道氯的化合价为-1,可以预测在氯与钠发生反应时,氯会接受钠的电子而形成氯离子;2. 化学式的编写:化合价的了解有助于编写化合物的化学式。
化学元素周期表 化合价 巧背诵方法 读音

看着个顺口溜:
钾钠氢银正一价;钙镁钡锌铜正二价.
铝是正三氧负二;铁有正二正三价.
硫有负二正四六;磷有正五正负三.
正一五七负一氯;大家一定要记熟.
1.化合价的概念
一二铜,二三铁
1氢(qīng) 2氦(hài) 3锂(lǐ) 4铍(pí)5 硼(péng) 6碳(tàn) 7氮(dàn)8 氧(yǎng) 9氟(fú)10 氖(nǎi)11钠(nà) 12镁(měi) 13铝(lǚ)
14 硅(guī)15 磷(lín) 16硫(liú) 17氯(lǜ) 18氩(yà)19钾(jiǎ) 20钙(gài) 21钪(kàng) 22钛(tài)23 钒(fán) 24铬(gè) 25锰(měng) 26铁(tiě) 27钴(gǔ)28 镍(niè)29 铜(tóng)30 锌(xīn) 31镓(jiā) 32锗(zhě) 33砷(shēn) 34硒(xī) 35溴(xiù)36 氪(kè)
85砹(ài)86 氡(dōng)87钫(fāng) 88镭(léi)89 锕(ā) 90钍(tǔ)91 镤(pú) 92铀(yóu) 93镎(ná)94 钚(bù)95 镅(méi) 96锔(jú)
97 锫(péi)98 锎(kāi) 99锿(āi) 100镄(fèi) 101钔(mén) 102锘(nuò)103 铹(láo)104 钅卢(lú) 105钅杜(dù)106钅喜(xǐ)
氦氖氩氪氙氡 害耐亚克先动
化合价可以这样记忆:
一家请驴脚拿银,(一价氢氯钾钠银)
二家羊盖美背心。(二价氧钙镁钡锌)
一价氢氯钾钠银 二价氧钙钡镁锌
初中化学元素化合价完整版

一、常见元素化合价
元素名称
元素符号
常见化合价
元素名称
元素符号
常见化合价
钾
K
+1
氢
H
+1
钠
Na
+1
氯
Cl
-1+5+7
银
Ag
+1
溴
Br
-1
钙
Ca
+2
碘
I
-1
镁
Mg
+2
氧
O
-2
硫
S
-2+4+6
钡
Ba
+2
碳
C
+2+4
锌
Zn
+2
硅
Si
+4
铜
Cu
+2-1
氮
N
-3+2+4+5
铝
Al
+3
磷
P
+5
铁
溶
不
Fe2+
不
溶
溶
溶
不
Fe3+
不
溶
溶
溶
—
Cu2+
不
溶
溶
溶
不
Ag+
—
溶
不
微
不
Fe
+2+3
二、常见原子团化合价原子团
名称原子团
名称
原子团
符号
原子团
化合价
原子团
名称原子团Fra bibliotek符号原子团
化合价
氢氧根
常见元素及原子团的化合价表
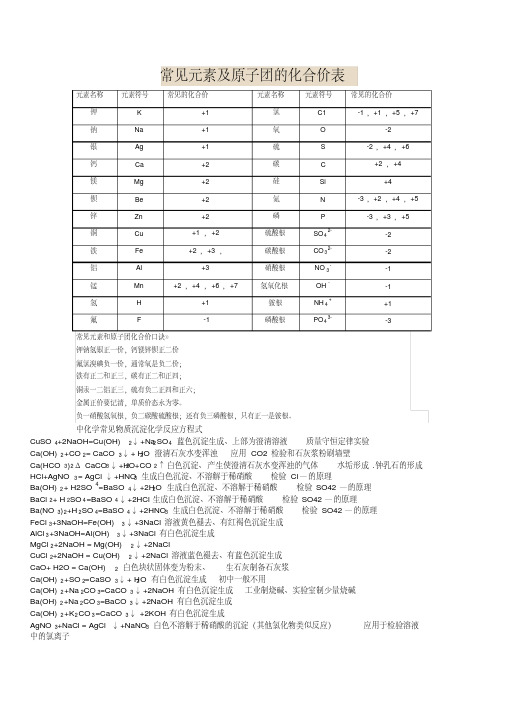
常见元素及原子团的化合价表元素名称元素符号常见的化合价元素名称元素符号常见的化合价钾K +1 氯C1 -1,+1,+5,+7 钠Na +1 氧O -2银Ag +1 硫S -2,+4,+6 钙Ca +2 碳 C +2,+4 镁Mg +2 硅Si +4钡Be +2 氮N -3,+2,+4,+5 锌Zn +2 磷P -3,+3,+5 铜Cu +1,+2 硫酸根SO42--2铁Fe +2,+3,碳酸根CO32--2铝Al +3 硝酸根NO3--1锰Mn +2,+4,+6,+7 氢氧化根OH--1氢H +1 铵根NH4++1氟 F -1 磷酸根PO43--3 常见元素和原子团化合价口诀》钾钠氢银正一价,钙镁锌钡正二价氟氯溴碘负一价,通常氧是负二价;铁有正二和正三,碳有正二和正四;铜汞一二铝正三,硫有负二正四和正六;金属正价要记清,单质价态永为零。
负一硝酸氢氧根,负二碳酸硫酸根;还有负三磷酸根,只有正一是铵根。
中化学常见物质沉淀化学反应方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验Ca(OH)2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁Ca(HCO3)2Δ CaCO3↓+H2O+CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成HCl+AgNO3= AgCl↓+HNO3生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Ba(OH)2+ H2SO4=BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+ H2SO4=BaSO4↓+2HCl 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4=BaSO4↓+2HNO3生成白色沉淀、不溶解于稀硝酸检验SO42—的原理FeCl3+3NaOH=Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH=Al(OH)3↓+3NaCl 有白色沉淀生成MgCl2+2NaOH = Mg(OH)2↓+2NaClCuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O = Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2=CaSO3↓+ H2O 有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3=BaCO3↓+2NaOH 有白色沉淀生成Ca(OH)2+K2CO3=CaCO3↓ +2KOH 有白色沉淀生成AgNO3+NaCl = AgCl↓+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子精品文库初中常见物质俗称1、氯化钠(NaCl):食盐2、碳酸钠(Na2CO3) :纯碱,苏打,口碱3、氢氧化钠(NaOH):火碱,烧碱,苛性钠4、氧化钙(CaO):生石灰5、氢氧化钙(Ca(OH)2):熟石灰,消石灰 6 、二氧化碳固体(CO2):干冰7、氢氯酸(HCl):盐酸8、碱式碳酸铜(Cu2(OH)2CO3):铜绿9、硫酸铜晶体(CuSO4 .5H2O):蓝矾,胆矾10、甲烷(CH4):沼气11、乙醇(C2H5OH):酒精12、乙酸(CH3COOH):醋酸13、过氧化氢(H2O2):双氧水14、汞(Hg):水银15、碳酸氢钠(NaHCO3):小苏打中化学常见物质的颜色(一)、固体的颜色1、黑色固体(5种):木炭,氧化铜,二氧化锰,四氧化三铁,铁粉2、红色固体:铜——紫红色,氧化铁Fe2O3——红(棕)色3、蓝色晶体:硫酸铜晶体CuSO4·5H2O4、蓝色沉淀:氢氧化铜5、红褐色沉淀:氢氧化铁6、白色沉淀(6种):碳酸钙,碳酸钡,碳酸银;氢氧化镁;硫酸钡,氯化银。
常见元素化合价表

中学阶段常见元素化合价表注:本表不列出稀有气体、金属的0价及非常见价态等。
元素常见化合价【主要离子】例子该化合价的性质元素及单质的其他性质+1(主要)【H+】在大多数化合物中,如HCl、H2O、NaHCO3、NH3等●有三种同位素:1H、2H(或D)、3H(或T)●单质有还原性●可燃●密度最小的气体●无色无味-1 【H-】在活泼金属氢化物中及其衍生物,如NaH、KH、CaH2、KBH4等有强还原性,可以和水反应放出H2+1 【Li+】锂化合物如LiCl、LiOH、Li2O等焰色为深红色●银白色的活泼金属,可以和水反应●熔点比水高,密度很小●同位素6Li用在核反应堆内吸收中子●使用于电池内●在空气中燃烧生成Li2O●强还原剂+1 【Na+】钠化合物如NaCl、Na2O2等焰色为黄色●银白色的活泼金属,可以和水反应,保存在煤油中●熔点比水低,密度、硬度小●和醇、酸反应放出氢气●在空气中燃烧生成Na2O2●强还原剂+1 【K+】钾化合物如KCl、KNO3等焰色为紫色(混有Na+时会为黄色,透过蓝色钴玻璃才能看到紫色)●银白色活泼金属,可以和水反应,比钠更剧烈,保存在煤油中●熔点比水低、密度、硬度小●强还原剂●在空气中燃烧生成K2O2和KO2●钾钠合金用作核反应堆的冷却剂+1 【Rb+】【Cs+】铷、铯化合物如RbCl、CsCl等铷的焰色为浅紫色,铯的焰色为天蓝色●铷是银白色金属,铯是略带金黄色光泽的金属,熔点低,和水极其猛烈地反应●铯可以在空气中自燃●强还原剂+2【Mg2+】镁化合物如MgCl2、MgSO4等●银白色活泼金属,和沸水略有反应●在空气中燃烧生成MgO,也有Mg3N2生成●能在CO2等大多数气体中燃烧●和酸剧烈反应●强还原剂●军事上用作照明弹+2 【Ca2+】钙化合物如CaCl2、CaSO4、CaO等焰色为砖红色●银白色活泼金属,和水反应●密度比水大●在空气中缓慢氧化或燃烧生成CaO ●强还原剂+2 【Sr 2+】 【Ba 2+】锶、钡化合物如SrCl 2、BaSO 4等锶的焰色为深红色,钡的焰色为黄绿色;Ba 2+有毒●银白色活泼金属,可以和水反应●密度比水大●强还原剂●可以在空气中燃烧 +3 【BO 33-】大多数硼化合物如H 3BO 3、B 2O 3等+3 【Al 3+】 【AlO 2-】(偏铝酸根)大多数铝化合物如Al 2O 3、NaAlO 2等●银白色活泼金属,在空气中生成致密的氧化膜阻止进一步氧化●两性金属,可以和强酸、强碱反应●在浓硫酸、浓硝酸中钝化●高温下有强还原性,铝热反应的原料+1 【Tl +】 亚铊化合物如TlCl 等 剧毒●较软的银白色金属,和酸反应生成亚铊化合物●剧毒+3 【Tl 3+】三价铊化合物如Tl 2O 3等 剧毒;强氧化性+3【Ga 3+、In 3+】 大多数镓、铟化合物中●镓的熔点低于体温+2 CO 等 有还原性 ●有多种同素异形体,如金刚石、石墨、C 60等●高温下有还原性,可以还原金属氧化物、CO 2等●可以在纯氧中燃烧发出耀眼白光●同位素14C 用于考古+4 【CO 32-】 【HCO 3-】等 CO 2、CS 2等其他金属碳化物中碳显负价(如CaC 2等);有机物一般不讨论碳的化合价负价的碳化合物有还原性+4 【SiO 32-】 硅酸盐如Na 2SiO 3、硅酸、SiF 4、氟硅酸盐等 ●半导体材料●用作电脑芯片●可以和碱反应放出氢气+3 SiHCl3-4 【Si 4-】某些硅化物如Mg 2Si 、Ca 2Si 等 和水反应放出自燃性的硅烷 +4 GeO 2等●半导体材料+4 【Sn 4+】 四价锡化合物如SnO 2、SnCl 4等可溶于过量强碱●熔点较低,常用来制备合金,如青铜(传统的青铜是铜锡合金)、焊锡等+2 【Sn 2+】亚锡化合物如SnCl 2、SnSO 4等有还原性;溶于过量强碱 +4 【Pb 4+】四价铅化合物如Pb(CH 3COO)4、PbO 2等;Pb 3O 4含有+2和+4价的铅。
化学元素化合价及相对原子质量表
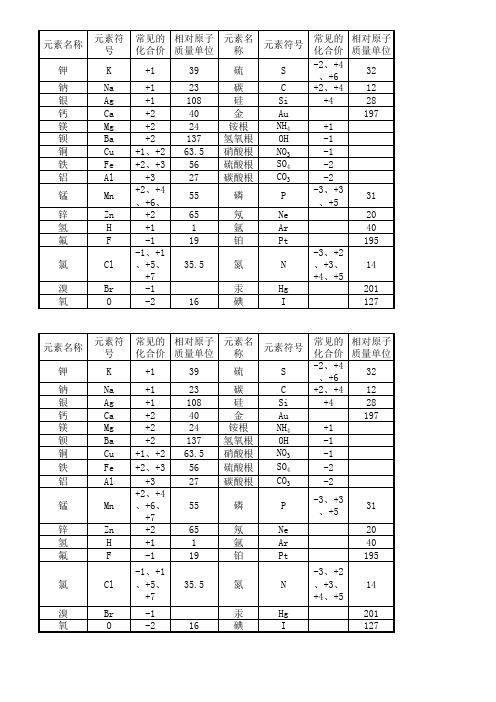
常见的 相对原子 常见的 相对原子 元素名称 元素符号 化合价 质量单位 化合价 质量单位 -2、+4 +1 39 硫 S 32 、+6 +1 23 碳 C +2、+4 12 +1 108 硅 Si +4 28 +2 40 金 Au 197 +2 24 铵根 NH4 +1 +2 137 氢氧根 OH -1 NO3 +1、+2 63.5 硝酸根 -1 SO4 +2、+3 56 硫酸根 -2 CO3 +3 27 碳酸根 -2 +2、+4 -3、+3 55 磷 P 31 、+6、 、+5 +2 65 氖 Ne 20 +1 1 氩 Ar 40 -1 19 铂 Pt 195 -1、+1 -3、+2 35.5 氮 N 14 、+5、 、+3、 +7 +4、+5 -1 汞 Hg 201 -2 16 碘 I 127
元素名称 元素符号 钾 钠 银 钙 镁 钡 铜 铁 铝 锰 锌 氢 氟 氯 溴 氧 K Na Ag Ca Mg Ba Cu Fe Al Mn Zn H F Cl Br O
常见的 相对原子 常见的 相对原子 元素名称 元素符号 化合价 质量单位 化合价 质量单位 -2、+4 +1 39 硫 S 32 、+6 +1 23 碳 C +2、+4 12 +1 108 硅 Si +4 28 +2 40 金 Au 197 NH4 +2 24 铵根 +1 +2 137 氢氧根 OH -1 NO3 +1、+2 63.5 硝酸根 -1 SO4 +2、+3 56 硫酸根 -2 CO3 +3 27 碳酸根 -2 +2、+4 -3、+3 55 磷 P 31 、+6、 、+5 +7 +2 65 氖 Ne 20 +1 1 氩 Ar 40 -1 19 铂 Pt 195 -1、+1 、+5、 +7 -1 -2 35.5 氮 汞 碘 N Hg I -3、+2 、+3、 +4、+5 14 201 127
初中化学化合价一览表
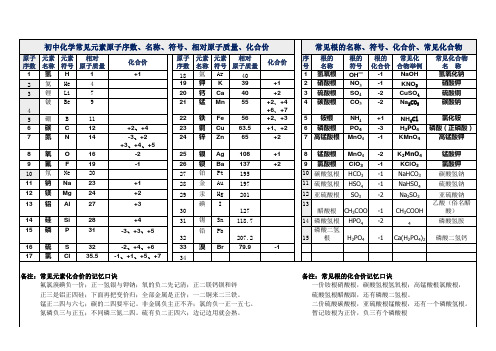
+2、+4 -3、+2 +3、+4、+5 -2
9 氯酸根 10 碳酸氢根 11 硫酸氢根
12 亚硫酸根 SO3 13 醋酸根 CH3COO 14 磷酸氢根 HPO4 15 磷酸二氢根 H2PO4
CH3COOH 乙酸(俗名醋酸)
备注:常见元素化合价的记忆口诀 氟氯溴碘负一价;正一氢银与钾钠;氧的负二先记清;正二镁钙钡和锌 正三是铝正四硅;下面再把变价归;全部金属是正价;一二铜来二三铁。 锰正二四与六七;碳的二四要牢记。非金属负主正不齐;氯的负一正一五七。 氮磷负三与正五;不同磷三氮二四。硫有负二正四六;边记边用就会熟。 附:字体加粗的内容是重点记忆并且必须熟练、准确书写与运用的内容,切记!!!
原子序数1元素名称氢元素符号h相对原子质量1化合价原子序数元素名称氩元素符号ar相对原子质量化合价序号1根的名称氢氧根根的符号ohno3根的化合价1常见化合物举例naoh常见化合物名称氢氧化钠1181940392氦he4钾k12硝酸根122kno3cuso4na2co3硝酸钾3锂li72021钙camn4055234硫酸根so4co3硫酸铜4铍be9锰246723122碳酸根碳酸钠567硼碳bcn111214222324铁fecuzn5663565567铵根nh4131nh4clh3po4kmno4氯化铵24323452铜磷酸根po4mno4磷酸正磷酸氮锌高锰酸根高锰酸钾8氧o1625银ag10818锰酸根mno42k2mno4锰酸钾9氟f19126钡ba13729氯酸根clo31kclo3氯酸钾1011氖ne2027铂pt19510碳酸氢根hco31nahco3碳酸氢钠钠na23128金au19711硫酸氢根hso41nahso4硫酸氢钠12镁mg24229汞hg20112亚硫酸根so32na2so3亚硫酸钠13铝al27330碘i12713醋酸根ch3coo1ch3cooh乙酸俗名醋酸14硅si28431锡sn118
化合价、化学方程式整理

初中化学整理一、常见元素化合价钾钠银氢+1价,钙镁钡锌+2价,一、二铜,二、三铁;氟氯溴碘-1价,氧硫通常-2价,单质化合价为零二、常见原子团化合价四、化学式的书写1、单质:(1)由原子直接构成(元素符号):a.金属:钾K、钙Ca、钠Na、镁Mg、铝Al、锌Zn、铁Fe、锡Sn、铅Pb、氢H、铜Cu、汞Hg、银Ag、铂Pt、金Au 钡Ba、钨Wb.稀有气体:氦He、氖Ne、氩Ar、氪Kr、氙Xe、氡Rnc.部分固态非金属:金刚石/石墨/碳C、硅Si、磷P、硫S(2)双原子分子:a.固体:碘I2;b.常见气体:氢气H2、氮气N2、氧气O2、氯气Cl2、氟气F2;c.液态:溴Br2(3)三原子分子:臭氧O32、化合物:按照化合价,利用化合价交叉法进行书写(1)氧化物:由两种元素组成,其中一种为氧元素的化合物a.非金属氧化物:水H2O、一氧化碳CO、二氧化碳CO2、二氧化硫SO2、三氧化硫SO3、二氧化硅SiO2、一氧化氮NO、二氧化氮NO2、五氧化二磷P2O5b.金属氧化物:氧化钾K2O、氧化钠Na2O、氧化银Ag2O、氧化亚铜Cu2O、氧化钙CaO、氧化镁MgO、氧化钡BaO、氧化锌ZnO、氧化铜CuO、氧化亚铁FeO、三氧化二铁(氧化铁)Fe2O3、四氧化三铁Fe3O4、三氧化二铝Al2O3、二氧化锰MnO2、三氧化钨WO3、氧化铅PbO(2)常见的酸(阳离子只有H+的化合物):硫酸H2SO4、盐酸HCl、硝酸HNO3、磷酸H3PO4、硫化氢H2S、碳酸H2CO3、醋酸CH3COOH(3)常见的碱(阴离子只有OH¯的化合物):氢氧化钾KOH、氢氧化钠NaOH、氢氧化钙Ca(OH)2、氢氧化镁Mg(OH)2、氢氧化钡Ba(OH)2、氢氧化锌Zn(OH) 2、氢氧化铜Cu(OH) 2、氢氧化亚铁Fe(OH) 2、氢氧化铁Fe(OH) 3、氢氧化铝Al(OH) 3(4)盐:由金属阳离子(或铵根离子)和酸根离子构成的化合物a.氯化物/盐酸盐:氯化钾KCl、氯化钠(食盐)NaCl、氯化银AgCl、氯化钙CaCl2、氯化镁MgCl2、氯化钡BaCl2、氯化锌ZnCl2、氯化铜CuCl2、氯化亚铁FeCl2、氯化铁FeCl3、氯化铝AlCl3b.硝酸盐:硝酸钾KNO3、硝酸钠NaNO3、硝酸银AgNO3、硝酸钙Ca(NO3)2、硝酸镁Mg(NO3)2、硝酸钡Ba(NO3)2、硝酸锌Zn(NO3)2、硝酸铜Cu(NO3)2、硝酸亚铁Fe(NO3)2、硝酸铁Fe(NO3)3、硝酸铝Al(NO3)3c.硫酸盐:硫酸钾K2SO4、硫酸钠Na2SO4、硫酸银Ag2SO4、硫酸钙CaSO4、硫酸镁MgSO4、硫酸钡BaSO4、硫酸锌ZnSO4、硫酸铜CuSO4、硫酸亚铁FeSO4、硫酸铁Fe2 (SO4) 3、硫酸铝Al2 (SO4) 3d.碳酸盐:碳酸钾K2CO3、碳酸钠Na2CO3、碳酸银Ag2CO3、碳酸钙CaCO3、碳酸镁MgCO3、碳酸钡BaCO3、碳酸锌ZnCO3、碳酸铜Cu CO3、碳酸亚铁Fe CO3、e.铵盐:氯化铵NH4Cl、硝酸铵NH4NO3、碳酸铵(NH4)2CO3、硫酸铵(NH4)2SO4、磷酸铵(NH4)3PO4、碳酸氢铵NH4HCO3f.其他:高锰酸钾KMnO4、锰酸钾K2MnO4、氯酸钾KClO3、氨气NH3、过氧化氢H2O2g.常见化肥:尿素CO(NH2)2(N%=46.7%)、硝酸铵NH4NO3(N%=35%)、硫酸铵(NH4)2SO4(N%=21.2%)、碳酸氢铵NH4HCO3(N%=17.7%)、硫酸钾K2SO4、氯化钾KCl(5)有机物(含碳化合物):甲烷CH4、乙炔C2H2、乙醇(酒精)C2H5OH、乙酸CH3COOH、葡萄糖C6H12O6(6)常见结晶水合物:五水硫酸铜CuSO4·H2O、明矾KAl(SO4) 2•12H2O、碳酸钠晶体Na2CO3•10H2O3、常见沉淀及其颜色:白色:CaCO3、CaSO4(微溶)、BaCO3、BaSO4、AgCO3、AgCl、AgOH、Fe(OH) 2、Mg(OH) 2红色:Cu、Fe(OH) 3(红褐色)、Fe2O3蓝色:Cu(OH)2(絮状)黑色:MnO2、CuO、Fe、C、Fe3O4、FeSO4五、溶解性表:OH¯:铵、钾、钠、钡、钙(微);NO3¯:全溶;Cl¯:AgCl(白色沉淀);SO42-:BaSO4(白色沉淀);CO32-:铵、钾、钠六、共存问题1、OH¯+H+→H2O2、OH¯+部分金属离子→碱↓3、Ba2++SO42—→BaSO44、Ag++Cl—→AgCl5、CO32—+部分金属离子→盐↓6、H++CO32—→H2O+CO2↑7、NH4++ OH¯→NH3↑+ H2O8、HCO3—+ H+→H2O+CO2↑9、无色:Fe2+(淡绿)、Fe3+(黄)、Cu2+(蓝)七、化合反应:两种或两种以上物质反应生成另一种物质。
初中必背的元素周期表及化合价

初中要背的元素周期表
化合价口诀
一价氢氯钾钠银;二价氧钙钡镁锌。
三铝四硅五价磷,变价元素记在心。
二三铁,二四碳,一七氯,三五氮。
二四六硫要分清,铜汞一二也都有。
单质元素价为零,
负一硝酸氢氧根,负二碳酸硫酸根。
负三记住磷酸根,正一价的是铵根。
化学式的意义
例:下列化学符号中关于数字“2”的意义
A.2CO-----表示2个一氧化碳分子
B.NO2-----表示1个二氧化氮分子中含有2个氧原子
C.Ca2+-----表示1个钙离子带2个单位的正电荷
D.Hg+2O-----表示氧化汞中汞元素的化合价为+2价
E.2Na-----表示2个钠原子
F.2OH------表示2个氢氧根离子
+-m aR b n+- a:表示粒子个数
b:一个粒子中所含某原子或原子团的个数m:表示元素或原子团的化合价
n:一个离子所带的电荷数。
化学常见元素化合价表

计划方案二
时间安排二
张老师
主要内容二
计划方案二
时间安排二
张老师王老师Biblioteka 主要内容一计划方案一
时间安排一
王老师
主要内容一
计划方案一
时间安排一
王老师
主要内容一
计划方案一
时间安排一
王老师
主要内容二
计划方案二
时间安排二
张老师
主要内容二
计划方案二
时间安排二
张老师
主要内容二
计划方案二
时间安排二
张老师
主要内容二
计划方案二
时间安排二
张老师
主要内容二
计划方案二
时间安排二
张老师
主要内容二
序号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
化学常见元素化合价表
主要内容
计划方案
时间安排
责任人
备注
主要内容一
计划方案一
时间安排一
王老师
主要内容一
计划方案一
时间安排一
王老师
主要内容一
计划方案一
时间安排一
王老师
主要内容一
计划方案一
时间安排一
王老师
主要内容一
计划方案一
时间安排一
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Hg
HgF2
HgCl2
HgO
HgS
Hg(OH)2
Hg(NO3)2
HgCO3
HgSO4
汞+2
氟化汞
氯化汞
氧化汞Leabharlann 硫化汞氢氧化汞硝酸汞
碳酸汞
硫酸汞
Al
AlF3
AlCl3
Al2O3
Al2S3
Al(OH)3
Al(NO3)3
Al2(CO3)3
Al2(SO4)3
铝+3
氟化铝
氯化铝
氧化铝
硫化铝
氢氧化铝
硝酸铝
碳酸铝
硫酸铝
Fe
FeF3
FeCl3
Fe2O3
Fe2S3
Fe(OH)3
Fe(NO3)3
Fe2(CO3)3
Fe2(SO4)3
铁+3
氟化铁
氯化铁
氧化铁
硫化铁
氢氧化铁
硝酸铁
碳酸铁
硫酸铁
Na2CO3
Na2SO4
钠+1
氟化钠
氯化钠
氧化钠
硫化钠
氢氧化钠
硝酸钠
碳酸钠
硫酸钠
K
KF
KCl
K2O
K2S
KOH
KNO3
K2CO3
K2SO4
钾+1
氟化钾
氯化钾
氧化钾
硫化钾
氢氧化钾
硝酸钾
碳酸钾
硫酸钾
Ag
AgF
AgCl
Ag2O
Ag2S
AgOH
AgNO3
Ag2CO3
Ag2SO4
银+1
氟化银
氯化银
氧化银
硫化银
F
Cl
O
S
OH
NO3
CO3
SO4
氟-1
氯-1
氧-2
硫-2
氢氧根-1
硝酸根-1
碳酸根-2
硫酸根-2
H
HF
HCl
H2O
H2S
H2O
HNO3
H3CO3
H2SO4
氢+1
氟化氢
入水溶液:氢氟酸
氯化氢
入水溶液:氢氯酸(盐酸)
水
硫化氢
入水溶液:氢硫酸
水
硝酸
碳酸
硫酸
Na
NaF
NaCl
Na2O
Na2S
NaOH
NaNO3
氢氧化银
硝酸银
碳酸银
硫酸银
Cu
CuF2
CuCl2
CuO
CuS
Cu(OH)2
Cu(NO3)2
CuCO3
CuSO4
铜+2
氟化铜
氯化铜
氧化铜
硫化铜
氢氧化铜
硝酸铜
碳酸铜
硫酸铜
Zn
ZnF2
ZnCl2
ZnO
ZnS
Zn(OH)2
Zn(NO3)2
ZnCO3
ZnSO4
锌+2
氟化锌
氯化锌
氧化锌
硫化锌
氢氧化锌
硝酸锌
碳酸锌
